壊死の主な形態学的タイプ。 凝固壊死:説明、原因、治療。
壊死は、病原性細菌への曝露によって引き起こされる、人間の臓器である細胞の破壊と死の不可逆的なプロセスです。 発症の原因としては、高温(火傷を伴う)、化学物質または感染症への曝露、 機械的損傷。 壊死は凝固性(乾性)または凝固性(湿性)の場合があります。 この記事では、乾燥性壊死の原因とその治療方法について詳しく検討します。
凝固性壊死とは何ですか
乾性壊死は、多くの場合、タンパク質は豊富だが体液の含有量が少ない臓器に影響を与えます。 これらには次のものが含まれます。
- 腎臓。
- 副腎;
- 脾臓;
- 心筋。
器官細胞の死は、熱的、化学的、機械的、毒性による損傷の結果、血液供給と酸素富化が不十分なために起こります。 その結果、死んだ細胞が乾燥し、ミイラ化のプロセスが起こります。 死んだ細胞は生きた細胞から明確な線で分離されます。
乾燥性壊死の発症の理由
乾燥壊死は次の場合に形成されます。
- 特定の臓器の特定の領域への血液供給に違反するプロセスがあり、その結果、酸素と必須栄養素の欠乏が発生しました。
- 病気は徐々に進行しました。
- 臓器の患部には十分な水分(脂肪層、 筋肉組織);
- 病原性微生物は細胞の患部には存在しませんでした。
免疫力が強く栄養失調の人は、乾燥性壊死が発生しやすくなります。
凝固壊死: 発症のメカニズム
細胞の酸素飽和度が不十分で血液供給が障害されると、原形質の凝固と圧縮のプロセスが発生し、患部が乾燥します。 損傷した部分は、隣接する生体組織に有毒な影響を及ぼします。
患部には特徴がある 外観: 死んだ細胞は明確な線で輪郭が描かれ、顕著な黄灰色または粘土黄色の色をしています。 この領域は時間の経過とともに厚くなります。 切断すると、組織は完全に乾燥しており、固まった状態ですが、パターンはぼやけていることがわかります。 細胞核が崩壊した結果、均一な細胞質の塊のように見えます。 さらに、壊死や炎症が進行すると、死んだ組織の拒絶反応に気づくことがあります。 この病気が人の耳介や骨に影響を与えると、瘻孔が形成されます。 しかし、凝固性壊死の発症メカニズムはまだ完全には理解されていません。
凝固性壊死の種類
凝固壊死にはいくつかのタイプがあります。
- 心臓発作が最も一般的なタイプです。 虚血性疾患により発症します。 脳組織では発生しません。 心臓発作の場合、損傷した組織の完全な再生が可能です。
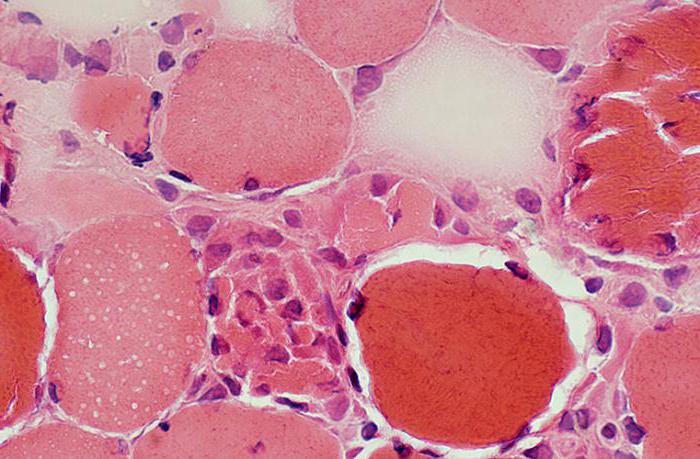
- Waxy (Zenker) - 重度の感染性損傷の結果として発症します。 この病気は筋肉組織に影響を及ぼし、多くの場合、大腿部の筋肉や前腹壁に影響を及ぼします。 壊死の発症は、発疹や患部が灰色になるなど、以前の病気によって引き起こされます。
- 乾酪壊死は特殊な種類の病気です。 結核、梅毒、ハンセン病、ウェゲナーの仲間。 このタイプの壊死では、間質と実質 (線維と細胞) が死滅します。 特殊性 この病気つまり、乾燥した領域に加えて、ペースト状または凝固した肉芽腫が形成されます。 影響を受けた組織は明るいピンク色になります。 乾酪壊死は、広大な領域を「破壊」する可能性があるため、最も危険なタイプの1つです。
- フィブリノイド - 結合組織が損傷する病気。 壊死は、狼瘡やリウマチなどの自己免疫疾患で発生します。 この病気は平滑筋と血管の線維に最も深刻な影響を与えます。 フィブリノイド壊死は、コラーゲン線維の正常な状態の変化と壊死物質の蓄積を特徴とします。 顕微鏡検査では、影響を受けた組織はフィブリンのように見えます。 同時に、死んだものは明るいピンク色になります。 フィブリノイド壊死の影響を受けた領域には、フィブリンやコラーゲンの分解産物に加えて、大量の免疫グロブリンが含まれています。
- 脂肪 - この病気は打撲や出血、組織の破壊の結果として形成されます。 甲状腺。 壊死では、腹膜と乳腺が影響を受けます。
- 壊疽 - 乾燥、湿潤、ガスが発生する可能性があります。 寝たきり患者の褥瘡もこのタイプの壊死に属します。 ほとんどの場合、病気の発症は、患部に侵入した細菌によって促進されます。
凝固性壊死の一種としての乾性壊疽
乾性壊疽は、外部環境と接触した皮膚が壊死を起こす病気です。 原則として、病気の発症に微生物は関与しません。 乾性壊疽は、ほとんどの場合、四肢に影響を及ぼします。 損傷した組織は暗く、ほぼ黒色で、輪郭がはっきりしています。 硫化水素の影響で色が変化します。 これは、ヘモグロビン色素が硫化鉄に変換されるために起こります。 乾性壊疽は以下の条件下で発生します。
- 動脈血栓症と四肢のアテローム性動脈硬化症を伴います。
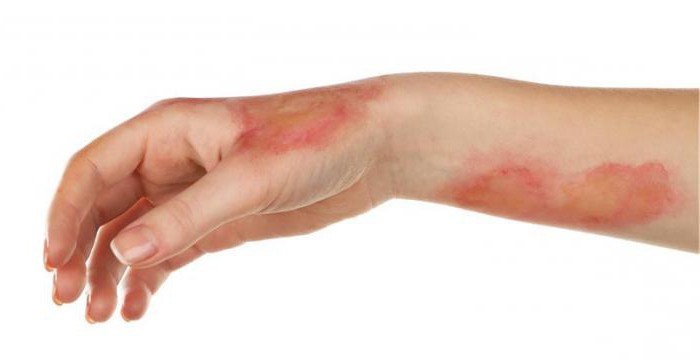
- 手足が高温または低温にさらされた場合(火傷または凍傷)。
- 開発に伴い
- 次のような感染症の存在下では、
治療は死んだ組織を外科的に除去することによってのみ行われます。

湿性壊疽
湿性壊疽は次のような場合に発症する病気です。 細菌感染損傷した組織に。 この病気は水分が豊富な臓器に影響を及ぼし、皮膚に発生することもありますが、内臓に広がることがより多くなります。 湿性壊疽は腸(動脈の閉塞を伴う)と肺(肺炎の結果として発生します)に影響を与えます。
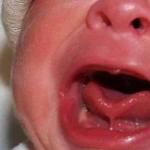
多くの場合、この病気は小児に発生します。これは、感染症に罹患すると免疫力が低下して壊疽が形成されやすくなるためです。 頬と会陰の軟組織が影響を受けます。 この病気は水がんと呼ばれています。 患部は非常に腫れ上がり、 暗色。 境界を示す輪郭がないため、治療が困難な病気です 外科的治療影響を受けた組織がどこで終わるかを判断するのは難しいためです。 壊疽の領域は非常に 悪臭そしてこの病気はしばしば死につながります。
ガス壊疽と床ずれ
その症状はウェットと非常に似ていますが、発症の原因は異なります。 このタイプの壊疽は、ウェルシュ菌種の細菌が感染した初心者に侵入し、活発に増殖した場合に発症します。 細菌は生命活動の過程で特定のガスを放出し、それが影響を受けた組織で見られます。 この病気による死亡率は非常に高いです。
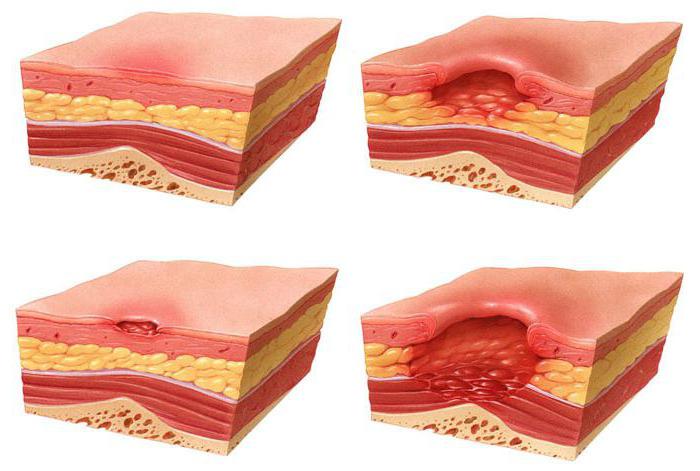 褥瘡は壊疽の一種で、組織の死滅が起こります。 寝たきりの患者は、長時間動かないことで体の特定の部分に圧力がかかり、血液とともに必要な物質が届かないため、病気に最もかかりやすくなります。 その結果、皮膚細胞が死滅します。 仙骨、かかと、大腿骨の領域は最も損傷を受けやすい部分です。
褥瘡は壊疽の一種で、組織の死滅が起こります。 寝たきりの患者は、長時間動かないことで体の特定の部分に圧力がかかり、血液とともに必要な物質が届かないため、病気に最もかかりやすくなります。 その結果、皮膚細胞が死滅します。 仙骨、かかと、大腿骨の領域は最も損傷を受けやすい部分です。
凝固性壊死の診断
「凝固性壊死」の診断を下すには、損傷が表面的であれば、医師が分析のために血液と損傷組織のサンプルを採取するだけで十分です。
臓器壊死の疑いがある場合は、より詳細な検査が行われます。 このためには次のものが必要です。
- X線写真を撮ります。 特に関連性の高い この研究ガス壊疽が疑われる場合。
- 放射性同位元素の研究を実施します。 X線検査で変化が見られなかった場合に処方されます( 初期病気)。 放射性物質が人体に取り込まれる。 臓器の組織に壊死性変化がある場合、それは暗いスポットによって強調表示されます。
- CTスキャンを行います。 骨損傷の疑いがある場合に行われます。
- MRIを受けてください。 血液循環障害に伴うわずかな変化も明らかにするため、最も効果的な研究方法です。
壊死の合併症
壊死は、損傷を受けた臓器や組織の「死」です。 したがって、心臓発作、脳、腎臓、肝臓の壊死など、さまざまな種類の病気が人の死につながる可能性があります。
また、広範な壊死は重篤な合併症を引き起こす可能性があり、たとえば複数の床ずれが発生すると、危険な感染症が追加される可能性があります。 死んだ組織はその崩壊生成物を体内に放出し、有毒な合併症を引き起こします。 軽度の病気であっても、心筋の瘢痕化や脳の嚢胞形成などの不快な結果を引き起こす可能性があります。
壊死の治療
壊死の治療は、壊死の種類を特定し、壊死によって引き起こされる損傷を評価し、付随する疾患を特定することから始まります。
乾燥性皮膚壊死を診断する場合、次のような局所治療が処方されます。
- 緑色のペイントで患部を治療します。
- 消毒剤を使用して皮膚の表面を洗浄します。
- 「クロルヘキシジン」の溶液を包帯に巻きます。
患者さんには薬が処方されており、 外科的治療患部を含む正常な血液循環を回復するために。 死んだ細胞を除去するには、患部を切除する外科手術が最もよく行われます。 手足の切断は、健康な領域を病気の蔓延から守るために行われます。

内臓の乾性壊死は、抗炎症薬、血管拡張薬、軟骨保護薬の使用で治療されます。 治療効果が無い場合には外科的治療が行われます。
壊死 (ギリシャ語から。 ネクロス- 死亡) - 病原性因子の影響下での生体内の細胞および組織の壊死、死。 このタイプの細胞死は遺伝的に制御されていません。
壊死を引き起こす要因:
ü 物理的(銃創、放射線、電気、低温および高温 - 凍傷および火傷)。
ü 有毒(酸、アルカリ、重金属の塩、酵素、薬物、エチルアルコールなど)。
ü 生物学的(細菌、ウイルス、原生動物など)。
ü アレルギー(エンド抗原およびエキソ抗原、たとえば、感染性アレルギー疾患および自己免疫疾患におけるフィブリノイド壊死、アルサス現象)。
ü 血管(心臓発作 - 血管壊死);
ü トロフォネロティック(褥瘡、非治癒性潰瘍)。
病原性因子の作用機序に応じて、次のようなものがあります。
- 因子の直接作用による直接壊死(外傷性壊死、毒性壊死、生物学的壊死)。
- 血管および神経内分泌系を介して間接的に起こる間接的壊死(アレルギー性壊死、血管壊死、およびトロフォンニューロシス壊死)。
壊死の形態学的兆候
壊死の前には壊死の期間があり、その形態学的基質は異栄養性変化である。
カーネルの変更.
死んだ細胞のクロマチンは凝縮して大きな塊になります。 核は体積が減少し、しわが寄って緻密になり、非常に好塩基性になります。つまり、ヘマトキシリンで濃い青色に染まります。 このプロセスの名前は 核濃縮症(しわが寄る)。 その後、濃縮核は破裂して多数の小さな好塩基性粒子になる可能性があります。 (核崩壊)または、リソソームデオキシリボヌクレアーゼの作用の結果として溶解(溶解)を受けます。 (核分解)。その後、体積が増加し、ヘマトキシリンで弱く染色され、核の輪郭が徐々に失われます。 急速に進行する壊死により、核は濃縮段階を経ずに溶解を起こします。
細胞質の変化。
- 細胞質タンパク質の凝固とリボソームの破壊(消失)の結果、細胞の細胞質は均一になり、顕著な好酸性になります。
- ミトコンドリアの膨張と細胞小器官膜の破壊(破壊)により、細胞質の空胞化が引き起こされます。
- 自身のリソソームから放出される酵素による細胞の消化により、細胞溶解(自己溶解)が引き起こされます。
したがって、タンパク質の凝固は細胞質内で起こり、通常はそれらの凝集に置き換わります。
細胞間物質の変化間質物質と繊維構造の両方をカバーします。 ほとんどの場合、フィブリノイド壊死に特徴的な変化が起こります。コラーゲン、弾性繊維、レチクリン線維が緻密で均質なピンク色の、場合によっては好塩基性の塊に変化し、断片化、塊状の崩壊、または溶解が起こる可能性があります。 頻度は低いですが、線維構造の浮腫、溶解、粘液が観察されることがありますが、これはコリコート壊死の特徴です。
壊死の臨床的および形態学的形態
凝固(乾性)壊死と凝集性(湿性)壊死を区別します。
A. 凝固(乾燥)壊死。
凝固性壊死は通常、腎臓、心筋、副腎、脾臓など、タンパク質が豊富で体液に乏しい臓器で発生します。通常、循環不全や酸素欠乏、物理的、化学的、その他の損傷因子の作用の結果として発生します。たとえば、ウイルス損傷による肝細胞の凝固壊死、または細菌および非細菌起源の有毒物質の作用下での肝細胞の凝固性壊死。 凝固壊死は、それに伴って発生する死んだ領域が乾燥し、密で、崩れ、白または黄色になるという事実を特徴とするため、乾燥とも呼ばれます。
凝固壊死には次のようなものがあります。
心臓発作- 内臓(脳を除く)の一種の血管(虚血性)壊死。 これは最も一般的なタイプの壊死です。
心臓発作(緯度から) 梗塞-詰め物、充填)は、血流の突然の停止(虚血)の結果として血液循環から遮断された、器官または組織の死んだ領域です。 心臓発作は、血管(虚血性)凝固または凝固壊死の一種です。 これは最も一般的なタイプの壊死です。
実質細胞と間質組織は両方とも壊死を起こします。 ほとんどの場合、心臓発作は血栓症または塞栓症、けいれん、圧迫を伴って起こります。 動脈血管。 非常にまれに、心臓発作の原因が静脈流出の違反である場合があります。
心臓発作が発症する理由:
- 長期にわたるけいれん、血栓症または塞栓症、動脈の圧迫による急性虚血。
- 血液供給が不十分な状態での臓器の機能的緊張。 心臓発作の発生にとって非常に重要なのは、吻合部と側副動脈の不全であり、これは動脈壁の損傷や内腔の狭窄(アテローム性動脈硬化、閉塞性動脈内膜炎)の程度、循環障害の程度によって決まります。 (静脈うっ滞など)、血栓や塞栓による動脈の遮断のレベルも含まれます。
したがって、心臓発作は通常、動脈壁の重篤な変化や全身循環障害を特徴とする病気で発生します。 これ:
- リウマチ性疾患;
- 心臓の欠陥。
- アテローム性動脈硬化症;
- 高張性疾患;
- 細菌性(感染性)心内膜炎。
心臓発作の形態
心臓発作のマクロ写真。 心臓発作の形、大きさ、色、硬さは異なる場合があります。
心臓発作の一種。通常、梗塞はくさび形です。 この場合、くさびの尖った部分がオルガンのゲートに面し、 幅広部分臓器の被膜の下、腹膜の下(脾臓梗塞)、胸膜の下(肺梗塞)など、末梢にまで行きます。 腎臓、脾臓、肺における心臓発作の特徴的な形態は、これらの臓器の血管構造の性質、つまり動脈の分岐の主な(対称的な二分法)タイプによって決まります。 まれに、心臓発作の形が不規則になります。 このような心臓発作は、心臓、脳、腸で発生します。これらの臓器では、動脈の主要な分岐ではなく、緩やかな分岐または混合型の分岐が優勢であるためです。
心臓発作の大きさ。心臓発作は、臓器の大部分または全体を覆う場合(亜計または全心臓発作)、または顕微鏡下でのみ検出される場合(微小梗塞)があります。
梗塞の色と質感。心臓発作が凝固性壊死として発症した場合、壊死領域の組織は厚くなり、乾燥して白黄色になります(心筋梗塞、腎臓、脾臓)。 コリコート壊死のタイプによって梗塞が形成された場合、死んだ組織は軟化して液化します(脳梗塞または灰色の軟化巣)。
開発と外観のメカニズムに応じて、次のようなものがあります。
- 白色(虚血性)梗塞。
- 赤色(出血性)心臓発作。
- 出血性の花冠を伴う白い梗塞。
白(虚血性)梗塞は、例えば心臓、腎臓、脾臓、ウィリス輪より上の脳などの臓器における動脈血流の完全な停止の結果として発生します。 これは通常、側副循環が十分に発達していない、単一の血流系 (動脈の主な分岐タイプ) がある領域で発生します。 虚血組織からの妨害されない静脈の流出と動脈の遠位部分のけいれんにより、血流の停止後にこれらの梗塞の蒼白が観察される。 白色(虚血性)梗塞は、周囲の組織から明確に区切られた、白黄色の構造のない領域です。
出血性の花冠を伴う白い梗塞は白黄色の領域で表されますが、この領域は出血領域に囲まれています。 これは、梗塞の周囲に沿った血管けいれんが麻痺の拡大と出血の発症によって置き換えられるという事実の結果として形成されます。 このような心臓発作は腎臓や心筋で発生する可能性があります。
赤色(出血性)心臓発作は、壊死部位が血液で飽和しており、暗赤色で境界がはっきりしているのが特徴です。 梗塞領域の微小血管系の壊死血管から血液が放出されるため、梗塞部分は赤くなります。 赤色梗塞の発症には、臓器の血管構造の特徴が重要です - 2つ以上の血流系、側副動脈の発達:肺では - 気管支と肺の間の吻合の存在 肺動脈、腸では腸間膜動脈の枝の間に大量の吻合があり、脳では内頸動脈と脳底動脈の枝の間にウィリス輪の吻合が存在します。 閉塞血栓が溶解または断片化(崩壊)し、梗塞領域の動脈血流が再開されると、組織内に赤色梗塞が発生することもあります。
腎臓や心臓に出血性梗塞が起こることはまれです。 このような出血性含浸に必要な条件は静脈うっ滞である。
静脈梗塞は、組織の静脈排水系全体が閉塞した場合に発生します(例、上矢状静脈洞血栓症、腎静脈血栓症、上腸間膜静脈血栓症)。 これにより、重度の浮腫、うっ血、出血が生じ、組織内の静水圧が徐々に増加します。 静水圧が大きく上昇すると、組織への動脈血の流れが困難になり、虚血や梗塞が起こります。 静脈梗塞は常に出血を伴います。
顕微鏡的には、死んだ領域は、構造、細胞輪郭の喪失、および核の消失によって特徴付けられます。
心臓(心筋)、脳、腸、肺、腎臓、脾臓の梗塞は臨床的に最も重要です。
心の中で梗塞は通常、出血性の花冠を備えた白色で、不規則な形をしており、左心室と心室中隔でより頻繁に発生しますが、右心室と心房で発生することは非常にまれです。 壊死は、心内膜の下(心内膜下梗塞)、心外膜(心外膜梗塞)、心筋の厚さ内(壁内)に局在する場合もあれば、心筋の厚さ全体を覆う場合(貫壁梗塞)もあります。 梗塞領域では、血栓性沈着物が心内膜に形成されることが多く、線維素沈着物が心膜に形成されることが多く、これは壊死領域の周囲での反応性炎症の発生と関連しています。 ほとんどの場合、心筋梗塞はアテローム性動脈硬化を背景に発生します。 高血圧動脈のけいれんや血栓症が加わると、 急性型虚血性心疾患。
脳の中でウィリス輪の上に白い梗塞が発生し、すぐに軟化します(脳の灰色の軟化の焦点)。 重大な循環障害、静脈うっ血を背景に心臓発作が発生した場合、脳壊死の焦点は血液で飽和し、赤くなります(脳の赤い軟化の焦点)。 ウィリス輪の下の脳幹の領域にも赤い梗塞が発生します。 心臓発作は通常、皮質下の結節に局在し、脳の経路を破壊し、麻痺として現れます。 脳梗塞は心筋梗塞と同様、アテローム性動脈硬化や高血圧を背景に発生することが多く、脳血管疾患の症状の一つです。
肺の中でほとんどの場合、出血性梗塞が形成されます。 その原因は血栓塞栓症であることが多く、血管炎における血栓症であることはあまりありません。 梗塞領域は明確に境界が定められており、円錐形をしており、その底部は胸膜に面しています。 梗塞領域の胸膜にフィブリンのオーバーレイが現れます (反応性胸膜炎)。 向いている円錐の先端に 肺根、血栓または塞栓が肺動脈の枝で見つかることがよくあります。 死んだ組織は緻密で粒状で、暗赤色です。 出血性肺梗塞は通常、静脈うっ血を背景に発生し、その発症は肺の血管構造の特徴、肺動脈と気管支動脈の系間の吻合の存在によって主に決定されます。 うっ血性充血と肺動脈の枝の内腔の閉鎖の状態では、血液が気管支動脈から肺組織の壊死領域に入り、毛細血管が破壊されて肺胞の内腔に流れ込みます。 心臓発作の周囲では、多くの場合、肺組織の炎症が発生します(梗塞周囲肺炎)。 大量出血性肺梗塞は肝上黄疸の原因となる可能性があります。 肺の白心発作は非常にまれです。 それは気管支動脈の内腔の硬化と閉塞によって起こります。
腎臓で梗塞は、原則として、出血性花冠を伴う白色で、円錐形の壊死領域が皮質物質または実質の厚さ全体を覆います。 主動脈幹が閉鎖すると、全腎梗塞または亜全腎梗塞が発生します。 特殊な種類の心臓発作は、腎臓の皮質物質の対称的な壊死であり、急性の心臓発作の発症につながります。 腎不全。 腎臓の虚血性梗塞の発症は通常、血栓塞栓症を伴いますが、リウマチ、細菌性心内膜炎、高血圧、冠状動脈性心疾患における腎動脈枝の血栓症を伴うことはあまりありません。 まれに、腎静脈血栓症により腎臓の静脈梗塞が発生することがあります。
脾臓で白い梗塞があり、多くの場合被膜の反応性線維性炎症とそれに続く横隔膜、壁側腹膜、腸ループとの癒着の形成を伴います。脾臓の虚血性梗塞は血栓症や塞栓症と関連しています。 脾静脈の血栓症により、非常にまれに静脈梗塞が発生することがあります。
腸内心臓発作は出血性であり、必ず敗血症性腐敗を起こし、腸壁の穿孔や腹膜炎の発症につながります。 原因は、ほとんどの場合、捻転、腸陥入、絞扼性ヘルニアですが、頻度は低いですが、血栓症を伴うアテローム性動脈硬化症です。
乾酪(凝固)壊死結核、梅毒、ハンセン病のほか、リンパ肉芽腫症でも発症します。 特定の感染性肉芽腫で最も頻繁に見られるため、特異的とも呼ばれます。 の 内臓白っぽい黄色の組織の乾燥した崩れかけた限られた領域が現れます。 梅毒性肉芽腫では、そのような領域はもろくなく、アラビアの接着剤を思わせるペースト状であることがよくあります。 これは混合型(つまり、細胞外と細胞内)の壊死であり、実質と間質(細胞と線維の両方)の両方が同時に死滅します。 顕微鏡的には、そのような組織領域はヘマトキシリンとエオシンで染色された構造のない均質なピンク色のように見え、核クロマチンの塊(核破壊)がはっきりと見えます。
ワックス状壊死またはゼンカー壊死(筋肉壊死、しばしば前部 腹壁および太もも、重度の感染症(腸チフス、発疹チフス、コレラ)を伴う)。
フィブリノイド壊死- 結合組織壊死の一種。 アレルギー疾患や自己免疫疾患(リウマチなど)で観察されます。 関節リウマチおよび全身性エリテマトーデス)。 血管の中膜のコラーゲン線維と平滑筋が損傷します。 細動脈のフィブリノイド壊死は悪性高血圧症で観察されます。 この壊死は、正常なコラーゲン線維構造の喪失と、顕微鏡でフィブリンを模倣した均一な明るいピンク色の壊死物質の蓄積によって特徴付けられます。
脂肪壊死。
酵素的脂肪壊死:脂肪壊死は、膵臓酵素が管から周囲の組織に漏れ出すときに、急性膵炎や膵臓損傷で最も一般的に発生します。 同時に、不透明な白い(チョークのような)プラークや小結節(脂肪壊死)が膵臓の周囲の脂肪組織に現れます。
非酵素的脂肪壊死:非酵素的脂肪壊死は、乳腺、皮下脂肪組織、および脂肪組織で観察されます。 腹腔。 ほとんどの患者には外傷歴があります。 非酵素的脂肪壊死は、泡沫状の細胞質を有する多数のマクロファージ、好中球、およびリンパ球の存在を特徴とする炎症反応を引き起こします。 これに続いて線維化が起こり、このプロセスを腫瘍と区別するのが難しい場合があります。
壊疽(ギリシャ語から。 ガングライナ- 火):これは、外部環境と通信し、その影響下で変化する組織の壊死です。 乾性、湿性、ガス壊疽、床ずれがあります。
乾燥性壊疽- これは外部環境と接触した組織の壊死であり、微生物の関与なしに進行します。 乾性壊疽は、虚血性凝固組織壊死の結果として四肢に発生することがほとんどです。 壊死組織は黒く乾燥して見え、隣接する生存組織と明確に区別されます。 健康な組織との境界では、境界炎症が発生します。 色の変化は、硫化水素の存在下でのヘモグロビン生成色素の硫化鉄への変換によるものです。 例としては乾性壊疽があります。
- アテローム性動脈硬化と動脈の血栓症(アテローム性動脈硬化性壊疽)を伴う手足、潰瘍性動脈内膜炎。
- 凍傷または火傷を伴う。
- レイノー病または振動病のある指。
- 発疹チフスやその他の感染症のある皮膚。
湿性壊疽:重度の細菌感染による壊死組織変化が重なった結果として発症します。 微生物酵素の作用下で、二次的な凝集が起こります。 湿性壊疽は通常、水分が豊富な組織で発生します。 四肢に発生することもありますが、腸間膜動脈閉塞による腸(血栓症、塞栓症)や肺炎(インフルエンザ、麻疹)の合併症としての肺などの内臓に発生することが多いです。 弱体化した 感染症(通常は麻疹)子供たちは頬や会陰の軟組織に湿性壊疽を発症することがあります。これはノーマ(ギリシャ語の名から水の癌)と呼ばれます。
褥瘡(褥瘡):壊疽の一種として、褥瘡が分離されます。これは、長時間の圧力にさらされた組織(皮膚、軟組織)の壊死です。 床ずれは、仙骨、椎骨の棘突起、大転子の領域によく発生します。 大腿骨(寝たきり患者の場合)。 原因としては、これは血管や神経が圧迫されることによるトロフォン神経性壊死であり、心血管疾患、腫瘍疾患、感染症、または神経疾患を患う重篤な患者の組織栄養障害を悪化させます。
B. 凝集(湿潤)壊死
死んだ組織が溶けるのが特徴です。 それは、加水分解プロセスにとって好ましい条件が存在する、タンパク質が比較的少なく、体液が豊富な組織で発生します。 細胞溶解は、それ自体の酵素の作用の結果として起こります (自己溶解)。 湿性凝集性壊死の典型的な例は、脳の灰色の軟化(虚血性梗塞)の焦点です。
壊死の結果。
壊死の好ましい結果:
- 溶解;
- このような場合、組織の壊死部位に瘢痕が形成されます(心臓発作部位の瘢痕)。
- カプセル化。
- 石化。
- 骨化;
- 嚢胞の形成。
壊死の有害な結果:
- 壊死の病巣が化膿性(敗血症性)で溶ける。
- 隔離とは、自己消化や組織化を受けない死んだ組織の領域の形成です。 隔離者は通常、骨髄の炎症、つまり骨髄炎を伴う骨で発生します。 このような隔離器の周囲には、隔離嚢と膿で満たされた空洞が形成されます。
- 切断 - 壊死組織の拒絶。
アポトーシス 、またはプログラムされた細胞死は、内部または外部の要因が遺伝的プログラムを活性化し、細胞死とその死を引き起こすプロセスです。 効果的な除去生地から。 形態学的には、アポトーシスは、ランダムに配置された単一の細胞の死によって現れ、これには、周囲の細胞によって直ちに貪食される、膜に囲まれた丸い体(「アポトーシス体」)の形成が伴います。
これは、体の不要な細胞や欠陥細胞が除去されるエネルギー依存のプロセスです。 それは形態形成において重要な役割を果たし、器官のサイズを一定に制御するためのメカニズムです。 アポトーシスの減少に伴い、細胞の蓄積が起こり、一例として腫瘍の増殖が挙げられます。 アポトーシスの増加に伴い、組織内の細胞数の漸進的な減少が観察され、その一例が萎縮です。
アポトーシスの形態学的発現
アポトーシス細胞は、核クロマチンの高密度の断片を含む、非常に好酸性の細胞質の円形または楕円形の塊として現れます。 細胞の圧縮とアポトーシス体の形成は急速に起こり、また細胞は急速に貪食され、崩壊し、または臓器の内腔に排出されるため、重度の場合には組織学的標本上で発見されます。 さらに、アポトーシスは、壊死とは異なり、炎症反応を伴わないため、組織学的検出も困難になります。
ネクローシスとアポトーシスの比較特性
|
誘導 |
生理学的または病理学的刺激によって活性化される |
ダメージ要因によって異なる |
|
有病率 |
シングルケージ |
細胞群 |
|
生化学的変化 |
内在性エンドヌクレアーゼによるエネルギー依存性の DNA 断片化。 |
イオン交換の違反または終了。 |
|
DNAの崩壊 |
断片への分裂を伴う核内凝縮 |
壊死細胞におけるびまん性局在 |
|
細胞膜の完全性 |
保存されました |
違反しました |
|
形態学 |
圧縮されたクロマチンによるアポトーシス小体の形成による細胞の縮小と断片化 |
腫れと細胞溶解 |
|
炎症反応 |
通常はそこにあります |
|
|
死んだ細胞の除去 |
隣接する細胞による吸収(貪食) |
好中球とマクロファージによる食作用 |
米。 1. アポトーシス (右) と壊死 (左) の間の一連の超微細構造変化
1 - 正常な細胞。 2 - アポトーシスの始まり。 3 - アポトーシス細胞の断片化。 4 - 周囲の細胞によるアポトーシス体の貪食。 5 - 壊死中の細胞内構造の死。 6 - 細胞膜の破壊。
アポトーシスは、次の生理学的および病理学的プロセスに関与しています。
ü 胚形成(着床、器官形成を含む)中のプログラムされた細胞破壊。
ü 成人におけるホルモン依存性の臓器退縮(例:子宮内膜の拒絶反応) 月経周期、閉経期における卵巣の卵胞閉鎖および授乳停止後の乳腺の後退。
細胞集団の増殖中の一部の細胞の除去。
ü 腫瘍内の個々の細胞の死。主にその退縮中に起こるが、活発に増殖している腫瘍でも起こる。
o 細胞死 免疫系サイトカインの枯渇後、および胸腺での発生中の自己反応性 T 細胞の死後の B リンパ球と T リンパ球の両方。
ü 膵臓や膵臓で観察される、排泄管の閉塞後の実質臓器の病理学的萎縮。 唾液腺、腎臓。
ü 細胞傷害性 T 細胞の作用によって引き起こされる細胞死(移植片拒絶反応や移植片対宿主病など)。
一部の細胞損傷 ウイルス性疾患たとえば、次のようなとき ウイルス性肝炎カウンシルマンの遺体のように、アポトーシスを起こした細胞の断片が肝臓で見つかったとき。
アポトーシスの制御
アポトーシスは遺伝的に制御された細胞死です。 現在、アポトーシスの制御に必要な物質をコードする多数の遺伝子が同定されている。
アポトーシスは次のように制御できます。
- 外部要因、
- 自律的なメカニズム。
壊死、アポトーシス、萎縮
トピックの関連性
生物学的概念としての死は、生物の生命の不可逆的な停止の表現です。 死が始まると、人は死体、死体(死体)になります。 法的な観点から見ると、ほとんどの国では、脳の活動が完全かつ不可逆的に停止した場合、生物は死んだものとみなされます。 しかし同時に、法的に死んだ生物の多数の細胞や組織は、死後しばらくの間生存し続けます。 これらの臓器および組織は、移植の主な供給源を構成します。
細胞死は体の生命活動の継続的な現れであり、健康な状態では細胞の生理学的再生によってバランスが保たれているということを知っておく必要があります。 細胞の構造コンポーネントと細胞全体の両方が摩耗し、老化し、死滅し、交換する必要があります。 さまざまな臓器や組織を健康な状態に維持することは、「自然な」生理学的再生がなければ不可能であり、したがって個々の細胞が死ななければなりません。 この細胞死は 1972 年に「アポトーシス」と呼ばれました。 アポトーシスはプログラムされた細胞死です。 アポトーシスと多くの病理学的状態との直接的な関係は、今日ではもはや疑いの余地がありません。 アポトーシスを制御する多くの遺伝子の機能不全を研究することで、これらの疾患の治療におけるまったく新しい方向性の開発が可能になるでしょう。 発達 薬アポトーシスを調節することができるため、悪性腫瘍、ウイルス感染症、神経系の特定の疾患、免疫不全および自己免疫疾患の治療に新たな可能性が開かれます。 たとえば、悪性腫瘍やリンパ増殖性疾患ではアポトーシスを強化する必要があり、細胞損傷を特徴とする疾患ではアポトーシスを弱める必要があります。
しかし、細胞死は、外部の損傷(病原性)因子の「暴力的な」作用の結果として、生体において発生する可能性があります。 この細胞の死は壊死と呼ばれます。 死んだ細胞は完全に機能を停止します。 細胞死には、不可逆的な生化学的および構造的変化が伴います。
したがって、 細胞死次の 2 つの方法で発生する可能性があります。 壊死とアポトーシス。ネクローシスとアポトーシスの生物学的兆候と重要性は異なるため、この章ではこれらのプロセスを個別に検討します。
学習の主な目標 – 壊死、アポトーシス、萎縮の主な巨視的および微視的兆候を認識し、それらの原因と発生メカニズムを説明し、起こり得る結果を評価し、身体にとってこれらのプロセスの重要性を判断できる。
知っておく必要がある理由:
– 光光学レベルと超微細構造レベルの両方で、壊死とアポトーシスの特徴的な形態学的兆候を判断する。
- 肉眼的徴候によってさまざまな凝固および凝固壊死を診断する。
– さまざまな局在の壊死とアポトーシスの重要性を評価します。
– 無形成、無形成および低形成からの萎縮の際立った形態学的特徴を決定し、重要性を評価する 他の種類臓器および生物全体の機能の萎縮。
伝統的に、細胞死の研究は壊死から始まりますが、アポトーシスは体の一般的な病理学的および生理学的プロセスの一部を伴い、場合によっては調節するため、アポトーシスの方が確かにはるかに一般的です。
壊死(ギリシャ語から。 ネクロス- 死亡) - 病原性因子の影響下での生体内の細胞および組織の壊死、死。 このタイプの細胞死は遺伝的に制御されていません。
壊死の原因。 壊死を引き起こす要因:
-物理的(銃創、放射線、電気、低温および高温 - 凍傷および火傷);
-毒(酸、アルカリ、重金属塩、酵素、薬物、エチルアルコールなど);
-生物学的(細菌、ウイルス、原生動物など);
-アレルギー(エンド抗原およびエキソ抗原、たとえば、感染性アレルギー疾患および自己免疫疾患におけるフィブリノイド壊死、アルサス現象)。
-血管(心臓発作 - 血管壊死);
-トロフォニューロティック(褥瘡、治癒しない潰瘍)。
病原性因子の作用機序に応じて、次のようなものがあります。
-直接壊死要因(外傷性、毒性、生物学的壊死)の直接作用により、
-間接的な壊死これは、血管および神経内分泌系を介して間接的に起こります(アレルギー性、血管およびトロフォン神経性壊死)。
壊死の形態学的兆候
壊死の前には壊死の期間があり、その形態学的基質は異栄養性変化である。
A. 初期の変更:ネクロバイオシスの初期段階では、細胞は形態学的に変化していません。 電子顕微鏡または組織化学検査で認識できる変化が現れるまでには 1 ~ 3 時間かかり、光学顕微鏡検査で変化が検出されるまでには少なくとも 6 ~ 8 時間かかります。 巨視的な変化は後になっても現れます。 たとえば、心筋梗塞の患者が狭心症発作(心筋への血流不足による痛み)の発症から数分後に死亡した場合、剖検では壊死の構造的証拠は明らかになりません。 急性発作後2日目に死亡した場合、変化は明らかです。
B. 組織化学的変化:細胞へのカルシウムイオンの流入は、不可逆的な損傷および壊死の形態学的兆候の出現と密接に関連しています。 正常な細胞では、細胞内カルシウム濃度は細胞外液の濃度の約 0.001 です。 この勾配は細胞膜によって維持され、細胞膜はカルシウムイオンを細胞外に積極的に輸送します。 虚血の結果として、またはさまざまな有毒物質の影響下で細胞が損傷した場合、その変化が不可逆的な場合にのみ細胞内のカルシウムの蓄積が観察されることが実験的に証明されています。 カルシウムは、エンドヌクレアーゼ (加水分解、DNA 切断)、ホスホリパーゼ (膜破壊)、およびプロテアーゼ (細胞骨格の破壊、消化) を活性化します。 それらの活性の増加は組織化学的方法によって検出されます。 酸化還元酵素(コハク酸デヒドロゲナーゼなど)の活性が急激に低下するか、消失します。
B. カーネルの変更:細胞壊死の重要かつ明白な形態学的兆候の 1 つは、核の構造の変化です。 死んだ細胞のクロマチンは凝縮して大きな塊になります。 核は体積が減少し、しわが寄って緻密になり、非常に好塩基性になります。つまり、ヘマトキシリンで濃い青色に染まります。 このプロセスは核濃縮(しわ)と呼ばれます。 その後、濃縮核は多数の小さな好塩基性粒子に破裂するか (核破壊)、またはリソソーム デオキシリボヌクレアーゼの作用の結果として溶解 (溶解) を受けることがあります (核分解)。 その後、体積が増加し、ヘマトキシリンで弱く染色され、核の輪郭が徐々に失われます。 急速に進行する壊死により、核は濃縮段階を経ずに溶解を起こします。
D. 細胞質の変化:細胞が壊死を起こしてから約 6 時間後、その細胞質は均一になり、好酸性が顕著になります。つまり、強酸性の染料で染色されます。たとえば、エオシンで染色するとピンク色になります。 これは光学顕微鏡によって検出される最初の変化であり、細胞質タンパク質の凝固とリボソームの破壊(消失)の結果として起こります。 リボソーム RNA は正常な細胞質に好塩基性の色合いを与えます。 心筋細胞の筋原線維などの特殊な細胞小器官が最初に消失します。 ミトコンドリアの膨張と細胞小器官膜の破壊(破壊)により、細胞質の空胞化が起こります。 最後に、細胞自体のリソソームから放出される酵素による細胞の消化により、細胞溶解 (自己溶解) が引き起こされます。 したがって、タンパク質の凝固は細胞質内で起こり、通常はそれらの凝集に置き換わります。
D. 細胞間物質の変化間質物質と繊維構造の両方をカバーします。 ほとんどの場合、フィブリノイド壊死に特徴的な変化が起こります。コラーゲン、弾性繊維、レチクリン線維が緻密で均質なピンク色の、場合によっては好塩基性の塊に変化し、断片化、塊状の崩壊、または溶解が起こる可能性があります。 頻度は低いですが、線維構造の浮腫、溶解、粘液が観察されることがありますが、これはコリコート壊死の特徴です。
壊死の臨床的および形態学的形態
壊死は、さまざまな臨床的および形態学的変化として現れます。 その違いは、臓器や組織の構造的および機能的特徴、壊死の速度と種類、およびその発生原因と発生条件によって異なります。 壊死の臨床的および形態学的形態の中で、凝固(乾性)壊死と液状(湿性)壊死が区別されます。
凝固性(乾性)壊死
このタイプの壊死では、死んだ細胞は数日間その形状を保ちます。 核を欠いた細胞は、凝固した均質なピンク色の細胞質の塊として現れます。
凝固性壊死のメカニズムはよくわかっていません。 細胞質タンパク質が凝固すると、細胞質タンパク質はリソソーム酵素の作用に対して耐性が生じ、その結果、液化が遅くなります。
凝固性壊死は、通常、腎臓、心筋、副腎、脾臓など、タンパク質が豊富で体液に乏しい臓器で発生します。通常、血液循環不足や酸素欠乏、物理的、化学的、その他の損傷因子の作用の結果として発生します。ウイルス感染による、または細菌および非細菌起源の有毒物質の作用による肝細胞の凝固性壊死(図6.1)。 凝固壊死は、それに伴って発生する死んだ領域が乾燥し、密で、崩れ、白または黄色になるという事実を特徴とするため、乾燥とも呼ばれます。
凝固壊死には次のようなものがあります。
A. 心臓発作- 内臓(脳を除く)の一種の血管(虚血性)壊死。 これは最も一般的なタイプの壊死です。
B. 乾酪(凝固)壊死結核、梅毒、ハンセン病のほか、リンパ肉芽腫症でも発症します。 特定の感染性肉芽腫で最も頻繁に見られるため、特異的とも呼ばれます。 内臓では、白っぽい黄色の組織の乾燥した崩れかけた限られた領域が現れます。 梅毒性肉芽腫では、そのような領域はもろくなく、アラビアの接着剤を思わせるペースト状であることがよくあります。 これは混合型(つまり、細胞外と細胞内)の壊死であり、実質と間質(細胞と線維の両方)の両方が同時に死滅します。 顕微鏡的には、そのような組織領域はヘマトキシリンとエオシンで染色された構造のない均質なピンク色のように見え、核クロマチンの塊(核破壊)がはっきりと見えます。
B. ワックス状壊死またはゼンカー壊死(筋肉壊死、多くの場合、前腹壁と大腿の内転筋の壊死。重度の感染症 - 腸チフス、発疹チフス、コレラを伴う)。
D. フィブリノイド壊死- フィブリノイドの腫れの結果として生じる結合組織壊死の一種。 フィブリノイド壊死は、アレルギー疾患や自己免疫疾患(リウマチ、関節リウマチ、全身性エリテマトーデスなど)で見られます。 血管の中膜のコラーゲン線維と平滑筋は最も深刻な損傷を受けます。 細動脈のフィブリノイド壊死は悪性高血圧症で観察されます。 この壊死は、正常なコラーゲン線維構造の喪失と、顕微鏡でフィブリンを模倣した均一な明るいピンク色の壊死物質の蓄積によって特徴付けられます。 「フィブリノイド」という用語は、「フィブリン性」という用語とは異なることに注意してください。後者は、たとえば血液凝固や炎症におけるフィブリンの蓄積を指します。 フィブリノイド壊死の領域には、さまざまな量の免疫グロブリン、補体、アルブミン、コラーゲンの分解産物、フィブリンが含まれています。
D. 脂肪壊死:
1.酵素的脂肪壊死:脂肪壊死は、膵臓酵素が管から周囲の組織に漏れ出すときに、急性膵炎や膵臓損傷で最も一般的に発生します。 膵リパーゼは脂肪細胞内のトリグリセリドに作用してグリセロールと脂肪酸に分解し、これらが血漿カルシウムイオンと相互作用してカルシウム石鹸を形成します。 同時に、不透明な白い(チョークのような)プラークや小結節(脂肪壊死)が膵臓の周囲の脂肪組織に現れます。
膵炎では、リパーゼが血流に入り、広範囲に分布し、体の多くの部分で脂肪壊死を引き起こす可能性があります。 最も一般的に損傷を受けるのは皮下脂肪と骨髄です。
2. 非酵素的脂肪壊死:非酵素的脂肪壊死は、乳腺、皮下脂肪組織および腹腔で観察されます。 ほとんどの患者には外傷歴があります。 非酵素的脂肪壊死は、外傷が根本的な原因として特定されない場合でも、外傷性脂肪壊死とも呼ばれます。 非酵素的脂肪壊死は、泡沫状の細胞質を有する多数のマクロファージ、好中球、およびリンパ球の存在を特徴とする炎症反応を引き起こします。 これに続いて線維化が起こり、このプロセスを腫瘍と区別するのが難しい場合があります。
E.壊疽(ギリシャ語から。 ガングライナ- 火):これは、外部環境と通信し、その影響下で変化する組織の壊死です。 「壊疽」という用語は、さまざまな重症度の二次細菌感染によって組織壊死が複雑になったり、外部環境と接触して二次的な変化を起こしたりする臨床的および形態学的状態を指すのに広く使用されています。 乾性、湿性、ガス壊疽、床ずれがあります。
1. 乾性壊疽- これは外部環境と接触した組織の壊死であり、微生物の関与なしに進行します。 乾性壊疽は、虚血性凝固組織壊死の結果として四肢に発生することがほとんどです。 壊死組織は黒く乾燥して見え、隣接する生存組織と明確に区別されます。 健康な組織との境界では、境界炎症が発生します。 色の変化は、硫化水素の存在下でのヘモグロビン生成色素の硫化鉄への変換によるものです。 例としては乾性壊疽があります。
アテローム性動脈硬化症と動脈の血栓症 (アテローム性動脈硬化性壊疽) を伴う手足、潰瘍性動脈内膜炎。
凍傷や火傷がある場合。
レイノー病または振動病のある指。
発疹チフスやその他の感染症のある皮膚。
治療は、境界線を目安に死んだ組織を外科的に除去することで行われます。
2. 湿性壊疽:重度の細菌感染による壊死組織変化が重なった結果として発症します。 微生物酵素の作用下で、二次的な凝集が起こります。 細胞自体では形成されず、外部から浸透する酵素による細胞溶解は、不均一溶解と呼ばれます。 微生物の種類は壊疽の局在に依存します。 湿性壊疽は通常、水分が豊富な組織で発生します。 四肢に発生することもありますが、腸間膜動脈閉塞による腸(血栓症、塞栓症)や肺炎(インフルエンザ、麻疹)の合併症としての肺などの内臓に発生することが多いです。 感染症(通常は麻疹)で衰弱した子供は、頬や会陰の軟部組織に湿性壊疽を発症することがあります。これはノーマ(ギリシャ語の名から水の癌)と呼ばれます。 急性の炎症と細菌の増殖により、壊死領域が浮腫状になり赤黒くなり、死んだ組織が広範囲に液状化します。 湿性壊疽では、隣接する健康な組織と明確に区別されずに広がる壊死性炎症が発生する可能性があるため、外科的治療が困難です。 細菌の活発な活動の結果、特有の臭いが発生します。 死亡率が非常に高い。
3.ガス壊疽:ガス壊疽は、傷口が嫌気性菌叢に感染すると発生します。 ウェルシュ菌およびこのグループの他の微生物。 これは、細菌の酵素活性の結果としての広範な組織壊死とガス形成を特徴とします。 主な症状は湿性壊疽に似ていますが、組織内にガスがさらに存在します。 クレピタス(触診時のパチパチ感) - 一般的 臨床症状で ガス壊疽。 死亡率も非常に高いです。
4.褥瘡(褥瘡):壊疽の一種として、褥瘡が分離されます。これは、床と骨の間で圧迫された身体の表面部分(皮膚、軟組織)の壊死です。 したがって、褥瘡は仙骨の領域、椎骨の棘突起、および大腿骨の大転子の領域に現れることがよくあります。 原因としては、これは血管や神経が圧迫されることによるトロフォン神経性壊死であり、心血管疾患、腫瘍疾患、感染症、または神経疾患を患う重篤な患者の組織栄養障害を悪化させます。
凝集(湿潤)壊死
凝集(湿潤)壊死は、死んだ組織の融合によって特徴付けられます。 それは、加水分解プロセスにとって好ましい条件が存在する、タンパク質が比較的少なく、体液が豊富な組織で発生します。 細胞溶解は、それ自体の酵素の作用の結果として起こります (自己溶解)。 湿性凝集性壊死の典型的な例は、脳の灰色の軟化(虚血性梗塞)の焦点です。
脳梗塞は、主な肉眼的兆候が常に病変部の脳組織の弾性の低下であるため、脳梗塞は軟化と呼ばれることがよくあります。 初日は、触ると柔らかい、チアノーゼの色合いのはっきりと限られた領域で表されます。 1日目が終わる頃には、焦点がより鮮明になり、青白くなります。 翌日、この領域の脳の物質はさらにたるんだ、黄色がかった色になり、場合によっては緑がかった色になることもあります。 最初の数週間は、浮腫により脳の体積がわずかに増加します。 1~1.5ヶ月後。 梗塞の部位には、かなり明確に定義された空洞が形成され、 濁った液体そしてデトリタス。 心臓発作の正確なタイミングを判断することは、外観だけでなく組織学的画像からも非常に困難です。
顕微鏡的に見ると、脳組織は均質で構造がなく、ヘマトキシリンとエオシンで染色するとわずかにピンク色になります。 死んだ組織の吸収は、脂肪粒状の球のように見えるマクロファージによって行われます。
壊死の臨床症状
全身的な症状:壊死を伴うと、通常、発熱(壊死細胞および組織からの発熱性物質の放出による)および好中球性白血球増加症(急性炎症反応-境界炎症の存在による)が現れます。 壊死細胞内容物の放出:壊死細胞の細胞質内容物の放出された成分(酵素など)は血流に入り、その存在により壊死の局在が診断されます。 これらの酵素は、さまざまな実験室の方法で検出できます (表 6.1)。 酵素の出現の特異性は、体のさまざまな組織における酵素の主な局在に依存します。 たとえば、クレアチンキナーゼの MB アイソザイムのレベルの増加は、心筋壊死の特徴です。これは、この酵素が心筋細胞にのみ存在するためです。 アスパラギン酸アミノトランスフェラーゼ (AST) は心筋だけでなく肝臓や他の組織にも存在するため、アスパラギン酸アミノトランスフェラーゼ (AST) のレベルの増加はあまり特異的ではありません。 トランスアミナーゼの出現は肝細胞壊死の特徴です。
局所的な症状:消化管の粘膜の潰瘍は、出血や出血によって複雑になる場合があります(出血性消化性潰瘍など)。 浮腫の結果として組織体積が増加すると、限られた空間(たとえば、虚血性壊死または出血性壊死を伴う頭蓋腔内)内で重大な圧力上昇が生じる可能性があります。
機能障害:壊死は臓器の機能不全を引き起こします。たとえば、心筋(急性心筋)の広範な壊死(梗塞)の結果として急性心不全が発生します。 虚血性疾患ハート)。 臨床症状の重症度は、種類、罹患組織の総量に対する体積、および残りの生体組織の機能の維持によって異なります。 たとえ腎臓全体が失われたとしても、もう一方の腎臓がその損失を補うことができるため、一方の腎臓の壊死は腎不全を引き起こしません。 しかし、大脳皮質の対応する部分の小さな領域が壊死すると、対応する筋肉群の麻痺が引き起こされます。
壊死の結果。壊死は不可逆的なプロセスです。 比較的良好な結果では、死んだ組織の周囲で反応性炎症が発生し、死んだ組織の境界が決まります。 このような炎症は境界と呼ばれ、境界領域は境界領域と呼ばれます。 このゾーンでは 血管膨張、充血、浮腫が現れ、多数の白血球が現れ、加水分解酵素を放出して壊死塊を溶かします。 壊死塊はマクロファージによって吸収されます。 これに続いて、結合組織の細胞が増殖し、壊死領域に置き換わるか、過剰増殖します。 死んだ塊を結合組織に置き換えるとき、彼らはその組織について話します。 このような場合の壊死部位には瘢痕が形成されます(心臓発作部位の瘢痕)。 壊死領域の汚れ 結合組織カプセル化につながります。 カルシウム塩は、乾燥壊死の際の死塊内、および組織化された壊死の中心に沈着する可能性があります。 この場合、壊死の焦点の石灰化(石化)が発生します。 場合によっては、壊死の領域で骨形成、つまり骨化が認められます。 組織残骸の吸収とカプセルの形成により、通常は湿性壊死で最も多くの場合脳内で発生し、壊死部位に空洞嚢胞が現れます。
壊死の好ましくない結果は、壊死の病巣が化膿性(敗血症)で溶けることです。 隔離とは、自己消化を受けず、結合組織によって置き換えられず、生きた組織の間に自由に位置する死んだ組織の領域の形成です。 隔離者は通常、骨髄の炎症、つまり骨髄炎を伴う骨で発生します。 このような隔離器の周囲には、隔離嚢と膿で満たされた空洞が形成されます。 非常に多くの場合、隔離器は、完全に配置された後にのみ閉じられる瘻孔を介して空洞を残します。 指の端の隔離、切断、拒絶反応の一種。
壊死の意味。それはその本質、つまり「局所的な死」とそのようなゾーンの機能からの除外によって決定されるため、重要な臓器、特にそれらの広い領域の壊死はしばしば死につながります。 心筋梗塞、脳の虚血性壊死、腎臓の皮質壊死、進行性肝壊死、膵臓壊死を合併した急性膵炎などです。 多くの場合、組織壊死は、多くの病気の重篤な合併症(筋軟化症における心破裂、出血性脳卒中や虚血性脳卒中の麻痺、大きな床ずれによる感染症、壊疽などの組織崩壊生成物の体内への曝露による中毒)の原因となります。手足など)。 臨床症状壊死は非常に多様である可能性があります。 脳または心筋の壊死領域で発生する異常な電気活動は、てんかん発作や心臓不整脈を引き起こす可能性があります。 壊死した腸における蠕動運動の違反は、機能的(動的)腸閉塞を引き起こす可能性があります。 壊死組織への出血、たとえば肺壊死を伴う喀血(喀血)がよく観察されます。
体内の細胞死は、壊死とアポトーシスの 2 つの方法で発生します。 アポトーシスは、細胞自体がその死の過程に積極的に関与する一種の細胞死です。 細胞は自己破壊します。 アポトーシスは、壊死とは異なり、活発なプロセスです。病因因子にさらされると、特定の遺伝子の活性化、タンパク質や酵素の合成を伴い、遺伝的にプログラムされた反応カスケードが引き起こされ、効果的かつ迅速な細胞の除去につながります。ティッシュから。
アポトーシスの理由:
1. 胚形成中、アポトーシスはさまざまな組織原基の破壊と器官の形成において重要な役割を果たします。
2. サイトカインの供給を使い果たしたリンパ球など、発生サイクルを完了した老化細胞ではアポトーシスが発生します。
3. 成長中の組織では、娘細胞の特定の部分がアポトーシスを起こします。 死滅する細胞の割合は、全身および局所のホルモンによって制御できます。
4. アポトーシスの原因は、損傷因子の弱い影響である可能性があり、強度が高くなると壊死を引き起こす可能性があります(低酸素、電離放射線、毒素など)。
アポトーシスの病因:
修復システムによって修復できない DNA 損傷が核に発生すると、細胞はアポトーシスを起こします。 このプロセスは、p53 遺伝子によってコードされるタンパク質によって監視されます。 p53タンパク質の作用下でDNA欠陥を除去できない場合、アポトーシスプログラムが活性化されます。
多くの細胞には受容体があり、その受容体への影響によりアポトーシスが活性化されます。 最もよく研究されているのは、リンパ球に見られる Fas 受容体と、多くの細胞に見られる腫瘍壊死因子アルファ (TNF-α) 受容体です。 これらの受容体は、自己反応性リンパ球の除去と、フィードバック方式による細胞集団のサイズの一定性の制御において重要な役割を果たします。
抗炎症性サイトカイン、ステロイドホルモン、一酸化窒素 (NO)、フリーラジカルなど、さまざまな代謝産物やホルモンがアポトーシスを活性化する可能性があります。
組織内の酸素が不足すると、細胞のアポトーシスが活性化されます。 その活性化の理由は、フリーラジカルの作用、DNA修復のエネルギー依存プロセスの中断などである可能性があります。
アポトーシスは、細胞間マトリックス、基底膜、または隣接する細胞との接触を失った細胞に起こります。 腫瘍細胞におけるこのアポトーシス機構の喪失は、転移能力の出現につながります。
一部のウイルスタンパク質は、ウイルスが感染細胞内で自己集合した後、細胞のアポトーシスを活性化する可能性があります。 隣接する細胞によるアポトーシス小体の吸収により、ウイルスが感染します。 エイズウイルスは、表面に CD4 受容体を持つ未感染細胞のアポトーシスを活性化することもあります。
アポトーシスを防ぐ要因もあります。 性ホルモンや炎症促進性サイトカインなどの多くの代謝産物やホルモンは、アポトーシスを遅らせることができます。 アポトーシスは、p53 遺伝子の変異やアポトーシスを阻害する遺伝子 (bcl-2) の活性化など、細胞死のメカニズムの欠陥によって劇的に遅くなる可能性があります。 多くのウイルスは、ウイルス自身の構造タンパク質の合成期間中にウイルス自身の DNA を細胞ゲノムに組み込んだ後、アポトーシスを阻害する能力を持っています。
アポトーシスの形態学的発現
壊死
壊死は、生体内の個々の細胞、器官および組織の一部の死を特徴とする不可逆的なプロセスです。 病理学的状態における壊死はさまざまな疾患で観察され、このプロセスの一般的なパターン、その形態学的および臨床的兆候についての知識は、壊死のプロセスで発生する疾患の診断と治療に役立ちます。そのため、さまざまな専門分野の代表者がこの研究に従事しています。壊死の研究。 その主な目標は、これらのプロセスを制御する能力、つまり細胞、組織、器官の進行性の破壊をそれら自体の酵素の影響下に置くことを可能にする手段の探索です。 したがって、当然のことながら、壊死の形態および病因の研究、ならびに生理的条件下で遺伝子型の特徴によってプログラムされた細胞死(アポトーシス)の研究が、非常に初期の変化と最も重要な変化に重点を置いた研究である。 初期段階。 したがって、さまざまなレベルでの壊死とアポトーシスの研究は、死の過程についてより深い知識を得る可能性をもたらします。 同時に、器官、組織、細胞の構造的および機能的特徴、および個々の特徴に応じて、壊死の発生原因、発現メカニズム、結果、および壊死の詳細を確認することが重要です。マクロ生物。
用語
壊疽(ガングレイン - 火) - 外部環境と接触した組織の壊死。
心臓発作(梗塞 - 詰め物) - 内臓の組織壊死(1)、血液循環が障害されたときに発生する組織壊死(2)。 機能的な末端血管を持つ臓器の急性循環障害(血栓症、塞栓症、長期の血管けいれん)で発生する壊死の一種(つまり、血管壊死)。 内臓の死んだ組織の肉眼で見える領域(3)。
マランティック壊死 - 悪液質や精神異常の症状を伴う、栄養失調の患者や高齢者の褥瘡。
筋軟化症(マラカス - 柔らかい) - 死んだ組織の溶解。
ミイラ化 (mumificatio - 乾燥) - 死んだ組織の乾燥、圧縮。
ノーマ(ノーム - 「水がん」) - 子供の頬の軟部組織の湿った壊疽。
壊死 (nekros - 死) - 壊死、生体内の細胞および組織の死。
ネクロバイオシス(nekros - 死、bios - 生命) - 壊死に先行する変化、可逆的なジストロフィープロセス。 ゆっくりとした死のプロセス。
Sequestrum (sequestrum) - 自己消化を受けず、結合組織に置き換えられず、生きた組織の間に自由に位置する死んだ組織の一部。
弾性分解 - 弾性繊維の膨張、崩壊、溶融。
死
死生物学的概念としてのそれは、生物の生命の不可逆的な停止を表現したものです。 死が始まると、人は死体、つまり死体になります。 (死体)。
と 法的な観点ほとんどの国で 脳活動が完全かつ不可逆的に停止した場合、生物は死んだものとみなされます。 .
しかし同時に、法的に死んだ生物の多数の細胞や組織は、死後しばらくの間生存し続けます。
これらの臓器および組織は、移植用の臓器の主な供給源を構成します。
壊死(局所的死)
細胞死は体の生命活動の継続的な現れであり、健康な状態では細胞の生理学的再生によってバランスが保たれているということを知っておく必要があります。 細胞の構造コンポーネントと細胞全体の両方が摩耗し、老化し、死滅し、交換する必要があります。 さまざまな臓器や組織を健康な状態に維持することは、「自然な」生理学的再生がなければ不可能であり、したがって個々の細胞が死ななければなりません。 この細胞死は 1972 年に「細胞死」と呼ばれました。 アポトーシス」。 アポトーシス - プログラムされた細胞死です。 。 しかし、細胞死は、外部の損傷(病原性)因子の「暴力的な」作用の結果として、生体において発生する可能性があります。 この細胞死を 「壊死」。死んだ細胞は完全に機能を停止します。 細胞死には、不可逆的な生化学的および構造的変化が伴います。
アポトーシス - 細胞への事前の不可逆的な損傷を伴わない細胞死ですが、細胞の死を事前に決定する遺伝的プログラムが組み込まれた結果、1964 年にプログラム細胞死と呼ばれました。プログラム細胞死は、発生、成長、生存中に発生します。組織の形成、および形態形成の過程で構造を構築する際には、一部の細胞(損傷を受けてライフサイクルを完了した細胞を含む)を除去する必要があります。 逆説的な状況が生じます。組織、器官、生物など、全体を保存するために細胞が自らの命を犠牲にし、自殺するのです。 したがって、プログラム細胞死の生物学的重要性は生命の維持にあります。 プログラムされた細胞死は、以下のような生物学的プロセスに不可欠な部分です。 胚の発生、生物の形態形成と変態。 の 多細胞生物プログラムされた細胞死と有糸分裂の間のバランスが組織の恒常性をもたらします。
「プログラムされた細胞死」と「アポトーシス」という用語は同義語ではありません。 「プログラムされた細胞死」という用語は、文献において狭義と広義の両方で使用されます。
狭義には、プログラムされた細胞死はアポトーシスとは対照的です。前者は通常、生物の発育中および組織の恒常性を維持しながら発生するためです。 同時に、病理学的条件下ではアポトーシス、つまり細胞の自殺が発生します。
広い意味では、「プログラムされた細胞死」の概念は、アポトーシスによる細胞死だけでなく、液胞死、オートファジー死、萎縮死、細胞が最終分化に達した後の死など、他の多くの種類の細胞死も意味します。 。
したがって、 細胞死次の 2 つの方法で発生する可能性があります。 壊死とアポトーシス。 生物学的兆候、および壊死とアポトーシスの重要性は大きく異なるため、これらのプロセスは個別に考慮されます。
壊死(ギリシャ語から。 ネクロス- 死亡) - 病原性因子の影響下での生体内の細胞および組織の壊死、死。 このタイプの細胞死 遺伝子的に制御されていない。
壊死の原因。 壊死を引き起こす要因:
- 物理的 (銃創、放射線、電気、低温および高温 - 凍傷および火傷);
- 毒 (酸、アルカリ、重金属塩、酵素、薬物、エチルアルコールなど);
- 生物学的 (細菌、ウイルス、原生動物など);
- アレルギー性 (エンド抗原およびエキソ抗原、たとえば、感染性アレルギー疾患および自己免疫疾患におけるフィブリノイド壊死、アルサス現象)。
- 血管 (心臓発作 - 血管壊死);
- トロフォニューロティック (褥瘡、治癒しない潰瘍)。
状況に応じて、 病原因子の作用機序 区別:
- 直接壊死要因(外傷性、毒性、生物学的壊死)の直接作用により、
- 間接的な壊死これは、血管および神経内分泌系を介して間接的に起こります(アレルギー性、血管およびトロフォン神経性壊死)。
壊死の病因の種類:
1. 外傷性 - 物理的および化学的要因の作用下で発生します。
2. 有毒 - 細菌などの毒素の作用により発生します。
3. トロフォン神経症 - 微小循環と組織の神経支配の障害に関連します。
4. アレルギー - 免疫病理学的反応を伴って発症します。
5. 血管 - 臓器または組織への血液供給の障害に関連します。
壊死のメカニズム
壊死のメカニズムは自己消化のメカニズムとは異なり、多様であり、損傷因子の性質と、壊死が発生する細胞、組織、器官の構造的および機能的特徴に大きく依存します。 壊死のすべての病因メカニズムの最終結果は、細胞内カオスの発生です。 壊死のさまざまな病因経路の中から、おそらく最も重要な 5 つの経路を区別することができます: 1) ユビキチンへの細胞タンパク質の結合、2) ATP 欠乏、3) 活性酸素種の生成、4) カルシウム恒常性の障害、および 5)細胞膜による選択的透過性の喪失。
• 最も保存されたタンパク質の 1 つであるユビキチンは、プロテアソームの一部として他のタンパク質のポリペプチド鎖のリジン残基と共有結合を形成します。 ユビキチンおよび熱ショックタンパク質ファミリーのタンパク質の合成は、さまざまな損傷を増強します。 したがって、アルツハイマー病やパーキンソン病の中枢神経系の細胞、およびアルコール性肝障害のある肝細胞には、タンパク質とユビキチンの複合体であるプロテオソームが見つかります。 肝細胞内のこのような複合体は、マロリー小体として長い間知られてきました。
• 死にかけている細胞では ATP 欠乏が常に見られます。 長い間、虚血中の心筋細胞壊死の主な原因は、マクロ作動性化合物の形成が一定レベルまで減少することであると考えられていた。 近年、虚血性損傷には他のメカニズムが関与していることが示されています。 したがって、虚血性心筋が再灌流を受けると、壊死性変化がより迅速かつ大規模に発生します。 記載されている変化は再灌流損傷と呼ばれます。 カルシウム阻害剤(クロルプロマジンなど)や抗酸化剤を使用しているにもかかわらず 低レベル ATP は再灌流損傷を軽減します。これは、ATP 欠乏だけでは壊死の発症に十分ではないことを示しています。
• 活性酸素種 (一重項酸素、スーパーオキシドアニオンラジカル、ヒドロキシルアニオン、過酸化水素など) の生成は、生細胞内で常に発生します。 膜脂質や DNA 分子と相互作用して酸化ストレスを引き起こし、活性酸素種は膜透過性を高め、カチオンポンプを阻害し、ATP 欠乏と過剰な細胞内カルシウムを増強し、細胞や組織の損傷を引き起こします。 最高値活性酸素種は、酸素療法の結果として発症する新生児窮迫症候群における肺細胞壊死、心筋梗塞における再灌流傷害、およびパラセタモール過剰摂取における肝細胞壊死の病因に関与している。
• カルシウム恒常性の違反は、死にかけている細胞における細胞内カルシウムの蓄積によって特徴付けられます。 生きた細胞では、細胞内のカルシウムイオン濃度は細胞外の濃度の約1,000分の1です。 損傷の初期変化は、ATP 欠乏によるカチオンポンプの機能不全に関連しています。 この場合、カルシウムは細胞内、主にミトコンドリアに蓄積します。 Ca2+ 依存性プロテアーゼとホスホリパーゼが活性化され、膜 (ミトコンドリア、細胞質) に不可逆的な損傷を与え、透過性がさらに損なわれ、細胞死につながります。
細胞質膜の選択的透過性の喪失は、その原因の 1 つです。 特性補体曝露による壊死、ウイルス感染、低酸素損傷。 この場合、細胞内への特定の物質の通過を調節する膜貫通タンパク質、受容体、酵素系に損傷が発生します。 補体とパーフォリンの影響下で、タンパク質ポリメラーゼが細胞膜に挿入されます。 溶解ウイルスはまた、膜脂質と相互作用し、ウイルスカプシドタンパク質を膜脂質に取り込み、ウイルスが感染細胞から離れる瞬間に細胞膜の破壊を引き起こします。 虚血にさらされた細胞では、膜貫通タンパク質の配置が乱れ、特徴的なタンパク質の「低酸素」シールが形成されます。
壊死の形態形成壊死プロセスは、壊死、壊死、細胞死、自己消化などのさまざまな形態形成段階を経ます。
壊死不全 - 壊死と似ていますが、可逆的な変化です。
ネクロバイオシスは、同化反応よりも異化反応が優勢であることを特徴とする不可逆的な変性変化です。
細胞死。その時間を確定するのは困難です。
自己分解 - 死んだ細胞および炎症性浸潤の細胞の加水分解酵素の作用による死んだ基質の分解。
形態学的基準は、細胞死を判定するために最も一般的に使用されます。 EM における細胞損傷の不可逆性に関するこのような信頼できる基準は、ミトコンドリアにおけるタンパク質とカルシウム塩を含む電子密度の高い沈着物の沈着とその内膜の破壊です。 SM では、細胞構造の変化は自己消化の段階でのみ目に見えます。 したがって、壊死の顕微鏡的兆候と言えば、実際には自己消化の段階での形態学的変化について話していることになります。
壊死の形態
壊死の肉眼的兆候
すべての形態の壊死に共通するのは、壊死組織の色、粘稠度、および場合によっては臭いの変化です。 壊死した組織は緻密で乾燥した質感を持つ場合があり、これは凝固性壊死で観察されます。 この場合、組織はミイラ化される可能性があります。 他の場合には、死んだ組織はたるんだもので、大量の体液を含み、筋軟化症(ギリシャ語のマラカスから - 柔らかい)を起こします。 このような一貫性のある壊死は共液性と呼ばれます。 壊死性腫瘤の色は、血液の不純物やさまざまな色素の存在によって決まりますが、また、死んだ組織と生きた組織の境界に赤茶色の境界炎症領域が発生することにも起因します。 死んだ組織は白または黄色がかっており、多くの場合赤茶色の花冠に囲まれています。 血液が染み込むと、壊死塊は赤から茶色、黄色、緑色に変化します(壊死塊中の特定のヘモグロビン色素の優勢に応じて)。 場合によっては、壊死の病巣が胆汁で染色されることがあります。 腐敗が溶けると、死んだ組織は特有の悪臭を放ちます。 心臓発作は色によって、白(脾臓、脳)、出血性の花冠を伴う白(心臓、腎臓)、赤(出血性)に分けられます。 出血性花冠は、死んだ組織と生きた組織の境界で自然に発生する境界炎症領域によって形成されます。 梗塞の赤い色は、慢性静脈充血を背景とした肺梗塞の場合と同様、壊死組織に血液が染み込むことによるものです。
壊死の形態学的兆候
壊死の前には壊死の期間があり、その形態学的基質は異栄養性変化である。
A. 初期の変更:ネクロバイオシスの初期段階では、細胞は形態学的に変化していません。 電子顕微鏡または組織化学検査で認識できる変化が現れるまでには 1 ~ 3 時間かかり、光学顕微鏡検査で変化が検出されるまでには少なくとも 6 ~ 8 時間かかります。 巨視的な変化は後になっても現れます。 たとえば、心筋梗塞の患者が狭心症発作(心筋への血流不足による痛み)の発症から数分後に死亡した場合、剖検では壊死の構造的証拠は明らかになりません。 急性発作後2日目に死亡した場合、変化は明らかです。
B. 組織化学的変化:細胞へのカルシウムイオンの流入は、不可逆的な損傷および壊死の形態学的発現の出現と密接に関連しています。 正常な細胞では、細胞内カルシウム濃度は細胞外液の濃度の約 0.001 です。 この勾配は細胞膜によって維持され、細胞膜はカルシウムイオンを細胞外に積極的に輸送します。 虚血の結果として、またはさまざまな有毒物質の影響下で細胞が損傷した場合、その変化が不可逆的な場合にのみ細胞内のカルシウムの蓄積が観察されることが実験的に証明されています。 カルシウムは、エンドヌクレアーゼ (加水分解、DNA 切断)、ホスホリパーゼ (膜破壊)、およびプロテアーゼ (細胞骨格の破壊、消化) を活性化します。 それらの活性の増加は組織化学的方法によって検出されます。 酸化還元酵素(コハク酸デヒドロゲナーゼなど)の活性が急激に低下するか、消失します。
B. カーネルの変更:核の変化は細胞壊死の最良の証拠です。 死んだ細胞のクロマチンは凝縮して大きな塊となり、核は体積が減少し、しわが寄り、密度が高く、好塩基性が強くなり、つまりヘマトキシリンで濃い青色に染まります。 このプロセスの名前は 核濃縮症(しわ)。その後、濃縮核は破裂して多数の小さな好塩基性粒子になる可能性があります ( 核崩壊症)、またはリソソームデオキシリボヌクレアーゼの作用の結果として溶解(溶解)を受けます。 (核分解)。 その後、体積が増加し、ヘマトキシリンで弱く染色され、核の輪郭が徐々に失われます。 急速に進行する壊死により、核は濃縮段階を経ずに溶解を起こします。
D. 細胞質の変化:細胞が壊死を起こしてから約 6 時間後、その細胞質は均一になり、強好酸性になります。つまり、強酸性の染料で染色されます (たとえば、エオシンで染色するとピンク色になります)。 これは光学顕微鏡によって検出される最初の変化であり、細胞質タンパク質の凝固とリボソームの破壊(消失)の結果として起こります。 リボソーム RNA は正常な細胞質に好塩基性の色合いを与えます。 心筋細胞の筋原線維などの特殊な細胞小器官が最初に消失します。 ミトコンドリアの膨張と細胞小器官膜の破壊(破壊)により、細胞質の空胞化が起こります。 最後に、細胞自体のリソソームから放出される酵素による細胞の消化により、細胞溶解 (自己溶解) が引き起こされます。 このように、細胞質では タンパク質の凝固、通常は次のように置き換えられます 共謀。
D. 細胞間物質の変化間質物質と繊維構造の両方をカバーします。 ほとんどの場合、フィブリノイド壊死に特徴的な変化が起こります。コラーゲン、弾性繊維、レチクリン線維が緻密で均質なピンク色の、場合によっては好塩基性の塊に変化し、断片化、塊状の崩壊、または溶解が起こる可能性があります。 頻度は低いですが、線維構造の浮腫、溶解、粘液が観察されることがありますが、これはコリコート壊死の特徴です。
壊死の臨床的および形態学的形態
壊死は、さまざまな臨床的および形態学的変化として現れます。 その違いは、臓器や組織の構造的および機能的特徴、壊死の速度と種類、およびその発生原因と発生条件によって異なります。 壊死の臨床的および形態学的形態には、次のものがあります。 凝固(乾燥)壊死と 共和(湿式)壊死。
A. 凝固(乾性)壊死:このタイプの壊死では、死んだ細胞は数日間その形状を保ちます。 核を欠いた細胞は、凝固した均質なピンク色の細胞質の塊として現れます。
凝固性壊死のメカニズムはよくわかっていません。 細胞質タンパク質が凝固すると、細胞質タンパク質はリソソーム酵素の作用に対して耐性が生じ、その結果、液化が遅くなります。
凝固壊死 通常はで起こります タンパク質が豊富で体液が少ない臓器 例えば、腎臓、心筋、副腎、脾臓では、通常、不十分な血液循環や酸素欠乏、物理的、化学的、その他の損傷因子の作用の結果として起こります。例えば、ウイルス損傷時またはウイルス損傷時の肝細胞の凝固壊死などです。細菌および非細菌起源の有毒物質の作用。 凝固壊死 とも呼ばれている ドライ 、それに伴って発生する死んだ領域が乾燥し、密で、崩れ、白または黄色であるという事実が特徴であるためです。
凝固壊死には次のようなものがあります。
- 心臓発作 - バラエティ 血管(虚血性)壊死 内臓(脳を除く - 脳卒中)。 これは最も一般的なタイプの壊死です。
- 硬質(凝固した)壊死は、結核、梅毒、ハンセン病、さらにはリンパ肉芽腫症でも発生します。 特定の感染性肉芽腫で最も頻繁に見られるため、特異的とも呼ばれます。 内臓では、限られた領域の組織が現れ、乾燥して崩れ、色は白っぽい黄色になります。 梅毒性肉芽腫では、そのような領域はもろくなく、アラビアの接着剤を思わせるペースト状であることがよくあります。 これは混合型(つまり、細胞外と細胞内)の壊死であり、実質と間質(細胞と線維の両方)の両方が同時に死滅します。 顕微鏡で見ると、そのような組織領域は構造がなく均質で、ヘマトキシリンとエオシンでピンク色に染まり、核クロマチンの塊(核破壊)がはっきりと見えます。
- ワックス状、またはゼンカー壊死(筋肉壊死、より多くの場合、前腹壁と大腿部で、重度の感染症 - 腸チフス、発疹チフス、コレラを伴う);
- フィブリノイド壊死- 結合組織壊死の一種で、フィブリノイドの腫れの結果としてすでに研究されており、アレルギー疾患や自己免疫疾患(リウマチ、関節リウマチ、全身性エリテマトーデスなど)で最もよく観察されます。 血管の中膜のコラーゲン線維と平滑筋は最も深刻な損傷を受けます。 細動脈のフィブリノイド壊死は悪性高血圧症で観察されます。 フィブリノイド壊死は、正常な構造の喪失と、顕微鏡で見るとフィブリンのように見える均一な明るいピンク色の壊死物質の蓄積を特徴とします。 「フィブリノイド」は「フィブリン性」とは異なることに注意してください。後者は、血液凝固や炎症などにおけるフィブリンの蓄積を指します。 フィブリノイド壊死の領域には、さまざまな量の免疫グロブリン、補体、アルブミン、コラーゲンの分解産物、フィブリンが含まれています。
- 脂肪壊死:
1. 酵素的脂肪壊死: 脂肪壊死は、膵臓酵素が管から周囲の組織に漏れ出すときに、急性膵炎や膵臓損傷で最も一般的に発生します。 膵リパーゼは脂肪細胞内のトリグリセリドに作用してグリセロールと脂肪酸に分解し、これらが血漿カルシウムイオンと相互作用してカルシウム石鹸を形成します。 同時に、不透明な白い(チョークのような)プラークや小結節(脂肪壊死)が膵臓の周囲の脂肪組織に現れます。
膵炎では、リパーゼが血流に入り、広範囲に分布し、体の多くの部分で脂肪壊死を引き起こす可能性があります。 最も一般的に損傷を受けるのは皮下脂肪と骨髄です。
2. 非酵素的脂肪壊死: 非酵素的脂肪壊死は、乳腺、皮下脂肪組織および腹腔で観察されます。 ほとんどの患者には外傷歴があります。 非酵素的脂肪壊死は、外傷が根本的な原因として特定されない場合でも、外傷性脂肪壊死とも呼ばれます。 非酵素的脂肪壊死は、泡沫状の細胞質を有する多数のマクロファージ、好中球、およびリンパ球の存在を特徴とする炎症反応を引き起こします。 これに続いて線維化が起こり、このプロセスを腫瘍と区別するのが難しい場合があります。
- 壊疽 (ギリシャ語から ガングライナ- 火) : これは、外部環境と通信し、その影響下で変化する組織の壊死です。 「壊疽」という用語は、さまざまな重症度の二次細菌感染によって組織壊死が複雑化したり、外部環境との接触によって二次変化が生じたりする臨床的および形態学的状態を指すのに広く使用されています。 乾性、湿性、ガス壊疽、床ずれがあります。
1. 乾燥性壊疽 - これは外部環境と接触した組織の壊死であり、微生物の関与なしに進行します。 乾性壊疽は、虚血性凝固組織壊死の結果として四肢に発生することがほとんどです。 壊死組織は黒く乾燥して見え、隣接する生存組織と明確に区別されます。 健康な組織との境界では、境界炎症が発生します。 色の変化は、硫化水素の存在下でのヘモグロビン生成色素の硫化鉄への変換によるものです。 例としては次のようなものが考えられます 乾燥性壊疽 :
アテローム性動脈硬化症と動脈血栓症のある手足 ( アテローム性動脈硬化性壊疽 )、動脈内膜炎を消滅させる。
凍傷や火傷がある場合。
レイノー病または振動病のある指。
発疹チフスやその他の感染症のある皮膚。
治療は、境界線を目安に死んだ組織を外科的に除去することで行われます。
2. 湿性壊疽 :重度の細菌感染による壊死組織変化が重なった結果として発症します。 微生物酵素の作用下で、二次的な凝集が起こります。 細胞自体で発生するのではなく、外部から浸透する酵素による細胞の溶解は、 不均一分解。 微生物の種類は壊疽の局在に依存します。 湿性壊疽は通常、水分が豊富な組織で発生します。 四肢に発生することもありますが、腸間膜動脈閉塞による腸(血栓症、塞栓症)や肺炎(インフルエンザ、麻疹)の合併症としての肺などの内臓に発生することが多いです。 感染症(通常は麻疹)で衰弱した子供は、頬や会陰の軟部組織に湿性壊疽を発症することがあります。これは「ノーマ」(ギリシャ語から)と呼ばれます。 名前- 水ザリガニ)。 急性の炎症と細菌の増殖により、壊死領域が浮腫状になり赤黒くなり、死んだ組織が広範囲に液状化します。 湿性壊疽では、隣接する健康な組織と明確に区別されずに広がる壊死性炎症が発生する可能性があるため、外科的治療が困難です。 細菌の活発な活動の結果、特有の臭いが発生します。 死亡率が非常に高い。
3. ガス壊疽 : ガス壊疽は、傷口が嫌気性菌叢に感染すると発生します。 ウェルシュ菌およびこのグループの他の微生物。 これは、細菌の酵素活性の結果としての広範な組織壊死とガス形成を特徴とします。 主な症状は湿性壊疽に似ていますが、組織内にガスがさらに存在します。 クレピタス(触診上のパチパチ音現象)は、ガス壊疽の一般的な臨床症状です。 死亡率も非常に高いです。
4.褥瘡(褥瘡): 壊疽の一種として、褥瘡が分離されます。これは、床と骨の間で圧迫された身体の表面部分(皮膚、軟組織)の壊死です。 したがって、褥瘡は仙骨の領域、椎骨の棘突起、および大腿骨の大転子の領域に現れることがよくあります。 原因としては、これは血管や神経が圧迫されることによるトロフォン神経性壊死であり、心血管疾患、腫瘍疾患、感染症、または神経疾患を患う重篤な患者の組織栄養障害を悪化させます。
B. コリケート(湿潤)壊死:死んだ組織が溶けることが特徴です。 タンパク質が比較的少なく、体液が豊富な組織で発生します。 加水分解プロセス . 細胞溶解それ自体の酵素の作用の結果として起こります( 自己消化)。 湿性凝集性壊死の典型的な例は、脳の灰色の軟化(虚血性梗塞)の焦点です。
脳梗塞はしばしば軟化と呼ばれます。 巨視的 兆候は、病変内の脳組織の弾性が常に低下していることです。 初日は、触ると柔らかい、チアノーゼの色合いのはっきりと限られた領域で表されます。 1日目が終わる頃には、焦点がより鮮明になり、青白くなります。 翌日、この領域の脳の物質はさらに弛緩し、その色は黄色がかったり、緑色がかった色になったりします。 最初の数週間は、浮腫により脳の体積がわずかに増加します。 1~1.5ヶ月後。 梗塞の部位には、濁った液体と残骸を含むかなりはっきりとした空洞が形成されます。 心臓発作の正確なタイミングを判断することは、外観だけでなく組織学的画像からも非常に困難です。
顕微鏡的に 脳組織は均質で構造がなく、ヘマトキシリンとエオシンで染色するとわずかにピンク色になります。 死んだ組織の吸収は、脂肪粒状の球のように見えるマクロファージによって行われます。
壊死の臨床症状
全身的な症状:壊死を伴うと、通常、発熱(壊死細胞および組織からの発熱性物質の放出による)および好中球性白血球増加症(急性炎症反応-境界炎症の存在による)が現れます。 壊死細胞の内容物の放出: 壊死細胞の細胞質内容物の放出された成分(酵素など)が血流に入り、その存在が 診断値壊死の位置を特定します。 これらの酵素はさまざまな場所で見つけることができます。 実験方法。 酵素の出現の特異性は、体のさまざまな組織における酵素の主な局在に依存します。 たとえば、クレアチンキナーゼの MB アイソザイムのレベルの増加は、心筋壊死の特徴です。これは、この酵素が心筋細胞にのみ存在するためです。 アスパラギン酸アミノトランスフェラーゼ (AST) は心筋だけでなく肝臓や他の組織にも存在するため、アスパラギン酸アミノトランスフェラーゼ (AST) のレベルの増加はあまり特異的ではありません。 トランスアミナーゼの出現は肝細胞壊死の特徴です。
局所的な症状:消化管の粘膜の潰瘍は、出血や出血によって複雑になる場合があります(出血性消化性潰瘍など)。 浮腫の結果として組織体積が増加すると、限られた空間(たとえば、虚血性壊死または出血性壊死を伴う頭蓋腔内)内で重大な圧力上昇が生じる可能性があります。
機能違反:壊死は臓器の機能不全につながります。たとえば、心筋の広範な壊死(梗塞)の結果として急性心不全が発生します(急性冠状動脈性心疾患)。 臨床症状の重症度は、種類、罹患組織の総量に対する体積、および残りの生体組織の機能の維持によって異なります。 たとえ腎臓全体が失われたとしても、もう一方の腎臓がその損失を補うことができるため、一方の腎臓の壊死は腎不全を引き起こしません。 しかし、運動皮質の小さな領域が壊死すると、対応する筋肉群の麻痺が引き起こされます。
壊死の結果。 壊死は不可逆的なプロセスです。で 比較的有利な 死んだ組織の周囲で結果が発生する 反応性炎症 、死んだ組織を区切ります。 この炎症はこう呼ばれます 境界線 , そして境界ゾーン 境界ゾーン。 このゾーンでは、血管が拡張し、充血、浮腫が発生し、多数の白血球が現れ、加水分解酵素を放出し、壊死塊を溶かします。 壊死塊はマクロファージによって吸収されます。 これに続いて、結合組織の細胞が増殖し、壊死領域に置き換わるか、過剰増殖します。 死んだ塊を結合組織に置き換えるとき、彼らは次のように話します。 組織 . このような場合、壊死部位では、 傷跡 (梗塞部位の傷跡)。 壊死領域が結合組織で汚れると、 カプセル化 と。 カルシウム塩は、乾燥壊死の際の死塊内、および組織化された壊死の中心に沈着する可能性があります。 この場合、発展するのは、 石灰化(石化) 壊死の焦点 . 場合によっては、壊死部位に骨形成が認められることもあります。 骨化 . 組織残骸の吸収とカプセルの形成により、通常は湿性壊死とともに起こり、最も多くの場合脳内で、壊死部位に空洞が現れます。 嚢胞。
不利な結果 壊死 - 壊死の焦点の化膿性(敗血症性)の溶解。 隔離 - これは、自己消化を受けず、結合組織によって置き換えられず、生きた組織の間に自由に位置する死んだ組織の一部の形成です。 隔離者は通常、骨髄の炎症、つまり骨髄炎を伴う骨で発生します。 このような隔離器の周囲には、隔離嚢と膿で満たされた空洞が形成されます。 非常に多くの場合、隔離器は、完全に配置された後にのみ閉じられる瘻孔を介して空洞を残します。 隔離の一種 切断 - 指の先端の拒絶反応。
壊死の意味。それはその本質、つまり「局所的な死」とそのようなゾーンの機能からの除外によって決定されるため、重要な臓器、特にそれらの広い領域の壊死はしばしば死につながります。 心筋梗塞、脳の虚血性壊死、腎臓の皮質壊死、進行性肝壊死、膵臓壊死を合併した急性膵炎などです。 多くの場合、組織壊死は、多くの病気の重篤な合併症(筋軟化症における心破裂、出血性脳卒中や虚血性脳卒中の麻痺、大きな床ずれによる感染症、壊疽などの組織崩壊生成物の体内への曝露による中毒)の原因となります。手足など)。 壊死の臨床症状は非常に多様です。 脳または心筋の壊死領域で発生する異常な電気活動は、てんかん発作や心臓不整脈を引き起こす可能性があります。 壊死した腸における蠕動運動の違反は、機能的(動的)腸閉塞を引き起こす可能性があります。 多くの場合、壊死組織での出血、たとえば肺壊死を伴う喀血(喀血)が発生します。
アポトーシス
アポトーシス、また プログラムされた細胞死 、内部または外部の要因が影響するプロセスです。 遺伝プログラムを活性化する 鉛 細胞死と組織からの効果的な除去につながります。アポトーシス- これは細胞死のメカニズムであり、壊死による多くの独特の生化学的および形態学的特徴を持っています。
アポトーシス- これ 生化学的に特異的なタイプの細胞死 、活性化が特徴です 非リソソーム内因性エンドヌクレアーゼ 、分割した 核DNA小さな断片に。 形態学的アポトーシス表示されます ランダムに配置された単一細胞の死 丸みを帯びた形状を伴い、 膜に囲まれた おうし座 (「アポトーシス体」)、 周囲の細胞によってすぐに貪食されます。
これは、体の不要な細胞や欠陥細胞が除去されるエネルギー依存のプロセスです。 彼は大きな役割を果たしています 形態形成において 臓器のサイズを一定に制御するためのメカニズムです。 アポトーシスが減少すると、細胞の蓄積が起こります。たとえば、 腫瘍の増殖。 アポトーシスの増加に伴い、組織内の細胞数の漸進的な減少が観察されます。たとえば、 萎縮 .
アポトーシスの形態学的発現
アポトーシスには、光学レベルと超微細構造レベルの両方で、独自の独特の形態学的特徴があります。 ヘマトキシリン・エオシンで染色すると、アポトーシスが判定されます。 単細胞 また 小さな細胞のグループ . アポトーシス細胞は、核クロマチンの高密度の断片を含む、非常に好酸性の細胞質の円形または楕円形の塊として現れます。 細胞の収縮と形成が行われるため、 アポトーシス体 急速に発生し、それと同じくらい急速に貪食され、分解され、または臓器の内腔に排出され、その後、 組織学的標本では、重大な重症度の場合に見られます。。 そのほか アポトーシス - 壊死とは対照的に - 炎症反応を伴うことはありませんそのため、組織学的同定も複雑になります。
ネクローシスとアポトーシスの比較特性
| サイン | アポトーシス | 壊死 |
| 誘導 | 生理学的または病理学的刺激によって活性化される | ダメージ要因に応じてさまざま |
| 有病率 | シングルケージ | 細胞群 |
| 生化学的変化 | 内在性エンドヌクレアーゼによるエネルギー依存性の DNA 断片化。 リソソームは無傷です。 |
イオン交換の違反または終了。 酵素はリソソームから放出されます。 |
| DNAの崩壊 | 断片への分裂を伴う核内凝縮 | 壊死細胞におけるびまん性局在 |
| 細胞膜の完全性 | 保存されました | 違反しました |
| 形態学 | 圧縮されたクロマチンによるアポトーシス小体の形成による細胞の縮小と断片化 | 細胞の膨張と溶解。 |
| 炎症反応 | いいえ | 通常はそこにあります |
| 死んだ細胞の除去 | 隣接する細胞による吸収(貪食) | 好中球およびマクロファージによる吸収(食作用)。 |
形態学的特徴が最も明確に明らかになります 電子顕微鏡による観察。 アポトーシスを起こしている細胞は次のような特徴を持ちます ( アポトーシス 形態形成 ):
細胞の収縮。セルのサイズが縮小されます。 細胞質が厚くなる。 比較的正常に見える細胞小器官はよりコンパクトです。
細胞の形状と体積の違反は、アポトーシス細胞におけるトランスグルタミナーゼの活性化の結果として起こると考えられています。 この酵素は細胞質タンパク質の架橋形成を進行させ、これにより上皮細胞の角質化と同様に、細胞膜の下に一種の殻が形成されます。
クロマチンの凝縮。これはアポトーシスの最も特徴的な症状です。 クロマチンは核膜の下の周囲に沿って凝縮し、明確に定義された高密度の塊を形成します。 さまざまな形そしてサイズ。 核は 2 つ以上の断片に分解されることがあります。
機構 クロマチン凝縮よく勉強しました。 これらの変化は、個々のヌクレオソームに結合する部位での核 DNA の切断に関連しており、塩基対の数が 180 ~ 200 で割り切れる多数の断片の発生につながります。 これらの断片は、電気泳動中の階段の特徴的な画像を示します。 このパターンは、DNA 断片の長さが変化する細胞壊死のパターンとは異なります。 ヌクレオソームにおける DNA の断片化は、カルシウム感受性エンドヌクレアーゼの作用下で発生します。 エンドヌクレアーゼは一部の細胞 (胸腺細胞など) に永続的に存在し、細胞質内に遊離カルシウムが出現することによって活性化されますが、他の細胞ではアポトーシスが始まる前に合成されます。 しかし、エンドヌクレアーゼによる DNA 切断後にクロマチン凝縮がどのように起こるかはまだ確立されていません。
細胞質における空洞およびアポトーシス体の形成。アポトーシス細胞では、最初に深い表面の陥入が形成されて空洞が形成され、核断片の有無にかかわらず、細胞質と密に詰まった細胞小器官からなる膜で囲まれたアポトーシス小体の形成による細胞断片化が引き起こされます。
アポトーシス細胞またはアポトーシス体の食作用 周囲の健康な細胞、実質、またはマクロファージ 。 アポトーシス小体はリソソーム内で急速に破壊され、周囲の細胞が移動または分裂して、細胞死後に空いた空間を埋めます。
食作用マクロファージまたは他の細胞によるアポトーシス小体は、これらの細胞上の受容体によって活性化され、アポトーシス細胞を捕捉して飲み込みます。 マクロファージ上のそのような受容体の 1 つはビトロネクチン受容体であり、これは b 3 インテグリンであり、アポトーシスを起こした好中球の食作用を活性化します。
アポトーシス以下に参加します 生理学的および病理学的プロセス:
胚形成中のプログラムされた細胞破壊 (着床、器官形成を含む)および 変態。 胚形成中のアポトーシスは必ずしも「プログラムされた細胞死」を反映しているわけではないという事実にもかかわらず、このアポトーシスの定義はさまざまな研究者によって広く使用されています。
成人におけるホルモン依存性臓器退縮 , 例えば、月経周期中の子宮内膜の脱落、閉経期における卵胞の閉鎖、授乳の停止後の乳腺の退縮などです。
細胞集団の増殖中の一部の細胞の除去
腫瘍内の個々の細胞の死 主にその退縮ですが、活発に成長する腫瘍にも当てはまります。
免疫系の細胞の死 , サイトカインの枯渇後のBリンパ球とTリンパ球の両方、および胸腺での発達中の自己反応性T細胞の死。
ホルモン依存性臓器の病的萎縮、 たとえば、去勢後の前立腺の萎縮やグルココルチコイド療法中の胸腺のリンパ球の枯渇などです。
排泄管閉塞後の実質臓器の病的萎縮 , 膵臓や唾液腺、腎臓で観察されるもの。
細胞傷害性T細胞の作用による細胞死 , たとえば、移植拒絶反応や移植片対宿主病などです。
一部のウイルス疾患における細胞損傷 , たとえば、ウイルス性肝炎では、アポトーシス細胞の断片がカウンシルマン小体として肝臓内で検出されます。
さまざまな損傷因子の作用による細胞死、 壊死を引き起こす可能性がありますが、少量で作用します。 高温、電離放射線、抗がん剤。
アポトーシスの制御
アポトーシスは遺伝的に制御された細胞死です。 。 現在、アポトーシスの制御に必要な物質をコードする多数の遺伝子が同定されている。 これらの遺伝子の多くは、回虫から昆虫、哺乳類に至る進化の過程で保存されてきました。 それらの一部はウイルスのゲノムにも含まれています。 したがって、主な 生化学プロセス異なる実験系(主に回虫やハエを対象とした研究が行われます)におけるアポトーシスは同一であるため、研究結果を他の系(人体など)に直接転送することができます。
アポトーシス調整できます:
- 外部要因 ,
- 自律メカニズム .
A. 外部要因の影響。
アポトーシスは、次のような多くの外部要因によって制御されます。 DNA損傷。 で 回復不能な DNA損傷 アポトーシスによって、身体にとって潜在的に危険な細胞が除去されます。 このプロセスにおいて重要な役割を果たすのは、 p53腫瘍抑制遺伝子 。 アポトーシスの活性化にもつながります ウイルス感染症、細胞増殖の調節不全、細胞の損傷、組織の周囲または基底物質との接触の喪失。 アポトーシスは損傷した細胞の存続に対する身体の防御であり、多細胞生物にとって潜在的に危険な場合があります。
何かで組織を刺激すると、 マイトジェン その細胞は有糸分裂活動が亢進した状態に入り、これには必然的に何らかの影響が伴います。 アポトーシスの活性化 。 娘細胞の運命は、生き残るかアポトーシスを起こすかによって決まります。 アポトーシスの活性化因子と阻害因子の比率 :
阻害剤含む 成長因子、細胞基質、性ステロイド、一部のウイルスタンパク質。
活性化因子には、成長因子の欠如、マトリックス結合の喪失、グルココルチコイド、一部のウイルス、フリーラジカル、電離放射線が含まれます。
活性化剤にさらされた場合、または阻害剤が存在しない場合、 アクティベーション 内因性プロテアーゼと エンドヌクレアーゼ . これは細胞骨格の破壊、DNA断片化、ミトコンドリアの機能障害を引き起こします。 細胞は縮小しますが、その膜は無傷のままですが、細胞への損傷は食作用の活性化につながります。 死んだ細胞は膜に囲まれた小さな断片に崩壊し、これをアポトーシス小体と呼びます。 アポトーシス細胞に対する炎症反応は起こらない .
B. アポトーシスの自律的メカニズム。
胚の発生中に、自律的アポトーシスの 3 つのカテゴリが区別されます。 形態形成、組織形成、系統発生。
形態形成アポトーシス さまざまな組織の基礎の破壊に関与します。 例は次のとおりです。
- 指間隙の細胞の破壊。
細胞死は、硬口蓋の形成中の口蓋突起の融合中に過剰な上皮の破壊を引き起こします。
- 閉鎖中の神経管の背側部分における細胞死。これは上皮、神経管の両側および関連する中胚葉の一体化を達成するために必要です。
これら 3 つの局在における形態形成アポトーシスの違反が発生につながります。 それぞれ合指症、口蓋裂、二分脊椎症です。
組織遺伝学的アポトーシス これは組織や器官の分化の際に観察され、例えば組織原基からの生殖器官のホルモン依存性分化で観察されます。 したがって、男性では、胎児の睾丸のセルトリ細胞が、アポトーシスによるミュラー管(女性ではそこから卵管、子宮、上部膣が形成される)の退行を引き起こすホルモンを合成します。
系統発生的なアポトーシス 前腎などの胚の基本的な構造の除去に関与します。
さまざまな条件下で次のように観察できます。 アポトーシスの加速と減速。 それでも アポトーシス特定の細胞型に特有のさまざまな要因によって活性化される可能性がありますが、 アポトーシスの最終経路は、十分に確立された遺伝子によって制御されており、アポトーシス活性化の原因に関係なく一般的です。
アポトーシスを強化または弱めるすべての要因が作用する可能性があります
- 細胞死のメカニズムに直接影響する ,
- 転写制御に影響を与えることにより間接的に .
場合によっては、これらの因子がアポトーシスに与える影響が決定的なものになることがあります(たとえば、 グルココルチコイド依存性胸腺細胞アポトーシス )、他の場合では特に重要ではありません(たとえば、 Fas および TNF 依存性のアポトーシス )。 規制プロセスには多数の物質が関与しており、その中で最も研究されているのは、 家族 bcl-2
Bcl-2 遺伝子は、濾胞性リンパ腫細胞内で転座し、アポトーシスを阻害する遺伝子として最初に記載されました。 さらに調査を進めたところ、次のことが判明しました。 Bcl-2 は多重遺伝子です回虫にも存在します。 また、一部のウイルスでは相同遺伝子が見つかっています。 このクラスに属するすべての物質は次のように分類されます。 アポトーシスの活性化剤と阻害剤 .
に 阻害剤関連: bcl-2、 bcl-xL、Mcl-1、bcl-w、 アデノウイルス E1B 19K、エプスタイン・バーウイルス BHRF1。
活性化剤へ関連 バックス、 bak、Nbk/Bik1、不良、bcl-xS。
この家族のメンバーは互いに交流します。 の一つ 規制のレベル アポトーシスは相互作用です タンパク質-タンパク質。 bcl-2 ファミリーのタンパク質は、ホモ二量体とヘテロ二量体の両方を形成します。 たとえば、bcl-2 阻害剤は bcl-2 活性化剤と二量体を形成する可能性があります。 したがって 細胞生存率はアポトーシスの活性化因子と阻害因子の比率に依存します。 たとえば、bcl-2 は bax と相互作用しますが、前者が優勢であれば細胞生存率は増加し、後者が過剰であれば細胞生存率は低下します。 さらに、bcl-2 ファミリーのタンパク質は、このシステムに属さないタンパク質と相互作用する可能性があります。 たとえば、bcl-2 は R- とペアにすることができます。 ラスアポトーシスを活性化します。 別のタンパク質である Bag-1 は、アポトーシスを阻害する bcl-2 の能力を強化します。
現在認められているのは、 遺伝子参加している 腫瘍の成長と発達の調節において (がん遺伝子とがん抑制遺伝子 )、 遊ぶ 規制の役割 V 誘導 アポトーシス。 これらには次のものが含まれます。
bcl-2 癌遺伝子 , どれの 阻害するホルモンやサイトカインによって引き起こされるアポトーシス。細胞生存率の増加につながります。
タンパク質 バックス (家族からも bcl-2 ) 二量体を形成する バックス、バックス , アポトーシス活性化因子の作用を強化します。 bcl-2 と bax の比率は、アポトーシス因子に対する細胞の感受性を決定し、組織が成長するか萎縮するかを決定する「分子スイッチ」です。
c-myc 癌遺伝子 , だれの タンパク質製品アポトーシスまたは細胞増殖のいずれかを刺激することができます(たとえば、他の生存シグナルの存在下で) bcl-2)
p53遺伝子 , 通常はアポトーシスを活性化しますが(野生型 - 野生型)、突然変異した場合(変異型 - 通常、腫瘍細胞で免疫組織化学的研究が行われます。この場合、野生型の量は無視され、これに基づいて挙動が予測されます)腫瘍組織の一部が構築される、つまり、p53 遺伝子のタンパク質産物が大量に形成される - アポトーシスの阻害について話しているため、予後は好ましくありません)または欠如(一部の腫瘍で見られる)により、細胞の生存率が増加します。 p53は、電離放射線による細胞損傷の場合のアポトーシスに必要であるが、グルココルチコイドや老化によって引き起こされるアポトーシスには必要ではないことが確立されています。
アポトーシスの減少
p53 遺伝子産物は、有糸分裂中のゲノムの完全性を監視します。 ゲノムの完全性に違反する セルはに切り替わります アポトーシス。逆に、 タンパク質 bcl-2アポトーシスを阻害する。 したがって、 p53の欠如またはbcl-2の過剰は細胞の蓄積を引き起こす : これらの障害はさまざまな腫瘍で観察されます。 アポトーシスを制御する因子の研究は発達において重要です 薬悪性新生物細胞の死を促進します。
自己免疫疾患は、自己抗原と反応できるリンパ球におけるアポトーシスの誘導の障害を反映している可能性があります。 たとえば、全身性エリテマトーデスでは、次のような違反があります。 Fas受容体リンパ球の細胞表面に存在し、アポトーシスの活性化につながります。 いくつかの ウイルスは感染細胞のアポトーシスを阻害することで生存率を高めます。 たとえば、エプスタイン・バーウイルスは代謝に影響を与える可能性があります。 bcl-2 .
アポトーシスの促進
アポトーシスの加速は、後天性免疫不全症候群(AIDS)、神経栄養性疾患、および形成要素が欠乏している一部の血液疾患で証明されています。 エイズでは、免疫不全ウイルスが活性化する可能性があります。 CD4受容体 感染していないTリンパ球について したがって、アポトーシスが加速され、このタイプの細胞の枯渇につながります。
生物の発生および病理学的過程におけるアポトーシスの重要性
アポトーシスは、哺乳動物の発生およびさまざまな病理学的プロセスにおいて重要な役割を果たします。 機能している bcl-2胚発生中にリンパ球、メラノサイト、腸上皮、腎臓細胞の生存能力を維持するために必要です。 bcl-x は、胚形成中の細胞死、特に神経系の細胞死を抑制するために必要です。 Bax は、胸腺細胞のアポトーシスと、精子の発生中の生存能力の維持に必要です。 p53 は腫瘍抑制遺伝子であるため、胚形成には特別な役割を果たしませんが、腫瘍の増殖抑制には必要です。 両方の p53 遺伝子を欠損したマウスでは、前腫瘍細胞のアポトーシスが完全または部分的に損なわれた結果、悪性腫瘍を発症する極めて高い傾向が観察されました。 bcl-2 遺伝子によってコードされるタンパク質の合成が増加すると、アポトーシスが抑制され、それに応じて腫瘍の発生が抑制されます。 この現象はB細胞濾胞性リンパ腫細胞で見られます。
マウスのリンパ増殖性疾患および全身性エリテマトーデス様疾患では、Fas リガンドまたは Fas 受容体の機能が障害されます。 Fas リガンド合成の増加により、移植片の拒絶反応が防止される可能性があります。
アポトーシスは、細胞がアデノウイルス、HIV、インフルエンザウイルスに感染したときの病理学的プロセスの一部です。 感染が持続する潜伏期にはアポトーシスの阻害が観察され、アデノウイルス、おそらくヘルペスウイルス、エプスタイン・バーウイルス、HIVの複製の増加に伴ってアポトーシスの活性化が観察され、これがウイルスの広範な蔓延に寄与します。アポトーシスと多くの病理学的状態との直接的な関係は明らかです。 アポトーシスを制御する多くの遺伝子の機能不全の研究は、これらの疾患の治療におけるまったく新しい方向性を開発する機会を提供します。 アポトーシスを制御できる薬剤の開発は、悪性腫瘍、ウイルス感染症、および一部の疾患の治療に新たな可能性を開くでしょう。 神経系、免疫不全および自己免疫疾患。 たとえば、次のようなとき 悪性腫瘍リンパ増殖性疾患ではアポトーシスを増強する必要があり、細胞損傷を特徴とする疾患ではアポトーシスを弱める必要があります。
詳細
壊死- 壊死、つまり生体内の細胞や組織が死滅し、その生命活動が完全に停止すること。
壊死プロセスは一連の過程を経ます 段階 :
- 壊死不全 - 壊死と同様の可逆的な変化
- 壊死症 - 不可逆的なジストロフィー変化(同時に、異化反応が同化反応よりも優勢になります)
- 細胞死
- 自己分解 - 加水分解酵素とマクロファージの作用による死んだ基質の分解
壊死の顕微鏡的兆候:
1) カーネルの変更
- 核濃縮症- 核のしわ。 この段階では、非常に好塩基性になり、ヘマトキシリンで濃い青色に染まります。
- 核崩壊症- 核の好塩基性断片への崩壊。
- 核分解- 核の溶解
核のピクノーシス、レクシス、溶解が次々に起こり、プロテアーゼ(リボヌクレアーゼとデオキシリボヌクレアーゼ)の活性化のダイナミクスを反映しています。 壊死が急速に進行すると、核濃縮の段階を経ずに核が溶解します。
2) 細胞質の変化
- 血漿凝固。 まず、細胞質が均質かつ好酸性になり、その後タンパク質の凝固が起こります。
- プラズマヘキシス
- 原形質溶解
融解によって細胞全体が捕捉される場合(細胞溶解)もあれば、一部のみが捕捉される場合(限局性結石壊死またはバルーンジストロフィー)もあります。
3) 細胞間物質の変化
A) コラーゲン線維、弾性線維、レチクリン線維血漿タンパク質を含浸して膨潤し、緻密で均質な塊に変化し、断片化または塊状の崩壊または溶解を起こします。
線維構造の破壊は、コラゲナーゼとエラスターゼの活性化に関連しています。
レチクリン線維は、非常に長期間壊死変化を受けないため、多くの壊死組織で見られます。
b) 中間物質は、グリコサミノグリカンの解重合と血漿タンパク質の含浸により膨潤し、融解します。
組織が壊死すると、組織の粘稠度、色、匂いが変化します。 組織が緻密で乾燥したり(ミイラ化)、たるんだり溶けたりすることがあります。
生地は白や白黄色のものが多いです。 また、血液が染み込んでいると暗赤色になることもあります。 皮膚、子宮、皮膚の壊死は、多くの場合、灰緑色、黒色になります。
壊死の原因。
壊死の原因に応じて、次のタイプが区別されます。
1) 外傷性壊死
物理的および化学的要因(放射線、温度、電気など)が組織に直接作用した結果です。
例: 高温にさらされると組織の火傷が発生し、低温にさらされると凍傷が発生します。
2) 有毒 壊死
これは、細菌および非細菌起源の毒素が組織に直接作用した結果です。
例: ジフテリア外毒素の影響下での心筋細胞の壊死。
3) トロフォニューロティック 壊死
神経組織の栄養が障害されると発生します。 その結果、循環障害、ジストロフィー性および壊死を引き起こす壊死性変化が生じます。
例:床ずれ。
4) アレルギー 壊死
これは、感作された生物における即時型過敏反応の発現です。
例: アルサス現象。
5) 血管 壊死- 心臓発作
血栓塞栓症、長期にわたるけいれんにより動脈内の血流が侵害または停止した場合に発生します。 血流が不十分になると、酸化還元プロセスの停止により虚血、低酸素、組織死が引き起こされます。
に 直接壊死には、外傷性壊死と中毒性壊死が含まれます。 直接的な壊死は、病原性因子の直接的な影響によるものです。
間接的壊死は血管系および神経内分泌系を介して間接的に発生します。 この壊死発生のメカニズムは、種 3 ~ 5 に典型的です。
壊死の臨床的および形態学的形態。
それらは、壊死が発生する臓器や組織の構造的および機能的特徴、その発生の原因、および発生の条件を考慮して区別されます。
1) 凝固(乾性)壊死
乾性壊死は、長期間加水分解を受けない可能性のある難溶性化合物の形成を伴うタンパク質変性のプロセスに基づいています。
結果として生じる死んだ領域は、乾燥し、密な、灰色がかった黄色になります。
凝固性壊死は、タンパク質が豊富で体液が少ない臓器(腎臓、心筋、副腎など)で発生します。
一般に、死んだ組織と生きた組織との間の明確な境界を明確に認識することができる。 境界に強い境界炎症があります。
例:
ワックス状(ゼンカー)壊死(急性感染症における腹直筋)
心臓発作
梅毒、結核による乾酪(チーズ状壊死)
乾燥性壊疽
フィブリノイド - アレルギー疾患や自己免疫疾患で観察される結合組織の壊死。 血管の中膜のコラーゲン線維と平滑筋は深刻な損傷を受けます。 これは、コラーゲン線維の正常な構造が失われ、フィブリンに似た(!)明るいピンク色の均一な壊死物質が蓄積することを特徴としています。
2)共液性(湿性)壊死
それは死んだ組織の溶解、嚢胞の形成を特徴とします。 タンパク質が比較的少なく、体液が豊富な組織で発生します。 細胞溶解は、それ自体の酵素の作用の結果として起こります (自己溶解)。
死んだ組織と生きた組織の間に明確な領域はありません。
例:
虚血性脳梗塞
乾燥壊死の塊が溶けると、二次凝集が起こります。
3) 壊疽
壊疽- 外部環境(皮膚、腸、肺)と接触した組織の壊死。 この場合、組織は灰褐色または黒色になりますが、これは血液色素の硫化鉄への変換に関連しています。
a) 乾性壊疽
微生物の関与なしに外部環境と接触した組織の壊死。 ほとんどの場合、虚血性凝固壊死の結果として四肢に発生します。
壊死した組織は空気の影響で乾燥し、しぼんで圧縮され、生存可能な組織とは明確に区別されます。 健康な組織との境界では、境界炎症が発生します。
境界炎症- 死んだ組織の境界を定める死んだ組織の周囲の反応性炎症。 制限ゾーンはそれぞれ境界です。
例: - アテローム性動脈硬化症および血栓症における四肢壊疽
凍傷または火傷
b) 湿性壊疽
これは、細菌感染による壊死組織変化が重なった結果として発症します。 酵素の作用下で、二次的な凝集が起こります。
組織は腫れ、浮腫状になり、悪臭を放つようになります。
湿性壊疽の発生は、循環障害、リンパ循環によって促進されます。
湿性壊疽では、生きた組織と死んだ組織の明確な区別がないため、治療が複雑になります。 治療のためには、濡れた壊疽を乾燥させてから切断する必要があります。
例:
腸の壊疽。 腸間膜動脈の閉塞(血栓、塞栓症)、虚血性大腸炎、急性腹膜炎によって発症します。 漿膜は鈍く、フィブリンで覆われています。
床ずれ。 褥瘡 - 圧力を受けた体の表面領域の壊死。
ノーマは水っぽい癌です。
c) ガス壊疽
傷口が嫌気性菌叢に感染すると発生します。 これは、広範囲の組織壊死と細菌の酵素活性の結果としてのガスの形成を特徴とします。 一般的な臨床症状はクレピタスです。
4) 隔離者
自己消化を受けない死んだ組織の領域は、結合組織によって置き換えられず、生きた組織の間に自由に位置します。
例: - 骨髄炎の隔離剤。 このような隔離器の周りには、カプセルと膿で満たされた空洞が形成されます。
軟組織
5) 心臓発作
血管壊死、虚血の結果および極度の発現。 心臓発作の発症の理由は、長期にわたるけいれん、血栓症、動脈塞栓症、および血液供給が不十分な状態での臓器の機能的ストレスです。
a) 心臓発作の形態
ほとんどの場合、心臓発作はくさび形です(くさびの基部が嚢に面し、先端が臓器の門に面しています)。 このような心臓発作は脾臓、腎臓、肺で発生しますが、これらの臓器の構造の性質、つまり動脈の主な分岐の種類によって決まります。
まれに、壊死の形状が不規則になります。 このような壊死は、心臓、腸、すなわち、主要でない、緩い、または混合型の動脈の分岐が優勢な臓器で発生する。
b) 値
心臓発作は臓器の大部分または全体に及ぶ場合もあり(亜計または全心臓発作)、顕微鏡下でのみ検出される場合(微小梗塞)もあります。
c) 外観
- 白
これは白黄色の領域であり、周囲の組織から十分に区切られています。 通常、側副循環が不十分な組織(脾臓、腎臓)で発生します。
- 出血性のハローのある白色
これは白と黄色の領域で表されますが、この領域は出血領域に囲まれています。 これは、梗塞の周囲に沿った血管のけいれんが血管の拡張と出血の発症に取って代わられるという事実の結果として形成されます。 このような心臓発作は心筋で発生します。
- 赤(出血性)
壊死部位は血液で飽和しており、暗赤色で境界がはっきりしています。 これは、主要な種類の血液供給がない、静脈うっ血が特徴的な臓器で発生します。 それは肺(気管支動脈と肺動脈の間に吻合があるため)、腸で発生します。
壊死の臨床症状。
1) 全身症状:発熱、好中球性白血球増加症。 細胞内酵素は血液中で決定されます。クラチンキナーゼの MB アイソザイムは心筋壊死とともに増加します。
2) 地元 症状
3) 機能障害
壊死の結果:
1) 境界線
比較的良好な結果では、死んだ組織の周囲に反応性炎症が発生し、死んだ組織と健康な組織とが区別されます。 このゾーンでは、血管が拡張し、充血や浮腫が発生し、多数の白血球が現れます。
2) 組織
死んだ塊を結合組織に置き換えます。 このような場合、壊死部位に瘢痕が形成されます。
3) カプセル化
結合組織による壊死領域の汚れ。
4) 石化
石灰化。 カプセル内にカルシウム塩が蓄積する。
5) 骨化
極度の石化。 壊死部位での骨形成。
6) 化膿性融合
これが敗血症における心臓発作の化膿性融合です。