A méhnyak rosszindulatú daganata, meghatározatlan rész. Méhnyakrák - leírás, kezelés. Kapjon kezelést Koreában, Izraelben, Németországban és az Egyesült Államokban
A betegség egyszerűbb megjelölésére kitalálták a betegségek nemzetközi osztályozását, amelybe beletartoznak az onkológiai betegségek is. A méhrák ICD 10 kódja van kijelölve C54.
Letisztult lokalizáció
- C54.0 - Inferior szegmens vagy isthmus.
- C54.1 - Endometriumrák.
- C54.2 - Myometrium.
- C54.3 - Méhfenék.
- C54.8 - A méh teste a fenti területeken túlnyúlik.
- C54.9 - Finomítatlan zóna
A női nemi szervek daganata
Ez a csoport magában foglalja az összes rosszindulatú daganatot, amely a női reproduktív rendszerben található.
- C51 - Vulva.
- C52 - Hüvelyek.
- C53 - Méhnyak.
- C54 - Test.
- C55 - A méh finomítatlan zónája.
- C56 - Petefészek.
- C57 - A nőgyógyászati női reproduktív rendszer finomítatlan lokalizációja.
- C58 - Placenta.
Ez a csoport viszont szerepel a felsőoktatási rendszerben C00 - D48.
Onkológia
A test vagy a méhnyak rákja - a szerv nyálkahártyájának hámsejtjeinek mutációja következtében alakul ki, ami ellenőrizetlen osztódással járó új növekedést okoz, amely növekszik és elpusztítja a közeli sejteket és szöveteket.
Okok és tényezők
A méhrák gyakrabban fordul elő idősebb nőknél a menopauza kezdete után. De fiatal lányok között is vannak speciális esetek fiatalabb korban.
- Genetikai hajlam.
- A szexuális tevékenység megtagadása.
- Meddőség.
- Nők, akik 25 év után soha nem szültek.
- Elhízás és rossz táplálkozás.
- Dohányzás, alkoholfogyasztás.
- Cukorbetegség.
- A hormonális fogamzásgátlók és gyógyszerek helytelen használata.
A női test bármely hormonális egyensúlyhiánya esetén a talaj a hormonfüggő karcinóma kialakulásához.
Jelek, tünetek, rendellenességek
- Gyakori láz, egyéb észrevehető tünet nélkül.
- Súlyos hasi fájdalom.
- Később a fájdalom az ágyéki régióba kezd kisugározni.
- Véres vagy akár gennyes hüvelyváladék, kellemetlen szaggal. Ebben az esetben a vér a menstruációs cikluson kívül áramolhat.
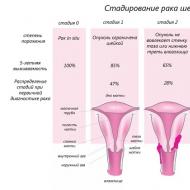
Szakasz

- 1. szakasz - a kezdeti szakaszban a neoplazma az endometrium zónájában található, és nem lépi át a bélést.
- 2. szakasz - a daganat hatással lehet a nyaki csatornára és az intracervikális mirigyekre.
- 3. szakasz - a helyi nyirokcsomók, a hüvely és a hasüreg károsodása és áttét.
- 4. szakasz - a metasztázisok a véren keresztül behatolnak a távoli szervekbe.
Diagnosztika
- Szemrevételezéses vizsgálat nőgyógyász által.
- Biopszia a gyanús képződményekről.
- A hasüreg ultrahangja.
- MRI a részletesebb vizsgálathoz.
- Tumormarkerek tesztjei a tumornövekedés dinamikájának és a kezelés minőségének nyomon követésére.
RCHR (A Kazah Köztársaság Egészségügyi Minisztériumának Köztársasági Egészségfejlesztési Központja)
Változat: Archívum – A Kazah Köztársaság Egészségügyi Minisztériumának klinikai jegyzőkönyvei – 2012 (883. sz., 165. sz. rendelet)
Méhnyak, nem meghatározott rész (C53.9)
Általános információ
Rövid leírás
Klinikai protokoll "Méhnyakrák"
Jelenleg a világ fejlett országaiban jelentős előrelépés történt a méhnyakrák (CC) megelőzésében, korai diagnosztizálásában és kezelésében. Ez elsősorban annak tudható be, hogy a méhnyakrák előfordulása más onkológiai betegségektől eltérően jól kontrollált, hiszen a betegségnek egyértelmű etiológiája, egyértelmű és gyakran hosszú rákmegelőző stádiuma és egyértelmű lokális terjedési tendenciája van.
Így Ausztráliában egy szűrőprogram 1994-es bevezetésével közel 2-szeresére - 100 ezer női lakosságra vetítve - 13,2-ről 6,9-re sikerült csökkenteni az incidenciát, míg az Ausztrál Egészségügyi Intézet szerint a méhnyakrák okozta halálozást 4,0-ról 1,9-re csökkent (1).
Így ha a fejlett országok megtanulták kontrollálni a CC miatti megbetegedést és mortalitást, akkor a világ nagy része még mindig úton van e felé. A WHO statisztikái pedig ezt igazolják: 2005-ben például több mint 500 000 ezer új megbetegedést regisztráltak, és ezek 90%-a fejlődő gazdaságú országokhoz tartozott.
Szintén 2005-ben 260 000 nő halt bele a betegségbe, körülbelül 95%-uk a fejlődő országokban, többségük meg nem erősített diagnózissal, és nem jutott hozzá a megfelelő kezeléshez, amely meghosszabbíthatta volna az életét.
A Kazah Köztársaságban 2007 végén 9269 nő állt onkológus felügyelete alatt, 1233 új esetet regisztráltak, és 631 halálesetet regisztráltak ebből a betegségből (Arzykulov Zh.A. et al., 2008).
A méhnyakrák helyzetének javítását célzó program modern koncepciója a fejlett országok tapasztalatai alapján három fő elven alapul:
1. Primer prevenció (egészséges életmód az esetleges rizikófaktorok kizárásával, a lakosság egyes csoportjainak védőoltása).
2. Másodlagos prevenció (a női lakosság magas színvonalú és jól szervezett szűrése).
3. Egységes protokollok bevezetése az invazív méhnyakrák korszerű diagnosztikájához és kezeléséhez.
Csak egy ilyen integrált megközelítés teszi lehetővé, hogy megbízhatóan csökkentsük hazánkban a méhnyakrák előfordulását és halálozását.
Protokoll kód:РH-O-002 "Méhnyakrák"
ICD kód: C 53
1. A méhnyak rosszindulatú daganatai (C 53).
2. Belső rész (C 53.0).
3. Külső rész (C 53.1).
4. A méhnyak károsodása, amely túlnyúlik a fenti lokalizációk közül egy vagy többen (C 53.8).
5. Méhnyak, nem meghatározott rész (C 53.9).
A protokollban használt rövidítések:
1. FIGO – Nemzetközi Nőgyógyászati és Szülészeti Szövetség.
2. WHO – Egészségügyi Világszervezet.
3. CC - méhnyakrák.
4. CIN - cervicalis intraepiteliális neoplázia.
A jegyzőkönyv kidolgozásának időpontja: 2011
Protokoll felhasználók: méhnyakrákos betegek diagnosztizálásában, kezelésében és rehabilitációjában részt vevő orvosok.
Összeférhetetlenség közlése: A fejlesztőknek nincs anyagi érdekeltsége a jelen dokumentum tárgyában, és nem állnak semmilyen kapcsolatban a jelen dokumentumban meghatározott gyógyszerek, berendezések stb. értékesítésével, gyártásával vagy forgalmazásával.
Osztályozás
A méhnyakrák stádiuma
A méhnyakrák stádiumának meghatározására a Nőgyógyászok és Szülészeti Szakorvosok Nemzetközi Szövetségének klinikai osztályozását használják szerte a világon (1. táblázat); a sebészeti beavatkozáson átesett eseteket a TNM szerint is osztályozzák (7. kiadás, 2009).
A méhnyakrák stádiumba vételének szabályai
A méhnyakrák stádiumának meghatározása kizárólag a klinikai értékelésen alapul, ezért alapos klinikai kivizsgálásra abszolút minden esetben szükség van, esetenként altatásban. Emlékeztetni kell arra, hogy a klinikai stádium nem változik a későbbi diagnosztikai eredmények függvényében. Ha kétségei vannak a színpad kiválasztásával kapcsolatban, előnyben részesítik a kisebb színpadot.
Az alábbi vizsgálati módszereket alkalmazzák a stádiumba állításhoz:
1. A FIGO staging kizárólag klinikai adatok (vizsgálat és kolposzkópia), mellkas röntgen, intravénás urográfia, biopszia és a méhnyakcsatorna és a méh üreg kürettájának felhasználásán alapul.
2. Cisztoszkópia és rektoszkópia a klinikai stádium meghatározásához csírázási gyanú esetén alkalmazható: morfológiai megerősítés szükséges!
3. Klinikai stádium meghatározásához limfográfia, CT, MRI, PET, laparoszkópia nem használható.
4. Ha az intravénás urográfia kóros elváltozásokat észlel, az esetet a IIIB stádiumba kell besorolni.
5. A méhnyak regionális nyirokcsomói paracervikális, parametrikus, hypogastricus, obturátor, belső, külső és közös csípő, presacral, sacralis.
6. A további vizsgálati módszerek, mint laparoszkópia, ultrahang, CT, MRI, PET során feltárt leletek értékesek a kezelési mód kiválasztásához, de mivel nem mindenhol végzik el, értelmezésük az orvos szakképzettségétől függ, nem használják klinikai stádium meghatározására, és adataik nem változtatják meg a betegség stádiumát.
1. táblázat: Méhnyakrák – FIGO (2009) és TNM stádiumbesorolás (7. kiadás, 2009)
| FIGO színpad | TNM kategória | |
| Az elsődleges daganat nem határozható meg | Tx | |
| Az elsődleges daganatnak nincs megnyilvánulása | T0 | |
| Preinvazív rák (carcinoma in situ) | Tis | |
| én | A méhre korlátozódó daganat (a méh testére terjedését nem vesszük figyelembe) | T1 |
| IA | Az invazív rákot csak mikroszkóposan diagnosztizálják (minden makroszkóposan látható elváltozás, még felületes invázió esetén is, 1B stádiumú) | T1a |
| I A1 | Stromális invázió legfeljebb 3 mm mélységben és vízszintes terjedés legfeljebb 7 mm* | T1a1 |
| I A2 | A stroma invázió legfeljebb 5 mm mélységű és vízszintes kiterjedés legfeljebb 7 mm | T1a2 |
| IB | Klinikailag látható nyaki elváltozások vagy 1A2/T1A2-nél nagyobb mikroszkopikus léziók | T1b |
| I B1 | Klinikailag látható elváltozások a legnagyobb méretben, legfeljebb 4 cm | T1b1 |
| I B2 | Klinikailag látható elváltozások 4 cm-nél nagyobb méretben | T1b2 |
| II | A daganat a méh testére korlátozódik, anélkül, hogy érintené a medence falát és a hüvely alsó harmadát | T2 |
| II A | Paraméterek bevonása nélkül | T2a |
| II A1 | A daganat a legnagyobb méretben 4 cm-nél kisebb | T2a1 |
| II A2 | A daganat a legnagyobb méretben 4 cm-nél nagyobb | T2a2 |
| II B | Paraméterek bevonásával | T2b |
| III |
A medencecsontokat és/vagy a hüvely alsó harmadát elérő daganat és/vagy hidronephrosis vagy nem működő vese jelenléte |
T3 |
| III A | A hüvely alsó harmadának érintettsége a medencefalak érintettsége nélkül | T3a |
| III B | A medencecsontok kiterjedése és/vagy hydronephrosis és/vagy néma vese jelenléte | T3b |
| IV A | A hólyag és/vagy végbél nyálkahártyájának inváziója anélkül, hogy a medencén túlnyúlna* | T4a |
| IV B | Távoli metasztázisok | T4b |
|
A FIGO 2006-ban javasolta az állomásozás módosítását, amely az IIA szakasz felosztásából áll az IB szakasz elve szerint, amely 2010. január 1-jén lépett hatályba. A 0. szakasz az új kiadásban ki van zárva a FIGO osztályozásból. A pN0 beállításához legalább 6 nyirokcsomó vizsgálata szükséges, metasztázis hiányában és kevesebb nyirokcsomó esetén az N0 is be van állítva. |
||
Patológiás (sebészeti) TNM stádiummeghatározás (1. táblázat)
A műtét során eltávolított szövetek alapos morfológiai vizsgálatából nyert adatokat kell felhasználni a folyamat mértékének legpontosabb felmérésére. Ezek az eredmények nem teszik lehetővé a klinikai stádium meghatározásának megváltoztatását, de fel kell használni, és tükröződni kell a kóros stádiummeghatározási protokollban. Erre a célra a TNM nómenklatúrát használják.
Előfordul, hogy a méhnyakrák egyéb indikációra történő méheltávolítás utáni véletlen lelet is lehet - ilyen esetekben klinikai stádiummeghatározás nem végezhető, és ezek az esetek nem szerepelnek a terápiás statisztikákban, de célszerű külön jelenteni. A kezdetben kialakult stádium nem változik, ha visszaesés következik be.
A klinikák és a különböző kezelési módszerek kezelési eredményeinek összehasonlítása csak akkor lehetséges, ha minden szakaszolási szabályt gondosan betartanak.
A színrevitel jellemzői
Az IAl és IA2 stádiumok diagnózisa kizárólag az eltávolított szövet mikroszkópos vizsgálatán alapul (biopsziás anyag - lehetőleg nyakkúp, amelynek a teljes érintett területet le kell fednie). Az invázió mélysége nem lehet 5 mm-nél nagyobb az alaphártyától vagy annak a mirigynek a felszínétől, ahonnan a tömeg származik.
A vízszintes távolság nem haladhatja meg a 7 mm-t. Az érrendszeri és/vagy nyirokrendszeri invázió jelenléte nem növeli a betegség stádiumát, de ennek tükröződnie kell a diagnózisban, mivel befolyásolhatja a kezelés megválasztását a jövőben.
A szemmel látható nagyobb elváltozásokat IB-ként rendezik. Általában lehetetlen szemmel felmérni, hogy van-e a méhtest kiterjedése. Ezért a méh testére való klinikailag feltételezett kiterjedést nem szabad figyelembe venni.
Azokat a betegeket, akiknél a daganat a kismedencei fal felé terjeszkedik, amely rövid, indurált területnek számít, IIB-ként kell kezelni. A klinikai staging során lehetetlen megbízhatóan megítélni, hogy a hüvelyboltozatok megrövidülése és a sűrű beszűrődés a parametriumban valóban daganatos vagy gyulladásos-e.
Harmadik szakasz akkor van beállítva, ha a medencecsontok beszűrődnek, vagy a daganat közvetlen növekedése eléri a medencecsontokat. A hidronephrosis vagy a nem működő vese jelenléte a daganat által okozott húgycsőszűkület következménye, és ilyen esetekben III. stádiumot rendelnek hozzá, még akkor is, ha más kutatási módszerek szerint a daganat I. vagy II. stádiumba sorolható.
A bullosus ödéma jelenléte nem ad okot arra, hogy a betegséget a IV. stádiumba sorolják. A hólyag lumenébe benyúló bordák és barázdák formájában kialakuló képződmények gyakran annak a következményei, hogy a hólyag nyálkahártya alatti rétege részt vesz a daganatnövekedésben.
A tumorsejtek jelenléte a hólyagmosásban további morfológiai vizsgálatot igényel az eset IVA stádiumba sorolásához.
Kezelés külföldön
Kapjon kezelést Koreában, Izraelben, Németországban és az Egyesült Államokban
Kérjen tanácsot a gyógyturizmussal kapcsolatban
Kezelés
Méhnyakrák kezelése
Mikroinvazív rák
Az IA1-es vagy IA2-es stádiumú méhnyakrák diagnózisa kizárólag a negatív reszekciós szélekkel rendelkező nyakkúp morfológiai vizsgálata alapján, vagy trachelektómia vagy méheltávolítás után eltávolított minta alapján történik. Ha CIN III-as vagy invazív rákot észlelnek a reszekciós széleken a méhnyak konizációját követően, meg kell ismételni a konizációt vagy a beteget az IB1 stádiumú betegséghez hasonlóan kezelni (2). Vaginoszkópiát (kolposzkópot!) végeznek az egyidejű vaginális intraepiteliális neoplasia (VAIN) kizárására a kezelési módszer kiválasztása előtt.
IA1. szakasz
A méhnyakrák fő kezelési módja ebben a szakaszban a teljes hasi vagy hüvelyi méheltávolítás. Hüvelyi intraepiteliális neoplázia jelenlétében a hüvelycső megfelelő részének eltávolítása szükséges (3). Ha a termékenység megőrzése szükséges, a méhnyak széles konizációja után negatív reszekciós szélekkel megfigyelhető Pap-teszt elvégzése mellett. Pap-tesztet 6, 12 hónapos korban, majd ezt követően évente, ha az előző két teszt negatív volt. A bizonyítékok szintje B.
IA2 szakasz
Az IA2 stádiumú betegségben szenvedő betegeknél fennáll a nyirokáttét kialakulásának bizonyos lehetősége, ezért a műtéti kezelés során kismedencei lymphadenectomiát kell végezni (4,5). Ezekre a klinikai esetekre megfelelő műtét a módosított radikális hysterectomia (2-es típusú műtét), amelyet kétoldali kismedencei lymphadenectomiával egészítenek ki. Az előzetes biopszia alapján lymphovascularis invázió hiányában kismedencei lymphadenectomiával extrafasciális extirpáció (1. típusú műtét) végezhető. A bizonyítékok szintje C.
Ha a termékenység megőrzése szükséges, a kezelési lehetőségek a következők:
A méhnyak széles konizációja, kiegészítve a medencei nyirokcsomók extraperitoneális vagy laparoszkópos eltávolításával;
Radikális trachelektómia, kiegészítve a medencei nyirokcsomók extraperitoneális, transzperitoneális vagy laparoszkópos eltávolításával (6).
Ennek a betegcsoportnak a monitorozása főként a 6. és 12. hónapos korban elvégzett két negatív teszt után évente elvégzett Pap-teszten alapul.
Invazív méhnyakrák
Azoknál a betegeknél, akiknél a méhnyakon látható elváltozások vannak, biopszia szükséges a diagnózis morfológiai megerősítéséhez (szükség esetén altatásban); vaginoszkópiát végeznek a vaginális intraepiteliális neoplázia (VAIN) kizárására. Az egyidejű tüneteket (hólyagból és végbélből) meg kell vizsgálni: cisztoszkópia és rektoszkópia szükséges. Mellkasröntgen és vesevizsgálat (ultrahang, kiválasztó urográfia, CT és MRI) is szükséges. CT-t és MRI-t is végeznek a regionális nyirokcsomók állapotának és a daganat lokális terjedésének felmérésére. Ha rendelkezésre áll PET, akkor használható.
A betegség IB1, IIA1 stádiumai (tumor< 4 см)
A méhnyakrák korai stádiumai (IB1, IIA< 4см) имеют хороший прогноз и могут одинаково успешно лечиться как хирургическим, так и лучевым методом (7,8). A bizonyítékok szintje A.
A kezelési módszer megválasztása a megfelelő erőforrások rendelkezésre állásától függ: képzett nőgyógyász onkológustól, a beteg életkorától és általános állapotától. Célszerű egy multidiszciplináris team (nőgyógyász onkológus, radiológus, kemoterápia) képességeit kihasználni a kezelési terv kidolgozásában és a beteg tájékoztatásában a különböző terápiás alternatívákról, azok mellékhatásairól és a várható kezelési eredményekről.
Jellemzően a műtéti és sugárkezelési módszerek kombinációja növeli a szövődmények számát, ezért a terápia kezdeti tervezése során kerülni kell a műtét és a posztoperatív besugárzás egyidejű alkalmazását. A bizonyítékok szintje A.
Sebészet: szabvány az IB1/IIA1 stádiumú méhnyakrák műtéti kezelésére (< 4 см в диаметре) является модифицированная или радикальная абдоминальная гистерэктомия (класс II или III согласно классификации Piver, Rutledge, Smith, 1974 г.) в сочетании с тазовой лимфаденэктомией. У молодых пациенток яичники сохраняются и выводятся из полости малого таза в брюшную полость (транспозиция) для сохранения их функции на случай проведения послеоперационной лучевой терапии. В отдельных случаях возможно выполнение радикальной трахелэктомии с лапароскопической тазовой лимфаденэктомией (9,10). A bizonyítékok szintje C.
Sugárkezelés: standard sugárterápia IB1/IIA1 stádiumú méhnyakrák esetén (< 4 см в диаметре) является сочетанная лучевая терапия. Рекомендуемые дозы для дистанционного компонента и брахитерапии источником низкой мощности - 80-85 Грей на точку A и 50-55 Грей на точку B. Суммарная доза дистанционной лучевой терапии (EBRT) должна составлять 45-50 Грей при 1,8-2,0 Грей за фракцию. При использовании источников высокой мощности для брахитерапии (ВТ), дозы определяются согласно биологической эквивалентности.
Adjuváns kezelés műtét után: a radikális sebészi kezelést követő relapszusok kockázata magas a nyirokcsomókban lévő áttétek, a pozitív reszekciós szegélyek és a parametriákban (paracervikális szövetek) daganatos elemek jelenléte esetén. Az adjuváns kompetitív kemoradioterápia (5FU + Cisplatin vagy Cisplatin alkalmazásával) javítja a kezelési eredményeket az egyidejű sugárkezeléshez képest ebben a betegcsoportban (11). A bizonyítékok szintje A.
A visszaesés kockázata megnő az érintett nyirokcsomók, nagy daganatok, a lymphovascularis tér érintettsége és a cervicalis stroma több mint 1/3-ának inváziója esetén. Ebben a betegcsoportban a kismedencei besugárzás csökkenti a kiújulás kockázatát és növeli a betegségmentes túlélést azokhoz a betegekhez képest, akik a műtét után nem kaptak adjuváns kezelést. Emellett a posztoperatív sugárterápia előnyös a nyaki adenokarcinómában és a nyaki mirigy laphámsejtes karcinómában szenvedő betegeknél (12). A bizonyítékok szintje A.
A kutatók két együttműködő csoportja elfogadható eredményekről számolt be a hüvelycsonkot és a parametriális szöveteket megcélzó posztoperatív kismezős sugárkezelés során (13,14). A besugárzás felső határa ebben az esetben az S1-2 szint, és nem az L5-S1, mint a hagyományos mezőknél. A bizonyítékok szintje C.
Alapvetően az 1. stádiumú CC esetén adjuváns sugárkezelés/kemoradioterápia felírásának kérdése a GOG pontozási skála alapján dől el, amelyet egy kiterjedt patológiai és sebészeti vizsgálat alapján dolgoztak ki (2. táblázat).
2. táblázat: A visszaesés relatív kockázata 1. stádiumú méhnyakrákban radikális méheltávolítás után
| Jel | Jelentése | Relatív kockázat |
| A stromába való behatolás mélysége, mm | ||
| Felszínes | 3 | 1.0 |
| 4 | 3.0 | |
| 5 | 7.2 | |
| 6 | 14 | |
| 7 | 21 | |
| 8 | 26 | |
| 10 | 31 | |
| Átlagos | 5 | 20 |
| 6 | 22 | |
| 7 | 23 | |
| 8 | 25 | |
| 10 | 28 | |
| 12 | 32 | |
| 14 | 36 | |
| Mély | 7 | 28 |
| 8 | 30 | |
| 10 | 34 | |
| 12 | 37 | |
| 14 | 41 | |
| 16 | 45 | |
| 18 | 49 | |
| 20 | 54 | |
| Klinikai daganat mérete | Nem látható | 1.0 |
| 1 | 1.6 | |
| 2 | 1.9 | |
| 3 | 2.4 | |
| 4 | 2.9 | |
| 6 | 4.4 | |
| 8 | 6.6 | |
| Lymphovascularis invázió | Eszik | 1.0 |
| Nem | 1.7 | |
|
A GOG pontszámot úgy számítják ki, hogy megszorozzák a relatív kockázati pontszámokat az invázió mélyére, a daganat méretére és a lymphovascularis invázióra |
||
IB2, IIA2 stádium (tumor > 4 cm)
A kiválasztási módszerek a következők:
1. Primer kompetitív kemoradioterápia (15).
2. Radikális méheltávolítás kismedencei lymphadenectomiával (III. típusú műtét), amelyet általában adjuváns sugárterápiával egészítenek ki.
Kompetitív kemoradioterápia: A legszélesebb körben alkalmazott kezelés a párhuzamos sugárterápia heti platina gyógyszeres kemoterápiával kombinálva.
A sugárterápia ajánlott dózisai az A pontban 85-90 Gray, a B pontban 55-60 Gray. A ciszplatint heti 40 mg/m2 dózisban írják fel a sugárterápia külső sugárkomponensével együtt. Azoknál a betegeknél, akiknél a paraorta és a közös csípőnyirokcsomók metasztázisai vannak, szükséges a besugárzási mező kiterjesztése a paraorta zónákra (17,18). Jelenleg kevés adat áll rendelkezésre a kibővített besugárzási mezőkkel összefüggő kompetitív kemosugárterápia toxicitására vonatkozóan. A bizonyítékok szintje A.
Elsődleges sebészeti kezelés lehetséges adjuváns sugárzással
Az első stádiumban végzett radikális méheltávolítás bizonyos előnyökkel jár, beleértve az alapos sebészi staging lehetőségét a primer tumor egyidejű eltávolításával, és ezáltal kiküszöböli a későbbi brachyterápia szükségességét (19).
Ezenkívül a műtét eltávolítja az összes regionális és minden beteg vagy megnagyobbodott nyirokcsomót, amelyek sokkal kisebb valószínűséggel reagálnak megfelelően a sugárzásra (20). Mivel ezek a daganatok eredendően nagyok, valószínűleg adjuváns sugárzást igényelnek a műtét után.
A kiújulás kockázata nő a lymphovascularis tér érintettségével és a cervicalis stroma több mint 1/3-ának daganatos inváziójával (21). A regionális nyirokcsomókban áttétek nélküli és a visszaesés nagy kockázatával rendelkező betegek a teljes medence külső besugárzásának (12) vagy kismezős besugárzásnak vannak kitéve (13,14).
A regionális nyirokcsomó-metasztázisokkal és gyakori csípő- és paraaorta nyirokcsomó-áttétekkel rendelkező betegeket kiterjesztett mezőnyalábos besugárzásban kell részesíteni kemoterápiával vagy anélkül (17,18). A bizonyítékok szintje C.
Neoadjuváns kemoterápia, majd radikális hysterectomia és lymphadenectomia: Randomizált vizsgálati adatok azt sugallják, hogy a preoperatív kemoterápia jobb kezelési eredményeket ér el, mint az elsődleges sugárzás (16, 22). Jelenleg nem állnak rendelkezésre adatok a neoadjuváns kemoterápia, majd a radikális méheltávolítás és az egyidejű kemoradioterápia eredményeinek összehasonlítására. A bizonyítékok szintje B.
Az argentin protokollban alkalmazott neoadjuváns kemoterápia a következő séma szerint történt (16):
1. Cisplatin 50 mg/m2 IV - 15 perces infúzió az 1. napon.
2. Vincristine 1 mg/m2 IV infúzió közvetlenül a ciszplatin után, az 1. napon.
3. Bleomycin 25 mg/m2 ezt követő 6 órás infúziók, az 1. naptól a 3. napig.
Ezt a rendszert 10 naponta háromszor megismételjük.
Lokálisan előrehaladott méhnyakrák (ideértve a IIB, III és IVA stádiumú betegséget)
A standard kezelés a kompetitív kemoterápiával kombinált sugárterápia (15,23). A bizonyítékok szintje A.
A IV A stádiumban már az első szakaszban lehetőség van kismedencei exenteráció elvégzésére, különösen cisztás vagy végbélfisztula jelenlétében, ami azonban nem kontraindikáció a radikális program szerinti kemoradioterápiára. A bizonyítékok szintje C.
3. táblázat: Lokálisan előrehaladott méhnyakrák kezelése
| Színpad | II B – IV A |
| Színreállítás |
Vizsgálati és kolposzkópiás adatok, mellkasröntgen, intravénás urográfia, biopszia és a méhnyakcsatorna és a méhüreg kúrettája |
| Sugárterápiás technika |
1. Elsődleges célpont: daganat + méh B. 2. Másodlagos célpont: kismedencei és közös csípőnyirokcsomók. Technika: 4 mezős. 1. A daganat meghatározása tapintással és CT-vizsgálattal történik (ha lehetséges) + 2 cm-re a szélétől 2. A-P mezők: Oldalsó: 2 cm-re oldalt a medence csontos határaitól Felül: L5 és S1 csigolyák határa Inferior: 2 cm-rel az obturátor foramen alatt vagy 2 cm-rel a tumor meghatározott határa alatt 3. Oldalsó mezők: Anterior = egyed, a daganat határai határozzák meg Posterior = egyed, a tumor határai határozzák meg |
| Primer tumoronkénti dózisok | Távoli besugárzás SOD-ban 50 Gray/5-6 hét + intracavitaris terápia 30-35 Gray az A pontban (IIB - IVA szakaszokhoz, 35-40 Gray) |
| A metasztázis regionális területeinek dózisai | Távoli besugárzás SOD 50 Gray-ben/5 hét |
| A teljes kezelési idő 6-7 hét | |
| Kompetitív kemoterápia: ciszplatin 40 mg/m2 | |
Sugárzástechnika és dózis: A dózisokat és a besugárzási mezőket a 3. táblázat mutatja be. A besugárzást megfelelő energiával, egyenletes dóziseloszlás mellett (± 5%) kell végezni az elsődleges daganat és a metasztázis regionális területei között. A besugárzandó daganat térfogatát klinikai vizsgálatok és lehetőség szerint CT segítségével kell meghatározni. A besugárzási technika legalább 4 mező használatából áll. A brachyterápia kis és nagy energiaforrással is elvégezhető.
A standard kezelés a kombinált sugárterápia és a platinaalapú gyógyszereken alapuló kompetitív kemoterápia. A ciszplatint hetente egyszer 40 mg/m2 dózisban írják fel külső sugárterápia során. Az ajánlott dózisok 85 és 90 Gray között mozognak az A pontban és 55 és 60 Gray között a B pontban. Azoknál a betegeknél, akiknél a közös csípő- és/vagy paraaorta nyirokcsomókban metasztázisok vannak, meg kell fontolni a sugárzási mezők kiterjesztését a para nyirokcsomókra. -aorta régió (17,18,24 ). A bizonyítékok szintje C.
IVB szakasz és visszaesések
A visszaesés lehet a medencében (lokális relapszusok) vagy a kismedencei szerveken kívül (távoli áttétek). Az elsődleges daganat nagy méretével nő a medencében visszaeső betegek száma és a távoli áttétek. A legtöbb relapszus az első két évben következik be, és a prognózis ebben a betegcsoportban kedvezőtlen, többségük a betegség progressziója miatt hal meg (25). A medián túlélés hét hónap.
Az előrehaladott méhnyakrák fő tünetei a fájdalom, a lábak duzzanata, az anorexia, a nemi szervek vérzése, a cachexia, a pszichés és egyéb problémák. A betegek e csoportjának kezelési és kezelési módszerének kiválasztásakor optimális a szakemberek egy egész csoportjának erőfeszítéseit kombinálni: nőgyógyász onkológusok, radiológusok, kemoterapeuták, pszichológusok, táplálkozási szakértők és speciálisan képzett nővérek. A fájdalom és más tünetek enyhítése, valamint az átfogó támogatás az egészségügyi személyzet fő célja.
Primer relapszusban szenvedő betegek kezelése: a kezelési mód megválasztása a beteg általános állapotán, a relapszus/metasztázis helyén, ezek prevalenciáján és az elsődleges kezelés módján alapul.
Az elsődleges radikális méheltávolítás utáni relapszusok lehetséges kezelései (4. táblázat): A radikális méheltávolítás után a medencében kialakuló recidívák mind sugárterápiával, mind műtéttel (medence exenteráció) kezelhetők. Az elsődleges sebészeti kezelést követő lokalizált kismedencei relapszusok radikális besugárzása (± kompetitív kemoterápia) jelentős számú betegnél hatásos (26). A sugárterápia dózisát és mennyiségét a betegség mértéke alapján kell meghatározni.
Így mikroszkopikus méretű tumorok esetén a szokásos dózis 50 Gray, ROD 1,8-2,0 Gray csökkentett besugárzási mezőméretekkel, nagy daganatok esetén pedig 64-66 Gray.
A betegség disszeminált formáiban vagy a sikertelen elsődleges kezelést követő lokális relapszusok esetén, amikor a hagyományos kezelés nem lehetséges, palliatív kemoterápiát vagy tüneti kezelést írnak elő. A ciszplatin az egyik leghatékonyabb CC gyógyszer (27,28). A várható átlagos élettartam ilyen esetekben 3-7 hónap.
4. táblázat: Helyi relapszusok méhnyakrák műtéti kezelését követően
Radikális méheltávolítást végeznek olyan betegeknél, akiknél enyhe recidíva van (< 2 см в диаметре), ограниченными шейкой матки. Несмотря на увеличение количества осложнений при операциях после первичной лучевой терапии, в большинстве случаев нет необходимости накладывать колостомы (29, 30).
A centrálisan lokalizált recidíva, a hólyag és a végbél érintettsége intraperitoneális disszemináció és távoli metasztázisok hiányában, valamint a méhnyak és a medencefal közötti szabad tér potenciális jelöltjei a kismedencei exenterációnak.
A tünetek hármasa - az alsó végtagok kétoldali nyiroködémája, isiász, a húgyutak elzáródása működésképtelen folyamatot jelez. Ebben a betegcsoportban palliatív és tüneti kezelés javasolt.
A legkedvezőbb prognózis a 6 hónapot meghaladó relapszusmentes periódus, a 3 cm-nél kisebb daganatméret és a beszűrődések hiánya a paraméterekben (31-34). Az 5 éves túlélési arány ebben a betegcsoportban 30-60%, és a perioperatív mortalitás nem haladja meg a 10%-ot.
5. táblázat: Helyi relapszusok méhnyakrák sugárkezelése után
A szisztémás kemoterápia szerepét a IVB stádiumban és a metasztatikus CC-ben a 6. táblázat mutatja be.
6. táblázat: Szisztémás kemoterápia metasztatikus CC esetén
| Ajánlások | A bizonyítékok szintje |
| A ciszplatin az egyetlen hatékony gyógyszer a méhnyakrák kezelésében. | BAN BEN |
| Az objektív hatások előfordulási gyakorisága 100 mg/m2 ciszplatin (31%) felírásakor magasabb, mint 50 mg/m2 (21%) adagolás esetén, de ez a hatásosság nem jár együtt a betegség fokozódásával. ingyenes és általános túlélés (28) | BAN BEN |
| A kemoterápiára kifejtett objektív hatások aránya magasabb azoknál a betegeknél, akiknek megfelelő az általános állapota és a metasztázisok extramedencei elhelyezkedése van, és szinte hatástalan a korábban besugárzott relapszusok esetén. | VAL VEL |
| A palliatív kemoterápia túlélésre gyakorolt hatása nem ismert | VAL VEL |
Távoli áttétek: A sugárterápia tüneti tumoráttétek esetén javallt palliatív kezelésként, például csontáttétek (34), megnagyobbodott paraaorta, szubklavia nyirokcsomók esetén fájdalomcsillapítás céljából, vagy agyi áttétek esetén (35).
Véletlenszerű méhnyakrák leletek
Ezek a leletek főként az invazív méhnyakrák eseteire vonatkoznak, amelyeket más indikációk alapján végzett egyszerű méheltávolítás után diagnosztizáltak. A kezelés megkezdése előtt ilyen helyzetekben további vizsgálatra van szükség: a kismedencei és hasi szervek CT vagy MRI vizsgálata, mellkas röntgen a folyamat mértékének tisztázása érdekében. A kezelés módját a morfológiai vizsgálat és a radiológiai leletek alapján kell meghatározni.
Patológiai leletek hiányában:
1. Az IA1 stádiumban további kezelést nem végeznek.
2. Az IA2 és magasabb stádiumok esetén a következő kezelés szükséges:
Pozitív reszekciós szélek, mély stromainvázió és a lymphovascularis tér érintettsége esetén kompetitív kemoradiációs kezelést írnak elő (38);
Azoknál a betegeknél, akiknél nincs mély stromainvázió, negatív reszekciós szélek, és nem érintett a lymphovascularis érintettség, radikális parametrectomiát végeznek a vagina felső harmadával és lymphadenectomiát a kompetitív kemoradiációs terápia alternatívájaként (39). A bizonyítékok szintje C.
CC terhesség alatt
A méhnyakrák terhesség alatti kezelése általában ugyanazokon az elveken alapul, mint a nem terhes nők esetében. Csak néhány konkrét ajánlás létezik. A méhnyak konizációját csak akkor végezzük, ha citológiai vizsgálat és kolposzkópia alapján invazív növekedés gyanúja merül fel a vérzés, a vetélés vagy a koraszülés magas kockázata miatt.
A méhnyakrákos terhes nők kezelési taktikájának meghatározásának legfontosabb feltétele a multidiszciplináris megközelítés, amelyben a radiológus és kemoterapeuta mellett neonatológus és szülész-nőgyógyász is részt vesz. Magának a nőnek és párjának részvétele szükséges a döntéshozatalban, és figyelembe kell venni a terhesség folytatására irányuló vágyukat.
Mikroinvazív méhnyakrák gyanúja esetén a kezelés késése nem károsítja az anyát, és a magzat életképességének jelentős növekedésében nyilvánul meg.
Az IA1 stádiumú betegségben szenvedő nők, akiket konizációs és negatív reszekciós margók igazolnak, kihordhatják terhességüket, és hüvelyi úton szülhetnek. A mikroinvazív cervicalis carcinoma beadási módja nem befolyásolja a betegség kimenetelét.
Az IA2-es és magasabb stádiumú betegség esetén a kezelést egyénileg kell kiválasztani, a kezelés módjáról és időzítéséről szóló döntés elsősorban a betegség stádiumától és a terhesség stádiumától függ. A folyamat mértékének felmérésére MRI-t végeznek. Ha a diagnózist a terhesség 20. hete előtt állapítják meg, a kezelést azonnal el kell kezdeni. A választandó kezelés a magzat in situ radikális méheltávolítása. A kemoradioterápia során a terhesség megszakítása általában nem történik meg, mivel a kezelés megkezdése után spontán vetélés következik be.
Ha a terhesség 28. hetét követően méhnyakrákot észlelnek, ajánlatos elhalasztani a kezelést, amíg életképes magzatot nem kapnak. A méhnyakrák kezelése a terhesség 20. és 28. hete között az IA2 és IBI stádiumban elhalasztható az életképes magzat eléréséig anélkül, hogy az anyai prognózist jelentősen befolyásolná (40, 41). Ha a betegség stádiuma magasabb, mint az IBI, a kezelés késése jelentősen rontja a prognózist és befolyásolja a túlélést.
Meg kell jegyezni, hogy nincsenek szabványok annak meghatározására, hogy mennyi ideig lehet késleltetni a kezelés megkezdését. A gyakorlatban a késleltetés időtartama a betegség stádiumától, a morfológiai leletektől, a terhességi kortól és a szülők kívánságaitól függ. A lokálisan előrehaladott CC szülés időpontjának tervezésekor a betegség további progressziójának megelőzése érdekében lehet dönteni a neoadjuváns kemoterápia felírásáról (42) - dinamikus megfigyelés szükséges! A szülés legkésőbb a terhesség 34. hetében történik.
Ha a méhnyaktömeget nem távolítják el a diagnosztikus konizáció során, akkor a klasszikus császármetszés az előnyben részesített szülési mód, bár több retrospektív vizsgálat is kimutatta, hogy a szülés módja nincs hatással a méhnyakrák prognózisára (43).
Megfigyelés
A méhnyakrák kezelését követően a legtöbb relapszus az első 3 évben fordul elő, ami meghatározza a betegek gyakori ellenőrzésének szükségességét a kezelés után.
A minimális kutatási mennyiség egy nő látogatása során a következőkből áll:
1. Ellenőrzés tükrökben.
2. Nőgyógyászati vizsgálat.
3. Pap teszt.
Ezeket a vizsgálatokat legalább 3 havonta egyszer, az első 2 évben, legalább 4 havonta egyszer, a 3. évben, félévente egyszer, a 4. és 5. megfigyelési évben, majd évente végezzük.
Patológiai vizsgálat
7. táblázat A méhnyakrák gyógyszerének patomorfológiai vizsgálata
| Jel | Leírás | ||
| Makroszkópos értékelés | |||
| Drog | Méh mérete és súlya, méhnyak mérete, függelékei (külön jobb és bal), paracervikális szövetek mérete (jobb és bal), hüvelyi mandzsetta hossza | ||
| Tumor | Méret (3 méret), hely, megjelenés, invázió mélysége/nyaki stroma vastagsága, paracervicalis szövet érintettsége, méhtest érintettsége, hüvelyi mandzsetta, távolság a daganattól a hüvely reszekciós széléig, egyéb érintett struktúrák, jelenlévő és készült jelölések, kimetszett blokkok száma | ||
| Nyirokcsomók | Méret (tól és ig), a legnagyobb áttét mérete, a nyirokcsomók száma és a kazetták száma | ||
| Mikroszkópos kiértékelés |
Histotype CIN (fokozattal), ha van Az invázió maximális mélysége a felszíni hám alapjától (mm) A nyak vastagsága a legmélyebb invázió helyén (mm) Maximális vízszintes szóródás (mm) Multifokális invázió Invázió a limfovaszkuláris térbe A paracervikális szövetek állapota (parametriális invázió) |
Laphámrák | Adenokarcinóma |
| Magas fokú differenciálódás G1 | A fő sejtösszetétel tipikusan keratinizáló nagy sejtek. A legtöbb sejt (>75%) jól differenciált. A mitotikus aktivitás alacsony. A daganat papilláris és szilárd exofitikus struktúrákból áll; a határokat kötősejtek alkotják. | A daganat jól kialakított mirigyeket tartalmaz papillákkal. A sejtek megnyúltak, azonos ovális magokkal; minimális rétegződés (kevesebb mint három sor cella vastagsága). A mitózisok nem gyakoriak. | |
| Mérsékelt differenciálódás G2 | A sejtek típusa általában nem keratinizáló, nagy. A sejtek körülbelül 50%-a jól differenciált; az egyes sejtek keratinizálódnak. A mitotikus aktivitás fokozódik. A daganatoknak beszivárgó határai vannak; Az atipikus gyulladás gyakori. | A daganatok összetett mirigyeket tartalmaznak, amelyekben gyakran képződnek hidak és bölcsők. A szilárd területek gyakoriak, de még mindig a daganat kevesebb mint felét foglalják el. A magok lekerekítettebbek és egyenetlenebbek; mikronukleolusok vannak. Gyakoribb mitózisok. | |
| Alacsony differenciálódás G3 | A fő sejtösszetétel kis sejtek. A sejtek bazofil citoplazmájával rendelkeznek, magas sejtmag-citoplazma aránnyal. A sejtek és a magok mérete megegyezik. A sejtek kevesebb mint 25%-a differenciálódik. Számos mitózis, kóros mitózisok vannak. A daganatok általában infiltratívak, rosszindulatú sejtekkel a határon. |
A daganat rosszindulatú sejtmezőket tartalmaz; ritka mirigyek láthatók (<50%). Клетки крупные и неравномерные с плеоморфными ядрами. Встречаются случайные перстневидные клетки. Много митозов, в том числе аномальных. Выраженная десмоплазия и частые некрозы.
InformációEllenőrzők: 1. Kozhakhmetov B.Sh. - Az Almati Állami Orvostudományi Haladó Intézet Onkológiai Osztályának vezetője, az orvostudományok doktora, professzor. 2. Abisatov G.Kh. - A Kazah-Orosz Orvostudományi Egyetem Onkológiai, Mammológiai Tanszékének vezetője, az orvostudományok doktora, professzor. Külső ellenőrzés eredményei: pozitív döntés. Az előzetes tesztelés eredménye: Az ezen protokollok szerinti kezelést a Kazah Köztársaság Egészségügyi Minisztériumának Kazah Onkológiai és Radiológiai Kutatóintézetének nőgyógyászati onkológiai osztályán végzik. Protokollfejlesztők listája: 1. klinikai munkáért felelős igazgatóhelyettes, az orvostudományok doktora Chingisova Zh.K. 2. Fej Onkogynekológiai és Emlődaganatok Osztálya, az orvostudományok doktora Kairbaev M.R. 3. Fej Kontakt Sugárterápiás Osztály, az orvostudományok doktora Telguzieva Zh.A. 4. Fej Nappali Kórházi Sugárterápiás Osztály, Ph.D. Savkhatova A.D. 5. Az Onkoginekológiai és Emlődaganatok Klinika tudományos főmunkatársa, Ph.D. Kukubasov E.K. Figyelem!
|
Az ICD-10 szerint rosszindulatú daganatnak minősül. Ha a daganat belsőleg lokalizált, akkor az ICD-kódja C53.0, kívülről pedig C53.1. A méhnyak olyan elváltozásai esetén, amelyek egy vagy több helyen túlnyúlnak, a C53.8 kóddal rendelkeznek. Ez a besorolás nem tekinthető klinikainak, és nem befolyásolja a kezelési módszer kiválasztását.
Statisztika
A női nemi szervek valamennyi típusú onkológiai patológiája közül a méhnyakrák körülbelül 15%-át teszi ki, és a 3. helyen áll az endometrium és az emlő rosszindulatú daganatai után. Ez a diagnózis évente több mint 200 ezer nő életét követeli szerte a világon. Oroszországban ez a fajta onkológia az 5. helyen áll a rosszindulatú daganatok miatti halálozási okok között. Az elmúlt években ezt az onkológiai patológiát leggyakrabban 40 év alatti nőknél azonosították.
Egyéni megközelítés a kezeléshez
Az orvosok betartják a méhnyakrák kezelésének standardjait (az ICD-10 - C53 szerint), innovatív sebészeti beavatkozási technikákat, sugárkezelést és a leghatékonyabb daganatellenes gyógyszereket alkalmaznak. Ugyanakkor rendkívül fontos az egyes betegek kezelési módszerének egyéni megközelítése. A modern diagnosztikai technikák, a terápia, beleértve a sebészeti módszereket, az immunterápia, a kemoterápia és a sugárzás alkalmazása lehetővé teszi az onkológusok számára, hogy növeljék a beteg nők túlélési arányát.
A fejlesztés okai
Jelenleg a tudósok nem állapították meg azokat a tényezőket, amelyek provokálják a méhnyakrák kialakulását (az ICD-10 - C53 szerint). Úgy gondolják, hogy az onkológiai folyamatok különböző okok hatására fejlődnek ki. A vírusfertőzések, a női testre gyakorolt kémiai hatások és a nyaki szövet mechanikai károsodása exogénnek minősül.

Az ilyen kóros folyamat kialakulásában a következő endogén tényezőket azonosítják:
- hormonális egyensúlyhiány;
- genetikai hajlam;
- anyagcserezavarok;
- a női test csökkent immunrezisztenciája.
HPV
Az esetek 90% -ában ennek a betegségnek a kiváltó oka a HPV. A leggyakoribb rosszindulatú daganatok a 16, 31, 18, 33 típusúak. Jellemzően méhnyakrákban mutatják ki a 16-os típusú vírust, melynek onkogenitása jelentősen megnő a szervezet immunválaszának csökkenésével. A vírus, amely részt vesz a patológia mechanizmusában, szexuális érintkezés útján terjed. A legtöbb esetben spontán gyógyulás következik be. De ha a kórokozó mikroorganizmusok folyamatosan a méhnyakban maradnak, rákos daganat alakul ki.
Krónikus gyulladás
A patológia kialakulását provokáló jelentős tényezők közé tartozik a krónikus gyulladásos folyamat. Disztrófiás változások kialakulásához vezet a nyaki epitélium szerkezetében, ami végső soron súlyos szövődmények kialakulását okozza. Ugyanilyen fontos tényező az ilyen típusú onkológia kialakulásában az abortusz, a szülés során, valamint bizonyos fogamzásgátlási eszközök által okozott traumás sérülés.

Exogén és endogén tényezők
A szakértők a méhnyakrák exogén okai közé sorolják a különböző szexuális partnerekkel folytatott korai szexuális tevékenységet, valamint a dohányzást (az ICD-10 - C53 szerint). A következő endogén tényezőket azonosítják:
- megnövekedett ösztrogénszint a vérben;
- immunhiányos állapotok nőknél, beleértve a HIV-fertőzés jelenlétét;
- orális hormonális fogamzásgátlók hosszú távú alkalmazása.
Nem szabad megfeledkezni a különféle foglalkozási veszélyekről, a minőségről és az életmódról sem.
A betegség tünetei

Kialakulásának kezdetén a méhnyakrák (az ICD-10 - C53 szerint) nem jelentkezik olyan kóros jelekkel, amelyek nagymértékben zavarhatják a nőt. Csak akkor, amikor a rosszindulatú formáció elkezd szétesni, a következő kifejezett jelek jelennek meg:
- különböző típusú leucorrhoea;
- fájdalom, leggyakrabban az alsó hasban, a hátban és a végbélben;
- lokális, még meglehetősen enyhe trauma során fellépő vérzés a daganatképződés felületesen elhelyezkedő kis, törékeny ereinek szakadása következtében.
Az onkológiai daganat a nyirokereken keresztül csírázással áttétet juttathat a hüvely falába azokon a helyeken, ahol az onkológiai daganattal érintkezik. Az ureter a leginkább ellenálló a daganat növekedésével szemben. A szakemberek sokkal gyakrabban észlelik az ureterek összenyomódását onkológiai beszűrődések által, ennek eredményeként a vizelet normális kiáramlása megszakad.
A daganat növekedése a végbélben az onkológiai folyamat figyelmen kívül hagyását jelzi. A végbél nyálkahártyája általában nem marad hosszú ideig mozgékony a daganat felett. Nagyon ritkán a méhnyakrák átterjedhet a petefészkekre és a petevezetékekre. Előrehaladott esetekben a távoli szövetekben és szervekben metasztázisok ritka előfordulások.
A nőgyógyászok azon a véleményen vannak, hogy a méhnyakrák leggyakrabban hosszú ideig „lokális folyamat” marad. Az általános fertőzés klinikai tüneteit mutató metasztázis rendkívül ritka. A beteg nők hőmérséklete magas szinten marad, néha remissziós időszakokat ad. A rák cachexia a rákos daganatok kialakulásának késői szakaszában figyelhető meg, és különféle kóros szövődmények okozzák.

A méhnyakrák (ICD-10 - C53) tüneteit nem szabad figyelmen kívül hagyni.
A rosszindulatú daganat kialakulásával az egész méhnyak vagy egyes szakaszai tapintásra sűrűnek, megnagyobbodottnak tűnnek, a nyálkahártya megvastagszik. A felszíni hám rendellenességei gyakran láthatóak helyenként. Gyakran látható a felesleges szövet különböző formájú és méretű fehéres területek formájában.
Mi a teendő, ha méhnyakrákra gyanakszik (ICD-10 kód C53)?
A patológia diagnosztizálása
Jelenleg számos diagnosztikai módszer létezik. A méhnyak onkológia diagnosztizálásának alapja a nő teljes körű kivizsgálása, az élet- és betegség- és panaszok helyes összegyűjtése, a beteg állapota súlyosságának megfelelő felmérése és a nőgyógyászati vizsgálat tükrök segítségével. A betegség diagnosztizálására a következő instrumentális módszereket alkalmazzák:
- kolposzkópia;
- laboratóriumi vizsgálatok STI-k kimutatására;
- anyag vétele biopsziához;
- citológiai szűrés.
A kolposzkópia az egyik leghatékonyabb módszer mind a közvetlenül rosszindulatú méhnyakrák (ICD-10-C53), mind a rákmegelőző állapotok diagnosztizálására. Ennek a módszernek a hatékonysága eléri a 80%-ot. Az onkológusok kombinálják más modern technológiákkal. A kolposzkópia lehetővé teszi a méhnyak egészének károsodásának mélységének és természetének, az érintett terület határainak és méreteinek meghatározását, hogy ezt követően néhány morfológiai vizsgálatot lehessen végezni.

A cervikoszkópia fontos a patológia diagnosztizálásában. Ezt a vizsgálatot hiszteroszkóppal végezzük. Ennek a technikának van néhány ellenjavallata:
- terhesség;
- gyulladásos folyamatok;
- vérzés.
A cervikoszkópia lehetővé teszi a nyaki csatorna klinikai állapotának felmérését, és akár 150-szeres növekedést mutat, aminek következtében célzott biopsziát végeznek. A daganatok helyének meghatározásának egyik hatékony módszere a citológiai vizsgálat, amelyet világszerte elismernek és a WHO is ajánl. A kolposzkópiával kombinálva ennek a vizsgálatnak a hatékonysága eléri a 90-95% -ot. A citológia lényege, hogy a méhnyakból sejteket gyűjtünk és mikroszkóposan vizsgáljuk a kóros elemek kimutatása érdekében. A diagnosztikában döntő szerepet a biopsziával nyert bioanyag szövettani vizsgálata kap.
Kezelés
A méhnyakrák kezelési módszerének megválasztását (ICD-10 kód - C53) egyénileg határozzák meg. A terápia a rákos folyamat mértékétől és az egyidejű patológiák súlyosságától függ. A nő kora számít a legkevésbé. A betegség kezelésének hagyományos módszerei a következők:
- sebészeti;
- kombinált;
- sugár.

Jelenleg a tudósok aktívan tanulmányozzák a méhnyakrák kemosugárzásos kezelésének lehetőségeit (az ICD-10 szerint, C53 kód) és a gyógyszeres terápiát.
Súlyos intraepiteliális rák esetén elektromos késsel, szikével vagy lézersugárral a méh diagnosztikai külön küretálása és a méhnyak konizációja történik.
Jelenleg az 1. és 2. stádiumú invazív rák kezelésében a méh és a függelékek kiterjesztett extirpációját (Wertheim-műtét) alkalmazzák. A kombinált kezelés sugárterápiát és műtétet foglal magában, különböző sorrendben.
A méhnyakrák egy invazív folyamat, amely általában ott kezdődik, ahol a rétegzett laphám egyrétegű oszlophámmá alakul át, és rétegzett laphám vagy mirigyhám képviseli.
A méhnyakrák a rák okozta halálozás egyik vezető oka annak ellenére, hogy az elmúlt 30 évben 50%-kal csökkent e betegség előfordulása.
Statisztikai adat
Előfordulás: 15,9/100 000 női lakosság 2001-ben
. Túlnyomó életkor
Az invazív méhnyakrákot leggyakrabban 40 és 50 éves kor között észlelik.
30 év előtt és 70 év után az elsődleges méhnyakrákot a nők megközelítőleg 7%-ánál, illetve 16%-ánál mutatják ki.
Kockázati tényezők
HPV vírussal, 2-es típusú HSV-vel (HSV-2), HIV-vel való fertőzés
. Dohányzó
. A dietil-stilbesztrol expozíció a méhen belül
. A szexuális tevékenység korai kezdete
. A szexuális partnerek nagy száma
. Korai első szülés
. Nemi betegségek
. Orális fogamzásgátlók szedése.
Patomorfológia
. A leggyakoribb típus az invazív laphámsejtes karcinóma (80-85%)
. A második helyet az invazív adenokarcinóma foglalja el (15-20%)
. Ritkábban diagnosztizálják a kissejtes karcinómát, a szemölcsös karcinómát és a limfómát.
Klinikai kép
. Szabálytalan spontán hüvelyi vérzés
. Széles körben elterjedt helyi károsodás esetén bűzös véres váladékozás és tompa fájdalom jelentkezik az alsó hasban
. Hüvelyi vérzés szexuális kapcsolat után
. Dyspareunia
. Hematuria
. Rektális vérzés
. A méhnyak megnagyobbodása.
Osztályozás
A TNM rendszer szerint
Tis - in situ rák
Tl - méhnyakrák, korlátozott (a szervezetre való terjedést nem veszik figyelembe)
T1a - invazív karcinóma, csak mikroszkóposan diagnosztizálják
T1 a 1 - stromális invázió legfeljebb 3,0 mm mélységig és legfeljebb 7,0 mm vízszintesen
T1 a2 - invázió a stromába legfeljebb 5,0 mm, vízszintes terjedés 7,0 mm-ig
Tib - klinikailag látható daganat, amely a méhnyakra korlátozódik, vagy mikroszkopikus daganat, amely nagyobb, mint a T1a2 Tlbl - klinikailag kimutatható daganat 4,0 cm-ig a legnagyobb méretig
T1b2 - klinikailag kimutatható daganat, amelynek mérete meghaladja a 4,0 cm-t
. T2 - a daganat túlnyúlik a méhen, de a medencefal vagy a hüvely alsó harmadának inváziója nélkül
T2a - parametrium invázió nélkül
T2b - parametrium invázióval
. T3 - méhnyakrák a medence falára terjedve és/vagy a hüvely alsó harmadának érintettségével, és/vagy hidronephrosishoz vagy nem működő veséhez vezet
T3 - a daganat a hüvely alsó harmadába nő, de nem terjed át a medence falára
T3 - a daganat a medence falára terjed és/vagy hydronephrosishoz vagy nem működő veséhez vezet
. T4 – a daganat a hólyag vagy a végbél nyálkahártyáját érinti és/vagy a medencén túlnyúlik (a bullosus ödéma jelenléte nem utal olyan daganatkategóriára, mint a T4)
Regionális nyirokcsomók
N1 - metasztázisok a regionális nyirokcsomókban
Távoli metasztázisok. Ml - távoli metasztázisok vannak.
Csoportosítás szakaszok szerint
0. szakasz: TisNOMO
1A1 szakasz: TlalNOMO
IA2 szakasz: Tla2N0M0
IB1 szakasz: TlblNOMO
IB2 szakasz: Tlb2N0M0
NA szakasz: T2aN0M0
IIB szakasz: T2bN0M0
IIIA szakasz: T3aN0M0
IIIB szakasz: o T1N1 MO T2N1 MO T3aN 1 MO o T3bN0- 1M0
IV A szakasz: T4N0-1M0
IV B szakasz: T0-4N0-1M1.
Laboratóriumi kutatás
. UAC (lehetséges vérszegénység krónikus vérveszteség miatt)
. Szérum kreatinin (lehetséges húgyúti elzáródás)
. Májfunkciós vizsgálatok (lehetséges áttét)
. Pap kenet.
Speciális tanulmányok
. A kolposzkópia magában foglalja a transzformációs zóna, valamint a laphám és oszlophám határának vizsgálatát 7,5-30-szoros nagyítással 3-5%-os ecetsavoldat alkalmazása után
. A nyaki csatorna küretezése kolposzkópiával kombinálva történik, hogy kizárják a kolposzkópia során nem észlelt diszpláziát
. Nyaki biopszia. A darabnak megfelelő méretűnek kell lennie ahhoz, hogy beleférjen a nyaki stromába, ami az invázió mértékének meghatározásához szükséges
A nyaki kúp biopsziát az invázió kezdeti fokára vagy a lézió mélységének tisztázására használják
. A szövettanilag igazolt invazív méhnyakrák kezelés előtti vizsgálata az ismert terjedési útvonalak (közvetlen terjedés, nyirokcsomó érintettség vagy hematogén terjedés) vizsgálatára irányul.
Kötelező tanulmányok
A mellkasi szervek röntgenfelvétele
Intravénás pyelográfia
Irrigográfia
Cisztoszkópia és szigmoidoszkópia altatásban
Az opcionális vizsgálatok közé tartozik a CT, MRI, limfangiográfia és finom tűs tumor biopszia.
Megkülönböztető diagnózis
. Súlyos cervicitis
. Nyaki polip
. Endometriumrák a méhnyakra terjedéssel
. Metasztatikus elváltozások, beleértve a choriocarcinomát.
KEZELÉS
A kezelési taktika a beteg korától, általános állapotától és a rák klinikai stádiumától függ.
A diszpláziát és a karcinómát in situ műtéti úton kezelik.
Az IA szakaszban
Mikroinvázióval (1 mm-ig) a fiatal nők széles és magas konizációt hajthatnak végre
3 mm-es invázió esetén (T1 a 1) - méheltávolítás (45 éves korig - függelékek nélkül)
3-5 mm-es invázió esetén (T1a2) - a méh kiterjesztett extirpációja függelékekkel
50 év feletti korban, amikor a méhnyakcsatornában lokalizálódik, gyakori anaplasztikus variáns, méhmiómával vagy a függelékek daganataival kombinálva, korábbi műtétek után relapszus, hysterectomia javallt. Ha a műtét ellenjavallata van, intracavitaris sugárterápiát végeznek.
Az IB-IIA szakaszban a reproduktív korú nők kombinált kezelésen esnek át (Wertheim-műtét és sugárterápia).
A IIB és több stádiumban, valamint a ritkábban előforduló daganatokban és a műtéti ellenjavallatok jelenlétében a választott módszer a kombinált sugárterápia.
A polikemoterápia kiegészíti a IV. stádiumban lévő betegek kezelését (a sugárterápiával párhuzamosan).
Visszaesések
Ha a folyamat lokalizált, részleges vagy teljes kismedencei exenteráció történik (a méh, a méhnyak, a hüvely, a parametrium, a hólyag és a végbél egyetlen blokkjában történő eltávolítás)
Távoli metasztázisok jelenlétében a betegek általában kemoterápiát kapnak. A sugárterápia a fájdalmas áttétek palliatív kezelésére alkalmazható.
Drog terápia
A sugárterápia hatásának fokozására
Fluorouracil
Hidroxi-karbamid
Ciszplatin
Kiújulásra és metasztázisra
Bleomicin
Etoposide
Ciszplatin vagy karboplatin
Ifoszfamid
Hányinger és hányás megelőzésére és enyhítésére - ondan-szetron, metoklopramid.
Megfigyelés
. A kezelés során fizikális vizsgálat és Pap-kenet
. A kezelés után - rendszeres látogatások az orvoshoz, hogy megvizsgálják a kismedencei szerveket és Pap-kenetet vegyenek; a vizsgálatok közé tartozik a mellkasröntgen és az intravénás pyelography is
Az első évben - 3 havonta
Ezután 5 évig - 6 havonta
5 év elteltével az ellenőrzést évente végzik el
. Gyanús jelek és tünetek
A méhnyak krónikus gyulladása
Megmagyarázhatatlan fogyás
Az alsó végtag duzzanata az egyik oldalon
Fájdalom az alsó hasban vagy az ülőideg vetületében
Nyálkahártya-véres hüvelyfolyás
Progresszív ureter-elzáródás
Megnagyobbodott supraclavicularis nyirokcsomók
Tartós köhögés vagy hemoptysis.
Megelőzés
. Pap-kenet vizsgálat
A rendszeres vizsgálatokat a szexuális tevékenység megkezdésekor kell elkezdeni
Ha vannak magas kockázati tényezők, a vizsgálatot évente kell elvégezni
Ha a daganat kialakulásának kockázata alacsony és két egymást követő negatív Pap-kenet eredménye, a vizsgálat 2 évente elvégezhető
. Leszokni a dohányzásról
. Az STD-k megelőzése.
Komplikációk
. Fistula a húgycsőben (kezelt esetek kevesebb mint 2%-a)
. Hidronephrosis
. Uremia.
Lefolyás és prognózis
Megfelelő kombinált sugárkezelés mellett a betegség III. stádiumában is akár 70%-os az 5 éves túlélés
. Lokálisan korlátozott visszaesések. A kezdetben műtétileg kezelt betegek 25%-a megkímélhető a betegség kiújulásától kismedencei sugárkezeléssel
Metasztatikus visszaesések. A gyógyulási esetek rendkívül ritkák, a terápiás hatás egyéni és rövid életű.
Egyidejű patológia
. In situ rák és invazív hüvelyrák
. In situ rák és a szeméremtest invazív rákja
. Szemölcsök.
Jellemzők a terhesség alatt. A terhes nők méhnyakrákja az ezen a helyen előforduló összes daganatos eset 1%-ában fordul elő
. Rák in situ. A kezelést a szülésig elhalasztják (a hüvelyi szülőcsatornán keresztül is végezhető)
.Invazív rák
I trimeszter - radikális méheltávolítás vagy sugárterápia a terhesség megszakítása után
II trimeszter - a magzatot hiszterotómiával eltávolítják, majd sugárterápiát vagy sebészeti kezelést végeznek
III trimeszter - a kezelést elhalasztják a magzat életképességének eléréséig. A természetes szülés ellenjavallt.
ICD-10
. C53 A méhnyak rosszindulatú daganata
. D06 A méhnyak in situ carcinoma.
Valerij Zolotov
Olvasási idő: 4 perc
A A
Blastoma az összes daganat általános neve: jóindulatú és rosszindulatú. Amikor azonban nyaki blastomáról beszélünk, gyakran rosszindulatú daganatokról kell beszélnünk. Ezért ebben a cikkben a méhnyak daganatát fogjuk megvizsgálni, ICD kód 10 C53. Megmondjuk, mi ez, hogyan lehet megszabadulni a blastomától, és hogyan lehet megelőzni a megjelenését.
Néhány általános információ
A Betegségek Nemzetközi Osztályozása C53 kódot tartalmaz, ami a méhnyak rosszindulatú daganatát jelenti. A statisztikák szerint ez az egyik leggyakoribb rákbetegség a nők körében. A patológia leggyakrabban reproduktív korú nőknél fordul elő. Ha ezt a betegséget a fejlődés korai szakaszában észlelik, a prognózis kedvező lesz. Ellenkező esetben drága, hosszú távú kezeléssel kell szembenéznie.
A daganat előfordulása a méhnyakban lokalizált atipikus sejtek megjelenésével jár. A természetes endometrium sejtek degenerálódnak, ami rosszindulatú daganatot eredményez. A betegség rendkívül gyorsan fejlődik, először a szomszédos szöveteket és szerveket, majd a távoliakat fertőzi meg. A kezdeti szakaszban a daganat nem veszélyes az egészségre.
Jelenleg az orvosok a cervicalis blastoma fejlődésének négy szakaszát különböztetik meg. Mindegyikük speciális megközelítést igényel a kezeléshez, és eltérő tünetekkel és következményekkel jár.
- Kezdetben atipikus sejtek csoportja lokalizálódik a méh testében, ahol elsődleges fejlődése megtörténik. Ebben a szakaszban még nincsenek áttétek, a beteg jól érzi magát, és lehet, hogy nem is veszi észre, hogy valami nincs rendben a szervezetében. Ebben a szakaszban nőgyógyászati vizsgálat és műszeres vizsgálat során észlelik a rákot.
- A második szakaszban egy rosszindulatú daganat növekedése figyelhető meg a méhnyakban. Még mindig nincsenek áttétek, de a daganat tovább halad, és új területeket támad meg. Megjelenhetnek az első tünetek: fájdalom, vérzés. Ebben a szakaszban a betegség gyakran tünetmentes.
- Most a blastoma túlnyúlik a méhen, és hatással van a kismedencei szervekre és a szomszédos nyirokcsomókra. A metasztázisok átterjednek a közeli szervekre, és másodlagos rákos daganatok jelennek meg. Ebben a szakaszban a kezelés sokkal összetettebbé válik. El kell távolítani az érintett szerveket a keletkező daganatokkal együtt, és sugárterápiát és kemoterápiát kell végezni.
- A negyedik szakasz a legrosszabb prognózisú. Az a tény, hogy a daganat még távoli szervekre is metasztatizál. Néha előfordul, hogy a másodlagos daganatok létfontosságú, pótolhatatlan szerveket érintenek, majd működésképtelenné válnak, és a terápia tünetivé válik.
Miért fordul elő blastoma?
A jóindulatú és rosszindulatú blastomák szinte ugyanabban a forgatókönyvben fordulnak elő. Mint fentebb említettük, az atipikus sejtek megjelenése a hibás, de nem minden olyan egyszerű. A mutáló sejtek nagy számban jelennek meg az emberi szervezetben nap mint nap. Normál helyzetben az immunrendszer sikeresen megbirkózik velük. Néhány közülük azonban hiányzik neki. Ez egy igazi rejtély a modern orvosok számára. Még mindig senki sem érti, miért történik ez.
Ezután néhány kockázati tényezőről szeretnék beszélni. Minél több ilyen van valakiben, annál valószínűbb, hogy megkapja ezt a betegséget. A gyakorlatban kiderül, hogy a 30 és 35 év közötti nők többsége veszélyeztetett. De ez nem jelenti azt, hogy halálra vannak ítélve. Csak jobban oda kell figyelnie az egészségére, és időben meg kell vizsgálnia egy nőgyógyászt.
Most térjünk át a kockázati tényezőkre. Ha 2 vagy több van belőlük, akkor óvatosnak kell lennie. Érdemes lehet életmódot váltani, vagy orvoshoz fordulni kivizsgálás céljából.
- Gyakori menstruációs zavarok, állandó késések. A hormonális változások, az ösztrogén és a progeszteron egyensúlyhiánya miatt az ovulációval kapcsolatos problémák figyelhetők meg. A tojás nem érik, vagy egyáltalán nem szabadul fel.
- Meddőség.
- Nincsenek gyerekek. A gyakorlat azt mutatja, hogy azok a nők, akik soha nem szültek, hajlamosabbak a méhnyakrák kialakulására. Ráadásul a valószínűség körülbelül 2,5-szeresére nő.
- Túl hosszú gyermekvállalási időszak. Ha a menstruáció korán kezdődött és későn ért véget, ez súlyos, hosszú távú hatásokat jelent a nemi szervekre. Mint ismeretes, bármely emberi szervre gyakorolt hosszan tartó mechanikai hatás gyakran daganatok kialakulásához vezet.
- A szexuális tevékenység kezdete 16 éves kor előtt.
- Túlsúly. Itt is a hormontermelésben van a probléma. Az orvosok bebizonyították, hogy a zsírszövet elősegíti az ösztrogén fokozott termelését. Fontos tudni, hogy még a norma enyhe túllépése is növeli a rosszindulatú daganat kialakulásának valószínűségét. Így a normához képest 10 kg-os súlynövekedés háromszorosára, 25-re pedig 9-re növeli az esélyt!
- Hosszú távú hormonterápia ösztrogén alkalmazásával. Minél hosszabb, annál nagyobb a valószínűsége a betegségnek.
- Jóindulatú daganatok jelenléte a testben vagy a méhnyakban.
- Cukorbetegség inzulinfüggőséggel. Ez a betegség hormonális egyensúlyhiányt is okoz a szervezetben.
- Örökletes hajlam. Ha közeli hozzátartozóinál valaha rákot diagnosztizáltak, akkor Ön veszélyben van.
- A méhben lokalizált krónikus gyulladásos betegségek.
- Rossz szokások. Az alkohol és a nikotin súlyos negatív hatással van a szervezetre, és növelheti a rák kialakulásának esélyét. A kábítószer-függőség még rosszabb. Ráadásul mindezek a szokások nem hoznak semmi jót az egészségedre.
- Promiscuous szexuális élet és a nemi úton terjedő betegségek jelenléte.
- Érett kor. Amint fentebb említettük, a valószínűsége nő a 30 és 35 év közötti nőknél.
Emlékeztetünk arra, hogy mindezek a tényezők nem halálos ítéletek. Ezek csak azt jelentik, hogy jobban kell vigyáznia az egészségére. Ezen túlmenően ezen tényezők közül sok befolyásolja a rák kialakulásának valószínűségét általában, és nem csak a méhnyak rosszindulatú daganatait.
Tünetek
A daganat méhnyakbeli lokalizációja sajátos tüneteket ad, így a beteg könnyen rájön, hogy melyik szervről van szó (csak nem az első szakaszokban). De fontos figyelni a problémára, amint a jelek felfedezik.
A veszélyeztetett nőknek rendszeresen meg kell látogatniuk a nőgyógyászt. A szervek rendszeres vizsgálata során az orvos képes azonosítani a daganatot és részletesebb vizsgálatra küldeni. Így a rákos daganat rövid kezelés után nagy valószínűséggel abbahagyja a zavarását.
A következő tünetek a méhnyakrák lehetséges diagnózisára utalhatnak:
- menstruációval nem járó vérzés;
- nem jellemző váladék rendkívül kellemetlen szaggal;
- vér a menopauza után;
- vérzés bármilyen szexuális kapcsolat után;
- fájdalom a medence területén a közösülés során;
- állandó fájdalom, amely idővel fokozódik;
- hirtelen változások a menstruációs ciklusban;
- a székletürítés és a vizelés folyamatának megzavarása.
A kezelés jellemzői
A méhben lévő blastomát általában műtéti úton távolítják el. A választás azonban mindig az orvosnál marad. Mindez a beteg életkorától és aktuális állapotától függ. A daganat mérete, benőttségének mértéke, a betegség stádiuma, a metasztázisok elhelyezkedése – minden szerepet játszik a kezelés megválasztásában. A műtéten kívül más kezelési lehetőségek is vannak:
- kemoterápia;
- sugárkezelés;
- Immun terápia.
Természetesen vannak kísérleti kezelések is, de még korai lenne ezeket felvenni ebbe a listába, mivel hatékonyságuk nem bizonyított.
A műtét szinte mindig a daganat eltávolítását jelenti a méhvel és annak függelékeivel együtt. Igen, egy nő teljesen megfosztott attól, hogy a jövőben anyává váljon. De egyébként normális ember marad, és ugyanolyan minőségben folytathatja az életét. Jelenleg ez a legjobb módja a rák elleni küzdelemnek. Bizonyos esetekben el kell távolítani a szomszédos nyirokcsomókat is, ha rosszindulatú daganat részeit találják bennük.
A műtét után sugárterápiát alkalmaznak. Csak olyan esetekben kerülhető el, amikor a blastomát a korai szakaszban eltávolították. A sugárterápia célja, hogy jelentősen csökkentse a visszaesés valószínűségét. A sugárzás csak a test érintett területét érinti.
A kemoterápiát sugárzással kombinálva alkalmazzák, és csökkentheti annak az esélyét, hogy a daganat ugyanazon a helyen ismét megjelenjen. Mindenesetre a kezelés után rendszeresen fel kell keresnie az orvost, hogy megbizonyosodjon arról, hogy egészségi állapota normális.
|
Mik a bélblasztóma tünetei? (3 perc alatt olvasható) |