A hipotalamusz hormonjai. Az agyalapi mirigy trópusi hormonjai
A hipotalamusz az agy fontos része. A magasabb vegetatív központ számos testrendszer komplex vezérlését és szabályozását végzi. A jó érzelmi állapot, a gerjesztési és gátlási folyamatok egyensúlya, az idegimpulzusok időben történő átadása egy fontos elem megfelelő működésének következménye.
A diencephalon szerkezetének károsodása negatívan befolyásolja a szív- és érrendszeri, légzőrendszeri, endokrin rendszer működését és az ember általános állapotát. Érdekes és hasznos tudni, hogy mi a hipotalamusz, és miért felelős. A cikk sok információt tartalmaz a fontos struktúrák felépítéséről, funkcióiról, betegségeiről, a kóros elváltozások jeleiről és a modern kezelési módszerekről.
Milyen szerv ez

A diencephalon szakasz befolyásolja a belső környezet stabilitását, biztosítja az egyes rendszerek kölcsönhatását és optimális kombinációját a szervezet holisztikus működésével. Egy fontos szerkezet három alosztályú hormonok komplexét állítja elő.
A neuroszekréciós és idegvezetési sejtek a diencephalon fontos elemének alapját képezik. A szerves patológiák a funkciók károsodásával kombinálva megzavarják a szervezet számos folyamatának periodikusságát.
A hipotalamusz kiterjedt kapcsolatban áll más agyi struktúrákkal, és folyamatosan kölcsönhatásba lép az agykéreggel és az alkéreggel, ami optimális pszicho-érzelmi állapotot biztosít. A díszítés provokálja a „képzelt düh” szindróma kialakulását.
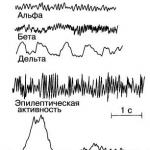
A fertőzések, a daganatos folyamatok, a veleszületett rendellenességek, az agy egy fontos részének sérülései negatívan befolyásolják a neurohumorális szabályozást, zavarják a szívből, a tüdőből, az emésztőszervekből és a test más elemeiből érkező impulzusok átvitelét. A hipotalamusz különböző lebenyeinek megsemmisítése megzavarja az alvást, az anyagcsere folyamatokat, provokálja az epilepszia, az elhízás, a hőmérséklet-csökkenés és az érzelmi zavarok kialakulását.
Nem mindenki tudja, hol található a hipotalamusz. A diencephalon elem a hypothalamus sulcus alatt, a thalamus alatt található. A szerkezet sejtcsoportjai simán átalakulnak átlátszó szeptummá. A kis szerv szerkezete összetett, 32 pár idegsejtekből álló hipotalamusz magból áll.
A hipotalamusz három régióból áll, amelyek között nincs egyértelmű határ. Az artériás kör ágai biztosítják az agy egy fontos részének teljes vérellátását. Ennek az elemnek az edényeinek sajátossága az, hogy a fehérjemolekulák, még a nagyok is, képesek áthatolni a falakon.
Ő miért felelős?
A hipotalamusz funkciói a szervezetben:
- szabályozza a légzőszervi, az emésztőrendszer, a szív, az erek működését, a hőszabályozást;
- fenntartja az endokrin és kiválasztó rendszer optimális állapotát;
- befolyásolja az ivarmirigyek, a petefészkek, az agyalapi mirigy, a mellékvesék, a hasnyálmirigy és a hasnyálmirigy működését;
- felelős az emberi érzelmi viselkedésért;
- részt vesz az ébrenlét és az alvás szabályozásának folyamatában, melatonin hormont termel, melynek hiánya álmatlansághoz, az alvás minőségének romlásához vezet;
- Optimális testhőmérsékletet biztosít. A hipotalamusz hátsó részének patológiás változásaival, ennek a zónának a pusztulása, a hőmérséklet csökken, gyengeség alakul ki, és az anyagcsere folyamatok lassabban mennek végbe. Gyakran előfordul a szubfertilis hőmérséklet hirtelen emelkedése;
- befolyásolja az idegimpulzusok átvitelét;
- hormonok komplexét állítja elő, amelyek megfelelő mennyisége nélkül a szervezet megfelelő működése lehetetlen.
Hipotalamusz hormonok

Az agy egy fontos eleme több szabályozócsoportot termel:
- sztatinok: prolaktosztatin, melanotatin, szomatosztatin;
- az agyalapi mirigy hátsó lebenyének hormonjai: vazopresszin, oxitocin;
- felszabadító hormonok: folliliberin, kortikoliberin, prolaktoliberin, melanoliberin, szomatoliberin, luliberin, tiroliberin.
Problémák okai
A hipotalamusz szerkezeti elemeinek károsodása több tényező hatásának következménye:
- traumás agyi sérülések;
- bakteriális, vírusos fertőzések: limfogranulomatózis, szifilisz, bazális meningitis, leukémia, sarcoidosis;
- daganatos folyamat;
- az endokrin mirigyek működésének megzavarása;
- a test mérgezése;
- különböző típusú gyulladásos folyamatok;
- érrendszeri patológiák, amelyek befolyásolják a hipotalamusz sejtjeinek tápanyag- és oxigénellátásának mennyiségét és sebességét;
- a fiziológiai folyamatok megzavarása;
- az érfal permeabilitásának megsértése a fertőző ágensek behatolása miatt.
Betegségek
A negatív folyamatok egy fontos szerkezet közvetlen diszfunkciójának hátterében fordulnak elő. A daganatos folyamat a legtöbb esetben jóindulatú, de negatív tényezők hatására gyakran előfordul sejt rosszindulatú daganata.
Jegyzet! A hipotalamusz elváltozások kezelése integrált megközelítést igényel, a terápia számos kockázattal és nehézséggel jár. Ha onkológiai patológiákat észlelnek, az idegsebész eltávolítja a daganatot, majd a beteg kemoterápiás és sugárterápiás üléseken megy keresztül. A problémás részleg működésének stabilizálása érdekében gyógyszerek komplexét írják elő.
A hipotalamusz daganatok fő típusai a következők:
- teratomák;
- meningiómák;
- craniopharyngiomák;
- gliomák;
- adenomák (az agyalapi mirigyből nőnek);
- pinealomas.
Tünetek

A hipotalamusz károsodott működése negatív tünetek együttesét váltja ki:
- étkezési zavarok, ellenőrizetlen étvágy, hirtelen fogyás vagy súlyos elhízás;
- tachycardia, vérnyomás-ingadozások, fájdalom a szegycsontban, aritmia;
- csökkent libidó, menstruáció hiánya;
- korai pubertás egy veszélyes daganat hátterében - hamartoma;
- fejfájás, súlyos agresszió, fékezhetetlen sírás vagy nevetésrohamok, görcsrohamok;
- kifejezett ok nélküli agresszió, dührohamok;
- hipotalamusz epilepszia, nagy gyakorisággal rohamok egész nap;
- böfögés, hasmenés, fájdalom az epigasztrikus régióban és a hasban;
- izomgyengeség, a beteg nehezen áll és jár;
- neuropszichiátriai rendellenességek: hallucinációk, pszichózis, szorongás, depresszió, hipochondria, hangulati ingadozások;
- súlyos fejfájás a megnövekedett koponyaűri nyomás miatt;
- alvászavar, éjszakai többszöri ébredés, fáradtság, gyengeség, fejfájás reggel. Ennek oka a melatonin fontos hormon hiánya. A zavarok kiküszöbölése érdekében módosítania kell az ébrenléti és éjszakai alvási szokásait, és egy fontos szabályozó hangerejét helyreállító gyógyszeres kúrát kell bevennie. Jó terápiás hatást biztosít - egy új generációs gyógyszer minimális mellékhatással, addikciós szindróma nélkül;
- homályos látás, rossz memória az új információkra;
- a hőmérséklet éles emelkedése vagy a mutatók csökkenése. Amikor a hőmérséklet emelkedik, gyakran nehéz megérteni, hogy mi okozza a negatív változásokat. A hipotalamusz károsodását az endokrin rendszer károsodására utaló jelek összessége gyaníthatja: kontrollálatlan éhség, szomjúság, elhízás, fokozott vizeletürítés.
Látogasson el a címre, és olvassa el a táplálkozási szabályokról és a 2-es típusú cukorbetegség kezeléséről szóló információkat.
Diagnosztika
A hipotalamusz károsodásának tünetei annyira változatosak, hogy számos diagnosztikai eljárást kell elvégezni. Nagyon informatív módszerek: ultrahang, EKG, MRI. Feltétlenül vizsgálja meg a mellékveséket, a pajzsmirigyet, a hasi szerveket, a petefészket, az agyat és az érrendszert.
Fontos a vér- és vizeletvizsgálat, a glükóz, ESR, karbamid, leukociták és hormonszintek ellenőrzése. A páciens endokrinológust, urológust, nőgyógyászt, szemészt, endokrinológust, neurológust keres fel. Ha daganatot észlelnek, konzultálnia kell az idegsebészeti osztály szakemberével.
Kezelés
A hipotalamusz elváltozások kezelési rendje több területet foglal magában:

- a napi rutin korrekciója a melatonin termelésének stabilizálása érdekében, megszüntetve a túlzott izgatottság, idegi feszültség vagy apátia okait;
- az étrend megváltoztatása az idegrendszer és az erek állapotát normalizáló vitaminok és ásványi anyagok optimális mennyiségének biztosítása érdekében;
- gyógyszeres kezelés gyulladásos folyamatok kimutatása esetén az agy egyes részeinek károsodásával járó fertőzéssel (antibiotikumok, glükokortikoszteroidok, vírusellenes szerek, helyreállító vegyületek, vitaminok, NSAID-ok);
- nyugtatók, nyugtatók fogadása;
- sebészeti kezelés rosszindulatú és jóindulatú daganatok eltávolítására. Az agy onkológiai patológiái esetén besugárzást végeznek, kemoterápiát és immunmodulátorokat írnak elő;
- Az étkezési zavarok kezelésében jó hatást ér el a diéta, az idegi aktivitást szabályozó vitaminok (B1 és B12) injekciói, valamint a kontrollálhatatlan étvágyat elnyomó gyógyszerek.
Fontos tudni, hogy a hipotalamusz károsodása miért vezethet a szervezet élettani folyamatainak gyors egyensúlyhiányához. Ha az agy ezen részének patológiáit azonosítják, átfogó vizsgálatot kell végezni, és több orvoshoz kell fordulni. A terápia időben történő megkezdésével a prognózis kedvező. Különös felelősségre van szükség a daganatos folyamat kialakulásának megerősítésekor: bizonyos típusú neoplazmák atipikus sejtekből állnak.
A videó megtekintése után tudjon meg többet arról, hogy mi a hipotalamusz, és miért felelős ez a fontos szerv:
A hipotalamusz a központi idegrendszer és az endokrin rendszer magasabb részei közötti közvetlen kölcsönhatás helyeként szolgál. A központi idegrendszer és az endokrin rendszer között fennálló kapcsolatok természete az elmúlt évtizedekben kezdett világosodni, amikor a hipotalamuszból izolálták az első humorális faktorokat, amelyekről kiderült, hogy rendkívül magas biológiai aktivitású hormonális anyagok. Sok munkára és kísérleti készségre volt szükség annak bizonyítására, hogy ezek az anyagok a hipotalamusz idegsejtjeiben képződnek, ahonnan a portális kapilláris rendszeren keresztül eljutnak az agyalapi mirigybe és szabályozzák az agyalapi mirigy hormonok szekrécióját, pontosabban azok felszabadulását (esetleg bioszintézis). Ezeket az anyagokat eleinte neurohormonoknak, majd felszabadító faktoroknak (az angol release - to release) vagy liberineknek nevezték. Ellentétes hatású anyagok, pl. Az agyalapi mirigy hormonok felszabadulásának (és esetleg bioszintézisének) gátlását gátló faktoroknak vagy statinoknak kezdték nevezni. Így a hipotalamusz hormonjai kulcsszerepet játszanak az egyes szervek, szövetek és az egész szervezet többoldalú biológiai funkcióinak hormonális szabályozásának élettani rendszerében.
Eddig 7 stimulánst (liberint) és 3 gátlót (sztatint) fedeztek fel a hypothalamusban az agyalapi mirigy hormonok kiválasztására, nevezetesen: kortikoliberin, tiroliberin, luliberin, folliliberin, szomatoliberin, prolaktoliberin, melanoliberin, szomatosztatin, prolaktosztatin (T és melanosztatin). 8.1) . Öt hormont izoláltak tiszta formában, amelyek elsődleges szerkezetét kémiai szintézissel igazolták.
A hypothalamus hormonok tiszta formájú beszerzésének nagy nehézségeit az magyarázza, hogy rendkívül alacsony tartalommal rendelkeznek az eredeti szövetben. Így ahhoz, hogy csak 1 mg tiroliberint izoláljunk, 7 tonna, 5 millió juhból nyert hipotalamusz feldolgozására volt szükség.
Meg kell jegyezni, hogy nem minden hipotalamusz hormon tűnik szigorúan egyetlen hipofízishormonnak sem. A tirotropin-felszabadító hormonról kimutatták, hogy a tirotropin mellett prolaktint is, a luliberin esetében pedig a luteinizáló hormonon kívül tüszőstimuláló hormont is.

1 A hipotalamusz hormonoknak nincs határozott neve. Javasoljuk, hogy az agyalapi mirigy hormon nevének első részéhez a „liberin” végződést adják hozzá; például a „tirotropin-felszabadító hormon” olyan hipotalamusz hormont jelent, amely serkenti a tirotropin, az agyalapi mirigy megfelelő hormonjának felszabadulását (és esetleg szintézisét). Az agyalapi mirigy trópusi hormonjainak felszabadulását (és esetleg szintézisét) gátló hipotalamusz faktorok nevei hasonló módon alakulnak ki - a „statin” végződést hozzáadjuk. Például a „szomatosztatin” egy hipotalamusz peptidet jelent, amely gátolja az agyalapi mirigy növekedési hormonjának, a szomatotropinnak a felszabadulását (vagy szintézisét).
Megállapítást nyert, hogy kémiai szerkezete szerint minden hipotalamusz hormon kis molekulatömegű peptid, úgynevezett szokatlan szerkezetű oligopeptid, bár a pontos aminosav-összetétel és primer szerkezet nem mindegyiknél tisztázott. Bemutatjuk az eddig megszerzett adatokat a hipotalamusz ismert 10 hormonja közül hat kémiai természetére vonatkozóan.
1. Tiroliberin(Pyro-Glu-Gis-Pro-NH 2):

A tiroliberint egy tripeptid képviseli, amely piroglutaminsavból (ciklusos) savból, hisztidinből és prolinamidból áll, amelyeket peptidkötések kapcsolnak össze. A klasszikus peptidekkel ellentétben az N- és C-terminális aminosavaknál nem tartalmaz szabad NH 2 - és COOH csoportokat.
2. GnRH egy dekapeptid, amely 10 aminosavból áll a következő sorrendben:
Pyro-Glu-Gis-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-NH 2
A terminális C-aminosav a glicinamid.
3. Szomatosztatin egy ciklikus tetradekapeptid (14 aminosavból áll):
Ez a hormon abban különbözik az előző két hormontól a ciklikus szerkezeten kívül, hogy az N-terminálison nem tartalmaz piroglutaminsavat: a 3. és 14. pozícióban lévő két cisztein között diszulfid kötés jön létre. Meg kell jegyezni, hogy a szomatosztatin szintetikus lineáris analógja is hasonló biológiai aktivitással rendelkezik, ami a természetes hormon diszulfidhídjának jelentéktelenségét jelzi. A szomatosztatint a hipotalamusz mellett a központi és a perifériás idegrendszer neuronjai termelik, valamint a hasnyálmirigy-szigetek (Langerhans-szigetek) S-sejtjei szintetizálják a hasnyálmirigyben és a bélsejtekben. Biológiai hatásainak széles skálája van; különösen kimutatták a növekedési hormon szintézisére gyakorolt gátló hatást az adenohipofízisben, valamint közvetlen gátló hatását az inzulin és a glukagon bioszintézisére a Langerhans-szigetek β- és α-sejtjeiben.
4. Szomatoliberin a közelmúltban természetes forrásokból izolálták. 44 aminosavból áll, teljesen feltárt szekvenciával. Ezenkívül a kémiailag szintetizált dekapeptid a szomatoliberin biológiai aktivitásával rendelkezik:
N-Val-Gis-Lei-Ser-Ala-Glu-Gln-Liz-Glu-Ala-ON.
Ez a dekapeptid serkenti a hipofízis növekedési hormon szomatotropin szintézisét és szekrécióját.
5. Melanoliberin, amelynek kémiai szerkezete hasonló a nyitott gyűrűs hormon oxitocinéhez (tripeptid oldallánc nélkül), szerkezete a következő:
N-Cisz-Tyr-Ile-Gln-Asn-Cis-OH.
6. Melanostatin(melanotropin inhibitor faktor) vagy egy tripeptid: Pyro-Glu-Leu-Gly-NH 2, vagy egy pentapeptid a következő szekvenciával:
Pyro-Glu-Gis-Phen-Arg-Gly-NNH 2.
Meg kell jegyezni, hogy a melanoliberin stimuláló hatású, a melanostatin pedig éppen ellenkezőleg, gátló hatással van a melanotropin szintézisére és szekréciójára az agyalapi mirigy elülső részében.
A felsorolt hipotalamusz hormonokon kívül egy másik hormon kémiai természetét is intenzíven tanulmányozták - kortikoliberin. Aktív készítményeit mind a hipotalamusz szövetéből, mind az agyalapi mirigy hátsó lebenyéből izolálták; Van egy vélemény, hogy az utóbbi hormonraktárként szolgálhat a vazopresszin és az oxitocin számára. A közelmúltban 41 aminosavból álló, tisztázott szekvenciájú kortikoliberint izoláltak a birka hipotalamuszából.
A hipotalamusz hormonjainak szintézisének helye valószínűleg az idegvégződések - a hipotalamusz szinaptoszómái, mivel itt található a hormonok és a biogén aminok legmagasabb koncentrációja. Ez utóbbiakat a perifériás endokrin mirigyek hormonjaival együtt a visszacsatolási elv alapján a hipotalamusz hormonok szekréciójának és szintézisének fő szabályozóinak tekintik. A tiroliberin bioszintézisének mechanizmusa, amely nagy valószínűséggel a nem riboszómális úton megy végbe, magában foglalja az SH-tartalmú szintetáz vagy olyan enzimkomplex részvételét, amelyek katalizálják a glutaminsav piroglutaminsavvá történő ciklizációját, peptidkötés kialakulását és a a prolin amidálása glutamin jelenlétében. Hasonló bioszintézis mechanizmus létezését a megfelelő szintetázok részvételével a gonadoliberin és a szomatoliberin vonatkozásában is feltételezik.
A hipotalamusz hormonok inaktiválásának módjait nem vizsgálták kellőképpen. A tirotropin-releasing hormon felezési ideje patkányvérben 4 perc. Az inaktiváció akkor következik be, amikor a peptidkötés megszakad (patkány és humán vérszérum exo- és endopeptidázai hatására), és amikor a prolinamid molekulából eltávolítják az amidcsoportot. Az emberek és számos állat hipotalamuszában egy specifikus enzimet, a piroglutamil-peptidázt fedeztek fel, amely katalizálja a piroglutaminsav molekulának a tiroliberinről vagy gonadoliberinről való lehasadását.
A hipotalamusz hormonok közvetlenül befolyásolják a „kész” hormonok szekrécióját (pontosabban felszabadulását), illetve ezeknek a hormonoknak a de novo bioszintézisét. Bebizonyosodott, hogy a cAMP részt vesz a hormonális jelátvitelben. Kimutatták, hogy az agyalapi mirigy sejtek plazmamembránjaiban specifikus adenohipofízis receptorok léteznek, amelyekhez hipotalamusz hormonok kötődnek, majd Ca 2+ és cAMP ionok szabadulnak fel az adenilát-cikláz és a Ca 2+ -ATP és Mg 2 membránkomplexek rendszerén keresztül. + -ATP; ez utóbbi a megfelelő agyalapi mirigy hormon felszabadulására és szintézisére egyaránt hat a protein kináz aktiválásával (lásd alább).
A felszabadító faktorok hatásmechanizmusának tisztázásában, beleértve a megfelelő receptorokkal való kölcsönhatásukat, a tiroliberin és a gonadoliberin szerkezeti analógjai fontos szerepet játszottak. Ezen analógok némelyike még magasabb hormonaktivitású és elhúzódó hatású, mint a hipotalamusz természetes hormonjai. Azonban még sok munka vár még a már felfedezett felszabadító faktorok kémiai szerkezetének tisztázására és hatásuk molekuláris mechanizmusainak megfejtésére.
A felszabadító hormonok emberi neurohormonok, amelyeket a hipotalamusz magjai szintetizálnak. Gátolják (sztatinok) vagy serkentik (liberinek) az agyalapi mirigy trópusi hormonjainak termelését. Az endokrin mirigyek munkája aktiválódik, és szabályozzák a hormonok felszabadulását. A központi idegrendszer magasabb részei a hormonok felszabadulásának köszönhetően szoros kapcsolatban állnak egymással.
A hipotalamusz funkciói
Az endokrin rendszer egyik fontos alkotóeleme, amely a hormontermelésért felelős, a hipotalamusz. A hipotalamusz által termelt anyagok a szervezet anyagcsere-folyamataiban részt vevő hormonok.
A hipotalamusz idegsejteket tartalmaz, amelyek biztosítják a szervezet normális működéséhez szükséges alapvető anyagok termelését. Ezeket a sejteket neuroszekréciós sejteknek nevezik. Feladatuk az idegrendszer különböző részei által továbbított impulzusok fogadása. Az elemek felszabadulása axovasális szinapszisokon keresztül történik.
A hipotalamusz által termelt felszabadító hormonok, vagy más néven sztatinok és liberinek nélkülözhetetlenek az agyalapi mirigy normális működéséhez. Kémiai természetüknél fogva peptidek. A kémiai és idegi impulzusoknak köszönhetően szintézisük megtörténik, és a hypothalamus-hipofízis rendszeren keresztül a vérrel az agyalapi mirigybe kerülnek.
A hormonok osztályozása
Nézzük a leghíresebb felszabadító hormonokat:
- Szekréciót gátló - szomatosztatinról, melanosztatinról, prolaktosztatinról beszélünk.
- Stimuláló - melanoliberinről, prolaktoliberinről, folliberinről, luliberinről, szomatoliberinről, tiroliberinről, gonadoliberinről és kortikoliberinről beszélünk.
A felsorolt anyagokat, vagy inkább azok egy részét, nem csak a hipotalamusz (például a hasnyálmirigy) más szervek is előállíthatják.
Statinok és liberinek
Az agyalapi mirigy működése közvetlenül függ tőlük. A perifériás endokrin mirigyek működését is befolyásolják:
- pajzsmirigy;
- petefészkek lányoknál;
- herék férfiaknál.

A legismertebb sztatinok és liberinek:
- dopamin;
- gonadoliberin (lyuliberin, folliberin);
- melonosztatin;
- szomatosztatin;
- Pajzsmirigy hormon.
A luteinizáló és tüszőstimuláló hormonok agyalapi mirigy általi kiválasztását a gonadoliberinek biztosítják.
A férfiaknál az androgének aktivitását a gonadoliberinek is befolyásolják, amelyek hozzájárulnak a spermiumok aktivitásának és a libidó szintjének növekedéséhez.
A nőknél pedig a neurohormonok felelősek a menstruációs ciklusért, a hormonok mennyisége pedig a ciklus fázisától függően változik.
A felszabadító hormonok elégtelen termelése gyakran meddőséget és impotenciát okoz.
A hormonok jellemzői
A szorongásért felelős kortikoliberin hormont a hipotalamusz termeli. Ez egy másik fontos felszabadító tényező, amely az agyalapi mirigy hormonjaival együtt hat, és befolyásolja a mellékvesék működését. E hormon hiányában szenvedők gyakran magas vérnyomásban és mellékvese-elégtelenségben szenvednek.
A gonadotropin-felszabadító hormon, egy olyan hormon, amely fokozza a gonadotropinok termelését, szintén a hipotalamusz terméke. Gonadotropin-felszabadító hormonnak is nevezik.
A nemi szervek normális működése nem létezhet GnRH nélkül. Ez a hormon felelős a nők menstruációs ciklusának természetes lefolyásáért. Részvételével megtörténik a tojás érésének és felszabadulásának folyamata. Ez a hormon felelős a libidóért (szexuális vágy). Ennek a hormonnak a hipotalamusz általi elégtelen termelésével a nők gyakran meddőséget okoznak. Milyen egyéb felszabadító hormonok léteznek?

Szomatoliberin
Legfeltűnőbb gyermek- és serdülőkorban. Fő tulajdonsága a szervek és testrendszerek növekedési folyamatainak normalizálása. A gyermek teljes fejlődése és formálódása a termeléstől függ. Ennek a hormonnak a hipotalamusz általi elégtelen termelése vezethet
Prolaktoliberin
Termelése a legaktívabban a terhesség alatt és a gyermek anya általi táplálásának teljes időtartama alatt történik. Ez a felszabadító faktor normalizálja a prolaktin termelését, amely az emlőmirigyek csatornáit képezi.
Prolaktosztatin
A prolaktosztatin a hipotalamusz által termelt sztatinok egy alosztályába tartozik, és a prolaktin gátlásáért felelős.
A prolaktosztatinok közé tartoznak:
· dopamin;
szomatosztatin;
· melanostatin.
Fő tevékenységük az agyalapi mirigy és a hipotalamusz trópusi hormonjainak elnyomására irányul.
Melanotropin-felszabadító hormon
A melanintermelés folyamatát és a pigmentsejtek osztódását a melanoliberin befolyásolja. Az agyalapi mirigy PRD-jének elemeit is érinti.
Befolyásolja az emberi neurofiziológiai viselkedést. A depresszió enyhítésére és a parkinsonizmus kezelésére használják.
Tirotropin-felszabadító hormon (TRH)
A hipotalamusz tirotropin-felszabadító hormonjai közé tartozik a tirotropin-felszabadító hormon is. Elősegíti az adenohypophysis pajzsmirigy-stimuláló hormonjainak termelődését.
Kismértékben befolyásolja a prolaktin termelési folyamatát. A tiroliberin biztosítja a tiroxin koncentrációjának növekedését a vérben.
A központi idegrendszer nagy hatással van a hormontermelés folyamataira. A szabályozó rendszer neuroszekréciós sejtjei felelősek a neurohormonok termeléséért.
A liberinek fő funkciói

Ezek a hipotalamusz felszabadító hormonjai. A gonadotropin-felszabadító hormonok normalizálják a nők és férfiak reproduktív rendszerének működését.
Felelősek a tüszőstimuláló hormonok szaporodásáért, és befolyásolják a herék és a petefészkek működését.
Egy olyan komponens, mint a luliberin, elválasztó hatást fejt ki az ovulációra, megteremtve a magzat fogantatásának lehetőségét.
Az intim élet iránt közömbös nőkben a luliberin és a folliberin nem termelődik elegendő mennyiségben.
A hipotalamusz középső lebenyéhez kapcsolódnak felszabadító faktorok is, de ezek kapcsolatát az agyalapi mirigy és az adenohypophysis elemeivel nem vizsgálták.
Hormonfelszabadító agonisták: gyógyszerek
Mint már említettük, ezeket a hormonokat a hipotalamusz termeli. Ha a petefészkeket stimulálni kell, például IVF-eljárás előtt, agonistákat vagy felszabadító hormonok analógjait alkalmazzák. Vagyis ugyanolyan hatással vannak a szervezetre, mint a saját hormonja.
De nagy a valószínűsége a nemkívánatos reakciók kialakulásának a női test részéről. Ez az ösztrogénszint csökkenése miatt következik be. A leggyakoribb jelenségek a következők:
- fejfájás;
- túlzott izzadás;
- árapály;
- hüvelyi szárazság;
- hangulatingadozás;
- depresszív állapotok.
A következő gyógyszereket használják:


Áttekintettük a hormon felszabadító hormon agonisták.
Antagonisták
Mivel az ösztradiol szintje rendkívül megemelkedik hormon-felszabadító hormon agonisták szedésekor, a luteinizáló hormon szintje megnövekedhet. Ez idő előtti ovulációhoz és a petehalálhoz vezet. Ennek megakadályozására hormonfelszabadító hormon antagonistákat alkalmaznak. Hatásuk következtében az agyalapi mirigy ismét stimulálható. nem nyilvánul meg, de ez gyakran előfordult a GnRH agonisták hosszú távú alkalmazása miatt. Öt nappal a tüszőstimuláló hormon használatának megkezdése után adják be.
Ahhoz, hogy a terápia sikeres legyen, minden gyógyszerfelírást csak szakember végezhet.
Libériaiak:
- tiroliberin;
- kortikoliberin;
- szomatoliberin;
- prolaktoliberin;
- melanoliberin;
- gonadoliberin (lyuliberin és follyliberin)
- szomatosztatin;
- prolaktosztatin (dopamin);
- melanostatin;
- kortikosztatin
Neuropeptidek:
- enkefalinok (leucin-enkefalin (leu-enkefalin), metionin-enkefapin (met-enkefalin));
- endorfinok (a-endorfin, (β-endorfin, γ-endorfin);
- dinorfin A és B;
- proopiomelanokortin;
- neurotenzin;
- anyag P;
- kiotorfin;
- vasointestinalis peptid (VIP);
- kolecisztokinin;
- neuropeptid-Y;
- agouterin fehérje;
- orexin A és B (hipokretinek 1 és 2);
- ghrelin;
- delta alvást indukáló peptid (DSIP) stb.
Hipotalamusz-hátsó hipofízis hormonok:
- vazopresszin vagy antidiuretikus hormon (ADH);
- oxitocin
Monoaminok:
- szerotonin;
- noradrenalin;
- adrenalin;
- dopamin
A hypothalamus és a neurohypophysis effektorhormonjai
A hypothalamus és a neurohypophysis effektorhormonjai a vazopresszin és az oxitocin. A hypothalamus SON és PVN magnocelluláris neuronjaiban szintetizálódnak, axonális transzporttal jutnak el a neurohypophysisbe, és az arteria hypophysis inferior kapillárisainak vérébe kerülnek (1. ábra).
vazopresszin
Antidiuretikus hormon(ADG, ill vazopresszin) - 9 aminosavból álló peptid, tartalma 0,5-5 ng/ml.
A hormon bazális szekréciójának napi ritmusa van, maximum a kora reggeli órákban. A hormon szabad formában kerül szállításra a vérben. Felezési ideje 5-10 perc. Az ADH a membrán 7-TMS receptorainak és másodlagos hírvivőinek stimulálásával hat a célsejtekre.
Az ADH funkciói a szervezetbenAz ADH célsejtjei a vese gyűjtőcsatornáinak hámsejtjei és az érfalak sima myocytái. A vese gyűjtőcsatornáinak hámsejtjeiben lévő V 2 receptorok stimulálása és a bennük lévő cAMP szintjének növelése révén az ADH növeli a víz visszaszívását (10-15%-kal vagy 15-22 l/nap), elősegíti a koncentrációt. és a végső vizelet mennyiségének csökkenése. Ezt a folyamatot antidiurézisnek, az ezt okozó vazopresszint pedig ADH-nak nevezik.
A hormon nagy koncentrációban a vaszkuláris sima myociták V 1 receptoraihoz kötődik, és a bennük lévő IPG és Ca 2+ -ionok szintjének emelkedésén keresztül a szívizomsejtek összehúzódását, az artériák szűkülését és a vérnyomás emelkedését okozza. A hormonnak az erekre gyakorolt hatását pressornak nevezik, innen ered a hormon neve - vazopresszin. Az ADH emellett részt vesz az ACTH szekréció stimulálásában stressz alatt (V 3 receptorokon és intracelluláris IPG és Ca 2+ ionokon keresztül), a szomjúságmotiváció és az ivási magatartás kialakításában, valamint a memóriamechanizmusokban.
Rizs. 1. Hipotalamusz és hipofízis hormonok (RG - releasing hormonok (liberinek), ST - sztatinok). Magyarázatok a szövegben
Az ADH szintézise és felszabadulása fiziológiás körülmények között serkenti a vér ozmotikus nyomásának (hiperozmolaritás) növekedését. A hiperozmolaritást a hipotalamusz ozmoszenzitív neuronjainak aktiválása kíséri, amelyek viszont serkentik az ADH szekrécióját a SOY és a PVN neuroszekréciós sejtjei által. Ezek a sejtek a vazomotoros centrum neuronjaihoz is kapcsolódnak, amelyek a pitvar és a sinocarotis zóna mechano- és baroreceptoraitól kapnak információt a véráramlásról. Ezeken a kapcsolatokon keresztül reflexszerűen serkentik az ADH szekrécióját, amikor a keringő vértérfogat (CBV) csökken és a vérnyomás csökken.
A vazopresszin fő hatásai
- Aktiválja
- Serkenti a vaszkuláris simaizom összehúzódását
- Aktiválja a szomjúságközpontot
- Részt vesz a tanulási mechanizmusokban és
- Szabályozza a hőszabályozási folyamatokat
- Neuroendokrin funkciókat lát el, az autonóm idegrendszer közvetítője
- Részt vesz a szervezésben
- Befolyásolja az érzelmi viselkedést
Fokozott ADH-szekréciót figyeltek meg az angiotenzin II megnövekedett vérszintje, stressz és fizikai aktivitás mellett is.
Az ADH felszabadulása csökken a vér ozmotikus nyomásának csökkenésével, a vértérfogat és (vagy) vérnyomás növekedésével, valamint az etil-alkohol hatására.
Az ADH szekréciójának és hatásának elégtelensége a hypothalamus és a neurohypophysis endokrin funkciójának elégtelenségéből, valamint az ADH-receptorok működési zavarából (a vese gyűjtőcsatornáinak hámjában a V 2 receptorok hiánya, csökkent érzékenysége) lehet a következménye. ), amely a kis sűrűségű vizelet túlzott, akár 10-15 l/nap kiválasztásával és a testszövetek hipohidratációjával jár együtt. Ezt a betegséget nevezték el diabetes insipidus. Ellentétben a cukorbetegséggel, amelyben a túlzott vizelettermelést a vér glükózszintjének emelkedése okozza, diabetes insipidus A vércukorszint normális marad.
Az ADH túlzott szekréciója a szervezetben a diurézis és a vízvisszatartás csökkenésében nyilvánul meg, egészen a sejtödéma és a vízmérgezés kialakulásáig.
Oxitocin
Az oxitocin funkciói a szervezetbenOxitocin- 9 aminosavból álló peptid, amelyet a vér szabad formában szállít, felezési idő - 5-10 perc, a membrán stimulálásával hat a célsejtekre (a méh sima myocytáira és az emlőcsatornák myoepitslialis sejtjeire) 7-TMS receptorok és az IPE és Ca 2+ ionok szintjének növekedése bennük.
A terhesség vége felé természetesen megfigyelhető hormonszint-emelkedés a szülés és a szülés utáni időszakban fokozott méhösszehúzódást okoz. A hormon serkenti az emlőmirigy-csatornák myoepithelialis sejtjeinek összehúzódását, elősegítve a tejelválasztást az újszülöttek táplálásakor.
Az oxitocin főbb hatásai:
- Serkenti a méhösszehúzódásokat
- Aktiválja a tejelválasztást
- Vízhajtó és nátriuretikus hatása van, részt vesz a víz-só viselkedésben
- Szabályozza az ivási viselkedést
- Növeli az adenohypophysis hormonok szekrécióját
- Részt vesz a tanulási és memóriamechanizmusokban
- Hipotenzív hatása van
Az oxitocin szintézise a megnövekedett ösztrogénszint hatására fokozódik, felszabadulását pedig egy reflexpálya fokozza, amikor a méhnyak mechanoreceptorai irritálódnak a szülés közbeni nyújtás során, valamint az emlőmirigyek mellbimbóinak mechanoreceptorai. stimulálják a gyermek táplálása során.
A hormon elégtelen működése a méhen belüli vajúdás gyengeségében és a tejelválasztás zavarában nyilvánul meg.
A perifériás endokrin mirigyek funkcióinak bemutatásakor szó esik a hipotalamusz felszabadító hormonokról.
Az agyalapi mirigy effektor hormonjai
Ezek tartalmazzák növekedési hormon(GR), prolaktin(laktotrop hormon - LTG) az adenohypophysis és melanocita stimuláló hormon(MSG) az agyalapi mirigy köztes lebenyének (lásd 1. ábra).

Rizs. 1. Hipotalamusz és hipofízis hormonok (RG - releasing hormonok (liberinek), ST - sztatinok). Magyarázatok a szövegben
szomatotropin
Növekedési hormon (szomatotropin, szomatotrop hormon GH)- 191 aminosavból álló polipeptid, amelyet az adenohypophysis - szomatotrófok - vörös acidofil sejtjei alkotnak. A felezési idő 20-25 perc. Vérrel szállítva szabad formában.
A GH célpontjai a csont-, porc-, izom-, zsírszövet- és májsejtek. Közvetlen hatással van a célsejtekre a katalitikus tirozin kináz aktivitású 1-TMS receptorok stimulálásával, valamint közvetett hatással van a szomatomedinek - inzulinszerű növekedési faktorok (IGF-I, IGF-II) révén, amelyek a májban és a májban képződnek. más szövetek a GR hatásra válaszul.
A szomatomedinek jellemzői
A GH-tartalom az életkortól függ, és kifejezett napi gyakorisággal rendelkezik. A legmagasabb hormontartalom kora gyermekkorban volt megfigyelhető, fokozatos csökkenéssel: 5-ről 20 évre - 6 ng/ml (a pubertás alatti csúcs), 20-40 év között - körülbelül 3 ng/ml, 40 év után - 1 ng/ml ml. A nap folyamán a GH ciklikusan lép be a vérbe - a szekréció hiánya „váladékrobbanással” váltakozik, alvás közbeni maximummal.
A GH fő funkciói a szervezetbenA növekedési hormon közvetlen hatással van a célsejtek anyagcseréjére, valamint a szervek és szövetek növekedésére, ami mind a célsejtekre gyakorolt közvetlen hatásával, mind pedig a szomatomedin C és A (inzulinszerű növekedési faktorok) közvetett hatására érhető el. hepatociták és chondrocyták, amikor GR hatásnak vannak kitéve rajtuk.
A növekedési hormon az inzulinhoz hasonlóan elősegíti a sejtek glükóz felszívódását és hasznosítását, serkenti a glikogén szintézist és részt vesz a normál vércukorszint fenntartásában. Ugyanakkor a GH serkenti a glükoneogenezist és a glikogenolízist a májban; az inzulinszerű hatást felváltja a szigetellenes hatás. Ennek következtében hiperglikémia alakul ki. A GH serkenti a glukagon felszabadulását, ami szintén hozzájárul a hiperglikémia kialakulásához. Ugyanakkor az inzulin képződése nő, de a sejtek érzékenysége csökken.
A növekedési hormon aktiválja a zsírszövet sejtjeiben a lipolízist, elősegíti a szabad zsírsavak mobilizálását a vérbe, és a sejtek energiaként történő felhasználását.
A növekedési hormon serkenti a fehérje anabolizmusát, elősegíti az aminosavak bejutását a máj, az izmok, a porcok és a csontszövet sejtjébe, és aktiválja a fehérje- és nukleinsavak szintézisét. Ez segít az alap anyagcsere intenzitásának növelésében, az izomszövet tömegének növelésében és a csőcsontok növekedésének felgyorsításában.
A GH anabolikus hatását testtömeg-növekedés kíséri zsírfelhalmozódás nélkül. Ugyanakkor a GH elősegíti a nitrogén, foszfor, kalcium, nátrium és víz visszatartását a szervezetben. Mint már említettük, a GH anabolikus hatással bír, és serkenti a növekedést a növekedési faktorok májban és porcokban történő fokozott szintézisén és szekrécióján keresztül, amelyek serkentik a porcsejtek differenciálódását és a csontok megnyúlását. A növekedési faktorok hatására fokozódik a miociták aminosav-ellátása és az izomfehérjék szintézise, ami az izomszövet tömegének növekedésével jár.
A GH szintézisét és szekrécióját a hypothalamus hormon, a szomatoliberin (SGHR - növekedési hormon felszabadító hormon) szabályozza, amely fokozza a GH szekrécióját, valamint a szomatosztatin (SS), amely gátolja a GH szintézisét és szekrécióját. A GH szintje fokozatosan növekszik alvás közben (a hormon maximális tartalma a vérben az alvás első 2 órájában és reggel 4-6 órakor következik be). A hipoglikémia és a szabad zsírsavak hiánya (böjt közben), a felesleges aminosavak (evés után) a vérben növelik a szomatoliberin és a GH szekrécióját. A kortizol hormonok, amelyek szintje fájdalomstressz, sérülés, hideghatás, érzelmi izgalom hatására emelkedik, T 4 és T 3, fokozzák a szomatoliberin szomatotrófokra kifejtett hatását és fokozzák a GH szekréciót. A szomatomedinek, a vér magas glükóz- és szabad zsírsavszintje, valamint az exogén GH gátolják az agyalapi mirigy GH szekrécióját.

Rizs. A szomatotropin szekréció szabályozása

Rizs. A szomatomedinek szerepe a szomatotropin hatásában
A GH túlzott vagy elégtelen szekréciójának élettani következményeit olyan neuroendokrin betegségekben szenvedő betegeknél vizsgálták, akiknél a kóros folyamatot a hipotalamusz és (vagy) az agyalapi mirigy endokrin funkciójának megzavarása kísérte. A GH hatásának csökkenését is tanulmányozták azokban az esetekben, amikor a célsejtek károsodott választ adnak a GH hatására, ami a hormon-receptor kölcsönhatás hibáihoz kapcsolódik.

Rizs. A szomatotropin szekréció napi ritmusa
A GH túlzott szekréciója gyermekkorban a növekedés éles felgyorsulásával (több mint 12 cm/év) és a felnőttkori gigantizmus kialakulásával nyilvánul meg (a férfiak testmagassága meghaladja a 2 métert, a nőknél pedig az 1,9 métert). A test arányai megmaradnak. Felnőtteknél a hormon túltermelése (például agyalapi mirigy daganata esetén) akromegáliával jár – a test egyes részeinek aránytalan növekedésével, amelyek még mindig megőrzik növekedési képességüket. Ez az állkapocs aránytalan fejlődése, a végtagok túlzott megnyúlása miatt megváltozik az ember megjelenése, és az inzulinszám csökkenése miatt kialakuló inzulinrezisztencia miatt diabetes mellitus is társulhat. receptorok a sejtekben és az inzulináz enzim szintézisének aktiválása a májban, amely elpusztítja az inzulint.
A szomatotropin fő hatásaiMetabolikus:
- fehérje anyagcsere: serkenti a fehérjeszintézist, megkönnyíti az aminosavak bejutását a sejtekbe;
- zsíranyagcsere: serkenti a lipolízist, megemelkedik a zsírsavak szintje a vérben, és ezek válnak a fő energiaforrássá;
- szénhidrát-anyagcsere: serkenti az inzulin és a glukagon termelését, aktiválja a máj inzulinázát. Magas koncentrációban serkenti a glikogenolízist, növeli a vércukorszintet, és gátolja a felhasználását
Funkcionális:
- késlelteti a nitrogén, foszfor, kálium, nátrium, víz szervezetét;
- fokozza a katekolaminok és glükokortikoidok lipolitikus hatását;
- aktiválja a szöveti eredetű növekedési faktorokat;
- serkenti a tejtermelést;
- fajspecifikus.
Asztal. A szomatotropin termelés változásának megnyilvánulásai
A gyermekkori GH elégtelen szekréciója vagy a hormon és a receptor közötti kapcsolat megszakadása a növekedési ráta (4 cm/év alatti) gátlásában nyilvánul meg a testarányok és a szellemi fejlődés megőrzése mellett. Ebben az esetben egy felnőttnél törpeség alakul ki (a nők magassága nem haladja meg a 120 cm-t, a férfiaké pedig a 130 cm-t). A törpeséget gyakran szexuális fejletlenség kíséri. Ennek a betegségnek a második neve az agyalapi mirigy törpesége. Felnőtteknél a GH-szekréció hiánya a bazális anyagcsere, a vázizomzat csökkenésében és a zsírtömeg növekedésében nyilvánul meg.
prolaktin
Prolaktin (laktotrop hormon)- LTG) egy 198 aminosavból álló polipeptid, amely ugyanabba a családba tartozik, mint a szomatotronin, és hasonló kémiai szerkezettel rendelkezik.
Az adenohypophysis sárga laktotrófjai (sejtjeinek 10-25% -a, terhesség alatt - akár 70%) kiválasztják a vérbe, szabad formában a vér szállítja, a felezési idő 10-25 perc. A prolaktin az 1-TMS receptorok stimulálásával hat az emlőmirigyek célsejtjeire. A prolaktin receptorok megtalálhatók még a petefészkek, a herék, a méh sejtjeiben, valamint a szívben, a tüdőben, a csecsemőmirigyben, a májban, a lépben, a hasnyálmirigyben, a vesében, a mellékvesékben, a vázizmokban, a bőrben és a központi idegrendszer egyes részeiben.
A prolaktin fő hatása a reproduktív funkcióhoz kapcsolódik. Ezek közül a legfontosabb a laktáció biztosítása az emlőmirigyben lévő mirigyszövet fejlődésének serkentésével a terhesség alatt, illetve a szülés után - a kolosztrum képződése és anyatejré történő átalakulása (laktoalbumin, tejzsírok és szénhidrátok képződése). Magát a tejelválasztást azonban nem befolyásolja, ami a baba táplálása során reflexszerűen történik.
A prolaktin elnyomja a gonadotropinok agyalapi mirigy általi felszabadulását, serkenti a sárgatest fejlődését, csökkenti a progeszteron képződését, gátolja az ovulációt és a terhességet a szoptatás alatt. A prolaktin a terhesség alatt is hozzájárul az anyai szülői ösztön kialakulásához.
A pajzsmirigyhormonokkal, a növekedési hormonnal és a szteroid hormonokkal együtt a prolaktin serkenti a felületaktív anyag termelését a magzat tüdejében, és enyhén csökkenti az anya fájdalomérzékenységét. Gyermekeknél a prolaktin serkenti a csecsemőmirigy fejlődését, és részt vesz az immunreakciók kialakulásában.
A prolaktin képződését és kiválasztását az agyalapi mirigyben a hipotalamusz hormonjai szabályozzák. A prolaktosztatin egy dopamin, amely gátolja a prolaktin szekrécióját. A prolaktoliberin, amelynek természetét nem határozták meg véglegesen, növeli a hormon szekrécióját. A prolaktin szekrécióját serkenti a dopaminszint csökkenése, az ösztrogénszint emelkedése a terhesség alatt, a szerotonin és a melatonin tartalom növekedése, valamint egy reflexút, amikor a mellbimbó mechanoreceptorai irritálódnak a mellbimbó működése során. szívás, a jelek, amelyekből a hipotalamuszba jutnak, és serkentik a prolaktoliberin felszabadulását.

Rizs. A prolaktin szekréció szabályozása
A prolaktintermelés jelentősen megnő szorongás, stressz, depresszió és súlyos fájdalom esetén. Az FSH, az LH és a progeszteron gátolják a prolaktin szekrécióját.
A prolaktin fő hatásai:
- Fokozza a mell növekedését
- Beindítja a tejszintézist terhesség és szoptatás alatt
- Aktiválja a corpus luteum szekréciós aktivitását
- Serkenti a vazopresszin és az aldoszteron kiválasztását
- Részt vesz a víz-só anyagcsere szabályozásában
- Serkenti a belső szervek növekedését
- Részt vesz az anyai ösztön megvalósításában
- Növeli a zsír- és fehérjeszintézist
- Hiperglikémiát okoz
- Autokrin és parakrin moduláló hatása van az immunválaszra (prolaktin receptorok a T-limfocitákon)
A hormon feleslege (hiperprolaktinémia) lehet fiziológiás és kóros. A prolaktinszint emelkedése egészséges embernél terhesség, szoptatás, intenzív fizikai aktivitás után és mély alvás alatt figyelhető meg. A prolaktin kóros hiperprodukciója az agyalapi mirigy adenomához kapcsolódik, és megfigyelhető a pajzsmirigy betegségeiben, a májcirrhosisban és más patológiákban.
A hiperprolaktinémia a nőknél menstruációs rendellenességeket, hipogonadizmust és az ivarmirigyek csökkent működését, az emlőmirigyek méretének növekedését, galaktorrhoeát okozhat szoptató nőknél (fokozott tejtermelés és -elválasztás); férfiaknál - impotencia és meddőség.
A prolaktinszint csökkenése (hipoprolaktinémia) megfigyelhető az agyalapi mirigy elégtelenségével, terhesség utáni terhességgel vagy számos gyógyszer bevétele után. Az egyik megnyilvánulása az elégtelen laktáció vagy annak hiánya.
Melantropin
Melanocita stimuláló hormon(MSG, melanotropin, intermedin) egy 13 aminosavból álló peptid, amely magzatban és újszülöttben az agyalapi mirigy köztes zónájában képződik. Felnőtteknél ez a zóna csökken, és az MSH korlátozott mennyiségben termelődik.
Az MSH prekurzora a proopiomelanocortin polipeptid, amelyből adrenokortikotrop hormon (ACTH) és β-lipotroin is képződik. Az MSH-nak három típusa van - a-MSH, β-MSH, y-MSH, amelyek közül az a-MSH rendelkezik a legnagyobb aktivitással.
Az MSH fő funkciói a szervezetbenA hormon a tirozináz enzim szintézisét és a melanin képződését (melanogenezist) indukálja a G-proteinhez kapcsolódó specifikus 7-TMS receptorok stimulálásával a célsejtekben, amelyek a bőr, a haj és a retina pigmenthámjának melanocitái. Az MSH a melanoszómák szétszóródását okozza a bőrsejtekben, ami a bőr sötétedésével jár együtt. Ilyen sötétedés akkor következik be, amikor az MSH-tartalom emelkedik, például terhesség vagy mellékvese-betegség (Addison-kór) idején, amikor nemcsak az MSH, hanem az ACTH és a β-lipotropin szintje is megemelkedik a vérben. Ez utóbbiak a pro-opiomelanocortin származékaiként szintén fokozhatják a pigmentációt, és ha egy felnőtt szervezetében az MSH szintje nem megfelelő, akkor funkcióit részben kompenzálni tudja.
Melantropinok:
- Aktiválja a tirozináz enzim szintézisét a melanoszómákban, amit melanin képződés kísér
- Részt vesznek a melanoszómák bőrsejtekben való diszperziójában. A diszpergált melanin granulátum külső tényezők (világítás stb.) részvételével aggregálódik, így a bőr sötét színt kap.
- Vegyen részt az immunválasz szabályozásában
Az agyalapi mirigy trópusi hormonjai
Az adenogynophysisben képződnek, és szabályozzák a perifériás endokrin mirigyek célsejtjeinek, valamint a nem endokrin sejtek működését. A pajzsmirigy, a mellékvesekéreg és az ivarmirigyek azok a mirigyek, amelyek működését a hipotalamusz-hipofízis-endokrin rendszer hormonjai szabályozzák.
Tirotropin
Pajzsmirigy-stimuláló hormon(HKT, tirotropin) az adenohypophysis bazofil tirotrófjai által szintetizált, a- és β-alegységekből álló glikoprotein, melynek szintézisét különböző gének határozzák meg.
A TSH a-alegység szerkezete hasonló a placentában képződő lugeinizáló hormon, tüszőstimuláló hormon és humán koriongonadotropin összetételében lévő alegységeihez. A TSH a-alegysége nem specifikus, és nem határozza meg közvetlenül biológiai hatását.
A tirotropin a-alegységét a vérszérum körülbelül 0,5-2,0 μg/l mennyiségben tartalmazhatja. Koncentrációjának magasabb szintje lehet a TSH-t kiválasztó agyalapi mirigy daganat kialakulásának egyik jele, és a menopauza utáni nőknél figyelhető meg.
Ez az alegység szükséges ahhoz, hogy specifitást adjon a TSH molekula térszerkezetének, mivel a tirotropin képessé válik a pajzsmirigy pajzsmirigy pajzsmirigyének membránreceptorainak stimulálására és biológiai hatásainak kiváltására. A TSH ezen szerkezete a molekula a- és béta-láncainak nem kovalens kötődése után jön létre. Ezenkívül a 112 aminosavból álló p-alegység szerkezete a meghatározó a TSH biológiai aktivitásának megnyilvánulására. Ezenkívül a TSH biológiai aktivitásának és metabolizmusának fokozása érdekében a TSH molekula glikozilációja szükséges a tirotrófok durva endoplazmatikus retikulumában és a Golgi apparátusban.
Ismertek olyan esetek, amikor a gyerekekben a szintézist kódoló gén pontmutációja van (a TSH β-lánca, aminek eredményeként a megváltozott szerkezetű P-alegység szintetizálódik, nem képes kölcsönhatásba lépni az α-alegységgel és biológiailag aktív képződni) tnrotropin.Hasonló patológiájú gyermekeknél a hypothyreosis klinikai tünetei vannak.
A TSH koncentrációja a vérben 0,5 és 5,0 μU/ml között van, és éjfél és négy óra között éri el a maximumát. A TSH szekréció délutánonként minimális. A TSH-szint ezen ingadozása a nap különböző szakaszaiban nincs jelentős hatással a T4 és T3 koncentrációjára a vérben, mivel a szervezetben nagy mennyiségű extrathyreoidális T4 található. A TSH felezési ideje a vérplazmában körülbelül fél óra, napi termelése 40-150 mU.
A tirotropin szintézisét és szekrécióját számos biológiailag aktív anyag szabályozza, amelyek közül vezető szerepet tölt be a hipotalamusz TRH-ja és a pajzsmirigy által a vérbe szekretált szabad T4, T3.
A tirotropin felszabadító hormon egy hipotalamusz neuropeptid, amelyet a hipotalamusz neuroszekréciós sejtjei termelnek, és serkentik a TSH szekrécióját. A TRH-t a hipotalamusz sejtjei axovasalis szinapszisokon keresztül választják ki az agyalapi mirigy portális ereinek vérébe, ahol a thyrotroph receptorokhoz kötődik, serkentve a TSH szintézisét. A TRH szintézist serkenti a T4 és T3 csökkent szintje a vérben. A TRH szekréciót egy negatív visszacsatolási csatornán keresztül is szabályozza a tirotropin szintje.
A TRH többféle hatással van a szervezetre. Serkenti a prolaktin szekrécióját, és ha a TRH szintje megemelkedett, a nők hiperprolaktinémia hatását tapasztalhatják. Ez az állapot akkor alakulhat ki, ha a pajzsmirigy működése csökken, és a TRH-szint emelkedik. A TRH az agy más struktúráiban is megtalálható, a gyomor-bél traktus falaiban. Úgy gondolják, hogy szinapszisokban neuromodulátorként használják, és depresszióban antidepresszáns hatású.
Asztal. A tirotropin fő hatásai
A TSH szekréciója és szintje a plazmában fordítottan arányos a vér szabad T 4, T 3 és T 2 koncentrációjával. Ezek a hormonok egy negatív visszacsatolási csatornán keresztül elnyomják a tirotropin szintézisét, mind közvetlenül magukra a tirotrófokra hatnak, mind pedig a hipotalamusz TRH szekréciójának csökkentésén keresztül (a hipotalamusz neuroszekréciós sejtjei, amelyek a TRH-t és a hipofízis thyreotrófokat alkotják a T 4 és T 3 célsejtjei). Amikor a pajzsmirigyhormonok koncentrációja a vérben csökken, például hypothyreosis esetén, az adenohypophysis sejtjei között megnövekszik a thyrotroph populáció százalékos aránya, fokozódik a TSH szintézise és emelkedik a vérszintje. .
Ezek a hatások az agyalapi mirigy thyreotrophjaiban expresszálódó TR 1 és TR 2 receptorok pajzsmirigyhormonok általi stimulációjának következményei. Kísérletek kimutatták, hogy a TG receptor TR 2 izoformája kulcsfontosságú a TSH gén expressziójában. Nyilvánvaló, hogy a pajzsmirigyhormon-receptorok expressziójának, szerkezetének vagy affinitásának megsértése az agyalapi mirigyben a TSH képződésének és a pajzsmirigy működésének megsértéseként nyilvánulhat meg.
A szomatosztatin, a szerotonin, a dopamin, valamint az IL-1 és IL-6, amelyek szintje a szervezetben a gyulladásos folyamatok során megemelkedik, gátló hatással van az agyalapi mirigy TSH-szekréciójára. Gátolja a TSH noradrenalin és glükokortikoid hormonok szekrécióját, ami stressz körülmények között is megfigyelhető. A TSH szint megemelkedik a pajzsmirigy alulműködésével, és emelkedhet részleges thyrsoidectomia és (vagy) pajzsmirigydaganatok radiojód-kezelése után. Ezt az információt az orvosoknak figyelembe kell venniük a pajzsmirigy-rendszeri betegségekben szenvedő betegek vizsgálatakor a betegség okainak helyes diagnosztizálása érdekében.
A tirotropin a pajzsmirigy-funkciók fő szabályozója, felgyorsítja a TG szintézisének, tárolásának és kiválasztásának szinte minden szakaszát. A TSH hatására felgyorsul a pajzsmirigyek szaporodása, megnő a tüszők és maga a pajzsmirigy mérete, erezettsége fokozódik.
Mindezek a hatások komplex biokémiai és fizikai-kémiai reakciók eredménye, amelyek a tirotropinnak a pajzsmirigy alapmembránján található receptorához való kötődése és a G-fehérjéhez kapcsolt adenilát-cikláz aktiválódása után következnek be, ami a a cAMP szintje, a cAMP-dependens protein kináz A aktiválása, amely a pajzsmirigyekben a kulcsenzimeket foszforilezi. A pajzsmirigysejtekben a kalcium szintje nő, a jodid felszívódása nő, transzportja és beépülése a pajzsmirigy-peroxidáz enzim részvételével a tiroglobulin szerkezetébe felgyorsul.
A TSH hatására a pszeudopodia képződési folyamatok aktiválódnak, felgyorsítva a tiroglobulin felszívódását a kolloidból a pajzsmirigyekbe, felgyorsul a kolloid cseppek képződése a tüszőkben és a tiroglobulin hidrolízise bennük a lizoszómális enzimek hatására, a pajzsmirigyek metabolizmusa aktiválódik, ami a glükóz, az oxigén és a glükóz felszívódásának sebességének növekedésével jár együtt a pajzsmirigysejtek általi glükóz oxidációjával, felgyorsítja a fehérjék és foszfolipidek szintézisét, amelyek szükségesek a pajzsmirigysejtek növekedéséhez és számának növekedéséhez és a tüszők képződése. Magas koncentrációban és hosszan tartó expozíció mellett a tirotropin a pajzsmirigysejtek szaporodását, tömegének és méretének növekedését (golyva), a hormonok szintézisének fokozódását és hiperfunkciójának kialakulását okozza (elegendő jóddal). A szervezetben kifejlődik a felesleges pajzsmirigyhormonok hatása (a központi idegrendszer fokozott ingerlékenysége, tachycardia, fokozott bazális anyagcsere és testhőmérséklet, kidudorodó szemek és egyéb változások).
A TSH hiánya a pajzsmirigy alulműködésének (hypothyreosis) gyors vagy fokozatos kialakulásához vezet. Egy személynél az alapvető anyagcsere csökkenése, álmosság, letargia, adynámia, bradycardia és egyéb változások lépnek fel.
A tirotropin, amely más szövetekben stimulálja a receptorokat, növeli a szelénfüggő dejodináz aktivitását, amely a tiroxint aktívabb trijódtironinná alakítja, valamint receptoraik érzékenységét, ezáltal „felkészíti” a szöveteket a pajzsmirigyhormonok hatásaira.
A TSH és a receptor kölcsönhatásának megszakadása, például a receptor szerkezetében vagy a TSH-hoz való affinitása miatt, számos pajzsmirigybetegség patogenezisének hátterében állhat. Különösen a TSH-receptor szerkezetének változása a szintézist kódoló gén mutációja következtében a pajzsmirigysejtek TSH-hatásra való érzékenységének csökkenéséhez vagy hiányához, valamint veleszületett primer hypothyreosis kialakulásához vezet.
Mivel a TSH és a gonadotropin α-alegységeinek szerkezete megegyezik, a gonadotropin magas koncentrációban (például chorionepitheliomákban) versenyezhet a TSH receptorokhoz való kötődésért, és serkenti a TG képződését és kiválasztását a pajzsmirigyben.
A TSH receptor nem csak a tirotropinhoz képes kötődni, hanem autoantitestekhez is - immunglobulinokhoz, amelyek stimulálják vagy blokkolják ezt a receptort. Ez a kötődés a pajzsmirigy autoimmun betegségeiben, és különösen az autoimmun pajzsmirigygyulladásban (Graves-kór) fordul elő. Ezen antitestek forrása általában a B-limfociták. A pajzsmirigy-stimuláló immunglobulinok a TSH receptorhoz kötődnek, és a TSH-hoz hasonlóan hatnak a mirigy pajzsmirigyeire.
Más esetekben autoantitestek jelenhetnek meg a szervezetben, blokkolva a receptor és a TSH kölcsönhatását, ami atrófiás pajzsmirigygyulladást, hypothyreosisot és myxedemát okozhat.
A TSH-receptor szintézisét befolyásoló gének mutációi TSH-rezisztencia kialakulásához vezethetnek. A TSH-val szembeni teljes rezisztencia esetén a pajzsmirigy gynoplasztikus, nem képes elegendő mennyiségű pajzsmirigyhormont szintetizálni és kiválasztani.
A hypothalamus-hyophysealis-pajzsmirigy rendszer kapcsolatától függően, amely változás a pajzsmirigy működésében rendellenességek kialakulásához vezetett, szokás megkülönböztetni: primer hypo- vagy hyperthyreosis, amikor a rendellenesség közvetlenül kapcsolódik a pajzsmirigy működéséhez. a pajzsmirigy; másodlagos, amikor a rendellenességet az agyalapi mirigy változásai okozzák; harmadlagos - a hipotalamuszban.
Lutropin
A gonadotropinok fő funkciói a női testbenGonadotropinok - tüszőstimuláló hormon(FSH), ill follitropinÉs luteinizáló hormon(LH), vagy lutropin, - glikoproteinek, amelyek az adenohipofízis különböző vagy azonos bazofil sejtjeiben (gonadotrófokban) képződnek, szabályozzák az ivarmirigyek endokrin funkcióinak fejlődését férfiakban és nőkben, a 7-TMS receptorok stimulálásával és a cAMP szintjének növelésével hatnak a célsejtekre. őket. Terhesség alatt FSH és LH termelődhet a placentában.
A menstruációs ciklus első napjaiban emelkedő FSH-szint hatására az elsődleges tüsző érik, és megnő az ösztradiol koncentrációja a vérben. A ciklus közepén kialakuló csúcs LH szint hatása a tüszőrepedés és a sárgatestté való átalakulás közvetlen oka. Az LH csúcskoncentrációjától az ovulációig tartó látens időszak 24-36 óra Az LH a legfontosabb hormon, amely serkenti a progeszteron és az ösztrogének képződését a petefészekben.
A gonadotropinok fő funkciói a férfi testbenAz FSH elősegíti a herék növekedését, serkenti az Ssrtoli sejteket és elősegíti az androgénkötő fehérje képződését, valamint serkenti ezen sejtek inhibin polipeptid termelését, ami csökkenti az FSH és a GnRH szekrécióját. Az LH serkenti a Leydig-sejtek érését és differenciálódását, valamint a tesztoszteron szintézisét és szekrécióját ezekben a sejtekben. Az FSH, LH és tesztoszteron együttes hatása szükséges a spermatogenezishez.
Asztal. A gonadotropinok fő hatásai

Az FSH és LH szekrécióját a hipotalamusz gonadotropin-releasing hormonja (GHR), más néven GnRH és LH szabályozza, amely serkenti azok vérbe jutását, elsősorban az FSH-t. A nők vérének ösztrogéntartalmának növekedése a menstruációs ciklus bizonyos napjain serkenti az LH képződését a hipotalamuszban (pozitív visszajelzés). Az ösztrogének, a progesztinek és az inhibin hormon gátolják a GnRH, FSH és LH felszabadulását. A prolaktin gátolja az FSH és LH képződését.
A gonadotropinok kiválasztását férfiakban a GnrH (aktiválás), a szabad tesztoszteron (gátlás) és az inhibin (gátlás) szabályozza. Férfiaknál a GnRH szekréció folyamatosan megy végbe, ellentétben a nőkkel, akiknél ciklikusan történik.
Gyermekeknél a gonadotropinok felszabadulását a tobozmirigy melatonin hormonja gátolja. Ugyanakkor a gyermekeknél az FSH és LH csökkent szintjét az elsődleges és másodlagos szexuális jellemzők késői vagy elégtelen fejlődése, a csontok növekedési lemezeinek késői záródása (ösztrogén vagy tesztoszteron hiánya), valamint kórosan magas növekedés vagy gigantizmus kíséri. Nőknél az FSH és LH hiánya a menstruációs ciklus megszakadásával vagy leállásával jár. Szoptatós anyáknál ezek a ciklusváltozások a magas prolaktinszint miatt meglehetősen szembetűnőek lehetnek.
Az FSH és LH túlzott szekrécióját gyermekeknél korai pubertás, a növekedési lemezek záródása és a hypergonadalis alacsony termet kíséri.
Kortikotropin
Adrenokortikotrop hormon(ACTH, vagy kortikotropin) egy 39 aminosavból álló peptid, amelyet az adenohipofízis kortikotrófjai szintetizálnak, a célsejtekre hat, stimulálja a 7-TMS receptorokat és növeli a cAMP szintjét, a hormon felezési ideje legfeljebb 10 perc.
Az ACTH fő hatásai mellékvesére és extradrenálisra osztva. Az ACTH serkenti a mellékvesekéreg zona fasciculata és reticularis növekedését és fejlődését, valamint a glükokortikoidok (a zona fasciculata sejtjei által a kortizol és kortikoszteron, valamint kisebb mértékben a nemi hormonok (főleg androgének) szintézisét és felszabadulását) Az ACTH gyengén serkenti a mineralokortikoid aldoszteron felszabadulását a zona glomerulosa mellékvesekéreg sejtjei által.
Asztal. A kortikotropin fő hatásai
Az ACTH mellékvesén kívüli hatása a hormon más szervek sejtjeire gyakorolt hatása. Az ACTH lipolitikus hatást fejt ki a zsírsejtekben, és segít növelni a szabad zsírsavak szintjét a vérben; serkenti az inzulin kiválasztását a hasnyálmirigy béta-sejtjei által, és elősegíti a hipoglikémia kialakulását; serkenti a növekedési hormon szekrécióját az adenohypophysis szomatrófjai által; fokozza a bőr pigmentációját, mint az MSH, amelyhez hasonló szerkezetű.
Az ACTH szekréció szabályozását három fő mechanizmus végzi. A bazális ACTH szekréciót a hypothalamus általi kortikoliberin felszabadulás endogén ritmusa szabályozza (maximum reggel 6-8 óra, minimum szint 22-2 óra). A fokozott szekréciót a szervezetet megterhelő hatások (érzelmek, hideg, fájdalom, fizikai aktivitás stb.) során keletkező nagyobb mennyiségű kortikoliberin hatására érik el. Az ACTH szintjét egy negatív visszacsatolási mechanizmus is szabályozza: csökken, ha a kortizol glükokortikoid hormon szintje a vérben emelkedik, és nő, ha a vér kortizol szintje csökken. A kortizolszint növekedése a kortikoszteroid hormonok hipotalamusz általi szekréciójának gátlásával is együtt jár, ami szintén az ACTH képződésének csökkenéséhez vezet az agyalapi mirigyben.

Rizs. A kortikotropin szekréció szabályozása
Az ACTH túlzott szekréciója a terhesség alatt, valamint az adenohypophysis kortikotrófjainak elsődleges vagy másodlagos (a mellékvesék eltávolítása után) túlműködése során fordul elő. Megnyilvánulásai változatosak, és mind magának az ACTH-nak a hatásaihoz, mind pedig a mellékvesekéreg és más hormonok hormontermelésére kifejtett stimuláló hatásához kapcsolódnak. Az ACTH serkenti a növekedési hormon szekrécióját, melynek szintje fontos a szervezet normális növekedéséhez és fejlődéséhez. A megnövekedett ACTH-szint, különösen gyermekkorban, a növekedési hormon túlzott termeléséből adódó tünetekkel járhat (lásd fent). Az ACTH túlzott szintjével gyermekeknél, a mellékvesék általi nemi hormonok kiválasztásának serkentése miatt, korai pubertás, a férfi és női nemi hormonok egyensúlyának felborulása és a nőknél a férfiasodás jeleinek kialakulása figyelhető meg.
Magas koncentrációban a vérben az ACTH serkenti a lipolízist, a fehérjekatabolizmust és a bőr túlzott pigmentációjának kialakulását.
Az ACTH hiánya a szervezetben a piokokortikoidok elégtelen szekréciójához vezet a mellékvesekéreg sejtjeiben, ami anyagcserezavarokkal és a szervezet környezeti tényezők káros hatásaival szembeni ellenállásának csökkenésével jár.
Az ACTH egy prekurzorból (proopiomelanocortin) képződik, amelyből a- és β-MSH, valamint β- és γ-lipotropinok és endogén morfinszerű peptidek – endorfinok és enkefalinok – is szintetizálódnak. A lipotropinek aktiválják a lipolízist, az endorfinok és az enkefalinok pedig az agy antinociceptív (fájdalom) rendszerének fontos összetevői.