गर्भाशय ग्रीवा का घातक रसौली, अनिर्दिष्ट भाग। सर्वाइकल कैंसर - विवरण, उपचार। कोरिया, इजराइल, जर्मनी, अमेरिका में इलाज कराएं
रोग को अधिक सरलता से परिभाषित करने के लिए, रोगों के अंतर्राष्ट्रीय वर्गीकरण का आविष्कार किया गया, जिसमें ऑन्कोलॉजिकल रोग भी शामिल हैं। गर्भाशय कैंसर के लिए ICD 10 कोड निर्दिष्ट है सी54.
परिष्कृत स्थानीयकरण
- C54.0 - निचला खंड या इस्थमस।
- सी54.1 - एंडोमेट्रियल कैंसर।
- सी54.2 - मायोमेट्रियम।
- सी54.3 - गर्भाशय का कोष।
- सी54.8 - गर्भाशय का शरीर उपरोक्त क्षेत्रों से आगे तक फैला हुआ है।
- सी54.9 - अपरिष्कृत क्षेत्र
महिला जननांग अंगों का ट्यूमर
इस समूह में सभी घातक नवोप्लाज्म शामिल हैं जो महिला प्रजनन प्रणाली में स्थित हैं।
- C51 - वल्वा।
- C52 - योनि।
- C53 - गर्भाशय ग्रीवा।
- सी54 - शरीर।
- सी55 - गर्भाशय का अपरिष्कृत क्षेत्र।
- C56 - अंडाशय.
- सी57 - स्त्री रोग विज्ञान की महिला प्रजनन प्रणाली का अपरिष्कृत स्थानीयकरण।
- C58 - प्लेसेंटा.
बदले में, यह समूह उच्च शिक्षा प्रणाली C00 - D48 में शामिल है।
कैंसर विज्ञान
शरीर या गर्भाशय ग्रीवा का कैंसर - अंग के श्लेष्म झिल्ली की उपकला कोशिकाओं के उत्परिवर्तन के परिणामस्वरूप होता है, जो अनियंत्रित विभाजन के साथ एक नई वृद्धि का कारण बनता है जो बढ़ता है और आस-पास की कोशिकाओं और ऊतकों को नष्ट कर देता है।
कारण एवं कारक
रजोनिवृत्ति की शुरुआत के बाद वृद्ध महिलाओं में गर्भाशय कैंसर अधिक आम है। लेकिन युवा लड़कियों में कम उम्र में भी विशेष मामले होते हैं।
- आनुवंशिक प्रवृतियां।
- यौन क्रियाकलाप से इंकार.
- बांझपन.
- जिन महिलाओं ने 25 साल के बाद कभी बच्चे को जन्म नहीं दिया हो।
- मोटापा और ख़राब पोषण.
- धूम्रपान का दुरुपयोग, शराब।
- मधुमेह।
- हार्मोनल गर्भ निरोधकों और दवाओं का गलत उपयोग।
महिला शरीर में किसी भी हार्मोनल असंतुलन के साथ, हार्मोन-निर्भर कार्सिनोमा के विकास के लिए जमीन तैयार हो जाती है।
संकेत, लक्षण, असामान्यताएं
- बार-बार बुखार आना, बिना किसी अन्य लक्षण के।
- पेट में तेज दर्द.
- बाद में, दर्द काठ के क्षेत्र तक फैलना शुरू हो जाएगा।
- एक अप्रिय गंध के साथ खूनी या यहां तक कि शुद्ध योनि स्राव। इस मामले में, रक्त मासिक धर्म चक्र के बाहर बह सकता है।
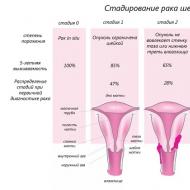
चरणों

- स्टेज 1 - प्रारंभिक चरण में, नियोप्लाज्म एंडोमेट्रियल ज़ोन में स्थित होता है और अस्तर को पार नहीं करता है।
- स्टेज 2 - ट्यूमर सर्वाइकल कैनाल और इंट्रासर्विकल ग्रंथियों को प्रभावित कर सकता है।
- चरण 3 - स्थानीय लिम्फ नोड्स, योनि और पेट की गुहा को क्षति और मेटास्टेसिस।
- चरण 4 - मेटास्टेस रक्त के माध्यम से दूर के अंगों तक प्रवेश करते हैं।
निदान
- स्त्री रोग विशेषज्ञ द्वारा दृश्य परीक्षण।
- संदिग्ध संरचनाओं की बायोप्सी।
- उदर गुहा का अल्ट्रासाउंड.
- अधिक विस्तृत जांच के लिए एमआरआई।
- ट्यूमर के विकास की गतिशीलता और उपचार की गुणवत्ता को ट्रैक करने के लिए ट्यूमर मार्करों के परीक्षण।
आरसीएचआर (कजाकिस्तान गणराज्य के स्वास्थ्य मंत्रालय के स्वास्थ्य विकास के लिए रिपब्लिकन सेंटर)
संस्करण: पुरालेख - कजाकिस्तान गणराज्य के स्वास्थ्य मंत्रालय के नैदानिक प्रोटोकॉल - 2012 (आदेश संख्या 883, संख्या 165)
गर्भाशय ग्रीवा, अनिर्दिष्ट भाग (C53.9)
सामान्य जानकारी
संक्षिप्त वर्णन
क्लिनिकल प्रोटोकॉल "सर्वाइकल कैंसर"
वर्तमान में, दुनिया के विकसित देशों में सर्वाइकल कैंसर (सीसी) की रोकथाम, शीघ्र निदान और उपचार में महत्वपूर्ण प्रगति हुई है। यह मुख्य रूप से इस तथ्य के कारण है कि, अन्य ऑन्कोलॉजिकल रोगों के विपरीत, गर्भाशय ग्रीवा के कैंसर की घटनाओं को अच्छी तरह से नियंत्रित किया जाता है, क्योंकि इस बीमारी में एक स्पष्ट एटियलजि, एक स्पष्ट और अक्सर लंबे समय तक कैंसरग्रस्त चरण और स्थानीय प्रसार की स्पष्ट प्रवृत्ति होती है।
इस प्रकार, ऑस्ट्रेलिया में, 1994 में एक स्क्रीनिंग कार्यक्रम की शुरुआत के साथ, घटनाओं को लगभग 2 गुना कम करना संभव हो गया - 13.2 से 6.9 प्रति 100 हजार महिला जनसंख्या, जबकि ऑस्ट्रेलियाई स्वास्थ्य संस्थान के अनुसार, गर्भाशय ग्रीवा के कैंसर से मृत्यु दर 4.0 से घटकर 1.9 (1) हो गया।
इस प्रकार, यदि विकसित देशों ने सीसी से रुग्णता और मृत्यु दर को नियंत्रित करना सीख लिया है, तो दुनिया का अधिकांश हिस्सा अभी भी इस राह पर है। और डब्ल्यूएचओ के आंकड़े इसकी पुष्टि करते हैं: उदाहरण के लिए, 2005 में, बीमारी के 500,000 हजार से अधिक नए मामले दर्ज किए गए थे और उनमें से 90% विकासशील अर्थव्यवस्था वाले देशों के थे।
इसके अलावा 2005 में, 260,000 महिलाओं की इस बीमारी से मृत्यु हो गई, जिनमें से लगभग 95% विकासशील देशों में थीं, अधिकांश अपुष्ट निदान और पर्याप्त उपचार तक पहुंच की कमी के कारण, जो उनके जीवन को लम्बा खींच सकता था।
कजाकिस्तान गणराज्य में, 2007 के अंत में, 9269 महिलाएं ऑन्कोलॉजिस्ट की देखरेख में थीं, 1233 नए मामले दर्ज किए गए और इस बीमारी से 631 मौतें दर्ज की गईं (अर्ज़ीकुलोव जेएच.ए. एट अल., 2008)।
विकसित देशों के अनुभव के आधार पर सर्वाइकल कैंसर की स्थिति में सुधार के लिए एक कार्यक्रम की आधुनिक अवधारणा तीन मुख्य सिद्धांतों पर आधारित है:
1. प्राथमिक रोकथाम (संभावित जोखिम कारकों के बहिष्कार के साथ स्वस्थ जीवनशैली, आबादी के कुछ समूहों का टीकाकरण)।
2. माध्यमिक रोकथाम (महिला आबादी की उच्च गुणवत्ता और सुव्यवस्थित जांच)।
3. आक्रामक सर्वाइकल कैंसर के सभी आधुनिक निदान और उपचार के लिए एक समान प्रोटोकॉल का परिचय।
केवल ऐसा एकीकृत दृष्टिकोण ही हमें अपने देश में सर्वाइकल कैंसर की घटनाओं और मृत्यु दर को विश्वसनीय रूप से कम करने की अनुमति देगा।
प्रोटोकॉल कोड:РH-O-002 "सर्वाइकल कैंसर"
आईसीडी कोड:सी 53
1. गर्भाशय ग्रीवा के घातक नवोप्लाज्म (सी 53)।
2. आंतरिक भाग (सी 53.0)।
3. बाहरी भाग (सी 53.1)।
4. गर्भाशय ग्रीवा को उपरोक्त स्थानीयकरणों में से एक या अधिक से अधिक क्षति (सी 53.8)।
5. गर्भाशय की ग्रीवा, अनिर्दिष्ट भाग (सी 53.9)।
प्रोटोकॉल में प्रयुक्त संक्षिप्ताक्षर:
1. FIGO - इंटरनेशनल फेडरेशन ऑफ गायनोकोलॉजी एंड ऑब्स्टेट्रिक्स।
2. WHO - विश्व स्वास्थ्य संगठन।
3. सीसी - सर्वाइकल कैंसर।
4. सीआईएन - सर्वाइकल इंट्रापीथेलियल नियोप्लासिया।
प्रोटोकॉल के विकास की तिथि: 2011
प्रोटोकॉल उपयोगकर्ता:सर्वाइकल कैंसर के रोगियों के निदान, उपचार और पुनर्वास में शामिल डॉक्टर।
हितों के टकराव का खुलासा नहीं:डेवलपर्स का इस दस्तावेज़ के विषय में कोई वित्तीय हित नहीं है, और इस दस्तावेज़ में निर्दिष्ट दवाओं, उपकरणों आदि की बिक्री, उत्पादन या वितरण से भी उनका कोई संबंध नहीं है।
वर्गीकरण
सर्वाइकल कैंसर का चरण
सर्वाइकल कैंसर के चरण को निर्धारित करने के लिए, दुनिया भर में इंटरनेशनल फेडरेशन ऑफ गायनेकोलॉजिस्ट्स एंड ऑब्स्टेट्रिशियन्स के नैदानिक वर्गीकरण का उपयोग किया जाता है (तालिका 1); सर्जिकल स्टेजिंग से गुजरने वाले मामलों को भी टीएनएम (7वां संस्करण, 2009) के अनुसार वर्गीकृत किया गया है।
सर्वाइकल कैंसर के स्टेजिंग के नियम
सर्वाइकल कैंसर का स्टेजिंग पूरी तरह से नैदानिक मूल्यांकन पर आधारित है, इसलिए सभी मामलों में, कुछ मामलों में एनेस्थीसिया के तहत, एक संपूर्ण नैदानिक परीक्षा आवश्यक है। यह याद रखना चाहिए कि नैदानिक चरण बाद के नैदानिक निष्कर्षों के आधार पर नहीं बदलता है। जब मंच के चुनाव के बारे में संदेह हो तो छोटे मंच को प्राथमिकता दी जाती है।
स्टेजिंग के लिए निम्नलिखित परीक्षा विधियों का उपयोग किया जाता है:
1. FIGO स्टेजिंग विशेष रूप से नैदानिक डेटा (परीक्षा और कोल्पोस्कोपी), छाती रेडियोग्राफी, अंतःशिरा यूरोग्राफी, बायोप्सी और गर्भाशय ग्रीवा नहर और गर्भाशय गुहा के इलाज के उपयोग पर आधारित है।
2. यदि अंकुरण का संदेह हो तो क्लिनिकल स्टेजिंग के लिए सिस्टोस्कोपी और रेक्टोस्कोपी का उपयोग किया जा सकता है: रूपात्मक पुष्टि की आवश्यकता है!
3. क्लिनिकल स्टेजिंग के लिए लिम्फोग्राफी, सीटी, एमआरआई, पीईटी, लैप्रोस्कोपी का उपयोग नहीं किया जा सकता है।
4. यदि अंतःशिरा यूरोग्राफी पर पैथोलॉजिकल परिवर्तन पाए जाते हैं, तो मामले को चरण IIIB के रूप में वर्गीकृत किया जाना चाहिए।
5. गर्भाशय ग्रीवा के लिए क्षेत्रीय लिम्फ नोड्स पैरासर्विकल, पैरामीट्रिक, हाइपोगैस्ट्रिक, ऑबट्यूरेटर, आंतरिक, बाहरी और सामान्य इलियाक, प्रीसेक्रल, सेक्रल हैं।
6. लैप्रोस्कोपी, अल्ट्रासाउंड, सीटी, एमआरआई, पीईटी जैसी अतिरिक्त जांच विधियों के दौरान खोजे गए निष्कर्ष उपचार पद्धति चुनने के लिए मूल्यवान हैं, लेकिन इस तथ्य के कारण कि वे हर जगह नहीं किए जाते हैं और उनकी व्याख्या डॉक्टर की योग्यता पर निर्भर करती है, उनका उपयोग क्लिनिकल स्टेजिंग के लिए नहीं किया जाता है और उनका डेटा रोग के चरण को नहीं बदलता है।
तालिका 1. सर्वाइकल कैंसर - FIGO (2009) और TNM स्टेजिंग (7वां संस्करण, 2009)
| FIGO चरण | टीएनएम द्वारा श्रेणी | |
| प्राथमिक ट्यूमर का निर्धारण नहीं किया जा सकता | टेक्सास | |
| प्राथमिक ट्यूमर की कोई अभिव्यक्ति नहीं | टी0 | |
| प्रीइनवेसिव कैंसर (कार्सिनोमा इन सीटू) | टीआई | |
| मैं | ट्यूमर गर्भाशय तक सीमित है (गर्भाशय के शरीर तक फैलने पर ध्यान नहीं दिया जाता है) | टी1 |
| मैं एक | आक्रामक कैंसर का निदान केवल सूक्ष्मदर्शी रूप से किया जाता है (सभी मैक्रोस्कोपिक रूप से दिखाई देने वाले घाव, यहां तक कि सतही आक्रमण के साथ, चरण 1बी हैं) | टी1ए |
| मैं ए1 | स्ट्रोमल आक्रमण की गहराई 3 मिमी से अधिक नहीं और क्षैतिज फैलाव 7 मिमी से अधिक नहीं* | T1a1 |
| मैं ए2 | स्ट्रोमल आक्रमण की गहराई 5 मिमी से अधिक नहीं और क्षैतिज विस्तार 7 मिमी से अधिक नहीं | T1a2 |
| आईबी | चिकित्सकीय दृष्टि से दिखाई देने वाले ग्रीवा घाव या 1A2/T1A2 से बड़े सूक्ष्म घाव | टी1बी |
| मैं बी1 | चिकित्सकीय रूप से दिखाई देने वाले घाव अधिकतम आयाम में 4 सेमी से अधिक नहीं | टी1बी1 |
| मैं बी2 | अधिकतम आयाम में 4 सेमी से अधिक बड़े चिकित्सकीय रूप से दिखाई देने वाले घाव | टी1बी2 |
| द्वितीय | ट्यूमर श्रोणि की दीवारों और योनि के निचले तीसरे हिस्से को शामिल किए बिना गर्भाशय के शरीर तक सीमित है | टी2 |
| द्वितीय ए | पैरामीट्रियम को शामिल किए बिना | टी2ए |
| द्वितीय ए1 | अधिकतम आयाम में 4 सेमी से कम का ट्यूमर | T2a1 |
| द्वितीय ए2 | अधिकतम आयाम में 4 सेमी से अधिक का ट्यूमर | T2a2 |
| द्वितीय बी | पैरामीट्रियम को शामिल करना | टी2बी |
| तृतीय |
पेल्विक हड्डियों और/या योनि के निचले तीसरे भाग तक पहुंचने वाला ट्यूमर और/या हाइड्रोनफ्रोसिस या गैर-कार्यशील किडनी की उपस्थिति |
टी3 |
| तृतीय ए | पैल्विक दीवारों की भागीदारी के बिना योनि के निचले तीसरे भाग का शामिल होना | टी3ए |
| तृतीय बी | पैल्विक हड्डियों का विस्तार और/या हाइड्रोनफ्रोसिस और/या साइलेंट किडनी की उपस्थिति | टी3बी |
| चतुर्थ ए | श्रोणि से आगे बढ़े बिना मूत्राशय और/या मलाशय की श्लेष्मा झिल्ली पर आक्रमण* | टी4ए |
| चतुर्थ बी | दूर के मेटास्टेस | टी4बी |
|
2006 में FIGO ने स्टेजिंग में बदलाव का प्रस्ताव रखा, जिसमें स्टेज IIA को स्टेज IB के सिद्धांत के अनुसार विभाजित करना शामिल था, जो 1 जनवरी 2010 को लागू हुआ। नए संस्करण में स्टेज 0 को FIGO वर्गीकरण से बाहर रखा गया है। पीएन0 सेट करने के लिए, कम से कम 6 लिम्फ नोड्स की जांच आवश्यक है; मेटास्टेस और कम लिम्फ नोड्स की अनुपस्थिति में, एन0 भी सेट किया जाता है। |
||
पैथोलॉजिकल (सर्जिकल) टीएनएम स्टेजिंग (तालिका 1)
सर्जरी के दौरान हटाए गए ऊतकों की संपूर्ण रूपात्मक जांच से प्राप्त डेटा का उपयोग प्रक्रिया की सीमा का सबसे सटीक आकलन करने के लिए किया जाना चाहिए। ये निष्कर्ष क्लिनिकल स्टेजिंग में बदलाव की अनुमति नहीं देते हैं, लेकिन पैथोलॉजिकल स्टेजिंग प्रोटोकॉल में इसका उपयोग और प्रतिबिंबित किया जाना चाहिए। इन उद्देश्यों के लिए, टीएनएम नामकरण का उपयोग किया जाता है।
कभी-कभी गर्भाशय ग्रीवा का कैंसर अन्य संकेतों के लिए हिस्टेरेक्टॉमी के बाद एक आकस्मिक खोज हो सकता है - ऐसे मामलों में, नैदानिक स्टेजिंग नहीं की जा सकती है और इन मामलों को चिकित्सीय आंकड़ों में शामिल नहीं किया जाता है, लेकिन यह सलाह दी जाती है कि उन्हें अलग से रिपोर्ट किया जाए। पुनरावर्तन होने पर प्रारंभिक रूप से स्थापित चरण नहीं बदलता है।
क्लीनिकों और विभिन्न उपचार विधियों के बीच उपचार परिणामों की तुलना केवल तभी संभव है जब सभी स्टेजिंग नियमों का सावधानीपूर्वक पालन किया जाए।
मंचन की विशेषताएं
चरणों IAl और IA2 का निदान पूरी तरह से हटाए गए ऊतक (बायोप्सी सामग्री - अधिमानतः एक ग्रीवा शंकु, जो पूरे प्रभावित क्षेत्र को कवर करना चाहिए) की सूक्ष्म जांच पर आधारित है। आक्रमण की गहराई बेसमेंट झिल्ली से या ग्रंथि की सतह से जहां से द्रव्यमान उत्पन्न होता है, 5 मिमी से अधिक नहीं होनी चाहिए।
क्षैतिज फैलाव 7 मिमी से अधिक नहीं होना चाहिए। संवहनी और/या लसीका आक्रमण की उपस्थिति रोग के चरण को नहीं बढ़ाती है, लेकिन निदान में प्रतिबिंबित होनी चाहिए, क्योंकि यह भविष्य में उपचार की पसंद को प्रभावित कर सकती है।
आंखों को दिखाई देने वाले बड़े घावों को आईबी के रूप में दर्शाया जाता है। एक नियम के रूप में, आंख से यह आकलन करना असंभव है कि गर्भाशय के शरीर में विस्तार है या नहीं। इसलिए, गर्भाशय के शरीर में चिकित्सकीय रूप से संदिग्ध विस्तार को ध्यान में नहीं रखा जाना चाहिए।
पेल्विक दीवार की ओर ट्यूमर के विस्तार वाले मरीजों, जिसे एक छोटे, प्रेरित क्षेत्र के रूप में परिभाषित किया गया है, को आईआईबी के रूप में चरणबद्ध किया जाना चाहिए। क्लिनिकल स्टेजिंग के दौरान, यह विश्वसनीय रूप से आकलन करना असंभव है कि क्या योनि वॉल्ट का छोटा होना और पैरामीट्रियम में सघन घुसपैठ वास्तव में प्रकृति में ट्यूमर या सूजन है।
तीसरा चरणयह तब सेट किया जाता है जब पेल्विक हड्डियों में घुसपैठ होती है, या सीधे ट्यूमर का विकास पेल्विक हड्डियों तक पहुंचता है। हाइड्रोनफ्रोसिस या गैर-कार्यशील किडनी की उपस्थिति ट्यूमर द्वारा मूत्रवाहिनी स्टेनोसिस का परिणाम है और ऐसे मामलों में चरण III निर्दिष्ट किया जाता है, भले ही, अन्य शोध विधियों के अनुसार, ट्यूमर को चरण I या II के रूप में वर्गीकृत किया जा सकता है।
बुलस एडिमा की उपस्थिति रोग को चरण IV के रूप में वर्गीकृत करने का आधार नहीं देती है। मूत्राशय के लुमेन में उभरी हुई लकीरें और खांचे के रूप में संरचनाएं अक्सर ट्यूमर के विकास में मूत्राशय की सबम्यूकोसल परत की भागीदारी का परिणाम होती हैं।
मूत्राशय की सफाई में ट्यूमर कोशिकाओं की उपस्थिति के लिए मामले को चरण IVA के रूप में वर्गीकृत करने के लिए अतिरिक्त रूपात्मक परीक्षा की आवश्यकता होती है।
विदेश में इलाज
कोरिया, इजराइल, जर्मनी, अमेरिका में इलाज कराएं
चिकित्सा पर्यटन पर सलाह लें
इलाज
सर्वाइकल कैंसर का इलाज
सूक्ष्म आक्रामक कैंसर
स्टेज IA1 या IA2 सर्वाइकल कैंसर का निदान पूरी तरह से नकारात्मक रिसेक्शन मार्जिन के साथ सर्वाइकल शंकु की रूपात्मक परीक्षा के आधार पर या ट्रेचेलेक्टॉमी या हिस्टेरेक्टॉमी के बाद हटाए गए नमूने के आधार पर किया जाता है। यदि ग्रीवा संकरण के बाद रिसेक्शन मार्जिन पर सीआईएन III या आक्रामक कैंसर का पता चलता है, तो चरण आईबी 1 रोग के लिए रोगी का पुन: संकरण या उपचार आवश्यक है (2)। उपचार विधि चुनने से पहले सहवर्ती योनि इंट्रापीथेलियल नियोप्लासिया (VAIN) को बाहर करने के लिए वैजिनोस्कोपी (कोल्पोस्कोप!) किया जाता है।
स्टेज IA1
इस स्तर पर सर्वाइकल कैंसर के लिए मुख्य उपचार विधि संपूर्ण पेट या योनि हिस्टेरेक्टॉमी है। योनि इंट्रापीथेलियल नियोप्लासिया की उपस्थिति में, योनि ट्यूब के संबंधित भाग को हटाना आवश्यक है (3)। यदि प्रजनन क्षमता को संरक्षित करना आवश्यक है, तो पैप परीक्षण के अधीन, नकारात्मक स्नेह मार्जिन के साथ गर्भाशय ग्रीवा के व्यापक शंकुकरण के बाद अवलोकन संभव है। यदि पिछले दो परीक्षण नकारात्मक थे तो पैप परीक्षण 6, 12 महीनों में और उसके बाद वार्षिक रूप से किया जाता है। साक्ष्य का स्तर बी.
स्टेज IA2
चरण IA2 रोग वाले रोगियों में लसीका मेटास्टेसिस की एक निश्चित संभावना होती है, और इसलिए सर्जिकल उपचार (4,5) के दौरान पेल्विक लिम्फैडेनेक्टॉमी करना आवश्यक है। इन नैदानिक मामलों के लिए एक पर्याप्त ऑपरेशन द्विपक्षीय पेल्विक लिम्फैडेनेक्टॉमी द्वारा पूरक एक संशोधित रेडिकल हिस्टेरेक्टॉमी (टाइप 2 ऑपरेशन) है। प्रारंभिक बायोप्सी के अनुसार लिम्फोवास्कुलर आक्रमण की अनुपस्थिति में, पेल्विक लिम्फैडेनेक्टॉमी के साथ एक्स्ट्राफेशियल एक्सटिरपेशन (टाइप 1 सर्जरी) करना संभव है। साक्ष्य का स्तर सी.
यदि प्रजनन संरक्षण वांछित है, तो उपचार के विकल्पों में शामिल हैं:
गर्भाशय ग्रीवा का व्यापक संकरण, पेल्विक लिम्फ नोड्स के एक्स्ट्रापेरिटोनियल या लेप्रोस्कोपिक निष्कासन द्वारा पूरक;
रेडिकल ट्रेचेलेक्टॉमी, पेल्विक लिम्फ नोड्स के एक्स्ट्रापेरिटोनियल, ट्रांसपेरिटोनियल या लेप्रोस्कोपिक निष्कासन द्वारा पूरक (6)।
रोगियों के इस समूह की निगरानी मुख्य रूप से 6 और 12 महीनों में दो नकारात्मक परीक्षणों के बाद वार्षिक पैप परीक्षण पर आधारित है।
आक्रामक गर्भाशय ग्रीवा का कैंसर
गर्भाशय ग्रीवा पर दिखाई देने वाले घावों वाले रोगियों में, रूपात्मक रूप से निदान की पुष्टि करने के लिए बायोप्सी की आवश्यकता होती है (यदि आवश्यक हो तो एनेस्थीसिया के तहत); योनि इंट्रापीथेलियल नियोप्लासिया (VAIN) को बाहर करने के लिए वैजिनोस्कोपी की जाती है। सहवर्ती लक्षणों (मूत्राशय और मलाशय से) की जांच की जानी चाहिए: सिस्टोस्कोपी और रेक्टोस्कोपी आवश्यक हैं। छाती का एक्स-रे और गुर्दे की जांच (अल्ट्रासाउंड, उत्सर्जन यूरोग्राफी, सीटी और एमआरआई) भी आवश्यक है। क्षेत्रीय लिम्फ नोड्स की स्थिति और ट्यूमर के स्थानीय प्रसार का आकलन करने के लिए सीटी और एमआरआई भी किया जाता है। यदि पीईटी उपलब्ध है, तो इसका उपयोग किया जा सकता है।
रोग के चरण IB1, IIA1 (ट्यूमर)।< 4 см)
सर्वाइकल कैंसर के प्रारंभिक चरण (IB1, IIA)।< 4см) имеют хороший прогноз и могут одинаково успешно лечиться как хирургическим, так и лучевым методом (7,8). साक्ष्य का स्तर ए.
उपचार पद्धति का चुनाव उपयुक्त संसाधनों की उपलब्धता पर निर्भर करता है: एक प्रशिक्षित स्त्री रोग विशेषज्ञ ऑन्कोलॉजिस्ट, रोगी की उम्र और सामान्य स्थिति। उपचार योजना विकसित करने और रोगी को विभिन्न चिकित्सीय विकल्पों, उनके दुष्प्रभावों और अपेक्षित उपचार परिणामों के बारे में सूचित करने के लिए एक बहु-विषयक टीम (स्त्री रोग ऑन्कोलॉजिस्ट, रेडियोलॉजिस्ट, कीमोथेरेपी) की क्षमताओं का उपयोग करना बेहतर है।
आमतौर पर, सर्जिकल और विकिरण उपचार विधियों के संयोजन से जटिलताओं की संख्या बढ़ जाती है, इसलिए, जब प्रारंभिक चिकित्सा की योजना बनाते हैं, तो सर्जरी और पोस्टऑपरेटिव विकिरण के एक साथ प्रशासन से बचा जाना चाहिए। साक्ष्य का स्तर ए.
शल्य चिकित्सा:स्टेज IB1/IIA1 सर्वाइकल कैंसर के सर्जिकल उपचार के लिए मानक (< 4 см в диаметре) является модифицированная или радикальная абдоминальная гистерэктомия (класс II или III согласно классификации Piver, Rutledge, Smith, 1974 г.) в сочетании с тазовой лимфаденэктомией. У молодых пациенток яичники сохраняются и выводятся из полости малого таза в брюшную полость (транспозиция) для сохранения их функции на случай проведения послеоперационной лучевой терапии. В отдельных случаях возможно выполнение радикальной трахелэктомии с лапароскопической тазовой лимфаденэктомией (9,10). साक्ष्य का स्तर सी.
विकिरण चिकित्सा:स्टेज IB1/IIA1 सर्वाइकल कैंसर के लिए मानक रेडियोथेरेपी (< 4 см в диаметре) является сочетанная лучевая терапия. Рекомендуемые дозы для дистанционного компонента и брахитерапии источником низкой мощности - 80-85 Грей на точку A и 50-55 Грей на точку B. Суммарная доза дистанционной лучевой терапии (EBRT) должна составлять 45-50 Грей при 1,8-2,0 Грей за фракцию. При использовании источников высокой мощности для брахитерапии (ВТ), дозы определяются согласно биологической эквивалентности.
सर्जरी के बाद सहायक उपचार:लिम्फ नोड्स में मेटास्टेसिस, पॉजिटिव रिसेक्शन मार्जिन और पैरामेट्रिया (पैरासर्विकल टिश्यू) में ट्यूमर तत्वों की उपस्थिति में कट्टरपंथी सर्जिकल उपचार के बाद पुनरावृत्ति का जोखिम अधिक होता है। सहायक प्रतिस्पर्धी केमोराडियोथेरेपी (5FU + सिस्प्लैटिन या सिस्प्लैटिन का उपयोग करके) इस श्रेणी के रोगियों (11) में सहवर्ती विकिरण चिकित्सा की तुलना में उपचार के परिणामों में सुधार करता है। साक्ष्य का स्तर ए.
गैर-शामिल लिम्फ नोड्स, बड़े ट्यूमर आकार, लिम्फोवास्कुलर स्पेस की भागीदारी और गर्भाशय ग्रीवा स्ट्रोमा के 1/3 से अधिक आक्रमण वाले मरीजों में पुनरावृत्ति का खतरा बढ़ जाता है। रोगियों के इस समूह में, पेल्विक विकिरण पुनरावृत्ति के जोखिम को कम करता है और उन रोगियों की तुलना में रोग-मुक्त अस्तित्व को बढ़ाता है, जिन्हें सर्जरी के बाद सहायक उपचार नहीं मिला था। इसके अलावा, सर्वाइकल एडेनोकार्सिनोमा और सर्वाइकल ग्लैंडुलर स्क्वैमस सेल कार्सिनोमा (12) वाले रोगियों में पोस्टऑपरेटिव विकिरण चिकित्सा को प्राथमिकता दी जाती है। साक्ष्य का स्तर ए.
जांचकर्ताओं के दो सहयोगी समूहों ने योनि स्टंप और पैरामीट्रियल ऊतकों (13,14) को लक्षित करने वाली पोस्टऑपरेटिव लघु-क्षेत्र रेडियोथेरेपी से स्वीकार्य परिणामों की सूचना दी। इस मामले में विकिरण की ऊपरी सीमा स्तर S1-2 है, न कि पारंपरिक क्षेत्रों की तरह L5-S1। साक्ष्य का स्तर सी.
मौलिक रूप से, चरण 1 सीसी के लिए सहायक विकिरण/केमोरेडियोथेरेपी निर्धारित करने का मुद्दा जीओजी स्कोरिंग स्केल के आधार पर तय किया जाता है, जो एक बड़े रोगविज्ञान और शल्य चिकित्सा अध्ययन (तालिका 2) के आधार पर विकसित किया गया है।
तालिका 2. रैडिकल हिस्टेरेक्टॉमी के बाद चरण 1 सर्वाइकल कैंसर में दोबारा होने का सापेक्ष जोखिम
| संकेत | अर्थ | सापेक्ष जोखिम |
| स्ट्रोमा में आक्रमण की गहराई, मिमी | ||
| सतही | 3 | 1.0 |
| 4 | 3.0 | |
| 5 | 7.2 | |
| 6 | 14 | |
| 7 | 21 | |
| 8 | 26 | |
| 10 | 31 | |
| औसत | 5 | 20 |
| 6 | 22 | |
| 7 | 23 | |
| 8 | 25 | |
| 10 | 28 | |
| 12 | 32 | |
| 14 | 36 | |
| गहरा | 7 | 28 |
| 8 | 30 | |
| 10 | 34 | |
| 12 | 37 | |
| 14 | 41 | |
| 16 | 45 | |
| 18 | 49 | |
| 20 | 54 | |
| क्लिनिकल ट्यूमर का आकार | दिखाई नहीं देना | 1.0 |
| 1 | 1.6 | |
| 2 | 1.9 | |
| 3 | 2.4 | |
| 4 | 2.9 | |
| 6 | 4.4 | |
| 8 | 6.6 | |
| लसीकावाहिका आक्रमण | खाओ | 1.0 |
| नहीं | 1.7 | |
|
जीओजी स्कोर की गणना आक्रमण की गहराई, ट्यूमर के आकार और लिम्फोवास्कुलर आक्रमण के सापेक्ष जोखिम स्कोर को गुणा करके की जाती है |
||
स्टेज IB2, IIA2 (ट्यूमर > 4 सेमी)
चयन विधियाँ हैं:
1. प्राथमिक प्रतिस्पर्धी रसायन चिकित्सा (15)।
2. पेल्विक लिम्फैडेनेक्टॉमी (टाइप III सर्जरी) के साथ रेडिकल हिस्टेरेक्टॉमी, जिसे आमतौर पर सहायक विकिरण चिकित्सा के साथ पूरक किया जाता है।
प्रतिस्पर्धी रसायन चिकित्सा:सबसे व्यापक रूप से इस्तेमाल किया जाने वाला उपचार साप्ताहिक प्लैटिनम-ड्रग कीमोथेरेपी के साथ संयुक्त समवर्ती रेडियोथेरेपी है।
बिंदु A के लिए विकिरण चिकित्सा की अनुशंसित खुराक 85-90 ग्रे हैं, बिंदु B के लिए 55-60 ग्रे हैं। सिस्प्लैटिन को विकिरण चिकित्सा के बाहरी बीम घटक के साथ साप्ताहिक 40 मिलीग्राम/एम2 की खुराक पर निर्धारित किया जाता है। पैरा-महाधमनी और सामान्य इलियाक लिम्फ नोड्स में मेटास्टेस वाले रोगियों में, विकिरण क्षेत्र को पैरा-महाधमनी क्षेत्रों (17,18) तक विस्तारित करना आवश्यक है। वर्तमान में, विस्तारित विकिरण क्षेत्रों से जुड़ी प्रतिस्पर्धी रसायन विकिरण चिकित्सा की विषाक्तता पर डेटा दुर्लभ है। साक्ष्य का स्तर ए.
संभावित सहायक विकिरण के साथ प्राथमिक शल्य चिकित्सा उपचार
पहले चरण में की गई रेडिकल हिस्टेरेक्टॉमी के कुछ फायदे हैं, जिसमें प्राथमिक ट्यूमर को एक साथ हटाने के साथ-साथ पूरी तरह से सर्जिकल स्टेजिंग की संभावना शामिल है और इस तरह बाद में ब्रैकीथेरेपी (19) की आवश्यकता समाप्त हो जाती है।
इसके अलावा, सर्जरी सभी क्षेत्रीय और किसी भी रोगग्रस्त या बढ़े हुए लिम्फ नोड्स को हटा देती है, जिनके विकिरण के प्रति पर्याप्त रूप से प्रतिक्रिया करने की संभावना बहुत कम होती है (20)। चूँकि ये ट्यूमर स्वाभाविक रूप से बड़े होते हैं, इसलिए इन्हें ऑपरेशन के बाद सहायक विकिरण की आवश्यकता होने की संभावना होती है।
लिम्फोवास्कुलर स्पेस के शामिल होने और सर्वाइकल स्ट्रोमा (21) के 1/3 से अधिक ट्यूमर के आक्रमण के साथ पुनरावृत्ति का खतरा बढ़ जाता है। जिन मरीजों में क्षेत्रीय लिम्फ नोड्स में कोई मेटास्टेसिस नहीं है और पुनरावृत्ति का उच्च जोखिम है, वे पूरे श्रोणि (12) या छोटे-क्षेत्र विकिरण (13,14) के बाहरी विकिरण के अधीन हैं।
क्षेत्रीय लिम्फ नोड मेटास्टेसिस और सामान्य इलियाक और पैरा-महाधमनी लिम्फ नोड मेटास्टेसिस वाले मरीजों को कीमोथेरेपी के साथ या उसके बिना विस्तारित-क्षेत्र बाहरी बीम विकिरण प्राप्त करना चाहिए (17,18)। साक्ष्य का स्तर सी.
नियोएडजुवेंट कीमोथेरेपी के बाद रेडिकल हिस्टेरेक्टॉमी और लिम्फैडेनेक्टॉमी:यादृच्छिक परीक्षण डेटा प्राथमिक विकिरण (16,22) की तुलना में प्रीऑपरेटिव कीमोथेरेपी के साथ बेहतर उपचार परिणामों का सुझाव देता है। रेडिकल हिस्टेरेक्टॉमी और समवर्ती केमोराडियोथेरेपी के बाद नियोएडजुवेंट कीमोथेरेपी के परिणामों की तुलना करने वाला कोई डेटा वर्तमान में नहीं है। साक्ष्य का स्तर बी.
अर्जेंटीना प्रोटोकॉल में प्रयुक्त नियोएडजुवेंट कीमोथेरेपी निम्नलिखित योजना (16) के अनुसार की गई थी:
1. सिस्प्लैटिन 50 मिलीग्राम/एम2 IV - पहले दिन 15 मिनट का आसव।
2. पहले दिन, सिस्प्लैटिन के तुरंत बाद विन्क्रिस्टाइन 1 मिलीग्राम/एम2 IV जलसेक।
3. ब्लेमाइसिन 25 मिलीग्राम/एम2 बाद में 6 घंटे का जलसेक, 1 से 3 दिन तक।
यह व्यवस्था हर 10 दिन में तीन बार दोहराई जाती है।
स्थानीय रूप से उन्नत गर्भाशय ग्रीवा कैंसर (चरण IIB, III और IVA रोग शामिल हैं)
मानक उपचार प्रतिस्पर्धी कीमोथेरेपी (15,23) के साथ संयुक्त रेडियोथेरेपी है। साक्ष्य का स्तर ए.
चरण IV ए में, पहले चरण में पेल्विक एक्सेंट्रेटेशन करना संभव है, विशेष रूप से सिस्टिक या रेक्टल फिस्टुला की उपस्थिति में, जो, हालांकि, एक कट्टरपंथी कार्यक्रम के अनुसार केमोराडियोथेरेपी के लिए एक विरोधाभास नहीं है। साक्ष्य का स्तर सी.
तालिका 3. स्थानीय रूप से उन्नत गर्भाशय ग्रीवा कैंसर का उपचार
| अवस्था | द्वितीय बी - चतुर्थ ए |
| मचान |
जांच और कोल्पोस्कोपी डेटा, छाती का एक्स-रे, अंतःशिरा यूरोग्राफी, बायोप्सी और ग्रीवा नहर और गर्भाशय गुहा का उपचार |
| रेडियोथेरेपी तकनीक |
1. प्राथमिक लक्ष्य: ट्यूमर + गर्भाशय बी. 2. द्वितीयक लक्ष्य: पेल्विक और सामान्य इलियाक लिम्फ नोड्स। तकनीक: 4-फ़ील्ड. 1. ट्यूमर का निर्धारण पैल्पेशन और सीटी स्कैन (यदि संभव हो) + किनारे से 2 सेमी द्वारा किया जाता है 2. ए-पी फ़ील्ड: पार्श्व: श्रोणि की हड्डी की सीमाओं से 2 सेमी पार्श्व सुपीरियर: कशेरुक L5 और S1 की सीमा निचला: ऑबट्यूरेटर फोरामेन से 2 सेमी नीचे या परिभाषित ट्यूमर सीमा से 2 सेमी नीचे 3. पार्श्व क्षेत्र: पूर्वकाल = व्यक्तिगत, ट्यूमर की सीमाओं द्वारा निर्धारित पश्च = व्यक्तिगत, ट्यूमर की सीमाओं द्वारा निर्धारित |
| प्रति प्राथमिक ट्यूमर खुराक | एसओडी 50 ग्रे/5-6 सप्ताह में दूरस्थ विकिरण + बिंदु ए पर इंट्राकेवेटरी थेरेपी 30-35 ग्रे (चरण आईआईबी - आईवीए, 35-40 ग्रे के लिए) |
| मेटास्टेसिस के क्षेत्रीय क्षेत्रों को खुराक | एसओडी 50 ग्रे/5 सप्ताह में दूरस्थ विकिरण |
| कुल उपचार समय 6-7 सप्ताह | |
| प्रतिस्पर्धी कीमोथेरेपी: सिस्प्लैटिन 40 मिलीग्राम/एम2 | |
विकिरण तकनीक और खुराक:खुराक और विकिरण क्षेत्र तालिका 3 में प्रस्तुत किए गए हैं। प्राथमिक ट्यूमर और मेटास्टेसिस के क्षेत्रीय क्षेत्रों के बीच एक समान खुराक वितरण (± 5%) के साथ उचित ऊर्जा के साथ विकिरण किया जाना चाहिए। विकिरणित किए जाने वाले ट्यूमर की मात्रा, जहां संभव हो, नैदानिक अध्ययन और सीटी का उपयोग करके निर्धारित की जानी चाहिए। विकिरण तकनीक में कम से कम 4 क्षेत्रों का उपयोग करना शामिल है। ब्रैकीथेरेपी कम और उच्च शक्ति दोनों स्रोतों के साथ की जा सकती है।
मानक उपचार प्लैटिनम-आधारित दवाओं पर आधारित प्रतिस्पर्धी कीमोथेरेपी के साथ संयुक्त विकिरण चिकित्सा है। बाहरी बीम विकिरण चिकित्सा के दौरान सिस्प्लैटिन को सप्ताह में एक बार 40 मिलीग्राम/एम2 की खुराक निर्धारित की जाती है। अनुशंसित खुराक बिंदु ए पर 85 से 90 ग्रे और बिंदु बी पर 55 से 60 ग्रे तक होती है। सामान्य इलियाक और/या पैरा-महाधमनी लिम्फ नोड्स में मेटास्टेस वाले रोगियों में, पैरा में विकिरण क्षेत्रों का विस्तार करने पर विचार करना आवश्यक है। -महाधमनी क्षेत्र (17,18,24 ). साक्ष्य का स्तर सी.
चरण IVB और पुनरावर्तन
पुनरावृत्ति श्रोणि में (स्थानीय पुनरावृत्ति) या श्रोणि अंगों के बाहर (दूरस्थ मेटास्टेस) हो सकती है। प्राथमिक ट्यूमर के बड़े आकार के साथ, श्रोणि में पुनरावृत्ति और दूर के मेटास्टेस वाले रोगियों की संख्या बढ़ जाती है। अधिकांश पुनरावृत्ति पहले दो वर्षों में होती है और इस श्रेणी के रोगियों के लिए रोग का निदान प्रतिकूल है, उनमें से अधिकांश रोग बढ़ने से मर जाते हैं (25)। औसत उत्तरजीविता सात महीने है।
सर्वाइकल कैंसर के बढ़ने पर इसके मुख्य लक्षण दर्द, पैरों में सूजन, एनोरेक्सिया, जननांग पथ से रक्तस्राव, कैचेक्सिया, मनोवैज्ञानिक और अन्य समस्याएं हैं। रोगियों के इस समूह के उपचार और प्रबंधन की एक विधि चुनते समय, विशेषज्ञों के एक पूरे समूह के प्रयासों को संयोजित करना इष्टतम होता है: स्त्री रोग विशेषज्ञ, रेडियोलॉजिस्ट, कीमोथेरेपिस्ट, मनोवैज्ञानिक, पोषण विशेषज्ञ और विशेष रूप से प्रशिक्षित नर्स। व्यापक सहायता के साथ-साथ दर्द और अन्य लक्षणों से राहत, चिकित्सा कर्मचारियों का मुख्य लक्ष्य है।
प्राथमिक पुनरावृत्ति वाले रोगियों का प्रबंधन:उपचार पद्धति का चुनाव रोगी की सामान्य स्थिति, पुनरावृत्ति/मेटास्टेसिस का स्थान, उनकी व्यापकता और प्राथमिक उपचार की विधि पर आधारित होता है।
प्राथमिक रैडिकल हिस्टेरेक्टॉमी के बाद पुनरावृत्ति के लिए संभावित उपचार (तालिका 4):रैडिकल हिस्टेरेक्टॉमी के बाद श्रोणि में पुनरावृत्ति का इलाज विकिरण चिकित्सा और सर्जरी (पेल्विक एक्सेंटरेशन) दोनों से किया जा सकता है। प्राथमिक शल्य चिकित्सा उपचार के बाद स्थानीयकृत पेल्विक रिलैप्स के लिए रेडिकल विकिरण (± प्रतिस्पर्धी कीमोथेरेपी) बड़ी संख्या में रोगियों (26) में प्रभावी है। विकिरण चिकित्सा की खुराक और मात्रा रोग की सीमा के अनुसार निर्धारित की जानी चाहिए।
इस प्रकार, सूक्ष्म ट्यूमर आकार के लिए, सामान्य खुराक कम विकिरण क्षेत्र आकार के साथ 1.8-2.0 ग्रे के आरओडी के साथ 50 ग्रे है, और बड़े ट्यूमर के लिए खुराक 64-66 ग्रे है।
रोग के प्रसारित रूपों या असफल प्राथमिक उपचार के बाद स्थानीय पुनरावृत्ति के मामले में, जब पारंपरिक उपचार करना संभव नहीं होता है, तो उपशामक कीमोथेरेपी या रोगसूचक उपचार निर्धारित किया जाता है। सिस्प्लैटिन सीसी (27,28) के लिए सबसे प्रभावी दवाओं में से एक है। ऐसे मामलों में औसत जीवन प्रत्याशा 3 से 7 महीने तक होती है।
तालिका 4. सर्वाइकल कैंसर के सर्जिकल उपचार के बाद स्थानीय पुनरावृत्ति
रेडिकल हिस्टेरेक्टॉमी मामूली पुनरावृत्ति वाले रोगियों में की जाती है (< 2 см в диаметре), ограниченными шейкой матки. Несмотря на увеличение количества осложнений при операциях после первичной лучевой терапии, в большинстве случаев нет необходимости накладывать колостомы (29, 30).
केंद्रीय रूप से स्थानीय पुनरावृत्ति वाले रोगी, इंट्रापेरिटोनियल प्रसार और दूर के मेटास्टेसिस की अनुपस्थिति में मूत्राशय और मलाशय की भागीदारी, और गर्भाशय ग्रीवा और श्रोणि दीवार के बीच मुक्त स्थान की उपस्थिति, श्रोणि प्रवेश के लिए संभावित उम्मीदवार हैं।
लक्षणों की एक त्रिमूर्ति - निचले छोरों की द्विपक्षीय लसीका सूजन, कटिस्नायुशूल, मूत्र पथ में रुकावट एक निष्क्रिय प्रक्रिया का संकेत देती है। रोगियों के इस समूह के लिए उपशामक और रोगसूचक उपचार का संकेत दिया गया है।
सबसे अनुकूल पूर्वानुमान 6 महीने से अधिक की पुनरावृत्ति-मुक्त अवधि, 3 सेमी से कम के ट्यूमर का आकार और मापदंडों में घुसपैठ की अनुपस्थिति (31-34) के साथ है। रोगियों के इस समूह में 5 साल की जीवित रहने की दर 30 से 60% तक होती है, और पेरिऑपरेटिव मृत्यु दर 10% से अधिक नहीं होती है।
तालिका 5. सर्वाइकल कैंसर के लिए रेडियोथेरेपी के बाद स्थानीय पुनरावृत्ति
चरण IVB और मेटास्टेटिक CC में प्रणालीगत कीमोथेरेपी की भूमिका तालिका 6 में प्रस्तुत की गई है।
तालिका 6. मेटास्टैटिक सीसी के लिए प्रणालीगत कीमोथेरेपी
| सिफारिशों | साक्ष्य का स्तर |
| सर्वाइकल कैंसर के इलाज के लिए सिस्प्लैटिन एकमात्र प्रभावी दवा है। | में |
| 100 मिलीग्राम/एम2 (31%) की खुराक पर सिस्प्लैटिन निर्धारित करते समय वस्तुनिष्ठ प्रभावों की घटना 50 मिलीग्राम/एम2 (21%) की खुराक निर्धारित करने की तुलना में अधिक है, लेकिन यह प्रभावशीलता बीमारी में वृद्धि से जुड़ी नहीं है- मुफ़्त और समग्र अस्तित्व (28) | में |
| संतोषजनक सामान्य स्थिति और मेटास्टेस के एक्स्ट्रापेल्विक स्थान वाले रोगियों में कीमोथेरेपी पर वस्तुनिष्ठ प्रभाव की दर अधिक होती है और पहले से विकिरणित पुनरावृत्तियों में यह लगभग अप्रभावी होती है। | साथ |
| जीवित रहने पर प्रशामक कीमोथेरेपी का प्रभाव अज्ञात है | साथ |
दूर के मेटास्टेस:विकिरण चिकित्सा को रोगसूचक ट्यूमर मेटास्टेसिस के लिए उपशामक उपचार के रूप में संकेत दिया जाता है, उदाहरण के लिए, हड्डी मेटास्टेसिस (34), बढ़े हुए पैरा-महाधमनी, दर्द से राहत के लिए सबक्लेवियन लिम्फ नोड्स, या मस्तिष्क मेटास्टेस (35) के लिए।
सर्वाइकल कैंसर का यादृच्छिक पता
ये निष्कर्ष मुख्य रूप से अन्य संकेतों के लिए की गई साधारण हिस्टेरेक्टॉमी के बाद निदान किए गए आक्रामक गर्भाशय ग्रीवा कैंसर के मामलों से संबंधित हैं। ऐसी स्थितियों में उपचार शुरू करने से पहले, अतिरिक्त जांच आवश्यक है: प्रक्रिया की सीमा को स्पष्ट करने के लिए श्रोणि और पेट के अंगों की सीटी या एमआरआई, छाती का एक्स-रे। उपचार पद्धति का निर्धारण रूपात्मक परीक्षण और रेडियोलॉजिकल निष्कर्षों के आधार पर किया जाना चाहिए।
पैथोलॉजिकल निष्कर्षों के अभाव में:
1. चरण IA1 के लिए, कोई अतिरिक्त उपचार नहीं किया जाता है।
2. स्टेज IA2 और उससे ऊपर के लिए, निम्नलिखित उपचार आवश्यक है:
सकारात्मक रिसेक्शन मार्जिन, गहरे स्ट्रोमल आक्रमण और लिम्फोवास्कुलर स्पेस की भागीदारी के मामलों में, प्रतिस्पर्धी केमोराडिएशन थेरेपी निर्धारित की जाती है (38);
गहरे स्ट्रोमल आक्रमण, नकारात्मक स्नेह मार्जिन और लिम्फोवास्कुलर भागीदारी के बिना रोगियों में, योनि के ऊपरी तीसरे भाग और लिम्फैडेनेक्टॉमी के साथ रेडिकल पैरामेट्रोक्टोमी को प्रतिस्पर्धी केमोराडिएशन थेरेपी (39) के विकल्प के रूप में किया जाता है। साक्ष्य का स्तर सी.
गर्भावस्था के दौरान सी.सी
सामान्य तौर पर, गर्भावस्था के दौरान गर्भाशय ग्रीवा के कैंसर का उपचार गैर-गर्भवती महिलाओं के समान सिद्धांतों पर आधारित होता है। केवल कुछ विशिष्ट सिफ़ारिशें हैं। गर्भाशय ग्रीवा का संकरण केवल तभी किया जाता है जब रक्तस्राव, गर्भपात या समय से पहले जन्म के उच्च जोखिम के कारण साइटोलॉजिकल परीक्षण और कोल्पोस्कोपी के आधार पर आक्रामक वृद्धि का संदेह हो।
सर्वाइकल कैंसर से पीड़ित गर्भवती महिलाओं के लिए प्रबंधन रणनीति निर्धारित करने में सबसे महत्वपूर्ण शर्त एक रेडियोलॉजिस्ट और कीमोथेरेपिस्ट के अलावा एक नवजातविज्ञानी और प्रसूति-स्त्री रोग विशेषज्ञ को शामिल करने वाला एक बहु-विषयक दृष्टिकोण है। निर्णय लेने में स्वयं महिला और उसके साथी की भागीदारी आवश्यक है, और गर्भावस्था को जारी रखने की उनकी इच्छा को ध्यान में रखा जाना चाहिए।
संदिग्ध माइक्रोइनवेसिव सर्वाइकल कैंसर वाले रोगियों में, उपचार में देरी से मां को कोई नुकसान नहीं होता है और भ्रूण की व्यवहार्यता में उल्लेखनीय वृद्धि होती है।
चरण IA1 रोग वाली महिलाएं, जिनकी पुष्टि गर्भाधान और नकारात्मक स्नेह मार्जिन द्वारा की गई है, वे अपनी गर्भावस्था को समाप्त कर सकती हैं और योनि से जन्म दे सकती हैं। माइक्रोइनवेसिव सर्वाइकल कार्सिनोमा के लिए डिलीवरी की विधि रोग के परिणाम को प्रभावित नहीं करती है।
रोग चरण IA2 और उच्चतर के लिए, उपचार को व्यक्तिगत रूप से चुना जाना चाहिए, मुख्य रूप से उपचार की विधि और उसके समय पर निर्णय रोग के चरण और गर्भावस्था के चरण पर आधारित होता है। प्रक्रिया की सीमा का आकलन करने के लिए एमआरआई किया जाता है। यदि गर्भधारण के 20 सप्ताह से पहले निदान किया जाता है, तो उपचार तुरंत शुरू होना चाहिए। पसंद का उपचार भ्रूण को यथास्थान रखते हुए रैडिकल हिस्टेरेक्टॉमी है। कीमोरेडियोथेरेपी करते समय, एक नियम के रूप में, गर्भावस्था की समाप्ति नहीं की जाती है, क्योंकि उपचार शुरू होने के बाद सहज गर्भपात होता है।
यदि गर्भावस्था के 28 सप्ताह के बाद सर्वाइकल कैंसर का पता चलता है, तो व्यवहार्य भ्रूण प्राप्त होने तक उपचार में देरी करने की सिफारिश की जाती है। स्टेज IA2 और IBI में गर्भधारण के 20 से 28 सप्ताह के बीच गर्भाशय ग्रीवा के कैंसर के उपचार में तब तक देरी हो सकती है जब तक कि मातृ पूर्वानुमान (40, 41) को प्रभावित किए बिना एक व्यवहार्य भ्रूण प्राप्त नहीं हो जाता। जब रोग की अवस्था आईबीआई से अधिक होती है, तो उपचार में देरी से रोग का पूर्वानुमान काफी खराब हो जाता है और जीवित रहने पर असर पड़ता है।
यह ध्यान दिया जाना चाहिए कि यह निर्धारित करने के लिए कोई मानक नहीं हैं कि उपचार की शुरुआत में कितनी देर हो सकती है। व्यवहार में, देरी की अवधि रोग की अवस्था, रूपात्मक निष्कर्ष, गर्भकालीन आयु और माता-पिता की इच्छा पर निर्भर करती है। स्थानीय रूप से उन्नत सीसी के लिए डिलीवरी के समय की योजना बनाते समय, रोग की आगे की प्रगति को रोकने के लिए नियोएडजुवेंट कीमोथेरेपी निर्धारित करने पर निर्णय लेना संभव है (42) - गतिशील निगरानी की आवश्यकता है! प्रसव गर्भधारण के 34 सप्ताह के बाद नहीं होता है।
यदि निदान गर्भाधान के समय गर्भाशय ग्रीवा के द्रव्यमान को नहीं हटाया जाता है, तो प्रसव की पसंदीदा विधि शास्त्रीय सिजेरियन सेक्शन है, हालांकि कई पूर्वव्यापी अध्ययनों से पता चला है कि प्रसव की विधि का गर्भाशय ग्रीवा के कैंसर के पूर्वानुमान पर कोई प्रभाव नहीं पड़ता है (43)।
अवलोकन
सर्वाइकल कैंसर के उपचार के बाद पुनरावृत्ति की सबसे बड़ी संख्या पहले 3 वर्षों में होती है, जो उपचार के बाद रोगियों की लगातार निगरानी की आवश्यकता को निर्धारित करती है।
किसी महिला की यात्रा के दौरान शोध की न्यूनतम मात्रा में शामिल हैं:
1. दर्पणों में निरीक्षण.
2. स्त्री रोग संबंधी परीक्षा।
3. पैप परीक्षण.
ये अध्ययन हर 3 महीने में कम से कम एक बार, पहले 2 वर्षों के दौरान, हर 4 महीने में कम से कम एक बार, तीसरे वर्ष के दौरान, हर छह महीने में एक बार, अवलोकन के चौथे और 5वें वर्ष के दौरान, फिर सालाना किया जाता है।
पैथोलॉजिकल जांच
तालिका 7. सर्वाइकल कैंसर के लिए दवा की पैथोमोर्फोलॉजिकल जांच
| संकेत | विवरण | ||
| स्थूल मूल्यांकन | |||
| एक दवा | गर्भाशय का आकार और वजन, गर्भाशय ग्रीवा का आकार, उपांग (दाएं और बाएं के लिए अलग-अलग), पैरासर्विकल ऊतकों का आकार (दाएं और बाएं), योनि कफ की लंबाई | ||
| फोडा | आकार (3 आयाम), स्थान, उपस्थिति, आक्रमण की गहराई/सरवाइकल स्ट्रोमा की मोटाई, पैरासर्वाइकल ऊतक की भागीदारी, गर्भाशय के शरीर की भागीदारी, योनि कफ, ट्यूमर से योनि के उच्छेदन मार्जिन तक की दूरी, शामिल अन्य संरचनाएं, मौजूद और बनाए गए निशान, निकाले गए ब्लॉकों की संख्या | ||
| लसीकापर्व | आकार (से और तक), सबसे बड़े मेटास्टेसिस का आकार, लिम्फ नोड्स की संख्या और कैसेट की संख्या | ||
| सूक्ष्म मूल्यांकन |
हिस्टोटाइप यदि उपलब्ध हो तो सीआईएन (डिग्री सहित)। सतह उपकला के आधार से आक्रमण की अधिकतम गहराई (मिमी) सबसे गहरे आक्रमण के स्थल पर गर्दन की मोटाई (मिमी) अधिकतम क्षैतिज फैलाव (मिमी) मल्टीफ़ोकल आक्रमण लिम्फोवास्कुलर स्पेस में आक्रमण पैरासर्वाइकल ऊतकों की स्थिति (पैरामेट्रियल आक्रमण) |
त्वचा कोशिकाओं का कार्सिनोमा | ग्रंथिकर्कटता |
| विभेदन की उच्च डिग्री G1 | मुख्य सेलुलर संरचना विशिष्ट केराटिनाइजिंग बड़ी कोशिकाएं हैं। अधिकांश कोशिकाएँ (>75%) अच्छी तरह से विभेदित हैं। माइटोटिक गतिविधि कम है. ट्यूमर में पैपिलरी और ठोस एक्सोफाइटिक संरचनाएं होती हैं; सीमाएँ संयोजी कोशिकाओं द्वारा निर्मित होती हैं। | ट्यूमर में पैपिला के साथ अच्छी तरह से गठित ग्रंथियां होती हैं। कोशिकाएँ समान अंडाकार नाभिक से लम्बी होती हैं; न्यूनतम स्तरीकरण (मोटाई में कोशिकाओं की तीन पंक्तियों से कम)। मिटोज़ अक्सर नहीं होते हैं। | |
| मध्यम विभेदन G2 | कोशिकाओं का प्रकार आमतौर पर गैर-केराटिनाइजिंग, बड़ा होता है। लगभग 50% कोशिकाएँ अच्छी तरह से विभेदित हैं; व्यक्तिगत कोशिकाओं में केराटिनाइजेशन होता है। माइटोटिक गतिविधि बढ़ जाती है। ट्यूमर की घुसपैठ की सीमाएँ होती हैं; असामान्य सूजन आम है। | ट्यूमर में जटिल ग्रंथियां होती हैं जिनमें बार-बार पुल और पालने का निर्माण होता है। ठोस क्षेत्र आम हैं लेकिन फिर भी ट्यूमर के आधे से भी कम हिस्से पर कब्जा करते हैं। गुठलियाँ अधिक गोल और असमान होती हैं; माइक्रोन्यूक्लिओली हैं। अधिक बार माइटोज़ होना। | |
| कम विभेदन G3 | मुख्य कोशिकीय संरचना छोटी कोशिकाएँ हैं। कोशिकाओं में उच्च परमाणु-साइटोप्लाज्मिक अनुपात के साथ बेसोफिलिक साइटोप्लाज्म होता है। कोशिकाओं और नाभिकों का आकार समान होता है। 25% से कम कोशिकाएँ विभेदित हैं। बड़ी संख्या में माइटोज़, पैथोलॉजिकल माइटोज़ होते हैं। ट्यूमर आमतौर पर घुसपैठ करने वाले होते हैं, जिनकी सीमा पर घातक कोशिकाएं होती हैं। |
ट्यूमर में घातक कोशिकाओं के क्षेत्र होते हैं; दुर्लभ ग्रंथियाँ दिखाई देती हैं (<50%). Клетки крупные и неравномерные с плеоморфными ядрами. Встречаются случайные перстневидные клетки. Много митозов, в том числе аномальных. Выраженная десмоплазия и частые некрозы.
जानकारीसमीक्षक: 1. कोज़ख्मेतोव बी.एस.एच. - ऑन्कोलॉजी विभाग के प्रमुख, अल्माटी स्टेट इंस्टीट्यूट फॉर एडवांस्ड मेडिकल स्टडीज, डॉक्टर ऑफ मेडिकल साइंसेज, प्रोफेसर। 2. अबिसाटोव जी.के.एच. - कज़ाख-रूसी चिकित्सा विश्वविद्यालय के ऑन्कोलॉजी, मैमोलॉजी विभाग के प्रमुख, चिकित्सा विज्ञान के डॉक्टर, प्रोफेसर। बाहरी समीक्षा परिणाम:सकारात्मक निर्णय. प्रारंभिक परीक्षण के परिणाम:इन प्रोटोकॉल के अनुसार उपचार कजाकिस्तान गणराज्य के स्वास्थ्य मंत्रालय के कज़ाख रिसर्च इंस्टीट्यूट ऑफ ऑन्कोलॉजी एंड रेडियोलॉजी के स्त्री रोग संबंधी ऑन्कोलॉजी विभाग में किया जाता है। प्रोटोकॉल डेवलपर्स की सूची: 1. नैदानिक कार्य के लिए उप निदेशक, चिकित्सा विज्ञान के डॉक्टर चिंगिसोवा Zh.K. 2. सिर ऑन्कोगायनेकोलॉजी और स्तन ट्यूमर विभाग, चिकित्सा विज्ञान के डॉक्टर कैरबाएव एम.आर. 3. सिर संपर्क विकिरण थेरेपी विभाग, चिकित्सा विज्ञान के डॉक्टर तेल्गुज़िवा Zh.A. 4. सिर डे हॉस्पिटल रेडियोथेरेपी विभाग, पीएच.डी. सवखतोवा ए.डी. 5. ऑन्कोगायनेकोलॉजी और स्तन ट्यूमर विभाग के वरिष्ठ शोधकर्ता, पीएच.डी. कुकुबासोव ई.के. ध्यान!
|
ICD-10 में इसे घातक नियोप्लाज्म के रूप में वर्गीकृत किया गया है। यदि ट्यूमर आंतरिक रूप से स्थानीयकृत है, तो इसका ICD कोड C53.0 है, और बाह्य रूप से - C53.1 है। गर्भाशय ग्रीवा के घावों के लिए जो इनमें से एक या अधिक स्थानों से आगे तक फैले हों, इसे कोड C53.8 दिया गया है। इस वर्गीकरण को नैदानिक नहीं माना जाता है और यह उपचार पद्धति की पसंद को प्रभावित नहीं करता है।
आंकड़े
महिला जननांग क्षेत्र के सभी प्रकार के ऑन्कोलॉजिकल विकृति विज्ञान में, गर्भाशय ग्रीवा का कैंसर लगभग 15% है और एंडोमेट्रियम और स्तन के घातक नवोप्लाज्म के बाद तीसरे स्थान पर है। यह निदान प्रतिवर्ष दुनिया भर में 200 हजार से अधिक महिलाओं के जीवन का दावा करता है। रूस में, इस प्रकार का ऑन्कोलॉजी घातक ट्यूमर से महिलाओं में मृत्यु के कारणों में 5वें स्थान पर है। हाल के वर्षों में, यह ऑन्कोलॉजिकल पैथोलॉजी 40 वर्ष से कम उम्र की महिलाओं में सबसे अधिक पहचानी जाने लगी है।
उपचार के लिए व्यक्तिगत दृष्टिकोण
डॉक्टर सर्जिकल हस्तक्षेप, विकिरण उपचार और सबसे प्रभावी एंटीट्यूमर दवाओं की नवीन तकनीकों का उपयोग करके सर्वाइकल कैंसर (ICD-10 - C53 के अनुसार) के उपचार के मानकों का पालन करते हैं। साथ ही, प्रत्येक रोगी के लिए उपचार पद्धति के चुनाव के लिए एक व्यक्तिगत दृष्टिकोण अत्यंत महत्वपूर्ण है। शल्य चिकित्सा पद्धतियों, इम्यूनोथेरेपी, कीमोथेरेपी और विकिरण सहित आधुनिक निदान तकनीकों, थेरेपी का उपयोग ऑन्कोलॉजिस्ट को बीमार महिलाओं की जीवित रहने की दर बढ़ाने की अनुमति देता है।
विकास के कारण
वर्तमान समय में, वैज्ञानिकों ने उन कारकों को स्थापित नहीं किया है जो गर्भाशय ग्रीवा के कैंसर के विकास को भड़काते हैं (ICD-10 - C53 के अनुसार)। ऐसा माना जाता है कि ऑन्कोलॉजिकल प्रक्रियाएं विभिन्न कारणों के प्रभाव में विकसित होती हैं। वायरल संक्रमण, महिला शरीर पर रासायनिक प्रभाव और गर्भाशय ग्रीवा के ऊतकों को यांत्रिक क्षति को बहिर्जात माना जाता है।

ऐसी रोग प्रक्रिया के विकास में निम्नलिखित अंतर्जात कारकों की पहचान की गई है:
- हार्मोनल असंतुलन;
- आनुवंशिक प्रवृतियां;
- चयापचयी विकार;
- महिला शरीर की प्रतिरोधक क्षमता में कमी।
एचपीवी
90% मामलों में, इस बीमारी का ट्रिगर एचपीवी है। सबसे आम घातक ट्यूमर प्रकार 16, 31, 18, 33 हैं। आमतौर पर, टाइप 16 वायरस सर्वाइकल कैंसर में पाया जाता है। शरीर की प्रतिरक्षा प्रतिक्रिया में कमी के साथ इसकी ऑन्कोजेनेसिटी काफी बढ़ जाती है। वायरस, जो विकृति विज्ञान के तंत्र में शामिल है, यौन संपर्क के माध्यम से फैलता है। ज्यादातर मामलों में, सहज पुनर्प्राप्ति होती है। लेकिन अगर रोगजनक सूक्ष्मजीव लगातार गर्भाशय ग्रीवा में रहते हैं, तो एक कैंसरयुक्त ट्यूमर विकसित हो जाता है।
जीर्ण सूजन
पैथोलॉजी के विकास को भड़काने वाले महत्वपूर्ण कारकों में पुरानी सूजन प्रक्रिया शामिल है। यह गर्भाशय ग्रीवा उपकला की संरचनाओं में डिस्ट्रोफिक परिवर्तनों के गठन की ओर जाता है, जो अंततः गंभीर जटिलताओं के विकास का कारण बनता है। इस प्रकार के ऑन्कोलॉजी के विकास में एक समान रूप से महत्वपूर्ण कारक गर्भपात के दौरान, प्रसव के दौरान, साथ ही गर्भनिरोधक के कुछ साधनों द्वारा दर्दनाक चोट माना जाता है।

बहिर्जात और अंतर्जात कारक
विशेषज्ञ विभिन्न यौन साझेदारों के साथ प्रारंभिक यौन गतिविधि के साथ-साथ धूम्रपान को सर्वाइकल कैंसर के बाहरी कारणों के रूप में शामिल करते हैं (ICD-10 - C53 के अनुसार)। निम्नलिखित अंतर्जात कारकों की पहचान की गई है:
- रक्त में एस्ट्रोजन का स्तर बढ़ा;
- एचआईवी संक्रमण की उपस्थिति सहित महिलाओं में इम्युनोडेफिशिएंसी की स्थिति;
- मौखिक हार्मोनल गर्भ निरोधकों का दीर्घकालिक उपयोग।
हमें विभिन्न व्यावसायिक खतरों, गुणवत्ता और जीवनशैली के बारे में भी नहीं भूलना चाहिए।
रोग के लक्षण

इसके गठन की प्रक्रिया की शुरुआत में, गर्भाशय ग्रीवा का कैंसर (ICD-10 - C53 के अनुसार) किसी भी रोग संबंधी लक्षण के साथ प्रकट नहीं होता है जो एक महिला को बहुत परेशान कर सकता है। केवल जब घातक गठन विघटित होने लगता है तो निम्नलिखित स्पष्ट लक्षण प्रकट होते हैं:
- विभिन्न प्रकार का प्रदर;
- दर्द, अक्सर पेट के निचले हिस्से, पीठ और मलाशय में स्थानीयकृत;
- रक्तस्राव जो स्थानीय, यहां तक कि सतही रूप से स्थित ट्यूमर गठन के छोटे, नाजुक जहाजों के टूटने के परिणामस्वरूप काफी हल्के आघात के दौरान होता है।
एक ऑन्कोलॉजिकल ट्यूमर उन स्थानों पर अंकुरण द्वारा योनि की दीवारों में लसीका वाहिकाओं के माध्यम से मेटास्टेसिस कर सकता है जहां यह ऑन्कोलॉजिकल ट्यूमर के संपर्क में आता है। मूत्रवाहिनी ट्यूमर के विकास के प्रति सबसे अधिक प्रतिरोधी होती है। बहुत अधिक बार, विशेषज्ञ ऑन्कोलॉजिकल घुसपैठ द्वारा मूत्रवाहिनी के संपीड़न का पता लगाते हैं; परिणामस्वरूप, मूत्र का सामान्य बहिर्वाह बाधित हो जाता है।
मलाशय में ट्यूमर का बढ़ना ऑन्कोलॉजिकल प्रक्रिया की उपेक्षा का संकेत देता है। मलाशय की श्लेष्मा झिल्ली, एक नियम के रूप में, ट्यूमर के ऊपर लंबे समय तक गतिशील नहीं रहती है। बहुत कम ही, सर्वाइकल कैंसर अंडाशय और फैलोपियन ट्यूब तक फैल सकता है। अप्रत्याशित मामलों में दूर के ऊतकों और अंगों में मेटास्टेसिस एक दुर्लभ घटना है।
स्त्री रोग विशेषज्ञों की राय है कि सर्वाइकल कैंसर अक्सर लंबे समय तक एक "स्थानीय प्रक्रिया" बना रहता है। मेटास्टेसिस, जो एक सामान्य संक्रमण के नैदानिक लक्षण देता है, अत्यंत दुर्लभ है। बीमार महिलाओं में तापमान उच्च स्तर पर रहता है, जिससे कभी-कभी कुछ समय के लिए आराम भी मिलता है। कैंसर कैशेक्सिया कैंसर ट्यूमर के गठन के अंतिम चरण में देखा जाता है और यह विभिन्न रोग संबंधी जटिलताओं के कारण होता है।

सर्वाइकल कैंसर (ICD-10 - C53) के लक्षणों पर ध्यान नहीं दिया जाना चाहिए।
एक घातक ट्यूमर के विकास के साथ, संपूर्ण गर्भाशय ग्रीवा या उसके अलग-अलग हिस्से स्पर्श करने पर घने, बढ़े हुए दिखाई देते हैं और श्लेष्मा झिल्ली मोटी हो जाती है। सतह उपकला की असामान्यताएं अक्सर स्थानों में देखी जाती हैं। आप अक्सर विभिन्न आकृतियों और आकारों के सफेद क्षेत्रों के रूप में अतिरिक्त ऊतक देख सकते हैं।
यदि आपको सर्वाइकल कैंसर (ICD-10 कोड C53) का संदेह है तो क्या करें?
पैथोलॉजी का निदान
वर्तमान में, निदान के विभिन्न तरीके मौजूद हैं। सर्वाइकल ऑन्कोलॉजी के निदान का आधार महिला की पूरी जांच, जीवन और बीमारी और शिकायतों के इतिहास का सही संग्रह, रोगी की स्थिति की गंभीरता का पर्याप्त मूल्यांकन और दर्पण का उपयोग करके स्त्री रोग संबंधी परीक्षा माना जाता है। इस रोग के निदान के लिए निम्नलिखित वाद्य विधियों का उपयोग किया जाता है:
- कोल्पोस्कोपी;
- एसटीआई के लिए प्रयोगशाला परीक्षण;
- बायोप्सी के लिए सामग्री लेना;
- साइटोलॉजिकल स्क्रीनिंग.
कोल्पोस्कोपी को सीधे तौर पर घातक सर्वाइकल कैंसर (ICD-10 - C53) और कैंसर पूर्व स्थितियों दोनों के निदान के लिए सबसे प्रभावी तरीकों में से एक माना जाता है। इस पद्धति की प्रभावशीलता 80% तक पहुँच जाती है। ऑन्कोलॉजिस्ट इसे अन्य आधुनिक तकनीकों के साथ जोड़ते हैं। कोल्पोस्कोपी आपको बाद में कुछ रूपात्मक अध्ययन करने के लिए, समग्र रूप से गर्भाशय ग्रीवा को नुकसान की गहराई और प्रकृति, प्रभावित क्षेत्र की सीमाओं और आयामों को निर्धारित करने की अनुमति देता है।

पैथोलॉजी के निदान में सर्विकोस्कोपी महत्वपूर्ण है। यह अध्ययन हिस्टेरोस्कोप का उपयोग करके किया जाता है। इस तकनीक में कुछ मतभेद हैं:
- गर्भावस्था;
- सूजन प्रक्रियाएं;
- खून बह रहा है।
सर्विकोस्कोपी आपको ग्रीवा नहर की नैदानिक स्थिति का आकलन करने की अनुमति देती है और 150 गुना तक की वृद्धि दिखाती है, जिसके कारण एक लक्षित बायोप्सी की जाती है। ट्यूमर के स्थान का निर्धारण करने के लिए प्रभावी तरीकों में से एक साइटोलॉजिकल परीक्षा है, जिसे दुनिया भर में मान्यता प्राप्त है और डब्ल्यूएचओ द्वारा अनुशंसित किया गया है। कोल्पोस्कोपी के संयोजन में, इस अध्ययन की प्रभावशीलता 90-95% तक पहुंच जाती है। कोशिका विज्ञान का सार गर्भाशय ग्रीवा से कोशिकाओं को इकट्ठा करना और रोग संबंधी तत्वों का पता लगाने के लिए उनका सूक्ष्म अध्ययन करना है। निदान में निर्णायक भूमिका बायोप्सी के माध्यम से प्राप्त बायोमटेरियल की हिस्टोलॉजिकल परीक्षा को दी जाती है।
इलाज
सर्वाइकल कैंसर (ICD-10 कोड - C53) के लिए उपचार पद्धति का चुनाव व्यक्तिगत रूप से निर्धारित किया जाता है। थेरेपी कैंसर प्रक्रिया की सीमा और सहवर्ती विकृति की गंभीरता पर निर्भर करती है। महिला की उम्र सबसे कम मायने रखती है। रोग के उपचार के पारंपरिक तरीकों में शामिल हैं:
- शल्य चिकित्सा;
- संयुक्त;
- किरण.

वर्तमान में, वैज्ञानिक सक्रिय रूप से सर्वाइकल कैंसर (ICD-10, कोड C53 के अनुसार) और ड्रग थेरेपी के कीमोरेडिएशन उपचार की संभावनाओं का अध्ययन कर रहे हैं।
गंभीर इंट्रापीथेलियल कैंसर के मामले में, गर्भाशय का निदान अलग-अलग इलाज और गर्भाशय ग्रीवा का शंकुकरण एक इलेक्ट्रिक चाकू, स्केलपेल या लेजर बीम का उपयोग करके किया जाता है।
वर्तमान में, चरण 1 और 2 के आक्रामक कैंसर के उपचार में, गर्भाशय और उपांगों के विस्तारित विलोपन (वर्टहाइम ऑपरेशन) का उपयोग किया जाता है। संयुक्त उपचार में विभिन्न अनुक्रमों में विकिरण चिकित्सा और सर्जरी शामिल होती है।
सर्वाइकल कैंसर एक आक्रामक प्रक्रिया है जो आम तौर पर स्तरीकृत स्क्वैमस एपिथेलियम से सिंगल-लेयर कॉलमर एपिथेलियम में संक्रमण के स्थल पर शुरू होती है और इसे स्तरीकृत स्क्वैमस या ग्रंथि संबंधी एपिथेलियम द्वारा दर्शाया जाता है।
पिछले 30 वर्षों में इस बीमारी की घटनाओं में 50% की कमी के बावजूद, सर्वाइकल कैंसर कैंसर से मृत्यु के प्रमुख कारणों में से एक है।
सांख्यिकीय डेटा
घटना: 2001 में प्रति 100,000 महिला जनसंख्या पर 15.9
. प्रमुख उम्र
आक्रामक सर्वाइकल कैंसर अक्सर 40 से 50 वर्ष की उम्र के बीच पाया जाता है।
30 वर्ष से पहले और 70 वर्ष के बाद, क्रमशः लगभग 7 और 16% महिलाओं में प्राथमिक गर्भाशय ग्रीवा कैंसर का पता चलता है।
जोखिम
एचपीवी वायरस, एचएसवी टाइप 2 (एचएसवी-2), एचआईवी से संक्रमण
. धूम्रपान
. गर्भाशय में डायथाइल स्टिलबेस्ट्रोल के संपर्क में आना
. यौन क्रिया की शीघ्र शुरुआत
. बड़ी संख्या में यौन साथी
. प्रारंभिक पहला जन्म
. यौन रोग
. मौखिक गर्भनिरोधक लेना।
pathomorphology
. सबसे आम प्रकार आक्रामक स्क्वैमस सेल कार्सिनोमा (80-85%) है
. आवृत्ति में दूसरे स्थान पर आक्रामक एडेनोकार्सिनोमा (15-20%) का कब्जा है
. छोटे सेल कार्सिनोमा, मस्सा कार्सिनोमा और लिंफोमा का आमतौर पर कम निदान किया जाता है।
नैदानिक तस्वीर
. अनियमित स्वतःस्फूर्त योनि से रक्तस्राव
. व्यापक स्थानीय क्षति के साथ, दुर्गंधयुक्त खूनी स्राव और पेट के निचले हिस्से में हल्का दर्द होता है
. संभोग के बाद योनि से रक्तस्राव
. dyspareunia
. रक्तमेह
. मलाशय से रक्तस्राव
. गर्भाशय ग्रीवा का बढ़ना.
वर्गीकरण
टीएनएम प्रणाली के अनुसार
टिस - यथास्थान कैंसर
टीएल - सर्वाइकल कैंसर, सीमित (शरीर में फैलने पर ध्यान नहीं दिया जाता)
T1a - आक्रामक कार्सिनोमा, जिसका निदान केवल सूक्ष्मदर्शी रूप से किया जाता है
टी1 ए 1 - स्ट्रोमल आक्रमण गहराई में 3.0 मिमी से अधिक और क्षैतिज रूप से 7.0 मिमी तक नहीं
टी1 ए2 - स्ट्रोमा में आक्रमण 5.0 मिमी से अधिक नहीं, क्षैतिज फैलाव 7.0 मिमी तक
टिब - गर्भाशय ग्रीवा तक सीमित एक चिकित्सकीय रूप से दिखाई देने वाला ट्यूमर, या T1a2 Tlbl से बड़ा एक सूक्ष्म ट्यूमर - सबसे बड़े आयाम में 4.0 सेमी तक का चिकित्सकीय रूप से पता लगाने योग्य ट्यूमर
T1b2 - चिकित्सकीय रूप से पता लगाने योग्य ट्यूमर, सबसे बड़े आयाम में 4.0 सेमी से अधिक
. टी2 - ट्यूमर गर्भाशय से आगे तक फैलता है, लेकिन पेल्विक दीवार या योनि के निचले तीसरे हिस्से पर आक्रमण किए बिना
T2a - पैरामीट्रियम आक्रमण के बिना
टी2बी - पैरामीट्रियम आक्रमण के साथ
. टी3 - गर्भाशय ग्रीवा का कैंसर, जो पेल्विक दीवार तक फैल जाता है और/या योनि के निचले तीसरे भाग में शामिल हो जाता है, और/या हाइड्रोनफ्रोसिस, या गैर-कार्यशील किडनी की ओर ले जाता है।
टी3 - ट्यूमर योनि के निचले तीसरे हिस्से में बढ़ता है, लेकिन पेल्विक दीवार तक नहीं फैलता है
टी3 - ट्यूमर पेल्विक दीवार तक फैल जाता है और/या हाइड्रोनफ्रोसिस, या गैर-कार्यशील किडनी की ओर ले जाता है
. टी4 - ट्यूमर में मूत्राशय या मलाशय का म्यूकोसा शामिल होता है और/या श्रोणि से परे तक फैला होता है (बुलस एडिमा की उपस्थिति टी4 जैसी ट्यूमर श्रेणी का संकेत नहीं देती है)
क्षेत्रीय लिम्फ नोड्स
एन1 - क्षेत्रीय लिम्फ नोड्स में मेटास्टेस
दूर के मेटास्टेस। एमएल - दूर के मेटास्टेस हैं।
चरणों के अनुसार समूहीकरण
स्टेज 0: टिसनोमो
चरण 1ए1: टालनोमो
स्टेज IA2: Tla2N0M0
स्टेज IB1: TlblNOMO
स्टेज IB2: Tlb2N0M0
स्टेज NA: T2aN0M0
स्टेज IIB: T2bN0M0
स्टेज IIIA: T3aN0M0
चरण IIIB: o T1N1 MO T2N1 MO T3aN 1 MO o T3bN0- 1M0
चरण IV A: T4N0-1M0
स्टेज IV बी: T0-4N0-1M1।
प्रयोगशाला अनुसंधान
. यूएसी (पुरानी रक्त हानि के कारण संभावित एनीमिया)
. सीरम क्रिएटिनिन (मूत्र पथ में संभावित रुकावट)
. लिवर फ़ंक्शन परीक्षण (संभावित मेटास्टेसिस)
. पेप स्मीयरों।
विशेष अध्ययन
. कोल्पोस्कोपी में 3-5% एसिटिक एसिड समाधान के आवेदन के बाद 7.5-30 गुना आवर्धन पर परिवर्तन क्षेत्र और स्क्वैमस और कॉलमर एपिथेलियम की सीमा की जांच शामिल है।
. कोल्पोस्कोपी के दौरान पता न चलने वाले डिसप्लेसिया को बाहर करने के लिए कोल्पोस्कोपी के साथ संयोजन में गर्भाशय ग्रीवा नहर का इलाज किया जाता है
. सरवाइकल बायोप्सी. गर्भाशय ग्रीवा स्ट्रोमा को शामिल करने के लिए टुकड़ा पर्याप्त आकार का होना चाहिए, जो आक्रमण की डिग्री निर्धारित करने के लिए आवश्यक है
सर्वाइकल कोन बायोप्सी का उपयोग आक्रमण की प्रारंभिक डिग्री के लिए या घाव की गहराई को स्पष्ट करने के लिए किया जाता है
. हिस्टोलॉजिकल रूप से पुष्टि किए गए आक्रामक गर्भाशय ग्रीवा कैंसर के लिए पूर्व-उपचार परीक्षण का उद्देश्य प्रसार के ज्ञात मार्गों (प्रत्यक्ष प्रसार, लिम्फ नोड भागीदारी या हेमटोजेनस प्रसार) की जांच करना है।
अनिवार्य अध्ययन
छाती के अंगों का एक्स-रे
अंतःशिरा पाइलोग्राफी
सिंचाई
एनेस्थीसिया के तहत सिस्टोस्कोपी और सिग्मायोडोस्कोपी
वैकल्पिक अध्ययन में सीटी, एमआरआई, लिम्फैंगियोग्राफी और फाइन नीडल ट्यूमर बायोप्सी शामिल हैं।
क्रमानुसार रोग का निदान
. गंभीर गर्भाशयग्रीवाशोथ
. सरवाइकल पॉलिप
. एंडोमेट्रियल कैंसर गर्भाशय ग्रीवा तक फैल गया
. कोरियोकार्सिनोमा सहित मेटास्टैटिक घाव।
इलाज
प्रबंधन रणनीति रोगी की उम्र, सामान्य स्थिति और कैंसर के नैदानिक चरण पर निर्भर करती है।
डिसप्लेसिया और कार्सिनोमा इन सीटू का उपचार शल्य चिकित्सा द्वारा किया जाता है।
चरण IA में
सूक्ष्म आक्रमण (1 मिमी तक) के साथ, युवा महिलाएं व्यापक और उच्च संकरण कर सकती हैं
3 मिमी (टी1 ए 1) तक के आक्रमण के लिए - हिस्टेरेक्टॉमी (45 वर्ष तक - बिना उपांग के)
3-5 मिमी (टी1ए2) के आक्रमण के साथ - उपांगों के साथ गर्भाशय का विस्तारित विलोपन
50 वर्ष से अधिक की आयु में, जब गर्भाशय ग्रीवा नहर में स्थानीयकरण होता है, तो एक सामान्य एनाप्लास्टिक प्रकार, गर्भाशय फाइब्रॉएड या उपांगों के ट्यूमर के साथ मिलकर, पिछले ऑपरेशन के बाद पुनरावृत्ति, हिस्टेरेक्टॉमी का संकेत दिया जाता है। यदि सर्जरी के लिए मतभेद हैं, तो इंट्राकैवेटरी रेडिएशन थेरेपी की जाती है।
आईबी-आईआईए चरणों में, प्रजनन आयु की महिलाएं संयुक्त उपचार (वर्टहाइम ऑपरेशन और विकिरण चिकित्सा) से गुजरती हैं।
चरण IIB और अधिक में, साथ ही कम आम ट्यूमर और सर्जरी के लिए मतभेदों की उपस्थिति में, पसंद की विधि संयुक्त विकिरण चिकित्सा है।
पॉलीकेमोथेरेपी चरण IV (विकिरण चिकित्सा के समानांतर) में रोगियों के उपचार को पूरक बनाती है।
पुनरावृत्ति
यदि प्रक्रिया स्थानीयकृत है, तो आंशिक या पूर्ण पैल्विक प्रवेश किया जाता है (गर्भाशय, गर्भाशय ग्रीवा, योनि, पैरामीट्रियम, मूत्राशय और मलाशय के एक ब्लॉक को हटाना)
दूर के मेटास्टेस की उपस्थिति में, रोगियों को आमतौर पर कीमोथेरेपी प्राप्त होती है। दर्दनाक मेटास्टेस के उपशामक उपचार के लिए विकिरण चिकित्सा का उपयोग किया जा सकता है।
दवाई से उपचार
विकिरण चिकित्सा के प्रभाव को बढ़ाने के लिए
फ्लूरोरासिल
हाइड्रोक्सीयूरिया
सिस्प्लैटिन
पुनरावृत्ति और मेटास्टेसिस के लिए
bleomycin
एटोपोसाइड
सिस्प्लैटिन या कार्बोप्लाटिन
Ifosfamide
मतली और उल्टी की रोकथाम और राहत के लिए - ओन्डान-सेट्रॉन, मेटोक्लोप्रामाइड।
अवलोकन
. उपचार के दौरान, शारीरिक परीक्षण और पैप स्मीयर
. उपचार के बाद - पैल्विक अंगों की जांच करने और पैप स्मीयर लेने के लिए समय-समय पर डॉक्टर के पास जाना; अध्ययनों में छाती का एक्स-रे और अंतःशिरा पाइलोग्राफी भी शामिल है
पहले वर्ष के दौरान - हर 3 महीने में
फिर 5 साल तक - हर 6 महीने में
5 वर्षों के बाद, नियंत्रण प्रतिवर्ष किया जाता है
. संदिग्ध संकेत और लक्षण
गर्भाशय ग्रीवा की पुरानी सूजन
अस्पष्टीकृत वजन घटना
निचले अंग की एक तरफ सूजन
पेट के निचले हिस्से में या कटिस्नायुशूल तंत्रिका के प्रक्षेपण में दर्द
श्लेष्म-खूनी योनि स्राव
प्रगतिशील मूत्रवाहिनी रुकावट
बढ़े हुए सुप्राक्लेविकुलर लिम्फ नोड्स
लगातार खांसी या हेमोप्टाइसिस।
रोकथाम
. पैप स्मीयर जांच
नियमित जांच यौन गतिविधि की शुरुआत के साथ शुरू होनी चाहिए
यदि उच्च जोखिम वाले कारक हैं, तो परीक्षा सालाना आयोजित की जाती है
यदि ट्यूमर विकसित होने का जोखिम कम है और लगातार दो नकारात्मक पैप स्मीयर परिणाम हैं, तो परीक्षण हर 2 साल में किया जा सकता है
. धूम्रपान छोड़ना
. एसटीडी की रोकथाम.
जटिलताओं
. मूत्रमार्ग में फिस्टुला (उपचार के साथ 2% से कम मामले)
. हाइड्रोनफ्रोसिस
. यूरीमिया।
पाठ्यक्रम और पूर्वानुमान
पर्याप्त संयुक्त विकिरण उपचार के साथ, बीमारी के चरण III में भी, 5 साल की जीवित रहने की दर 70% तक है
. स्थानीय रूप से सीमित पुनरावृत्ति। शुरुआत में शल्य चिकित्सा द्वारा इलाज किए गए 25% रोगियों को पेल्विक रेडिएशन थेरेपी से रोग की पुनरावृत्ति से बचाया जा सकता है
मेटास्टैटिक रिलैप्स. इलाज के मामले अत्यंत दुर्लभ हैं, और चिकित्सीय प्रभाव व्यक्तिगत और अल्पकालिक होता है।
सहवर्ती विकृति विज्ञान
. यथास्थान कैंसर और आक्रामक योनि कैंसर
. यथास्थान कैंसर और योनी का आक्रामक कैंसर
. मस्से.
गर्भावस्था के दौरान विशेषताएं. इस स्थान के कैंसर के 1% मामलों में गर्भवती महिलाओं में सर्वाइकल कैंसर होता है
. यथास्थान कैंसर. प्रसव तक उपचार स्थगित कर दिया जाता है (योनि जन्म नहर के माध्यम से किया जा सकता है)
.आक्रामक कैंसर
प्रथम तिमाही - गर्भावस्था की समाप्ति के बाद रैडिकल हिस्टेरेक्टॉमी या विकिरण चिकित्सा
द्वितीय तिमाही - भ्रूण को हिस्टेरोटॉमी द्वारा हटा दिया जाता है, फिर विकिरण चिकित्सा या शल्य चिकित्सा उपचार किया जाता है
तीसरी तिमाही - भ्रूण की व्यवहार्यता प्राप्त होने तक उपचार स्थगित कर दिया जाता है। प्राकृतिक प्रसव निषिद्ध है।
आईसीडी -10
. C53 गर्भाशय ग्रीवा का घातक रसौली
. D06 गर्भाशय ग्रीवा की स्थिति में कार्सिनोमा।
वालेरी ज़ोलोटोव
पढ़ने का समय: 4 मिनट
ए ए
ब्लास्टोमा सभी ट्यूमर का सामान्य नाम है: सौम्य और घातक। हालाँकि, जब हम सर्वाइकल ब्लास्टोमा के बारे में बात करते हैं, तो हमें अक्सर घातक नियोप्लाज्म के बारे में बात करनी पड़ती है। इसलिए, इस लेख में हम गर्भाशय ग्रीवा के ट्यूमर, आईसीडी कोड 10 सी53 पर विचार करेंगे। हम आपको बताएंगे कि यह क्या है, ब्लास्टोमा से कैसे छुटकारा पाया जाए और साथ ही इसकी उपस्थिति को कैसे रोका जाए।
कुछ सामान्य जानकारी
रोगों के अंतर्राष्ट्रीय वर्गीकरण में कोड C53 शामिल है, जिसका अर्थ है गर्भाशय ग्रीवा का घातक नवोप्लाज्म। आंकड़े कहते हैं कि यह महिलाओं में होने वाले सबसे आम कैंसर में से एक है। यह विकृति अक्सर प्रजनन आयु की महिलाओं में होती है। यदि विकास के प्रारंभिक चरण में इस बीमारी का पता चल जाए, तो पूर्वानुमान अनुकूल होगा। अन्यथा, आपको लंबे समय तक महंगे उपचार का सामना करना पड़ेगा।
ट्यूमर की घटना गर्भाशय ग्रीवा में स्थानीयकृत असामान्य कोशिकाओं की उपस्थिति से जुड़ी होती है। प्राकृतिक एंडोमेट्रियल कोशिकाएं नष्ट हो जाती हैं, जिसके परिणामस्वरूप एक घातक ट्यूमर बन जाता है। रोग बहुत तेज़ी से बढ़ता है, पहले आसन्न ऊतकों और अंगों को संक्रमित करता है, और फिर दूर के ऊतकों को संक्रमित करता है। शुरुआती चरण में ट्यूमर स्वास्थ्य के लिए खतरनाक नहीं होता है।
फिलहाल, डॉक्टर सर्वाइकल ब्लास्टोमा के विकास के चार चरणों में अंतर करते हैं। उनमें से प्रत्येक को उपचार के लिए एक विशेष दृष्टिकोण की आवश्यकता होती है और लक्षणों और परिणामों की एक अलग सूची होती है।
- प्रारंभ में, असामान्य कोशिकाओं का एक समूह गर्भाशय के शरीर में स्थानीयकृत होता है, जहां इसका प्राथमिक विकास होता है। इस स्तर पर, अभी तक कोई मेटास्टेस नहीं है, रोगी अच्छा महसूस करता है और उसे यह एहसास भी नहीं होता है कि उसके शरीर में कुछ गड़बड़ है। इस स्तर पर, स्त्री रोग संबंधी परीक्षण और वाद्य परीक्षण के दौरान कैंसर का पता लगाया जाता है।
- दूसरे चरण में, गर्भाशय ग्रीवा में एक घातक नियोप्लाज्म की वृद्धि देखी जा सकती है। अभी भी कोई मेटास्टेस नहीं हैं, लेकिन ट्यूमर लगातार प्रगति कर रहा है और नए क्षेत्रों पर आक्रमण कर रहा है। पहले लक्षण प्रकट हो सकते हैं: दर्द, रक्तस्राव। अक्सर इस स्तर पर रोग लक्षणहीन होता है।
- अब ब्लास्टोमा गर्भाशय से आगे तक फैल जाता है और पेल्विक अंगों और निकटवर्ती लिम्फ नोड्स को प्रभावित करता है। मेटास्टेस आस-पास के अंगों में फैल जाते हैं, और द्वितीयक कैंसरयुक्त ट्यूमर प्रकट होते हैं। इस स्तर पर, उपचार बहुत अधिक जटिल हो जाता है। परिणामी ट्यूमर के साथ-साथ प्रभावित अंगों को हटाना और विकिरण चिकित्सा और कीमोथेरेपी का एक कोर्स करना आवश्यक है।
- चौथे चरण में सबसे खराब पूर्वानुमान है। तथ्य यह है कि ट्यूमर दूर के अंगों तक भी मेटास्टेसिस कर देता है। कभी-कभी ऐसा होता है कि द्वितीयक ट्यूमर महत्वपूर्ण अपूरणीय अंगों को प्रभावित करते हैं, फिर वे निष्क्रिय हो जाते हैं और उपचार रोगसूचक हो जाता है।
ब्लास्टोमा क्यों होता है?
सौम्य और घातक ब्लास्टोमा लगभग एक ही परिदृश्य में उत्पन्न होते हैं। जैसा कि ऊपर उल्लेख किया गया है, असामान्य कोशिकाओं की उपस्थिति को दोष देना है, लेकिन सब कुछ इतना सरल नहीं है। मानव शरीर में प्रतिदिन बड़ी संख्या में उत्परिवर्तनकारी कोशिकाएँ दिखाई देती हैं। सामान्य स्थिति में, प्रतिरक्षा प्रणाली सफलतापूर्वक उनका सामना करती है। हालाँकि, वह उनमें से कुछ को मिस करती है। आधुनिक डॉक्टरों के लिए यह एक वास्तविक रहस्य है। ऐसा क्यों होता है ये आज भी कोई नहीं समझ पा रहा है.
आगे मैं कुछ जोखिम कारकों के बारे में बात करना चाहूंगा। किसी व्यक्ति में ये जितने अधिक होंगे, उसे यह रोग होने की संभावना उतनी ही अधिक होगी। व्यवहार में, यह पता चला है कि 30 से 35 वर्ष की आयु की अधिकांश महिलाएं जोखिम में हैं। लेकिन इसका मतलब यह नहीं है कि वे बर्बाद हो गये हैं. आपको बस अपने स्वास्थ्य के प्रति अधिक चौकस रहने और स्त्री रोग विशेषज्ञ से समय पर जांच कराने की जरूरत है।
अब चलिए जोखिम कारकों पर चलते हैं। यदि आपके पास उनमें से 2 या अधिक हैं, तो आपको सावधान रहने की आवश्यकता है। अपनी जीवनशैली में बदलाव करना या जांच के लिए डॉक्टर के पास जाना उचित हो सकता है।
- बार-बार मासिक धर्म की अनियमितता, लगातार देरी। हार्मोनल बदलाव, एस्ट्रोजन और प्रोजेस्टेरोन के असंतुलन के कारण ओव्यूलेशन में समस्या देखी जाती है। अंडा परिपक्व नहीं होता या निकलता ही नहीं।
- बांझपन.
- कोई बच्चे नहीं। अभ्यास से पता चलता है कि जिन महिलाओं ने कभी बच्चे को जन्म नहीं दिया है उनमें सर्वाइकल कैंसर होने की आशंका अधिक होती है। इसके अलावा, संभावना लगभग 2.5 गुना बढ़ जाती है।
- अत्यधिक लम्बी प्रसव अवधि। यदि मासिक धर्म जल्दी शुरू होता है और देर से समाप्त होता है, तो इसका मतलब प्रजनन अंगों पर गंभीर दीर्घकालिक प्रभाव होता है। जैसा कि ज्ञात है, किसी भी मानव अंग पर लंबे समय तक यांत्रिक प्रभाव से अक्सर ट्यूमर का निर्माण होता है।
- 16 वर्ष की आयु से पहले यौन गतिविधि की शुरुआत।
- अधिक वजन. यहां भी समस्या हार्मोन के उत्पादन में है। डॉक्टरों ने साबित किया है कि वसायुक्त ऊतक एस्ट्रोजेन के बढ़े हुए उत्पादन को बढ़ावा देता है। यह जानना महत्वपूर्ण है कि मानक की थोड़ी सी भी अधिकता से घातक नियोप्लाज्म विकसित होने की संभावना बढ़ जाती है। इस प्रकार, मानक से 10 किलो वजन बढ़ने से संभावना 3 गुना और 25 से 9 गुना बढ़ जाती है!
- एस्ट्रोजेन का उपयोग करके दीर्घकालिक हार्मोनल थेरेपी। जितना अधिक समय लगेगा, बीमारी होने की संभावना उतनी ही अधिक होगी।
- शरीर या गर्भाशय ग्रीवा में सौम्य रसौली की उपस्थिति।
- इंसुलिन निर्भरता के साथ मधुमेह मेलेटस। यह बीमारी शरीर में हार्मोनल असंतुलन का कारण भी बनती है।
- वंशानुगत प्रवृत्ति. यदि आपके करीबी रिश्तेदारों को कभी कैंसर हुआ है, तो आप जोखिम में हैं।
- गर्भाशय में स्थानीयकृत पुरानी सूजन संबंधी बीमारियाँ।
- बुरी आदतें होना. शराब और निकोटीन का शरीर पर गंभीर नकारात्मक प्रभाव पड़ता है और इससे कैंसर होने की संभावना बढ़ सकती है। नशे की लत तो और भी बुरी है. इसके अलावा, ये सभी आदतें आपके स्वास्थ्य के लिए कुछ भी अच्छा नहीं लाएंगी।
- स्वच्छंद यौन जीवन और यौन संचारित रोगों की उपस्थिति।
- परिपक्व उम्र. जैसा कि ऊपर बताया गया है, 30 से 35 वर्ष की महिलाओं में इसकी संभावना बढ़ जाती है।
हम आपको याद दिलाते हैं कि ये सभी कारक मौत की सजा नहीं हैं। उनका मतलब सिर्फ इतना है कि आपको अपने स्वास्थ्य के प्रति अधिक सावधान रहने की जरूरत है। इसके अलावा, इनमें से कई कारक सामान्य रूप से कैंसर के विकास की संभावना को प्रभावित करते हैं, न कि केवल गर्भाशय ग्रीवा में घातक नवोप्लाज्म को।
लक्षण
गर्भाशय ग्रीवा में ट्यूमर का स्थानीयकरण अपने स्वयं के अनूठे लक्षण देता है, इसलिए रोगी के लिए यह पता लगाना काफी आसान है कि समस्या किस अंग में है (सिर्फ पहले चरण में नहीं)। लेकिन संकेत मिलते ही समस्या पर ध्यान देना ज़रूरी है।
जो महिलाएं जोखिम में हैं उन्हें नियमित रूप से स्त्री रोग विशेषज्ञ से मिलना चाहिए। अंगों की नियमित जांच के दौरान, डॉक्टर ट्यूमर की पहचान करने और उसे अधिक विस्तृत अध्ययन के लिए भेजने में सक्षम होता है। इस प्रकार, उपचार के एक छोटे से कोर्स के बाद कैंसरग्रस्त ट्यूमर संभवतः आपको परेशान करना बंद कर देगा।
निम्नलिखित लक्षण सर्वाइकल कैंसर के संभावित निदान का संकेत दे सकते हैं:
- रक्तस्राव मासिक धर्म से जुड़ा नहीं है;
- अत्यंत अप्रिय गंध के साथ अस्वाभाविक निर्वहन;
- रजोनिवृत्ति के बाद रक्त;
- किसी भी संभोग के बाद रक्तस्राव;
- संभोग के दौरान श्रोणि क्षेत्र में दर्द;
- लगातार दर्द जो समय के साथ बढ़ता जाता है;
- मासिक धर्म चक्र में अचानक परिवर्तन;
- शौच और पेशाब की प्रक्रिया में व्यवधान।
उपचार की विशेषताएं
गर्भाशय में ब्लास्टोमा को आमतौर पर शल्य चिकित्सा द्वारा हटा दिया जाता है। हालाँकि, विकल्प हमेशा डॉक्टर के पास रहता है। यह सब रोगी की उम्र और वर्तमान स्थिति पर निर्भर करता है। ट्यूमर का आकार, उसके बढ़ने की डिग्री, रोग की अवस्था, मेटास्टेस का स्थान - सब कुछ उपचार के चुनाव में भूमिका निभाता है। सर्जरी के अलावा, उपचार के अन्य विकल्प भी हैं:
- कीमोथेरेपी;
- विकिरण चिकित्सा;
- इम्यूनोथेरेपी.
बेशक, प्रायोगिक उपचार भी हैं, लेकिन उन्हें इस सूची में शामिल करना जल्दबाजी होगी, क्योंकि उनकी प्रभावशीलता सिद्ध नहीं हुई है।
सर्जरी का मतलब लगभग हमेशा गर्भाशय और उसके उपांगों के साथ ट्यूमर को हटाना होता है। जी हां, एक महिला भविष्य में मां बनने से पूरी तरह वंचित हो जाती है। लेकिन अन्यथा वह एक सामान्य व्यक्ति बनी रहती है और उसी स्तर की गुणवत्ता के साथ जीवन जारी रख सकती है। यह वर्तमान में कैंसर से लड़ने का सबसे अच्छा तरीका है। कुछ मामलों में, आसन्न लिम्फ नोड्स को हटाना भी आवश्यक होता है यदि उनमें घातक नियोप्लाज्म के हिस्से पाए जाते हैं।
सर्जरी के बाद विकिरण चिकित्सा का उपयोग किया जाता है। इसे केवल उन मामलों में टाला जा सकता है जहां प्रारंभिक चरण में ब्लास्टोमा को हटा दिया गया था। विकिरण चिकित्सा को पुनरावृत्ति की संभावना को काफी कम करने के लिए डिज़ाइन किया गया है। विकिरण शरीर के केवल प्रभावित क्षेत्र को ही प्रभावित करता है।
कीमोथेरेपी का उपयोग विकिरण के साथ संयोजन में किया जाता है और यह उसी स्थान पर ट्यूमर के दोबारा उभरने की संभावना को भी कम कर सकता है। किसी भी मामले में, उपचार के दौरान, आपको यह सुनिश्चित करने के लिए नियमित रूप से डॉक्टर के पास जाने की आवश्यकता होगी कि आपका स्वास्थ्य सामान्य है।
|
आंत्र ब्लास्टोमा के लक्षण क्या हैं? (3 मिनट में पढ़ें) |