酢酸が得られる。 酢酸
間違いなく、脂肪族モノゼロ酸に関連する既知の溶媒から最も多用途はすべて既知の酢酸である。 それはまた他の名前を持っています:酢酸エッセンスまたはステンシル酸。 この物質の異なる濃度(3~100%)での安価、そして浄化の安定性、精製のシンプル性は、今日、有機のほとんどの物質を溶解するための特性を持つ最上級で最もよく知られているという事実につながりました。様々な分野では需要が高い起点。
酢酸 したがって、特定の産業におけるその使用の可能性は、濃度の程度によって異なります。 それは食べ物、すなわち、酢(3-15%)、そして技術的なエッセンス(70-80%)と氷(100%)にあります。
世帯レベルでは、一般に食品産業では、低い需要が低い溶液であり、酢酸の割合は約3~15%です。 彼らは完成した皿が多くの製品を風味にするために使用され、缶詰、マリネ、ならびに肉や魚の塩分などに欠かせないことが不可欠です。
テクニカル 酢酸70、購入 通常の食料品店では、食品とは異なり、化学工業では積極的に使用でき、優れた溶剤、化学試薬、例えばアセトンを合成する。
技術的な酢酸本質は、医療(例えばアスピリン)、パルプ、紙(染色およびタイポグラフィ)、ペイントおよびニス、テキスタイル香水、革およびその他の工業分野でよく使用されます。 それは香り物質を接続し、除草剤を生産し、アセテート(合成)繊維を作り出すために使用されます。
医療における酢酸の重要性 医薬品産業 また素晴らしいです。 この物質は多数の薬の不可欠な成分です 薬鉛とアルミニウム塩の酢酸、アセチルサリチル酸の酢酸など。 複合体では、数多くの治療に使用されています 炎症過程 様々な病気、主に睾丸、アルコール中毒、苔癬、放射性炎、多相性関節炎など。
酢酸エッセンス、そして 溶剤646、価格 どちらも小さいです、あなたは家庭用品の店を除くことなく、ほとんど誰でも買うことができます。 インターネットを通して注文して購入するのに十分です。 費用は安くなります。 これは、かなりの体積が必要であり、酢酸が他のもののように働く業界で働く人々にとって特に有益です。 化学溶媒それは多くのゴミのボトルと樽で実装されています。 したがって、すでに、この市場で自分自身をよく証明することができたサプライヤーをすでに購入するのが最善です。
閲覧数:11,857回
コースワーク
"酢酸"
実行された:_____________
______________________
チェック:_____________
______________________
volgograd 2004。
前書き ................................................. ......... 3
1.開口酢酸....................... 5
酢酸の性質...................13
3.酢酸の調製...................... 19
4.酢酸の応用....................... 22
結論............................................................... ..... 26.
使用されている参照のリスト.................. ... 27
前書き
酢酸、CH 3 COOH、無色の可燃性液体、鋭い臭い、水によく溶けない。 それは特徴的な酸味、電流が伝導しています。
酢酸は古代のギリシャ語を知っていた唯一の人でした。 ここからその名前: "OKSOS" - 酸っぱい、酸味。 酢酸 シンプルなビュー 植物と動物性脂肪の不可欠な部分である有機酸。 小さな濃度では、食品や飲料製品に存在し、果物の熟成における代謝過程に参加しています。 酢酸は動物の排出中に、植物によく見られます。 塩および酢酸エステルは酢酸塩と呼ばれる。
酢酸は弱い(解離化 水溶液 部分的にのみ)。 しかしながら、酸性媒体は微生物の寿命活動を抑制するので、酢酸は保存に使用される 食品例えば、マリネの一部として。
酢酸は、アセトアルデヒドの酸化および他の方法、エタノールの食品酢酸酢酸発酵によって得られる。 調味料、マリネ、缶詰食品の製造におけるテーブル酢の形で、溶媒(例えば、酢酸セルロースの製造中)などの薬剤および芳香剤を入手するために使用されます。 酢酸は、生物の多くの代謝過程に関与しています。 これは、ほとんどすべての食品、酸味、酢の主成分に存在する揮発性酸の1つです。
この研究の目的:酢酸の特性、産生および使用を探究する。
タスク この研究:
1.酢酸の開口部の歴史について教える
2.酢酸の性質を研究する
3.酢酸の製造方法を説明してください
4.酢酸の使用の特徴を明らかにする
1.酢酸を開く
酢酸の構造は、この発見がベルゼリウスの電気化学理論の維持まで吹き込みを引き起こしているため、トリクロロ酢酸のデュムの開口部からの化学者に興味があります。 電気陽性および電気陰性に及ぼす後者の分配要素は、深い変化なしに有機物質中の置換の可能性を認識しなかった 化学的特性 、水素(電気陽性の要素)クロロム(エレメント電気陰性)、そして平均的な夕方の観察によると(1839年)、「水素の場所における塩素の導入は変わらない」と判明した。分子の完全な外部特性...「DUMAと不思議」は、単純な体の分子(原子)に起因する極性についての電気化学的見解とアイデアがそのような明確な事実に載っているかどうか、それによってそれらは無条件の信仰の主題と考えることができます。それらは仮説と見なされるべきです、そして、これらの仮説が事実に適しているかどうか?よく知られています。有機化学では、同じ役割が交代の理論によって演奏されます。 同じ名前。 その間、クロロ酢酸塩とアルデヒドのクロロ酢酸塩とアルデヒドの変換に基づいて、およびこれらの場合の場合、すべての水素を主な化学的性質を変えることなくそれに等しい塩素で置換することができる。この物質は、有機化学において保存され、次いで同じ体積の塩素、臭素およびヨウ素を水素の場所に導入するタイプがあることが控除することができる。 これは、代替理論が事実に及び、有機化学において最も鮮やかなものであることを意味します。「スウェーデンのアカデミーの年次報告書(「Jahresberichtなど」、vol.19,1840、p.370 )。Burtsellius通知:「Dumaは、それが有理式C 4 Cl 6 O 3 + H 2 O(現代原子重量を与えた。トリクロロ酢酸は、水で無水物化合物と見なす。)。 この観察は、Les Plus Eclatants de La Chimie校正を獲得するために数えられます。 これはその代替理論の基礎です。 これは、彼の意見では、電気化学理論のチップを...、そしてその間、それがシュウ酸の化合物を持つためにいくらかの異なる方法で書くのはその式であることがわかりました。 それぞれの塩化物、C 2 Cl 6 + C 2 O 4 H 2は、シュウ酸および酸および塩に結合したままである。 したがって、我々は、そのような化合物の自家機を扱っており、その多くは多くの例が知られている。 多くの...シンプルで複雑なラジカルの両方が、それらの酸素含有部分が塩素含有部分との接触を失うことなく、それらの酸素含有部分が塩基との接続に入ることができるという性質を持っています。 この外観は夕暮れには与えられず、経験豊富な検証にさらされていない、そしてその間、それが本当であれば、最も理論的なアイデアを持つ互換性のない新しい教育、互換性が最も理論的な考えで、土壌の足の下から脱出されている。 「列挙」のいくつかの無機化合物、その意見では、クロロ酢酸(塩化クロミ酸無水物)(塩化クロム間にも、Suplornクロムの化合物(未知およびこの時点までにそれらを信じています)無水クロムで:3CrO 2 Cl 2 \u003d CrCl 6 + 2Cro 3)、ブリツェリウスは継続しています。 その中で、カーボンラジカルは酸素と塩素と接続されています。 したがって、半分の酸素が塩素で置換されている、または1原子(分子)のハーフクーラー炭素 - C 2 Cl 6を有するシュウ酸の化合物または1原子(分子)の化合物である。 第1の仮定は、塩素11/2の置換の可能性を可能にするので、(ベータシュソル酸によればC 2 O 3であった)。 DUMASでは、塩素が酸素で置き換えられず、電気陽性水素を形成する2つの前述の前述の2つのビューを完全に互換性があります。そして、Wからの特性に従って酸セーリングを与えるために3つの酸素原子を有することが可能であるが、比較から分かるように、それはそれから非常に優れている限り。酢酸およびトリクロロ酢酸の様々な構成は、その記事Gerar(「ジャー」、「PROG.F.PR.CH」に関して、その中で彼によって行われたコメント(「Jahresb」、19,1840,558)からのコメントから明らかである。 XIV、17):「Gerard、彼は言う、アルコール、エーテルおよびそれらの誘導体の組成を新たに表現した。 それは以下の通りである:既知のクロム、酸素および塩素化合物は式\u003d CRO 2 Cl 2を有する、塩素はそれに酸素原子を置き換える(無水クロム - CrO 3のベルゼリウス1の酸素原子によって意味する)。 W.酸C4H6 + 30は、シュウ酸の2原子(分子)を包含し、そのうち1つの酸素は水素\u003d C 2 O 3 + C 2 H 6で置換されている。 そして、そのようなゲームは37ページを満たしていました。 しかし、来年の夕暮れ、タイプの概念を発展させる、特性の特性の非常に題、トリクロロ酢酸の非常に題名と言えば、彼はそれらの化学的性質の同一性を意味し、例えばの類似的なものであることを示した。アルカリの影響下では、C 2 H 3 O 2 K + KOH \u003d CH 4+ K 2 CO 8およびC 2 Cl 3 O 2 K + KOH \u003d CHCl 3 + K 2 CO 3が同じ機械的タイプの代表であるため、C 2 H 3 O 2 K + K 2 CO 8およびC 2 Cl 3 O 2 K + KOH \u003d CHCl 3 + K 2 CO 8。 一方、LubihとGremisは、Malagetti、およびBritzeliusによって得られたクロロ産生普通エーテルと成形およびUの酸のエーテルを考慮して、置換理論の土壌で達成されたより簡単なシンプルさを高めて公に話しました。 5番目のEDにおける新しい事実の圧力をもたらす。 彼の「Lehrbuch der Chemie」(序文は1842年11月にマークされています)GERARDについての彼の鋭いレビューを忘れて、次のことを可能にしました:「塩素の影響下での酢酸の変換(テキスト分解)クロロアイド酸(クロロキシャル - クロロキサルス - ブリトゼリウス)はトリクロロ酢酸を求めている。(「Lehrbuch」、5ed。、P.629)。)、酢酸の組成を別の外観に見えるように思われる(酢酸は、Berzeliusアセチル散剤と呼ばれる。なお、塩素化基の複合基がC 2 Cl 6であると結合基(Paarling)がC 2 H 6であるシュウ酸を組み合わせて、酢酸に対する塩素の効果はC 2 Cl 6中のC 2 H 6の変換のみであろう。 。明確で、そのような表現がより正しいかどうかを判断することは不可能です。..しかし、それに注意を払うのは便利です。」
したがって、Berzeliusは、置換が起こる原稿の化学機能を変えることなく塩素による水素の置換の可能性を認めなければならなかった。 彼の景色の付録を他の化合物に止めることなく、私は酢酸のために、そしてその後他の限界のモノ異常酸のために、そしてバルシュリウス(Gerard)の見解と調和したいくつかの事実を見つけました。 KOLBEの作品の初期点は、CS2上のRoyal Vodkaの作用の下でBerzeliusとMarsaによって初期に得られたCCL4SO 2の組成物として機能し、CS2湿式塩素で作用している。 コルベの変換の近く(Kolbe、「Beitrage Znr Kenntniss Der Gepaarten verpanindungen」( "Ann.Ch.U。"、54,1845,145)を参照してください。)この体は現代の言語、無水塩素トリクロロメチルスルホン酸を表すことを表していることを示した。アルカリ特異的酸性酸、CCl3.SO 2(OH)[Clbaが+ C 2 Cl 3 S 2 O 5 - Chlorkohlenunurschwefelsaules](原子重量:H \u003d 2、Cl \u003d 71、Cl \u003d 71、Cl \u003d 71、Cl \u003d 2、Cl \u003d 71、Cl \u003d 71、C \u003d 2、Cl \u003d 71、C \u003d) 12とO \u003d 16;したがって、現代原子量では、亜鉛の影響下では、最初に1つの原子が水素と置き換えられ、酸Cl 2.2(OH)を形成する(Colbet - Wasserhaltige) Britzelius( "Jahresb" 25,1846,91)は、S 2 O 5ジチオン酸とクロロホルミングとの組み合わせでそれを考えるのが正しいことであり、なぜそれはCCL3SO2(OH)をKohlensupercrolurur(C2CL6)を呼び出す(S2O5)。水和物水、いつものように、Burtselliusは考慮されていません。)、そして設定 EMおよび他のもので、Colbe - ChlaralayLunterschwefelsaureの酸CH 2 Cl 2 Cl 2(OH)を形成し、最後に、電流またはカリウムアマルガムを復元すると(反応は、トリクロロ酢酸の減少に溶融物が酢酸の還元に適用される直前である。 。)水素と3つの原子全てを置き換え、メチルスルホン酸を形成します。 CH3.SO 2(OH)[Colbet - Methylunterschwefelsaure]。 葉酢酸を用いたこれらの化合物の類推は不合格的に打撃であった。 実際、次の式で、次のプレートから見た2つの平行な列が得られた:H 2 O + C 2 Cl 6.S 2 O 5 H 2 O + C 2 C 2 Cl 4 S 2 O 5 H 2 O + C 2 H 2 Cl 4.C 2 O 3 H 2 H 2 Cl 4 C 2 O 3 H 2 O + C 2 H 4 Cl 2 S 2 O 5 H 2 O + C 2 H 4 Cl 2 C 2 O 3 H 2 O + C 2 H 6. S 2 O 5 H 2 O + C 2 H 6 C 2 O 3これはColbaから滑らなかった。上 - H 2 O + C 2 Cl 6。 S 2 O 5)クロロ酢酸として知られている塩素除去酸に隣接しています。 液体クロロ - 炭素 - CCl(Cl \u003d 71、C \u003d 12;今我々はC 2 Cl 4を書き込むことである。それが水中で水で水にさらされるならば、彼は塩化ビスマス、塩素アンチモンなどのように、塩素酸素を置換することを期待することができます。 水中の軽量および塩素の作用は、水中の軽および塩素の作用において、C2Cl4の作用において、C2CL4の中で、ヘキサクロロエタンおよびトリクロロ酢酸を含むコレクを受け、そのような式での形質転換を発現させた。曝気した)チューブを透過した)チューブを透過し、CCl 4を作用して形成すると、CS2上のCl 2を加熱した場合、コルベ反応は元素からの酢酸の合成によって最初の時間的であった。)「同時に決定することは困難であり、そしてそれそれを解決するのは難しいです。酸、そしてそれは私のようです(kolbe I. p.186)、仮説の領域から出て、高度の確率を獲得します。 Holohlenoxalaure(Chlorkhhlenoxalsaure、Chlorkhhlenoxalsaureが今やクロロ酢酸を呼び出す)の場合、それはクロロゲン酸の組成と同様の組成を有しています、そしてそれはメチルサービスを満たし、それをメチル粉砕と考える酢酸も考慮しなければなりません。 :C2H6.C2O3(これは外観で、以前のGERARDで表したものです)。 将来的には、限られた情報のために現在、それが現在の情報のおかげで、将来的に数回の有機酸を摂取することは将来強制的ではありません - 我々は仮説的な基を受け入れます... "組み合わされた酸における置換現象、それらは、様々な、おそらく同型化合物が複合群の役割において互いに互いに置き換えることができるという事実において簡単な説明を受けている(ALS Rarlinge、L.PP 187)、必須酸特性を変えることなく本体の概念! "このような検証この外観フランクランドとコルベ憲法にあります:" Ueber Die Chemische憲法Der Sauren Der Reihe(CH2)2no4 under Den Namen "NiCerile" Bekannten VerbinDungen "(" Ann.Chem 。n。 薬品 "、65,1848,288)。系列(CH 2)2 NO 4の全ての酸がメチルキレイ酸のように構築されていることに基づいて(現在はCNH 2 NO 2を書き\u200b\u200b込み、メチルシー酸酸 - 酢酸を呼ぶ)、それらは以下のことに気付く:式H 2 O + H 2 \u003d C 2 O 3がギ酸の合理的組成の真の発現を表す場合、すなわちシュウ酸について考慮されれば、1当量の水素と組み合わされた場合(発現は真実ではない。 Kolbeは2 Nに相当する交差した文字を使用してから、変換を簡単に説明します。 高温 アンモニウム抗酸素酸水性シニル酸中へのアンモニウム抗酸素は、知られており、ドベイヤーはまた、水とシアンに加熱されたときに密着アンモニウムが分解されていることがわかった。 ギ酸中で合成された水素はシアンから結合するという事実によってのみ反応に関与している:アルカリ性の青色の影響からのギ酸の逆形成は、シアナの既知の変換の繰り返し以下のものである。違いのみで、シュウ酸とアンモニアの水に溶解した。 形成時には、シュウ酸を青酸の水素と組み合わせることができる。「ケイアン酸ベンゲン(C6H5CN)は、例えば酸性特性を有しておらず、ケルボールによるとベルリンラザリが形成されていない。フランクランド、塩化塩化塩化塩化塩化塩化塩化塩化物と並行してaGNO 3との反応、およびKolbolおよびFranklandの堆積の正確さは、ニトリル法による合成を証明した(ニトリルで、KCNを含む硫酸の蒸留(DUMASの方法) LEBEDとマラゲット):R. ".SO 3(OH)+ Kcn \u003d R.CN + KHSO 4)酢酸、プロピオン(次にメタアセトン、)およびカプロン酸、次いで、翌年、コレクを施行した。モノアキシャル限界酸の電解質塩およびそのスキームと一致して、酢酸の電解、エタンの教育、髄石酸および水素:H 2 O + C 2 H 6 C 2 O 3 \u003d H 2+、そしてバレアン電解 - オクタンで観察された。コアシン酸と水素:H 2 O + C 8 H 18 C 2 O 3 \u003d H 2+。 しかしながら、水素、すなわち水素、すなわち水素、すなわち水素に接続されている、すなわち水素、すなわちC 4 H 10に接続されていることから、ケルベが予想されることは不可能ではない。しかし、この期待では、酢酸を放棄し、C4H8O4ではなく、C4H8O4ではなく、C4H8O4のためのものではなく、C4H8O4ではないと考えられ、CryoScopic Dataで判断するのはどのような数式でもあると考えています。そして実際、そしてC2H4O2のために、そしてすべての現代の化学教科書に書かれているように。
名前:
酢酸(シノ酸)は脂肪族シリーズの単粒子カルボン酸である。
化学式:
開封履歴:
ワイン(ワイン酢)が形成されたときに形成されるので、酢酸は古代から知られています。
しかし、酢酸の構造と発生の原因、科学者たちは、水素塩素の有機化合物中の経験的な置換則のセンセーション統治の後にのみ興味がありました。 その前に、その理論はJacob Berzeliusによって指名された化学で支配的だった。 それは電気陽性および電気陰性に要素を分散させ、物質の化学構造を変えることなく、それぞれ水素と塩素の置換をそれぞれ完全に検出した。
その仕事では、1839年、スウェーデンのアカデミーのためのDUMAは、有機物質の経験的規則によって処方された最初の原則が統制され、特に酢酸のための報告を提示し、特に無機化学、Isoomorphism、Isomorphism事実は、それがよく知られているように、電気化学理論のないほとんど子音であるため、ガイドスレッドとして機能しています。 有機化学では、同じ役割が取り替えの理論によって演奏されています...そして将来は、両方の見解が同じ理由から従うと同じ名前でまとめることができるという両方の見解がより密接に関係していることを示しています。」
そのような結論に、彼は数歳でした。 DUMAは酢酸の研究から最初の実験を開始し、それを塩素酢酸に変えました。 この反応の水素は、主な化学的性質およびクラスへの物質の比を失うことなく、1:1の比、そして最も重要なことに完全に置き換えられる。 水素ヨウ素およびブロモムの置換を用いたさらなる実験は、これで科学者を最終的に納得させた。
無機化合物と有機化合物の形成との間の根本的な違いについての革命的なことは革命的でした。
しかし、彼の理論を保護するバルトセリウスは、シュウ酸の例とそれが塩化物と配合されたときに得られる塩の例を導き、それは酸性特性の損失を意味します。 それは、塩素含有部分との接触を失うことなく、それらの酸素含有部分を塩基と反応させ、それらを失うことができる有機および無機化合物の両方の例であると主張する。 化学者によると、この態様では、彼の実験で砂丘によって行われた主な省略 彼はこのようによく知られている事実を反論して確認しなかった。
どういうわけか説明した結果、結果によって得られた結果、バートリウスは前述の仮定を与えます: "葉塩塩酢酸、
明らかに、このクラスの化合物に属しています。 その中でカーボンラジカルが接続されています
そして酸素と塩素で。 それは、シュウ酸、で、
塩素、または1原子の化合物で置換されている半酸素
セミコーラーカーボンの1原子(分子)を有するシュウ酸の(分子)
C2CL6。 最初の仮定は許可されているので受け入れません。
塩素11/2、酸素原子の置き換えの可能性(ベルズリウスのオキサールによると
酸はC 2 O 3であった。)。 Dumasはまた、第3のプレゼンテーションを完全に保持しています
塩素が酸素に置き換えられない2つの上記と互換性がありませんが、
電気陽性水素、同じものを有するC 4 Cl 6炭化水素を形成する
c 4 H 6またはアセチルのような複合ラジカルの性質、および3から提案可能
酸素原子は酸を与えるために、Wの特性の特性を有するものであるが、見られるように
比較(彼らの物理的性質)、かなり優秀な」
しかし、砂漠に置かれた種子は彼らの芽を与えました。 今、多くの科学者たちはバルシェリウスの理論から継続的なイノベーションの理論を奪います。 そのため、ラジカルの理論にもかかわらず、Charles Frederick Gerard(創作者とその機能はバルシュリウスである)は、ラジカルが独立して存在しないが原子基 - 「残基」であることがわかった。 。 1851年の彼のエッセイ「酸の塩基度について」、彼はすべての化学化合物を4種類の水素、塩化物、水およびアンモニアの誘導体として分類することができるタイプの理論を開発した。 特に、トリクロロ酢酸と酢酸の類似性についての考えがあった。 彼の防衛では、Bercelius Parries: "Gerardがアルコール、エーテル、そして彼らの組成を新たに表現しました。
デリバティブ それは以下の通りである:クロム、酸素および塩素の周知の化合物
式\u003d CRO 2 Cl 2、塩素は酸素原子を置き換える(
無水クロム - CrO 3のベルゼリウス1酸素原子)。 W.酸C4H6 + 30
シュウ酸の2原子(分子)が含まれています。
酸素は水素\u003d C 2 O 3 + C 2 H 6に置き換えられます。 しかし、そのようなゲームは理論の権威を保持していませんでしたが、後でDumaは、アルカリの影響下でのトリクロロ酢酸と酢酸の同様の性質を調べる、Dumaはタイプの理論を発展させ、テクロロ酢酸と酢酸の同様の性質を調べます。
その一方で、ルビとグレムは公に話しました
検討中の置換理論の土壌で達成されるより大きな単純さ
antおよびUのクロロ産生普通エーテルおよびエーテル。
マラゲッティ。
第5回edでは、新しい事実の圧力より劣っているブリゼリウス。 彼の
"Lehrbuch der Chemie"(序文は1842年11月にマークされています)、709ページ
gerardについてのあなたの鋭いレビューを忘れて、次のことを可能にしました: "私たちが
変換を(テキスト分解)U。塩素の影響下での酸
クロシャル酸(Chloroschalevaleva - Chloroxalsaure - Burtsellius)
トリクロロ酢酸 、 そうみたいです
u.酸の組成、すなわちそれは、クロロチェル酸中の複合群がC 2 Cl 6であると結合基(Paarling)がC 2 H 6であり、次いで塩素の作用があると、それは複合群(Paarling)がC2H6であると、それは結合されたシュウ酸であり得る。 W.酸はC 2 Cl 6中のC 2 H 6を変換するのであろう。 明確で、そのような表現がより正しいかどうかを決めることは不可能です...しかしそれに注意を払うのは有用です。」
しかし、タイプの理論の支持者の連隊では、すべてが到着しました。 KOLBEの作品の初期点は、CS2上のRoyal Vodkaの作用の下でBerzeliusとMarsaによって初期に得られたCCL4SO 2の組成物として機能し、CS2湿式塩素で作用している。 コレの変換の近くにそれを示した
体は現代の舌、無水塩素を発現する、表現する
トリクロロメチルスルホン酸、CCl 4 SO 2 \u003d CCl 3.2 Cl 3.それぞれの酸 - CCl 3.2(OH)の塩を得ることができるCCl 3.SO 2(OH)、それは亜鉛の影響下で、1つの原子を水素とし、酸Cl 2.2(OH)水和物水を形成する。いつものように、ベゼリウスは受け入れられません
アカウントを考慮に入れる。その後、Acid CH 2 Cl.SO 2(OH)を形成する(Collece -
ChlororelialTerschwefelsaure]、そして最後に、電流またはカリウムを回復するとき
amalgama(機械が溶けに適用される直前の反応
酢酸中のトリクロロ酢酸の修復)水素と全ての全てを置き換える
原子、メチルスルホン酸を形成する。 CH3.SO 2(OH)[コルバの上 -
メチランターシュノーフェルション]。
これらの化合物の葉酢酸との類推
意図せずに目に急いだ。 確かに、次に式、2
次のプレートから見た平行な行:H2O + C2CL6.S2O5
H 2 O + C 2 Cl 6.C 2 O 3 H 2 O + C 2 H 2 Cl 4 S 2 O 5 H 2 O + C 2 H 2 Cl 4 C 2 O 3 H 2 O + C 2 H 4 Cl 2 S 2 O 5
H 2 O + C 2 H 4 Cl 2 C 2 O 3 H 2 O + C 2 H 6.S 2 O 5 H 2 O + C 2 H 6.C 2 O 3これはColbaから脱出していない、
上記の複合硫黄には、注意事項(I.P.181):「
酸および直接クロロ発生剤除草性酸(上)
H 2 O + C 2 Cl 6 S 2 O 5)と呼ばれる名前として知られている塩基酸に隣接して
葉酢酸。 液体クロロゲン - CCL(SL \u003d 71、C \u003d 12;今私達は書く
C 2 Cl 4はクロロエチレンである。)は、知っているように、影響下で光に変わる
塩素B - ヘキサクホルエエタンで、それが水で水で水にさらされた場合、塩化ビスマス、塩素アンチモンなどのように、塩素酸素に代わることが予想されます。 経験は想定を確認しました。
水中にいたC2Cl 4の塩素、Kolbeはヘキサックホルターンで連続していました
そしてトリクロロ酢酸およびそのような式による変換を発現した:( C2Cl 4として
anthearedのチューブを介して送信するときはCCL4から入手でき、CCL4
アクションの下で形成された、CS2上でCL2を加熱したら、その後、コレクの反応が
元素からのu。からの酸の最初の合成)」)」は同時に形成されている
そして遊離ソルバル酸、すぐに塩素があるので、解決するのは困難です
それをuで酸化します。酸」
クロロ酢酸のブリトセルスのレビュー
「素晴らしい方法(AUF Eine Tiberraschende Weise)が確認されています
硫酸を合わせた性質の存在と並列化、そして私のように
そうだ(kolbe i. p. p.186)、仮説の領域から出てくる
高度の確率を取得します。
有機酸のさらなる発見の彼の先見は、実験に頼っている記事によって確認されています。
将来私たちが融合した酸を取るように強制されることは素晴らしいです
現在、その中の有機酸の有意な数
私たちの情報の制限 - 私たちは仮説の根本を受け入れます... "。
彼はまた、ラジカルの理論に特有のもので、以前に発現されたものを追加していることを確認しています。「これらの結合酸の置換現象は、さまざまな、おそらく同型化合物が互いに交換することができるという事実で簡単な説明を受けます。それらと組み合わされた実質的に酸性の特性を変化させない組み合わせグループの役割
この一見のさらなる実験的確認は、フランクランドとコルベの記事にあります。
(CH 2)2 NO 4、メチルチン酸のように構築された(今我々はCNH 2 NO 2を書くと
メチルチシン酸 - 酢酸を呼び出します。 B.
彼が連絡するという事実によってのみ反応に関与するギ酸水素
菌株はシニル酸を形成する:からのギ酸の反対の形成
アルカリの影響下でのシニルは繰り返しのものに他なりません
シュウ酸およびアンモニア中の水シアナに溶解した既知の変換
違いだけで。 形成時にシュウ酸を組み合わせた
青酸の水素」
例えばフェレント上でのベンゼンシアン化ベンゼン(C 6 H 5 CN)が酸性特性を有さず、ベルリンラジウムが形成されないことは、KolbeおよびFanchandaによれば、エチルの塩化塩化塩化塩化物の不適合と並行してAgNO 3と並行して行うことができる。そして、彼らのガイダンスコルベIの正確さ。
フランクランドはニトリルの方法による合成を証明した(ニトリルが得られた
kCNを用いた硫酸の蒸留(LEBEDを用いたDUMAおよびMALAGETTI法):
R ".SO 3(OH)+ KCN \u003d R.cn + KHSO 4)U.、Propionova(次にメタアセトン、)および
カプロン酸。
その後、翌年、Kolbe露出アルカリ性電解を露出しました
単一の限界酸の塩およびそれらのスキームに従って、観察された
これは、酢酸の電気分解、エタン、亜亜酸の形成および
水素:
H 2 O + C 2 H 6.C 2 O 3 \u003d H 2 +
そして、バレリアン - オクタン酸、炭酸および水素の電気分解:H 2 O + C 8 H 18 C 2 O 3 \u003d H 2+。
酢酸の周りの構造の仕事、そして同時に
他の有機酸は最後にその後の化学者の役割によって明らかにされた。
理論的考察とGERARDの権威のために、部門のみを推進しています。
半分座式の半分に、それらを構造的な景色の言語に翻訳すること。
c 2 H 6 C 2 O 4 H 2式がCH 3 CO(OH)に変わったため。
取得方法
酢酸を製造するための主な技術的方法は、マンガン触媒の存在下での空気酸素のアセトアルデヒドの酸化である。
アセトアルデヒド酢酸
化学的特性:
インタラクション:
金属
酢酸マグネシウム
応用:
酢酸は業界で広く使用されています。
- 肉と魚の製品を缶詰
- 合成(アセテート)繊維の製造、
- 除草剤の製造、
- 香り物質および溶媒の合成、
- 革、繊維、その他の業界では、
- 広く使用されている酢酸塩 - 酢酸塩。
コースワーク
話題になっている:
"酢酸"
実行された:_____________
______________________
チェック:_____________
______________________
volgograd 2004。
前書き ................................................. ......... 3
1.開口酢酸....................... 5
酢酸の性質...................13
3.酢酸の調製...................... 19
4.酢酸の応用....................... 22
結論............................................................... ..... 26.
使用されている参照のリスト.................. ... 27
前書き
酢酸、CH 3 COOH、無色の可燃性液体、鋭い臭い、水によく溶けない。 それは特徴的な酸味、電流が伝導しています。
酢酸は古代のギリシャ語を知っていた唯一の人でした。 ここからその名前: "OKSOS" - 酸っぱい、酸味。 酢酸は最も単純な形態の有機酸であり、これは植物および動物性脂肪の不可欠な部分である。 小さな濃度では、食品や飲料製品に存在し、果物の熟成における代謝過程に参加しています。 酢酸は動物の排出中に、植物によく見られます。 塩および酢酸エステルは酢酸塩と呼ばれる。
酢酸は弱い(部分的にのみ水溶液中で解離する)。 しかしながら、酸性媒体は微生物の寿命活動を抑制するので、酢酸は、例えばマリネの一部として食品を保存する際に使用される。
酢酸は、アセトアルデヒドの酸化および他の方法、エタノールの食品酢酸酢酸発酵によって得られる。 調味料、マリネ、缶詰食品の製造におけるテーブル酢の形で、溶媒(例えば、酢酸セルロースの製造中)などの薬剤および芳香剤を入手するために使用されます。 酢酸は、生物の多くの代謝過程に関与しています。 これは、ほとんどすべての食品、酸味、酢の主成分に存在する揮発性酸の1つです。
この研究の目的:酢酸の特性、産生および使用を探究する。
この研究の課題:
1.酢酸の開口部の歴史について教える
2.酢酸の性質を研究する
3.酢酸の製造方法を説明してください
4.酢酸の使用の特徴を明らかにする
1.酢酸を開く
酢酸の構造は、この発見がベルゼリウスの電気化学理論の維持まで吹き込みを引き起こしているため、トリクロロ酢酸のデュムの開口部からの化学者に興味があります。 電気陽性および電気陰性に及ぼす要素の分配要素は、それらの化学的性質の深い変化、塩素(元素電気陰性要素)、そしてその間、砂の観察によって、有機物質中での置換の可能性を認識しなかった。 「水素の場所での塩素の導入は分子の完全な外部的な特性を変えない」「なぜ「なぜDuma and Wonders」が極性の視点とアイデアが起因するかどうかを「水素の完全に外部的に変化させない」と判明しました。単純な体の分子(原子)には、それらが無条件の信仰の主題と見なされることができれば、彼らが仮説と見なされるべきであるならば、これらの仮説は適切な事実のための仮説ですか?...認識されるべきです、それは続くべきですそれが異なるということ。無機化学、同型性、理論に基づく、事実に基づく、電気化学理論ではほとんど子音が少ない。有機化学物質では そして同じ役割は交換の理論によって再生されます...そして将来は両方の見解が同じ理由から従うことを彼ら自身の間でより密接に関連していることを示すでしょう。 その間、クロロ酢酸塩とアルデヒドのクロロ酢酸塩とアルデヒドの変換に基づいて、およびこれらの場合の場合、すべての水素を主な化学的性質を変えることなくそれに等しい塩素で置換することができる。この物質は、有機化学において保存され、次いで同じ体積の塩素、臭素およびヨウ素を水素の場所に導入するタイプがあることが控除することができる。 これは、代替理論が事実に及び、有機化学において最も鮮やかなものであることを意味します。「スウェーデンのアカデミーの年次報告書(「Jahresberichtなど」、vol.19,1840、p.370 )。Burtsellius通知:「Dumaは、それが有理式C 4 Cl 6 O 3 + H 2 O(現代原子重量を与えた。トリクロロ酢酸は、水で無水物化合物と見なす。)。 この観察は、Les Plus Eclatants de La Chimie校正を獲得するために数えられます。 これはその代替理論の基礎です。 これは、彼の意見では、電気化学理論のチップを...、そしてその間、それがシュウ酸の化合物を持つためにいくらかの異なる方法で書くのはその式であることがわかりました。 それぞれの塩化物、C 2 Cl 6 + C 2 O 4 H 2は、シュウ酸および酸および塩に結合したままである。 したがって、我々は、そのような化合物の自家機を扱っており、その多くは多くの例が知られている。 多くの...シンプルで複雑なラジカルの両方が、それらの酸素含有部分が塩素含有部分との接触を失うことなく、それらの酸素含有部分が塩基との接続に入ることができるという性質を持っています。 この外観は夕暮れには与えられず、経験豊富な検証にさらされていない、そしてその間、それが本当であれば、最も理論的なアイデアを持つ互換性のない新しい教育、互換性が最も理論的な考えで、土壌の足の下から脱出されている。 「列挙」のいくつかの無機化合物、その意見では、クロロ酢酸(塩化クロミ酸無水物)(塩化クロム間にも、Suplornクロムの化合物(未知およびこの時点までにそれらを信じています)無水クロムで:3CrO 2 Cl 2 \u003d CrCl 6 + 2Cro 3)、ブリツェリウスは継続しています。 その中で、カーボンラジカルは酸素と塩素と接続されています。 したがって、半分の酸素が塩素で置換されている、または1原子(分子)のハーフクーラー炭素 - C 2 Cl 6を有するシュウ酸の化合物または1原子(分子)の化合物である。 第1の仮定は、塩素11/2の置換の可能性を可能にするので、(ベータシュソル酸によればC 2 O 3であった)。 DUMASでは、塩素が酸素で置き換えられず、電気陽性水素を形成する2つの前述の前述の2つのビューを完全に互換性があります。そして、Wからの特性に従って酸セーリングを与えるために3つの酸素原子を有することが可能であるが、比較から分かるように、それはそれから非常に優れている限り。酢酸およびトリクロロ酢酸の様々な構成は、その記事Gerar(「ジャー」、「PROG.F.PR.CH」に関して、その中で彼によって行われたコメント(「Jahresb」、19,1840,558)からのコメントから明らかである。 XIV、17):「Gerard、彼は言う、アルコール、エーテルおよびそれらの誘導体の組成を新たに表現した。 それは以下の通りである:既知のクロム、酸素および塩素化合物は式\u003d CRO 2 Cl 2を有する、塩素はそれに酸素原子を置き換える(無水クロム - CrO 3のベルゼリウス1の酸素原子によって意味する)。 W.酸C4H6 + 30は、シュウ酸の2原子(分子)を包含し、そのうち1つの酸素は水素\u003d C 2 O 3 + C 2 H 6で置換されている。 そして、そのようなゲームは37ページを満たしていました。 しかし、来年の夕暮れ、タイプの概念を発展させる、特性の特性の非常に題、トリクロロ酢酸の非常に題名と言えば、彼はそれらの化学的性質の同一性を意味し、例えばの類似的なものであることを示した。アルカリの影響下では、C 2 H 3 O 2 K + KOH \u003d CH 4+ K 2 CO 8およびC 2 Cl 3 O 2 K + KOH \u003d CHCl 3 + K 2 CO 3が同じ機械的タイプの代表であるため、C 2 H 3 O 2 K + K 2 CO 8およびC 2 Cl 3 O 2 K + KOH \u003d CHCl 3 + K 2 CO 8。 一方、LubihとGremisは、Malagetti、およびBritzeliusによって得られたクロロ産生普通エーテルと成形およびUの酸のエーテルを考慮して、置換理論の土壌で達成されたより簡単なシンプルさを高めて公に話しました。 5番目のEDにおける新しい事実の圧力をもたらす。 彼の「Lehrbuch der Chemie」(序文は1842年11月にマークされています)GERARDについての彼の鋭いレビューを忘れて、次のことを可能にしました:「塩素の影響下での酢酸の変換(テキスト分解)クロロアイド酸(クロロキシャル - クロロキサルス - ブリトゼリウス)はトリクロロ酢酸を求めている。(「Lehrbuch」、5ed。、P.629)。)、酢酸の組成を別の外観に見えるように思われる(酢酸は、Berzeliusアセチル散剤と呼ばれる。なお、塩素化基の複合基がC 2 Cl 6であると結合基(Paarling)がC 2 H 6であるシュウ酸を組み合わせて、酢酸に対する塩素の効果はC 2 Cl 6中のC 2 H 6の変換のみであろう。 。明確で、そのような表現がより正しいかどうかを判断することは不可能です。..しかし、それに注意を払うのは便利です。」
したがって、Berzeliusは、置換が起こる原稿の化学機能を変えることなく塩素による水素の置換の可能性を認めなければならなかった。 彼の景色の付録を他の化合物に止めることなく、私は酢酸のために、そしてその後他の限界のモノ異常酸のために、そしてバルシュリウス(Gerard)の見解と調和したいくつかの事実を見つけました。 KOLBEの作品の初期点は、CS2上のRoyal Vodkaの作用の下でBerzeliusとMarsaによって初期に得られたCCL4SO 2の組成物として機能し、CS2湿式塩素で作用している。 コルベの変換の近く(Kolbe、「Beitrage Znr Kenntniss Der Gepaarten verpanindungen」( "Ann.Ch.U。"、54,1845,145)を参照してください。)この体は現代の言語、無水塩素トリクロロメチルスルホン酸を表すことを表していることを示した。アルカリ特異的酸性酸、CCl3.SO 2(OH)[Clbaが+ C 2 Cl 3 S 2 O 5 - Chlorkohlenunurschwefelsaules](原子重量:H \u003d 2、Cl \u003d 71、Cl \u003d 71、Cl \u003d 71、Cl \u003d 2、Cl \u003d 71、Cl \u003d 71、C \u003d 2、Cl \u003d 71、C \u003d) 12とO \u003d 16;したがって、現代原子量では、亜鉛の影響下では、最初に1つの原子が水素と置き換えられ、酸Cl 2.2(OH)を形成する(Colbet - Wasserhaltige) Britzelius( "Jahresb" 25,1846,91)は、S 2 O 5ジチオン酸とクロロホルミングとの組み合わせでそれを考えるのが正しいことであり、なぜそれはCCL3SO2(OH)をKohlensupercrolurur(C2CL6)を呼び出す(S2O5)。水和物水、いつものように、Burtselliusは考慮されていません。)、そして設定 EMおよび他のもので、Colbe - ChlaralayLunterschwefelsaureの酸CH 2 Cl 2 Cl 2(OH)を形成し、最後に、電流またはカリウムアマルガムを復元すると(反応は、トリクロロ酢酸の減少に溶融物が酢酸の還元に適用される直前である。 。)水素と3つの原子全てを置き換え、メチルスルホン酸を形成します。 CH3.SO 2(OH)[Colbet - Methylunterschwefelsaure]。 葉酢酸を用いたこれらの化合物の類推は不合格的に打撃であった。 実際、次の式で、次のプレートから見た2つの平行な列が得られた:H 2 O + C 2 Cl 6.S 2 O 5 H 2 O + C 2 C 2 Cl 4 S 2 O 5 H 2 O + C 2 H 2 Cl 4.C 2 O 3 H 2 H 2 Cl 4 C 2 O 3 H 2 O + C 2 H 4 Cl 2 S 2 O 5 H 2 O + C 2 H 4 Cl 2 C 2 O 3 H 2 O + C 2 H 6. S 2 O 5 H 2 O + C 2 H 6 C 2 O 3これはColbaから滑らなかった。これは、上記の合成硫酸に上記および直接クロロ - 炭素および酸に直接含んでいる(P.181)。上 - H 2 O + C 2 Cl 6。 S 2 O 5)クロロ酢酸として知られている塩素除去酸に隣接しています。 液体クロロ - 炭素 - CCl(Cl \u003d 71、C \u003d 12;今我々はC 2 Cl 4を書き込むことである。それが水中で水で水にさらされるならば、彼は塩化ビスマス、塩素アンチモンなどのように、塩素酸素を置換することを期待することができます。 水中の軽量および塩素の作用は、水中の軽および塩素の作用において、C2Cl4の作用において、C2CL4の中で、ヘキサクロロエタンおよびトリクロロ酢酸を含むコレクを受け、そのような式での形質転換を発現させた:(C 2 Cl 4はCCL 4から得ることができるので曝気した)チューブを透過した)チューブを透過し、CCl 4を作用して形成すると、CS2上のCl 2を加熱した場合、コルベ反応は元素からの酢酸の合成によって最初の時間的であった。)「同時に決定することは困難であり、そしてそれそれを解決するのは難しいです、塩素は直ちに酢酸中でそれを酸化するので、「クロロ酢酸上のバルセリウムの見方」と驚くべき方法(Auf Eine Tiberraschende Weise)が硫酸の組み合わせの特性の存在と並列性によって確認されます。酸、そしてそれは私のようです(kolbe I. p.186)、仮説の領域から出て、高度の確率を獲得します。 Holohlenoxalaure(Chlorkhhlenoxalsaure、Chlorkhhlenoxalsaureが今やクロロ酢酸を呼び出す)の場合、それはクロロゲン酸の組成と同様の組成を有しています、そしてそれはメチルサービスを満たし、それをメチル粉砕と考える酢酸も考慮しなければなりません。 :C2H6.C2O3(これは外観で、以前のGERARDで表したものです)。 将来的には、限られた情報のために現在、それが現在の情報のおかげで、将来的に数回の有機酸を摂取することは将来強制的ではありません。組み合わされた酸における置換現象、それらは、様々な、おそらく同型化合物が複合群の役割において互いに互いに置き換えることができるという事実において簡単な説明を受けている(ALS Rarlinge、L.PP 187)、必須酸特性を変えることなく本体の概念! "このような検証この外観フランクランドとコルベ憲法にあります:" Ueber Die Chemische憲法Der Sauren Der Reihe(CH2)2no4 under Den Namen "NiCerile" Bekannten VerbinDungen "(" Ann.Chem 。n。 薬品 "、65,1848,288)。系列(CH 2)2 NO 4の全ての酸がメチルキレイ酸のように構築されていることに基づいて(現在はCNH 2 NO 2を書き\u200b\u200b込み、メチルシー酸酸 - 酢酸を呼ぶ)、それらは以下のことに気付く:式H 2 O + H 2 \u003d C 2 O 3がギ酸の合理的組成の真の発現を表す場合、すなわちシュウ酸について考慮されれば、1当量の水素と組み合わされた場合(発現は真実ではない。 KOLBEは2Nに相当する交差した文字を使用して、それは高温のシニル酸への高温での変換によって簡単に説明され、それが知られており、そしてドープレが見つけられることがわかった水とシアンに加熱されたときに播種アンモニウムが分解されること。 ギ酸中で合成された水素はシアンから結合するという事実によってのみ反応に関与している:アルカリ性の青色の影響からのギ酸の逆形成は、シアナの既知の変換の繰り返し以下のものである。違いのみで、シュウ酸とアンモニアの水に溶解した。 形成時には、シュウ酸を青酸の水素と組み合わせることができる。「ケイアン酸ベンゲン(C6H5CN)は、例えば酸性特性を有しておらず、ケルボールによるとベルリンラザリが形成されていない。フランクランド、塩化塩化塩化塩化塩化塩化塩化塩化物と並行してaGNO 3との反応、およびKolbolおよびFranklandの堆積の正確さは、ニトリル法による合成を証明した(ニトリルで、KCNを含む硫酸の蒸留(DUMASの方法) LEBEDとマラゲット):R. ".SO 3(OH)+ Kcn \u003d R.CN + KHSO 4)酢酸、プロピオン(次にメタアセトン、)およびカプロン酸、次いで、翌年、コレクを施行した。モノアキシャル限界酸の電解質塩およびそのスキームと一致して、酢酸の電解、エタンの教育、髄石酸および水素:H 2 O + C 2 H 6 C 2 O 3 \u003d H 2+、そしてバレアン電解 - オクタンで観察された。コアシン酸と水素:H 2 O + C 8 H 18 C 2 O 3 \u003d H 2+。 しかしながら、水素、すなわち水素、すなわち水素、すなわち水素に接続されている、すなわち水素、すなわちC 4 H 10に接続されていることから、ケルベが予想されることは不可能ではない。しかし、この期待では、酢酸を放棄し、C4H8O4ではなく、C4H8O4ではなく、C4H8O4のためのものではなく、C4H8O4ではないと考えられ、CryoScopic Dataで判断するのはどのような数式でもあると考えています。そして実際、そしてC2H4O2のために、そしてすべての現代の化学教科書に書かれているように。
同時に、コレックワークス、そして同時に、他のすべての有機酸が清澄化され、そしてその後の化学者の役割は、理論的考察およびGERARDの権威、半分ZA公式のために分裂にのみ減少した。それらを構造的ビューの言語に変換することで、式C2H6.c 2 O 4 H 2がCH 3 CO(OH)に変わった。
2. 酢酸の性質
カルボン酸は、炭化水素基と関連する1つ以上のカルボキシル基を含有する有機化合物である。
カルボン酸の酸特性は、電子密度のカルボニル酸素への変位、そしてこの追加(アルコールと比較して)によって引き起こされたO - N連絡の偏光によるものである。
水溶液中で、カルボン酸はイオンに解離する。
水中の酸の分子量溶解度が低下すると減少する。
カルボキシル基の数によれば、酸は単粒子(モノカルボン)および多軸(ジカルボン酸、トリカルボキシなど)に分けられる。
炭化水素基の性質によると、酸は区別され、不飽和および芳香族。
系統的酸名は、接尾辞の追加を伴って対応する炭化水素の名前によって与えられます - Comm. そして言葉 酸 。 些細な名前も使用されます。
いくつかの限界モノアイス酸
カルボン酸は高い反応性を示す。 それらは異なる物質と反応し、そして様々な化合物を形成し、その中で非常に重要である 機能的誘導体 。 カルボキシル基の反応の結果として得られた化合物。
2.1塩の形成
a)金属と対話するとき:
2RCOOH +MG®(RCOO)2 mg + H 2
b)金属水酸化物との反応
2RCOOH + NaOH(登録商標)rcoona + H 2 O
カルボン酸の代わりに、それらのハロゲンキズリドがしばしば使用される。
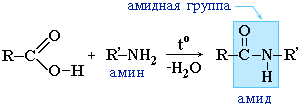 |
アミドは、カルボン酸(それらのハロゲナントリドまたは無水物)の有機アンモニア誘導体(アミン)との相互作用においても形成される。
アミドは本質的に重要な役割を果たしています。 天然ペプチドおよびタンパク質の分子は、アミド基の関与を有するA-アミノ酸から構築されている - ペプチドの結合。
酢酸(エッチング酸)。
式:CH 3 - ゾーム; 鋭い無色の液体が鋭い無色の液体。 氷塊と同様に融点(融点16.6℃)の下に(したがって、濃縮酢酸とも呼ばれる)。 水、エタノールに溶ける。
表1.酢酸の物理的性質
合成食品酢酸は、酢の鋭い臭いを持つ無色、透明な可燃性の液体です。 合成食品酢酸は、ロジウム触媒中のメタノールおよび一酸化炭素から得られる。 合成食品酢酸は、化学的、医薬品および軽産業、ならびに防腐剤としての食品産業において使用されています。 式CH 3 COXY。
合成食品酢酸を濃縮し(99.7%)、水溶液(80%)の形態で製造する。
物理的および化学的な指標では、合成食品酢酸は以下の標準に準拠しなければならない。
表2.基本的な技術要件
| インジケータの名前 | 正当 |
| 外観 | 機械的不純物のない無色の透明な液体 |
| 水溶性 | フル、ソリューションの透明 |
| 3.酢酸の質量分率、%、それほどない | 99,5 |
| 4.酢酸アルデヒドの質量分率、%、それ以上 | 0,004 |
| 5.ギ酸、%、それ以上の質量分率 | 0,05 |
| 6.硫酸塩の質量分率(SO 4)、%、それ以上 | 0,0003 |
| 7.塩化物(Cl)、%、それ以上の質量分率 | 0,0004 |
| 8.硫化水素(PB)により沈殿した重金属の質量分率(PB)、これ以上 | 0,0004 |
| 9.鉄の質量分率(Fe)、%、それ以上 | 0,0004 |
| 10.不揮発性残渣の質量分率、%、それ以上 | 0,004 |
| 11.マンガン固体カリウムの溶液の色の安定性、最小限ではない | 60 |
| 2軸カリウム、CM 3チオ硫酸ナトリウム溶液、濃度C(Na 2 SO 3×5H 2 O)\u003d 0.1mol / dm 3(0.1h)の質量分率 | 5,0 |
合成食品酢酸 - 可燃性液体は、体への衝撃の程度に応じて、第3のハザードクラスの物質を指す。 酢酸を処理するときは適用されるべきです 個人の意味 保護(濾過ガスマスク)。 燃やした最初の援助 - 水で豊富な散水。
合成食品酢酸を純粋な鉄道タンク、ステンレス鋼の内面を持つタンクトラック、コンテナ、コンテナ、ステンレス鋼バレル、最大275 dm 3の容量、キャパシティ付きのガラス瓶およびポリエチレンバレルに注がれます。最大50 dm 3 ポリマー容器は湾の湾と貯蔵に適しています。 合成食品酢酸は密封されたステンレス鋼タンクに貯蔵されています。 容器、容器、樽、ボトルおよびプラスチックフラスコは、保管室に保管されており、キャノピーの下に保管されています。 強化酸化剤(硝酸、硫酸、過マンガン酸カリウムなど)との共貯蔵はできません。
それは上の梅を持つステンレス鋼ブランド12x18h10tまたは10x17h13m 2からなる鉄道タンクで輸送されます。
酢酸の調製
酢酸は、エステル、モノマー(酢酸ビニル)、食品産業などの調製のための産業において広く使用されている最も重要な化学品です。 世界生産は年間500万トンに達します。 最近までの酢酸の調製は石油化学物質原料に基づいていた。 ウォーカープロセスにおいて、穏やかな条件下でのエチレンは、触媒系PDCl 2およびCuCl 2の存在下で空気酸素によってアセトアルデヒドに酸化される。 次に、アセトアルデヒドを酢酸に酸化する。
CH2 \u003d CH2 + 1/2 O2 CH3CHO CH3COOH.
他の方法では、コバルト触媒の存在下で200℃の温度および50気圧の圧力でH-ブタンを酸化することによって酢酸が得られる。
エレガントなウォーカープロセスは、石炭原料の使用に基づく新しい方法によって徐々に交換された石油化学の開発の象徴の1つです。 メタノールから酢酸を得るための方法が開発されました:
CH 3 OH + CO CH 3 COOH.
大きな工業的価値を有するこの反応は、成功を示す優れた例である。 均質触媒作用。 反応の両方の成分は石炭から得ることができるので、石油価格が上昇するにつれてカルボニル化プロセスはより経済的になるはずである。 2つの工業用メタノールカルボニル化プロセスがあります。 BASFで開発された高齢の方法では、コバルト触媒を使用し、反応条件は硬質であった:温度250℃および圧力500-700 ATM。 他の方法では、ロジウム触媒を別の方法で使用し、反応をより低温(150~200℃)および圧力(1~40気圧)で行った。 このプロセスの開口部の歴史。 科学者企業はリフェリリホスフィン触媒を用いた調査を行った。 石油化学部門の技術部長は、メタノールのカルボニル化のために同じ触媒を使用することを提案した。 実験の結果は陰性であることが判明し、これらは金属 - 炭素接続を形成することの難しさに関連していた。 しかし、ヨジスタンメチルの金属錯体の最も簡単な酸化的なアクセシブに関する会社のコンサルタントの講義を覚えておくと、研究者は反応混合物にヨウ素プロモーターを添加し、最初に信じられない鮮やかな結果を受けました。 そのような発見はまた、競合した会社「ユニオンカーバイド」からの科学者によって行われた。 1ヶ月の集中的な仕事におけるメタノールカルボニル化技術のチームは、1970年に15万トンの酢酸が得られたモンサントの工業的プロセスを作成しました。 このプロセスは科学の範囲のハーマーであり、これはC1化学と呼ばれていました。
カルボニル化メカニズムを注意深く調べた。 反応の実施に必要なヨウ素メチルは式によって得られる
CH 3 OH + HI CH 3 I + H 2 O.
触媒サイクルは次のように提示することができる。
平らな錯体 - (i)は、6座標錯体IIの形成を用いてメチルをメチルに結合し、次いでメチル - ロードの導入の結果として、アセチルロディン複合体(III)が形成される。 酢酸無水物の還元除去は触媒を再生し、ヨウダンジドの加水分解は酢酸を生成する。
工業用酢酸合成:
a)ブタンの触媒酸化
2CH 3 -CH 2 -CH 2 -CH 3 + 5 O 2 T 4 CH 3 COOH + 2 H 2 O
b)触媒上の酸化炭素(II)とメタノールの混合物を加熱する
CH 3 OH + CO CH 3 COOH.
酢酸発酵(酢酸発酵)の製造。
原料:エタノール変化液体(ワイン、生まれたジュース)、酸素。
補助物質:酢酸細菌の酵素。
化学反応:エタノールは生体触媒的に酢酸に酸化されている。
CH 2 - CH - He + O 2 CH 2 - SOAM + H 2 O
主な製品:酢酸。
酢酸の適用
酢酸は、調味料、マリネ、缶詰の食品の製造におけるテーブル酢の形で、溶媒として(例えば、酢酸セルロースの産生)として薬剤および香りのある物質を得るために使用される。
酢酸水溶液は、風味および保存手段(食品への調味料、マリネのキノコ、野菜)として使用されます。
酢の組成には、リンゴ、乳製品、アスコルビック、酢酸などの酸が含まれます。
アップルビネガー(4%酢酸)
Apple酢には、酢酸、プロピオン、ミルクなど、20人の最も重要な鉱物とマイクロエレメントが含まれています。 レモン酸多数の酵素およびアミノ酸、じゃばり、ペクチンなどの貴重なバラスト物質。 アップル酢は様々な料理や保存の調製に広く使用されています。 新鮮な野菜や肉や魚の両方、あらゆる種類のサラダと完全に組み合わされています。 それは海洋の肉、きゅうり、キャベツ、ケッパー、標識、トリュフをすることができます。 しかし、西部では、アップルな酢はそのために知られています 医学的特性。 それは血圧、片頭痛、喘息、頭痛、アルコール依存症、めまい、関節炎、腎臓の疾患、高温、火傷、交渉などで使用されています。
健康的な人々は便利でさわやかな飲み物を使うために毎日推薦されます。 りんご酢。 体重を減らすことを望む、私たちは食品の毎回排水の2つのスプーンの廃水を飲みながら推薦します。
酢はさまざまな要塞のマリネの準備のために家庭缶詰に広く使用されています。 at 民間薬 酢は、(3:1の割合で水と酢の溶液で拭くことによって)非特異的解熱剤として使用されています(3:1の割合で)、そして川の方法によって頭痛を伴う。 酢の使用は、圧縮によって昆虫の咬傷に一般的です。
美容学においてアルコール酢を使用することが知られています。 すなわち、化学カールと永久色の後に柔らかさと光沢のある髪を与えること。 このために、アルコール酢(水1リットル当たり - 3~4種類の酢1リットルあたり)で髪をすすぐことが推奨されています。
ビネガーブドウ(4%酢酸)
ブドウ酢はスロベニアだけでなく世界中のリーディングシェフによって広く使用されています。 スロベニアでは、それは伝統的にさまざまな野菜や季節のサラダの調製に使用されています(2-3 TBSP。サラダボウルのスプーン)。 彼は料理のユニークで洗練された味を与えます。 また、ブドウ酢は様々な魚のサラダや海洋製品からの皿と完全に組み合わされています。 様々な品種の肉からケバブを調理するとき、特に豚肉からのぶどうの酢は単に不可欠です。
酢酸は医薬品を製造するためにも使用されます。
錠剤アスピリン(ES)は酢酸エーテルである活性成分アセチルサリチル酸を含む。 サリチル酸.
アセチルサリチル酸 それは、少量の硫酸の存在下でサリチル酸を無水酢酸で加熱することによって(触媒として)製造される。
水溶液中で水酸化ナトリウム(NaOH)で加熱したら、アセチルサリチル酸をサリチル酸ナトリウムおよび酢酸ナトリウムに加水分解する。 培地が酸性化されると、サリチル酸が沈殿し、融点(156~1600℃)によって同定することができる。 加水分解中に形成されたサリチル酸を同定する他の方法は、塩化鉄(FeCl 3)を添加するときにその溶液を暗い紫色に染色している\u200b\u200b。 濾液中に存在する酢酸はエタノールおよび硫酸でエタノールと共に加熱され、それはその特徴的な臭いによって容易に認識され得る。 さらに、アセチルサリチル酸は様々なクロマトグラフィー法を用いて同定することができる。
アセチルサリチル酸は、無色の単斜晶性多面体または針、少し酸味の味を形成して結晶化します。 それらは乾燥空気中で安定であるが、湿った培地中で、サリチル酸および酢酸に徐々に加水分解された(LeesonおよびMattocks、1958; Stempel、1961)。 きれいな物質はほとんど臭いを持っていない白い結晶性粉末です。 酢酸の臭いは、物質が加水分解し始めたことを示しています。 アセチルサリチル酸は、アルカリ水酸化物、アルカリ重炭酸アルカリ性、ならびに沸騰水中のエステル化に曝される。
アセチルサリチル酸は、抗炎症性、解熱防止剤、および痛みを伴う効果を有し、そして発熱状態、頭痛、神経痛などに広く使用されており、そして腫瘍性薬剤としても広く使用されている。
酢酸は化学産業(アセチルセルロースの製造、酢酸繊維、有機ガラス、フィルム;染料、医薬品およびエステルの合成のために)、香水製品の製造において、 、染料の合成中の溶媒、 薬用物質例えばアスピリン。 酢酸塩は植物の害虫と闘うために使用されます。
結論
それで、酢酸(CH 3 COOH)、鮮明な臭いを持つ無色の可燃性液体、水によく溶けない。 それは特徴的な酸味、電流が伝導しています。 業界における酢酸の使用は非常に大きいです。
ロシアで生産された酢酸は最高の世界規格のレベルにあり、世界市場では需要が高く、世界の多くの国に輸出されています。
酢酸の生産は多くの特定の要件を持っているので、専門家は自動化とプロセス管理と議事録の分野だけでなく、この業界の特別な要件も明確に理解しています。
中古文学のリスト
1. Alexander IvanovichのArtemenko。 化学のための参照ガイド/ A. artyomenko、I.V. Tikunova、V.a. 男性。 - 2番目のED。、Pererarab。 そして追加します。 - M。:高等学校、2002年 - 367
2.アッヘメ、ネイルシブガトヴィシです。 一般的および無機化学:スタッドのための教科書。 彼のテーノル。 専門家。 大学/ Akhmetov N.S.-4th Ed。/大学 - M。:高等学校、2002年 - 743 P。
3. Berezin、Boris Dmitrievich。 現代の有機化学の過程:研究。 研究のためのマニュアル 大学、レジャー。 彼の中で - テヘル。 スペック。/ベレジンB.D。、Berezin D. B.-M:高等学校、2001.-768 P。
4. I. G. Bolsheov、G.S. Zaitseva。 カルボン酸およびそれらの誘導体(合成、反応性、有機合成の適用)。 有機化学一般経過における方法論的材料。 問題5. Moscow 1997
Zommer K.化学の電池の知識。 あたり。 彼と。、2番目の編。 - M。:1985年:1985年 - 294 p。
カラカノフE.A. 油の代替物としての合成ガス。 I.フィッシャー - トロプシュプロセスとオキソ合成//シリア教育雑誌。 1997. No. 3. P. 69-74。
Karavaev M.、Leonov E.V.、Popov I.、Shepelev e.t. 合成メタノールの技術 M.、1984. 239 P。
C1化学/ edにおける触媒作用。 母艦隊。 M.、1983. 296 p。
9. Reutov、Oleksandrovich。 有機化学:スタッドのためのチュートリアル。 大学、レジャー。 例えば そして特別な。 「化学」/レートフO.A.、Kurtz A.L。 ブチンk.p.-m:Moscow State University.-21 CH.1.-1999.-560 P.
10.ソビエト百科事典辞書、CH。 ed。 am. Prokhorov - モスクワ、ソビエト百科事典、1989年
ケミストリー:リファレンスガイド、CH。 ed。 n Lieberman - サンクトペテルブルク、出版ハウス「化学」、1975
化学:有機化学:10 Clのための訓練版。 環境 SHK。 - モスクワ、啓発、1993年
化学の雑誌K.知識バッテリー。 あたり。 彼と。、2番目の編。 - M.:1985年。P. 199。
I. G. Bolsheov、G.S. Zaitseva。 カルボン酸およびそれらの誘導体(合成、反応性、有機合成の適用)。 有機化学一般経過における方法論的材料。 問題5. Moscow 1997 P. 23
化学の雑誌K.知識バッテリー。 あたり。 彼と。、2番目の編。 - M:1985年:P. 201
Karakhanov E.A. 油の代替物としての合成ガス。 I.フィッシャー - トロプシュプロセスとオキソ合成//シリア教育雑誌。 1997. No. 3. P. 69
化学の雑誌K.知識バッテリー。 あたり。 彼と。、2番目の編。 - M:1985年。P. 258。
化学の雑誌K.知識バッテリー。 あたり。 彼と。、2番目の編。 - M:1985年:P. 264