骨組織のデンシトメトリーは、骨強度を評価する方法である。 骨のミネラル密度の使い方
診断検索には次のタスクが含まれます。
- 骨減少症(骨密度の低下の症状)の確立とその合併症の特定 - 骨折。
- の代謝率の推定 骨組織 骨吸収および骨形成の生化学的および/または形態学的マーカー、ならびにカルシウム代謝パラメータを研究することによって評価することができる。
- osteopeniaの原因の解明と代謝性骨障害の他の形態との鑑別診断。
骨減少症の局所診断 |
ほぼすべての医療機関で、骨の状態を評価する最もアクセス可能な方法は、 ラジオグラフィー。 しかし、X線撮影では、骨喪失が30%以上の場合にのみ、骨密度を評価することができます。これは、R画像が大幹骨パターンを示し、皮質層が薄くなり、エッジが強調されます。 椎骨における骨粗鬆症は、小柱パターンの変化(椎体の透明度の増加)、関節腔の終板の薄化およびそれらのコントラストの増加によって示される。 骨粗鬆症の進行とともに、小柱パターンは病理学的再編成を受ける:水平骨梁の数が減少する。 主な機械的荷重を支えて、垂直線維柱は持続し、垂直線条を形成する。 いくつかの垂直ビームは厚くなり、水平ビームは完全に消える傾向があります。 骨粗鬆症がさらに進行すると、小柱パターンは見えなくなり、この場合、それは「空の」椎体である。 椎体の変形は、小柱の微小骨折の結果であり、胸椎の下三分の一に発生することが最も多い。 椎体の圧迫骨折の徴候は、その高さの減少、くさびまたは両凹面変形(「魚」脊椎骨)の出現である。 骨盤の骨の検査では、股関節、股関節の頸部および骨盤の骨の変化を評価することができます。
骨粗しょう症 - 骨減少症の初期症状は、日常的な放射線撮影では診断できません。
現在、 早期診断 骨粗鬆症が使用される 様々な方法 骨 デンシトメトリー疾患の発症中の骨密度のダイナミクスまたは治療の有効性を評価するために、既に2〜5%の骨損失を同定することを可能にする。 適用対象:
- 一次元及び二光子デンシトメトリーは、(骨組織に放射性同位体を導入し、それは骨密度に比例する測定同位体分布密度は、このように体積骨密度を算出することにより、放射線により記録されるG \\ cm 3)と
- 1エネルギーおよび2エネルギーのX線吸収測定(骨組織の密度(g / cm 2単位)が測定される)。 二重エネルギー吸光光度法を用いて、軸骨格(腰椎および近位部分)の骨密度を測定する 大腿骨)および周辺領域。
単一エネルギー吸光光度法は、骨格の1つの部分(より多くの場合、前腕の遠位部分)の骨組織の密度のみを決定することを可能にする。 この方法による研究での放射線負荷は非常に低く、適切な部屋なしで使用することができます。
- Quantitative Computed Tomography - 腰椎の海綿質組織のかさ密度(g / cm 3)を測定することができます。 この方法の主な利点は、スポンジ状およびコンパクトな骨の選択的分析の可能性である。 この方法は、代謝障害を有する肥満患者における椎骨の状態を評価することを可能にする。 動的観察中の高い総放射負荷におけるこの方法の欠点は、周辺骨格の骨を研究することが困難である。
- 超音波濃度測定 - デバイスによっては、超音波伝播速度の種々の骨(脛骨、踵)の状態を評価することを可能にします。
1光子、単一エネルギおよび超音波デンシトメトリーは、骨格の周辺部分を研究することを可能にする。 これらの方法は、骨粗鬆症または予備診断のスクリーニングに最も適している。
二重エネルギーX線吸収測定法(DEPA)は、骨密度測定法の中で「金」標準と考えられている。 この方法は、骨格の任意の部分に、骨減少症および骨粗鬆症(等しい5.2%以上で骨物質の損失)の早期診断を可能にし、またカルシウム塩の含有量を決定するために、脂肪及び 筋肉量 体全体に、動的には、治療の有効性を制御を行使するために、疾患の発症時に骨密度を定量化します。 そのような濃度計のための標準的な(自動)プログラムは、プログラムの腰椎、近位大腿骨、前腕及びプログラム「全身」のためのものです。
しかし、我々は間接的にしか骨の機械的強度を決定し、骨のミネラルの飽和を判断できるように、研究の専門性の高いもの、そのosteodensitometryを覚えておく必要があります。 それ自体で、それは骨格の他の病気を診断する機会はなく、古典的なX線検査のための代替を与えるものではありません。 彼女はBMDとその変化のダイナミクスを評価する。 対照の動的デンシトメトリーは、通常9-12ヶ月後に実施される。
デンシトメトリーのための骨組織部位の選択は、研究の重要なポイントである。 この選択をするには、骨組織には2つの異なる層があることを覚えておく必要があります。 コンパクトな(皮質)層は、骨の強さに主に寄与するが、代謝過程の速度は低いという特徴がある。 対照的に、海綿質(小柱)層は代謝に関して非常に活性であり、性ホルモンの欠乏に反応する。 異なる種類の骨粗鬆症は、これらの2つの層に異なる影響を及ぼすことに留意した。 骨柱状物質の優勢な病変では、閉経後、性腺機能低下症、ステロイド骨粗鬆症が発症する。 皮質物質 - 老人性、甲状腺機能亢進症、副甲状腺機能亢進症、糖尿病性骨粗鬆症。 骨粗鬆症の多くのタイプでは、緩やかな傾向は、周辺に、軸骨格(特に脊椎骨)の骨粗しょう症、骨粗しょう症の最初の徴候を「拡散」があります。 したがって、骨粗鬆症の早期診断の驚異的な価値を考えると、一般に、軸骨格の研究が優先されるべきである。 末梢部(脛骨、踵骨、指の指骨)の研究は、しばしばスクリーニングと呼ばれます。
骨密度の測定は、同時にいくつかの骨で行う必要があります。 時には大腿骨の近位部分では、骨粗鬆症が観察され、腰椎には存在しない。 脊椎自体に骨粗鬆症の異なる状態が存在する可能性がある。 これは、リモデリングスポンジ層の強度は、皮質よりも5倍高く、したがって、骨粗鬆症の治療以前のこれらの領域に現れる効果と他よりもより顕著に変化するという事実にあります。
研究成果の解釈
標準試験を行った後、以下のパラメータユニットに組み込まれた、研究データベースから取得した自動比較結果を作りました。
- 正常ピーク骨量(T-スケール) - 測定された密度の比較は、骨格の領域における骨密度が最大になる年齢の骨密度の平均値を用いて行われる
- 年齢基準(Zスケール) - 患者の年齢に対する骨格のこの部分の骨密度の平均値との比較
両方の場合において、結果は、対応する平均BMD-骨ミネラル密度の百分率として表され、100%または標準偏差単位(SD)として取られる。
比較結果は、年の観測の間およびパーセントの変化率として期間のパーセンテージ変化のダイナミクスに提示されています。
T-基準に従ってWHO推奨によれば、骨減少症または骨粗鬆症の重症度(健常人における最大骨密度に対して)評価されます。
- 骨粗しょう症を開発:若い健康な女性での平均ピーク骨量以下のBMDは、より多くの2,5 SDよりも、骨折があります
- 骨粗鬆症:若年健康な女性の平均ピーク骨量を下回る骨密度が2.5 SD以上
- 低骨量(オステオペニア):若年健康な女性のピーク骨量の平均値から1-2.5SD以内のBMD
- ノルム:健常な若年女性のピーク骨量の平均値から1DD以下のBMD
現代の濃度計で使用される参照曲線において、2SD(Tスケール)の偏差はピーク骨質量の約80%に相当する。
試験で得られた特定のBMD値に関連した骨折リスクの評価
試験で得られた特定のBMD値に関連した骨折リスクの評価
50歳で、次の30年間(80年に達するまで)
| BMD(T-scale)の値は、 | 骨折頻度、% |
| 骨折のリスクは、Tスケールで1回のSD偏差(年平均骨量減少レベル)で2倍増加します。 | |
| 腰椎骨折のリスク | |
| 90%未満 | 最大30% |
| 80%未満 | 最大60% |
| 70%未満 | 最大100% |
| 股関節骨折のリスク | |
| 80%未満 | 最大6% |
| 70%未満 | 最大12% |
| 骨折のリスクを評価する上で重要なその他の要素:骨折の存在。 壊死の椎骨の1つの骨折 - 新しい骨折の確率は5倍増加し、2回の骨折は12倍増加する。 | |
骨粗鬆症および放射線濃度測定データの診断にデータ身体検査、骨代謝、カルシウムfosofrnogo交換のマーカーの生化学的分析と、必要であれば、骨組織の形態学的パラメータを交換すると共に考慮されなければなりません。
骨吸収と骨形成:骨代謝の生化学的マーカーは、骨リモデリングおよび高または低骨代謝回転速度および解離不均衡又はその成分と骨粗しょう症の診断のプロセスの速度を推定するために検討しました。
骨形成マーカー
- 総アルカリホスファターゼ血 [ショー]
アルカリホスファターゼ (APF) - リン酸交換の反応に関与する酵素で、最適pHは8.6~10.1である。
リン酸と有機化合物のエステルの加水分解を触媒する。 ALPの最高濃度は、骨(骨芽細胞)、肝細胞、腎尿細管細胞、腸粘膜および胎盤で見つかりました。
FDAは骨の成長に関連する過程に関与しているため、小児の血清中の活性は成人よりも高い。 血清アルカリホスファターゼ活性の病理学的増加は、主に骨疾患(骨形成)および肝臓(胆管閉塞)に関連する。 未熟児では、積極的な成長期の子供、妊娠(第3期)、APの生理活性が増加する可能性がある。
参考値: (おおよその)
アルカリ性リン濃度の上昇
アルカリ性燐光物質のレベルの低下:
- 遺伝gipofosfatazemiya(血清および骨における通常、非常に低いアルカリホスファターゼ活性の血清中のカルシウムおよびリン濃度の骨石灰化違反により特徴付けられる常染色体劣性障害です。)。
- 骨成長障害(軟骨無形成症、クレチン病、アスコルビン酸欠乏症);
- 甲状腺機能低下症;
- kwashiorkor;
- ダイエット中の亜鉛とマグネシウムの不足。
- エストロゲン、経口避妊薬、ダナゾール、アザチオプリン、クロフィブレート
- アルカリホスファターゼの骨イソ酵素 [ショー]
電気泳動法は、アルカリホスファターゼ(APF)の少なくとも11種のアイソザイムの存在を示しているが、電気泳動は、アルカリホスファターゼのアイソザイムの分離のための臨床診断研究所では一般的に使用されていない。 この目的のために、熱不活性化またはL-フェニルテルラニンおよび尿素の活性の阻害が提案されている。 骨のアイソザイムは熱不活性化に対して最も敏感であり、肝臓アイソザイムは中間の位置を占め、胎盤アイソザイムは最も安定である。 腸および胎盤アイソザイムはL-フェニルアラニンによって阻害されるが、骨および肝臓のイソ酵素はこのアミノ酸に対して事実上感受性ではない。 肝臓および腎臓のFDAは尿素によって強く不活性化されるが、この効果は骨の鉱物組織に対する尿素の作用と比較してそれほど顕著ではなく、これはほとんど完全に阻害される。 尿素は胎盤性ホスファターゼに対する弱い阻害効果を有し、腸粘膜からのアルカリホスファターゼの活性に影響しない。
参考値: (おおよその)
大人:
- アルカリホスファターゼの骨イソ酵素20〜120U / l
- 肝臓イソ酵素20-130U / l
- 腸のアイソザイム0-18U / l
骨のアイソザイムの活性の増加
- パジェット病
- 骨のがん
肝臓アイソザイムの活性の増加
- 原発性および続発性肝腫瘍
- 肝胆汁うっ滞
腸のアイソザイムの活性の増加
- 肝硬変
- オステオカルシン(骨芽細胞により合成されたglaprotein) [ショー]
最も重要な非コラーゲンマトリックス骨タンパク質
オステオカルシン (オステオカルシン、GLAタンパク質) - カルシウムとヒドロキシアパタイトの結合に関与する主な非コラーゲン骨タンパク質。 これは、骨芽細胞および象牙芽細胞によって合成され、49個のアミノ酸からなる。 分子量は約5800Dである。これはγ-カルボキシグルタミン酸の3残基を含む。
オステオカルシン(OK)は、骨組織代謝の感受性マーカーである。 血液中のその濃度は、血液のオステオカルシンが新しい合成の結果であり、骨吸収時の放出ではないため、骨組織の骨芽細胞の代謝活性を反映する。
オステオカルシンは再吸収プロセスの調節に関与すると推定される。 高レベルのオステオカルシンでは、骨吸収が高い。 これは、骨代謝のレベルの指標であり、骨疾患の増加の予測可能な指標でもあります。
オステオカルシンは、ビタミンK依存性タンパク質である。 さらに、カルシトニン、副甲状腺ホルモン、ビタミンD、および骨芽細胞の活性を変化させる他の調節因子であるカルシウム調節ホルモンによって、その合成に対する直接の影響がもたらされる。
若年成人で破骨細胞によって合成されたオステオブラストンの90%以上および成人で約70%が骨基質に含まれ、残りは血流に入る。 OCのこの割合は、骨の代謝異常の性質に依存して変化し得る。
腎臓による血流からOK(腎尿細管における糸球体濾過および分解を介して)、したがって血液中のレベルは腎臓の機能状態に依存する。 血液中のOKレベルは、日々の大きな変動の影響を受けます。
診断に加えて、骨粗鬆症患者の再吸収治療を監視するために使用されます。 オステオカルシンは尿中のDPIDと同時に測定することをお勧めします。
参考値: (おおよその)
オステオカルシンのレベルを上げる:
- 閉経後の骨粗鬆症;
- 骨軟化症;
- 原発性および二次性副甲状腺機能亢進症;
- パジェット病;
- 腎性骨ジストロフィー;
- 腫瘍、骨転移;
- 拡散毒性甲状腺腫;
- 青少年の急速な成長;
- 慢性腎不全
注目してください! 糸球体ろ過の著しい減少、特に慢性のものでは 腎不全血液中のOKレベルが高すぎる可能性があります。 循環プロテアーゼの影響下での血管床における部分的破壊または骨吸収中の破壊の結果としての血流中のOC断片の存在は、OKの決定において過大評価されることもある。
オステオカルシンのレベルを下げる:
- 大食症(病気およびItenko-Cushing症候群);
- グルココルチコイドホルモンによる治療;
- 副甲状腺機能低下症;
- 原発性胆汁性肝硬変;
- 妊娠;
- ソマトトロピン欠乏症
- 1型コラーゲンのプロペプチド(P1NP) [ショー]
骨の有機マトリックス(ベース)は、線維芽細胞および骨芽細胞によって合成された1型プロコラーゲンから形成される主に1型コラーゲンである。 コラーゲン1の形成およびその骨基質への取り込みの間、N末端プロセルゲンプロペプチドは、細胞間の空間および血流中に放出される。
したがって、P1NPは、骨形成の活性を反映するマーカーの1つである。 血流に入るP1NP(全P1NP)は、三次元構造を有していてもよいが、速やかに単量体画分に分解する。
参考値: (おおよその)
14歳以上の女性:8〜80 ng / ml;
- 18〜23歳:40.5〜107.4ng / ml;
- 24〜30年:22.5〜120ng / ml;
- 30年以上:10.2〜95.0ng / ml
値の増加:
- 骨粗鬆症(小);
- 老人性骨粗鬆症(小);
- 骨軟化症;
- 不完全な骨形成;
- パジェット病;
- 腎性骨ジストロフィ(小);
- 骨組織の転移病変
骨再吸収のマーカー
- オキシプロリン、ヒドロキシプロリン尿
- 酸酒石酸耐性ホスファターゼの活性
- コラーゲンピリジノリン、デオキシピリジノリン(DPID)分解物、 [ショー]
主な材料は、骨のコラーゲン架橋である。
これは、安定化に大きな役割を果たし、個々のコラーゲン分子間の骨コラーゲン架橋、を特徴とし、デオキシピリジノリン(リジルピリジノリ、DPID)およびピリジノリン(oksilizilpiridinolina PID)として提示しました。 クロスリンクは、マトリックス中のコラーゲン分子の沈着後に細胞外に形成される。 デオキシピリドノリンは、成熟コラーゲンに固有の十字形のピリジン結合であり、さらなる代謝変化を受けない。
骨からの血管チャネルへのDPIDおよびPIDの出力は、破骨細胞によるその破壊(再吸収)の結果として起こる - コラーゲンの破壊である。
骨に最も特有のものはDPIDであり、それは主に骨に存在し、象牙質、大動脈および靭帯の中の少量にしか見られないからである。 骨に加えて、PIDもまた、軟骨に十分な量で見出される。 骨では、骨のDPIDとPIDは4:1の比率です。
DPIDおよびPIDは尿中で遊離形態(約40%)およびペプチド関連形態(60%)で排泄される。 骨組織は絶えず密接に関連し、ホルモン調節の対象とされている合成および再吸収のプロセスが起こっている(副甲状腺ホルモン、カルシトニン、ビタミンD、甲状腺ホルモン、成長ホルモン、ホルモンおよびグルココルチコイドらが。)。 骨基質の特異的分解産物の測定は、骨代謝の速度を特徴付ける。 病理学的状態では、これらのプロセスは切断され、再吸収が形成を超えた場合、骨損失が観察される。 DPIDおよびPIDは現在、骨再吸収のための最も適切な(特にDPID)マーカーであると考えられている。
小児におけるPIDおよびDPIDのレベルは、骨代謝の割合が高いため、成人よりも有意に高い。 閉経後の女性では、骨吸収の増加および骨組織の構造の変化を特徴とする閉経後の骨粗鬆症は、エストロゲンレベルの低下の結果としてしばしば発症し、骨折の可能性を増加させる。 この状態は、DPIDの排泄の増加と相関する。 食物と共に摂取されたDPIDおよびPIDは腸内で吸収されないので、食餌の性質はDPID排泄の大きさに影響を及ぼさない。
参照値 (成人):
- 19歳以上の女性:クレアチニン3.0〜7.4nmol DPID /モル;
- 19歳以上の男性:2.3〜5.4nmol DPID /クレアチニン1モル
DPIDのレベルの増加:
- 副甲状腺機能亢進症;
- 甲状腺機能亢進症;
- パジェット病;
- 骨粗鬆症;
- 変形性関節症;
- 関節リウマチ
DPIDレベルの低下: これらの疾患および症候群の成功した治療
- 空腹時尿中のN末端テロペプチド(PINP)
- 血液中のI型コラーゲンのC末端テロペプチド(PICP、Beta-Cross laps) [ショー]
骨吸収のマーカー。
血清のb-クロスラップは、骨の有機マトリックスの90%以上である1型コラーゲンの分解産物である。 通常分解されて形成されるコラーゲンの小さな断片が血液に入り、尿とともに腎臓から排泄されます。 それらの濃度は概日リズムであり、最大値は真夜中に観察される。
生理的または病理学的に増加した骨吸収(例えば、老齢または骨粗鬆症の結果として)では、1型コラーゲンの分解速度がそれぞれ増加し、血清中のその断片の含量が増加する。
C末端テロペプチドに含まれるアルファ - アスパラギン酸はベータ型に変換される(b-CTx、b-CrossLaps)。
これらの異性化テロペプチドは、1型コラーゲンの特異的分解産物であり、そのレベルは骨吸収の増加した患者において増加する。 それらは骨組織にのみ特異的である。 血液中のそれらの定義は、さらなる異化作用を受けないので、重要な利点を有する。
このテロペプチドの定義は、骨粗鬆症治療の有効性の診断および制御に用いられ、 関節リウマチ、パジェット病、代謝性骨障害、多発性骨髄腫および副甲状腺機能亢進症が挙げられる。
骨吸収を阻害することを目的とした治療の背景において、血清中のb-CrossLapsのレベルは徐々に正常に回復する(数週間以内ではない)。 骨吸収(状態の副甲状腺機能亢進症、甲状腺機能亢進症)のレベルに影響を与えるさまざまな臨床状況は、研究の結果に影響を与える可能性があることに注意してください。
腎機能障害を有する患者では、血清中のb-CrossLapsは排泄の減少により増加する。
参考値:
- 55歳未満の女性:0.573ng / ml未満; 55歳以上:1.008ng / ml未満;
- 50歳未満の男性:0.580ng / ml未満; 50〜70歳:0.700ng / ml未満; 70歳以上:0.854ng / ml未満
値の増加:
- 副甲状腺機能亢進症;
- 骨粗鬆症;
- パジェット病;
- 閉経;
- 関節リウマチ;
- 腎不全
骨吸収の最も有益なマーカーは、デオキシピリジノリン(DPID)およびテロペプチドである。
その他の研究
- 決意インジケータカルシウム - リン代謝(総カルシウム、イオン化カルシウム、クレアチニン排泄への血液およびカルシウム排泄相対リン)。 閉経後の骨粗しょう症では、尿中の尿中排泄が増加するだけです。 血液中のカルシウムとリンの含有量は有益ではありません。
原因不明の骨粗しょう症のプロセスでは、腸骨翅の頂部からの骨組織の生検が鑑別診断において重要な役割を果たす。 それはあなたがOPや骨軟化症だけでなく、骨病態の他のタイプを区別することができ、組織形態計測研究生検は、骨組織における交流の種類を指定します。
主に骨軟化症で行う二次OPの発達によって特徴付けられる疾患の非存在下での主要ODの鑑別診断は、骨原発性副甲状腺機能亢進症、パジェット病、骨粗鬆症形態多発性骨髄腫および骨転移を形成します。
骨粗しょう症の診断手技
| 必須 | 追加 |
| 性行為および身体検査 | 血清および尿中の骨組織の代謝マーカー |
ID:2014-06-6-A-4022
原著(自由構造)
Yusupov KS、Anisimova EA、Anisimov DI
ロシア保健省のFBU「Saratov NIITO」、 ГБОУВПО«サラトフ州立医療大学は、名前を付けられました。 V.I. Razumovsky "ロシア保健省
要約
ゴール:electroneuromyographic displaticheskomのcoxarthrosis様々な重症度で骨密度と性能の指標を識別します。 メソッド。 デンシトメトリー、電気的ニューロマイクログラフパラメータの決定。 結果。 骨密度の減少と形成異常の重症度の間には直接的な相関はなかった。 DKA患者の下肢の削減electroneuromyographicパフォーマンス末梢神経は、大腿骨と脛骨のレベルではなく、脊髄神経根のレベルだけでなく、神経幹の病変を示しています。
キーワード
異形成性共凝塊症、骨ミネラル密度、電気的神経心理学的パラメータ
記事
K.S. ユスポフ - FBU "Saratov NIITO"、ロシア保健省、外傷専門医 - 整形外科医。 E.A. アニシモワ - サラトフ州立医科大学。 V.I. ロシアの保健省の「Razumovsky」、 D.I. アニシモフ - FBU "Saratov NIITO"、ロシア保健省、外傷専門医 - 整形外科医。
はじめに。 形成異常性共凝塊症 - 先天性欠損による継続的進行性疾患 結合組織 そして、寛骨臼の発現変形及び近位大腿骨はdiskongruentnostiおよび生体力学的関節不良につながるで股関節の発育不全。 これは、30歳以上の人を中心とした二次的な関節症の発症をもたらすのは、関節表面の解剖学的および生体力学的障害である。
Crowe et al。 (1979)は、大腿骨の頭部の頭蓋骨の変位レベルの評価に基づく分類を提案し、4つのタイプを含む。 著者らは、正常のレントゲン写真 股関節の ヘッドの高さが骨盤の高さの20%であるように下図の境界と首における大腿骨頭の遷移の場所を引き裂くが同じレベルです。 一方、タイプIII、ヘッド高さの50から75パーセント、または骨盤の高さの10〜15% - - オフセット・クロウ近位ヘッドによってタイプにI II型と、骨盤の高さヘッドの高さの50%まで又は10%までであり、75から100パーセントまたは15- 20%であった。
IV型クロウは、骨盤の高さの100%以上または20%以上の近位頭部変位を特徴とする。 デジタルパラメータのおかげで、クロウの分類が明確で曖昧であるが、それは完全に寛骨臼補綴コンポーネントのインストールを計画する上で重要である異形成の程度に応じて寛骨臼に変化を考慮に入れていません(図1、2)。
図1 1.股関節の骨要素の正常な関係と比較したCrowe I-IV型による異形成性共凝塊の分類のスキーム
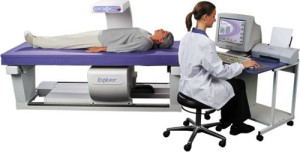
図1 2. Croweによる異形成性共凝塊の分類:a - 裂傷の図形から大腿骨頭の首に接続する場所までの距離B / A<0,1 (менее 10% от высоты таза) - Crowe I; б - расстояние от фигуры слезы до места соединения головки бедра с шейкой 0,1-1,5 (10-15% от высоты таза) - Crowe II; в - расстояние от фигуры слезы до места соединения головки бедра с шейкой B/A≥0,2 (равно или более 20% от высоты таза) - Crowe III-IV
骨密度は、正常なレベルを有することができる、とのデンシトメトリーによって決定されるが、異形成coxarthrosisのより重篤度と骨減少症および骨粗鬆症増加を有する患者の数。
異形成性の異所性関節症の重症度に応じて、電気的ニューログラフィックのパラメータも変化する。
目的:electroneuromyographic displaticheskomのcoxarthrosisが厳しさを変化させながら骨密度と性能のパラメータを決定します。
メソッド。 すべての患者は、分類に応じて異形成coxarthrosis(DKA)の重症度に応じて3つのグループに分け、クロウは、治療を行いました。 ヘッド又は10〜15%の高さの50から75パーセント - 第1グループは、II型と、10%の骨盤の高さに、ヘッド高さの50%まで、または最大オフセット近位ヘッドにDFA I-II型クロウ(タイプIから35人が含まれ 標準的な手順に従って、人工股関節全置換術(TPE)を受け骨盤の高さ)。 グループ2は、によって開発された寛骨臼関節形成術と組み合わせてリング16人の患者及びTPE補強antiprotruzionnyh TICを用いて行ったタイプDFA IIIクロウ(ヘッド変位が75から100パーセントまたは骨盤の高さの15〜20%である)を有する29人の患者から成りました FGBI "SarNIITO" 方法(特許は236918№、PUBL。2010年8月20日)。 著者特許によって開発された二重V字状の転子下骨切り術と組み合わせてTPE - 42人の患者の第三の群は、組み合わされた方法により操作DFA IV型クロウ(骨盤のヘッド100%以上または20%以上の近位変位によって特徴付けられる高さ)を、実施しました。 №2518141、公開。 10.06.14、04.19.13紀要からアプリケーション№2013118381)が16№します。
すべてのグループでの関節内の異形成変化への女性の素因を示し、女性であったことに留意すべきです。
骨密度(BMD)を評価するために、 "ゴールドスタンダード" 二重エネルギーX線吸光光度法(DEXA12.2013グラムまで)X線濃度計«GE LUNAR株式会社»会社プロディジー英国の生産には(REG。数126分の2002、アクション。)特殊なテーブルの上にカドミウム - 亜鉛 - telluridovoy検出器アレイを使用して。 バック回転が15°だけ内側ストップに、(図3)のプログラム「全身」を、近位大腿骨、腰椎で行わBMDの決意 - 研究における患者の位置。

図1 BMD標準ゾーン( - 腰椎、2 - 大腿骨頸部1)の3決意
1回の検査で患者が受けた放射線量は0.05 mSvであった。 結果の比較評価は、性別にピーク骨量のT検定により行った標準(SD)で個体をマッチ:-1SDにT検定 - ノルム。 -1SDから-2.5SD-骨減少症のT検定; T検定は骨粗鬆症-2.5 SD未満です。
すべての患者における術前の期間では(electroneuromyographic)electroneuromyographic行ったとアクセサリーデンマークによって生成電「キーポイント」しっかり「AlpaynBiomedApS」の筋電図検査(EMG)の研究(REG。FS証明書が2009年5月13日の街から2009/04288を№)
両側の研究ENMGプロファイル大腿骨、脛骨および腓骨神経の所見は、F-波L 3 -S 1つの脊髄レベルは、客観的ステートマシン神経筋下肢を評価することを可能と神経生理学的パラメータが標準からの逸脱を識別します。 標準的な放電電極によって記録された誘発された筋肉応答のパラメータを、遠位および近位の点における神経の刺激について評価した。 神経および/または脊髄神経根:それから、年齢規範とのずれの程度は傷害のレベルを決定し、患者の脊髄神経の末梢神経や根のインデックスを比較しました。
患者調査の結果の統計分析は、Microsoft Excel用のAtteStatソフトウェアパッケージを使用して実施した。 統計調査では、以下の作業を設定しました。1.患者と健常人の分析サンプルの指標を比較します。 2.治療前後の患者サンプルのパラメータを比較する。 3.治療の有効性を評価する。 指標の分布の正常性は、Shapiro-Wilk検定およびグラフ分析を用いて決定した。 この問題を解決するために、各試料の容量が100未満であるため、ノンパラメトリックな基準が用いられた。 独立したサンプル間の差は、Mann-Whitney検定を用いて決定した。 患者の治療のダイナミクスにおけるパラメータと治療の有効性の比較は、対比較のWilcoxon T検定を用いて行った。
結果全ての群の患者の49.1パーセントにかかわらず、DFAは、そのような大関節における重い変化さえ存在が実際にBMDの変化の度合い(表1)と相関していないタイプの通常観察パラメータT検定を有していました。
同時に、第2および第3の研究グループには、BMDが減少した多数の患者が存在し、両方のTBSの首にBMDが局所的に減少する。
DKAタイプI-IIクロウを有する患者では、下肢の神経のENMG指数のほとんど全てが年齢基準から著しい偏差を有していた。 従って、形成異常の側TBS振幅M-応答ライン大腿筋は反対側が正常の下限に対応する上で、正常値75.6%の減少であった2.2±0.5 mVのを超えませんでした。 近位セグメント(F-波PLの潜伏期間)のレベルで脈拍数の平均時間は27.7±4.0ミリ秒に対応し、7.9±1.5ミリ秒の値は、対側(表2)を超え。
第1群の患者の大多数 - 27人(77.1%)が腓骨神経の指数に変化を示した。 当事者間のM-反応の振幅の平均値に有意差はなかったが、年齢基準からの有意な減少は55.1%であった。 異形成のTBS側に46.4±1.6メートル/秒に脛骨に低下IPN effの登録されたが、近位セグメントと細根L 5のレベルの病巣脱髄の機能が同定されています。 脊髄運動ニューロンの抗喘息反応は本質的に不規則であった。
脛骨神経の研究にのみ影響を受ける側に、両側の近位セグメントのレベルで遠位セグメント(3.7±0.3秒)のレベルでのパルスのレベルの時間からの有意差を明らかにしました。 22(62.8パーセント)の患者経験豊富な側異形成TBSと反対側の12(34.2パーセント)の患者の運動応答の振幅を減少させます。 7例(20%)の患者では、M-応答は0.9-1.6 mVであり、これはM-応答の振幅が年齢標準に比べて50%低下することを確認した。 両側が20~25%によって大きさが大きい許容値の減少から遠位端と近位M-応答の振幅を比較した場合、即ち 近位セグメントのレベルでは、神経の伝導率はほぼ2倍に低下した。
坐骨神経および/または脊髄S 1のルート上階層および/または局所病変の指標とした、多くの場合、記録された求心性神経伝導脛骨追加、固定波長の研究で。
19.7 26.3ミリ秒の待ち時間で波を記録M-およびF-A-波間の求心性神経伝導の研究でDFA I-IIクロウ型12(34.2パーセント)の患者で。 重要な変更は、脛骨、腓骨、大腿神経の機能の類似した信頼性の高い指標が一つの研究として結果を解釈することが可能となっている、例の患者2番目と3番目のグループで明らかにしました。
すべての観察群の患者における大腿、腓骨および脛骨神経のM-応答の振幅の値の比較を図4に示す。

図1 年齢ノルムのインジケータを有する基の大腿骨、脛骨および腓骨神経1-3患者のM-応答4.比較
群間比較ENMGパラメータ大腿神経は2番目と3番目のグループが観察で平均M-応答直筋サイド異形成TBSグループ1よりも2倍、相対インデックスが減少した大腿ことが明らかになった場合 年齢基準は56.7%であった。 近位セグメントのレベルで患者の2番目と3番目のグループの導電性能は、神経線維の異常興奮ことを示す、高かったです。
両側の2番目と3番目のグループの患者のパフォーマンスelectroneuromyographic腓骨神経を減少し、しかし、彼らはグループ1の患者の研究の結果と同等であり、年齢規範の減少は55.1パーセントでした。 このすべては、腰椎のレベルで、ならびに反対側の代償機構の違反を構成しています。
ほとんどの場合、患者におけるENMGデータ脛骨神経2番目と3番目のグループは正常に対応し、得られたを減少、病理学的プロセスにおいてより少ない関与を特徴付ける、特に側反対TBSに、第1群の患者よりも約2倍高かったです 年齢基準に対する値は最大29.7%であった。
PL F-波ように、近位セグメントで有意に上昇した導電率が登録されENMGパラメータはそれほど深刻な病変根第仙骨脊髄神経(S 1)を示す、第1群に比べ未満4-6ミリ秒でした。
異形成TBSの反対側にこれらの変更の患者の神経生理学的研究第2及び第3グループのグレーター重症度は、神経根病変を有する腰仙脊柱および腰部と臀部の筋肉群でmiofibrozaのセンターの発展の合併症の存在によって説明することができます。
議論。 患者の半数近くは関係なく、全身性疾患として骨粗しょう症についての理論をサポートタイプDFAの通常観察グループBMDの指標を持っていました。 しかし、BMDの減少は、DKAIIIおよびIV型でより一般的である。
A波のelectroneuromyographic-指標を研究する際に、脊髄損傷の脊椎の背景上に、坐骨神経の慢性神経障害を示し、近位筒の圧縮に応じて担保軸索の局所増殖の兆候です。
結論。このように、DKA患者の下肢の初期electroneuromyographicパフォーマンス末梢神経は、大腿部と下腿部のレベルではなく、脊髄神経根のレベルだけでなく、神経幹の病変を示しています。 ロング既存の痛み、身体活動の制限、短縮は腰椎と開発mieloradikulopatyを分娩含む複雑な代償適応メカニズムにつながりました。
神経生理学的モニタリング結果の解析ではDKAの患者の下肢の末梢神経の損傷のほとんどは、二国間の性質のだったし、グループ1の患者においてより顕著であることを明らかにしました。
同時に、長い時間のための反対の四肢への負荷の再配分は、客観的、より重要な病理学的シフトのENMGパラメータ、対患者2番目と3番目のグループを確認したトリガーポイントを形成するために、永続的な神経学的障害およびmiofastsikulyarnyh症候群に貢献しています。
利害の衝突。 作業は、研究FBGU「サラトフNIITO」健康のロシア省のプログラムの一環として行われました。
文学
- 寛骨臼の骨構造の形態および股関節の大腿骨構成要素/ EA Anisimova、K.S. Yusupov、D.I. Anisimov、E.V. Bondareva // Saratov Journal of Medical Scientific Research。 2014. T. 10、No. 1。P. 32-38。
- Rentgenoanatomicheskieと股関節/ KSの異形成脱臼の患者の生体力学的特性 Yusupov、E.A. Anisimova、N.N. Pavlenko [およびその他] // Saratov Journal of Medical Scientific Research。 2014. T. 10、No. 1。P.114-119。
- 異形成性共凝塊症(外科的予防および治療)/А.А. Korzh、E.S. Tikhonenkov、V.A. Andrianov [と他の人]。 M。:Medicine、1986. 108 pp。
- Kadurina TI、Gorbunova VN 結合組織の異形成:手で医師のための、SPbと:。Elsbi-SPbと、2009年722頁
- Loskutov AE、Zub TA、Loskutov OA 成人における異形成異型症の分類について//整形外科、外傷学および補綴学:科学的かつ実践的な雑誌。 №2。P. 83-87。
- Eskelinen A. 55歳未満の患者を対象とした若年患者の股関節全置換術および股関節学的論文の発達性異形成症患者への全股関節形成術。 ヘルシンキ、2006年。128 p。
- Yang S.、Cui Q.発達性股関節形成術における股関節全置換術:解剖学、技術および結果のレビュー//世界矯正医学雑誌。 Vol。 18日 , №3(5)。 P. 42-48。
- Hip / J.F.の先天性転位および異形成の総股関節置換 Crowe、V.J. Mani、C.S. Ranawat // J. Bone Joint Surg。 Amer。 1979年、Vol。 61. P. 15-23。
- Kaznacheeva TV、Osipova AA 現代の骨密度測定方法/ /再生の問題。 2007.№6. 57-61と。
- 人工股関節形成術の有効性に関する生体力学的および神経生理学的評価 Letov、Yu.N. Barabash、D.A. Markov [および他の者] // Tambov大学のBulletin。 シリーズ:自然科学と技術科学。 2012. T. 17、No. 5。P. 1433-1440。
- 人間の骨格に影響を与える重大な疾患。 骨粗鬆症などの診断を確立するには、一つの症状では不十分であるため、追加の検査を行う必要があります。 非常に良い方法は骨密度測定法です。 それはあなたが骨のミネラル密度を測定することができます。 デンシトメトリーの研究は、疾患のタイムリーな検出に貢献し、その発症の程度を評価することを可能にするので、非常に重要である。
デンシトメトリーの種類
- X線タイプの濃度計。 それはいくつかのタイプに分かれています。 二重エネルギー調査があります。 その基礎は、骨によるX線吸収の測定である。 このような解析の結果は、光線がどのように骨を通過するかによって決まります。 それは十分に密である、通路は悪いです。 通常、股関節および椎骨の骨のために、異なる種類の光線が使用される。 X線デンシトメトリー法、すなわちそのパラメータは非常に正確です。 デンシトメトリーの結果は、軟組織と骨による放射線吸収の比較に基づいています。 周辺デンシトメトリーもある。 密度はX線デンシトメトリーと同じ方法で測定されるが、放射線量は小さい。 この方法では、脚と手の骨の石灰化の程度を判断することができます。 しかし、この方法は、股関節および脊椎の骨を研究するためには機能しません。
- 光子吸収測定法。 この場合、骨密度は、骨による放射性同位体の吸収の推定値を用いて測定される。 放出される線量は小さい。 周辺骨の密度を測定するためだけに使用されるモノクロームデンシトメトリーがあります。 二色性の方法に関する分析の結果は、股関節および脊椎の骨の「緩み」の程度を決定することを可能にする。
- 超音波デンシトメトリー。 この検査方法は最も安全であると考えられていますが、その精度は以前に検討された方法ほど高くはありません。 骨部位からの超音波の反射における骨密度の超音波測定方法およびその厚さにおける分散は、基準となる。 超音波法では、骨の弾力性、剛性、密度の程度を理解することができます。 もちろん、X線検査法に劣るが、妊娠中の女性や子供でさえ、一次診断として使用することができる。 さらに、治療療法の有効性を評価するために何度も使用することができます。
超音波検査は、2種類の装置を用いて行われる。 いわゆる乾式濃度計がある。 ゲルは調査中の領域に適用されるが、他の超音波検査で使用されるゲルの他の形態とは異なる。 また、人の手足や彼自身が蒸留水を入れた容器に置かれているときは水分計があります。 それほど前には、2次元スキャナーが登場しましたが、患者の足は液体中にあるべきである一方で、かかとの骨でのみ機能することができます。 これらの技術を使用した分析の結果は非常に正確です。
空間イメージはコンピュータ研究を与える。 これは、海綿質および皮質骨に適用される。 インジケータは平面ではなく容積であるので、解析の結果は真の骨密度である。
メソッド評価
この分析の結果、骨組織のミネラル密度はほとんど測定されないことを理解することが重要です。 ZおよびT基準が評価される。 つまり、一定の規範があり、その偏差は骨粗鬆症の明確な段階と考えられています。
T-基準は、30〜35歳の年齢層の若年女性の平均骨量指数の標準偏差の標準偏差の数である。 年齢が上がると、骨量も正常に減少するので、基準も低下する。
Z-基準は、標準偏差の平均よりも低いまたは高い標準偏差の数であるが、既に平均年齢の患者にある。 この基準は、年齢とともに生じるノルム内の骨密度の減少さえも考慮に入れることを可能にする。

スケジュールによる方法の評価
骨粗鬆症の有無およびその重篤度は、T検定によって決定される。 骨密度の評価は、特に危険因子がある場合は、1年に1回実施することをお勧めします。
分析の可能な指標、すなわち、標準内にあるものと病気の存在について話すものを考慮すれば、 良好な指標 - T検定による骨ピーク質量から-1標準偏差以内。 骨減少症が発症した場合、その程度に応じて、結果は-2.5以下になります。 骨粗鬆症の場合、指標は体重よりも大きい。
この方法を使用する場合
骨組織の骨粗鬆症の有無とその程度を判断する必要がある場合には、分析としての組織骨の骨密度測定法が明らかになった。 この病気を発症する危険性がある人々のグループと、それが現れる可能性のある状況があります。 したがって、以下の場合にデンシトメトリーを行う必要があります。
- 軽度の損傷を伴う骨折;
- 閉経、特に50歳以前に起こった場合;
- グルココルチコイドの受容、全身性エリテマトーデス、血管炎および他のリウマチ性疾患を発症する場合;
- 座っている生活様式。
- あらゆる骨の外傷
禁忌については、私はこの分析をしない絶対的な理由はない、ということをあなたに保証したいと思います。 しかし、妊娠、腰椎脊柱の変化、および授乳に関連する禁忌がある。
研究の原理
この手順は、特別なセンサを備えたX線濃度計を用いて行われる。 体を通過する光線の強度を測定するのはこのセンサーです。 検査の結果は、疾患の存在、すなわち骨の状態を示す。
デンシトメトリーはどのように行われますか? その人は、服を脱がないで広いテーブルに横たわっています。 その上に、比喩的に言えば、2光子濃度測定が行われる場合には、一定の割合で骨格を走査するスクリーンが浮遊する。 単一光子検査が行われる場合、前腕、脛および手のみが走査される。 この手技では痛みは生じません。その結果は非常に正確です。 デンシトメトリーのための特別な準備もありません。
デンシトメトリーは、異なる医療センターで行うことができます。 心配しないでください。これは骨の無害な研究です。 しかし、それは骨疾患の初期段階を特定することができるので、非常に重要です。 これは分析を行うことができません。
検査時 骨密度 (BMD)は、特別なX線、コンピュータ断層撮影(CT)または超音波を使用して、骨のミネラル(例えばカルシウム)の密度を測定します。 この情報(結果)は、骨組織の強度と強度を測定するために使用されます。
年齢とともに、我々はすべて骨量を失う。 骨が自然に薄くなり(骨減少症)、我々が年を重ねるにつれて、既存の骨は新しい骨よりも速く破断する。 これが起こると、私たちの骨量はカルシウムや他のミネラルを失い、より軽く、密度が低く、より多孔性になります。 これは骨を弱くし、骨折する可能性を高めます(骨折(翻訳の前の部分のリンクの翻訳を参照))。
年齢とともに骨量が減少するにつれて、骨減少症は骨粗鬆症につながる可能性があります。 したがって、あなたの骨が太くなればなるほど、骨粗鬆症の過程が長くなります。 骨粗鬆症は男性によって影響を受けることがありますが、この病気は65歳以上の女性に最も一般的です。
あなたの骨密度が通常よりも低い場合は、骨密度を強化し、骨折に曝される可能性を減らす手段を講じることができます。 増加、骨密度及びその強化のいくつかの方法は、(例えば、歩行)重量負荷のために運動して、食品添加物の形態で、カルシウム時間及びビタミンDをマージ含む、(シミュレータに例えば、重量持ち上げる、または演習)をウエイトリフティングと演習 そのような薬剤の受信カルシトニン(Miakaltsin)として、アレンドロネート(フォサマックス)、またはリセドロネート(アクトネル)。 閉経後、女性はホルモン療法を受け、骨密度を増加させることを目的とラロキシフェン(エビスタ)を、受け取ることができます。
BMDを測定するにはいくつかの方法があります。
二重エネルギーX線吸光光度法(DERA)。 BMDを測定する最も正確な方法です。 2つの異なるX線ビームを使用して、背骨および大腿部の骨密度を測定する。 強く密な骨を介して、X線ビームはより少ない程度で通過する。 硬く柔らかい骨組織によってブロックされ、各X線ビームの通過度が互いに比較される。 DERAは年に最大2%の骨量を測定することができます。 このプロセスは迅速に進み、非常に低線量の放射線が使用されるが、依然としてこの検査は超音波検査よりも高価である。 Odnoenergeticheskayaの線吸収(OPA)は、前腕とかかと、OPAでの骨密度を測定するために使用されることはなく、できるだけ頻繁DEXAとして使用することができます。 太ももや背骨のDERA研究の結果の写真を見てください。
末梢二重エネルギーX線吸光光度法(pDERA)。 PEDAはDERA調査の一種である。 それは腕や脚の骨量、例えば手首を測定します。骨や脊椎の骨折の可能性が最も高い骨の密度を測定することはできません。 このデバイスはポータブルであり、医者のオフィスで使用することができます。 PEDAはまた、低線量の放射線を使用し、その結果は標準のDERA調査よりも速い。 pDERAは、骨粗鬆症の治療のために採取された薬剤を、どのように効果的な決定においてDEXAほど有用ではありません。
二光子吸光光度法(DFA)。 この調査では、放射性物質を使用して骨組織の密度を測定しています。 その助けを借りれば、股関節と脊柱のBMDを測定することが可能です。 DFAは非常に低い線量を使用しますが、他の検査方法よりも処理時間が長くかかります。
超音波。 この調査は、通常、問題を確立するために実施されます。 超音波検査の結果が骨組織の密度が低い場合は、DERA検査を受けて結果を確認することを推奨します。 超音波では、いくつかの音波を使用してBMDを測定します。通常はかかとにあります。 一部のデバイスは、空気と一部の水を介して音波を伝導します。 超音波検査は、潜在的に有害なX線放射を使用しない迅速かつ痛みのない手順です。 超音波の欠点の1つは、骨粗鬆症により骨折(大腿骨および脊椎骨折)が最も起こりそうな骨の密度を測定できないことです。 骨粗しょう症を治療する目的で薬がどれほど効果的であるかを見るために使用することはできません。 超音波検査が骨粗鬆症の骨密度を確認する信頼できる方法であるかどうかを調べるために、多くの研究が行われています。
定量的コンピュータ断層撮影(CT)。 これは、背骨(椎骨)の骨密度を測定するCTのタイプの1つです。 CCPの1つのタイプは末梢CCP(PCT)と呼ばれ、通常は手首の腕または脚の骨組織の密度を測定する。 DERA、pDERA、DPAと比較すると、手順が高価で大量の放射線が使用されるだけでなく、結果があまり正確でないため、CCPは通常使用されません。
なぜ?
骨密度(BMD)の検査が推奨される:
60歳以上の閉経後の女性で、骨粗鬆症の危険性がある女性。
すべての女性は65歳以上です。
70歳以上の男性、または骨粗鬆症のリスクがある人。
副甲状腺機能亢進症を有する男性および女性。
プレドニゾンなどの長期間コルチコステロイドを服用している男性および女性。
2年以上治療を受けている男性および女性の骨粗しょう症治療の有効性をコントロールする場合。
準備
金属のボタンやバックルで服を着用しないでください。 離陸して飾る必要があるかもしれません。これは、あなたの手首を調べると、例えば、ブレスレットのような調査を妨げることがあります。
プロセス
骨ミネラル密度検査は、通常、科学技術者が特別な放射線部門または診療所で行う。 末梢二重エネルギーX線吸収(PDERA)装置はポータブルなので、医院で使用することができます。
あなたは柔らかい机の上に背中を伏せる必要があります。 通常、あなたは服を着ることができます。 まっすぐな脚で寝るか、下の脚をテーブルに組み込まれた特別なプラットフォームに下ろす必要があります。
デバイスはあなたのスケルトンをスキャンし、それが吸収する放射線の量を測定します。 太ももと背骨をスキャンするDERAメソッドは約20分かかります。 他の方法には30〜45分かかります。
ポータブルデバイス(pDERA)は、手首または前腕の骨密度を測定することができます。 超音波検査は、通常、かかとに対して行われる。 これらの調査中に、あなたは椅子に座ることができます。
一度に少なくとも2つの異なる骨(好ましくは、股関節および脊柱)の調査がBMDを測定する最も信頼できる方法である。 同じ骨を検査するのが最善であり、同じ調査方法および装置を使用してその後の毎回BMDを測定することが最善である。
感覚
骨密度の検査は無痛です。 背中の痛みがある場合は、検査中にテーブルの上に横たわっているのが不快なことがあります。
リスク
骨密度の検査中、あなたは非常に少量の放射線に曝されます。 BMD検査は、胎児への放射線の影響により妊婦には推奨されません。
結果
BMD(骨密度)を調べるときは、特殊なX線写真、コンピュータ断層撮影(CT)または超音波を使用して、骨のミネラル(例えばカルシウム)の密度を測定します。 結果は、通常、2〜3日間は準備ができています。
骨ミネラル密度の検査の結果は、いくつかのバージョンにすることができます。
Tスコア
あなたのT値は健康な30歳の人の平均と比較してBMDです。 それらは標準偏差(CO)の形で表され、これはグループからの各人の指標がグループの平均指数にどれほど近いかの統計的測定値である。 平均BMDは、30歳の大きなグループ(若年成人の基準値)の骨組織の密度を測定することによって決定される。 BMD値は、この対照群の平均値からの標準偏差として報告される。 ほとんど全ての30歳者は、この平均から2標準偏差以内のBMD値を有する。
マイナス( - )の値は、平均30歳の人よりも骨が薄い(骨密度が低い)ことを意味します。 値が低いほど、平均30歳の人と比較して骨密度が低くなります。
プラス(+)の値は、骨が平均30歳の人よりも厚くて強いことを意味します。
この表には、世界保健機構の骨粗鬆症の定義が含まれており、骨密度のT指数に基づいています。
|
骨組織のミネラル密度 |
|
|
T - インジケータ |
|
|
ノルム: |
若年成人の基準値から-1標準偏差(CO)以上(-1以上) |
|
低骨密度(骨減少症): |
若年成人の基準値(-1〜-2.5)より1〜2.5CO低いところでは、 |
|
骨粗鬆症: |
2.5以上では、COは若年成人の基準値(-2.5以下)より低く、 |
骨密度の検査結果が低い場合:
おそらくあなたは骨粗鬆症を持っています。 医師は通常、骨粗鬆症の診断に最低T値を使用します。 例えば、あなたの背骨のインデックスが-3で、T - ヒップのパラメータが-2、Tならば、骨折の診断に骨の指標が使用されます。
あなたの骨の骨折の可能性は平均以上です。 Tスコアが低いほど、倒れたときや軽いけがのために骨折の可能性が高くなります。 1 COの変化があっても、ここでは骨折のリスクが二倍に増加することを意味します。 たとえば、Tスコアが-1の場合、骨折の可能性は、Tスコアが0の場合の2倍です。
低いBMD値は、以下を含む他の問題によって引き起こされる可能性があります。
特定の薬を服用する。
癌、例えば、多発性骨髄腫。
Itenko-Cushing症候群、甲状腺機能亢進症または副甲状腺機能亢進症。
脊椎の疾患、例えば強直性脊椎炎。
早産の閉経。
ビタミンDの不足、例えば、くる病。
Z - インジケータ
BMDの価値は、あなたの年齢、性別、人種の他の人々の価値と比較することもできます。 これはZ-インジケータと呼ばれます。 あなたの年齢層の平均値からの標準偏差(CO)として表示されます。
マイナス( - )の値は、あなたの骨があなたの年齢のほとんどの人よりも薄い(骨密度が低い)ことを意味します。 値が低いほど、あなたの年齢層の他の人と比べて骨密度が低くなります。
正(+)の値は、あなたの年齢層のほとんどの人よりも太くて強い骨を意味します。
試験にどのような影響を与えますか?
あなたが調査に合格できない理由、または得られた結果の役に立たない理由は次のとおりです。
調査中に適切に対応することはできません。
あなたは過去に骨折していました。 これは、誤った高いBMD値の原因となり得る。
あなたには脊椎の関節炎があります。 この場合、脊椎の関節炎によって引き起こされる変化は、脊椎が骨粗鬆症の測定に適していないという事実に寄与し得る。
太ももや骨折後の再建手術中に金属製のインプラントを埋め込んでいます。
あなたはBMD検査の10日前にバリウムを使ってX線検査を受けました。
何を考えるか
閉経期にあって、骨折のリスクが高い女性。
骨量(骨減少症)や骨粗しょう症による骨折の増加損失を持っている人。
長期のコルチコステロイドを摂取する人々。
2年以上骨粗鬆症治療薬を使用している人。
副甲状腺機能亢進症を有する人々。
専門家は、BMD検査を実施するのが最良である骨について意見を分けた。 ほとんどの場合、下部の背骨または大腿部の骨が検査されます。 これらの骨では、一般に、骨密度の最大の損失が起こり、骨折の影響を最も受けやすい。 手首の骨が検査されることもあります。 超音波は踵骨を測定する。
BMD測定は、調査から得られた情報が治療に関する決定に影響を及ぼす場合にのみ実施すべきである。 BMDは、治療の有効性を判定するために2年に1回以上測定されるべきではない。
骨密度を測定する際のDERAの使用は、二光子吸光光度法(DFA)のような古い方法に取って代わります。
通常のX線では骨の平均損失レベルを検出することはできません。 骨は少なくとも4分の1の質量を失うはずです。そのため、X線で問題が顕著になります。
あなたの骨量の密度が通常よりも低い場合は、シミュレータ上の重みやトレーニングを持ち上げ、運動し、栄養補助食品の形態で、骨密度とカルシウムとビタミンDの受信とその効果を高めるだけでなく、いくつかの薬を受信することができます。
米国では、(骨量の測定の費用をカバーする標準法と呼ばれる)の法律は国家プログラムから利益を得られるの対象となっている人々に骨密度の調査の費用を支払うため高齢者のための無料の医療の状態のプログラムを必要とし、失う危険にさらされています 骨量は、すなわち:
デンシトメトリー、骨折することなく、骨強度、中にあなたのパス「インディアンサマー」のマージンを決定する最も正確な方法。
強度試験。
骨粗鬆症は、私たちはしばしば、高齢者で、年齢に関連した疾患のために取ります。 この妄想はくつろぎます。 しかし、骨の中のカルシウムのすでに30歳店舗が重要最小に達することが50に縮小し始め、そして時間がアクションを取らない場合、それが遅くなります。

骨粗鬆症は治癒可能ですが、初期段階のみです。 それを検出し、X線デンシトメトリーを助ける。
私はテーブルに尋ねる。
この方法は、あなたが迅速、安全かつ正確に骨密度を決定することができます:高いそれは骨折し、より安定した骨です。 「X線」という言葉を恐れている必要はありません。 400倍少ない、通常のX線よりも優れています。 デンシトメーターのオペレーターは特別な保護を使用しません。
あなたは、服を脱いでなくて、あなたの上に長く、幅の広いテーブルの上に横たわっ「スキャン」は、2つの以上の投影で全体の骨格は、二光子デンシトメトリーを行っている場合という特殊な画面を「泳ぎます」。 唯一の骨、前腕とすね、単一光子デンシトメトリー。 これらの部門最初は少ないにおける骨密度 - まずpredpochtitelnee.Naibolshyの関心は、頚椎のミネラル密度及び近位大腿骨上のデータです。
手術は無痛で、予備的な準備は必要ありません。 デンシトメータのオペレータは結果を確定し、結論と写真を引き渡す。 これは通常、リウマチ専門医や整形外科医結果や他の専門家の診断を解釈します。
私たちはあなたを失うことはありません!
デンシトメトリーは、45年後にすべての女性に2年ごとに渡されるべきである。 しかし、唯一の母親(早期閉経を含む)月経障害を持っていない人と明確な低体重に苦しむない人、骨粗しょう症に苦しむしなかったものについては、この規範。 あなたの生活の中でこれらの危険因子が存在している場合は、2人の以上の子を持つ、あるいは逆に、あなたは一度も出産していない、とあなたは骨折があった場合、40年に前に試験に合格します。
あなたの人生で骨折が頻繁に起こった場合は、年齢にかかわらずデンシトメトリーに急いでください。 医師は、同じことを行うことをお勧めしている(気管支喘息、慢性関節リウマチ)の長期的なコルチコステロイドを取ることを余儀なくされている方に、抗凝固剤(ヘパリン)、利尿薬(ヒドロクロロチアジド、フロセミド)および抗痙攣薬(フェノバルビタール)。 男性はまた、骨の強さをチェックするように勧められますが、後で、50年後に。
デンシトメトリーは最小2〜5%の骨損失をも固定することができます。 だから、それはまだ修正することができる場合でも、骨減少症の段階では、一番最初に骨粗しょう症を識別します。
異なる診療所で異なる装置で得られた結果は異なるが、重要ではない。 あなたは骨粗しょう症の治療を受けている場合は、1で骨密度の変化と誤った結果を取得しないように、同様の機器を制御することが望ましいです。 2年ごとにこれもやってください。
患者にはしばしば疑問が生じます。 ここに彼らの答えがあります。
超音波デンシトメトリーで行うことができますか?自分自身を放射線にさらすことはできませんか?
超音波を使用すると、指やかかとの骨の密度を測定するために - 圧入装置では、患者は自分の指を置きます(またはヒールを発生させます)。 しかしこれはあまり有益な研究ではない。 その基づき暫定的な結論を行うことができ、必要に応じて、その後、背骨、腰や全身の完全なX線デンシトメトリーに提出し、正確な診断がなされています。
一部の人々は、完全なX線検査を受けることを好む、それはより信頼性がありますか?
通常のX線検査では、骨密度の30%が失われている病気の段階だけが見えます。 彼は可能性のある合併症を診断するためだけに任命される。 この場合、胸部および腰椎のX線が側方投影に提供される。 骨粗鬆症の早期兆候、彼は検出できません。
血液検査によると、カルシウムの欠乏、ひいては骨粗しょう症のリスクを判断することは可能ですか?
骨粗鬆症は、女性ホルモンエストロゲンの不足に関連している。 しかし、たとえ分析がレベルの低下を示したとしても、これは診断の基礎ではなく、さらなる検討のための言い訳です。 カルシウム含有量の血液検査は、骨粗鬆症とは全く関係ありません。 この病気では、血液中のカルシウムレベルは正常です。 ちょうどそれが骨から洗い流されたという事実のために。 したがって、「骨粗鬆症」の正確な診断を可能にすることができる基礎検査室検査は存在しません。
デンシトメトリーの結果を誰が評価するのですか?
放射線医は写真を分析し、結果を説明する。 リウマチ学者または整形外科医は、検査の結果を評価することができる。
通常、調査の結果には2つの指標が含まれます:TスコアとZスコア。 Tスコアは、あなたの骨組織の密度を、若者の骨密度の参照指標と比較して示します。
正規指数はT(-1)である。 Tの(-2.5)への減少は、骨密度の減少(骨減少症、および骨粗鬆症についてのさらなる減少)を示す。

骨折リスクの程度を評価するためにTスコアも使用される。 Zスコアは、患者の骨量の密度を、対応する年齢群の平均と比較して反映する。 このインジケーターが高すぎるか低すぎる場合は、追加の健康診断が必要であることを示します。
デンシトメトリーの結果が正常であれば、予防的カルシウム摂取は必要ありませんか?
体が主に乳製品から食品からカルシウム(1200mg)を毎日受け取るようにするだけで十分です。 もし何らかの理由でそれを手に入れなければ、さらにカルシウムを服用することができます。