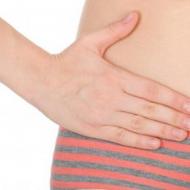
Atsauksmes uz dimia. Dimia asiņošana cikla vidū Sākās menstruācijas no dimia 18 tabletēm
Catad_pgroup Kombinētie perorālie kontracepcijas līdzekļi
Fizioloģiskākais kontracepcijas līdzeklis, kas saglabā dzimumdzīves kvalitāti. Smagas un/vai ilgstošas menstruālās asiņošanas ārstēšanai bez organiskām patoloģijām.
INFORMĀCIJA TIEK STIPRINĀTA
VESELĪBAS APRŪPES PROFESIONĀLIEM
Dimia - oficiālās lietošanas instrukcijas
Reģistrācijas numurs:
LP-001179Zāļu tirdzniecības nosaukums:
Dimia® (Dimia®)Starptautiskais nepatentētais nosaukums:
drospirenons + etinilestradiols (drospirenons + etinilestradiols)Devas forma:
apvalkotās tabletes [komplekts]Savienojums:
uz 1 tableti:
Drospirenona + etinilestradiola tabletes
aktīvā viela: drospirenons 3,000 mg, etinilestradiols 0,020 mg;
Palīgvielas: laktozes monohidrāts, kukurūzas ciete, preželatinizēta kukurūzas ciete, makrogola un polivinilspirta kopolimērs, magnija stearāts.
Plēves korpuss (Opadray II balts*): polivinilspirts, titāna dioksīds, makrogols-3350, talks, sojas lecitīns.
*kods 85G18490
placebo tabletes
mikrokristāliskā celuloze, laktoze, preželatinizēta kukurūzas ciete, magnija stearāts, koloidālais silīcija dioksīds.
Plēves apvalks (Opadry II zaļš**): polivinilspirts, titāna dioksīds, makrogols-3350, talks, indigokarmīns, hinolīna dzeltenā krāsviela, dzelzs oksīda melnā krāsviela; krāso saulainu saulrietu dzeltenā krāsā.
** kods 85F21389
Apraksts:
Drospirenona + etinilestradiola tabletēm:
Apaļas, abpusēji izliektas, baltas vai gandrīz baltas apvalkotās tabletes ar marķējumu "G73" vienā tabletes pusē un iespiests. Šķērsgriezumā kodols ir balts vai gandrīz balts.
Par placebo tabletēm:
Apaļas, abpusēji izliektas, zaļas apvalkotās tabletes. Šķērsgriezumā kodols ir balts vai gandrīz balts.
Farmakoterapeitiskā grupa:
kombinētais kontracepcijas līdzeklis (estrogēns + gestagēns)ATX kods:
G03AA12Farmakoloģiskās īpašības
Farmakodinamika
Dimia® ir kombinēts hormonālais kontracepcijas līdzeklis ar antimineralokortikoīdu un antiandrogēnu iedarbību. Kombinēto perorālo kontracepcijas līdzekļu (COC) kontraceptīvā iedarbība balstās uz dažādu faktoru mijiedarbību, no kuriem svarīgākie ir ovulācijas nomākšana un izmaiņas dzemdes kakla sekrēta īpašībās, kā rezultātā tas kļūst mazāk caurlaidīgs. uz spermatozoīdiem.
Pareizi lietojot, Pērļu indekss (grūtniecību skaits uz 100 sievietēm gadā) ir mazāks par 1. Ja tabletes tiek izlaistas vai lietotas nepareizi, Pērļu indekss var palielināties.
Sievietēm, kuras lieto KPKL, menstruālais cikls kļūst regulārāks, sāpīgas menstruācijas ir retāk sastopamas, samazinās asiņošanas intensitāte, kas samazina anēmijas risku. Turklāt saskaņā ar epidemioloģiskiem pētījumiem KPKL lietošana samazina endometrija vēža un olnīcu vēža attīstības risku.
Dimia® sastāvā esošajam drospirenonam piemīt antimineralokortikoīdu iedarbība. Novērš svara pieaugumu un tūskas parādīšanos, kas saistīta ar estrogēnu izraisītu šķidruma aizturi, kas nodrošina labu zāļu panesamību. Drospirenonam ir pozitīva ietekme uz premenstruālo sindromu (PMS). Ir pierādīts, ka drospirenona/etinilestradiola kombinācija ir klīniski efektīva smaga PMS simptomu mazināšanā, piemēram, smagus psihoemocionālus traucējumus, krūšu pietūkumu, galvassāpes, muskuļu un locītavu sāpes, svara pieaugumu un citus ar menstruālo ciklu saistītus simptomus. Drospirenonam ir arī antiandrogēna iedarbība un tas palīdz mazināt pūtītes (melno punktu), taukainas ādas un matu simptomus. Šī drospirenona darbība ir līdzīga dabiskā progesterona darbībai, ko ražo organisms.
Drospirenonam nav androgēnas, estrogēnas, glikokortikoīdu un antiglikokortikoīdu aktivitātes. Tas viss kopā ar antimineralokortikoīdu un antiandrogēnu iedarbību nodrošina drospirenonam bioķīmisko un farmakoloģisko profilu, kas ir līdzīgs dabiskajam progesteronam.
Kombinācijā ar etinilestradiolu drospirenonam ir labvēlīga ietekme uz lipīdu profilu, ko raksturo augsta blīvuma lipoproteīnu palielināšanās.
Farmakokinētika
Drospirenons
Sūkšana
Lietojot iekšķīgi, drospirenons ātri un gandrīz pilnībā uzsūcas no kuņģa-zarnu trakta. Maksimālā koncentrācija plazmā pēc vienreizējas iekšķīgas lietošanas tiek sasniegta apmēram pēc 1-2 stundām un ir aptuveni 38 ng/ml. Bioloģiskā pieejamība 76-85%. Vienlaicīga lietošana ar pārtiku neietekmē drospirenona biopieejamību.
Izplatīšana
Pēc perorālas lietošanas tiek novērota drospirenona koncentrācijas samazināšanās asins plazmā divfāzu līmenī ar pusperiodiem attiecīgi 1,6 ± 0,7 stundas un 27,0 ± 7,5 stundas Drospirenons saistās ar seruma albumīnu un nesaistās ar dzimumhormonu- saistošo globulīnu (SHBG) vai ar kortikosteroīdus saistošo globulīnu. Tikai 3-5% no kopējās drospirenona koncentrācijas plazmā ir brīvo steroīdu veidā. Etinilestradiola izraisītais SHBG pieaugums neietekmē drospirenona saistīšanos ar plazmas olbaltumvielām. Drospirenona vidējais šķietamais izkliedes tilpums ir 3,7±1,2 l/kg.
Vielmaiņa
Pēc iekšķīgas lietošanas drospirenons tiek plaši metabolizēts. Lielāko daļu metabolītu plazmā veido drospirenona skābās formas. Drospirenons ir arī substrāts oksidatīvajam metabolismam, ko katalizē citohroma P450 izoenzīms CYP3A4.
audzēšana
Drospirenona metaboliskā klīrensa ātrums plazmā ir 1,5±0,2 ml/min/kg. Neizmainīts drospirenons izdalās tikai nelielā daudzumā. Drospirenona metabolīti tiek izvadīti caur zarnām un nierēm proporcijā aptuveni 1,2:1,4. Metabolītu pussabrukšanas periods caur nierēm un caur zarnām ir aptuveni 40 stundas.
Līdzsvara koncentrācija
Cikliskas lietošanas laikā drospirenona maksimālā līdzsvara koncentrācija asins plazmā tiek sasniegta no 7. līdz 14. zāļu lietošanas dienai un ir aptuveni 70 ng / ml. Drospirenona koncentrācija plazmā palielinās apmēram 2-3 reizes (kumulācijas dēļ), ko izraisa terminālā pusperioda un dozēšanas intervāla attiecība. Turpmāka drospirenona koncentrācijas palielināšanās asins plazmā tiek novērota no 1 līdz 6 ievadīšanas cikliem, pēc tam koncentrācijas palielināšanās nav novērota.
Īpašas pacientu grupas
Pacienti ar nieru mazspēju
Drospirenona līdzsvara koncentrācija plazmā sievietēm ar vieglu nieru mazspēju (kreatinīna klīrenss (CC) 50–80 ml/min) bija salīdzināma ar koncentrāciju sievietēm ar normālu nieru darbību (CC>80 ml/min). Sievietēm ar vidēji smagu nieru mazspēju (CC 30-50 ml/min) drospirenona koncentrācija plazmā bija vidēji par 37% augstāka nekā sievietēm ar normālu nieru darbību. Ārstēšana ar drospirenonu bija labi panesama visās grupās. Drospirenonam nebija klīniski nozīmīgas ietekmes uz kālija koncentrāciju asins plazmā. Drospirenona farmakokinētika smagas nieru mazspējas gadījumā nav pētīta.
Pacienti ar aknu mazspēju
Drospirenonu labi panes pacienti ar viegliem vai vidēji smagiem aknu darbības traucējumiem (B klase pēc Child-Pugh). Farmakokinētika smagu aknu darbības traucējumu gadījumā nav pētīta.
Etinilestradiols
Sūkšana
Lietojot iekšķīgi, etinilestradiols uzsūcas ātri un pilnībā. Maksimālā koncentrācija plazmā pēc vienreizējas iekšķīgas lietošanas tiek sasniegta pēc 1-2 stundām un ir aptuveni 88-100 pg/ml. Absolūtā biopieejamība pirmā loka konjugācijas un pirmā loka metabolisma rezultātā ir aptuveni 60%. Vienlaicīga ēdiena uzņemšana samazināja etinilestradiola biopieejamību aptuveni 25% izmeklēto pacientu, savukārt citiem pacientiem šādas izmaiņas netika novērotas.
Izplatīšana
Etinilestradiola koncentrācija asins plazmā samazinās divfāzu fāzē, un terminālajai fāzei raksturīgs aptuveni 24 stundu eliminācijas pusperiods.
Etinilestradiols būtiski, bet nespecifiski, saistās ar seruma albumīnu (apmēram 98,5%) un izraisa SHBG koncentrācijas palielināšanos plazmā. Šķietamais izkliedes tilpums ir aptuveni 5 l/kg.
Vielmaiņa
Etinilestradiols tiek pakļauts nozīmīgam primārajam metabolismam zarnās un aknās. Etinilestradiols un tā oksidētie metabolīti galvenokārt ir konjugēti ar glikuronīdiem vai sulfātiem. Etinilestradiola metaboliskā klīrensa ātrums ir aptuveni 5 ml / min / kg.
audzēšana
Etinilestradiols praktiski neizdalās neizmainītā veidā. Etinilestradiola metabolīti tiek izvadīti caur nierēm un caur zarnām proporcijā 4:6. Metabolītu pusperiods ir aptuveni 24 stundas.
Līdzsvara koncentrācija
Līdzsvara koncentrācijas stāvoklis tiek sasniegts zāļu lietošanas cikla otrajā pusē, un etinilestradiola koncentrācija asins plazmā palielinās apmēram 1,5-2,3 reizes.
Preklīniskie drošības dati
Preklīniskie dati no standarta pētījumiem par atkārtotu devu toksicitāti, kā arī genotoksicitāti, kancerogenitātes potenciālu un toksicitāti reproduktīvajai sistēmai, neliecina par īpašu risku cilvēkiem. Tomēr jāatceras, ka dzimumhormoni var veicināt noteiktu no hormoniem atkarīgu audu un audzēju augšanu.
Lietošanas indikācijas
- Kontracepcija.
- Kontracepcija un mērenu aknes (acne vulgaris) ārstēšana.
- Kontracepcija un smaga premenstruālā sindroma (PMS) ārstēšana.
Kontrindikācijas
Dimia® ir kontrindicēts, ja ir kāds no tālāk uzskaitītajiem stāvokļiem, slimībām/riska faktoriem. Ja kāds no šiem stāvokļiem, slimībām/riska faktoriem pirmo reizi attīstās zāļu lietošanas laikā, zāles nekavējoties jāatceļ:
- tromboze (venoza un arteriāla) un trombembolija šobrīd vai anamnēzē (ieskaitot dziļo vēnu trombozi, plaušu emboliju, miokarda infarktu), smadzeņu asinsrites traucējumi;
- stāvokļi pirms trombozes (ieskaitot pārejošus išēmiskus lēkmes, stenokardiju), pašlaik vai anamnēzē;
- identificēta iegūta vai iedzimta nosliece uz venozo vai arteriālo trombozi, tai skaitā rezistence pret aktivētu proteīnu C, antitrombīna III deficīts, proteīna C deficīts, proteīna S deficīts, hiperhomocisteinēmija, antivielas pret fosfolipīdiem (antivielas pret kardiolipīnu, lupus antikoagulants);
- augsta venozās vai arteriālās trombozes riska klātbūtne (skatīt sadaļu "Īpaši norādījumi");
- migrēna ar fokāliem neiroloģiskiem simptomiem šobrīd vai anamnēzē;
- cukura diabēts ar asinsvadu komplikācijām;
- aknu mazspēja un smaga aknu slimība (pirms aknu funkcionālo testu normalizēšanas);
- aknu audzēji (labdabīgi vai ļaundabīgi) šobrīd vai anamnēzē;
- smaga nieru mazspēja, akūta nieru mazspēja;
- virsnieru mazspēja;
- konstatētas no hormoniem atkarīgas ļaundabīgas slimības (tai skaitā dzimumorgānu vai piena dziedzeru) vai aizdomas par tām;
- nezināmas izcelsmes asiņošana no maksts;
- grūtniecība vai aizdomas par to;
- zīdīšanas periods;
- paaugstināta jutība pret kādu no zāļu Dimia® sastāvdaļām;
- laktozes nepanesamība, laktāzes deficīts, glikozes-galaktozes malabsorbcija (preparāts satur laktozes monohidrātu);
- paaugstināta jutība pret zemesriekstiem vai soju.
Ja pašlaik pastāv kāds no tālāk uzskaitītajiem stāvokļiem, slimībām/riska faktoriem, tad KPKL lietošanas iespējamais risks un sagaidāmais ieguvums ir rūpīgi jāizvērtē katrā atsevišķā gadījumā:
- trombozes un trombembolijas attīstības riska faktori: smēķēšana; tromboze, miokarda infarkts vai smadzeņu asinsrites traucējumi, kas jaunāki par 50 gadiem kādam no tuvākajiem radiniekiem; liekais svars (ķermeņa masas indekss (ĶMI) mazāks par 30 kg / m 2); dislipoproteinēmija; kontrolēta arteriālā hipertensija; migrēna; nekomplicēta sirds vārstuļu slimība; sirds ritma pārkāpums;
- citas slimības, kuru gadījumā var rasties perifērās asinsrites traucējumi: cukura diabēts; sistēmiskā sarkanā vilkēde; hemolītiski-urēmiskais sindroms; Krona slimība un čūlainais kolīts; sirpjveida šūnu anēmija; kā arī virspusējo vēnu flebīts;
- iedzimta angioneirotiskā tūska;
- hipertrigliceridēmija;
- aknu slimība;
- slimības, kas pirmo reizi radušās vai saasinājušās grūtniecības laikā vai uz iepriekšējas dzimumhormonu uzņemšanas fona (piemēram, dzelte, holestāze, holelitiāze, otoskleroze ar dzirdes traucējumiem, porfīrija, grūtnieces herpes, Sidenhemas horeja);
- pēcdzemdību periods.
Lietojiet grūtniecības un zīdīšanas laikā
Grūtniecība
Dimia® ir kontrindicēts grūtniecības laikā. Ja paciente plāno grūtniecību, viņa jebkurā laikā var pārtraukt Dimia® lietošanu. Ja Dimia® lietošanas laikā tiek konstatēta grūtniecība, tā nekavējoties jāpārtrauc. Tomēr plaši epidemioloģiskie pētījumi nav atklājuši paaugstinātu anomāliju risku bērniem, kas dzimuši sievietēm, kuras pirms grūtniecības saņēmušas dzimumhormonus (tostarp KPKL), vai teratogenitāti, ja dzimumhormonus nejauši lietoja grūtniecības sākumā.
Esošie dati par Dimia® lietošanas rezultātiem grūtniecības laikā ir ierobežoti, kas neļauj izdarīt secinājumus par zāļu ietekmi uz grūtniecības gaitu, jaundzimušā un augļa veselību. Pašlaik nav nozīmīgu epidemioloģisko datu par Dimia®.
zīdīšanas periods
Dimia® lietošana zīdīšanas laikā ir kontrindicēta. KPKL lietošana var samazināt mātes piena daudzumu un mainīt tā sastāvu, tāpēc to lietošana nav ieteicama līdz zīdīšanas pārtraukšanai. Neliels daudzums dzimumhormonu un/vai to metabolītu var nonākt mātes pienā un ietekmēt jaundzimušā ķermeni.
Devas un ievadīšana
Lietošanas veids: iekšķīgai lietošanai.
Kā lietot Dimia®
Tabletes jālieto katru dienu, aptuveni vienā un tajā pašā laikā, uzdzerot nelielu daudzumu ūdens, tādā secībā, kā norādīts uz blistera iepakojuma. Tabletes lieto nepārtraukti 28 dienas, 1 tablete dienā. Tablešu lietošana no katra nākamā iepakojuma jāsāk nākamajā dienā pēc pēdējās tabletes ieņemšanas no iepriekšējā iepakojuma. Atcelšanas asiņošana parasti sākas 2-3 dienas pēc zaļo placebo tablešu lietošanas sākuma (pēdējā rinda) un var beigties pirms nākamā tablešu iepakojuma sākuma. Tabletes no jauna iepakojuma vienmēr jāsāk tajā pašā nedēļas dienā, un "izņemšanas" asiņošana notiks aptuveni tajās pašās dienās katru mēnesi.
Kā sākt lietot Dimia®
- Ja iepriekšējā mēnesī nav lietoti hormonālie kontracepcijas līdzekļi
Dimia® jāsāk lietot menstruālā cikla pirmajā dienā (t.i., pirmajā menstruālās asiņošanas dienā), un tādā gadījumā papildu kontracepcijas līdzekļi nav nepieciešami. Ir atļauts sākt lietot menstruālā cikla 2.-5.dienā, taču šajā gadījumā pirmajās 7 tablešu lietošanas dienās no pirmā iepakojuma ieteicams papildus lietot kontracepcijas barjermetodi. - Pārejot no citiem kombinētiem kontracepcijas līdzekļiem (KPKL, maksts gredzens vai transdermālais plāksteris)
Dimia vēlams sākt lietot nākamajā dienā pēc pēdējās neaktīvās tabletes ieņemšanas (preparātiem, kas satur 28 tabletes iepakojumā) vai nākamajā dienā pēc pēdējās aktīvās tabletes ieņemšanas no iepriekšējā iepakojuma, bet nekādā gadījumā ne vēlāk kā dienu pēc parastās 7. - dienas pārtraukums (preparātiem, kas satur 21 tableti). Dimia® jāsāk lietot maksts gredzena vai plākstera noņemšanas dienā, bet ne vēlāk kā dienā, kad jāievieto jauns gredzens vai plāksteris. - Pārejot no kontracepcijas līdzekļiem, kas satur tikai gestagēnus ("mini tabletes", injicējamās formas, implantus) vai no progestagēnu izdaloša intrauterīnās kontracepcijas līdzekļa
Sieviete var pāriet no mini dzēriena uz Dimia® jebkurā dienā (bez pārtraukuma); no implanta vai intrauterīnās kontracepcijas līdzekļa ar progestagēnu - tā izņemšanas dienā, no injicējamā kontracepcijas līdzekļa - dienā, kad jāveic nākamā injekcija. Visos gadījumos pirmajās 7 tablešu lietošanas dienās ir jāizmanto papildu kontracepcijas barjermetode. - Pēc aborta grūtniecības pirmajā trimestrī
Sieviete var sākt lietot zāles tūlīt pēc spontāna vai medicīniska aborta grūtniecības pirmajā trimestrī. Ja šis nosacījums ir izpildīts, sievietei nav nepieciešami papildu kontracepcijas līdzekļi. - Pēc aborta grūtniecības otrajā trimestrī vai dzemdībās
Zāles var sākt lietot 21-28 dienā pēc spontāna vai medicīniska aborta vai pēc dzemdībām, ja nav zīdīšanas. Ja uzņemšana tiek uzsākta vēlāk, pirmajās 7 tablešu lietošanas dienās ir jāizmanto papildu kontracepcijas barjermetode. Tomēr, ja dzimumakts jau ir noticis, pirms Dimia® lietošanas jāizslēdz grūtniecība vai arī jāsagaida pirmās menstruācijas.
Dimia® apturēšana
Jūs varat pārtraukt zāļu lietošanu jebkurā laikā. Ja sieviete neplāno grūtniecību vai grūtniecība ir kontrindicēta, jo viņa lieto zāles, kas potenciāli kaitē auglim, citas kontracepcijas metodes jāapspriež ar savu ārstu.
Ja sieviete plāno grūtniecību, ieteicams pārtraukt zāļu lietošanu un gaidīt dabisku menstruālo asiņošanu, un tikai tad mēģināt palikt stāvoklī. Tas palīdzēs precīzāk aprēķināt gestācijas vecumu un dzimšanas laiku.
Aizmirsto tablešu lietošana
Var ignorēt to, ka pēdējā (4.) blistera rindā trūkst placebo tabletes.
Tomēr tie ir jāiznīcina, lai nejauši nepagarinātu placebo fāzi. Šie ieteikumi attiecas tikai uz trūkstošām aktīvām tabletēm. Ja zāļu lietošanas kavēšanās bija mazāk nekā 24 stundas, kontracepcijas aizsardzība netiek samazināta. Sievietei pēc iespējas ātrāk jāiedzer aizmirstā tablete un jāieņem nākamā tablete parastajā laikā.
Ja tablešu lietošanas kavēšanās bija vairāk nekā 24 stundas, kontracepcijas aizsardzība var tikt samazināta. Jo vairāk tablešu izlaists un jo tuvāk izlaistas tabletes ir neaktīvo zaļo placebo tablešu fāzei, jo lielāka ir grūtniecības iespējamība.
Šajā gadījumā varat vadīties pēc diviem pamatnoteikumiem:
- Zāļu lietošanu nekad nedrīkst pārtraukt ilgāk par 7 dienām;
- Lai panāktu adekvātu hipotalāma-hipofīzes-olnīcu sistēmas nomākšanu, ir nepieciešama nepārtraukta 7 dienu tablešu lietošana.
Attiecīgi sievietei var sniegt šādus ieteikumus:
- Izlaižot tabletes laika posmā no 1 līdz 7 uzņemšanas dienām:
Sievietei jālieto pēdējā aizmirstā tablete, tiklīdz viņa to atceras, pat ja tas nozīmē divu tablešu lietošanu vienlaikus. Viņa turpina lietot nākamās tabletes parastajā laikā. Turklāt nākamo 7 dienu laikā Jums papildus jāizmanto kontracepcijas barjermetode (piemēram, prezervatīvs). Ja dzimumakts noticis 7 dienu laikā pirms tabletes izlaišanas, jāapsver grūtniecības iespējamība. - Izlaižot tabletes laika posmā no 8 līdz 14 uzņemšanas dienām:
Sievietei jālieto pēdējā aizmirstā tablete, tiklīdz viņa to atceras, pat ja tas nozīmē divu tablešu lietošanu vienlaikus. Viņa turpina lietot nākamās tabletes parastajā laikā. Ja 7 dienu laikā pirms pirmās aizmirstās tabletes sieviete tabletes lietoja pareizi, papildu kontracepcijas līdzekļi nav nepieciešami. Pretējā gadījumā, kā arī tad, ja esat izlaidis divas vai vairākas tabletes, papildus jālieto kontracepcijas barjermetodes (piemēram, prezervatīvs) 7 dienas. - Izlaižot tabletes laika posmā no 15 līdz 24 uzņemšanas dienām:
Samazinātas uzticamības risks ir neizbēgams, jo tuvojas neaktīvo zaļo placebo tablešu periods. Jums ir stingri jāievēro viena no divām tālāk norādītajām opcijām. Tādā gadījumā, ja 7 dienu laikā pirms pirmās aizmirstās tabletes visas tabletes tika lietotas pareizi, papildu kontracepcijas metodes nav jāizmanto. Pretējā gadījumā sievietei 7 dienas jāizmanto pirmais no tālāk norādītajiem režīmiem un papildus jāizmanto kontracepcijas barjermetode (piemēram, prezervatīvs).
- Sievietei jālieto pēdējā aizmirstā tablete, tiklīdz viņa to atceras, pat ja tas nozīmē divu tablešu lietošanu vienlaikus. Nākamās tabletes tiek lietotas parastajā laikā, līdz aktīvās tabletes iepakojumā ir beigušās, 4 zaļās placebo tabletes no pēdējās rindas ir jāizmet un tabletes no nākamā iepakojuma jāsāk lietot nekavējoties.
"Atcelšanas" asiņošana ir maz ticama, kamēr otrā iepakojuma tabletes nav pabeigtas, taču tablešu lietošanas laikā var rasties "smērēšanās" un/vai "izrāviena" asiņošana. - Sieviete var arī pārtraukt lietot aktīvās tabletes no pašreizējā iepakojuma. Pēc tam viņai ir jālieto zaļās placebo tabletes no pēdējās rindas 4 dienas, ieskaitot dienas, kad viņa izlaida tabletes, un pēc tam jāsāk lietot tabletes no jaunā iepakojuma.
Ja sieviete izlaiž aktīvās tabletes un, lietojot neaktīvās zaļās placebo tabletes, viņai nav abstinences asiņošanas, grūtniecības iespēja ir jāizslēdz.
Ieteikumi kuņģa-zarnu trakta traucējumiem
Smagu kuņģa-zarnu trakta traucējumu gadījumā uzsūkšanās var būt nepilnīga, tāpēc jāveic papildu kontracepcijas pasākumi. Ja 3-4 stundu laikā pēc aktīvās tabletes lietošanas ir vemšana vai caureja, jums jāievēro ieteikumi, izlaižot tabletes. Ja sieviete nevēlas mainīt ierasto režīmu un atlikt menstruāciju sākšanos uz citu nedēļas dienu, papildus jālieto aktīvā tablete.
Kā mainīt/aizkavēt atcelšanas asiņošanas laiku
Lai aizkavētu abstinences asiņošanas sākšanos, sievietei jāturpina lietot tabletes no nākamā Dimia® iepakojuma, izlaižot neaktīvās zaļās tabletes no pašreizējā iepakojuma. Tādējādi ciklu var pagarināt pēc vēlēšanās uz jebkuru periodu, līdz beigsies aktīvās tabletes no otrā iepakojuma, tas ir, apmēram 3 nedēļas vēlāk nekā parasti.
Ja plānojat sākt nākamo ciklu agrāk, jebkurā laikā jāpārtrauc aktīvās tabletes no otrā iepakojuma, atlikušās aktīvās tabletes jāizmet un jāsāk lietot neaktīvās zaļās tabletes (maksimums 4 dienu laikā), un tad jāsāk ņemot tabletes no jaunā iepakojuma. Šādā gadījumā aptuveni 2-3 dienas pēc pēdējās aktīvās tabletes lietošanas no iepriekšējā iepakojuma jāsākas "atcelšanas" asiņošanai. Lietojot zāles no otrā iepakojuma, sievietei var rasties "smērēšanās" izdalījumi un/vai "izrāviens" no dzemdes asiņošanas. Regulāra Dimia® lietošana tiek atsākta pēc neaktīvo zaļo tablešu lietošanas perioda beigām.
Lai pārplānotu "atcelšanas" asiņošanas sākšanos uz citu nedēļas dienu, sievietei jāsaīsina nākamās neaktīvās zaļās tabletes periods par vēlamo dienu skaitu. Jo īsāks intervāls, jo lielāks risks, ka viņai, lietojot tabletes no otrā iepakojuma, nākotnē nebūs "atcelšanas" asiņošanas un "smērēšanās" un/vai "izrāviena" asiņošana.
Lietošana īpašām pacientu kategorijām
Bērni un pusaudži
Zāles Dimia® ir indicētas tikai pēc menarhe sākuma. Pieejamie dati neliecina par devas pielāgošanu šai pacientu grupai.
Gados vecāki pacienti
Dimia® nav indicēts pēc menopauzes.
Pacienti ar traucētu aknu darbību
Dimia® ir kontrindicēts sievietēm ar smagu aknu slimību, līdz aknu funkcionālie rādītāji normalizējas (skatīt arī sadaļas "Kontrindikācijas" un "Farmakoloģiskās īpašības").
Pacienti ar pavājinātu nieru darbību
Dimia® ir kontrindicēts sievietēm ar smagu nieru mazspēju vai akūtu nieru mazspēju (skatīt arī sadaļas "Kontrindikācijas" un "Farmakoloģiskās īpašības").
Blakusefekts
Drospirenona/etinilestradiola kombinācijas lietošanas laikā ziņots par šādām blakusparādībām (NBP).
Zāļu nevēlamās blakusparādības ir sakārtotas pēc orgānu sistēmu klasēm saskaņā ar MedDRA klasifikāciju un ar sastopamības biežumu: bieži (> 1/100 un<1/10), нечасто (>1/1000 un<1/100) и редко (>1/10 000 un<1/1000). В пределах каждой группы, выделенной в зависимости от частоты возникновения, НЛР представлены в порядке уменьшения их тяжести. Для дополнительных нежелательных реакций, выявленных только в процессе пострегистрационных наблюдений, и для которых оценку частоты возникновения провести не представлялось возможным, указано «частота неизвестна».
* Neregulāras asiņošanas biežums samazinās, palielinoties Dimia® lietošanas ilgumam.
Papildus informācija
Tālāk ir uzskaitītas nevēlamās blakusparādības ar ļoti retu sastopamības biežumu vai ar aizkavētiem simptomiem, kuras, domājams, ir saistītas ar KPKL grupas medikamentu lietošanu (skatīt arī sadaļas "Kontrindikācijas" un "Īpaši norādījumi").
Audzēji
- Krūts vēža diagnosticēšanas biežums sievietēm, kuras lieto KPKL, ir nedaudz palielināts. Tā kā sievietēm, kas jaunākas par 40 gadiem, krūts vēzis ir reti sastopams, krūts vēža diagnožu skaita pieaugums sievietēm, kuras lieto KPKL, ir nenozīmīgs salīdzinājumā ar kopējo šīs slimības risku.
- Aknu audzēji (labdabīgi un ļaundabīgi).
Citi štati
- sievietēm ar hipertrigliceridēmiju KPKL lietošanas laikā ir palielināts pankreatīta risks;
- asinsspiediena paaugstināšanās;
- stāvokļi, kas attīstās vai pasliktinās KPKL lietošanas laikā, bet to savstarpējā saistība nav pierādīta: dzelte un/vai nieze, kas saistīta ar holestāzi; holelitiāze; porfīrija; sistēmiskā sarkanā vilkēde; hemolītiski-urēmiskais sindroms; horeja; herpes grūtniecības laikā; dzirdes zudums, kas saistīts ar otosklerozi;
- sievietēm ar iedzimtu angioedēmu estrogēni var izraisīt vai saasināt tās simptomus;
- aknu darbības traucējumi;
- glikozes tolerances izmaiņas vai ietekme uz insulīna rezistenci;
- Krona slimība, čūlainais kolīts;
- hloazma;
- paaugstināta jutība (tostarp tādi simptomi kā izsitumi, nātrene).
Mijiedarbība
KPKL mijiedarbība ar citām zālēm (enzīmu induktoriem) var izraisīt "izrāvienu" asiņošanu un/vai kontracepcijas efektivitātes samazināšanos (skatīt sadaļu "Mijiedarbība ar citām zālēm").
Ja kāda no instrukcijā minētajām blakusparādībām pasliktinās vai novērojat citas blakusparādības, kas nav minētas instrukcijā, pastāstiet par to savam ārstam.
Pārdozēšana
Nav ziņots par nopietniem pārkāpumiem pārdozēšanas gadījumā. Preklīniskajos pētījumos pārdozēšanas rezultātā netika konstatētas nopietnas nevēlamas blakusparādības.
Simptomi kas var rasties pārdozēšanas gadījumā: slikta dūša, vemšana, smērēšanās no maksts vai metrorāģija.
Ārstēšana. Specifiska antidota nav, jāveic simptomātiska ārstēšana.
Mijiedarbība ar citām zālēm
Citu zāļu ietekme uz Dimia®
Iespējama mijiedarbība ar zālēm, kas inducē mikrosomālos enzīmus, kā rezultātā var palielināties dzimumhormonu klīrenss, kas savukārt var izraisīt "izrāvienu" dzemdes asiņošanu un/vai kontracepcijas efekta samazināšanos. Sievietēm, kuras papildus Dimia® saņem ārstēšanu ar šādām zālēm, ieteicams lietot kontracepcijas barjermetodi vai izvēlēties citu nehormonālu kontracepcijas metodi (ja nepieciešama ilgstoša induktoru lietošana).
Kontracepcijas barjermetode jāizmanto visu vienlaicīgu zāļu lietošanas laiku, kā arī 28 dienu laikā pēc to atcelšanas. Ja mikrosomālo aknu enzīmu induktoru lietošana turpinās pēc aktīvo tablešu lietošanas beigām Dimia® iepakojumā, jāsāk lietot Dimia® tabletes no jaunā iepakojuma, neņemot zaļās placebo tabletes no vecā iepakojuma.
- Vielas, kas palielina Dimia® klīrensu(efektivitātes pavājināšanās ar enzīmu indukciju): fenitoīns, barbiturāti, primidons, karbamazepīns, rifampicīns un, iespējams, arī okskarbazepīns, topiramāts, felbamāts, grizeofulvīns un asinszāli saturoši preparāti.
- Vielas ar dažādu ietekmi uz Dimia® klīrensu
Lietojot vienlaikus ar Dimia, daudzi HIV vai C hepatīta proteāžu inhibitori un nenukleozīdu reversās transkriptāzes inhibitori var palielināt vai samazināt estrogēnu vai progestagēnu koncentrāciju plazmā. Dažos gadījumos šī ietekme var būt klīniski nozīmīga. - Vielas, kas samazina KPKL (enzīmu inhibitoru) klīrensu
Spēcīgi un vidēji spēcīgi CYP3A4 inhibitori, piemēram, azola grupas pretsēnīšu līdzekļi (piemēram, itrakonazols, vorikonazols, flukonazols), verapamils, makrolīdi (piemēram, klaritromicīns, eritromicīns), diltiazems un greipfrūtu sula var palielināt estrogēna vai progestagēna koncentrāciju plazmā, vai abus. Tika pierādīts, ka etorikoksibs devā 60 un 120 mg dienā, lietojot kopā ar KPKL, kas satur 0,035 mg etinilestradiola, palielina etinilestradiola koncentrāciju asins plazmā attiecīgi 1,4 un 1,6 reizes.
Dimia® ietekme uz citām zālēm
KPKL var traucēt citu zāļu metabolismu, izraisot plazmas un audu koncentrācijas palielināšanos (piemēram, ciklosporīna) vai samazināšanos (piemēram, lamotrigīna).
In vitro drospirenons spēj vāji vai mēreni inhibēt citohroma P450 izoenzīmus CYP1A1, CYP2C9, CYP2C19 un CYP3A4.
Pamatojoties uz in vivo mijiedarbības pētījumiem brīvprātīgajām sievietēm, kuras tika ārstētas ar omeprazolu, simvastatīnu vai midazolāmu kā marķiera substrātiem, var secināt, ka 3 mg drospirenona klīniski nozīmīga ietekme uz zāļu metabolismu, ko mediē citohroma P450 sistēmas enzīmi, ir maz ticama.
In vitro etinilestradiols ir atgriezenisks CYP2C19, CYP1A1 un CYP1A2 izoenzīmu inhibitors, kā arī neatgriezenisks CYP3A4/5, CYP2C8 un CYP2J2 izoenzīmu inhibitors. Klīniskajos pētījumos etinilestradiolu saturošu hormonālo kontracepcijas līdzekļu lietošana neizraisīja CYP3A4 izoenzīma substrātu (piemēram, midazolāma) koncentrācijas palielināšanos plazmā vai tikai nedaudz palielinājās, savukārt CYP1A2 izoenzīma substrātu koncentrācija asins plazmas līmenis var nedaudz palielināties (piemēram, teofilīns) vai mēreni (piemēram, melatonīns un tizanidīns).
Citi mijiedarbības veidi
Pacientiem ar saglabātu nieru darbību kombinēta drospirenona un angiotenzīnu konvertējošā enzīma inhibitoru vai nesteroīdo pretiekaisuma līdzekļu lietošana būtiski neietekmē kālija koncentrāciju asins plazmā. Tomēr Dimia® vienlaicīga lietošana ar aldosterona antagonistiem vai kāliju aizturošiem diurētiskiem līdzekļiem nav pētīta. Šādos gadījumos pirmajā zāļu lietošanas ciklā jākontrolē kālija koncentrācija asins plazmā (skatīt sadaļu "Īpaši norādījumi").
Speciālas instrukcijas
Ja pašlaik pastāv kāds no tālāk uzskaitītajiem stāvokļiem, slimībām/riska faktoriem, tad potenciālais risks un sagaidāmais ieguvums no KPKL lietošanas katrā atsevišķā gadījumā ir rūpīgi jāizvērtē un jāapspriež ar sievieti, pirms viņa nolemj sākt lietot šīs zāles. Ja kāds no šiem stāvokļiem, slimībām vai riska faktoriem pasliktinās, pasliktinās vai pirmo reizi parādās, sievietei jākonsultējas ar savu ārstu, kurš var izlemt par nepieciešamību pārtraukt zāļu lietošanu.
Sirds un asinsvadu sistēmas slimības
Epidemioloģisko pētījumu rezultāti liecina par saistību starp KPKL lietošanu un vēnu un artēriju trombozes un trombembolijas (piemēram, dziļo vēnu trombozes, plaušu embolijas, miokarda infarkta, cerebrovaskulāro traucējumu) sastopamības palielināšanos. Šīs slimības ir retas.
Venozās trombembolijas (VTE) attīstības risks ir visaugstākais pirmajā šo zāļu lietošanas gadā. Paaugstināts risks pastāv pēc KPKL sākotnējās lietošanas vai to pašu vai dažādu KPKL lietošanas atsākšanas (pēc 4 nedēļu vai ilgāku devu pārtraukuma). Dati no perspektīvā pētījuma, kurā piedalījās 3 pacientu grupas, liecina, ka šis paaugstinātais risks galvenokārt pastāv pirmajos 3 zāļu lietošanas mēnešos. Kopējais VTE risks pacientiem, kuri lieto mazu devu KPKL (<0,05 мг этинилэстрадиола) в 2-3 раза выше, чем у небеременных пациенток, которые не принимают КОК, тем не менее, этот риск остается более низким по сравнению с риском ВТЭ при беременности и родах. ВТЭ может угрожать жизни или привести к летальному исходу (в 1-2% случаев).
VTE, kas izpaužas kā dziļo vēnu tromboze vai plaušu embolija, var rasties, lietojot jebkuru KPKL.
Ļoti reti, lietojot KPKL, rodas citu asinsvadu tromboze, piemēram, aknu, apzarņa, nieru, smadzeņu vēnu un tīklenes artēriju vai asinsvadu tromboze. Nav vienprātības par saistību starp šo slimību rašanos un KPKL lietošanu.
Dziļo vēnu trombozes (DVT) simptomi ir šādi: vienpusējs apakšējās ekstremitātes pietūkums vai gar apakšējo ekstremitāšu vēnu, sāpes vai diskomforts apakšējā ekstremitātē tikai stāvot vai ejot, lokalizēts drudzis skartajā apakšējā ekstremitātē, apsārtums vai apakšējās ekstremitātes ādas krāsas maiņa.
Plaušu embolijas (PE) simptomi ir šādi: apgrūtināta vai ātra elpošana; pēkšņs klepus, ieskaitot hemoptīzi; asas sāpes krūtīs, kas var pastiprināties ar dziļu elpu; trauksmes sajūta; smags reibonis; ātra vai neregulāra sirdsdarbība. Daži no šiem simptomiem (piemēram, elpas trūkums, klepus) ir nespecifiski un var tikt nepareizi interpretēti kā citu vairāk vai mazāk smagu stāvokļu/slimību (piemēram, elpceļu infekcijas) pazīmes.
Arteriālā trombembolija var izraisīt insultu, asinsvadu oklūziju vai miokarda infarktu.
Insulta simptomi ir šādi: pēkšņs vājums vai sajūtas zudums sejā, ekstremitātēs, īpaši vienā ķermeņa pusē, pēkšņs apjukums, runas un izpratnes traucējumi; pēkšņs vienpusējs vai divpusējs redzes zudums; pēkšņi gaitas traucējumi, reibonis, līdzsvara vai kustību koordinācijas zudums; pēkšņas, smagas vai ilgstošas galvassāpes bez redzama iemesla; samaņas zudums vai ģībonis ar vai bez epilepsijas lēkmes.
Citas asinsvadu oklūzijas pazīmes: pēkšņas sāpes, pietūkums un neliels ekstremitāšu zilums, "akūts" vēders.
Miokarda infarkta simptomi ir: sāpes, diskomforts, spiediena sajūta, smaguma sajūta, saspiešana vai pilnuma sajūta krūtīs, rokā vai aiz krūšu kaula; diskomforts ar apstarošanu mugurā, vaigu kaulā, balsenē, rokā, vēderā; auksti sviedri, slikta dūša, vemšana vai reibonis, smags vājums, trauksmes sajūta vai elpas trūkums; ātra vai neregulāra sirdsdarbība.
Arteriālā trombembolija var būt dzīvībai bīstama vai letāla. Sievietēm, kurām ir vairāku riska faktoru kombinācija vai viena no tiem ir augsta smaguma pakāpe, jāapsver iespēja tos savstarpēji pastiprināt. Šādos gadījumos riska pieauguma pakāpe var būt lielāka nekā ar vienkāršu faktoru summēšanu. Šajā gadījumā Dimia® lietošana ir kontrindicēta (skatīt sadaļu "Kontrindikācijas").
Trombozes (venozās un/vai arteriālās) un trombembolijas attīstības risks palielinās:
- ar vecumu;
- smēķētājiem (palielinoties cigarešu skaitam vai pieaugot vecumam, risks palielinās, īpaši sievietēm, kas vecākas par 35 gadiem);
klātbūtnē:
- aptaukošanās (ĶMI virs 30 kg/m2);
- ģimenes anamnēze (piemēram, venoza vai arteriāla trombembolija tuviem radiniekiem vai vecākiem, kas jaunāki par 50 gadiem). Iedzimtas vai iegūtas noslieces gadījumā sieviete ir jāpārbauda atbilstošam speciālistam, lai izlemtu par KPKL lietošanas iespēju;
- ilgstoša imobilizācija, liela operācija, jebkura apakšējo ekstremitāšu operācija vai liela trauma. Šādos gadījumos Dimia® lietošana ir jāpārtrauc. Plānotās operācijas gadījumā zāļu lietošana jāpārtrauc vismaz 4 nedēļas pirms tās, un to nedrīkst atsākt divas nedēļas pēc pilnīgas motoriskās aktivitātes atjaunošanas. Īslaicīga imobilizācija (piemēram, lidojums ilgāk par 4 stundām) var būt arī venozās trombembolijas riska faktors, īpaši, ja pastāv citi riska faktori;
- dislipoproteinēmija;
- arteriālā hipertensija;
- migrēna;
- sirds vārstuļu slimība;
- priekškambaru fibrilācija.
Jebkuru kombinēto hormonālo kontracepcijas līdzekļu lietošana palielina VTE risku. Levonorgestrelu, norgestimātu vai noretisteronu saturošu zāļu lietošana ir saistīta ar zemāko VTE risku. Citu zāļu, piemēram, Dimia®, lietošana var izraisīt divkāršu riska pieaugumu. Lēmums lietot citas zāles, kas nav tās, kurām ir viszemākais VTE attīstības risks, jāpieņem tikai pēc pārrunām ar sievieti, lai pārliecinātos, ka viņa saprot, ka Dimia® lietošana ir saistīta ar VTE attīstības iespējamību, un izprot viņas risku. faktori ietekmē VTE attīstības iespējamību, kā arī saprot, ka katrā pirmajā zāļu lietošanas gadā VTE attīstības risks viņai ir vislielākais.
Jautājums par varikozu vēnu un virspusējo tromboflebīta iespējamo lomu vēnu trombembolijas attīstībā joprojām ir pretrunīgs.
Jāņem vērā paaugstināts trombembolijas risks pēcdzemdību periodā. Perifērās asinsrites traucējumi var rasties arī cukura diabēta, sistēmiskas sarkanās vilkēdes, hemolītiski urēmiskā sindroma, hroniskas iekaisīgas zarnu slimības (Krona slimības vai čūlainais kolīta) un sirpjveida šūnu anēmijas gadījumā.
Migrēnas biežuma un smaguma palielināšanās KPKL lietošanas laikā (kas var būt pirms cerebrovaskulāriem traucējumiem) ir pamats tūlītējai šo zāļu lietošanas pārtraukšanai.
Bioķīmiskie rādītāji, kas norāda uz iedzimtu vai iegūtu noslieci uz venozo vai arteriālo trombozi, ir šādi: rezistence pret aktivētu proteīnu C, hiperhomocisteinēmija, antitrombīna III deficīts, proteīna C deficīts, proteīna S deficīts, antifosfolipīdu antivielas (kardiolipīna antivielas, sarkanās vilkēdes antikoagulants).
Izvērtējot riska un ieguvuma attiecību, jāņem vērā, ka attiecīgā stāvokļa adekvāta ārstēšana var samazināt ar to saistīto trombozes risku. Jāņem vērā arī tas, ka trombozes un trombembolijas risks grūtniecības laikā ir lielāks nekā tad, ja tiek lietoti mazas devas KPKL (<0,05 мг этинилэстрадиола).
Audzēji
Nozīmīgākais dzemdes kakla vēža attīstības riska faktors ir pastāvīga cilvēka papilomas vīrusa infekcija. Ir ziņojumi par nelielu dzemdes kakla vēža attīstības riska palielināšanos, ilgstoši lietojot KPKL, taču saistība ar KPKL lietošanu nav pierādīta. Joprojām pastāv strīds par to, cik lielā mērā šie atklājumi ir saistīti ar dzemdes kakla patoloģijas vai seksuālās uzvedības skrīningu (mazāka kontracepcijas barjermetožu izmantošana).
54 epidemioloģisko pētījumu metaanalīze parādīja, ka sievietēm, kuras pašlaik lieto KPKL, ir nedaudz paaugstināts relatīvais krūts vēža attīstības risks (relatīvais risks 1,24). Paaugstinātais risks pakāpeniski izzūd 10 gadu laikā pēc šo zāļu lietošanas pārtraukšanas. Tā kā sievietēm, kas jaunākas par 40 gadiem, krūts vēzis ir reti sastopams, krūts vēža diagnožu skaita pieaugums sievietēm, kuras pašlaik lieto KPKL vai nesen tos lietojušas, ir nenozīmīgs attiecībā pret kopējo šīs slimības risku. Novērotais riska pieaugums var būt saistīts ar agrāku krūts vēža diagnozi sievietēm, kuras lieto KPKL, to bioloģisko ietekmi vai abu faktoru kombināciju. Sievietēm, kuras lietojušas KPKL, krūts vēzis tiek atklātas agrākās stadijās nekā sievietēm, kuras tos nekad nav lietojušas.
Retos gadījumos uz KPKL lietošanas fona tika novērota labdabīgu un ārkārtīgi retos gadījumos ļaundabīgu aknu audzēju attīstība, kas dažos gadījumos izraisīja dzīvībai bīstamu intraabdominālu asiņošanu. Šie apstākļi jāņem vērā, veicot diferenciāldiagnozi stipru vēdera sāpju, aknu palielināšanās vai intraabdominālas asiņošanas pazīmju gadījumā.
Audzēji var būt dzīvībai bīstami vai letāli.
Citi štati
Klīniskie pētījumi nav pierādījuši drospirenona ietekmi uz kālija koncentrāciju asins plazmā pacientiem ar vieglu vai vidēji smagu nieru mazspēju. Teorētiski pastāv hiperkaliēmijas attīstības risks pacientiem ar pavājinātu nieru darbību ar sākotnējo kālija koncentrāciju pie normas augšējās robežas, vienlaikus lietojot zāles, kas izraisa kālija aizturi organismā. Sievietēm ar paaugstinātu hiperkaliēmijas attīstības risku pirmajā Dimia® lietošanas ciklā ieteicams noteikt kālija koncentrāciju asins plazmā.
Sievietēm ar hipertrigliceridēmiju (vai šī stāvokļa ģimenes anamnēzē) KPKL lietošanas laikā var būt paaugstināts pankreatīta attīstības risks.
Lai gan daudzām sievietēm, kuras lieto KPKL, ir aprakstīts neliels asinsspiediena paaugstinājums, klīniski nozīmīgs paaugstinājums ir bijis reti. Tomēr, ja KPKL lietošanas laikā attīstās pastāvīgs klīniski nozīmīgs asinsspiediena paaugstinājums, šo zāļu lietošana jāpārtrauc un jāsāk arteriālās hipertensijas ārstēšana. KPKL lietošanu var turpināt, ja ar antihipertensīvo terapiju tiek sasniegtas normālas asinsspiediena vērtības.
Ir ziņots par šādu stāvokļu attīstību vai pasliktināšanos gan grūtniecības laikā, gan KPKL lietošanas laikā, taču to saistība ar KPKL lietošanu nav pierādīta: dzelte un/vai nieze, kas saistīta ar holestāzi; holelitiāze; porfīrija; sistēmiskā sarkanā vilkēde; hemolītiski-urēmiskais sindroms; horeja; herpes grūtniecības laikā; dzirdes zudums, kas saistīts ar otosklerozi. Ir arī aprakstīti endogēnās depresijas, epilepsijas, Krona slimības un čūlainā kolīta gaitas pasliktināšanās gadījumi KPKL lietošanas fona apstākļos.
Sievietēm ar iedzimtām angioneirotiskās tūskas formām eksogēni estrogēni var izraisīt vai pasliktināt angioneirotiskās tūskas simptomus.
Akūtas vai hroniskas aknu disfunkcijas gadījumā var būt jāpārtrauc KPKL lietošana, līdz aknu funkcionālie rādītāji normalizējas. Atkārtota holestātiskā dzelte, kas pirmo reizi attīstās grūtniecības vai iepriekšējas dzimumhormonu lietošanas laikā, prasa pārtraukt KPKL lietošanu.
Lai gan KPKL var ietekmēt insulīna rezistenci un glikozes toleranci, nav nepieciešams mainīt hipoglikēmisko zāļu devas pacientiem ar cukura diabētu, kuri lieto mazas devas KPKL.<0,05 мг этинил-эстрадиола). Тем не менее, женщины с сахарным диабетом должны тщательно наблюдаться во время приема КОК.
Reizēm var attīstīties hloazma, īpaši sievietēm, kurām anamnēzē ir bijusi hloazma grūtniecības laikā. Sievietēm, kurām ir tendence uz hloazmu KPKL lietošanas laikā, jāizvairās no ilgstošas uzturēšanās saulē un ultravioletā starojuma iedarbības.
Laboratorijas testi
KPKL lietošana var ietekmēt dažu laboratorisko izmeklējumu rezultātus, tostarp aknu, nieru, vairogdziedzera, virsnieru funkciju, plazmas transportproteīnu koncentrāciju, ogļhidrātu metabolismu, koagulācijas un fibrinolīzes parametrus. Izmaiņas parasti nepārsniedz normālo vērtību robežas. Drospirenons palielina plazmas renīna un aldosterona aktivitāti, kas ir saistīta ar tā antimineralokortikoīdu iedarbību.
Medicīniskās pārbaudes
Pirms Dimia® lietošanas sākšanas vai atsākšanas ir jāiepazīstas ar dzīves vēsturi, sievietes ģimenes vēsturi, jāveic rūpīga medicīniskā (tostarp asinsspiediena, sirdsdarbības, ĶMI mērījumi) un ginekoloģiskā izmeklēšana (ieskaitot piena dziedzeri un dzemdes kakla skrāpējuma citoloģiskā izmeklēšana), izslēdz grūtniecību. Papildus studiju apjoms un pēcpārbaužu biežums tiek noteikts individuāli. Parasti kontroles izmeklējumi jāveic vismaz 1 reizi 6 mēnešos.
Sievietes jābrīdina, ka KPKL neaizsargā pret HIV infekciju (AIDS) un citām seksuāli transmisīvām slimībām.
Samazināta efektivitāte
KPKL efektivitāte var samazināties šādos gadījumos: ja aktīvās tabletes ir izlaistas, ar vemšanu un caureju vai zāļu mijiedarbības rezultātā.
Nepietiekama menstruālā cikla kontrole
KPKL lietošanas laikā var rasties neregulāra asiņošana (“smērēšanās” un/vai “izrāviena” asiņošana), īpaši pirmajos lietošanas mēnešos. Tādēļ jebkuras neregulāras asiņošanas novērtējums jāveic tikai pēc aptuveni trīs ciklu adaptācijas perioda.
Ja neregulāra asiņošana atkārtojas vai attīstās pēc iepriekšējiem regulārajiem cikliem, jāveic rūpīga diagnostiskā izmeklēšana, lai izslēgtu ļaundabīgu audzēju vai grūtniecību.
Dažām sievietēm, lietojot zaļās neaktīvās placebo tabletes, var nebūt "atcelšanas" asiņošanas. Ja zāles tika lietotas atbilstoši norādījumiem, maz ticams, ka sieviete ir stāvoklī. Tomēr, ja zāles iepriekš lietotas neregulāri vai ja nav divu abstinences asiņošanas pēc kārtas, pirms zāļu lietošanas turpināšanas jāizslēdz grūtniecība.
Laktoze
Dimia®, apvalkotās tabletes, satur laktozi. Šīs zāles nevajadzētu lietot pacientiem ar retu iedzimtu galaktozes nepanesību, laktāzes deficītu un glikozes un galaktozes malabsorbciju.
Soja
Dimia® apvalkotās tabletes satur sojas lecitīnu. Pacienti ar zemesriekstu un sojas alerģiju nedrīkst lietot šīs zāles.
Ietekme uz spēju vadīt transportlīdzekļus un mehānismus
Nav atrasts.
Atbrīvošanas forma
Apvalkotās tabletes [komplekts], 3 mg + 0,02 mg.
24 tabletes drospirenona + etinilestradiola katrā un 4 tabletes placebo PVH/PE/PVDC-alumīnija folijas blisteriepakojumā.
1 vai 3 blisteri kartona kastītē kopā ar lietošanas instrukciju. Kartona plakans futrālis blistera uzglabāšanai ir ievietots kartona saišķī.
Uzglabāšanas apstākļi
No gaismas aizsargātā vietā temperatūrā, kas nepārsniedz 25 ° C.
Uzglabāt bērniem nepieejamā vietā!
Labākais pirms datums
2 gadi.
Nelietot pēc derīguma termiņa beigām, kas norādīts uz iepakojuma.
Brīvdienu nosacījumi
Izlaists pēc receptes.
Ražotājs
AAS "Gedeon Richter"
1103 Budapešta, st. Dömröi, 19-21, Ungārija
Patērētāju pretenzijas jānosūta uz:
AS "Gedeon Richter" Maskavas pārstāvniecība
119049 Maskava, 4. Dobriņinska josla, 8. ēka,
Sveika Alena!
Jūsu jautājumi ir ļoti izplatīti starp sievietēm, kuras pirmo reizi sāka lietot kombinētos perorālos kontracepcijas līdzekļus, tostarp Dimia, lai aizsargātu pret nevēlamu grūtniecību. Tāpēc es centīšos uz tiem atbildēt pēc iespējas detalizētāk un saprotamāk.
Kāpēc un kad parādās tablešu kontracepcijas efekts?
Kad sieviete sāk lietot kombinētos kontracepcijas līdzekļus, viņas organismā notiek nopietnas hormonālas izmaiņas. Lielākā daļa zāļu satur divu veidu hormonus - estrogēnu un progesteronu. Tātad "Dimia" satur apmēram 20 mikrogramus hormona, kas pieder pie estrogēnu grupas, un 3 mg hormona - progesterona analoga.
Lai tabletēm būtu kontracepcijas efekts, sievietes ķermenī būtiski jāmainās hormonālajam fonam. Tas notiek, jo hormoni no tabletēm regulāri nonāk asinsritē. Speciālie receptori informē smadzenes, ka šo hormonu līmenis asinīs ir paaugstināts, un tas nedod komandu veidot olšūnu. Tāpēc grūtniecība kļūst neiespējama.
Vidēji hormonālā fona atjaunošana aizņem apmēram septiņas dienas. Tāpēc pirmajā nedēļā (ja tabletes tiek lietotas pirmo reizi) var iestāties grūtniecība, un ir jāizmanto papildu metodes, lai aizsargātos pret to - piemēram, barjermetodes, kas ietver prezervatīvus. Augsts grūtniecības risks pastāv arī tad, ja pirmajā zāļu lietošanas nedēļā tika izlaista tablete vai pirmajās stundās pēc zāļu lietošanas radās vemšana.
Sākot ar otro nedēļu, hormonu līmenis asinīs kļūst stabils, olšūna neveidojas, un dzemdes kakla kanālā sabiezē gļotas, kas neļauj spermai iekļūt dzemdes dobumā. Tādējādi grūtniecība kļūst neiespējama. Pat ja viena no pēdējām aktīvajām tabletēm tika izlaista, ieņemšana ir maz ticama.
Katrs nākamais zāļu iepakojums palīdz uzturēt jau izveidoto hormonu līdzsvaru, tāpēc grūtniecības iespējamība kļūst vēl mazāka. Parasti pat pēc pilnīgas zāļu atcelšanas (ja tās tika lietotas sešus mēnešus vai ilgāk) ķermenim ir nepieciešams zināms laiks (dažreiz gadā), lai atjaunotu savu reproduktīvo funkciju.
Tāpēc, ja esat lietojis zāles mēnesi, neizlaižot tableti un neesat cietis no kuņģa darbības traucējumiem, jums nav jāaizsargā sevi no nevēlamas grūtniecības ar papildu līdzekļiem.
Menstruācijas KPKL lietošanas laikā
Lietojot KPK, menstruācijām līdzīga asiņošana sākas dažas dienas pēc pēdējās aktīvās tabletes lietošanas, jo līdz tam laikam no organisma tiek izvadīti "papildu" hormoni.
Lietojot Dimia, menstruācijām jāsākas dažas dienas pēc pēdējās rindas tablešu lietošanas – tās nesatur hormonus un tiek lietotas ērtībai, lai sieviete neaizmirstu par zāļu lietošanu un zinātu, kad sākt lietot nākamo iepakojumu.
Tādējādi jūsu gadījumā menstruāciju sākuma laikā nav novirzes no normas. Visticamāk, nākamajā mēnesī asiņošana sāksies tajā pašā dienā. Tas var beigties pirms aktīvo tablešu lietošanas vai turpināties vēl vairākas dienas.
Ar laba vēlējumiem, Svetlana.
Kombinētie perorālie kontracepcijas līdzekļi, ja tos lieto pareizi, ir visdrošākā kontracepcijas metode. Turklāt šādas zāles ietver sieviešu dzimuma hormonus stingri pielāgotā, nelielā devā. Un tas ļauj atrisināt daudzas sieviešu veselības problēmas, uzlabot ādas, matu un nagu stāvokli.
Dimia ir moderns, daudzfāžu kontracepcijas līdzeklis, kas saņēmis daudz pozitīvu atsauksmju. Kādas ir zāles īpašības, pēc kādas shēmas tabletes jālieto un kam vajadzētu atturēties no OK lietošanas?
Savienojums

Kontracepcijas līdzeklis ir apaļu, baltu un zaļu tablešu formā ar marķieri "G73", ir pieejams blisteriepakojumā pa 28 gabaliņiem. Izlaists pēc ārsta receptes.
Baltās tabletes satur šādas sastāvdaļas:
- Aktīvs. Tas ir mikrofolins, progestagēns, spironolaktona atvasinājums.
- Palīgdarbs. Šajā kategorijā ietilpst laktolīns, kukurūzas dekstrīns, polietilēnglikola kopolimērs, stearīnskābe, hipotētisks vinilspirta polimērs ar atkārtotu vienības strukturālo formulu.
Zaļās tabletes ir placebo. Satur:
- Piena cukurs.
- Diētiskās šķiedras no rafinētas kokvilnas celulozes.
- Stearīnskābe.
- Kukurūzas dekstrīns.
- Adsorbents ir pirogēns silīcija dioksīds.
Pašārstēšanās, jo īpaši nepareiza zāļu lietošana, var izraisīt blakusparādības vai samazināt zāļu kontracepcijas funkciju.
Farmakoloģija
Dimia, pirmkārt, ir efektīvs kontracepcijas līdzeklis. Ārsts viņu var izrakstīt kā nedzemdējušu un mākslīgi pārtrauktu grūtniecību pirmajā un otrajā trimestrī. Tas ir ieteicams arī sievietēm, kuras ir dzemdējušas un nebaro bērnu ar krūti.
Papildus tiešai lietošanai (aizsardzībai pret nevēlamu grūtniecību) zāles var ordinēt meitenēm reproduktīvā vecumā pūtītes, seborejas, smagas dismenorejas ārstēšanai. Turklāt KPKL lietošana samazina iespējamību, ka attīstīsies:
- Dzimumorgānu vēzis.
- Iegurņa orgānu iekaisuma slimības.
- Osteoporoze.
Tabletes ir paredzētas sievietēm, kurām ir bijusi ārpusdzemdes grūtniecība vai kurām ir nosliece uz to. Arī cieš no neauglības (palielina apaugļošanās iespējamību pēc KPKL lietošanas pārtraukšanas).
Jāpatur prātā, ka katras sievietes ķermenim ir savas īpašības. Tāpēc pirms kontracepcijas līdzekļa lietošanas ir obligāti jānokārto visi nepieciešamie testi par zāļu sastāvdaļu toleranci. Būtu lietderīgi savākt pilnīgu slimības vēsturi un konsultēties ar ārstējošo ginekologu.
Blakus efekti

Kontracepcijas tablešu lietošana Dimia var radīt nepatīkamas sekas, ja ir nepareizi izvēlēta zāļu deva, pacients regulāri pārkāpj zāļu lietošanas režīmu. Biežākās KPKL lietošanas blakusparādības ir: reibonis, slikta dūša, miega traucējumi, samaņas zudums, paaugstināts spiediens, depresija, depresija, asiņošana no deguna dobuma. Smagākie ir:
- Ādas slimības un ķermeņa alerģiskas reakcijas uz zāļu aktīvajām vai palīgkomponentēm (nieze, izsitumi, dedzināšanas sajūta).
- Žultspūšļa, maksts gļotādas iekaisums, dzemdes kakla kanāla un piena dziedzera audu lokāla proliferācija.
- Seksuāla disfunkcija un samazināta vēlme pēc dzimumakta.
- Menstruāciju pārtraukšana.
- Krūšu dobuma patoloģija ar šķidrumam līdzīgu saturu, sāpes krūtīs.
- Maksts sāpes, sausums makstī, piena sēnīte.
- Uzpūšanās vai sāpes vēderā.
- Galvas, muskuļu sāpes (spastisks raksturs), sāpes jostas-krustu daļā, ekstremitātēs.
- Motora funkciju traucējumi.
Narkotiku intoksikācijas gadījumi no Dimia lietošanas netika reģistrēti. Bet iespējamie narkotiku lietošanas sindromi, kas pārsniedz normu (pamatojoties uz citiem KPKL), var būt: slikta dūša, vemšana, neliela maksts asiņu izdalīšanās.
Kontrindikācijas

Tāpat kā lielāko daļu OK, Dimia kontracepcijas līdzekļus nedrīkst lietot grūtniecības vai zīdīšanas laikā. Tas ir saistīts ar faktu, ka paaugstināta hormonu koncentrācija var negatīvi ietekmēt augļa dabisko attīstību. Tāpat produkta sastāvā esošās aktīvās vielas var ne tikai samazināt tā daudzumu, bet arī mainīt sastāvu.
Kontrindikācijas kontracepcijas lietošanai ir sievietes klātbūtne:
- Nepanesība pret vienu vai vairākām zāļu sastāvdaļām.
- Akūts aizkuņģa dziedzera iekaisums.
- Ļaundabīgi ģeneratīvo orgānu, piena dziedzeru, aknu audzēji.
- Vienas vai vairāku aknu funkciju pārkāpumi.
- Augsts asinsspiediens, arteriālo asinsvadu, vēnu aizsprostojums.
- Kvantitatīvi un kvalitatīvi asins lipoproteīnu sastāva pārkāpumi.
- Slimības, kas saistītas ar nepietiekamu C1 inhibitora daudzumu vai aktivitāti, traucēta asinsrite perifērajās artērijās.
- Migrēna ar izteiktiem fokusa neiroloģiskiem simptomiem.
- Slimības, kas saistītas ar glikozes, laktozes uzsūkšanās traucējumiem.
- Supraventrikulāras tahiaritmijas ar haotisku priekškambaru elektrisko aktivitāti.
Noteikti konsultējieties ar savu ārstu, lai izrakstītu visefektīvāko Dimia kontracepcijas tablešu devu ar darbu saistītu slimību gadījumā:
- Aknas.
- Sirds muskulis.
- Asins plūsma un citi akūti vai hroniski stāvokļi.
Turklāt sievietes pēcdzemdību periodā, lietojot Dimia, jāizturas īpaši uzmanīgi un piesardzīgi. Tāpat piesardzīgi līdzeklis tiek nozīmēts tiem, kam ir bijušas slimības, ko izraisījusi grūtniecība vai hormonu saturošu zāļu lietošana (herpes, dzelte, porfirīna slimība utt.).
Sievietēm, kuras cieš no aptaukošanās, tabakas intoksikācijas un sirds patoloģijām, ir paaugstināts blakusparādību risks.
Uzņemšanas noteikumi

Uzņemšana Dimia ir paredzēta 28 dienām, kuru laikā sievietei katru dienu jālieto viena tablete (pārmaiņus ar aktīvo un placebo). Tas ir aptuveni nepieciešams vienlaikus, dzerot daudz tīra, negāzēta ūdens. Kad iepakojums ir beidzies, jums nekavējoties jāsāk lietot jauns, bez pārtraukumiem. Zāļu lietošanu no viena blistera nedrīkst pārtraukt ilgāk par vienu nedēļu (7 dienām).
- Ja sieviete iepriekš nav lietojusi perorālos kontracepcijas līdzekļus vai ieturējusi to lietošanas pārtraukumu 30–31 dienu, tad zāļu lietošana jāsāk menstruāciju pirmajā dienā. Tas ir pieļaujams arī 2-5 cikla dienas, bet tajā pašā laikā dzimumakta laikā papildus jālieto barjeras kontracepcijas līdzekļi.
- Pārejot uz Dimia no citiem OC, uzņemšana jāsāk nākamajā dienā pēc placebo tablešu (zāles paredzētas 28 dienām) vai tablešu ar aktīvo vielu (kontracepcijas līdzekļiem, kas paredzēti 21 dienai) lietošanas.
- Ja implanti, injekcijas, hormonālās minimālās tabletes vai intrauterīnās kontracepcijas līdzekļi tiek atmesti par labu KPKL, perorālo kontracepcijas līdzekļu lietošanu ieteicams sākt dienā, kad tiek pārtraukta injekcija vai kontracepcijas formas.
- Zāļu lietošana ar kavēšanos ne vairāk kā 12 stundas neietekmēs zāļu kontracepcijas aizsardzības kvalitāti. Ja kopš paredzamā uzņemšanas laika ir pagājušas vairāk nekā 12 stundas bez zāļu lietošanas, tad tablete jālieto, tiklīdz sieviete to atceras, pat ja tas noved pie vairāku tablešu kopīgas lietošanas. Turklāt kontracepcijas līdzeklis jālieto saskaņā ar parasto shēmu.
Adaptācijas periods (primārajai un sekundārajai), bet pēc ievērojama kontracepcijas līdzekļa lietošanas pārtraukuma, vidēji ir līdz trim mēnešiem.
Ja pēc šī perioda kontracepcijas līdzekļu lietošanu pavada nepatīkamas sajūtas, tad jums jāsazinās ar savu ārstu, lai pielāgotu režīmu vai jaunu tikšanos.
Mijiedarbība ar citām zālēm

Reaģējot ar citām zālēm, Dimia efektivitāti var samazināt vai palielināt. Tādējādi, vienlaikus lietojot antibiotikas (īpaši ampicilīnu, tetraciklīnu), tiek novērota kontracepcijas līdzekļa galvenās funkcijas samazināšanās.
Stiprināt aktīvo vielu metabolisma procesu OK var:
- Pretvīrusu un sedatīvi līdzekļi.
- Zāles, kas paredzētas infekcioza rakstura elpceļu un urīnceļu, aknu un kuņģa-zarnu trakta slimību ārstēšanai.
- Perorālo kontracepcijas līdzekļu iedarbību var pastiprināt un palielināt, lietojot metronidazolu un C vitamīnu.
Tajā pašā laikā OC aktīvo vielu ātru metabolismu novērš:
- Granātābolu sula.
- III paaudzes lipīdu līmeni pazeminošās zāles no statīnu grupas.
Turklāt KPKL var ietekmēt arī zāļu koncentrācijas līmeni asinīs. Tātad, zāles spēj:
- Lai pazeminātu noteiktu zāļu koncentrāciju plazmā no grupas: aldehīdi (Paracetamols), IV paaudzes fluorhinoloni (trovafloksacīns), salicilskābe.
- Palieliniet kofeīna, noteiktu antidepresantu (imipramīna), imūnsupresantu (piemēram, ciklosporīna) ietekmes pakāpi uz ķermeni.
Dimia ir lielisks kontracepcijas līdzeklis, taču pat tas ir jālieto ar ginekologa atļauju.
Visefektīvākā kontracepcijas metode, kas ir populāra Rietumeiropā un Krievijā, ir hormonālo tablešu, tostarp estrogēnu un progestogēnu, lietošana.
Pašlaik ir izstrādātas daudzas dažādas zāles ar minimālām blakusparādībām, no kurām viena ir Dimia. Atsauksmes par šo jauno narkotiku liecina par tās labo panesību un blakusparādību rašanos tikai nelielam skaitam sieviešu.
Zāļu sastāvdaļas
Zāles satur divu veidu tabletes: 24 tabletes, kas satur 0,02 etinilestradiolu un 3 mg drospirenona, un 4 tabletes, kas ir knupji. Tas tiek darīts sieviešu ērtībām. Pirmās 24 tabletes lieto pa vienai katru dienu noteiktā diennakts laikā. Sievietes savā mobilajā tālrunī visbiežāk uzstāda atgādinājumu. Tieši tā sastāvā iekļautie hormoni nodrošina kontracepcijas efektu.
Pēc tam, lai sāktos menstruācijas, ir nepieciešams tablešu lietošanas pārtraukums. 4 placebo tabletes ļauj turpināt lietot Dimia. Lai neapjuktu ar kontracepcijas līdzekļu lietošanu un katru dienu lietotu tabletes, tiek izmantoti šie knupji. Tādējādi tiek nodrošināta pastāvīga kontracepcijas līdzekļu lietošana.
Kā zāles darbojas
Etinilestradiols zāļu sastāvā atbalsta endometrija proliferāciju vai augšanu, tādējādi nodrošinot tā saukto cikla kontroli - starpmenstruālās asiņošanas neesamību Dimia lietošanas laikā. Ārstu komentāri liecina, ka, ja olnīcās nav pietiekama daudzuma estradiola, lietojot jebkuru perorālo kontracepcijas līdzekli, tā ražošanu aizstāj sintētiskais etinilestradiols.

Drospirenons ir sintētisks progestagēns, spironolaktona atvasinājums, kam ir vairākas iedarbības, kas nosaka zāļu kontracepcijas efektu. Šis:
- endometrija sekrēcijas deģenerācija, ko izraisa estrogēns;
- mijiedarbojoties ar progesterona receptoriem, tas novērš gonadotropīnu izdalīšanos no hipofīzes, kas izraisa ovulācijas nomākšanu;
- bloķē citu steroīdu hormonu receptorus: androgēnu, glikokortikoīdu un mineralokortikoīdu, kas samazina dažādu blakusparādību risku, kas raksturīgs dažādiem hormonālajiem kontracepcijas līdzekļiem.
Blakusparādības, lietojot "Dimia"
Tā kā preparātā ir zems hormonu saturs, pareizi lietojot, izteiktas blakusparādības netiek novērotas. To var uzzināt, izlasot atsauksmes. "Dimia" - kontracepcijas tabletes, kas izraisa nelielus nepatīkamus simptomus:
- galvassāpes, reibonis;
- meteorisms, slikta dūša, vemšana;
- diskinēzija;
- pastāvīga mastodinija - piena dziedzeru spriedze;
- asinsspiediena skaitļu paaugstināšanās;
- tromboflebīts;
- traucējumi asins koagulācijas sistēmā;
- krampji;
- nervozitāte, aizkaitināmība, depresija;
- libido samazināšanās;
- ievērojams svara pieaugums;
- asiņošana starp menstruācijām;
- izrāviena asiņošana;
- menstruāciju trūkums pēc zāļu lietošanas.
Katra blakusparādība ir atkarīga no individuālas nepanesības un ieteikumu ievērošanas vai neievērošanas laikā, kad tiek lietotas Dimia kontracepcijas tabletes. Sieviešu atsauksmēs teikts, ka, lietojot šīs tabletes, tiek normalizēta vispārējā pašsajūta, uzlabojas ādas stāvoklis - pazūd seboreja un pinnes, samazinās pietūkums, tiek novērsti pirmsmenstruālā spriedzes simptomi. Asins izpētē tiek noteikts testosterona samazinājums un ir normāli asins olbaltumvielu un lipīdu sastāva rādītāji. Tika atzīmēts, ka, lietojot šīs tabletes 3 mēnešus, sievietes zaudēja vidēji 0,8 kg.

Kontrindikācijas perorālo kontracepcijas līdzekļu lietošanai
Dimia lietošanai ir absolūtas un relatīvas kontrindikācijas. Lietošanas instrukcijas (ārstu atsauksmes par to arī brīdina) aizliedz lietot zāles šādos gadījumos:
- dziļo un virspusējo vēnu tromboze;
- kompleksa ķirurģiska iejaukšanās, pēc kuras tiek nodrošināta ilgstoša rehabilitācija;
- iedzimta trombofilija ar paaugstinātu asins recēšanas līmeni;
- sirds išēmiskā slimība, insults;
- arteriālā hipertensija, kad skaitļi pārsniedz 160 sistolisko un 100 diastolisko spiedienu;
- sarežģītas sirds vārstuļu aparāta slimības;
- divu vai vairāku riska faktoru kombinācija: vecums 35 gadi vai vairāk, smēķēšana vairāk nekā 10 cigaretes dienā, cukura diabēts, hipertensija;
- aknu slimības;
- migrēna ar fokāliem neiroloģiskiem simptomiem un bez tiem;
- cukura diabēts vairāk nekā 20 gadus;
- krūts vēzis;
- grūtniecība un laktācija.
Tāpat nav ieteicams lietot zāles, ja sievietei ir bijusi plaušu embolija. Ir relatīvas kontrindikācijas, kurās ir iespējama zāļu iecelšana, taču tas jādara uzmanīgi pēc sievietes iepriekšējas pārbaudes. Katrā gadījumā Jums jāsāk lietot zāles pēc konsultēšanās ar ārstu.

Cik bieži vajadzētu apmeklēt ārstu
Lietojot Dimia tabletes, sievietei jābūt sava ginekologa uzraudzībā. Par to liecina pacientu atsauksmes. Reizi pusgadā vēlams apmeklēt ginekologu. Šajā gadījumā nepieciešama izmeklēšana ar citoloģisko uztriepes ņemšanu, kolposkopiju, piena dziedzeru palpāciju, asinsspiediena kontroli, nepieciešamības gadījumā speciāla izmeklēšana: ultraskaņa, bioķīmiskā asins analīze u.c.
Pareiza tablešu lietošana
Tikai akušieris-ginekologs, ņemot vērā indikācijas un kontrindikācijas, nosaka Dimia tablešu lietošanas noteikumus. Sieviešu atsauksmes, ka zāles var lietot un parakstīt neatkarīgi, nekaitējot veselībai, nevar uzskatīt par patiesām. Tas var izraisīt nevēlamas komplikācijas.
Sākotnējā perorālo kontracepcijas līdzekļu lietošana jāieceļ no cikla pirmās dienas. Ja tabletes tika lietotas no 5. dienas, papildus ir jāizmanto citas kontracepcijas metodes.
Pēc aborta jebkurā laikā un pēc septiska pārtraukuma uzņemšana tiek uzsākta nekavējoties tajā pašā dienā. Pēc dzemdībām zāles nav norādītas. Ja nav laktācijas, tad var sākt no 21. dienas.

Ir vairāki ieteikumi pacientiem, kuri lieto kontracepcijas tabletes "Dimia". Atsauksmes liecina, ka, ievērojot šos ieteikumus, zāļu negatīvā ietekme uz ķermeni samazināsies. Ārsti iesaka:
- pārstāj smēķēt;
- neizlaidiet tablešu lietošanu;
- lietot tabletes vienlaikus, vēlams pirms gulētiešanas;
- paturiet pa rokai Aizmirsto tablešu noteikumus;
- ja pirmajos trīs menstruālās asiņošanas mēnešos rodas starpmenstruālā asiņošana, jums jākonsultējas ar ārstu, lai noskaidrotu cēloni;
- ar amenoreju ir jāizslēdz grūtniecība;
- ja zāles tiek pārtrauktas, grūtniecība var iestāties pirmajā mēnesī;
- vienlaicīga "Dimia" un antibiotiku vai pretkrampju līdzekļu lietošana samazina kontracepcijas efektu;
- ja rodas vemšana vai caureja, uzņemšana jāpapildina ar citu tableti;
- stipru galvassāpju parādīšanās, sāpes sirdī, akūti redzes traucējumi, elpas trūkums, dzelte, paaugstināts asinsspiediens virs normas liecina, ka ir steidzami jāpārtrauc zāļu lietošana un jākonsultējas ar ārstu.

Zāļu "Dimia" analogi
Zāles ražo Ungārijas uzņēmums Gedeon Richter. "Jess", "Midiana", "Yarina" ir 100% kontracepcijas līdzekļa "Dimia" analogi. Norādījumi, pārskati liecina, ka šo zāļu sastāvs neatšķiras no Ungārijas zālēm, kontracepcijas efekts un blakusparādības ir vienādas, taču Dimia cena ir daudz zemāka, kas ir visērtāk sievietēm, kurām ir jālieto kontracepcijas līdzeklis. gadā.
Ginekoloģisko slimību ārstēšana
Jāatzīmē, ka zāles "Dimia" lieto arī noteiktu slimību ārstēšanai. Ginekologu atsauksmes liecina par tā pozitīvo ietekmi šādu slimību ārstēšanā: endometrioze, fibroids, policistisko olnīcu sindroms, dzelzs deficīta anēmija reproduktīvā vecumā, premenstruālais sindroms un menstruālā cikla disfunkcija.
Arī endometrija hiperplastisko procesu profilaksei tiek izmantotas Dimia tabletes. Atsauksmes par ārstiem, kuri dod priekšroku šai konkrētajai narkotikai, ir pozitīvi. Pēc pacientu pārbaudes zāļu lietošanas laikā viņi atzīmē, ka sievietēm ir ievērojami samazināts endometrija biezums, kas samazina dzemdes, kā arī piena dziedzeru onkoloģisko bojājumu attīstības risku.

Nevar neteikt par Dimia tablešu pozitīvo ietekmi uz reproduktīvo funkciju. Gan ārstu, gan pacientu atsauksmes liecina, ka pēc šo zāļu lietošanas trīs līdz četrus mēnešus (pēc lietošanas pārtraukšanas) rodas abstinences sindroms un iestājas grūtniecība.
balta vai gandrīz balta, apaļa, abpusēji izliekta, ar marķējumu "G73" vienā tabletes pusē, uzklāta ar reljefu; šķērsgriezumā serde ir balta vai gandrīz balta (24 gabali blisterī).
Palīgvielas: laktozes monohidrāts - 48,53 mg, kukurūzas ciete - 16,6 mg, preželatinizēta kukurūzas ciete - 9,6 mg, makrogola un polivinilspirta kopolimērs - 1,45 mg, magnija stearāts - 0,8 mg.
Filmas apvalka sastāvs: Opadry II white 85G18490 - 2 mg (polivinilspirts - 0,88 mg, titāna dioksīds - 0,403 mg, makrogols 3350 - 0,247 mg, talks - 0,4 mg, sojas lecitīns - 0,07 mg).
placebo tabletes
Apvalkotās tabletes zaļa, apaļa, abpusēji izliekta; šķērsgriezumā serde ir balta vai gandrīz balta (4 gabali blisterī).
Palīgvielas: mikrokristāliskā celuloze - 42,39 mg, laktoze - 37,26 mg, preželatinizēta kukurūzas ciete - 9 mg, magnija stearāts - 0,9 mg, koloidālais silīcija dioksīds - 0,45 mg.
Filmas apvalka sastāvs: Opadry II zaļš 85F21389 - 3 mg (polivinilspirts - 1,2 mg, titāna dioksīds - 0,7086 mg, makrogols 3350 - 0,606 mg, talks - 0,444 mg, indigokarmīns - 0,0177 mg, hinolīna oksīds0, irons 0,0 -7 mg krāsviela). 3 mg , krāsviela saulrieta dzeltenā krāsā - 0,003 mg).
28 gab. - blisteri (1) - kartona iepakojumi.
28 gab. - blisteri (3) - kartona iepakojumi.
farmakoloģiskā iedarbība
Dimia ® ir kombinēts vienfāzu perorālais kontracepcijas līdzeklis, kas satur drospirenonu un etinilestradiolu. Pēc tā farmakoloģiskā profila drospirenons ir tuvs dabiskajam progesteronam: tam nav estrogēna, glikokortikoīdu un antiglikokortikoīdu aktivitātes, un tam ir raksturīga izteikta antiandrogēna un mērena antimineralokortikoīdu iedarbība. Kontracepcijas efekts balstās uz dažādu faktoru mijiedarbību, no kuriem svarīgākie ir ovulācijas kavēšana, dzemdes kakla sekrēta viskozitātes palielināšanās un endometrija izmaiņas. Pērļu indekss, rādītājs, kas atspoguļo grūtniecības biežumu 100 sievietēm reproduktīvā vecumā kontracepcijas līdzekļa lietošanas gadā, ir mazāks par 1.
Farmakokinētika
Drospirenons
Sūkšana
Lietojot iekšķīgi, drospirenons ātri un gandrīz pilnībā uzsūcas no kuņģa-zarnu trakta. Drospirenona C max serumā ir aptuveni 38 ng/ml un tiek sasniegta aptuveni 1-2 stundas pēc vienas devas lietošanas.
Bioloģiskā pieejamība - 76-85%. Vienlaicīga lietošana ar pārtiku neietekmē drospirenona biopieejamību.
Izplatīšana
Pēc perorālas lietošanas drospirenona koncentrācija plazmā pazeminājās ar galīgo pusperiodu 31. Drospirenons saistās ar seruma albumīnu un nesaistās ar dzimumhormonus saistošo globulīnu (SHBG) vai kortikosteroīdus saistošo globulīnu (transkortīnu). Tikai 3-5% no kopējās drospirenona koncentrācijas serumā pastāv kā brīvi steroīdi. Etinilestradiola izraisītais SHBG pieaugums neietekmē drospirenona saistīšanos ar seruma olbaltumvielām. Drospirenona vidējais šķietamais V d ir 3,7 ± 1,2 l/kg.
Ārstēšanas cikla laikā C ss max drospirenona līmenis plazmā ir aptuveni 70 ng/ml, tas tiek sasniegts pēc 8 ārstēšanas dienām. Drospirenona koncentrācija serumā palielinās aptuveni 3 reizes, jo ir attiecība starp galīgo T 1/2 un dozēšanas intervālu.
Vielmaiņa
Pēc iekšķīgas lietošanas drospirenons tiek plaši metabolizēts. Galvenie metabolīti asins plazmā ir drospirenona skābās formas, kas veidojas laktona gredzena atvēršanas laikā, un 4,5-dihidrodrospirenona-3-sulfāts, abi veidojas bez P450 sistēmas līdzdalības. Drospirenonu nelielā mērā metabolizē CYP3A4, un tas spēj inhibēt šo enzīmu, kā arī CYP1A1, CYP2C9 un CYP2C19 in vitro.
audzēšana
Drospirenona metabolītu nieru klīrenss serumā ir 1,5±0,2 ml/min/kg. Drospirenons izdalās tikai nelielā daudzumā nemainītā veidā. Drospirenona metabolīti tiek izvadīti caur nierēm un caur zarnām ar ekskrēcijas attiecību aptuveni 1,2:1,4. T 1/2 metabolīti caur nierēm un caur zarnām ir aptuveni 40 stundas.
Etinilestradiols
Sūkšana
Lietojot iekšķīgi, etinilestradiols uzsūcas ātri un pilnībā. C max serumā ir aptuveni 33 pg/ml un tiek sasniegts 1-2 stundu laikā pēc vienreizējas perorālas lietošanas. Absolūtā biopieejamība pirmā loka konjugācijas un pirmā loka metabolisma rezultātā ir aptuveni 60%. Vienlaicīga ēdiena uzņemšana samazināja etinilestradiola biopieejamību aptuveni 25% izmeklēto pacientu; citu izmaiņu nebija.
Izplatīšana
Etinilestradiola koncentrācija serumā samazinājās divfāzu veidā, pēdējā izkliedes fāzē T 1/2 ir aptuveni 24 stundas Etinilestradiols labi, bet nespecifiski saistās ar seruma albumīnu (apmēram 98,5%) un izraisa SHBG koncentrācijas palielināšanos serumā. Šķietamais V d ir aptuveni 5 l/kg.
C ss tiek sasniegts ārstēšanas cikla otrajā pusē, un etinilestradiola koncentrācija serumā palielinās 2-2,3 reizes.
Vielmaiņa
Etinilestradiols ir substrāts presistēmiskai konjugācijai tievās zarnas gļotādā un aknās. Etinilestradiols galvenokārt tiek metabolizēts aromātiskās hidroksilēšanas ceļā, veidojot plašu hidroksilētu un metilētu metabolītu klāstu, kas ir gan brīvā veidā, gan konjugātu veidā ar glikuronskābi. Etinilestradiola metabolītu nieru klīrenss ir aptuveni 5 ml/min/kg.
audzēšana
Neizmainīts etinilestradiols praktiski netiek izvadīts no organisma. Etinilestradiola metabolīti tiek izvadīti caur nierēm un caur zarnām proporcijā 4:6. T 1/2 metabolīti ir aptuveni 24 stundas.
Farmakokinētika īpašās klīniskās situācijās
Nieru darbības traucējumu gadījumā
C ss drospirenona līmenis plazmā sievietēm ar vieglu nieru mazspēju (CC 50-80 ml/min) bija salīdzināms ar atbilstošiem rādītājiem sievietēm ar normālu nieru darbību (CC > 80 ml/min). Sievietēm ar vidēji smagu nieru mazspēju (CC no 30 ml/min līdz 50 ml/min) drospirenona koncentrācija plazmā bija vidēji par 37% augstāka nekā sievietēm ar normālu nieru darbību. Drospirenons bija labi panesams visās grupās. Drospirenonam nebija klīniski nozīmīgas ietekmes uz kālija saturu asins serumā. Farmakokinētika smagas nieru mazspējas gadījumā nav pētīta.
Pārkāpjot aknu darbību
Drospirenonu labi panes pacienti ar viegliem vai vidēji smagiem aknu darbības traucējumiem (B klase pēc Child-Pugh). Farmakokinētika smagu aknu darbības traucējumu gadījumā nav pētīta.
Indikācijas
Perorālā kontracepcija.
Dozēšanas režīms
Tabletes jālieto katru dienu, aptuveni vienā un tajā pašā laikā, uzdzerot nelielu daudzumu ūdens, tādā secībā, kā norādīts uz blistera iepakojuma. Tabletes lieto nepārtraukti 28 dienas, 1 tablete dienā. Tablešu lietošana no nākamā iepakojuma sākas pēc pēdējās tabletes ieņemšanas no iepriekšējā iepakojuma. "Atcelšanas" asiņošana parasti sākas 2-3 dienas pēc placebo tablešu lietošanas sākuma (pēdējā rinda) un ne vienmēr beidzas līdz nākamā iepakojuma sākumam.
Kā sākt lietot Dimia ®
Ja pēdējā mēneša laikā nav lietoti hormonālie kontracepcijas līdzekļi, Dimia ® sāk lietot menstruālā cikla pirmajā dienā (t.i., pirmajā menstruālās asiņošanas dienā). To var sākt lietot arī menstruālā cikla 2.-5.dienā, tādā gadījumā papildus ir nepieciešama kontracepcijas barjermetodes lietošana pirmajās 7 dienās pēc tablešu lietošanas no pirmā iepakojuma.
Pāreja no citiem kombinētiem kontracepcijas līdzekļiem (kombinētās perorālās kontracepcijas tabletes, maksts gredzens vai transdermālais plāksteris)
Dimia® jāsāk lietot nākamajā dienā pēc pēdējās neaktīvās tabletes ieņemšanas (preparātiem, kas satur 28 tabletes) vai nākamajā dienā pēc pēdējās aktīvās tabletes ieņemšanas no iepriekšējā iepakojuma (iespējams, nākamajā dienā pēc parastā 7 dienu pārtraukuma beigām). - preparātiem, kas satur 21 tableti iepakojumā. Ja sieviete lieto maksts gredzenu vai transdermālo plāksteri, Dimia ® ieteicams sākt lietot to noņemšanas dienā vai, vēlākais, dienā, kad plānots ievietot jaunu gredzenu vai plāksteri.
Pāreja no tikai progestogēnu saturošiem kontracepcijas līdzekļiem (minitabletēm, injekcijām, implantiem) vai intrauterīnās sistēmas (IUD), kas atbrīvo progestagēnus.
Sieviete var pāriet no minitabletes uz Dimia ® lietošanu jebkurā dienā (no implanta vai spirāles dienā, kad tās tiek izņemtas, no injicējamām zāļu formām dienā, kad bija jāveic nākamā injekcija), bet visās gadījumos pirmajās 7 tablešu lietošanas dienās ir jāizmanto papildu kontracepcijas barjermetode.
Pēc aborta grūtniecības pirmajā trimestrī
Zāļu Dimia ® lietošanu var sākt pēc ārsta receptes grūtniecības pārtraukšanas dienā. Šajā gadījumā sievietei nav jāveic papildu kontracepcijas līdzekļi.
Pēc dzemdībām vai aborta grūtniecības otrajā trimestrī.
Sievietei ieteicams sākt lietot zāles 21-28 dienā pēc dzemdībām (ar nosacījumu, ka viņa nebaro bērnu ar krūti) vai aborta grūtniecības otrajā trimestrī. Ja uzņemšana tiek uzsākta vēlāk, sievietei jāizmanto papildu kontracepcijas barjermetode pirmajās 7 dienās pēc Dimia® lietošanas uzsākšanas. Atsākot seksuālo aktivitāti (pirms Dimia® lietošanas sākuma), grūtniecība ir jāizslēdz.
Aizmirsto tablešu lietošana
Var ignorēt to, ka pēdējā (4.) blistera rindā trūkst placebo tabletes. Tomēr tie ir jāiznīcina, lai nejauši nepagarinātu placebo fāzi. Tālāk norādītās norādes attiecas tikai uz aizmirstajām tabletēm, kas satur aktīvās sastāvdaļas.
Ja kavēšanās ar tablešu lietošanu bija mazāk nekā 12 stundas, kontracepcijas aizsardzība netiek samazināta. Sievietei jālieto aizmirstā tablete pēc iespējas ātrāk (tiklīdz viņa to atceras) un nākamā tablete parastajā laikā.
Ja vēlu pārsniedz 12 stundas, kontracepcijas aizsardzība var tikt samazināta. Šajā gadījumā jūs varat vadīties pēc diviem pamatnoteikumiem:
1. Tablešu lietošanu nekad nedrīkst pārtraukt ilgāk par 7 dienām;
2. Lai panāktu adekvātu hipotalāma-hipofīzes-olnīcu sistēmas nomākšanu, nepieciešama nepārtraukta tablešu uzņemšana 7 dienas.
Attiecīgi sievietēm var sniegt šādus ieteikumus:
1.-7. diena
Sievietei jāizdzer aizmirstā tablete, tiklīdz viņa to atceras, pat ja tas nozīmē divu tablešu lietošanu vienlaikus. Tad viņai jālieto tabletes parastajā laikā. Nākamās 7 dienas jāizmanto arī barjermetode, piemēram, prezervatīvs. Ja pēdējo 7 dienu laikā ir bijis dzimumakts, jāapsver grūtniecības iespējamība. Jo vairāk tablešu ir izlaists un jo tuvāk ir 7 dienu pārtraukums zāļu lietošanas laikā, jo lielāks ir grūtniecības iestāšanās risks.
8.-14. diena
Sievietei jālieto aizmirstā tablete, tiklīdz viņa to atceras, pat ja tas nozīmē divu tablešu lietošanu vienlaikus. Tad viņai jālieto tabletes parastajā laikā. Ja 7 dienu laikā pirms pirmās aizmirstās tabletes sieviete lietoja tabletes, kā paredzēts, papildu kontracepcijas pasākumi nav nepieciešami. Tomēr, ja viņa izlaidusi vairāk nekā 1 tableti, 7 dienas ir nepieciešama papildu kontracepcijas metode (barjers - piemēram, prezervatīvs).
15.-24. diena
Metodes uzticamība neizbēgami samazinās, tuvojoties placebo tablešu fāzei. Tomēr tablešu režīma korekcija joprojām var palīdzēt novērst grūtniecību. Ja tiek ievērota viena no divām zemāk aprakstītajām shēmām un sieviete ir ievērojusi zāļu lietošanas shēmu iepriekšējās 7 dienās pirms tablešu lietošanas izlaišanas, papildu kontracepcijas līdzekļi nebūs jāizmanto. Ja tas tā nav, viņai ir jāpabeidz pirmā no divām shēmām un jāievēro papildu piesardzības pasākumi nākamās 7 dienas.
1. Sievietei jālieto pēdējā aizmirstā tablete, tiklīdz viņa to atceras, pat ja tas nozīmē divu tablešu lietošanu vienlaikus. Tad viņai jālieto tabletes parastajā laikā, līdz beigsies aktīvās tabletes. Nedrīkst lietot 4 placebo tabletes no pēdējās rindas, nekavējoties jāsāk lietot tabletes no nākamā blistera iepakojuma. Visticamāk, līdz otrā iepakojuma beigām "izņemšanas" asiņošanas nebūs, taču var būt smērēšanās vai "atcelšanas" asiņošana dienās, kad tiek lietotas zāles no otrā iepakojuma.
2. Sieviete var arī pārtraukt aktīvo tablešu lietošanu no iesāktā iepakojuma. Tā vietā viņai ir jālieto placebo tabletes no pēdējās rindas 4 dienas, ieskaitot dienas, kad viņa izlaida tabletes, un pēc tam jāsāk lietot tabletes no nākamā iepakojuma.
Ja sieviete ir izlaidusi tableti un pēc tam placebo tablešu fāzē nejūt "atcelšanas" asiņošanu, jāapsver grūtniecības iespējamība.
Zāļu lietošana kuņģa-zarnu trakta traucējumu gadījumā
Smagu kuņģa-zarnu trakta traucējumu (piemēram, vemšanas vai caurejas) gadījumā zāļu uzsūkšanās būs nepilnīga un būs nepieciešami papildu kontracepcijas pasākumi. Ja vemšana notiek 3-4 stundu laikā pēc aktīvās tabletes lietošanas, pēc iespējas ātrāk jālieto jauna (aizstājēja) tablete. Ja iespējams, nākamā tablete jālieto 12 stundu laikā pēc parastā tablešu lietošanas laika. Ja ir pagājušas vairāk nekā 12 stundas, ieteicams rīkoties saskaņā ar norādījumiem par tablešu izlaišanu. Ja sieviete nevēlas mainīt savu parasto tablešu lietošanas shēmu, viņai papildus jālieto tablete no cita iepakojuma.
Menstruālās asiņošanas "atcelšanas" atlikšana
Lai aizkavētu asiņošanu, sievietei jāizlaiž placebo tablešu lietošana no iesāktā iepakojuma un jāsāk lietot drospirenona + etinilestradiola tabletes no jaunā iepakojuma. Aizkavēšanos var pagarināt, līdz beigsies aktīvās tabletes otrajā iepakojumā. Kavēšanās laikā sievietei var rasties acikliska, bagātīga vai smērējoša asiņošana no maksts. Regulāra Dimia ® lietošana tiek atsākta pēc placebo fāzes.
Lai pārceltu asiņošanu uz citu nedēļas dienu, ir ieteicams saīsināt nākamo placebo tablešu lietošanas posmu par vēlamo dienu skaitu. Ja cikls ir saīsināts, pastāv lielāka iespēja, ka sievietei nebūs menstruācijām līdzīga "atcelšanas" asiņošana, bet, lietojot nākamo iepakojumu, būs acikliska vai smērējoša asiņošana no maksts (tāpat kā ar cikla pagarināšanu).
Blakusefekts
Lietojot Dimia®, ziņots par šādām blakusparādībām:
| Orgānu sistēmu klase | Bieža (≥1/100 līdz | Retāk (≥1/1000 līdz | Reti (≥ 1/10 000 līdz |
| Infekcijas un invāzijas | kandidoze, t.sk. mutes dobums | ||
| No asinīm un limfātiskās sistēmas | anēmija, trombocitopēnija | ||
| No imūnsistēmas puses | alerģiskas reakcijas | ||
| No vielmaiņas un uztura puses | svara pieaugums | palielināta apetīte, anoreksija, hiperkaliēmija, hiponatriēmija, svara zudums | |
| No psihes puses | emocionālā labilitāte | depresija, samazināts libido, nervozitāte, miegainība | anorgasmija, bezmiegs |
| No nervu sistēmas puses | galvassāpes | reibonis, parestēzija | vertigo, trīce |
| No redzes orgāna | konjunktivīts, acs gļotādas sausums, redzes traucējumi | ||
| No sirds un asinsvadu sistēmas puses | migrēna, flebeirisma, asinsspiediena paaugstināšanās | tahikardija, flebīts, asinsvadu bojājumi, deguna asiņošana, ģībonis | |
| No gremošanas sistēmas | slikta dūša, sāpes vēderā | vemšana, caureja | |
| No aknu un žults ceļu puses | sāpes žultspūslī holecistīts | ||
| No ādas un zemādas audiem | izsitumi (ieskaitot pinnes), nieze | hloazma, ekzēma, alopēcija, aknes dermatīts, sausa āda, mezglainā eritēma, hipertrichoze, ādas bojājumi, ādas strijas, kontaktdermatīts, fotodermatīts, ādas mezgliņi | |
| No muskuļu un skeleta sistēmas | muguras sāpes, sāpes ekstremitātēs, muskuļu krampji | ||
| No reproduktīvās sistēmas un piena dziedzeriem | sāpes krūtīs, nav abstinences asiņošanas | maksts kandidoze, iegurņa sāpes, krūšu palielināšanās, fibrocistiskā krūts, maksts izdalījumi, asins pietvīkums vaginīts, acikliska smērēšanās, sāpīga menstruālā asiņošana bagātīga asiņošana "izņemšana", neliela menstruālā asiņošana, maksts gļotādas sausums, citoloģiskā attēla izmaiņas Pap uztriepē | sāpīgs dzimumakts, vulvovaginīts, pēcdzimuma asiņošana, krūšu cista, krūšu hiperplāzija, piena vēzis, dzemdes kakla polipi, endometrija atrofija, olnīcu cista, dzemdes palielināšanās |
| Ir izplatītas traucējumi | astēnija, pastiprināta svīšana, tūska (ģeneralizēta tūska, perifēra tūska, sejas tūska) | diskomforta sajūta |
Sievietēm, kuras lieto kombinētos perorālos kontracepcijas līdzekļus (KPK), ir bijušas šādas nopietnas blakusparādības:
Vēnu trombemboliskas slimības;
Arteriālās trombemboliskās slimības;
Aknu audzēji;
Tādu stāvokļu rašanās vai saasināšanās, kuru saistība ar KPKL lietošanu nav pierādīta: Krona slimība, čūlainais kolīts, epilepsija, migrēna, endometrioze, dzemdes fibroīdi, porfīrija, sistēmiskā sarkanā vilkēde, herpes iepriekšējās grūtniecības laikā, reimatiska horeja, hemolītiska slimība urēmiskais sindroms, holestātiska dzelte;
Hloazma;
Akūtas vai hroniskas aknu slimības gadījumā var būt jāpārtrauc KPKL lietošana, līdz aknu funkcionālie rādītāji normalizējas;
Sievietēm ar iedzimtu angioneirotisko tūsku eksogēni estrogēni var izraisīt vai saasināt angioneirotiskās tūskas simptomus.
Kontrindikācijas lietošanai
Dimia®, tāpat kā citi kombinētie perorālie kontracepcijas līdzekļi, ir kontrindicēts jebkurā no šiem stāvokļiem:
Tromboze (arteriālā un venozā) un trombembolija šobrīd vai anamnēzē (tostarp tromboze, dziļo vēnu tromboflebīts; plaušu embolija, miokarda infarkts, insults, cerebrovaskulāri traucējumi);
Stāvokļi pirms trombozes (ieskaitot pārejošus išēmiskus lēkmes, stenokardiju) pašlaik vai vēsturē;
Vairāki vai izteikti vēnu vai artēriju trombozes riska faktori, t.sk. sarežģīti sirds vārstuļu aparāta bojājumi, priekškambaru mirdzēšana, smadzeņu asinsvadu vai koronāro artēriju slimības; nekontrolēta arteriālā hipertensija, liela operācija ar ilgstošu imobilizāciju, smēķēšana pēc 35 gadu vecuma, aptaukošanās ar ĶMI >30 kg/m 2 ;
Iedzimta vai iegūta nosliece uz vēnu vai artēriju trombozi, piemēram, rezistence pret aktivētu proteīnu C, antitrombīna III deficīts, proteīna C deficīts, proteīna S deficīts, hiperhomocisteinēmija un antivielas pret fosfolipīdiem (antivielu klātbūtne pret fosfolipīdiem - antivielas pret kardikoolipīdiem, antivielas pret cardikoolipine). ;
Pankreatīts ar smagu hipertrigliceridēmiju pašlaik vai anamnēzē;
Smaga hroniska vai akūta nieru mazspēja;
Aknu audzējs (labdabīgs vai ļaundabīgs) šobrīd vai anamnēzē;
No hormoniem atkarīgi dzimumorgānu vai krūts ļaundabīgi audzēji šobrīd vai anamnēzē;
Nezināmas izcelsmes asiņošana no maksts;
Migrēna ar fokusa neiroloģiskiem simptomiem anamnēzē;
Laktāzes deficīts, laktozes nepanesamība, glikozes-galaktozes malabsorbcija, lapp laktāzes deficīts (laktāzes deficīts dažās ziemeļu tautās);
Grūtniecība un aizdomas par to;
laktācijas periods;
Paaugstināta jutība pret zālēm vai kādu no zāļu sastāvdaļām.
AR piesardzību
Trombozes un trombembolijas attīstības riska faktori: smēķēšana līdz 35 gadu vecumam, aptaukošanās, dislipoproteinēmija, kontrolēta arteriālā hipertensija, migrēna bez fokāliem neiroloģiskiem simptomiem, nekomplicēta sirds vārstuļu slimība, iedzimta nosliece uz trombozi (tromboze, miokarda infarkts vai smadzeņu asinsrites traucējumi) jauns vecums vienā no tuvākajiem radiniekiem);
Slimības, kurās var rasties perifērās asinsrites traucējumi: cukura diabēts bez asinsvadu komplikācijām, sistēmiskā sarkanā vilkēde (SLE), hemolītiski-urēmiskais sindroms, Krona slimība, čūlainais kolīts, sirpjveida šūnu anēmija, virspusējo vēnu flebīts;
iedzimta angioneirotiskā tūska;
Hipertrigliceridēmija;
Smaga aknu slimība (pirms aknu funkcionālo testu normalizēšanas);
Slimības, kas pirmo reizi parādījās vai saasinājās grūtniecības laikā vai uz iepriekšējas dzimumhormonu uzņemšanas fona (tostarp dzelte un/vai nieze, kas saistīta ar holestāzi, holelitiāze, otoskleroze ar dzirdes traucējumiem, porfīrija, herpes grūtniecības laikā anamnēzē, neliela horeja (Sidenham slimība). ), hloazma);
pēcdzemdību periods.
Lietojiet grūtniecības un laktācijas laikā
Zāles Dimia® ir kontrindicētas grūtniecības laikā.
Ja grūtniecība iestājas Dimia® lietošanas laikā, tā nekavējoties jāpārtrauc. Paplašinātos epidemioloģiskajos pētījumos nav konstatēts ne paaugstināts iedzimtu defektu risks bērniem, kas dzimuši sievietēm, kuras pirms grūtniecības lietojušas KPKL, ne teratogēna iedarbība, ja KPKL tās nejauši lietotas grūtniecības laikā.
Saskaņā ar preklīniskajiem pētījumiem nevar izslēgt nevēlamas blakusparādības, kas ietekmē grūtniecības gaitu un augļa attīstību aktīvo komponentu hormonālās darbības dēļ.
Zāles Dimia ® var ietekmēt laktāciju: samazināt piena daudzumu un mainīt tā sastāvu. KPKL lietošanas laikā neliels daudzums kontracepcijas steroīdu un/vai to metabolītu var izdalīties pienā. Šīs summas var ietekmēt bērnu. Zāļu Dimia® lietošana zīdīšanas laikā ir kontrindicēta.
Pieteikums par aknu darbības traucējumiem
Kontrindicēts:
Esoša (vai anamnēzē) smaga aknu slimība, ja aknu darbība pašlaik nav normāla;
Aknu audzējs (labdabīgs vai ļaundabīgs) pašlaik vai vēsturē.
Pieteikums par nieru darbības traucējumiem
Kontrindicēts:
Smaga hroniska vai akūta nieru mazspēja
Lietošana bērniem
Zāļu lietošana pirms menarhijas sākuma nav norādīta.
Speciālas instrukcijas
Ja pastāv kāds no tālāk minētajiem stāvokļiem/riska faktoriem, KPKL lietošanas ieguvumi katrai sievietei jāizvērtē individuāli un jāapspriež ar viņu pirms lietošanas uzsākšanas. Ja blakusparādība pasliktinās vai parādās kāds no šiem stāvokļiem vai riska faktoriem, sievietei jāsazinās ar savu ārstu. Ārstam jāizlemj, vai pārtraukt KPKL lietošanu.
Asinsrites traucējumi
Jebkuru kombinēto perorālo kontracepcijas līdzekļu lietošana palielina venozās trombembolijas (VTE) risku. Palielināts VTE risks ir visizteiktākais pirmajā gadā, kad sieviete lieto kombinētos perorālos kontracepcijas līdzekļus.
Epidemioloģiskie pētījumi liecina, ka VTE sastopamība sievietēm bez riska faktoriem, kuras lietoja nelielas estrogēna devas.
Dati no liela, perspektīva, 3 grupu pētījuma parādīja, ka VTE sastopamība sievietēm ar vai bez citiem venozās trombembolijas riska faktoriem, kuras lietoja etinilestradiola un drospirenona kombināciju 0,03 mg + 3 mg, sakrita ar VTE biežumu sievietes, kuras lietoja levonorgestrelu saturošus perorālos kontracepcijas līdzekļus un citus rokas datorus. Venozās trombembolijas riska pakāpe, lietojot Dimia®, vēl nav noteikta.
Epidemioloģiskie pētījumi arī atklāja saistību starp KPKL lietošanu un paaugstinātu arteriālās trombembolijas (miokarda infarkta, pārejošu išēmisku traucējumu) risku.
Sievietēm, kuras lieto perorālos kontracepcijas līdzekļus, ļoti reti ir novērota citu asinsvadu, piemēram, aknu vēnu un artēriju, apzarņa, nieru, smadzeņu vai tīklenes tromboze. Nav vienprātības par šo parādību saistību ar hormonālo kontracepcijas līdzekļu lietošanu.
Venozu vai arteriālu trombotisku/trombembolisku notikumu vai akūtu smadzeņu asinsrites traucējumu simptomi:
Neparastas vienpusējas sāpes un/vai apakšējo ekstremitāšu pietūkums;
Pēkšņas stipras sāpes krūtīs neatkarīgi no tā, vai tās izstaro uz kreiso roku vai nē;
pēkšņs elpas trūkums;
Pēkšņs klepus sākums;
jebkādas neparastas smagas ilgstošas galvassāpes;
Pēkšņs daļējs vai pilnīgs redzes zudums;
Diplopija;
Runas traucējumi vai afāzija;
Vertigo;
Kolapss ar vai bez daļējiem epilepsijas lēkmēm;
Vājums vai ļoti jūtams nejutīgums, kas pēkšņi skar vienu ķermeņa pusi vai vienu daļu;
Kustību traucējumi;
Simptomu komplekss "akūts" vēders.
Pirms KPKL lietošanas sievietei jākonsultējas ar speciālistu.
Risks vēnu trombembolijas traucējumi
Palielinot vecumu;
iedzimta predispozīcija (venozā trombembolija kādreiz ir bijusi brāļiem un māsām vai vecākiem salīdzinoši agrā vecumā);
Ilgstoša imobilizācija, progresīva operācija, jebkura ķirurģiska iejaukšanās apakšējās ekstremitātēs vai liela trauma. Šādās situācijās ir ieteicams pārtraukt zāļu lietošanu (plānotas ķirurģiskas iejaukšanās gadījumā vismaz četras nedēļas iepriekš) un atsākt ne agrāk kā divas nedēļas pēc pilnīgas mobilitātes atjaunošanas. Ja zāļu lietošana nav iepriekš pārtraukta, jāapsver antikoagulantu terapija;
Vienprātības trūkums par varikozu vēnu un virspusēja tromboflebīta iespējamo lomu vēnu trombozes parādīšanā vai saasināšanā.
Risks arteriālas trombemboliskas komplikācijas vai akūts cerebrovaskulārs negadījums Lietojot KPKL, palielinās ar:
Palielinot vecumu;
Smēķēšana (sievietēm, kas vecākas par 35 gadiem, ir ļoti ieteicams pārtraukt smēķēšanu, ja viņas vēlas lietot KPKL);
Dislipoproteinēmija;
arteriālā hipertensija;
Migrēnas bez fokāliem neiroloģiskiem simptomiem;
Aptaukošanās (ĶMI virs 30 kg/m2);
Iedzimta predispozīcija (artēriju trombembolija brāļiem un māsām vai vecākiem salīdzinoši agrā vecumā). Ja ir iespējama iedzimta predispozīcija, sievietei pirms KPKL lietošanas jākonsultējas ar speciālistu;
Sirds vārstuļu bojājumi;
Priekškambaru fibrilācija.
Kontrindikācija var būt arī viena liela vēnu slimības riska faktora vai vairāku artēriju slimības riska faktoru klātbūtne. Jāapsver arī antikoagulantu terapija. Sievietēm, kuras lieto KPKL, ir atbilstoši jāinformē ārsts, ja ir aizdomas par trombozes simptomiem. Ja ir aizdomas par trombozi vai to apstiprina, KPKL lietošana jāpārtrauc. Nepieciešams uzsākt adekvātu alternatīvu kontracepciju antikoagulantu terapijas (netiešie antikoagulanti - kumarīna atvasinājumi) teratogēnuma dēļ.
Jāņem vērā paaugstināts trombembolijas risks pēcdzemdību periodā.
Citi veselības stāvokļi, kas saistīti ar nevēlamiem asinsvadu notikumiem, ir cukura diabēts, sistēmiskā sarkanā vilkēde, hemolītiski urēmiskais sindroms, hroniska iekaisīga zarnu slimība (Krona slimība vai čūlainais kolīts) un sirpjveida šūnu anēmija.
Migrēnas biežuma vai smaguma palielināšanās KPKL lietošanas laikā var būt norāde uz tūlītēju kombinēto perorālo kontracepcijas līdzekļu atcelšanu.
Audzēji
Nozīmīgākais dzemdes kakla vēža attīstības riska faktors ir inficēšanās ar cilvēka papilomas vīrusu. Dažos epidemioloģiskajos pētījumos ziņots par paaugstinātu dzemdes kakla vēža risku, ilgstoši lietojot kombinētos perorālos kontracepcijas līdzekļus, taču joprojām pastāv pretrunīgi viedokļi par to, cik lielā mērā šie atklājumi ir saistīti ar vienlaicīgiem faktoriem, piemēram, dzemdes kakla vēža testēšanu vai barjermetožu izmantošanu. par kontracepciju.
54 epidemioloģisko pētījumu metaanalīze atklāja nelielu krūts vēža relatīvā riska (RR = 1,24) palielināšanos sievietēm, kuras pašlaik lieto KPKL. Risks pakāpeniski samazinās 10 gadu laikā pēc KPKL lietošanas pārtraukšanas. Jo krūts vēzis reti attīstās sievietēm, kas jaunākas par 40 gadiem, KPKL lietotāju diagnosticēto krūts vēža gadījumu skaita palielināšanās maz ietekmē kopējo krūts vēža iespējamību. Šajos pētījumos netika atrasti pietiekami pierādījumi par cēloņsakarību. Palielināts risks var būt saistīts ar agrāku krūts vēža diagnozi KPKL lietotājiem, KPKL bioloģisko ietekmi vai abu kombināciju. Diagnosticētais krūts vēzis sievietēm, kuras jebkad lietojušas KPKL, bija klīniski mazāk smaga slimības agrīnas diagnostikas dēļ.
Retos gadījumos sievietēm, kuras lieto KPKL, ir bijuši labdabīgi aknu audzēji un vēl retāk ļaundabīgi aknu audzēji. Dažos gadījumos šie audzēji bija dzīvībai bīstami intraabdominālas asiņošanas dēļ. Tas jāņem vērā, veicot diferenciāldiagnozi stipru vēdera sāpju, aknu palielināšanās vai intraabdominālas asiņošanas pazīmju gadījumā.
Citi štati
Dimia ® progestagēna sastāvdaļa ir aldosterona antagonists, kas saglabā kāliju organismā. Vairumā gadījumu kālija satura pieaugums nav gaidāms. Tomēr klīniskā pētījumā dažiem pacientiem ar vieglu vai vidēji smagu nieru slimību, kuri lietoja kāliju aizturošas zāles, drospirenona lietošanas laikā kālija līmenis serumā nedaudz palielinājās. Tādēļ pacientiem ar nieru mazspēju, kuriem kālija līmenis serumā pirms ārstēšanas un īpaši kāliju aizturošu zāļu lietošanas laikā, pirmajā ārstēšanas ciklā ir ieteicams kontrolēt kālija līmeni serumā.
Sievietēm ar hipertrigliceridēmiju vai iedzimtu noslieci uz to, lietojot KPKL, var palielināties pankreatīta risks.
Lai gan daudzām sievietēm, kuras lieto KPKL, tika novērots neliels asinsspiediena paaugstinājums, klīniski nozīmīgs paaugstinājums bija reti. Tikai šajos retos gadījumos ir nepieciešama tūlītēja KPKL lietošanas pārtraukšana. Ja, lietojot KPKL pacientiem ar vienlaikus arteriālo hipertensiju, pastāvīgi paaugstinās asinsspiediens vai
Pārdozēšana
Dimia ® pārdozēšanas gadījumi vēl nav bijuši. Pamatojoties uz vispārējo pieredzi ar kombinēto perorālo kontracepcijas līdzekļu lietošanu, potenciāls simptomiem pārdozēšana var būt: slikta dūša, vemšana, nedaudz izteikta asiņošana no maksts.
Ārstēšana: nav pretlīdzekļu. Ārstēšanai jābūt simptomātiskai.
zāļu mijiedarbība
Citu zāļu ietekme uz Dimia ®
Perorālo kontracepcijas līdzekļu un citu zāļu mijiedarbība var izraisīt aciklisku asiņošanu un/vai kontracepcijas neveiksmi. Tālāk aprakstītā mijiedarbība ir atspoguļota zinātniskajā literatūrā.
Mijiedarbības mehānisms ar hidantoīnu, barbiturātiem, primidonu, karbamazepīnu un rifampicīnu; Okskarbazepīns, topiramāts, felbamāts, ritonavīrs, grizeofulvīns un asinszāles (Hypericum perforatum) preparāti ir balstīti uz šo aktīvo vielu spēju inducēt mikrosomālos aknu enzīmus. Maksimālā mikrosomālo aknu enzīmu indukcija netiek sasniegta 2-3 nedēļu laikā, bet pēc tam tā saglabājas vismaz 4 nedēļas pēc zāļu terapijas pārtraukšanas.
Ir ziņots arī par kontracepcijas neveiksmi, lietojot antibiotikas, piemēram, ampicilīnu un tetraciklīnu. Šīs parādības mehānisms nav skaidrs.
Sievietēm ar īslaicīgu (līdz vienai nedēļai) kādu no iepriekšminētajām zāļu grupām vai atsevišķām zālēm papildus PDA jālieto īslaicīgi (citu zāļu vienlaicīgas lietošanas laikā un vēl 7 dienas pēc tās pabeigšanas). , kontracepcijas barjermetodes.
Sievietēm, kuras saņem terapiju ar rifampicīnu, papildus KPKL lietošanai jāizmanto kontracepcijas barjermetode un jāturpina tā lietošana 28 dienas pēc rifampicīna terapijas pārtraukšanas. Ja vienlaikus lietotās zāles ilgst ilgāk par iepakojumā esošo aktīvo tablešu derīguma termiņu, neaktīvo tablešu lietošana jāpārtrauc un nekavējoties jāsāk lietot drospirenona + etinilestradiola tabletes no nākamā iepakojuma.
Ja sieviete pastāvīgi lieto zāles - mikrosomālo aknu enzīmu induktorus, viņai jāizmanto citas uzticamas nehormonālas kontracepcijas metodes.
Galvenie drospirenona metabolīti cilvēka plazmā veidojas bez citohroma P450 sistēmas līdzdalības. Tāpēc maz ticams, ka citohroma P450 inhibitori varētu ietekmēt drospirenona metabolismu.
Dimia ® ietekme uz citām zālēm
Perorālie kontracepcijas līdzekļi var ietekmēt dažu citu aktīvo vielu metabolismu. Attiecīgi šo vielu koncentrācija asins plazmā vai audos var vai nu palielināties (piemēram, ciklosporīns), vai samazināties (piemēram, lamotrigīns).
Pamatojoties uz in vitro inhibīcijas un in vivo mijiedarbības pētījumiem brīvprātīgajām sievietēm, kuras tika ārstētas ar omeprazolu, simvastatīnu un midazolāmu kā substrātu, drospirenona 3 mg devas ietekme uz citu aktīvo vielu metabolismu ir maz ticama.
Citas mijiedarbības
Pacientiem bez nieru mazspējas vienlaicīga drospirenona un AKE inhibitoru vai NPL lietošana būtiski neietekmē kālija saturu asins serumā. Tomēr zāļu Dimia ® vienlaicīga lietošana ar aldosterona antagonistiem vai kāliju aizturošiem diurētiskiem līdzekļiem nav pētīta. Šajā gadījumā pirmajā ārstēšanas ciklā ir nepieciešams kontrolēt kālija koncentrāciju serumā.
Laboratorijas testi
Kontracepcijas steroīdu lietošana var ietekmēt dažu laboratorisko pārbaužu rezultātus, tostarp aknu, vairogdziedzera, virsnieru un nieru darbības bioķīmiskos parametrus, plazmas olbaltumvielu (transportera) koncentrāciju, piemēram, kortikosteroīdus saistošos proteīnus un lipīdu/lipoproteīnu frakcijas, ogļhidrātu metabolisma parametrus un parametrus. asins recēšanu un fibrinolīzi. Kopumā izmaiņas paliek normālo vērtību robežās. Drospirenons izraisa plazmas renīna aktivitātes palielināšanos un mazās antimineralokortikoīdu aktivitātes dēļ samazina aldosterona koncentrāciju plazmā.
Uzglabāšanas noteikumi un nosacījumi
Zāles jāuzglabā bērniem nepieejamā vietā, sargājot no gaismas temperatūrā, kas nepārsniedz 25°C. Derīguma termiņš - 2 gadi.
Izsniegšanas noteikumi no aptiekām
Zāles tiek izsniegtas pēc receptes.