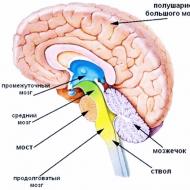
Nāvējošo indīgo gāzu saraksts un to ietekme uz cilvēkiem. Galvenie gāzu veidi Oglekļa dioksīds un tā nozīme
Šķidrs un gāzveida. Gandrīz jebkurš šķidrums var iegūt katru no atlikušajiem diviem. Daudzas cietās vielas, kūstot, iztvaikojot vai degot, var papildināt gaisa saturu. Bet ne katra gāze var kļūt par cietu materiālu vai šķidrumu sastāvdaļu. Ir dažādi gāzu veidi, kas atšķiras viens no otra pēc īpašībām, izcelsmes un pielietojuma iezīmēm.
Definīcija un īpašības
Gāze ir viela, ko raksturo starpmolekulāro saišu neesamība vai minimāla vērtība, kā arī daļiņu aktīvā mobilitāte. Galvenās visu veidu gāzu īpašības:
- Šķidrums, deformējamība, nepastāvība, vēlme pēc maksimālā tilpuma, atomu un molekulu reakcija uz temperatūras pazemināšanos vai paaugstināšanos, kas izpaužas kā to kustības intensitātes maiņa.
- Tie pastāv temperatūrā, kurā spiediena palielināšanās neizraisa pāreju uz šķidru stāvokli.
- Viegli saspiežams, samazinās apjoms. Tas atvieglo transportēšanu un lietošanu.
- Lielākā daļa tiek sašķidrināti, saspiežot noteiktās spiediena un kritisko siltuma vērtību robežās.
Pētījumu nepieejamības dēļ tie tiek aprakstīti, izmantojot šādus pamatparametrus: temperatūra, spiediens, tilpums, molārā masa.
Klasifikācija pēc depozīta
Dabiskajā vidē visa veida gāzes ir atrodamas gaisā, zemē un ūdenī.
- Gaisa sastāvdaļas: skābeklis, slāpeklis, oglekļa dioksīds, argons, slāpekļa oksīds ar neona, kriptona, ūdeņraža, metāna piemaisījumiem.
- Zemes garozā slāpeklis, ūdeņradis, metāns un citi ogļūdeņraži, oglekļa dioksīds, sēra oksīds un citi atrodas gāzveida un šķidrā stāvoklī. Cietajā frakcijā ir arī gāzes nogulsnes, kas sajauktas ar ūdens slāņiem aptuveni 250 atm spiedienā. salīdzinoši zemā temperatūrā (līdz 20˚С).
- Rezervuāros ir šķīstošās gāzes – hlorūdeņradis, amonjaks un slikti šķīstošās gāzes – skābeklis, slāpeklis, ūdeņradis, oglekļa dioksīds u.c.
Dabas liegumi krietni pārsniedz iespējamo mākslīgi izveidoto daudzumu.

Klasifikācija pēc uzliesmojamības pakāpes
Visu veidu gāzes, atkarībā no to uzvedības īpašībām aizdegšanās un sadegšanas procesos, iedala oksidētājos, inertās un uzliesmojošās.
- Oksidētāji veicina degšanu un veicina degšanu, bet paši nedeg: gaiss, skābeklis, fluors, hlors, slāpekļa oksīds un dioksīds.
- Inerti nepiedalās degšanā, bet tiem ir tendence izspiest skābekli un samazināt procesa intensitāti: hēlijs, neons, ksenons, slāpeklis, argons,
- Uzliesmojošas vielas aizdegas vai eksplodē kopā ar skābekli: metāns, amonjaks, ūdeņradis, acetilēns, propāns, butāns, etāns, etilēns. Lielākajai daļai no tiem ir raksturīga sadegšana tikai noteikta gāzu maisījuma sastāva apstākļos. Pateicoties šim īpašumam, mūsdienās gāze ir visizplatītākais degvielas veids. Šajā gadījumā tiek izmantots metāns, propāns un butāns.

Oglekļa dioksīds un tā loma
Tā ir viena no visbiežāk sastopamajām gāzēm atmosfērā (0,04%). Normālā temperatūrā un atmosfēras spiedienā tā blīvums ir 1,98 kg/m3. Tas var būt cietā un šķidrā stāvoklī. Cietā fāze notiek pie negatīva siltuma līmeņa un nemainīga atmosfēras spiediena; to sauc par "sauso ledu". CO 2 šķidrā fāze ir iespējama, palielinoties spiedienam. Šis īpašums tiek izmantots uzglabāšanai, transportēšanai un tehnoloģiskām vajadzībām. Sublimācija (pāreja uz gāzveida stāvokli no cietas, bez šķidrās starpfāzes) iespējama pie -77 - -79˚С. Šķīdība ūdenī attiecībā 1:1 tiek realizēta pie t=14-16˚С.
Atkarībā no to izcelsmes izšķir oglekļa dioksīda veidus:
- Augu un dzīvnieku atkritumi, vulkānu emisijas, gāzu emisijas no zemes zarnām, iztvaikošana no rezervuāru virsmas.
- Cilvēku darbības rezultāti, tostarp emisijas no visa veida degvielas sadegšanas.

Kā noderīgu vielu to izmanto:
- Oglekļa dioksīda ugunsdzēšamos aparātos.
- Balonos loka metināšanai atbilstošā CO 2 vidē.
- Pārtikas rūpniecībā kā konservants un ūdens gāzēšanai.
- Kā aukstumaģents īslaicīgai dzesēšanai.
- Ķīmiskajā rūpniecībā.
- Metalurģijā.
Būdams planētas, cilvēku, mašīnu un veselu rūpnīcu dzīves neaizstājams komponents, tas uzkrājas atmosfēras apakšējā un augšējā slānī, aizkavējot siltuma izdalīšanos un radot “siltumnīcas efektu”.

un viņa lomu
Starp dabiskas izcelsmes un tehnoloģiskiem nolūkiem vielām ir tādas, kurām ir augsta uzliesmojamības pakāpe un siltumspēja. Uzglabāšanai, transportēšanai un lietošanai tiek izmantoti šādi sašķidrinātās gāzes veidi: metāns, propāns, butāns, kā arī propāna-butāna maisījumi.
Butāns (C 4 H 10) un propāns ir naftas gāzu sastāvdaļas. Pirmais sašķidrinās pie -1 - -0,5˚С. Tīra butāna transportēšana un izmantošana salnā laikā netiek veikta tā sasalšanas dēļ. Sašķidrināšanas temperatūra propānam (C 3 H 8) -41 - -42˚C, kritiskais spiediens - 4,27 MPa.
Metāns (CH 4) ir galvenā sastāvdaļa.Gāzes avotu veidi - naftas atradnes, biogēno procesu produkti. Sašķidrināšana notiek, pakāpeniski saspiežot un samazinot siltumu līdz -160 - -161˚С. Katrā posmā tas tiek saspiests 5-10 reizes.
Sašķidrināšana tiek veikta īpašās iekārtās. Propāns, butāns, kā arī to maisījums sadzīves un rūpnieciskai lietošanai tiek ražots atsevišķi. Metānu izmanto rūpniecībā un kā degvielu transportā. Pēdējo var izdot arī saspiestā veidā.

Saspiestā gāze un tās loma
Pēdējā laikā saspiestā dabasgāze ir ieguvusi popularitāti. Ja propānam un butānam izmanto tikai sašķidrināšanu, tad metānu var izdalīt gan sašķidrinātā, gan saspiestā stāvoklī. Gāzei balonos zem augsta spiediena 20 MPa ir vairākas priekšrocības salīdzinājumā ar labi zināmo sašķidrināto gāzi.
- Augsts iztvaikošanas ātrums, arī pie negatīvas gaisa temperatūras, negatīvu uzkrāšanās parādību trūkums.
- Zemāks toksicitātes līmenis.
- Pilnīga sadegšana, augsta efektivitāte, nav negatīvas ietekmes uz aprīkojumu un atmosfēru.
To arvien vairāk izmanto ne tikai kravas automašīnām, bet arī vieglajām automašīnām, kā arī katlu iekārtām.

Gāze ir neuzkrītoša, bet cilvēka dzīvībai neaizstājama viela. Dažu no tiem augstā siltumspēja attaisno dažādu dabasgāzes komponentu plašu izmantošanu kā degvielu rūpniecībā un transportā.
Gāzes, iespējams, ir visbīstamākās toksiskās vielas. Lielākā daļa no tām ir bez smaržas un bezkrāsas, un tāpēc vielas iedarbību nevar uzreiz atpazīt. Lai izvairītos no negatīvām sekām, jāzina, kuras gāzes ir indīgākās, simptomi, kas rodas, saskaroties ar tām, kā arī pirmā palīdzība.
Starp toksiskajām vielām gāzes ir vismānīgākās. Atšķirībā no šķidrumiem un cietām vielām, tie izplatās visā telpas tilpumā, un šim sadalījumam nav robežu. Ļoti bieži indīgai gāzei nav ne krāsas, ne smaržas, tās klātbūtne var būt kāda cilvēka neuzmanības vai ļauna nolūka rezultāts, un saindēšanos var neatpazīt uzreiz. Zināšanas par šādu indu īpašībām, drošības noteikumu un civilās aizsardzības standartu ievērošana, kā arī spēja sniegt pirmo palīdzību ir jūsu drošības atslēga.
Jēdzieni “indīga gāze” un “gāze kā vielas agregācijas stāvoklis” fizikā un ķīmijā ir nedaudz atšķirīgi.
Tādējādi pie pirmajiem pieder dažādi aerosoli un gaistoši šķidrumi, kuru iztvaikošanas temperatūra ir cilvēkam “ērtos” apstākļos.
Šādas toksiskas vielas var klasificēt divējādi – pēc mērķa un darbības principa.
Praktiska lietošana
Savādi, ka lielākā daļa šo vielu nav paredzētas, lai kādu saindētu. Viņiem ir pilnīgi likumīgi pielietojumi, un tie tiek aktīvi izmantoti saimniecībā. Tātad, saskaņā ar lietošanas kritēriju, tos var iedalīt:
- (BOV);
- rūpniecībā un sadzīvē izmantojamās vielas;
- ķīmisko reakciju blakusprodukti.
Pirmajā grupā ietilpst šādas gāzes un aerosoli: ciānūdeņražskābe, ciānhlorīds, sinepju gāze, zarīns un vairāki fosfora savienojumi. Otrajā ietilpst hlors, amonjaks un dažādi dezinfekcijas līdzekļi, bet trešajā - sērūdeņradis, oglekļa monoksīds un slāpekļa oksīdi (visi tie ir indīgi).
Darbības princips
Jebkuras vielas toksicitāte izpaužas dažādos veidos, un gāzes nav izņēmums. Simptomi, ko izraisa toksisko gāzu iekļūšana organismā, ievērojami atšķiras. Pēc darbības principa izšķir šādas grupas:
- nervu paralītisks, tas ir, izraisot vispārēju vai lokālu paralīzi;
- tulznas, kas iznīcina ādu;
- smacējošs;
- asaru;
- psihotomimētiķis;
- kairinošas gļotādas;
- vispārēja toksicitāte.
Dažiem ir sarežģīta ietekme uz ķermeni.
Toksisko vielu raksturojums
Lai atšķirtu toksiskas vielas vienu no otras, jums jāzina to fizikālās un ķīmiskās īpašības. Liela nozīme ir arī iespējai atrast vielu noteiktā vietā un tās koncentrācijai. Nāves iespēja no indīgās gāzes iedarbības ir atkarīga no pēdējās. Tabulu sarakstā ir parādīti daži to rekvizīti.
| indīga viela | ķīmiskā formula | fizikālās īpašības | darbības princips | letāla koncentrācija |
| hlors | Cl2 | dzeltenzaļa gāze ar saldenu smaržu, smagāka par gaisu | asfiksējošs, ieelpojot plaušās, veidojas sālsskābe | 6 mg/m3 |
| C4H10FO2P | Bezkrāsains un bez smaržas šķidrums, gaistošs 20 grādu temperatūrā | nervu gāze | 70 mg/m3 uz 1 elpošanas minūti | |
| sinepju gāze | C4H8Cl2S | Bezkrāsains šķidrums ar ķiploku vai sinepju smaržu | pūslīši, iznīcina šūnu membrānas; ļoti agresīvs | jebkuros daudzumos |
| oglekļa monoksīds, oglekļa monoksīds (II), oglekļa monoksīds | CO | toksiska gāze, bezkrāsaina un bez smaržas | vispārēji toksisks, traucē orgānu apgādi ar skābekli | 29 mg/m3 |
| fosgēns | COCl2 | bezkrāsaina indīga gāze ar sapuvuša siena smaku | smacējošs | 4 mg/m3 |
| slāpekļa oksīds (IV) | NĒ | brūnā gāze, rūpnieciskie atkritumi | asfiksējošs, veido slāpekļskābi plaušās | 40 mg/m3 |
| ciānūdeņražskābe | HCN | bezkrāsains, iztvaiko 26 grādos | vispārēji toksisks, bloķē skābekļa plūsmu audos | 11 mg/m3 |
| adamsīts | C12H19AsClN | dzeltens pulveris, ko izmanto kā aerosolu | kairinošs gļotādām | 1 g vienai personai |
| BZ | C21H23NO3 | bezkrāsaini kristāli, izsmidzināmi | psihomimētiskais BOV, izraisa akūtu psihozi ar halucinācijām | nav konstatēts, efekts ir spēkā 80 stundas, lietojot 1 mg vienai personai |
| brombenzilcianīds | C8H6BrN | bezkrāsains šķidrums | asaru | 4 2 minūtēs |
| lewisite | C2H2AsCl3 | brūns šķidrums ar spēcīgu ģerānijas smaržu | pūslīši un vispārēji toksiski | 5-10 mg uz kg svara |
| Ūdeņraža sulfīds | H2S | gāze ar sapuvušu olu smaku | vispārējs toksisks un nervu paralītisks | 0,1% |
| cianogēna hlorīds | ClCN | bezkrāsaina gāze ar asu smaku | vispārēji toksisks, līdzīgi kā ciānūdeņražskābe, iekļūst gāzmaskas filtrā | 0,4 mg/l, nāve 1 minūtes laikā |
Kur gaida briesmas
Ķīmisko kaujas līdzekļu kategorijā ietilpst tādas vielas kā zarīns, sinepju gāze, fosgēns, adamsīts, ciānhlorīds, leizīts, ciānūdeņražskābe, hloracetofenons, CS, CR, somans, VX, CX, difenilcianarsīns, hloropikrīns. Tie ir iekļauti aizliegto lietojumu sarakstos kaujas operāciju laikā, taču, acīmredzot, dažās militārajās vienībās tie ir pieejami. Par to liecina fakts, ka civilās aizsardzības un skolas dzīvības drošības kursos joprojām māca gāzmaskas uzvilkšanas iemaņas, bet militārajās daļās - ķīmiskās aizsardzības tērpus (CHS). Pretlīdzekļi pret vairākām ķīmiskajām vielām ir iekļauti militārajās pirmās palīdzības komplektos.
Dažas ķīmiskās kaujas vielas tiek izmantotas pilnīgi miermīlīgiem nolūkiem. Piemēram:
- fosgēnu izmanto krāsvielu un polikarbonāta ražošanai;
- ciānūdeņražskābe un tās atvasinājumi - ieguves rūpniecībā, plastmasas ražošanā, kā herbicīds;
Hlora gāzi izmanto kā dezinfekcijas līdzekli, tāpēc mucas ar zaļu svītru, kur tā tiek glabāta, atrodas centralizētajā ūdensapgādē iesaistītajos uzņēmumos.
Sērūdeņradi nelielos daudzumos ražo dzīvi organismi, un tas veidojas arī to sadalīšanās laikā. Tā atradusi savu vietu ķīmiskajā rūpniecībā un medicīnā – sērūdeņraža vannas ir viena no atsevišķu slimību rehabilitācijas sastāvdaļām.
To ražo arī uzņēmumos, un to izmanto minerālmēslu un gāzes ģeneratoru maisījumu ražošanai. Taču ikdienā tas nav vajadzīgs un ir cilvēka darbības blakusprodukts. Tas ir atrodams transportlīdzekļu izplūdes gāzēs un veidojas sildīšanas ierīču nepareizas lietošanas dēļ.
Atbrīvošanas veidlapas
Nodaļa ar šo nosaukumu ir veltīta tiem, kam patīk staigāt pa pamestām rūpnīcām, militārajām vienībām un doties tur, kur nevajadzētu. Pirms izvēlaties iepakojumu ar dažiem burtiem un cipariem, ir vērts noskaidrot vismaz to dekodēšanu.
Jāsaka, ka ne vienmēr ir vienādi. Dažādas nozares ir pieņēmušas dažādas marķēšanas sistēmas, un par citu valstu standartiem nav ko teikt. Bet indēm ir viens universāls apzīmējums, un tas izskatās šādi:
Iespējams, ka nav trīsstūra, bet galvaskauss ir obligāts, ja runa ir par uzglabāšanas konteineriem. Var būt arī brīdinājumi ar vārdiem “nāvējoši” un “nāvējoši”. Kaujas vienības to var nesaturēt, galu galā tās nav radītas dekorēšanai.
| BOV | Krievu marķējumi | Amerikāņu marķējums | atbrīvošanas forma | Piezīme |
| zarīns | R-35 | GB | metāla mucas un konteineri lietošanai termosa izmērā, stikla pērlītes | dažreiz jūs varat atrast nosaukumu T-144 un T-46 (trilons) |
| soman | R-55 | G.D. | līdzīgas mucas un čaumalas | |
| vi-gāze | VR | VX-GAS | mucas, čaumalas | izmanto kā pesticīdu |
| ciānūdeņražskābe | parasti uzrakstiet ķīmisko formulu | A.C. | dažādi plastmasas konteineri un citi neitrāli materiāli | izmanto kā deratizācijas līdzekli |
| cianogēna hlorīds | izmanto rūpniecībā, uzrakstiet nosaukumu un formulu | CK | lielas tvertnes, zem spiediena | pesticīdu un krāsu produkts |
| cianogēna bromīds | līdzīgs cianogēna hlorīdam | sausā veidā (pulverī), jo tas ir sprādzienbīstams | ||
| fosgēns | R-10 | C.G. | mucas un cilindri | |
| difosgēns | D.P. | cisternas un baloni – tikai starpkonteineri | izmanto fosgēna ražošanā | |
| sinepju gāze | R-5, VR-16 | H, HD, VV | dažāda izmēra mucas un čaumalas | |
| slāpekļa sinepes | HN | mucas, čaumalas | ||
| lewisite | R-43 | L | mucas, tanki | izmanto ražošanai |
| difenilhlorarsīns | D.A. | Pirmajā pasaules karā to izmantoja bumbās, mucās un gāzes dzinējos | cits vārds: Klārks I | |
| adamsīts | R-15 | DM | mucas | iespējams, guļ Baltijas jūras dzelmē |
| ceriņi | ceriņi | C.S. | aerosola kārbas | pieejams bezmaksas pārdošanai |
| dibenzoksazepīns | algogēns | CR | aerosola kārbas | pārdod veikalos kā individuālos aizsardzības līdzekļus |
| hloracetofenons | putnu ķirsis | CN | baloni, smidzināšanas kannas, dūmu bumbas | |
| brombenzilcianīds | kamit | C.A. | nav lietots kopš Pirmā pasaules kara | |
| hloropikrīns | nitrohloroforms | plastmasas konteiners | lauksaimniecības pesticīds, inde | |
| BZ | R-78 | BZ | pulveris; pielietošana – caur aerosola ģeneratoru | pastāv aviācijas kasešu veidā |
Ja tev nepaveicas
Vairumā gadījumu saindēšanās ar gāzi ir ārkārtējs notikums. Senākos laikos cilvēki dzīvoja ar krāsns apkuri, un tas notika biežāk; Vēlāk, kad ķīmiskās vielas nonāca karadarbībā, šādas saindēšanās kļuva par problēmu, un līdz šim lielākā daļa valstu ir ratificējušas Ķīmisko ieroču konvenciju. Taču vienošanās ir viena lieta, bet prakse ir pavisam kas cits. Cilvēki turpina mirt dažādu apstākļu dēļ.
Ja jūs nonākat saskarē ar indīgu gāzi, jums vajadzētu pievērst uzmanību kādai no šīm pazīmēm:

Ja konstatējat sevī kādas pazīmes, nekavējoties konsultējieties ar ārstu; Dažas gāzes var jūs paralizēt salīdzinoši īsā laikā.
Savlaicīga pretindes ievadīšana un pirmā palīdzība ļaus glābt dzīvību un vismaz dažas veselības paliekas.
Lietvārds, m., lietots. salīdzināt bieži Morfoloģija: (nē) kas? gāze un gāze, ko? gāze, (skat) ko? gāze, kas? gāze, par ko? par gāzi un par gāzi; pl. Kas? gāzes, (nē) ko? gāzes, kāpēc? gāzes, (es redzu) ko? gāzes, ko? gāzes, par ko? par gāzēm 1. Gāze ir... ... Dmitrijeva vārdnīca
BEZKRĀSAMS- BEZKRĀSAIS, bezkrāsains, bezkrāsains; bezkrāsains, bezkrāsains, bezkrāsains. 1. Bez krāsas, krāsojuma. Bezkrāsaina gāze. 2. trans. Blāvi, neievērojami, neoriģināli. Bezkrāsains stils. Ušakova skaidrojošā vārdnīca. D.N. Ušakovs. 1935 1940 ... Ušakova skaidrojošā vārdnīca
bezkrāsains- ak, ak; desmit, tna, tno. 1. Bez krāsas, izteikta krāsa. B. gāze. Lietots šķidrums. B. laka. Lietotas acis, mati. B o seja. 2. Trūkst oriģinalitātes, izteiksmīguma; nekas īpašs, parasts. B. stāsts. Bth loma. Otrā dzīve. ◁…… enciklopēdiskā vārdnīca
bezkrāsains- ak, ak; desmit, tna, tno. Skatīt arī bezkrāsains, bezkrāsains 1) Bez krāsas, izteikta krāsa. Bezkrāsaina gāze. Lietots šķidrums. Caurspīdīga laka. B y... Daudzu izteicienu vārdnīca
Oglekļa dioksīds, oglekļa dioksīda gāze- bezkrāsaina gāze, kas vielmaiņas rezultātā veidojas audos un ar asinsriti tiek transportēta uz plaušām, no kurienes elpošanas laikā tiek izelpota (šīs gāzes koncentrācijas palielināšana asinīs stimulē elpošanas procesu). Nelielos daudzumos oglekļa dioksīds...... Medicīniskie termini
Oglekļa monoksīds- Oglekļa monoksīds Vispārīgs Sistemātiskais nosaukums Oglekļa monoksīds Ķīmiskā formula ... Wikipedia
Smieklu gāze- Slāpekļa oksīds(I) Vispārīgs Sistemātiskais nosaukums Slāpekļa oksīds(I) Ķīmiskā formula N2O Rel. molekulārā masa 44 a. e.m... Vikipēdija
Purva gāze vai metāns- (arī metilūdeņradis, formēns) piesātināts ogļūdeņradis ar sastāvu CH4, pirmais sērijas СnН2n+n dalībnieks, viens no vienkāršākajiem oglekļa savienojumiem, ap kuru grupējas visi pārējie un no kura tos var iegūt, aizvietojot atomus. .. ... Enciklopēdiskā vārdnīca F.A. Brokhauss un I.A. Efrons
Oglekļa dioksīds- Oglekļa dioksīds Citi nosaukumi oglekļa dioksīds, oglekļa dioksīds, sausais ledus (ciets) Formula CO2 Molārais ... Wikipedia
STO Gazprom 5.12-2008: Dabiski uzliesmojoša gāze. Sēru saturošu komponentu noteikšana ar hromatogrāfijas metodi- Terminoloģija STO Gazprom 5.12 2008: Dabiski uzliesmojoša gāze. Sēru saturošu komponentu noteikšana ar hromatogrāfijas metodi: karbonilsulfīds COS: toksiska, bezkrāsaina gāze, kas dažkārt atrodas HGP. Termina definīcijas no dažādiem dokumentiem: ... ... Normatīvās un tehniskās dokumentācijas terminu vārdnīca-uzziņu grāmata
Oglekļa dioksīds- oglekļa dioksīds (a. oglekļa dioksīds; n. Kohlensaure, gasformige Kohlensaure, Kohlendioxyd; f. gaz carbonique; i. gas carbonico), oglekļa anhidrīds (CO2). U.g. ir bezkrāsaina gāze ar viegli skābu garšu un smaržu; blīvuma relatīvais...... Ģeoloģiskā enciklopēdija
Definīcija
Dabasgāze ir minerāls gāzveida stāvoklī. To plaši izmanto kā degvielu. Bet pati dabasgāze netiek izmantota kā degviela, tās sastāvdaļas tiek atdalītas no tās atsevišķai lietošanai.
Dabasgāzes sastāvs
Līdz 98% dabasgāzes ir metāns, tajā ietilpst arī metāna homologi - etāns, propāns un butāns. Dažreiz var būt oglekļa dioksīds, sērūdeņradis un hēlijs. Tas ir dabasgāzes sastāvs.
Fizikālās īpašības
Dabasgāze ir bezkrāsaina un bez smaržas (ja tā nesatur sērūdeņradi), tā ir vieglāka par gaisu. Uzliesmojošs un sprādzienbīstams.
Tālāk ir sniegtas sīkākas dabasgāzes komponentu īpašības.
Dabasgāzes atsevišķu komponentu īpašības (apsveriet detalizētu dabasgāzes sastāvu)
Metāns(CH4) ir bezkrāsaina gāze bez smaržas, vieglāka par gaisu. Tas ir viegli uzliesmojošs, taču to joprojām var viegli uzglabāt.
Etāns(C2H6) ir bezkrāsaina, bez smaržas un bezkrāsas gāze, nedaudz smagāka par gaisu. Arī uzliesmojošs, bet netiek izmantots kā degviela.
Propāns(C3H8) ir bezkrāsaina gāze bez smaržas, indīga. Tam ir noderīga īpašība: propāns sašķidrinās zemā spiedienā, kas ļauj to viegli atdalīt no piemaisījumiem un transportēt.
Butāns(C4H10) – tā īpašības ir līdzīgas propānam, bet tam ir lielāks blīvums. Divreiz smagāks par gaisu.
Oglekļa dioksīds(CO2) ir bezkrāsaina gāze bez smaržas ar skābu garšu. Atšķirībā no citām dabasgāzes sastāvdaļām (izņemot hēliju), oglekļa dioksīds nedeg. Oglekļa dioksīds ir viena no vismazāk toksiskajām gāzēm.
Hēlijs(Viņš) ir bezkrāsains, ļoti viegls (otra vieglākā gāze pēc ūdeņraža), bezkrāsains un bez smaržas. Īpaši inerts, normālos apstākļos nereaģē ne ar vienu no vielām. Nedeg. Tas nav toksisks, bet paaugstinātā spiedienā, tāpat kā citas inertās gāzes, var izraisīt narkozi.
Ūdeņraža sulfīds(H2S) ir bezkrāsaina smaga gāze ar sapuvušu olu smaku. Ļoti indīgs, pat ļoti zemā koncentrācijā izraisa ožas nerva paralīzi.
Dažu citu gāzu īpašības, kas neietilpst dabasgāzē, bet kuru pielietojums ir tuvu dabasgāzes izmantošanai
Etilēns(C2H4) – bezkrāsaina gāze ar patīkamu smaržu. Tās īpašības ir līdzīgas etānam, bet atšķiras no tā ar mazāku blīvumu un uzliesmojamību.
Acetilēns(C2H2) ir ļoti viegli uzliesmojoša un sprādzienbīstama bezkrāsaina gāze. Spēcīgas saspiešanas rezultātā var eksplodēt. Ikdienā to neizmanto ļoti augsta aizdegšanās vai sprādziena riska dēļ. Galvenais pielietojums ir metināšanas darbos.
Pieteikums
Metāns izmanto kā degvielu gāzes plītis.
Propāns un butāns– kā degviela dažās automašīnās. Šķiltavas pilda arī ar sašķidrinātu propānu.
Etāns To reti izmanto kā degvielu; tā galvenais lietojums ir etilēna ražošana.
Etilēns ir viena no visvairāk ražotajām organiskajām vielām pasaulē. Tā ir izejviela polietilēna ražošanai.
Acetilēns izmanto ļoti augstu temperatūru radīšanai metalurģijā (metālu pārbaudei un griešanai). Acetilēns Tas ir ļoti viegli uzliesmojošs, tāpēc netiek izmantots kā degviela automašīnās, un arī bez tā stingri jāievēro tā uzglabāšanas nosacījumi.
Ūdeņraža sulfīds, neskatoties uz savu toksicitāti, nelielos daudzumos izmanto t.s. sērūdeņraža vannas. Tie izmanto dažas no sērūdeņraža antiseptiskajām īpašībām.
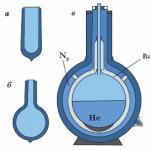
Galvenais noderīgais īpašums hēlijs ir tā ļoti zemais blīvums (7 reizes vieglāks par gaisu). Baloni un dirižabļi ir piepildīti ar hēliju. Ūdeņradis ir pat vieglāks par hēliju, bet tajā pašā laikā viegli uzliesmojošs. Ar hēliju piepūsti baloni ir ļoti populāri bērnu vidū.
Toksicitāte
Oglekļa dioksīds. Pat liels oglekļa dioksīda daudzums neietekmē cilvēka veselību. Tomēr tas novērš skābekļa uzsūkšanos, ja saturs atmosfērā ir no 3% līdz 10% pēc tilpuma. Pie šādas koncentrācijas sākas nosmakšana un pat nāve.
Hēlijs. Hēlijs normālos apstākļos ir pilnīgi netoksisks sava inerces dēļ. Bet ar paaugstinātu asinsspiedienu sākas anestēzijas sākuma stadija, līdzīgi kā smieklu gāzes* iedarbība.
Ūdeņraža sulfīds. Šīs gāzes toksiskās īpašības ir lieliskas. Ilgstoši pakļaujoties ožas sajūtai, rodas reibonis un vemšana. Arī ožas nervs ir paralizēts, tāpēc rodas ilūzija par sērūdeņraža neesamību, bet patiesībā organisms to vienkārši vairs nejūt. Saindēšanās ar sērūdeņradi notiek koncentrācijā 0,2–0,3 mg/m3, koncentrācija virs 1 mg/m3 ir letāla.
Degšanas process
Visi ogļūdeņraži, pilnībā oksidējoties (pārmērīgs skābeklis), izdala oglekļa dioksīdu un ūdeni. Piemēram:
CH4 + 3O2 = CO2 + 2H2O
Nepilnīgas (skābekļa trūkuma) gadījumā - oglekļa monoksīds un ūdens:
2CH4 + 6O2 = 2CO + 4H2O
Ar vēl mazāku skābekļa daudzumu izdalās smalki izkliedēts ogleklis (kvēpi):
CH4 + O2 = C + 2H2O.
Metāns deg ar zilu liesmu, etāns ir gandrīz bezkrāsains, tāpat kā alkohols, propāns un butāns ir dzelteni, etilēns ir gaišs, oglekļa monoksīds ir gaiši zils. Acetilēns ir dzeltenīgs un stipri smēķē. Ja jums mājās ir gāzes plīts un ierastās zilās liesmas vietā redzat dzeltenu, ziniet, ka metāns tiek atšķaidīts ar propānu.
Piezīmes
Hēlijs, atšķirībā no jebkuras citas gāzes, nepastāv cietā stāvoklī.
Smieklu gāze ir slāpekļa oksīda N2O triviālais nosaukums.
Komentāri un raksta papildinājumi ir komentāros.