血小板凝集を阻害するという意味です。 血小板凝集阻害剤。 ADPによる血小板凝集
27.1。 血小板凝集を抑制する薬(抗血小板薬)
血小板は、骨髄巨核球の断片として形成される小さな円盤状の血球です。 血小板は血液中を 6 ~ 12 日間循環し、その後組織のマクロファージによって捕捉されます。
血管内皮は血小板の機能活性に影響を与えます。 内皮細胞は血流中にプロスタサイクリン (プロスタグランジン I 2) と一酸化窒素 - NO で識別される内皮弛緩因子を分泌します。 これらの物質は血小板の凝集を防ぎます。 さらに、内皮細胞は血液凝固を軽減し、血栓溶解を促進する物質を分泌します。 これらすべてが、無傷の血管内皮の抗血栓形成特性を提供します。
さまざまな要因(機械的外傷、感染症、血管壁のアテローム性動脈硬化性変化、血圧上昇など)によって血管内皮が損傷した場合、内皮の抗血栓形成特性が低下し、次のような状態が生じます。血栓の形成。 プロスタサイクリンと内皮弛緩因子の合成が損なわれるため、接触が促進されます。
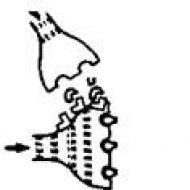
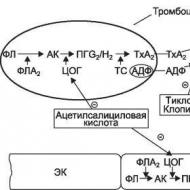
内皮表面が損傷した血小板。 血小板は損傷部位に蓄積し、血管内皮下と相互作用します。直接またはフォン・ヴィレブランド因子(活性化された血小板および内皮細胞によって分泌される)を介して、血管内皮下に局在する特定の糖タンパク質の関与により、コラーゲンおよび他の内皮下タンパク質に結合します。血小板膜。 フォン・ヴィレブランド因子は血小板膜の糖タンパク質Ibに結合し、コラーゲンは血小板膜の糖タンパク質Iaに結合する(図27-1を参照)。 血小板に対するコラーゲン(および血栓形成の初期段階ですでに局所的に少量形成されるトロンビン)の影響により、血小板の状態の変化、つまり活性化が引き起こされます。 血小板はその形状を変化させ(円板状から多くの過程を経て平らになり、仮足になります)、血管の損傷した表面を覆います。
血小板は活性化されると、さまざまな生理活性物質を放出します。これらの物質は、活性化されていない血小板では顆粒内に存在します(α顆粒、緻密顆粒)。 緻密な顆粒は、血小板凝集を刺激する物質、つまり ADP とセロトニンの宝庫です。 血小板顆粒からのこれらの物質の放出は、血小板に対するコラーゲン、トロンビン、およびADP自体を含む他の凝集誘導物質の作用下での細胞内Ca 2+ 濃度の増加の結果として起こります。 血流に放出された ADP は、血小板膜に局在する特定の (プリン作動性) 受容体を刺激します。 Gタンパク質に関連する受容体(P2Y 12 プリン作動性受容体)を介して、ADPはアデニル酸シクラーゼの阻害およびcAMPレベルの低下を引き起こし、それが血小板細胞質におけるCa 2 レベルの増加をもたらす(図27-2)。
さらに、血小板が活性化されると、膜リン脂質からのアラキドン酸の生成に関与する酵素である血小板膜のホスホリパーゼ A 2 の活性が増加します。 アラキドン酸からの血小板では、シクロオキシゲナーゼの影響下で、環状エンドペルオキシド(プロスタグランジン G 2 / H 2)が最初に合成され、それらからトロンボキサンシンの参加により合成されます。
テターゼ、トロンボキサン A 2 が形成されます。これは血小板凝集の活性刺激因子であり、血管収縮因子です。 血流に放出された後、トロンボキサン A 2 は血小板膜上のトロンボキサン受容体を刺激します。 その結果、ホスホリパーゼ C は、これらの受容体に関連する Cq タンパク質を通じて活性化され、
米。 27-1.血管壁の損傷による血小板の接着と凝集: EC - 内皮細胞。 PV - フォン・ヴィレブランド係数。 TxA 2 - トロンボキサン A 2; PGI 2 - プロスタサイクリン。 NO - 内皮弛緩因子。 GP - 糖タンパク質。 GP llb/lla - llb/lla 糖タンパク質 (出典: Katzung B.G. Bazic and Clinical Pharmacology - ニューヨーク、2001 年、修正済み)
イノシトール-1,4,5-三リン酸は、血小板の細胞内貯蔵所からのCa 2+ の放出を促進します(血小板におけるカルシウム貯蔵所の役割は、緻密な尿細管のシステムによって行われます)。 これは、Ca 2+ の細胞質濃度の増加をもたらします (図 27-2)。 トロンボキサン A 2 は、血管平滑筋細胞内の Ca 2+ 濃度の増加を引き起こし、血管収縮を引き起こします。

米。 27-2. 抗血小板薬(アセチルサリチル酸、チクロピジン、エポプロステノール)の作用機序: EC - 内皮細胞。 PL - 細胞膜のリン脂質。 AA - アルキドン酸; PLA 2 - ホスホリパーゼ A 2; COX - シクロオキシゲナーゼ。 TS - トロンボキサン合成酵素。 PS - プロスタサイクリン合成酵素。 PGG 2 /H 2 - 環状エンドペルオキシド; TxA 2 - トロンボキサン A 2; PGI 2 - プロスタサイクリン。 AC - アデニル酸シクラーゼ。 FLS - ホスホリパーゼ C; IP 3 - イノシトール-1,4,5-三リン酸
したがって、ADP およびトロンボキサン A 2 は、血小板細胞質内の Ca 2+ レベルを増加させます。 細胞質 Ca 2+ は、血小板膜の糖タンパク質 IIb / IIIa の立体構造に変化を引き起こし、その結果、糖タンパク質はフィブリノーゲンに結合する能力を獲得します。 1 つのフィブリノーゲン分子には糖タンパク質 IIb / IIIa に対する 2 つの結合部位があるため、2 つの血小板を結合できます (図 27-3)。 フィブリノーゲン架橋による多くの血小板の結合により、血小板凝集体の形成が引き起こされます。
逆に、血小板凝集はプロスタサイクリン (プロスタグランジン I 2) の影響を受けます。 トロンボキサン、プロスタサイクリンなど
環状エンドペルオキシドから形成されますが、別の酵素であるプロスタサイクリン合成酵素の作用下にあります。 プロスタサイクリンは内皮細胞によって合成され、血流に放出され、そこで血小板膜のプロスタサイクリン受容体を刺激し、Gs タンパク質アデニル酸シクラーゼを介してプロスタサイクリン受容体と結合します。 その結果、血小板中のcAMPレベルが増加し、細胞質Ca 2+ 濃度が減少する(図27-2を参照)。 これにより、IIb/IIIa 糖タンパク質の構造変化が妨げられ、糖タンパク質はフィブリノーゲンに結合する能力を失います。 したがって、プロスタサイクリンは血小板の凝集を防ぎます。 プロスタサイクリンの作用により、血管平滑筋細胞内の Ca 2+ 濃度が減少し、血管拡張が起こります。

血小板凝集につながる主なイベントの以下の順序を区別できます (スキーム 27-1 を参照)。
現在臨床現場で使用されている抗血小板薬の主な作用方向は、トロンボキサン A 2 および ADP の作用の除去、ならびに血小板膜の糖タンパク質 IIb / IIIa の遮断に関連しています。 異なる作用機序の物質も使用され、血小板中のcAMP濃度を増加させ、その結果、血小板中のCa 2+ 濃度を低下させる。
血小板凝集を低下させる薬剤には次のグループがあります。
2 . - シクロオキシゲナーゼ阻害剤:
アセチルサリチル酸。

スキーム27.1。 血小板凝集のメカニズム
シクロオキシゲナーゼおよびトロンボキサン合成酵素阻害剤: インドブフェン。
プロスタサイクリン受容体を刺激する薬剤:
エポプロステノール**。
血小板に対する ADP の作用を妨げる手段:
チクロピジン; クロピドグレル。
血小板ホスホジエステラーゼを阻害する手段:
ジピリダモール
血小板膜の糖タンパク質 IIb/IIIa をブロックする薬剤。
モノクローナル抗体: アブシキシマブ。
合成糖タンパク質 IIb/IIIa ブロッカー: エプチフィバチド; ティロフィバン。
トロンボキサン A の合成を阻害する薬剤 2
アセチルサリチル酸 (アスピリン*) は、よく知られた抗炎症剤、鎮痛剤、解熱剤です。 現在、抗血小板薬として広く使用されています。 アセチルサリチル酸の抗血小板効果は、血小板におけるトロンボキサン A 2 の合成に対するその阻害効果と関連しています。
アセチルサリチル酸はシクロオキシゲナーゼを不可逆的に阻害し(酵素の不可逆的なアセチル化を引き起こす)、その結果、アラキドン酸からのトロンボキサン A 2 およびプロスタグランジンの前駆体である環状エンドペルオキシドの形成を妨害します。 したがって、アセチルサリチル酸の作用下では、血小板におけるトロンボキサンA 2 の合成が減少するだけでなく、血管内皮細胞におけるプロスタサイクリンの合成も減少する(図27-2を参照)。 しかし、適切な用量と投与計画を選択することによって、トロンボキサン A 2 の合成に対するアセチルサリチル酸の優先的な効果を達成することが可能です。 これは、血小板と内皮細胞の大きな違いによるものです。
非核細胞である血小板にはタンパク質再合成システムがないため、シクロオキシゲナーゼを合成できません。 したがって、この酵素が不可逆的に阻害されると、トロンボキサン A 2 合成は血小板の生涯を通じて損なわれます。 7〜10日以内に。 新しい血小板が生成されるため、アセチルサリチル酸の抗血小板効果の持続期間が短くなるため、安定した薬効(トロンボキサン濃度の安定した低下)を得るには、アセチルサリチル酸を処方することが推奨されます。 1日1回です。
血管内皮細胞ではシクロオキシゲナーゼの再合成が起こり、アセチルサリチル酸を摂取すると数時間以内にこの酵素の活性が回復します。 したがって、1日1回薬を処方した場合、プロスタサイクリン合成の大幅な減少は起こりません。

さらに、アセチルサリチル酸の約 30% は肝臓で初回通過代謝を受けるため、体循環中のアセチルサリチル酸の濃度は門脈血中よりも低くなります。 その結果、アセチルサリチル酸は、全身血管の内皮細胞よりも門脈循環を循環する血小板に対して高濃度で作用します。 したがって、血小板におけるトロンボキサン A 2 の合成を抑制するには、内皮細胞におけるプロスタサイクリンの合成を抑制するよりも少ない用量のアセチルサリチル酸が必要である。
これらの理由により、アセチルサリチル酸の投与量と投与頻度が増加すると、プロスタサイクリン合成に対する阻害効果がより顕著になり、抗血小板効果が低下する可能性があります。 これらの特徴に関連して、抗血小板薬としてのアセチルサリチル酸は、1 日 1 回、少量(平均 100 mg)で処方されることが推奨されます。
抗血小板剤として、アセチルサリチル酸は、心筋梗塞、虚血性脳卒中、末梢血管血栓症の予防、冠動脈バイパス移植や冠動脈形成術中の血栓の形成を防ぐために、不安定狭心症に使用されます。 アセチルサリチル酸は、75〜160 mg(いくつかの適応症によると、50〜325 mgの用量範囲)の用量で1日1回、長期間経口的に処方されます。 現在、医師は血栓症の予防を目的としたアセチルサリチル酸製剤を自由に使用できます。これには、腸溶性コーティング錠(アセカルドール *、アスピコール *、カルディオピリン *、アスピリン カーディオ *、ノバンドール *、トロンボ ACC * など アセチルサリチル酸の抗血小板効果はすぐに現れます (20 ~ 30 分以内)。 腸溶性コーティング剤形は作用の開始がより遅くなりますが、長期間使用すると、その有効性は従来の錠剤の有効性と実質的に同じになります。 より早く効果を得るには、アセチルサリチル酸錠剤を噛む必要があります。
アセチルサリチル酸の主な副作用は、シクロオキシゲナーゼの阻害に関連しています。 これにより、分泌抑制効果と胃保護効果のあるプロスタグランジン E 2 および I 2 の生成が妨げられます (胃の壁側細胞による塩酸の分泌が減少し、粘液と重炭酸塩の分泌が増加します)。 その結果、たとえ短期間の使用であっても、アセチルサリチル酸は胃および十二指腸の上皮に損傷を引き起こす可能性があります(潰瘍形成効果)。 腸溶性コーティングを施した剤形を使用すると、胃粘膜への影響はそれほど顕著ではありません。 アセチルサリチル酸を使用すると、胃腸出血やその他の出血性合併症が発生する可能性があります。 このような合併症のリスクは、アセチルサリチル酸を 100 mg/日以下の用量で使用すると低くなります。 COX の選択的阻害により、アラキドン酸の変換および気管支収縮特性を持つロイコトリエンの形成のためのリポキシゲナーゼ経路が活性化されます。 気管支喘息患者において、アセチルサリチル酸は発作(「アスピリン喘息」)の発症を引き起こす可能性があります。 アレルギー反応が起こる可能性があります。
アセチルサリチル酸の潰瘍形成作用を軽減するために、水酸化マグネシウムを含む複合製剤カルジオマグニル * が提案されました。 水酸化マグネシウムは胃内の塩酸を中和し(制酸作用)、粘膜への損傷を軽減します。 この薬は、虚血性脳卒中の二次予防など、アセチルサリチル酸と同じ適応症に使用されます。
インドブフェン (イブストリン *) は、シクロオキシゲナーゼとトロンボキサン合成酵素を阻害しながら、トロンボキサン A 2 の合成を減少させます。 アセチルサリチル酸とは異なり、インドブフェンはシクロオキシゲナーゼの可逆的な阻害を引き起こします。 この薬を服用すると、プロスタサイクリンの量が相対的に増加します(プロスタサイクリン / トロンボキサン A 2 の比率が増加します)。 インドブフェンは血小板の接着と凝集を阻害します。 使用法、副作用等はアセチルサリチル酸と同様です。
プロスタサイクリン受容体を刺激する薬剤
血小板凝集を軽減する別の方法は、プロスタサイクリン受容体を刺激することです。 この目的のために、使用します
プロスタサイクリン・エポプロステノール * の調製。 プロスタサイクリンの作用は、血小板だけでなく血管の緊張に対してもトロンボキサン A 2 の作用とは逆です。 血管拡張と血圧低下を引き起こします。 プロスタサイクリンのこの効果は肺高血圧症に利用されます。 プロスタサイクリンは血中で急速に破壊され(t 1/2 約2分)、長く持続しないため、この薬は点滴によって投与されます。 エポプロステノール*は作用時間が短いため、抗血小板薬としては広く使用されていません。 エポプロステノールの抗血小板作用の用途として考えられるのは、体外循環における血小板凝集の防止です。
血小板に対するADPの作用を妨げる薬剤
チクロピジン (ticlid*) は、ADP によって引き起こされる血小板凝集を阻害するチエノピリジン誘導体です。 チクロピジンはプロドラッグであり、その抗血小板効果はミクロソーム肝酵素の関与による活性代謝物の形成に関連しています。 チクロピジン代謝物にはチオール基が含まれており、それを介して血小板膜の P2Y 12 プリン作動性受容体に不可逆的に結合します。 これにより、血小板に対する ADP の刺激効果が消失し、血小板中の細胞質 Ca 2+ 濃度が減少します。 その結果、血小板膜における糖タンパク質IIb / IIIaの発現およびフィブリノーゲンへのそれらの結合が減少します(図27-2を参照)。 作用の不可逆的な性質により、チクロピジンには長期にわたる抗血小板効果があります。
チクロピジンの継続使用による最大の効果は7~11日(活性代謝産物の作用の形成と発達に必要な時間)後に達成され、薬物の中止後もその効果は血小板の生涯を通じて持続します(7~10日)。 。
チクロピジンは、虚血性脳卒中の二次予防、下肢の閉塞性疾患、冠動脈バイパス移植術および冠動脈ステント留置術における血栓症の予防に処方されます。 この薬は、1日2回食事と一緒に経口摂取すると効果的です。
チクロピジンの使用は副作用のため制限されています。 食欲の低下、吐き気、嘔吐、下痢 (20%)、腹痛、皮膚の発疹 (11 ~ 14%) が発生する場合があります。 了解しました
血漿中のアテローム生成リポタンパク質のレベルの増加。 出血は、抗血小板薬の使用に伴う一般的な合併症です。 危険な合併症は好中球減少症で、治療開始から最初の 3 か月の間に患者の 1 ~ 2.4% に発生します。 血小板減少症、無顆粒球症、非常にまれに再生不良性貧血の可能性があります。 この点において、治療の最初の数か月間は、血液画像の系統的なモニタリングが必要です。
クロピドグレル (Plavix*、Zylt*) は、化学構造、主な効果、作用機序がチクロピジンに似ています。 チクロピジンと同様に、これはプロドラッグであり、肝臓で代謝されて活性代謝物を形成します。 血小板凝集の有意な阻害は治療の2日目から認められ、最大の効果は4~7日後に達成されます。 服用を中止しても効果は7~10日間持続します。 クロピドグレルは活性においてチクロピジンよりも優れており、1日量75mgで、1日量500mgのチクロピジンと同じ血小板凝集の減少と出血時間の延長を引き起こします。

クロピドグレルは、不耐性があるため、アセチルサリチル酸と同じ適応症に使用されます。 食事摂取量に関係なく、1日1回経口摂取してください。 クロピドグレルはアセチルサリチル酸と組み合わせることができます。これは、これらの薬物が血小板凝集のさまざまなメカニズムを阻害し、相互の作用を高めるためです(ただし、この組み合わせでは出血性合併症のリスクが高くなります)。
チクロピジンと比較して、クロピドグレルの副作用はそれほど顕著ではありません(下痢 - 4.5%、発疹 - 6%)。 クロピドグレルの使用は、好中球減少症 (0.1%) などの重篤な合併症のリスクが低下し、血小板減少症の発生頻度が低くなります。 まれな合併症として、チクロピジンと同様に、血栓性血小板減少性紫斑病が発生することがあります。
血小板ホスホジエステラーゼを阻害する薬剤
ジピリダモール (キュランチル*、ペルサンチン*) は、冠動脈拡張剤として最初に提案されました。 その後、血小板凝集を阻害する能力が明らかになりました。 現在、ジピリダモールは主に血栓症の予防のための抗血小板薬として使用されています。 ジピリダモールの抗血小板効果は、血小板中のcAMPレベルの増加と関連しており、その結果、血小板中の細胞質Ca 2+ 濃度が減少します。 これはいくつかの理由で発生します。 まず、ジピリダモールは、cAMP を不活性化するホスホジエステラーゼを阻害します。 さらに、ジピリダモールは、内皮細胞および赤血球によるアデノシンの取り込みとその代謝を阻害し(アデノシンデアミナーゼを阻害)、それによって血中のアデノシンレベルを増加させます(図27-4)。 アデノシンは血小板 A 2 受容体を刺激し、これらの受容体に関連するアデニル酸シクラーゼの活性を増加させます。その結果、血小板における cAMP の形成が増加し、細胞質 Ca 2+ レベルが減少します。 ジピリダモールはまた、血管平滑筋細胞の cAMP レベルを増加させ、血管弛緩を引き起こします。

ジピリダモールは、虚血性脳卒中や末梢動脈疾患の予防に使用されます(ジピリダモール自体は抗血小板作用が弱いため、主にアセチルサリチル酸と組み合わせて使用されます)。 1日3〜4回、食事の1時間前に内側に割り当ててください。 僧帽弁性心疾患における血栓の形成を防ぐために、経口抗凝固薬と組み合わせてジピリダモールが処方されます。
ジピリダモールを使用すると、頭痛、めまい、動脈性低血圧、消化不良、
皮膚の発疹。 出血のリスクはアセチルサリチル酸よりも少ないです。 ジピリダモールは、狭心症(「スティール症候群」の可能性)には禁忌です。

米。 27-4. ジピリダモールの抗血小板作用のメカニズム: EC - 内皮細胞。 A 2 -P - アデノシン A 2 受容体。 PDE-ホスホジエステラーゼ cAMP; AC - アデニル酸シクラーゼ。 GP IIb/IIIa - 糖タンパク質 IIb/IIIa
ペントキシフィリン (アガプリン*、トレンタール*) は、ジピリダモールと同様に、ホスホジエステラーゼを阻害し、cAMP レベルを増加させます。 その結果、血小板の細胞質 Ca 2+ レベルが減少し、血小板の凝集が減少します。 ペントキシフィリンには他の特性もあります。赤血球の変形性を高め、血液の粘度を低下させ、血管拡張効果があり、微小循環を改善します。
ペントキシフィリンは、脳循環障害、さまざまな原因による末梢循環障害、目の血管病理に使用されます(「脳循環に違反して使用される手段」の章を参照)。 副作用としては、消化不良、めまい、顔の赤み、血圧低下、頻脈、アレルギー反応、出血などが考えられます。 ジピリダモールと同様、狭心症の発作を引き起こす可能性があります。
血小板膜の糖タンパク質 IIb/IIIa をブロックする薬剤
このグループの抗凝集剤は、血小板膜の糖タンパク質 IIb/IIIa と直接相互作用し、フィブリノーゲンへの結合を破壊しますが、比較的最近出現しました。
アブシキシマブ (レオプロ *) - このグループの最初の薬剤は、「キメラ」マウス/ヒトモノクローナル抗体 (糖タンパク質 IIb / IIIa に対するマウス抗体の Fab フラグメント、ヒト Ig の Fc フラグメントに結合) です。 アブシキシマブは、血小板膜上の IIb/IIIa 糖タンパク質へのフィブリノーゲンの結合を非競合的に阻害し、その凝集を破壊します (図 27-3 を参照)。 血小板凝集は、1 回の注射から 48 時間後に正常化されます。 この薬剤は、冠状動脈の血管形成術における血栓症を予防するために静脈内(点滴として)投与されます。 アブシキシマブを使用すると、内部(胃腸、頭蓋内、尿路からの出血)、吐き気、嘔吐、低血圧、徐脈、アナフィラキシーショックに至るまでのアレルギー反応、血小板減少症などの出血が発生する可能性があります。
同じ作用機序を持つアレルギー誘発性の低い薬剤の探索により、糖タンパク質 IIb/IIIa の合成ブロッカーが作成されました。 バルボリン(コビトガラガラヘビの毒から単離されたペプチド)に基づいて、フィブリノーゲン鎖のアミノ酸配列を直接模倣する環状ヘクタペプチドである薬剤ept、f、bat、d(インテグリン*)が得られました。糖タンパク質 IIb / IIIa に結合します。 エプチフィバチドは、フィブリノーゲンを受容体との結合から競合的に追い出し、血小板凝集の可逆的な障害を引き起こします。 この薬は点滴として静脈内に投与されます。 抗血小板効果は 5 分以内に現れ、投与中止後 6 ~ 12 時間で消失します。 この薬は、不安定狭心症を伴う経皮的冠動脈形成術における血栓症の予防、心筋梗塞の予防に推奨されます。 エプチフィバチド使用時の危険な合併症は出血です。 血小板減少症の可能性。
チロフィバン (アグラスタット*) は、チロシンの類似体である非ペプチド糖タンパク質 IIb/IIIa ブロッカーです。 エプチフィバチドと同様に、チロフィバンは糖タンパク質 IIb/IIIa 受容体を競合的にブロックします。 薬は静脈内に投与されます(点滴)。 効果発現速度、作用持続時間、使用適応等はエプチフィバチドと同様です。 副作用 - 出血、血小板減少症。
このグループの薬剤の使用の可能性を広げるために、経口投与で効果を発揮する糖タンパク質IIb/IIIaのブロッカー(キセミロフィバン*、シブラフィバン*など)が作られました。しかし、これらの薬剤の試験では、効果が不十分であり、副作用が判明しました。重度の血小板減少症の形で。
血小板凝集は、血管壁の近くに位置し、その維持に関与している非常に小さな血球によって傷が塞がれるプロセスです。
毛細血管の完全性が侵害された場合、毛細血管は傷口に到達し、それを閉じて出血を防ぎます。 服用する薬を減らすにはどうすればよいですか?
説明
プラークが損傷箇所に押し寄せ、互いに重なり合い、血栓を形成します。この現象は癒着と凝集と呼ばれ、1つのシステムに融合するプロセス(凝集結合)は、傷が閉じるまで続きます。 このおかげで、人は大量の血液を失うことはありません。
血小板凝集の研究は、血漿を分析することによって行われます。 健康な人間では、これらの細胞は出血から体を保護しており、さまざまな病気を引き起こす逸脱が発生する可能性があります。 上がったり下がったりします。
年齢の指標
分析
血小板凝集検査は静脈から採取されます。 心臓、血管、血液の一部の病気に必要です。
分析の精度を高めるために、納品前に特定の条件を満たす必要があります。
- 3日間は医師の指示に従って食事療法を行ってください。
- 日中は薬の服用を拒否してください。
- 24時間飲酒、カフェイン、喫煙はしないでください。
すべての推奨事項に従えば、分析は真実となり、血栓のプロセスに影響を与える物質は存在しません。 研究室では、結果を得るために、ヒトの細胞を模倣した誘導因子(刺激因子)が血漿に追加されます。
分析が行われています:
- アデノシン二リン酸(ADP)。
- リストマイシン(リストマイシン、同義語リストセイン)抗生物質を使用。
- アドレナリン (エピネフリン) (L-1 (3,4-ジオキシフェニル)-2-メチルアミノエタノール) は、副腎髄質の主要なホルモンです。
- アラキドン酸(多価不飽和オメガ6脂肪酸)。
- コラーゲンは線維状タンパク質です。
- セロトニン - 5-ヒドロキシトリプタミン、神経伝達物質、幸福のホルモン。
誘導凝集は、特定の病気を診断するために実行されます。 このために、レーザー分析装置が使用されます。 血漿とインダクターがその中に導入され、その後装置がプラークの凝固能を計算します。
最もよく取られるのは次のとおりです。
- ADPを使って。
- アラキドン酸配合。
- アドレナリン(エピネフリン)あり。
- そしてリストセチンも配合。
最初の 3 つの刺激装置を使用すると、細胞をあらゆる側面から評価できます。4 番目の刺激装置は病理 (出血) です。
集約インジケーター - インダクターに応じた分析のデコード
種類
- 血漿が採取され、特別な装置に入れられ、一定の温度に加熱されると、血球の作用が明らかになる自然凝集。
- 誘導。特定の疾患を確立するために、誘導因子を使用した血小板凝集分析装置によって実行されます。
- 中等度 - 妊娠中の胎盤内の血液循環によって引き起こされます。
- 増加 - 血栓、浮腫の形成につながります。
分析
処方対象:
- 血栓症が早すぎる。
- 血栓静脈炎、血小板減少症。
- 出血しやすい(子宮、鼻)。
- 傷の治りが悪い。
- 歯ぐきから出血。
- 血液を薄くする薬(サリチル酸)の長期使用。
- 静脈瘤。
- 心臓、血管の病気。
- 妊娠中の合併症。
- 手術前。
却下
一部の疾患では凝集が低く、おそらく遺伝性です。 接着が不十分な場合、細胞は血液を止めるプロセスを阻害(抑制)し、重度の出血が発生する可能性があります。 これが起こります:
- 甲状腺ホルモンの欠乏、過剰。
- 重度の肝臓障害(肝硬変、肝炎)。
- 感染性、ウイルス性(麻疹、風疹)。
- 毒素中毒。
プラークの急速な減少は、重篤な病気、化学療法、または阻害剤の長期使用中に発生する可能性があります。
- 骨髄の癌病変、白血病。
- がん患者への放射線照射は血液の組成を大きく変化させます。
- 副作用のある薬(アセチルサリチル酸、レオピリン、抗生物質)。
細胞の減少につながる重篤な病気の場合は、凝固像(血液凝固)の追加分析が行われます。 次のことを行うことをお勧めします。
- 手術前。
- 妊娠の計画。
- 心臓の病状があると、心臓発作が起こります。
- 高血圧。
- 治療に長い間使用されてきた阻害剤。
凝固検査は、手術時の重度の出血、病気の深刻な結果を回避し、先天性の病状を確立するために必要です。 凝固不良はまれです。
増加
過剰な凝集は血液の粘度を高め、血栓の急速な形成に寄与します。 この現象は次の場合に発生します。
- 糖分が多い(糖尿病)。
- 高血圧。
- 腎臓、胃、白血病の腫瘍学。
- 止血障害を引き起こす出血症候群。
- 心臓、脳の血管のアテローム性動脈硬化症。
毛細血管内に塊(血栓)が形成されると、重大な結果が生じます。 動脈壁へのプラークの付着は内腔の減少をもたらし、血液循環に悪影響を及ぼします。
血栓の含有量の増加は、障害を引き起こす以下のような病気に該当する可能性があります。
- 循環障害により心筋が損傷し、心臓発作が発生します。
- 頭の血栓は脳卒中を引き起こします。
- 血栓が脚の静脈に沈着し、血栓性静脈炎を形成します。
血管の内腔が閉じると、死に至る重度の病状となり、治療が必要になります。 これらの目的のために、血小板凝集の阻害剤(阻害剤 - 阻害、遅延)があります。
この場合、細胞の接着プロセス、病状の形成に憂鬱に作用します。 以下は心血管疾患、腎不全の治療に使用される薬です。
使用される阻害剤であるエナジル、リシノプリル、ハーチル、ディロトンは圧力を下げません。 あらゆる分析はラボで行うことができ、緊急性とスピードが保証されます。
予防検診を受けて健康管理をしましょう。 ほとんどすべての病気は早期に治療できます。 新しい情報については、当社のウェブサイトをご覧ください。
血小板は、(白血球や赤血球と比較して) 最も小さな血球であり、失血から体を守るという最も重要な機能を果たします。 血小板凝集は細胞が接着するプロセスであり、血栓形成の初期段階です。
第 2 段階は、損傷した血管の壁に血小板を固定することです。 フィブリン鎖、他の要素、新しい接着細胞が血小板塊の上に重ねられます。 したがって、血栓は血管の直径を塞いで出血を止めることができるサイズまで成長します。 人の人生は、プロセスの速度に依存することがあります。
血液凝固の過程における血小板凝集の役割
血液凝固は多くの要因に依存します。 健康な生物におけるそれらの 1 つである血小板凝集は、保護的適応特性を持っています。 細胞は出血している血管内でのみくっつきます。 この場合、プロセスは積極的な役割を果たします。
しかし、血栓の形成は重要な臓器の栄養失調につながるため、望ましくない病理学的状態が知られています。 たとえば、心筋梗塞、脳卒中、主要動脈の血栓症などです。 血小板の凝集活動は病理学的変化の側面を持ちます。 さまざまな薬の助けを借りてこれと戦わなければなりません。
実際には、良好な血小板凝集と不良な血小板凝集を定量化する必要があります。 これを行うには、標準を使用し、逸脱を区別する必要があります。
正常と病理を判断するにはどうすればよいですか?
血液検査は特定の人の血小板の凝集能力を示すことができますか? 実際、この研究では血液が静脈から採取され、その瞬間から体の「命令」は血球に作用しません。 この種の分析は「in vitro」と呼ばれ、ラテン語の「ガラス上、試験管内」を直訳すると「in vitro」と呼ばれます。 科学者は常に人体に近い条件での反応を研究しようとしています。 この方法で取得されたデータのみが信頼できると見なされ、診断に使用できます。
血小板の能力は、誘導された凝集によって決まります。 これは、化学組成の点で身体にとって異質ではなく、血栓症を引き起こす可能性のある薬剤が誘導剤として使用されることを意味します。 血管壁の成分であるアデノシン二リン酸(ADP)、リストセチン(リストマイシン)、コラーゲン、セロトニン、アラキドン酸、アドレナリンは誘導物質として使用されます。
自発的な凝集は、誘導物質なしで決定されます。
定量的測定の技術は、多血小板血漿を通る光波の透過に基づいています。 凝集活性の程度は、凝固の開始前と最大の結果が得られた後の血漿の光密度の違いによって研究されます。 また、最初の 1 分間の凝集速度、波の性質と形状も決定します。
基準は物質誘導体、その濃度に依存します。
ADP による血小板凝集は、通常、コラーゲン、リストマイシン、アドレナリンと組み合わせて行われ、評価されます。
ADP を使用した分析の標準は 30.7 ~ 77.7% です。 アドレナリンによる血小板凝集の値は、35 ~ 92.5% の範囲で変化します。 コラーゲンを使った研究では、正常値は46.4~93.1%と考えられています。
分析を受けるための準備のルール
凝集能力を調べる血液検査を受けるには、準備規則に違反すると検査が不正確になることを理解する必要があります。 血液中には結果に影響を与える物質が存在します。
- 献血の 1 週間前には、すべてのアスピリン薬、ジピリダモール、インドメタシン、スルファピリダジン、抗うつ薬を中止する必要があります。 これらの薬剤の使用により、血栓症が阻害(抑制)されます。 服用を中止できない場合は、検査助手に知らせる必要があります。
- 少なくとも12時間は食事を摂ることができません。脂肪の多い食べ物は特に結果に影響します。
- 患者はできるだけ落ち着いて、肉体労働をしないでください。
- 一日の間、食事からコーヒー、アルコール、ニンニクを避け、喫煙しないでください。
- 活動的な炎症過程がある場合、分析は実行されません。
凝集した血小板が顕微鏡で見える
出血増加の診断のために、抗凝固薬による治療、その有効性の管理、最適な用量の選択が必要な場合、血小板凝集の血液検査が医師によって処方されます。
結果を解読する
3 つの標準的な誘導因子を一度に使用して研究を実施し、必要に応じて新しい誘導因子を追加する理由は、凝固因子の 1 つを活性化する主なメカニズムにあります。 たとえば、他のインダクタによるダイナミクスが存在しない場合の ADP で明らかになった変化したノルムには、診断上の価値があります。 結果の評価は医師によって行われます。
血小板凝集の減少は次の原因によって引き起こされる可能性があります。
- 抗血小板療法の成功した使用。
- 血小板症と呼ばれる一連の疾患。

集計用分析装置
血小板症の役割
血小板症は遺伝性である場合もあれば、他の疾患の結果として後天性である場合もあります。 統計によれば、世界人口の最大 10% がこの病状に苦しんでいます。 それらはすべて、特定の物質の蓄積に対する血小板の機能の違反に関連しています。
その結果、凝固や血栓の形成が起こらず、小さな傷や打撲による出血が増加します(内出血)。
病気はすでに小児期に現れており、歯ぐきの出血、頻繁な鼻血、子供の体に多くの打撲傷、打撲傷を伴う関節の腫れが見られます。 思春期の女の子には長くて重い月経が始まります。 出血は貧血(貧血)の発症につながります。
血小板症における低い凝集能は、ウイルスや細菌の感染、薬物、理学療法によって活性化される可能性があります。

鼻血の80%は血小板症が原因ですが、耳鼻咽喉科の疾患が原因の鼻血はわずか20%です
続発性血小板症
症候性(続発性)血小板症は、慢性白血病、多発性骨髄腫などで形成されます。 この状態は、甲状腺機能の低下である腎不全(尿毒症)の最終段階に典型的です。
血小板症は、外科的介入中に出血が増加する外科医によって遭遇されます。
血小板凝集の増加は、以下の場合に観察されます。
- 血管の広範なアテローム性動脈硬化症。
- 高血圧;
- 内臓の梗塞。
- 腹腔の動脈の血栓症。
- 脳卒中
- 糖尿病。
妊娠中の凝集の変化
妊娠中の血小板凝集は正常値から逸脱する可能性があります。
血小板の生産が不十分であるか、血小板の定性的組成が違反されているため、凝集が減少します。 これは出血、あざの存在によって現れます。 出産時には大量出血の可能性を考慮する必要があります。
凝集は、嘔吐や下痢による体液喪失による中毒症の際に最も多く増加します。 血中濃度の上昇は血栓症の増加につながります。 これは早期流産につながる可能性があります。 妊娠中の中程度の過剰凝集は正常であると考えられており、胎盤循環の発達に関連しています。
- 流産の場合。
- 不妊治療。
- 避妊薬の使用前および使用中。
- 計画された妊娠の前に。
血小板の凝集特性を分析することで、リスクを特定し、病気の経過における危険な合併症を予測し、予防療法をタイムリーに実施することができます。
血小板は色のない血球です。 それらは体内で重要な機能を果たし、失血から体を保護します。 このプロセスは血液中の血小板の凝集であり、独自の規範的な指標があります。
それが何であるかを理解するには、血栓の形成、既存の基準、正常値からの逸脱の危険性について理解する必要があります。
人体における説明と役割
組織損傷後、血小板は損傷した血管の壁に固定されます。 その結果、細胞同士が接着します。 フィブリン鎖、新しく接着した細胞、その他の要素が、時間の経過とともに結果として得られる塊に加わります。
このような背景から、血栓が成長し、大きなサイズに達すると、血管の閉塞や出血の停止につながる可能性があります。 このようなプロセスのスピードは非常に重要です。なぜなら、人命の保護がそれに依存している場合があるからです。

血液凝固は多くの要因の影響を受けます。 その 1 つは集約です。 病理学的状態がない場合、それは保護的な適応機能を実行します。
凝集の特徴は、損傷した容器内でのみ細胞を接着することにあります。 この場合、プロセスはポジティブとみなされます。
.jpg)
しかし、血栓症が望ましくない状況もあります。 たとえば、脳卒中であれば心筋梗塞と診断されます。
これは、血栓の形成により、重要な臓器への必要な物質の正常な流れが妨げられるためです。
この場合、血小板は病理学的プロセスの側にいます。。 規範からの逸脱に対処するには、薬の助けを借りてのみ必要です。
偏差から正常な指標を特定するには、ポジティブおよびネガティブな集計の定量分析を実行する必要があります。
種類
医療現場では、凝集を種類ごとに一定の分類が行われています。 これらには次のものが含まれます。

- 適度な凝集。 主に出産時に診断されます。 胎盤の循環がこの状態を引き起こす可能性があります。
- 自発的な凝集。 この定義にはインダクタは必要ありません。 凝集活動を検出するには、血液を試験管に注ぎ、それを特別な装置に置き、そこで 37 度に加熱します。
- 誘発された凝集。 研究のために、インダクターがプラズマに追加されます。 この場合、凝集はADP、コラーゲン、リストマイシン、アドレナリンで起こります。 この方法は、血液流体の何らかの病状を診断する必要がある場合に使用されます。
- 凝集の増加は血栓の形成に寄与します。 このような病的状態の特徴的な症状は、しびれと腫れです。
- 凝集の減少は、循環系の違反で最も頻繁に検出されます。 血小板数の減少はさまざまな出血を引き起こします。 それは月経周期中の公正なセックスで発生します。
凝集の増加と減少はどちらも人間の健康にとって危険です。 したがって、血液中の血小板のレベルを定期的に監視する必要があります。
指標からの逸脱の症状
過剰凝集は血液粘度の増加とその流量の低下を伴い、人間のすべてのシステムと器官に悪影響を及ぼします。
ただし、顕著な凝集が正常である場合には病理学的状態があり、これは凝固パラメーターの継続的な研究を拒否する理由とはみなされません。
これらの病気には次のようなものがあります。
- 血圧の上昇。
- 糖尿病;
- 腫瘍性疾患;
- 血管の病状。
過剰凝集が時期尚早に検出され、支援策が欠如すると、心臓発作、脳卒中、静脈血栓症の発症につながる可能性があります。
凝集パラメータの低下は、血腫の形成によって現れる内出血を含む長期にわたる出血を伴います。
標準とは何ですか
大人と子供の血小板レベルの基準はわずかに異なります。 インジケーターの最適値を以下の表に示します。
通常の集計値について言えば、25 ~ 75 パーセントになります。 この場合、血小板は偏ることなくくっつき、人体に危険を及ぼすことはありません。
どのような研究が行われているのか
血小板凝集分析装置は完全な血球計算です。 ただし、より正確な結果を提供する他の研究もあります。 主な方法には次のテストが含まれます。
.jpg)
- リー・ホワイトによれば、
- 凝固図。
それらの本質は、特別な物質が血液に干渉し、凝集を阻害するという事実にあります。.
これらの成分は、人体に含まれる血栓症を引き起こす物質と似ています。 このような部品はインダクタと呼ばれます。
分析の準備
分析を行う前に、いくつかの準備を行う必要があります。 結果をできるだけ正確にするためには、血液中に悪影響を及ぼす可能性のある物質が血液中に存在してはなりません。
準備活動:
- 分析の1週間前に、アスピリン薬は投与の結果として血栓形成が抑制されるため、除外されます。 これらの資金をキャンセルできない場合は、研究を実施する研究室助手に通知する必要があります。
- 12時間の間は食事を拒否する必要があります。 製品、特に高脂肪も結果に悪影響を及ぼします。
- 身体的および精神的なストレスを避けてください。
- 日中は、アルコール、コーヒー、ニンニクを摂取しないでください。また、喫煙もしないでください。
活発な炎症過程がある場合、分析は延期されます。
ホールディング
採血は朝の7時間から10時間の間に行われます。 研究は空腹時にのみ実行できます。 非炭酸水を飲むことは許可されています。
止血を行うには、静脈から血液を採取します。 これらの目的には、使い捨て注射器が使用されます。 その後、材料はクエン酸ナトリウムの 4% 溶液を含む凝集計に入れられます。 その後、容器を数回ひっくり返します。 その後、血液サンプルはさらなる分析のために研究室に送られます。
結果を解読する
研究で使用された物質を考慮して、分析が解読されます。 これを行うために、取得された指標が以下に示す通常の値と比較されます。
基準と比較して増加がある場合、過剰凝集と診断されます。 次のような病理学的状態で発生する可能性があります。
.jpg)
- 白血病;
- 胃腸管または腎臓の病理;
- アテローム性動脈硬化症;
- 糖尿病;
- 高血圧;
- 敗血症;
- リンパ肉芽腫症。
小さい方への逸脱がある場合、低凝集と診断されます。 血液の病状、抗血小板薬による治療によって引き起こされる可能性があります。
パーセンテージは、誘導物質をプラズマに添加した後のプラズマの光透過率を示します。 血小板の含有量が低い場合、この指標は 100% であり、血小板の含有量が増加すると、ゼロになります。
妊婦における凝集の特徴
妊娠中は標準からの逸脱が許容されますが、この期間中の許容範囲は 30 ~ 60 パーセントです。
脱凝集は、血小板の欠如や、出血や打撲によって現れる血小板の質的組成の変化がある場合に観察されます。
凝集の増加は中毒症で起こり、患者が嘔吐または下痢の結果として体液を大量に失った場合に起こります。 血中濃度の上昇は、血栓の形成の増加を引き起こします。 これは早期に流産する恐れがあります。
値を正規化するにはどうすればよいですか
血液凝固の違反が診断された場合は、病理学的状態を排除するための措置を直ちに講じる必要があります。 凝集の増加は血栓症を引き起こす可能性があり、凝集の減少は大量の危険な出血を引き起こす可能性があります。
過剰凝集の発症の初期段階では、専門家は血液を薄める薬を処方します。 通常のアスピリンでこの作業に対処できます。
追加の検査の結果に基づいて、次のことが処方されることがよくあります。
.jpg)
- 鎮痛剤;
- ノボカイン封鎖。
- 血管拡張を促進する薬。
- 急速な凝固を防ぐ抗凝固剤。
場合によっては、民間の方法も同様に効果的です。 このような治療法は必ず主治医の同意を得ることになることを覚えておく価値があります。
実証済みのレシピには次のようなものがあります。
- スイートクローバー大さじ1杯に200mlの沸騰したお湯を注ぎ、30分間醸造させます。 調製した組成物をその日に数回に分けて使用します。 治療期間は1か月です。
- 同量(小さじ1杯)の生姜と緑茶を1.5リットルの熱湯で淹れます。 シナモンをひとつまみ加えます。 15分ほど主張し、日中に服用してください。
- 毎日、絞りたてのオレンジジュースを飲みましょう。 かぼちゃと同じ割合で混ぜることもできます。
適切な食生活を続けることも重要です。。 食事には以下を含める必要があります。
- 柑橘類;
- ショウガ;
- ニンニク;
- 赤と緑の野菜。
- シーフード。
血液凝固が悪いと、薬を服用することは禁じられています。 血液を薄めるもの。 プロセスの経過が無視された形になった場合、治療措置は静止状態でのみ実行されます。
医薬品から次のものを任命します:

- エモシント;
- アミノカプロン酸とトラネキサム酸。
- ATPの導入;
食事には、そばのお粥、卵、ビート、ニンジン、ザクロ、牛レバー、赤身の肉の存在が必須です。
血液を正常な状態に保つためには、飲酒習慣を厳守する必要があります。 1日あたり少なくとも1.5リットルのきれいな水が標準とみなされます。 食べ物は新鮮でバランスのとれたものでなければなりません。
栄養の規則を遵守することは、人体の多くの病気の予防につながります。 身体活動も重要な役割を果たします。 それらは体の強化だけでなく、すべての内部プロセスの正常化にも貢献します。
集計指標の逸脱をタイムリーに診断することで、多くの病気や合併症を予防できます。 血小板凝集のレベルを定期的に監視する必要があります。
血小板は一次止血のプロセスに関与します。 それらの活性化には、1) 患部への接着、2) 放出反応 (血小板産物の分泌と主要な受容体の活性化)、および 3) 凝集の 3 つの段階が含まれます。 たとえば、血管が損傷すると、血小板は膜糖タンパク質受容体を使用して、アクセス可能になった内皮下腔の成分(コラーゲン)にすぐに付着します。 このプロセスはフォン ヴィレブランド因子によって制御されます。 血小板が血管壁に接着した後、その細胞質顆粒の内容物(カルシウム、ADP、セロトニン、トロンビンなど)が放出されます。 血小板の活性化と顆粒内容物の分泌は、アゴニスト (特にコラーゲンとトロンビン) への結合によって刺激されます。 このプロセス中に、血小板の活性化により、強力な血管収縮剤および凝集誘導剤であるトロンボキサン A2 (TXA2) の新規合成および分泌が誘導されます (図 17.17)。 ADP、トロンビン、TXA2 は血小板凝集を促進し、一次血栓の形成に寄与します。 血小板の活性化中に、糖タンパク質膜受容体 Ilb/IIIa の重要な構造変化が発生します。 これらの変化は、以前は不活性だったHb/IIIa受容体がフィブリノーゲン分子に結合し、その結果、血小板が互いにしっかりと結合して凝集体を形成するという事実につながります。
血小板活性化の調節は主に、血小板貯蔵所からの Ca ++ の放出によるものです。 その結果、細胞のサイトゾル内のカルシウム濃度が増加し、プロテインキナーゼが活性化され、最終的には血小板内の調節タンパク質がリン酸化されます。 さらに、細胞サイトゾル内の[Ca++]の増加はホスホリパーゼA2を刺激し、TXA2の前駆体であるアラキドン酸の放出を引き起こします(図17.17)。 カルシウムの放出はいくつかの要因によって調節されます。 トロンビンおよび他のアゴニストが血小板膜上の対応する受容体に結合すると、貯蔵所からのカルシウムの放出を刺激する中間化合物が形成されます。 TXA2は、血小板表面の受容体に結合することにより細胞内[Ca++]レベルを増加させ、アデニル酸シクラーゼの活性を阻害します。これにより、cAMPの産生が減少し、デポーからの[Ca++]放出が増加します(図17.17)。 。 対照的に、内皮細胞によって産生されるプロスタサイクリン (PGI2) は、アデニル酸シクラーゼの活性を刺激し、血小板内の cAMP 濃度を増加させ、貯蔵所からの [Ca++] 分泌を阻害します。
米。 17.17。 血小板の活性化は細胞内 [Ca++] によって媒介されます。 血小板の貯蔵庫からのカルシウムの放出を促進および阻害する因子が示されています。 特定の受容体に結合するトロンビンとセロトニンは、ホスホリパーゼ C (PLS) の作用下でホスファチジルイノシトール二リン酸 (FIFg) からのイノシトール三リン酸 (IFz) の生成を刺激します。 IGF は、細胞の細胞質へのカルシウムの放出を促進します。 トロンボキサン Ag (TXA2) もカルシウムの放出を促進します。トロンボキサン Ag (TXA2) は、サイクリック AMP (cAMP) の産生の減少を伴うアデニル酸シクラーゼ (AC) の活性を阻害します。 通常の条件下では、cAMP は ER からの [Ca++] の放出を防止するため、TXAg の作用によりこの効果が低下すると、細胞質へのカルシウムの放出が増加します。 内皮細胞で形成されるプロスタサイクリンは逆の効果をもたらします。AC の活性と cAMP の形成を刺激することにより、血小板内のカルシウムの放出を減少させます。 カルシウムはホスホリパーゼ Kj (PLA2) の活性を高め、その作用により細胞膜のリン脂質から TXAg 前駆体が形成されます。 血小板が活性化されると、[Ca++] が変化し、その結果カルシウム貯蔵庫の内容物が放出され、細胞骨格の再構成が起こり、糖タンパク質 IIb/IIIa 受容体の構造が大きく変化します。つまり、血小板の凝集に必要なプロセスが起こります。 ADP も血小板凝集に一定の寄与をしますが、このプロセスの仲介者はまだ確立されていません。
最新の抗血小板薬は、血小板の活性化および凝集プロセスのさまざまな段階で血小板の機能に影響を与えます。 最も一般的な抗血小板薬はアスピリンです。 クリニックで使用される他の薬剤には、ジピリダモールやチクロピジンなどがあります。 血小板 IIb/IIIa 受容体をブロックする可能性のある新薬が積極的に研究されており、心血管疾患の治療におけるその重要性が明らかにされています。