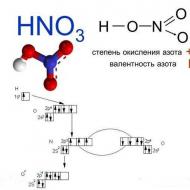
Milyen szennyeződések lehetnek a vízben és hogyan történik a tisztítás. A víz mindig tartalmaz különféle szennyeződéseket. A természetes vizek osztályozása A vízben található különféle szennyeződések
- A természetes vizek a Föld hidroszférájának természetes eredetű vizei. Két nagy osztályba sorolhatók: felszíni és földalatti (légköri vizek is megkülönböztethetők, de közvetlen felhasználásuk egzotikus). Felszíni vizek folyókban, tavakban, tározókban, mocsarakban és tengerekben, valamint csatornákban találhatók. A talajvizet a talaj és a sziklák pórusai tartalmazzák.
- A szennyvíz eredet szerint négy osztályba sorolható: háztartási (fekális), csapadékvíz, mezőgazdasági és ipari (ipari).
- Háztartási lefolyók akkor keletkeznek, amikor a csapvíz a háztartási és fiziológiai hulladékkal keveredik a szaniter készülékekben, és főleg szerves szennyeződéseket tartalmaz.
- Az ipari szennyvizek sokfélék, csakúgy, mint az anyagtermelés azon ágai, amelyek különféle szükségletekre vizet használnak fel.
Viharcsatornák Légköri csapadék keveréke a lakott és nem beépített területek felületéről lemosott szennyeződésekkel (szuszpenziók, olajtermékek stb.).
NAK NEK mezőgazdasági szennyvíz Az állattenyésztésből származó, a háztartási fekáliához hasonló összetételű, de csak töményebb összetételű szennyvizek mellett az öntözés során keletkező, gyakran növényvédőszert és ásványi műtrágyát tartalmazó visszatérő és lefolyó vizek is szerepelnek.
Természetes és szennyvíz szennyeződései
A vízben található szennyeződések sokfélesége megnehezíti osztályozásukat. Egészen a közelmúltig a szennyeződéseket a következő kritériumok szerint rendszerezték:- A vízszennyeződéseket természetüknél fogva ásványi, szerves és biológiai szennyeződésekre osztják. Az ásványi anyagok közé tartoznak a homok, agyag, érc, salak, ásványi olajok, sók, savak, bázisok stb. részecskéi. A szerves szennyeződések növényi, állati és mesterséges eredetűek. Növényi - ezek a növények maradványai, algák, bomlástermékeik stb. Az állati eredetű szennyeződések közé tartoznak az emberek és állatok fiziológiás ürülékei, állati szövetmaradványok, ragasztóanyagok stb. A szerves szennyeződések mesterséges eredetűek, amelyek például szerves kémiai vállalkozások, élelmiszeripar és sok más iparág termékeiből képződnek. A biológiai mikrobiális szennyeződéseket mikroorganizmusok képviselik, köztük mikroszkopikus algák és gombák, baktériumok és vírusok, amelyeket gyakran mikroflórának neveznek. A mikrofauna közé tartoznak a csillósok, a flagellák, a férgek és a rákfélék.
- Az oldhatóság mértéke szerint a szennyeződéseket oldhatatlanra és oldhatóra osztják. Az oldhatatlanokat szuszpendáltnak is nevezik, ezek közé tartoznak a homok, agyag, iszap részecskék. Az oldható szennyeződések lehetnek kolloidok (köztes helyzetet foglalnak el a szuszpendált és oldott anyagok között), vagy valóban oldható molekulák és ionok.
- A szennyeződések fázisállapot szerint lehetnek szilárd (például agyagszemcsék, algák), folyékonyak (emulziók, olajtermékek, zsírok), gázhalmazállapotúak (gázok oldatlan állapotban).
 |
A vízszennyeződéseket származásuk (természetes és mesterséges), a vízhez viszonyított sűrűségük (lebegő, süllyedő és függő) és egyéb jellemzők alapján is osztályozhatjuk.
A szennyezés egy speciális típusa a termikus szennyezés, amelyet a hűtött berendezésből való víz eltávolítása után megnövekedett hőmérséklet jellemez. A természetes termálvizek hőmérséklete is magasabb (50 °C-ig és afölötti).
A vízszennyeződések osztályozása fázisdiszperz állapotuk szerint
A szennyeződések és osztályozásukhoz szükséges jellemzők sokfélesége megnehezíti a szennyeződések vízből történő eltávolításának holisztikus észlelését és kiválasztását.
akadémikus L.A. Kulsky megalkotta saját táblázatos osztályozását a vízszennyeződésekről, látva a rendet és a logikát a változatosság mögött. Két fő tényezőre alapozta: a diszperzióra és azok fázisállapotára.
A szennyező részecskék diszperziójának (őrlésének) mértéke a d méret vagy a diszperzió mértéke D=1/d. A részecskék aprításával a méretük csökken, a diszperzió mértéke és a fajlagos felület (bizonyos térfogatú részecskék teljes felülete) nő, amint az az alábbi táblázatból is látható.
A szennyező részecskék diszperziójának jellemzői
| Jellegzetes | Index | |||
| Egyetlen szemcseméret, d, m | 0,01 | 0,001 | 0,0001 | 10 -7 |
| Diszperziós fok, D, m-1; | 100 | 1000 | 10 6 | 10 15 |
| A részecskék száma 1 cm³-ben | 1 | 1000 | 10 6 | 10 15 |
| A részecskék fajlagos felülete 1cm³, cm²-ben | 6 | 60 | 600 | 6*10 5 |
A részecskék fajlagos felülete a következő képlettel határozható meg: S UD = KD, ahol K a részecskék alakjától függő együttható.
A szennyeződéseket tartalmazó víz fizikai-kémiai rendszer (PCS). A benne lévő diszperziós közeg víz, a szennyeződések pedig a diszpergált fázist, az FCS különálló komponensét alkotják, amelyet a határfelület választ el a rendszer többi részecskéitől. A két vagy több fázisból álló FCS-t heterofázisnak (különböző fázisnak) nevezik. Ha a közeget és a szennyeződést egy fázis képviseli, a PCS-t homofázisnak (egyfázisúnak, homogénnek) nevezzük.
A vízbázisú heterofázisú FCS-eket szuszpenzióknak (ha a szennyeződés szilárd), emulzióknak (ha a szennyeződés folyadék) és haboknak (ha a szennyeződés gáz) nevezik.
L.A. Kulsky minden vízszennyeződést két osztályba osztott: heterogén (a heterofázisú PCS-nek megfelelő) és homogén (homofázisú PCS-ben), amelyek mindegyike két csoportra oszlik a részecskemérettől függően. A szennyeződések osztályozása L.A. A Kulsky-t az alábbi táblázat tartalmazza:
táblázat L.A. Kulsky
A szennyeződések jellemzői csoportonként
Az I. csoportba tartoznak a szuszpenziók (szuszpendált anyagok, durva szennyeződések). Ide tartoznak: finom homok, iszap, agyagos anyagok, hamu, vízkő, élelmiszer-maradványok, fém-hidroxidok és mások, pl. olyan szennyeződések, amelyeket a vízáramlás dinamikus erői szuszpenzióban tartanak; nyugalomban leülepednek (ha a sűrűség nagyobb, mint a víz sűrűsége) vagy lebegnek (ha a sűrűség kisebb, mint egység).
 |
A szuszpenziók a csatorna kőzeteinek eróziója, a csapadékvizek talajmosása miatt kerülnek a természetes vizekbe. A lebegő anyagok a szaniter berendezésekből (élelmiszermaradványok, talajrészecskék) vagy technológiai folyamatok eredményeként (például hengerműhengerek hűtésekor vízkő, szénszemcsék a bányavizekben) jutnak a szennyvízbe. Az antropogén eredetű szuszpenziók fokozott ellenálló képességgel rendelkeznek az ülepedéssel szemben.
A szuszpendált anyagok felületükön baktériumokat, vírusokat, peszticideket, radionuklidokat tartalmazhatnak.
A szennyeződések I. csoportjába tartozik még a plankton és a baktériumok. A baktériumok ártalmatlanok az emberi szervezetre és kórokozók lehetnek. Nem csapódnak ki és nem lebegnek állóvízben, hanem vagy szabad állapotban, vagy lebegő szilárd anyagok felszínén vannak. Az utóbbi lehetőség gyakoribb. A baktériumok víz útján terjednek.
A planktont általában zooplanktonra (rákfélék, férgek) és fitoplanktonokra (algák) osztják. Az első aktívan mozog a vízben. Az algák intenzíven fejlődnek a meleg évszakban lassan mozgó vízben (tározókban). Éghajlati viszonyaink között a leggyakoribbak a kék-zöld algák.
A II. szennyeződéscsoport (kolloidok) általánosabb neve szolok (diszperziós közeggel víz formájában, hidroszolok). Mivel a kolloid részecskék csak egy nagyságrenddel nagyobbak a molekuláknál, a szolokat mikroheterogén rendszereknek is nevezik; a szuszpenziók és a valódi oldatok között köztes helyzetet foglalnak el (kolloid oldatokról is beszélnek). Vannak hidrofób és hidrofil kolloidok.
 |
A hidrofób kolloidok nem oldódnak vízben, nem lépnek kölcsönhatásba a vízmolekulákkal, és tipikus kolloid rendszerek. Instabilok és fokozatosan lebomlanak, szétválasztják a diszpergált fázist, amikor a részecskék az intermolekuláris kohéziós erők hatására durvábbá válnak, és átmennek az I. szennyeződéscsoportba.
A hidrofil kolloidok kölcsönhatásba lépnek egy diszpergált közeggel, és abban képesek feloldódni. Valójában 104-106 egység molekulatömegű makromolekuláris vegyületek stabil oldatai.
A természetes vizek kolloid szennyeződései a talaj és a talaj ásványi és szerves ásványi részecskéi, a humusz nem disszociált és oldhatatlan formái. A humusz az erdei, mocsaras és tőzeges talajokból kimosódik, vagy víztestekben képződik a növények és algák élettevékenysége következtében. Kolloidok a legtöbb szennyvízben is megtalálhatók, különösen a petrolkémiai, valamint a cellulóz- és papíriparban.
A kolloid diszperziós szennyeződések nagy fajlagos felülettel és nagy felületi energiával rendelkeznek. A diszperzitás mértékének növekedésével a határfelületen lévő molekulák száma nő. Aszimmetrikus erőtérben helyezkednek el, és a kompenzálatlan molekuláris kötések miatt többlet szabad energiával rendelkeznek.
Kulsky a vírusokat is a szennyeződések II. csoportjába sorolja. Nem képesek tápközegen létezni és csak a gazdaszervezet sejtjeiben szaporodni.
A szennyeződések III. csoportjába tartoznak a biológiai és antropogén eredetű szerves vegyületek - zsírok, fehérjék, szénhidrátok, cukrok, baktériumok, algák, emberek és állatok salakanyagai), fenolok, alkoholok, aldehidek és hasonlók, vegyipari szennyvíz, humusz oldható formái (fulvosavak).
 |
Ezek a vegyületek gyakorlatilag nem disszociáltak, és nem elektrolitok. A vízzel való kölcsönhatás eredményeként hidrátokat képeznek, és egymással kölcsönhatásba lépve társulnak. Ezek a vegyületek termodinamikailag stabilak, és bármennyi ideig létezhetnek anélkül, hogy kikerülnének a vízből. Egy bizonyos koncentráció (oldhatósági határ) túllépése esetén kétfázisú rendszert képeznek (csapadék), és az első csoport szennyeződéseivé alakulnak át.
Ebbe a csoportba tartoznak az ásványi vegyületek - oldott gázok is. A természetes vizekben általában van oxigén, nitrogén, szén-dioxid. A talajvíz hidrogén-szulfidot is tartalmazhat. Ezek a gázok olyan vizekben is jelen vannak, ahol bomlási folyamatok zajlanak (háztartási fekáliák, mocsári vizek).
A IV. csoportba tartozó szennyeződések sók, savak és lúgok oldatai, valamint elektrolitok. Az ionos vagy erősen poláris kötésekkel rendelkező anyagok molekuláinak disszociációja eredményeként jönnek létre a vízmolekulák poláris szerkezetének hatására.
A természetes és szennyvizek túlnyomó többsége kalcium-, magnézium-, vas-, nátrium-, kálium-, mangán-, hidrogénionokat (hidroniumionok H 3 O +), valamint anionokat: bikarbonátokat (HCO 3 -), karbonátokat (CO 3) tartalmaz. 2-), szulfátok (SO 4 2-), kloridok (Cl), fluor (F -), foszfátok (PO 4 3-), nitrátok (NO 3), nitritek (NO 2 -), hidroszilikátok (HSiO 2 -) , hidroxilcsoportok oh-. Specifikus ionokat a galvánipar, a bőripar és a rádióelektronikai ipar szennyvizei tartalmaznak.
A kölcsönhatás eredményeként az ionok kevés vagy nem disszociált vegyületeket képezhetnek (például CO 2 gáz, Fe (OH) 3 csapadék), és így átjuthatnak más csoportok szennyeződéseibe.
"egy cikk, ahol megpróbálunk választ adni a kérdésre" Hogyan mérik a szennyeződéseket a vízben?". Miben - ez a "milyen mértékegységek" értelmében, csak hogy rövidebb és világosabb legyen.
Miben mérik a szennyeződéseket a vízben - ehhez a kérdéshez tudnia kell, miért kell mérni, hogy hány anyag van a vízben. Tehát bizonyos célokra egy mértékegységre lesz szükség, más célokra más célokra. De a cél nagyon-nagyon egyszerű. Elemezzük a vizet, hogy megértsük, mitől kell megtisztítani. Ezért a megfelelő berendezés kiválasztásához meg kell határozni, hogy ez a víz káros-e vagy sem bármely területen (ivóvíz, műszaki alkalmazások, technológiai berendezések stb.), megjósolni a víz jövőbeli hatását a berendezésekre, és sok minden mást. több.
Tehát visszatérve a kérdésünkhöz: hogyan mérik a vízben lévő anyagok mennyiségét? A válasz egyszerű: teljesen más egységekben. Ráadásul a különböző országokban egyes mértékegységek nem egyeznek meg egymással, ezek kiegyenlítéséhez átváltási tényezők szükségesek. Például az USA-ban, Németországban, Franciaországban, Oroszországban és Ukrajnában eltérően mérik a víz keménységét. De erről majd később. Kezdetnek pedig - gyakrabban használt mértékegységek.
Mi a leggyakoribb mértékegység a víz összetételének mérésére?
Ez a kívánt anyag tömegtartalmának a teljes vízmennyiséghez viszonyított aránya.
A grammok és a milligrammok egy liter vízre vonatkoznak (néha a mutatkozáshoz egy litert köbdeciméternek neveznek - dm 3). Vagy ezer literre (köbméter vízre). De leggyakrabban literre.
Ennek megfelelően megkapjuk a mértékegységet milligramm literenként: mg/l. Vagy, ami ugyanaz, de angol forrásokban - ppm (parts per million).
És ha azt látja, hogy például a vízanalízis 100 mg / l összsótartalmat mutat, akkor ha eltávolítja az összes vizet egy liter vízből, akkor 100 milligramm sót kap. Példák a leírt mértékegység gyakorlati használatára:
- teljes sótartalom A Dnyeper folyó vize (a benne oldott összes só) 200-1000 mg / l. Vagyis ha vesz egy liter vizet, és eltávolít belőle minden vizet, szerves anyagot, olajterméket stb., a sók 200 milligrammtól 1 grammig terjedő mennyiségben maradnak (a Dnyeper összetételének ingadozása attól függ, hogy milyen messze van a szennyvíz ürítési pont városok vagy vállalkozások találhatók).
- Nitrát tartalom kútvízben a Nikolaev régióban elérheti a 100 mg/l-t. Vagyis ha vesz egy liter vizet a Nikolaev régióban található kútból, eltávolítja az összes vizet, peszticideket, egyéb szerves anyagokat, minden sót, kivéve a nitrátokat, akkor 100 milligramm nitrát marad. Ez valamivel több mint kétszerese a vízben megengedett nitráttartalomnak.
- Maximum megengedett a mangán koncentrációja (tartalma).(nehézfém) az ivásra szánt vízben nem haladhatja meg a 0,1 mg/l-t. Vagyis a mangán egy liter vízben nem lehet több, mint egy tized milligramm.
Egy másik mértékegység a víz keménységi sótartalmát tükrözi.
Oroszországban és Ukrajnában a víz keménysége(kalcium- és magnézium-sók tartalma) milligramm-ekvivalens per liter vízben mérik. Vagy gramm 1000 liter víznek felel meg. Vagyis tonnánként. Vagy mólban egy köbméter vízben. Vagy millimol per literben. Mindennek ugyanaz a jelentése.
Mi itt az ekvivalens? Miért nem fejezzük ki a víz keménységét ugyanúgy, mint más normál anyagokat, mint például a teljes sótartalom és a nitrát? A helyzet az, hogy a víz keménységét egyszerre két anyag - kalcium- és magnéziumion - határozza meg. Ahhoz, hogy a különböző anyagok egybe kerüljenek (keménység), ki kell egyenlíteni őket. Ekvivalensekre elsősorban a víztisztító szűrők kiválasztásához van szükség, és különösen.
Tehát tegyük fel, hogy 20 mg / l magnézium van a vízben, és 120 mg / l kalcium (már tudjuk, mi az a mg / l). A víz keménysége ebben az esetben körülbelül 7 mg-ekv / l. A laboratóriumok általában a víz keménységét, majd a víz kalciumtartalmát határozzák meg. Ezután kivonással határozzuk meg a magnéziumtartalmat.
Más országoknak, például Németországnak megvan a maga módja a keménység tartalmának kifejezésére. Ezt német fokozatnak hívják, és d-vel és felül egy körrel jelölik. Tehát a mi 7 meq/l-es keménységünk megközelítőleg 20 német keménységi foknak felel meg. Ezen kívül van francia keménységi fok, amerikai keménységi fok stb.
Annak érdekében, hogy ne áltassa magát az átalakításokkal, egy kis programmal konvertálhatja a merevségi mértékegységeket egyikből a másikba. Amely a "Merevség mértékegységeinek átszámítása" linkről tölthető le.
Tehát rájöttünk a merevségre. Itt az idő hogy tovább lépj. Kevésbé gyakori, de még mindig megtalálható a mgO 2 / l egység (KOI Mn: O 2, ppm). Ő mér permanganát oxidálhatóság. Az oxidálhatóság egy összetett paraméter, amely megmutatja, hogy mennyi szerves anyag van a vízben. Nem konkrét szerves anyagokat, hanem általában szerves anyagokat.
Az oxidációs permanganátot azért nevezik így, mert kálium-permanganátot adnak cseppenként a vizsgált vízhez, és meghatározzák, hogy mennyi kálium-permanganátot (kálium-permanganátot) fordítottak az összes szerves anyag oxidálására. Ha más oxidálószert (például kálium-bikromátot) adnak hozzá, akkor az oxidálhatóságot dikromátnak nevezzük. De a fentiekben meghatározott céljainkhoz a víz permanganátos oxidálhatóságára van szükség. Ennek megfelelően egy bizonyos újraszámítás segítségével meghatározzák, hogy hány milligramm tiszta oxigén O 2 kellett a vízmintában lévő összes szerves anyag oxidálásához. Ezért a mértékegység - mgO 2 /l.
Ez a mutató gyakran megtalálható az ivóvízre vonatkozó utasításokban (például a permanganát oxidációja vízben nem haladhatja meg az 5 mgO 2 / l-t). Vagyis ha több szerves anyag van a vízben, mint amennyit a szűrő el tud távolítani, akkor a szűrő átengedi a felesleges szerves anyagot.
Csapvízben a permanganát oxidációja nem haladhatja meg az 5 mgO 2 /l értéket. Ha ránézünk, akkor ez a szervesanyag-érték megfelel a fürdőszobába általában befolyó, enyhén zöldessárga víznek. A fürdőszobában lévő víz átlátszó lesz, ha a permanganát oxidálhatósága kisebb, mint 1 mgO 2 /l.
Egyébként fontos megjegyezni, hogy a dm 3 megegyezik egy literrel. Most új divat van, egy litert köbdeciméternek nevezni. Valójában egy és ugyanaz.
04.09.2014 00:40
A víz fő problémái.
Fokozott zavarosság.
A fokozott zavarosság jellemző az artézi, a kút- és a csapvízre. A víz zavarosságát a fényt szóró lebegő és kolloid részecskék okozzák. Lehet szerves és szervetlen anyag is, vagy mindkettő egyszerre. Önmagukban a részecskék a legtöbb esetben nem jelentenek komoly egészségügyi veszélyt, de a korszerű berendezéseknél idő előtti meghibásodást okozhatnak. A csapvíz megnövekedett zavarossága gyakran összefügg a csővezetékek korróziós termékeinek és a központi vízellátó rendszerben kialakuló biofilmek mechanikai leválasztásával. Az artézi vizek fokozott zavarosodásának oka általában az agyag- vagy mészszuszpenziók, valamint a levegővel érintkezve képződő vas és más fémek oldhatatlan oxidjai.
A kutak vizének minősége a legkevésbé stabil, mivel a talajvíz külső hatásoknak van kitéve. A kutak vizének nagy zavarossága a technogén szennyezettségű talajokból nehezen oldódó természetes szerves anyagok talajvízbe jutásával hozható összefüggésbe. A nagy zavarosság hátrányosan befolyásolja a vízfertőtlenítés hatékonyságát, melynek eredményeként a részecskék felületére tapadt mikroorganizmusok túlélik és tovább fejlődnek a fogyasztóhoz vezető úton. Ezért a zavarosság csökkentése gyakran javítja a víz mikrobiológiai minőségét.
vasat vízben.
A csapvíz magas vastartalma különböző okokból adódik. Ezek a szennyeződések a vezetékek korróziója vagy a víztisztító telepeken vastartalmú koagulánsok alkalmazása következtében a csapvízbe, az artézi vizekbe pedig - vastartalmú ásványokkal való érintkezés következtében - kerülnek. Az artézi vizek vastartalma átlagosan 2-10-szeresével haladja meg a standard értéket. Egyes esetekben a többlet akár 30-40-szeres is lehet. Az artézi víz általában közvetlenül a beérkezés után nem mutat látható jeleket a vasvegyületek jelenlétére, azonban légköri oxigénnel érintkezve 2-3 óra múlva sárga szín jelenhet meg, hosszabb ülepedéssel pedig világosbarna csapadék alakulhat ki. megfigyelt. Mindez egy oxidációs folyamat eredménye, melynek során hő szabadul fel. A mirigyes baktériumok fejlődésének serkentése az artézi vízben.
mangán vízben.
Az artézi kutakból származó vízben a mangán szennyeződéseket a vasszennyeződésekkel egyidejűleg mutatják ki. Kézhezvételük forrása ugyanaz - a mangántartalmú ásványok feloldása. Az ivóvízben feleslegben lévő mangán rontja annak ízét, és amikor az ilyen vizet háztartási célokra használják, sötét lerakódások figyelhetők meg a csővezetékekben és a fűtőelemek felületén. A magas mangántartalmú vízzel történő kézmosás váratlan hatáshoz vezet - a bőr először szürkévé válik, majd teljesen elfeketedik. A magas mangántartalmú víz elhúzódó asszimilációjával nő az idegrendszeri betegségek kialakulásának kockázata.
Oxidáció és szín.
A felszíni és artézi vízforrások megnövekedett oxidálhatósága és színe azt jelzi, hogy a vízben természetes szerves anyagok - humin- és fulvosavak - szennyeződések vannak jelen, amelyek az élő és élettelen természeti tárgyak bomlástermékei. A felszíni vizek szervesanyag-tartalma magas az algapusztulás időszakában (július-augusztus). A szerves szennyeződések koncentrációjának egyik jellemzője a permanganát oxidálhatósága. A tőzeg előfordulási területén, különösen a távoli északi és kelet-szibériai régiókban, ez a paraméter tízszerese lehet a megengedett értéknek. A természetes szerves anyagok önmagukban nem jelentenek veszélyt az egészségre. A vas és a mangán egyidejű vízben való jelenléte esetén azonban szerves komplexeik keletkeznek, ami megnehezíti a levegőztetéssel, vagyis a légköri oxigénnel történő oxidációval történő szűrést. A természetes eredetű szerves anyagok jelenléte a vízben megnehezíti a víz oxidatív módszerekkel történő fertőtlenítését, mivel fertőtlenítési melléktermékek keletkeznek. Ide tartoznak a trihalogén-metánok, a halogén-ecetsav, a halogén-ketonok és a halogén-acetonitril. A legtöbb tanulmány azt mutatja, hogy az ebbe a csoportba tartozó anyagok rákkeltő hatásúak, valamint negatív hatással vannak az emésztőrendszer és az endokrin rendszer szerveire. A vízfertőtlenítés melléktermékei képződésének megelőzésének fő módja a természetes szerves anyagoktól való mélytisztítás a klórozási szakasz előtt, azonban a központi vízkezelés hagyományos módszerei ezt nem biztosítják.
A víz illata.
A csap, az artézi és a kútvíz illata fogyasztásra alkalmatlanná teszi. A vízminőség értékelése során a fogyasztókat az egyéni szag-, szín- és ízérzékelés vezérli.
Az ivóvíznek nem lehet a fogyasztó számára észrevehető szaga.
A csapvíz szagának oka leggyakrabban a központi vízkezelés során a fertőtlenítés szakaszában a vízbe jutó oldott klór.
Az artézi víz szaga összefüggésbe hozható az oldott gázok - hidrogén-szulfid, kén-oxid, metán, ammónia és mások - jelenlétével.
Egyes gázok lehetnek mikroorganizmusok létfontosságú tevékenységének termékei, vagy a vízforrások ipari szennyezésének eredménye.
A kút vize a leginkább érzékeny az idegen szennyezésre, ezért gyakran kellemetlen szag társulhat olajtermékek és háztartási vegyszerek nyomaihoz a vízben.
Nitrátok
A kút- és artézi vizekben található nitrátok komoly veszélyt jelenthetnek a fogyasztók egészségére, mivel tartalmuk többszöröse lehet az ivóvízre vonatkozó jelenlegi szabványnak.
A nitrátok felszíni és felszín alatti vizekbe kerülésének fő oka a műtrágyakomponensek talajban történő migrációja.
A magas nitráttartalmú víz használata methemoglobinémia kialakulásához vezet - egy olyan állapot, amelyet a methemoglobin megnövekedett (> 1%) vérben történő megjelenése jellemez, ami megzavarja az oxigénnek a tüdőből a szövetekbe történő átjutását. A nitrátmérgezés következtében a vér légzési funkciója élesen megzavarodik, és elkezdődhet a cianózis, a bőr és a nyálkahártyák kékes elszíneződése.
Ezenkívül számos tanulmány kimutatta a nitrátok negatív hatását a jód szervezetben történő felszívódására, valamint az emberi test különböző anyagaival való kölcsönhatás termékeinek rákkeltő hatását.
A víz keménysége.
A víz keménységét elsősorban a benne lévő kalcium- és magnéziumionok koncentrációja határozza meg.
Egyes vélemények szerint a kemény víz nem jelent veszélyt a fogyasztók egészségére, ez azonban ellentmond az egyik legnagyobb táplálkozáskutató, Paul Breguet amerikai kutató sokéves kutatásának következtetéseinek. Úgy véli, hogy sikerült megállapítania az emberi test korai öregedésének okát. Ennek oka a kemény víz. Paul Brega szerint a keménységi sók ugyanúgy „lelakkítják” az ereket, mint azok a csövek, amelyeken a víz folyik, magas keménységi sók tartalommal. Ez az edények rugalmasságának csökkenéséhez vezet, ami törékennyé teszi őket. Ez különösen szembetűnő az agykéreg vékony ereiben, ami Brega szerint időskorúak szenilis őrültségéhez vezet.
A kemény víz számos háztartási problémát okoz, lerakódásokat és ütéseket okozva a csővezetékek és a háztartási készülékek munkaelemeinek felületén. Ez a probléma különösen fontos a fűtőelemes készülékeknél - melegvíz-kazánok (bojlerek), mosógépek és mosogatógépek.
A mindennapi életben kemény víz használatakor a hőátadó felületeken folyamatosan növekszik a kalcium és magnézium sók lerakódási rétege, aminek következtében csökken a hőátadás hatásfoka, és nő a fűtésre felhasznált hőenergia. Egyes esetekben a munkaelemek túlmelegedése és megsemmisülése lehetséges.
Milyen szennyeződések vannak a vízben
A természetes víz nagyszámú különféle szennyeződést tartalmaz. 1 cm.3 ivóvíz megközelítőleg 10 ezer milliárd molekula szennyeződést tartalmaz, amely természetes körforgása különböző szakaszaiban kerül a vízbe. A légkörben lecsapódó nedvesség hatására eső és hó formájában víz hullik, oxigén, nitrogén, szén-dioxid, valamint különféle füst- és kipufogógázok alkotóanyagai oldódnak fel benne. A talajon áthaladva a víz találkozik a kőzetek összetevőivel (sók, szilikátok) és szerves anyagokkal, feloldva azokat.
Oxigén jelenlétében a nemfémek ásványi és egyéb savakká alakulnak (szénsav, salétromsav, kénsav, foszforsav). A savak mészkővel és más kőzetekkel kölcsönhatásba lépve kalcium-, magnézium- és vas-hidrogén-karbonátokat hoznak létre, amelyek jól oldódnak vízben. A szilikátok alacsony oldhatóságuk miatt kisebb mennyiségben jutnak vízbe. A víz talajon keresztül történő szűrésekor ioncsere adszorpció következik be, a talajkomplexek jól megtartják a foszfátokat; A talaj által adszorbeált Na+-ionok kicserélődnek K+-ionokra. Éppen ezért a felszíni források vizében a Na+ ionok koncentrációja átlagosan 10-szer magasabb, mint a K+ ionok koncentrációja. A felszíni vizek (folyók, tavak, tározók) ásványi összetétele függ a talajok jellegétől, ahonnan a folyóvizek gyűjthetők, valamint a meteorológiai viszonyoktól és az évszaktól. A tavaszi árvízi időszakban a víz minimális mennyiségben tartalmaz jelentős lebegő részecskék tartalmú sókat, amelyeket az olvadékvíz áramlása a talaj felszínéről elszállít. A folyók természetes vizébe különféle ipari és háztartási szennyvizek kerülhetnek, amelyek szennyeződéseket is juttatnak bele.
Kémiai összetételük szerint a természetes vizek szennyeződéseit ásványi és szerves anyagokra osztják. Az ásványi szennyeződések közé tartozik a nitrogén, oxigén, szén, kén ammónia formájában, metán, hidrogén-szulfid; különféle sók, savak és bázisaik, amelyek vizes oldatban nagyrészt ionokká disszociálnak. A természetes víz élelmiszeripari technológiai szükségleteinek kielégítésekor figyelembe kell venni ezen kationok azon képességét, hogy az élelmiszer-alapanyagok anionjaival nehezen oldódó vegyületeket képezzenek. A természetes vizek jelentős mennyiségben tartalmazhatnak Na+- és K+-ionokat, amelyek a Ca2+- és Mg2+-ionokkal ellentétben nem képeznek rosszul oldódó vegyületeket az élelmiszer-alapanyagok anionjaival. A természetes vízben lévő vasionok lehetnek formában (Fe2+) és oxidált (Fe3+) formában. A talajvízben a vas általában ionos formában, Fe2+ formájában található meg, amely oldott oxigén jelenlétében Fe3+-ra oxidálódik, és rosszul oldódó hidroxiddá hidrolizálódik, kolloid oldatot vagy finom szuszpenziót képezve. A felszíni vizekben a vas szerves anyagok része lehet, melynek jelenlétében vasbaktériumok fejlődnek ki. A víz sókomponenseinek jelentős része HCO3-, CO2- és hidratált szén-dioxid H2CO3 (szénsav). Arányuk vizes oldatban engedelmeskedik a disszociáció törvényeinek, és a pH-tól függ. pH = 4,3 esetén a vízben lévő összes szén-dioxidot CO2 és H2CO3 képviseli. A pH növekedésével a CO2 része csökken, a HCO3- rész egyidejű növekedésével; pH=8,35-nél szinte az összes szén-dioxid HCO3-, pH=12-nél pedig csak CO32- formában van.
Az oldatban a HCO3 bizonyos koncentrációjának fenntartásához a vízben egyenértékű mennyiségű CO2-nak kell jelen lennie. Ez az egyensúly eltolható a vizes oldat levegővel való érintkezésekor vagy az oldat telítési (CO2-vel való telítési) folyamatában. Ennek eredményeként a CO2-tartalom nagyobb vagy kisebb lehet, mint a HCO3-CO2 rendszerben az egyensúlyi tartalomnak megfelelő érték. Ca2+ jelenlétében a feleslegben lévő CO32- előre meghatározza a CaCO3 szilárd fázisának kicsapódását az oldatból, a CO32- ionok hiánya pedig a CaCO3 kioldódását okozza. A kloridionok (Сl-) nem hoznak létre gyengén oldódó sókat a kationokkal. A szulfátionok (SO42-) csak Ca2+-nal hoznak létre nehezen oldódó sót. A szerves szennyeződések nagy koncentrációja és oxigén hiánya esetén az SO42-anion kéntartalma S2-vé redukálható. Ebben az esetben a víz kellemetlen hidrogén-szulfid (H2S) szagot kap.
A savas szilíciumvegyületek gyakoriak a természetes vizekben. Ezek a savak a víz normál pH-értékén gyengén oldódnak, és képesek kolloid oldatok képzésére (a H2SiO3 oldhatósága 20°C-on 0,15 g/kg). A víz nagyon alacsony koncentrációban (akár 10-5 g/kg) tartalmaz brómot, arzént, molibdént, ólmot és néhány egyéb nyomelemet. A természetes vizek ásványi szennyeződéseinek összetételét általában a kiváló anion jellemzi. A hidrokarbonátos vizekben a HCO-anionok, a szulfátban - SO42-, a kloridban - a Cl- Szerves szennyeződések kerülnek a vízbe a növény- és állatvilág pusztulásakor, valamint háztartási és ipari hulladékkal, élelmiszeripari szennyvízzel. vállalkozások. A talaj és a tőzeglápok kimosása következtében humin anyagok, köztük huminsavak és sóik kerülnek a nyílt víztestekbe. Ez a víz sárga. A humuszvegyületek egyes vegyületeinek tartalma jelentősen befolyásolhatja a víztisztítás folyamatát. A szerves szennyeződések a fő okai a víz kellemetlen színének, ízének és szagának.
A természetes vizek szennyeződései a diszperzió mértékében különböznek. A szemcsemérettől függően az oldatok igazak (részecskeátmérő 10-7 cm), kolloidok (részecskeátmérő 10-7-10-5 cm) és szuszpenziók (részecskeátmérő 10-5 cm) Az igazi oldatok homogén rendszerek, amelyekben a részecskék a vízben egyedi molekulák és ionok formájában oszlanak meg.A kolloid oldatok heterogének, amelyekben a részecskék nagyszámú molekula agglomerátumaként és a szilárd fázis és a víz között elválasztó felületként oszlanak meg.A kis méretűek miatt kolloid részecskék mérete miatt nem válnak el a víztől üledékké a gravitációs erő hatására, és nem veszítik el diffúziós képességüket.A kolloid oldatok hajlamosak a fény szórására, ami a víz opálosságát okozza.A durván diszpergált (szuszpendált) részecskék tömege nagyobb, mint a kolloidé , és gyakorlatilag nem képesek a diffúzióra.Idővel ezek a szennyeződések kicsapódnak vagy lebegnek a felszínre "Az ilyen szennyeződések határozzák meg a víz zavarosságát. Természetes vizekben iszap, homok, növényi részecskék szuszpenzióban vannak. A természetes víz különböző természetes gázokat is tartalmaz. eredetű, amelynek vízben való oldhatósága függ a gázok kémiai természetétől, a hőmérséklettől, a víz mineralizációs fokától és attól, hogy a gáz milyen nyomáson van a víz felett. Vízben jól oldódó CO2 és H2S, amelyek általában szén- és hidrogén-szulfidsavat képeznek a vízzel. Rosszul
oldja a CH4, N2, O2, H2, Ar, He. Gyakorlatilag nem lépnek kémiai kölcsönhatásba vízzel, és molekulárisan diszpergált állapotban vannak. A hőmérséklet emelkedésével és az ásványi anyagok összetételének növekedésével a gázok oldhatósága csökken. Állandó hőmérsékleten a gázok oldhatósága a Henry-törvény szerint a nyomással egyenes arányban változik. Ezért általában minél mélyebbre kerül az artézi kutak vízfelvétele, annál jobban telítődik a víz gázokkal. Amikor ilyen víz kerül a felszínre, amikor a vízben lévő gáz rugalmassága nagyobb lesz, mint a légkörben, intenzív felszabadulás figyelhető meg. Az ilyen gázt spontánnak, a vizet gázosodásnak nevezzük. A természetes vizet az ásványi és szerves anyagokon kívül biológiai természetű szennyeződések is szennyezik. A víz különféle mikroorganizmusokat tartalmaz. Ezen kívül tartalmazhat penészgombákat, baktériumokat, élesztőket, gombákat, algákat, csillóféléket, bélféreg tojásait stb. A vízben fejlődő mikroorganizmusok csökkenthetik a benne lévő szerves anyagok tartalmát, mineralizálhatják azokat, ami hozzájárul a tisztításához.
A kórokozó (kórokozó) mikroorganizmusok emberi fertőző betegségeket (dizentéria, kolera, tífusz, gyermekbénulás stb.) okozhatnak, ezért az ivóvizet biológiailag kell tisztítani.
Egészen új a mindennapi életünkben. Független és állami szervezetek, intézmények által végzett elemzések azt állítják, hogy hazánkban napról napra kevesebb a tiszta és „jó” víz. Természetesen felidézhetjük a Bajkált - a világ legnagyobb édesvízkészletét, de területét szó szerint vissza kell nyerni akár azoktól, akik a közelben akarnak üzemet építeni, vagy más szerencsétlenségtől.
Azok vagyunk, amit iszunk. "Tiszta víz" csak laboratóriumokban fordul elő
A városlakók szó szerint bölcsőtől kezdve hozzászoknak a csapvíz sajátosságaihoz. A kóros mikroflórától megszabadulni, klórkészítményekkel bőkezűen fűszerezve, a központi autópályák régi fémcsövei sajátos ízt adnak.
A vízminőség javítása érdekében a felhasználók különféle szűrőket vásárolnak. Lehetnek helyhez kötöttek a vízellátásba való beépítéshez, vagy mobilak lehetnek kancsók formájában. Különféle ikonok biztatják a vásárlókat: „Jóváhagyva” és „Ajánlott”, de hogy valójában mit, hogyan tisztítanak, és hogy ettől lesz-e legalább egy kicsit jobb a víz, azt a hétköznapi polgár nem tudja.
Annak érdekében, hogy a szűrőket valóban helyesen használják, és előnyökkel járjanak, először elemezni kell az ivóvizet a különféle szennyeződések jelenlétére, és csak ezután, ha erre szükség van.
Nincs szabványos csodaszer, mert a víz a különböző településeken eltérő összetételű és ízű. És a városi vízellátás mellett saját vízvételi helyek is vannak: kutak, artézi és abesszin kutak, természetes források és források. A bennük lévő víz majdnem annyira különbözik, mint az ujjlenyomatok.
A szennyeződések veszélye abban rejlik, hogy legtöbbjük vízben oldva szabad szemmel láthatatlan. Ugyanolyan kristálytiszta és tiszta, a veszélyes összetevők jelenléte pedig csak laboratóriumi vizsgálatok segítségével mutatható ki.
Kiváló oldószer tulajdonságai miatt a víz útközben felvesz egy keveset minden átmosódó kőzetből vagy anyagból. A lehetséges szennyeződések száma a sima vízben elképesztő - körülbelül 70 000 különböző anyag, amelyből 13 000 különböző veszélyességű toxin.
Káros és hasznos
Ideális esetben az ivóvíz kiegyensúlyozott összetételű. Egy liter nyers folyadék körülbelül 500 mg különféle sókat és oldható anyagokat tartalmaz. Az osztályozás megkönnyítése érdekében ezeket általában négy kategóriába sorolják, amelyeket közös jellemzők egyesítenek:
- Oldhatatlan anyagok, amelyek szuszpenziókat és szuszpenziókat képeznek, amelyek aktív hidrodinamikai hatások nélkül kicsapódnak;
- Hidrofób és hidrofil szerves és kolloid ásványi anyagok, valamint humusz és vírusok, amelyek részecskéi arányosak velük;
- Molekulárisan oldódó anyagok - szerves anyagok és gázok;
- Ionokra osztott anyagok.
Szerves anyagok, fizikai részecskék, fémek, nemfémek, nitrátok vannak jelen a vízben. Az egészségügyi szabványok minden egyes anyagra vagy hasonló vegyületcsoportra (klórtermékekre) írják elő a megengedett koncentrációt. A csapvíz és a palackozott víz esetében szigorúbb az ellenőrzött összetevők listája, mint a háztartási kútból vagy kútból származó víz esetében.
A rengeteg szennyeződés közül kiemelik az osztályukban leggyakoribb és az emberi egészségre veszélyes szennyeződéseket. A szennyezett víz hosszú távú fogyasztása tele van betegségekkel.
nem fémek
Ebbe a csoportba tartozik a fluor. Mindenki, aki látott már fogkrémreklámokat, tudja annak fontosságát a szervezet számára, különös tekintettel a csontokra és a fogakra. Az emberi csontokban és fogakban található. Fluortöbblet esetén fluorózis jelenik meg. Először is a fogak szenvednek, a fogyasztási arány jelentős túllépése esetén a csontok szerkezete megzavarodik. Ha a felesleges fluort eltávolítják az étrendből, tünetei enyhülnek.
A víz brómos szennyeződése a vegyipari vállalkozások kibocsátása miatt következik be. Hiánya befolyásolja a normál alvási szokásokat és a vér összetételét, feleslege bromodermához (bőrbetegség) vezet.
A vízkezelő rendszerekkel kapcsolatban két általános vélemény létezik. Az első azt mondja, hogy ésszerűen meg kell tisztítani, és csak olyan elemzések elvégzése után, amelyek bizonyítják egy adott szennyeződés jelenlétét, a másik radikálisabb - jobb általános teljes tisztítást végezni, és megszabadulni mindentől, ami káros és hasznos, a lényeg az, hogy tiszta vizet igyunk
A jód létfontosságú nyomelem, amely minden élő szervezetben jelen van, de a természetes lerakódások nagyon ritkák. A hiány fejlődési rendellenességekkel jár: kreténizmus, pajzsmirigy alulműködés, pajzsmirigybetegség. Napi bevitele 0,2 mg, halálos adagja 2-3 g Jódmérgezés esetén minden szervezetrendszer érintett.
Az arzén egy kicsit hasonlít a jódhoz. Erősen mérgező, de szükséges a szervezet normális fejlődéséhez, felhalmozódik a szövetekben. A vegyiparon kívül számos természetes arzénforrás létezik (vulkáni hamu, fémérc, ásványforrások).
A túl sok kalcium és magnézium nem csak károsítja a vizet, hanem megkeményíti is. Forráskor sűrű sárgás bevonat képződik az edényeken és a fűtőelemeken.
A klór régi barát, enélkül nehéz elképzelni a városi vizet. Magánkutakban fertőtlenítésre is használják készítményeit. Hatással van a vesére és a májra, az idegrendszerre, csökkenti az immunitást, allergiát vált ki.

Azt a tényt, hogy a víz tartalmaz "néhány szennyeződést", úgy tudjuk meg, ha belenézünk a teáskannáinkba és edényeinkbe
Fémek
A víz összetételében található fémek köre kiterjedt. A radioaktív és nehéz anyagok kifejezett rákkeltő hatással rendelkeznek. Az ólmot az egyik legveszélyesebbnek tartják. Megzavarja a központi és perifériás idegrendszert, provokálja a neoplazmák kialakulását.
A higany hatással van a belső szervekre, a légzőrendszerre és a központi idegrendszerre.
A vas gyakran megtalálható az artézi vízben. Mint a legtöbb szennyeződés, ez is megüti a májat és a szívet, csökkenti a reproduktív funkciót. Mielőtt helyrehozhatatlan változások következnének be az egészségben, észrevehet vöröses csíkokat a vízvezetékeken és az edényeken, és behelyezheti a vízkezelő rendszert.
Összetett kapcsolatok
Ide tartoznak a peszticidek és a nitrátok. Ezek erős rákkeltő anyagok. Lehetetlen észrevenni a nitrátok keveredését a vízben. A kisgyermekek különösen érzékenyek a mérgezésre, és haláleseteket is feljegyeztek.
Számos káros szennyeződés lényege, hogy baktériumokkal vagy más szennyeződésekkel kölcsönhatásba lépve még egészségre veszélyesebb anyagokká alakulnak. A higanyból metil-higany lesz, ami hatással van az agyra, a réz pedig a kadmiummal együtt nagyon mérgező vegyületet képez.
Ezeknek az anyagoknak a koncentrációja arányos a mezőgazdasági tevékenységgel, és a műtrágyák és fertőtlenítőszerek szabálytalan használatával függ össze. Nincs idejük lebomlani, és csapadékkal kutakba és tározókba esnek.
Káros szerves anyagok
Ebbe a csoportba tartozik. Általában hiányozniuk kell az ivóvízből. Pozitívum, hogy főzéskor szinte mindegyik elpusztul, bár kielégítő körülmények között hetekig-hónapokig aktívak maradnak.
A kevésbé kellemetlen szerves szennyeződések közé tartoznak a növények és rovarok salakanyagai. Feltűnő megjelenésűek és jellegzetes szagot adnak a víznek.
Diagnosztikai intézkedések
Új kút rendezése vagy régi kút újraélesztése során a veszély kiküszöbölése érdekében a vizet elemzésre átadják a laboratóriumnak, fertőtlenítést végeznek. Csak a kielégítő eredmények elérése után lehet biztonságosan inni vizet közvetlenül a csapból vagy a szűrőrendszerből.
Egyes szennyeződések otthon is meghatározhatók. Kellemetlen szag formájában nyilvánulnak meg, különböző árnyalatokban színezve a vizet, üledék megjelenésében és az edények festésében. Az olajtermékek keverékét könnyű cserélni - olajosan irizáló film jelenik meg a vízen, a víz kellemetlen utóízt kap. A víz hőmérsékletének változása a kút rendetlenségének jele. A savasság közönséges lakmuszcsíkokkal határozható meg.