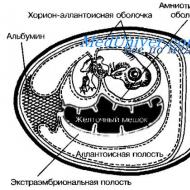
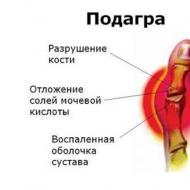
A fehérjeanyagcsere második szakaszának megsértése - az endogén fehérjeszintézis és lebontás folyamatai. A fehérjeanyagcsere zavarai az emberi szervezetben vagy a vegánság veszélye Mikrobák fehérjeszintézisének zavarai
A fehérjeanyagcsere jelentőségét a szervezet számára mindenekelőtt az határozza meg, hogy minden szöveti elemének alapját fehérjék alkotják, amelyek fő részeik asszimilációs és disszimilációs folyamatai miatt folyamatosan megújulnak. - aminosavak és komplexeik. Ezért a fehérje anyagcsere zavarai különböző változatokban kivétel nélkül minden kóros folyamat patogenezisének összetevői.
A fehérjék szerepe az emberi szervezetben:
· minden szövet szerkezete
növekedés és helyreállítás (regeneráció) a sejtekben
· az enzimek, gének, antitestek és hormonok fehérjetermékek
az onkotikus nyomáson keresztül befolyásolja a vízháztartást
· részvétel a sav-bázis egyensúly szabályozásában
A fehérjeanyagcsere-zavarokról általános képet kaphatunk a szervezet és a környezet nitrogén egyensúlyának tanulmányozásával.
1. Pozitív nitrogén egyensúly olyan állapot, amikor kevesebb nitrogén ürül ki a szervezetből, mint amennyi a táplálékból bekerül. Megfigyelhető a test növekedése során, terhesség alatt, koplalás után, az anabolikus hormonok (GH, androgének) túlzott szekréciójával.
2. Negatív nitrogén egyensúly olyan állapot, amikor több nitrogén ürül ki a szervezetből, mint amennyit a táplálékból beveszünk. Koplalással, proteinuriával, vérzéssel, katabolikus hormonok (tiroxin, glükokortikoidok) túlzott szekréciójával alakul ki.
Tipikus fehérje anyagcsere zavarok
1. A szervezetbe jutó fehérje mennyiségének és minőségének megsértése
2. A fehérjék felszívódásának és szintézisének károsodása
3. Az intersticiális aminosav-anyagcsere megsértése
4. A vér fehérje összetételének megsértése
5. A fehérjeanyagcsere végső szakaszának megsértése
1. A szervezetbe jutó fehérje mennyiségének és minőségének megsértése
A) A fehérjeanyagcsere-zavarok egyik leggyakoribb oka az mennyiségi vagy jó minőség fehérjehiány. Ennek oka a böjt alatti korlátozott exogén fehérjeellátás, az élelmiszer-fehérjék alacsony biológiai értéke és az esszenciális aminosavak hiánya.
A fehérjehiány megnyilvánulásai:
negatív nitrogénmérleg
a test növekedésének és fejlődésének lassulása
a szöveti regenerációs folyamatok elégtelensége
fogyás
Csökkent étvágy és fehérje felszívódás
A fehérjehiány szélsőséges megnyilvánulása a kwashiorkor és a táplálkozási marasmus.
A táplálkozási marasmus olyan kóros állapot, amely hosszan tartó teljes éhezés következtében alakul ki, és általános kimerültséggel, anyagcserezavarokkal, izomsorvadással és a legtöbb szerv és rendszer működési zavarával jellemezhető.
A Kwashiorkor egy olyan betegség, amely kisgyermekeket érint, és a fehérje minőségi és mennyiségi hiánya okozza az élelmiszer általános kalóriafeleslegét.
b)Túlzott fehérjebevitel a következő változásokat okozza a szervezetben:
pozitív nitrogén egyensúly
dyspepsia
· dysbacteriosis
intestinalis autoinfectio, autointoxication
idegenkedés a fehérjetartalmú ételektől
2. A fehérjék felszívódásának és szintézisének károsodása
· a fehérjék lebontásának zavarai a gyomorban (csökkent szekréciós aktivitású és alacsony savasságú gyomorhurut, gyomor reszekciók, gyomordaganatok). A fehérjék idegen antigén információ hordozói, és az emésztés során le kell bontani, elveszítik antigenicitásukat, különben hiányos lebontásuk ételallergiához vezet.
· felszívódási zavar a bélben (akut és krónikus hasnyálmirigy-gyulladás, hasnyálmirigy daganatok, duodenitis, enteritis, vékonybél reszekció)
szabályozó és szerkezeti gének patológiás mutációi
A fehérjeszintézis szabályozási zavara (az anabolikus és katabolikus hormonok arányának változása)
3. Az intersticiális aminosav-anyagcsere megsértése
1. Károsodott transzamináció (aminosavak képződése)
· piridoxin hiány (B6-vitamin)
· böjt
májbetegségek
2. A károsodott dezamináció (az aminosavak elpusztítása) hiperaminoacidémiát ® aminoaciduria ® az egyes aminosavak arányának változását okozza a vérben ® károsítja a fehérjeszintézist.
piridoxin, riboflavin (B 2), nikotinsav hiánya
hypoxia
· böjt
3. A károsodott dekarboxiláció (CO 2 és biogén aminok képződésével megy végbe) nagy mennyiségű biogén aminok megjelenéséhez vezet a szövetekben, és megzavarja a helyi vérkeringést, megnövekszik az érpermeabilitás és károsodik az idegrendszer.
hypoxia
ischaemia és szövetpusztulás
4. A vér fehérje összetételének megsértése
hiperproteinémia - plazmafehérje emelkedése > 80 g/l
A hiperproteinémia következményei: megnövekedett vérviszkozitás, reológiai tulajdonságainak megváltozása és károsodott mikrokeringés.
Hipoproteinémia- a fehérjeszint csökkenése a vérplazmában< 60 г/л
· böjt
Az emésztés és a fehérjék felszívódásának zavara
Károsodott fehérjeszintézis (májkárosodás)
fehérjeveszteség (vérveszteség, vesekárosodás, égési sérülések, gyulladás)
fokozott fehérjelebomlás (láz, daganatok, katabolikus hormonok)
A hipoproteinémia következményei:
· ¯ a test ellenállása és reakciókészsége
· az összes testrendszer működésének zavara, mert az enzimek, hormonok stb. szintézise megszakad.
5. A fehérjeanyagcsere végső szakaszának megsértése. A fehérjeanyagcsere végső szakaszának patofiziológiája magában foglalja a nitrogéntartalmú termékek képződésének és a szervezetből való eltávolításának folyamatait. A maradék vérnitrogén a fehérjék kicsapódása után visszamaradó nem fehérje nitrogén.
Általában 20-30 mg% összetétel:
· karbamid 50%
aminosavak 25%
· egyéb nitrogéntartalmú termékek 25%
Hiperazotémia - a maradék nitrogénszint növekedése a vérben
![]()
A maradék nitrogén felhalmozódása a vérben az egész szervezet, elsősorban a központi idegrendszer mérgezéséhez és kóma kialakulásához vezet.
A mikroorganizmusok riboszómáin lévő fehérjék szintézisében, amelyek 30S és 50S alegységekből állnak (emberben - 60S és 40S alegységek; ülepedési egységek), a következő szakaszokat különböztetjük meg:
1) megindítás, inicializálás– aminosavak összekapcsolása mRNS-sel tRNS segítségével (a tRNS antikodon triplett kölcsönhatásba lép az mRNS kodonnal);
2) megnyúlás– a tRNS új aminosavval történő kapcsolódása a riboszóma A (acil) helyén található mRNS kodonhoz;
3) transzpeptidáció– a P helyről (peptidil) már kialakult peptid kötődése egy új aminosavhoz a riboszóma A helyén;
4) transzlokáció– a riboszóma mRNS mentén történő mozgása miatt a keletkező peptid az A helyről a P helyre kerül; A tRNS leválik (83. ábra).
Rizs. 83. A fehérjeszintézis főbb szakaszai riboszómákon.
A fehérjeszintézist megzavaró antibiotikumok közé tartoznak az aminoglikozidok, tetraciklinek, kloramfenikol, makrolidok és linkozamidok.
Aminoglikozidok megzavarják az új aminosav megfelelő hozzáadását.
Tetraciklinek megakadályozzák, hogy a tRNS antikodon csatlakozzon az mRNS kodonhoz.
Klóramfenikol megzavarja a transzpeptidációt.
MakrolidokÉs linkozamidok befolyásolják a transzlokációs folyamatokat és versenyezhetnek egymással (egyidejűleg antibakteriális hatásuk gyengül).
Aminoglikozidok
Az aminoglikozidok széles spektrumú antibiotikumok. Gram-negatív és néhány gram-pozitív baktériumra hatnak. Ne hatjon meticillinrezisztens staphylococcusokra.
Az aminoglikozidok nem hatolnak át jól a bakteriális sejtfal porinjain. Az antibiotikumok (különösen a penicillinek), amelyek megzavarják a sejtfal integritását, megkönnyítik az aminoglikozidok behatolását a baktériumsejtbe.
Az aminoglikozidok oxigénfüggő aktív transzporttal hatolnak be a baktériumok citoplazmatikus membránján (ezért hatástalanok az anaerob baktériumokkal szemben).
A baktériumsejt citoplazmájába behatolva az aminoglikozidok a 30. riboszomális alegységre hatnak. Megzavarják a fehérjeszintézis kezdeti szakaszait a bakteriális riboszómákon. Az aminoglikozidok zavarják az mRNS helyes leolvasását. Ennek eredményeként az A helyre más aminosavak kerülnek (83. ábra), és „helytelen” (nem működő) fehérjék képződnek, amelyek károsító hatással vannak a citoplazma membránjára.
Nagyobb dózisokban az aminoglikozidok megzavarják a poliszómák képződését. Az aminoglikozidok hatására a poliszómák egyedi riboszómákra (monoszómákra) oszlanak, amelyek nem képesek az mRNS mentén mozogni.
Így az aminoglikozidok hatása megzavarja:
1) a citoplazma membrán permeabilitása;
2) bakteriális fehérjék szintézise.
Az aminoglikozidok baktericid hatásúak.
Az aminoglikozidok erősen poláris vegyületek (polikationok). Gyakorlatilag nem szívódnak fel a gyomor-bél traktusból, ezért intramuszkulárisan vagy intravénásan adják be. Ne hatoljon át a vér-agy gáton. Behatol a szem üvegtestébe. Áthatolni a placentán. Nagy koncentrációban a mirigyek váladékában, a pleurális folyadékban és az ízületekben határozzák meg.
Az aminoglikozidok rosszul metabolizálódnak a szervezetben; 50-60%-a változatlan formában ürül ki a vesén keresztül. Ez hozzájárul az aminoglikozidok hatékonyságához a vese- és húgyúti fertőző betegségekben. Ugyanakkor veseelégtelenség esetén az aminoglikozidok toxikus hatása (ototoxicitás, nefrotoxicitás) nő.
Az aminoglikozidokat főként az aminoglikozidokra érzékeny mikroorganizmusok által okozott súlyos fertőzések esetén alkalmazzák (szepszis, hashártyagyulladás, húgyúti fertőzések, tüdőgyulladás, seb- és égési fertőzések).
Az aminoglikozidok következő generációit különböztetjük meg:
I generáció– sztreptomicin, kanamicin, neomicin;
II generáció– gentamicin, tobramicin;
III generáció- amikacin, netilmicin.
Sztreptomicin(Streptomycin) az első olyan felfedezett antibiotikum, amely hatékony a Mycobacterium tuberculosis ellen. A sztreptomicin felfedezéséért S. A. Waksman (USA) 1952-ben Nobel-díjat kapott. Ő alkotta meg az „antibiotikum” kifejezést is.
A sztreptomicin rendkívül hatékony gyógyszernek bizonyult pestis, tularémia és brucellózis kezelésére is. Hatékony coccusok (a pneumococcusok viszonylag ellenállóak), Haemophilus influenzae, Klebsiella, Shigella, Salmonella ellen. Az anaerobok, a spirocheták, a rickettsiák és a Pseudomonas aeruginosa rezisztensek a sztreptomicinnel szemben. A sztreptomicint tuberkulózis, tularémia, pestis (doxiciklinnel együtt), brucellózis, valamint tüdőgyulladás és krónikus komplikált húgyúti fertőzések esetén alkalmazzák. Intramuszkulárisan vagy intravénásan beadva.
Kanamycin(Kanamycin) akkor alkalmazható, ha a Mycobacterium tuberculosis rezisztens a streptomycinnel szemben.
Neomicin(Neomicin) a nagyobb toxicitás miatt csak helyileg alkalmazzák. A gyógyszer enterálisan beadva nem szívódik fel, szájon át alkalmazható enteritis esetén, valamint a bélmikrobiális flóra műtét előtti elnyomására.
Tól től II generációs aminoglikozidok a leggyakrabban használt gentamicin.
Gentamicin(Gentamicin) hatásos staphylococcusok, enterococcusok, Escherichia coli, Shigella, Salmonella, Klebsiella, Proteus, tularemia bacillusok, Brucella ellen. Az első generációs gyógyszerekkel ellentétben a gentamicin és más második generációs gyógyszerek a Pseudomonas aeruginosa-ra hatnak. Az anaerob baktériumok, meningococcusok, Treponema pallidum, mycoplasmák, chlamydia, legionella rezisztensek a gentamicinnel szemben. A gentamicin hatástalan a tuberkulózis ellen. A gentamicint intramuszkulárisan vagy intravénásan (lassan vagy csepegtetve) adják be; t 1/2 gentamicin – 2-3 óra); A változatlan gentamicin 50-60%-a a vesén keresztül ürül.
A gentamicint tüdőgyulladás, tüdőtályog, szepszis, hashártyagyulladás, enterococcusok által okozott endocarditis (benzilpenicillinnel együtt), akut epehólyag- és cholangitis, akut és krónikus pyelonephritis, hólyaghurut, prosztatagyulladás, bőr gennyes fertőzései, lágyrész-gyulladás, csontritkulás esetén alkalmazzák. , ízületek, a gentamicinre érzékeny mikroorganizmusok által okozott seb- és égési fertőzésekre.
A gentamicint külsőleg pyoderma, fertőzött sebek kezelésére, valamint szemészeti gyakorlatban blefaritisz, kötőhártya-gyulladás kezelésére használják szemcsepp formájában (1 csepp naponta 4-6 alkalommal).
A gentamicin mellékhatásai:
- halláskárosodás;
- vesztibuláris rendellenességek;
- hányinger, hányás;
- májműködési zavar;
- proteinuria, izomgyengeség;
- leukopenia;
- bőrkiütések.
A gentamicin ellenjavallt myasthenia gravisban.
Tobramicin(Tobramycin) tulajdonságai és felhasználása hasonló a gentamicinhez. Hatékonyabb a Pseudomonas aeruginosa ellen. A gyógyszer formájában a Tobrex-et szemcseppként használják blepharitis, conjunctivitis, keratoconjunctivitis és iridocyclitis kezelésére.
Harmadik generációs aminoglikozidok– amikacin, netilmicin – hatásspektrumában hasonló a gentamicinhez és a tobramycinhez. Hatékony az első és második generációs aminoglikozidokra rezisztens baktériumok ellen.
Amikacin(amikacin) – a legszélesebb hatásspektrumú aminoglikozid; akkor alkalmazzák, ha a gentamicin hatástalan. Hatékony a Mycobacterium tuberculosis ellen.
Felhalmozódik az intercelluláris folyadékban, és a veséken keresztül nagy koncentrációban választódik ki a vizelettel. Az amikacint tüdőgyulladás, tüdőtályog, endocarditis, vese- és húgyúti fertőzések, osteomyelitis, égési fertőzések, valamint a tuberkulózis komplex kezelésére használják. Intramuszkulárisan vagy intravénásan beadva.
Netilmicin(Netilmycin) tulajdonságaiban hasonló az amikacinhoz.
Az orvosi gyakorlatban használt egyéb aminoglikozidok a szisomicin, a paromomicin és a framycetin.
Szizomycin(Sisomycin) intramuszkulárisan vagy intravénásan adják be az epe és a húgyúti fertőzések, tüdőgyulladás, agyhártyagyulladás, hashártyagyulladás, szepszis, fertőző ízületi gyulladás, osteomyelitis esetén.
paromomicin(Paromomycin) rosszul szívódik fel a gyomor-bél traktusból. Szájon át felírt gyomor-bélhurut, enterocolitis, szalmonellózis, shigellózis, amőbiasis, giardiasis kezelésére, valamint bélműtétekre való felkészülés során.
Framycetin(Framycetin) helyi használatra szánt gyógyszer. Orrspray formájában nátha, nasopharyngitis és arcüreggyulladás esetén használják.
Az aminoglikozidok mellékhatásai:
1) nefrotoxikus hatás(vesetubuláris károsodás) hosszú távú használat esetén (gentamicin > tobramycin > amikacin = sztreptomicin, netilmicin);
2) ototoxikus hatás(a cochlea és a vestibularis apparátus érzékeny sejtjeinek visszafordíthatatlan károsodása):
- A halláskárosodás leggyakrabban amikacin, netilmicin, tobramicin okozza;
- vestibularis rendellenességek(szédülés, ataxia, egyensúlyzavar) leggyakrabban amikacin, streptomycin, gentamicin okozza; az aminoglikozidok ototoxikus hatása jelentősen fokozódik, ha kacsdiuretikumokkal (furoszemid stb.) kombinálják, amelyek szintén ototoxikus tulajdonságokkal rendelkeznek;
- neuromuszkuláris átviteli zavarok(megakadályozza a Ca 2+ -ionok bejutását a motoros idegrostok végződéseibe a preszinaptikus membrán depolarizációja során); fokozhatja a cura-szerű gyógyszerek hatását;
- allergiás reakciók.
Az aminoglikozidok ellenjavallt myasthenia gravisban.
Aminociklitolok
Spectinomycin(Spectinomycin; trobicin) egy széles spektrumú antibiotikum. Kémiai szerkezetében hasonló az aminoglikozidokhoz, de hatásmechanizmusában különbözik tőlük. Megzavarja a fehérjeszintézist a transzlokációs szakaszban anélkül, hogy befolyásolná (az aminoglikozidokkal ellentétben) az mRNS kodon helyes leolvasását. Bakteriosztatikusan hat. Különösen hatékony (baktericid) a Neisseria gonorrhoeae ellen. Szinte teljesen (90%) változatlan formában ürül ki a veséken keresztül.
A Spectinomycint csak férfiak és nők urogenitális gonorrhoeájának kezelésére használják. A szövődménymentes gonorrhoea (akut urethritis, proctitis, cervicitis) egyetlen intramuszkuláris spektinomicin injekcióval gyógyítható.
Streptograminok
Quinupristin(Kvinupristin) és dalfoprisztin(Dalfopristin) megzavarja a fehérjeszintézist azáltal, hogy az 50S riboszomális alegységre hat, és gátolja a peptidil-transzferázt. Ezek a gyógyszerek külön-külön hatástalanok, de együtt alkalmazva baktericid hatásúak a gram-pozitív baktériumokkal, különösen a meticillin-rezisztens staphylococcusokkal, vancomycin-rezisztens enterococcusokkal, streptococcusokkal és staphylococcusokkal szemben. A dalfoprisztin megváltoztatja a riboszómák szerkezetét, növelve a quinupristin riboszómákhoz való kötődését.
Ezen vegyületek kombinációs készítményét intravénásan adják be vankomicinre rezisztens enterococcusok és staphylococcusok által okozott fertőzések kezelésére. A gyógyszer hatékony a Haemophilus influenzae, Moraxella, Mycoplasma, Legionella és Chlamydia által okozott fertőzések ellen. Nem érinti a Pseudomonas aeruginosa-t.
Mellékhatások:
- phlebitis;
- ízületi fájdalom;
- myalgia.
Tetraciklinek
A tetraciklinek (kémiai szerkezetükben 4 kondenzált gyűrűt tartalmaznak) széles spektrumú antibiotikumok. Megzavarják a fehérjeszintézist a bakteriális riboszómákon. A 30S riboszomális alegységre hat; megakadályozza, hogy a transzfer RNS (tRNS) az A helyen kapcsolódjon a következő aminosavhoz, megzavarva ezzel az elongációs folyamatot. A tetraciklinek hatása bakteriosztatikus.
A tetraciklinek jól behatolnak a sejtekbe, és hatnak az intracelluláris mikroorganizmusokra - chlamydia, legionella, mycoplasma, rickettsia.
A tetraciklinek (leggyakrabban a doxiciklin) a választott gyógyszerek rickettsiosis (tífusz stb.), brucellózis (gentamicinnel vagy rifampicinnel együtt), kolera, pestis, tüdő és húgyúti chlamydia, mycoplasma vagy ureaplasma okozta fertőzések, Lyme-kór esetén betegség (kullancs által terjesztett borreliosis).
A tetraciklinek a szifilisz, a gonorrhoea, a lépfene, a jersiniosis, a shigellosis és az amőbiasis tartalék gyógyszerei.
Hatékony coccusok, Haemophilus influenzae, Klebsiella, Legionella, Escherichia coli, H. pylori, Salmonella, tularemia kórokozók és Plasmodium malária ellen.
Nem hatnak a Pseudomonas aeruginosa, Bacteroides, Proteus, meticillinrezisztens staphylococcusokra.
A tetraciklinek szájon át adva felszívódnak (tetraciklin 60%, doxiciklin szinte teljesen). A tej, savkötők és vas-kiegészítők késleltethetik a tetraciklinek felszívódását, mivel a tetraciklinek kelátokat képeznek Ca 2+, Mg 2+, Al 3+, Fe 2+ ionokkal.
A Ca 2+ -ionokkal kelátvegyületek képződése miatt a tetraciklinek a csontszövetben, valamint a fogszövetben lerakódnak, és megzavarhatják fejlődésüket. A tetraciklineket nem szabad 8 év alatti gyermekeknek, terhes vagy szoptató nőknek felírni.
Doxiciklin(Doxycycline; vibramicin) szájon át írják fel rickettsiosis (tífusz, stb.), chlamydia okozta fertőzések (trachoma, psittacosis, urogenitális chlamydia), brucellózis, pestis, kolera, kullancs által terjesztett borreliosis (Lyme-kór), légúti fertőzések ( tüdőgyulladás, súlyosbodó krónikus hörghurut), gyomor-bél traktus, húgyúti rendszer, valamint lépfene, malária, mint tartalék gyógyszer szifiliszre.
Szinte teljesen felszívódik a bélben (kb. 90%). A hatás időtartama - 12 óra (napi kétszer előírva). A vesén keresztül inaktív metabolitok formájában ürül ki. A gyógyszert intravénásan is beadják.
A doxiciklin mellékhatásai:
- dyspeptikus rendellenességek;
- fejfájás;
- látás károsodás;
- hepatotoxikus hatás;
- a bőr fényérzékenysége;
- bél candidiasis;
- lehetséges pszeudomembranosus colitis.
Tetraciklin(Tetraciklint) szájon át ugyanazon indikációkra írják fel, mint más tetraciklineket. A hatás időtartama - 6 óra (napi 4 alkalommal). Helyileg kötőhártya- és blepharitis esetén tetraciklin szemkenőcsöt használnak (naponta 2-3 alkalommal a szemhéj mögé helyezve).
Oxitetraciklin(Oxitetraciklin) orálisan vagy intramuszkulárisan tüdőgyulladás, hörghurut, mandulagyulladás, epehólyag-gyulladás, pyelonephritis, bélfertőzések, endometritis, prosztatagyulladás, valamint rickettsiosis, szifilisz, gonorrhoea, brucellózis esetén írják fel. Az oxitetraciklint helyileg kenőcs formájában alkalmazzák kötőhártya-gyulladás, blepharitis és trachoma kezelésére.
A tetraciklinek mellékhatásai:
Hányinger, hányás, glossitis;
A szájüreg, a belek, a hüvely kandidózisa (a normál mikroflóra elnyomásával összefüggésben);
A máj diszfunkciója;
Bőrkiütések, fényérzékenység, allergiás reakciók;
A retina és a csontvelő működésének lehetséges rendellenességei (anémia, neutropenia).
A tetraciklinek a csontszövetben rakódnak le, így korai életkorban a csontszövet és a fogak fejlődési rendellenességei lehetségesek; A tetraciklinek alkalmazása nem javasolt 8 év alatti gyermekek, terhes vagy szoptató nők számára. A tetraciklinek hosszú távú alkalmazása esetén a makrofágok aktivitásának gátlása és az immunitás csökkenése lehetséges.
A tetraciklinek azáltal, hogy megzavarják a bakteriális fehérjék szintézisét, lelassítják növekedésüket, ezért gyengíthetik a penicillinek hatását, amelyek baktericid hatással vannak a baktériumok szaporodására.
Klóramfenikol
Klóramfenikol(klóramfenikol; kloramfenikol) egy széles spektrumú antibiotikum. Megzavarja a fehérjeszintézist a bakteriális riboszómákon. Az 50S riboszomális alegységre hat; gátolja a peptidiltranszferázt, és így megakadályozza a transzpeptidációt - a peptidlánc átvitelét a P helyről az A helyre, hogy egy új aminosavhoz kapcsolódjon (83. ábra). Bakteriosztatikus hatással van a legérzékenyebb mikroorganizmusokra.
Nagyon hatékony (baktericid) a meningococcusok, Haemophilus influenzae ellen (beleértve a más antibiotikumokkal szemben rezisztenseket is). Hatékony a penicillinázt nem termelő Shigella, Salmonella, Rickettsia, Brucella, Clostridia, Chlamydia, Mycoplasma, Streptococcus, Staphylococcus ellen. V. fragilis, Proteus.
A penicillinázt termelő Pseudomonas aeruginosa, Mycobacterium tuberculosis és staphylococcusok rezisztensek a kloramfenikollal szemben.
A kloramfenikolt szájon át írják fel (a gyógyszer szinte teljesen felszívódik a bélben); maximális hatás 2 óra elteltével; t 1/2 – 2 tk.
Súlyos esetekben a kloramfenikolt intravénásan adják be. A kloramfenikol áthatol a vér-agy gáton; a gyógyszer koncentrációja a cerebrospinális folyadékban a vérplazma koncentrációjának körülbelül 60%-a. A májban a kloramfenikol glükuronidáción megy keresztül a glükuronil-transzferáz hatására. A változatlan formában lévő kloramfenikol körülbelül 10%-a ürül a vizelettel.
A kloramfenikolt agyhártyagyulladásra használják, ha a penicillinek alkalmazása lehetetlen, a Haemophilus influenzae által okozott fertőzések esetén (ha a harmadik generációs cefalosporinok nem használhatók). A fluorokinolonok megjelenése előtt a kloramfenikol volt a választott gyógyszer a tífusz kezelésére. Jelenleg a kloramfenikol tartalék gyógyszer a tífusz és a paratífusz, a baciláris vérhas, a tífusz és más rickettsiosisok, a kolera, a pestis, a brucellózis, a tularémia és a chlamydia kezelésére.
Szemcseppek formájában kloramfenikol oldatot használnak kötőhártya-gyulladásra, blepharitisre (1 csepp naponta 4-6 alkalommal).
A kloramfenikol alkalmazását korlátozza a csontvelői vérképzésre gyakorolt gátló hatása (lehet leukopenia, agranulocitózis, aplasztikus anémia). Egyéb mellékhatások:
Szuperfertőzések (oropharyngealis candidiasis, staphylococcus enterocolitis);
Szájgyulladás, glossitis;
Optikai neuritis, encephalopathia.
Újszülötteknél a kloramfenikol ellenjavallt a kloramfenikol elégtelen glükuronidációs rendszere miatt ebben a korban; „szürke szindrómát” okozhat náluk - cianózis, szabálytalan légzés, érösszeomlás, hányás, hasmenés (laza zöld széklet), puffadás, hipotermia, hamuszürke bőrszín; halálozási arány - 40%.
A kloramfenikol gátolja a mikroszomális májenzimek szintézisét, ezért fokozhatja és meghosszabbíthatja az ezen enzimek által inaktivált gyógyszerek hatását. Így a kloramfenikol megnöveli a warfarin és a fenitoin felezési idejét.
A kloramfenikol azáltal, hogy megzavarja a bakteriális fehérjék szintézisét, lelassítja azok növekedését, ezért gyengítheti a penicillinek hatását, amelyek baktériumölő hatással vannak a szaporodó baktériumokra.
Makrolidok
A makrolidok makrociklusos vegyületek. A 14 tagú makrolidok közé tartozik az eritromicin és a klaritromicin, a 15 tagú makrolidok közé tartozik az azitromicin (azalidokként osztályozva), a 16 tagú makrolidok pedig a josamicin és a spiramicin.
A makrolidok a riboszómák 50S alegységére hatnak, és megzavarják a transzlokációt - ez a fehérjeszintézis végső szakasza a bakteriális riboszómákon (a képződött peptid mozgása az A helyről a P helyre a riboszóma mRNS mentén történő mozgása miatt - 83. ábra). Versenyezhet a linkozamidokkal a riboszómákhoz való kötődésért; ebben az esetben az antibiotikumok hatása kölcsönösen gyengül. Ezért a makrolidok linkozamidokkal kombinációban történő alkalmazása nem javasolt.
A makrolidok bakteriosztatikusan hatnak a legtöbb érzékeny mikroorganizmusra, és baktericid hatással vannak néhányra. Jól behatolnak a baktériumokkal fertőzött testsejtekbe. A makrolidok koncentrációja a sejtekben jelentősen meghaladja a vérplazmában lévő koncentrációjukat.
A makrolidok számos intracelluláris kórokozó (chlamydia, mycoplasma, ureaplasma, legionella) ellen hatékonyak. A coccusokra, a Haemophilus influenzae-ra, a diftéria- és lépfenebacilusokra, a borrelia-ra, a Treponema pallidumra, a H. pylori-ra hatnak.
A makrolidok nem hatolnak át a vér-agy gáton az ízületi folyadékba.
Az Escherichia coli, Shigella, Salmonella, Pseudomonas aeruginosa, Klebsiella, a pestis, a tularemia, a B. fragilis és a meticillinrezisztens staphylococcusok kórokozói ellenállnak a makrolidoknak.
A makrolidokat fül-orr-gégészeti fertőzések, chlamydia, mycoplasma, legionella okozta tüdőgyulladás, valamint húgyúti, bőr- és lágyszöveti fertőzések esetén alkalmazzák.
A Roxithromycint és a klaritromicint gyomor- és nyombélfekély esetén írják fel a H. pylori felszámolására.
Az azitromicin nagyon hatékony a húgycső chlamydia ellen.
Eritromicin(Erythromycin) baktériumölő hatású streptococcusok, pneumococcusok, bakteriosztatikus hatású staphylococcusok, gonococcusok, meningococcusok, Haemophilus influenzae, chlamydia, mycoplasma, legionella, treponema pallidum ellen. Az Escherichia coli, a Shigella, a Salmonella és a Pseudomonas aeruginosa rezisztens az eritromicinre.
A gyógyszer szájon át adva felszívódik, de a gyógyszer biohasznosulása alacsony (35%). A szövetekben oszlik el (kivéve a központi idegrendszert); behatol a prosztatába és a placentán keresztül. Más makrolidokhoz hasonlóan az eritromicin is jól behatol a szövetsejtekbe; a gyógyszer koncentrációja a sejtekben körülbelül 13-szor magasabb, mint a vérplazmában. A májban koncentrálódik, főként az epével ürül. Fél eliminációs időszak ( t 1/2) – 90 perc. A hatás időtartama - 6 óra.
Az eritromicin a választott gyógyszer az intracelluláris kórokozók (chlamydia, mycoplasma, legionella), pneumococcusok, streptococcusok, valamint a chlamydia, ureaplasma okozta húgyúti fertőzések (prosztatagyulladás, mellékhere, cervicitis, urethritis) okozta légúti fertőzések kezelésére. Az eritromicint tüdőgyulladás, fül-orr-gégészeti fertőzések, légionárius-betegség, trachoma, szamárköhögés, diftéria esetén alkalmazzák; tartalék gyógyszerként - skarlátra, brucellózisra, gonorrhoeára, szifiliszre.
Az eritromicint szájon át naponta 4 alkalommal írják fel. Szemkenőcsként használják kötőhártya- és blepharitis esetén (naponta kétszer a szemhéj mögé helyezve). Az eritromicin intramuszkuláris beadása lehetséges.
Az eritromicin mellékhatásai:
- epigasztrikus szorongás;
- hányinger, hányás, hasmenés;
- átmeneti halláskárosodás;
- kolesztatikus sárgaság;
- opportunista bélfertőzések.
Klaritromicin(Clarithromycin; Klacid) – 6-metoxi-eritromicin. Az eritromicinnel összehasonlítva hatékonyabb a Haemophilus influenzae ellen. Magasabb intracelluláris koncentrációt hoz létre, és hatékonyabb a chlamydia, a legionella, a moraxella, a mycoplasma, valamint a Lyme-kór kórokozója (Borrelia burgdorferi) ellen. Pneumococcusokra, streptococcusokra, gonococcusokra, Haemophilus influenzae, Moraxellára, H. pylorira hat. Jól behatol a makrofágokba és a neutrofilekbe. A vizelettel választódik ki (40%) metabolitok formájában.
Naponta kétszer szájon át vagy intravénásan írjon fel klaritromicint ( t 1/2 – 4-5 óra) a felső és alsó légúti fertőzések, valamint a bőr és a lágyrészek fertőzései esetén.
A klaritromicin mellékhatásai:
- hányinger;
– hasmenés;
– dózisfüggő süketség.
Roxitromicin(Roxithromycin; Rulid) szájon át naponta 1-2 alkalommal mandulagyulladás, pharyngitis, arcüreggyulladás, középfülgyulladás, szájfertőzések, hörghurut, tüdőgyulladás, chlamydia okozta húgyúti fertőzések, ureaplasma, bőrfertőzések (erysipela, kelések, pyoderma) kezelésére írják fel, valamint diftéria, szamárköhögés esetén. Az urogenitális chlamydia az esetek 100%-ában roxitromicinnel gyógyítható. A roxitromicin koncentrációja a neutrofilekben és a makrofágokban 34-szer, illetve 16-szor magasabb, mint a plazmában.
Azitromicin(Azithromycin; sumamed) – azalid (nitro- (azo-) csoport bevonása a makrolid ciklusba). Az eritromicinnel összehasonlítva kevésbé hatékony a staphylococcusok ellen, de szélesebb antimikrobiális hatásspektrummal rendelkezik. Hatékonyabb a Haemophilus influenzae és a Legionella ellen. Nagyon hatékony a toxoplazma ellen. Hatékony pneumococcusok, gonococcusok, Moraxella, chlamydia, mycoplasmák, ureaplasmák, Treponema pallidum, H. pylori, szamárköhögés kórokozói (Bordetella pertussis), gáz gangréna, Lyme-kór (Borrelia burgdoferi) ellen. Az azitromicin koncentrációja a fagocitákban 40-szer magasabb, mint a vérben. Az azitromicin aktív formában ürül az epével.
Az azitromicint szájon át naponta egyszer írják fel ( t 1/2 – 48 óra) felső légúti fertőzések és fül-orr-gégészeti fertőzések (mandulagyulladás, mandulagyulladás, arcüreggyulladás, középfülgyulladás), pneumococcusok által okozott alsó légúti fertőzések (bronchitis, tüdőgyulladás), Haemophilus influenzae, chlamydia, mycoplasma, skarlát, Lyme esetén betegség, chlamydia által okozott urethritis, mycoplasma, ureaplasma, cervicitis, gonorrhoea, bőr- és lágyrészfertőzések, a H. pylori felszámolására.
Az azitromicin mellékhatásai:
- hányinger;
– hasmenés;
– dózisfüggő süketség.
Az azitromicin terhesség, szoptatás, 12 év alatti gyermekek, valamint súlyos máj- és vesekárosodás esetén ellenjavallt.
Midecamycin(Midecamycin; macropen) szájon át alkalmazható intracelluláris kórokozók (chlamydia, moraxella, mycoplasma, ureaplasma, legionella) okozta légúti és húgyúti fertőzésekre, valamint streptococcus, staphylococcus fertőzésekre, diftéria, szamárköhögés kezelésére és megelőzésére. Campylobacter spp. által okozott gyomor-bélrendszeri fertőzésekre. A gyógyszer hatásos a H. pylori ellen.
spiramicin(Spiramicin; rovamicin) reverzibilisen kötődik az 50S riboszóma alegységhez, és megzavarja a fehérjeszintézist. Bakteriosztatikus hatása van. A spiramicint orálisan vagy intravénásan írják fel chlamydia, legionella, mycoplasma, krónikus hörghurut súlyosbodása, fül-orr-gégészeti betegségek (mandulagyulladás, sinusitis, otitis), urogenitális rendszer fertőzései (beleértve a chlamydia), fertőző ízületi gyulladás, osteomyelitis, bőrgyulladás esetén is. fertőzések és lágyszövetek. A josamicint (vilprafen) szájon át írják fel. Hatékony Chlamidia trachomatis, Chlamidia pneumoniae, Mycoplasma pneumoniae, Ureaplasma urealyticum, Legionella pneumophila, Treponema pallidum, valamint streptococcusok, pneumococcusok, staphylococcusok, gonococcusok, meningococcusok, diftéria diftéria, gangren cabacillus ellen. Különösen nagy koncentrációban a tüdőszövetben határozzák meg.
A Josamicint légúti és fül-orr-gégészeti fertőzések (pharyngitis, tonsillitis, gégegyulladás, arcüreggyulladás, középfülgyulladás), diftéria esetén (a diftéria toxoidos kezelés mellett), a húgyúti chlamydia, ureaplasma fertőzések, valamint a húgyúti fertőzések kezelésére használják. szifiliszre olyan esetekben, amikor a benzilpenicillin gyógyszerek alkalmazása lehetetlen.
Linkozamidok
A linkozamidok hatásmechanizmusa hasonló a makrolidokhoz. A kromoszómák 50S alegységére hatnak, és megzavarják a transzlokációs folyamatot. Elsősorban a gram-pozitív mikroorganizmusokra hatnak, főként bakteriosztatikusan. Hatékony aerob Gram-pozitív baktériumok ellen - staphylococcusok (beleértve a penicillinázt termelőket is), streptococcusok, pneumococcusok, valamint clostridiumok, mikoplazmák ellen. Hatékony az anaerob kórokozók (különösen a Bacteroides fragilis) ellen. A baktériumok lassan fejlesztenek rezisztenciát a linkozamidokkal szemben. A linkozamidok jól behatolnak a csontszövetbe. Ne hatoljon át a vér-agy gáton.
A meticillinrezisztens staphylococcusok, a legtöbb Gram-negatív baktérium, gomba, vírus és protozoa rezisztens a linkozamidokkal szemben.
Linkomicin(Lincomycin) hatásos a gram-pozitív coccusok, köztük a penicillináz-termelő staphylococcusok ellen. Rendkívül hatékony a baktériumok ellen. Inaktív meningococcusok és gonococcusok ellen. A linkomicin nincs hatással az Escherichia colira, a Shigellára, a Salmonellára, a Klebsiellára, a Legionellára, a Pseudomonas aeruginosa-ra és a Chlamydia-ra. A Trichomonas és Candida gombák rezisztensek a linkomicinnel szemben.
A gyomor-bél traktusban a linkomicin nem szívódik fel teljesen - 25-40%. Nagy koncentrációban rakódik le a csontszövetben. Az epével és a vizelettel választódik ki. A linkomicint orálisan, intramuszkulárisan, intravénásan és helyileg kenőcs formájában írják fel.
A linkomicin alkalmazására utaló jelek a szepszis, osteomyelitis, az állkapcsok fertőző betegségei, szeptikus endocarditis, tüdőgyulladás, tüdőtályog, erysipelas, otitis.
A linkomicin mellékhatásai:
- hányinger, hányás;
- glossitis, stomatitis;
– hasmenés;
- májműködési zavar;
- bőrkiütések;
- neutropenia, thrombocytopenia.
A linkomicin szájon át történő alkalmazása esetén intestinalis candidiasis és pszeudomembranosus colitis (Clostridium difficile által okozott), a normál bél mikroflóra elnyomásával társulva lehetséges (hasmenés esetén a gyógyszert abba kell hagyni). A metronidazolt és a vankomicint a pszeudomembranosus colitis kezelésére használják.
A súlyos mellékhatások miatt a linkomicint egyre inkább a kevésbé mérgező klindamicin váltja fel.
Klindamicin(klindamicin; dalacin C) – a linkomicin származéka; 2-10-szer aktívabb. Baktericid hatással van a gram-pozitív coccusokra, és bakteriosztatikus hatással van a bakteroidokra. Orális beadás esetén a gyógyszer 90%-a felszívódik. A klindamicin hatásideje 6 óra, a vesén és az epén keresztül ürül (10% változatlan formában). A linkomicinhez képest kevésbé irritálja a gyomor-bélrendszert, és kisebb valószínűséggel okoz pszeudomembranosus vastagbélgyulladást és egyéb mellékhatásokat.
A klindamicint naponta négyszer szájon át írják fel szeptikus endocarditis, az ENT szervek, a csontszövet, az ízületek, az állkapocs flegmonája, az érzékeny mikroorganizmusok által okozott hasi szervek fertőző betegségei miatt. Szeptikémia, tüdőgyulladás, tüdőtályog, peritonitis esetén a gyógyszert intramuszkulárisan vagy intravénásan adják be. Staphylococcus kötőhártya-gyulladás esetén a klindamicint szemcseppként írják fel. Gennyes-gyulladásos bőrbetegségek esetén külsőleg klindamicint tartalmazó gélt használnak; hüvelyi fertőzések esetén - hüvelykrém.
A szervek és szövetek fehérjéi folyamatos megújulásra szorulnak. A katabolizmus és az anabolizmus dinamikus egyensúlyának megzavarása kóros folyamatok kialakulásához vezethet.
A fehérjeszintézis a sejtek citoplazmájában megy végbe a riboszómákon. A fehérjeszintézis kezdeti szakasza az aminosavak aktiválása enzim és ATP hatására aminoacil-adenilátok képződésével. Az aktivált aminosav kölcsönhatásba lép a transzfer RNS-sel, és ez a komplex a riboszóma felé húzódik. A riboszómák viszont érintkezésbe kerülnek a hírvivő RNS-sel, és a hírvivő RNS lineáris szerkezete mentén haladva aminosavakat tartalmaznak egy bizonyos szekvenciában. A szintézis befejezése után a polipeptid lánc eltávolítódik a riboszómából a környezetbe, végül felveszi az erre a specifikus fehérjére jellemző térbeli konfigurációt. A fehérjeszintézis szabályozásában egy operátorgén és egy szabályozógén vesz részt. A szabályozó gén felelős a represszor szintéziséért, amely egy enzim, és gátolja a strukturális gének aktivitását. A represszor kölcsönhatásba lép az operátor génnel, amely szervesen kapcsolódik a szerkezeti génekhez. A represszor lehet aktív vagy inaktív állapotban. Az aktív represszor elnyomja az operátor gént, és a strukturális gének fehérjeszintézise leáll. A represszor aktivátora egy bizonyos koncentrációjú fehérje lehet a sejtben. Fehérjehiány esetén a represszor gátolt, és a strukturális gének fehérjeszintézise fokozódik. Az anabolikus hormonok és rákkeltő anyagok gátolják a represszort.
A fehérjeszintézis megzavarásának okai a sejtben:
1. oxigén csökkenése a légköri levegőben és a vérben;
2. az ATP termelés hiánya.
3. elégtelen fehérje- és esszenciális aminosav tartalom az élelmiszerekben (pl. triptofán hiányával - hipoproteinémia alakul ki, arginin - spermatogenezis csökken, metionin - zsíros beszűrődés alakul ki a májban, valin - izomgyengeség, növekedési visszamaradás, fogyás ill. keratózisok alakulnak ki);
4. az anabolikus hormonok hiánya.
5. a szerkezeti gének (mutációk) aktivitásának megzavarása (például ha a hemoglobin molekulában a glutaminsav helyett valin kerül be, sarlósejtes vérszegénység alakul ki);
6. a fehérje bioszintézis egyes szakaszainak megsértése: replikáció, transzkripció és transzláció.
7. ha represszor kötődik (például ha rákkeltő anyagok blokkolják, folyamatos fehérjeszintézis megy végbe);
8. ha a neuroendokrin szabályozás megbomlik (például idegek elvágása és anabolikus hormonok hiánya esetén csökken a fehérjetermelés és megváltozik a minősége).
A fehérjeanyagcserét szabályozó hormonokat a anabolikus és katabolikus. Az anabolikus hormonok közé tartoznak az agyalapi mirigy elülső részének szomatotrop és gonadotrop hormonjai, az ivarmirigyhormonok és az inzulin. A pajzsmirigyhormonok fiziológiás dózisokban egy növekvő szervezetben serkentik a fehérjeszintézist, a szövetek morfológiai és funkcionális differenciálódását. A normál adagok felnőtt szervezetben, elegendő és fokozott fehérje-táplálással, katabolikus hatást fejtenek ki, ami nem vezet a nitrogén egyensúly megzavarásához, és elősegíti a felesleges fehérje eltávolítását. A pajzsmirigyhormonok és glükokortikoidok túltermelése katabolikus hatású.
A szerzetteken kívül a fehérje bioszintézisének örökletes hibái is vannak (a véralvadási faktorok, a hemoglobin, a strukturális fehérjék károsodott képződése a szervezetben).
A fokozott fehérjelebontás okai:
1. katabolikus homonok túlzott bevitele, amelyek aktiválják a lizoszómákban lokalizált intracelluláris proteinázokat;
2. a lizoszómák permeabilitásának növelése bakteriális toxinok, szöveti bomlástermékek, acidózis, hipoxia és egyéb tényezők hatására, ami hozzájárul a katepsinek felszabadulásához és a katabolikus folyamatok fokozódásához.
A fehérjeszintézis zavarait okozó okok között fontos helyet foglalnak el a különféle táplálkozási hiányosságok (teljes, hiányos böjt, az esszenciális aminosavak hiánya az élelmiszerekben, a szervezetbe jutó esszenciális aminosavak meghatározott mennyiségi arányának megsértése).
Ha például a szöveti fehérje egyenlő arányban (1:1:1) tartalmaz triptofánt, lizint és valint, és ezek az aminosavak 1:1:0,5 arányban kerülnek táplálékfehérjével, akkor a szöveti fehérjeszintézis fele egyenletesen biztosítva lesz. Ha a sejtekben legalább egy (a 20-ból) esszenciális aminosav hiányzik, a fehérjeszintézis egésze leáll.
A fehérjeszintézis sebességének károsodását a megfelelő genetikai struktúrák működésének zavara okozhatja. A genetikai berendezés károsodása lehet örökletes vagy szerzett, különféle mutagén tényezők (ionizáló sugárzás, ultraibolya sugárzás stb.) hatására. Egyes antibiotikumok a fehérjeszintézis megzavarását okozzák. Így a genetikai kód leolvasásában „hibák” fordulhatnak elő sztreptomicin, neomicin és más antibiotikumok hatására. A tetraciklinek gátolják az új aminosavak hozzáadását a növekvő polipeptidlánchoz (erős kovalens kötések kialakulását a láncok között), megakadályozva a DNS-szálak szétválását.
A fehérjeszintézis megzavarásának egyik fontos oka ennek a folyamatnak a szabályozási zavara lehet. A fehérjeanyagcsere intenzitásának és irányának szabályozását az idegrendszer és az endokrin rendszer szabályozza, melynek hatásai különböző enzimrendszerek befolyásolásával valósulnak meg. Az állatok decebrációja csökkenti a
protein szintézis. A növekedési hormon, a nemi hormonok és az inzulin bizonyos körülmények között serkentik a fehérjeszintézist. Végül patológiájának oka a fehérjeszintézisben részt vevő sejtenzimrendszerek aktivitásának megváltozása lehet.
Ezen tényezők eredményeként csökken az egyes fehérjék szintézisének sebessége.
A fehérjeszintézis mennyiségi változásai az egyes fehérjefrakciók arányának megváltozásához vezethetnek a vérszérumban - dysproteinemia. A diszproteinémiának két formája van: hiperproteinémia (az összes vagy egyes fehérjetípusok megnövekedett tartalma) és hipoproteinémia (az összes vagy az egyes fehérjék csökkent tartalma). Így a máj (cirrhosis, hepatitis), a vesék (nephritis, nephrosis) egyes betegségeit az albuminszintézis csökkenése és a szérum tartalmának csökkenése kíséri. Számos fertőző betegség, amelyet kiterjedt gyulladásos folyamatok kísérnek, a szintézis növekedéséhez, majd a szérum gamma-globulin-tartalmának növekedéséhez vezet. A dysproteinémia kialakulása általában a homeosztázis eltolódásával jár együtt (romlott onkotikus nyomás, vízháztartás). A fehérjék, különösen az albuminok és a gamma-globulinok szintézisének jelentős csökkenése a szervezet fertőzésekkel szembeni ellenállásának éles csökkenéséhez vezet.
A máj és a vese károsodása esetén egyes akut és krónikus gyulladásos folyamatok (reuma, fertőző szívizomgyulladás, tüdőgyulladás), minőségi változások következnek be a fehérjeszintézisben, és speciális, megváltozott tulajdonságú fehérjéket szintetizálnak, például C-reaktív fehérjét. Példák a kóros fehérjék jelenléte által okozott betegségekre a patológiás hemoglobin jelenlétével kapcsolatos betegségek (hemoglobinózis), a véralvadási rendellenességek kóros fibrinogén megjelenésével. A szokatlan vérfehérjék közé tartoznak a krioglobulinok, amelyek 37 ° C alatti hőmérsékleten kicsapódhatnak (szisztémás betegségek, májcirrózis).
Preferanskaya Nina Germanovna
Docens, az Első Moszkvai Állami Orvostudományi Egyetem Gyógyszerészeti Kar Gyógyszerészeti Tanszékének docense. ŐKET. Sechenov
Az antibiotikumok főként bakteriosztatikus hatásúak, kivéve a baktericid hatású aminoglikozidokat és a nagy dózisban alkalmazott gyógyszereket. Ezek a gyógyszerek széles spektrumú antimikrobiális hatást fejtenek ki, és gyakran használják a klinikai gyakorlatban; különösen nélkülözhetetlenek olyan ritka fertőzések speciális kezelésében, mint a bartonellózis, brucellózis, kriptosporidiózis, cisztás fibrózis, toxoplazmózis, tularemia, tuberkulózis, lépfene, kolera, pestis stb.
I. rész. Makrolidok
A makrolidok az antibiotikumok egy osztálya, amelyek molekulájában makrociklusos laktongyűrűt tartalmaznak, amely aminocukrok szénhidrát-maradékaihoz kapcsolódik. A gyűrűt alkotó szénatomok számától függően 14-tagú, 15-tagú és 16-tagú makrolidokat különböztetünk meg. Az összes létező antibiotikum közül a makrolidok rendkívül hatékony és legbiztonságosabb kemoterápiás szereknek bizonyultak. A makrolidokat két csoportra osztják: természetes és félszintetikus .
A makrolidok antimikrobiális hatása a mikrobiális sejt riboszómáin a fehérjeszintézis megzavarásának köszönhető. A makrolidok reverzibilisen kötődnek az 50S riboszóma alegység katalitikus peptil-transzferáz centrumának különböző doménjeihez, és gátolják a peptidek transzlokációs és transzpeptidációs folyamatait, ami a fehérjemolekulák összeállításának leállásához vezet, és lelassítja a mikroorganizmusok osztódási és szaporodási képességét. A mikroorganizmus típusától és a gyógyszer koncentrációjától függően dózisfüggő hatást fejtenek ki, bakteriosztatikus hatást fejtenek ki, nagy dózisokban és egyes mikroorganizmus-törzseken pedig baktericid hatást fejtenek ki. Antimikrobiális hatásspektruma nagyon közel áll a természetes penicillinek csoportjához.
A makrolidok lipofil tulajdonságokkal rendelkeznek, gyorsan felszívódnak a gyomor-bél traktusban, magas szöveti és intracelluláris koncentrációt hoznak létre, számos szövetben és váladékban eloszlanak, rosszul megmaradnak az extracelluláris folyadékokban, és nem hatolnak be a BBB-be. Hatásuk főleg a szaporodási szakaszban nyilvánul meg. Kizárólag az aktívan osztódó mikroorganizmusok ellen hatásosak, ezért a betegség akut periódusának kezelésében is beváltak, és alig vagy egyáltalán nem hatnak a lassú folyamatokra.
Fokozott aktivitást mutatnak a Gram „+” coccusok és az intracelluláris kórokozók (chlamydia, mycoplasma, legionella) ellen, elnyomják a Gram-negatív coccusok, diftéria bacillusok, a brucellózis kórokozói, az amőb vérhas kialakulását. Az Enterobacteriaceae családba tartozó gramm „-” mikroorganizmusokon P. az aeruginosa és a gram „-” anaerobok rezisztensek. A Pseudomonas és az Acinetobacter természetesen rezisztens minden makroliddal szemben. A mikroorganizmusok ezzel a gyógyszercsoporttal szembeni rezisztenciája a riboszómák 50S alegységein lévő receptorok szerkezetének megváltozásával jár, ami az antibiotikum riboszómákhoz való kötődésének megzavarásához vezet. A makrolidokban, linkozamidokban és fenikolokban az 50S riboszomális alegységhez való kötődés különböző helyeken történik, ami keresztrezisztencia hiányát eredményezi. A makrolidok antimikrobiális hatásának sajátossága, hogy bakteriosztatikus hatást fejtenek ki a baktériumok azon formáival szemben, amelyek rezisztensek az olyan széles körben használt csoportokkal szemben, mint a penicillinek, sztreptomicinek és tetraciklinek.
A makrolidokat alsó légúti fertőzések kezelésére használják, beleértve az atipikus formákat, a krónikus bronchitis súlyosbodását és a közösségben szerzett tüdőgyulladást. Felső légúti fertőzésekre (sinusitis, otitis, pharyngitis, mandulagyulladás), szájüregi fertőzésekre, lágyszövetekre, bőrre, fertőzött pattanásokra és urogenitális fertőzésekre írják fel. Alkalmazásuk indikációi a mycobacteriosis megelőzése és kezelése, a reumás láz, az endocarditis megelőzése, a H. felszámolása céljából. pylori ( klaritromicin). A makrolidok immunmoduláló tulajdonságait panbronchonchiolitis esetén használják. klaritromicin, roxitromicin) és cisztás fibrózis ( azitromicin).
A makrolidok használatának fő mellékhatásai a gyomor-bélrendszeri rendellenességek, amelyek kockázata nem haladja meg az 5-8% -ot. Ritka esetekben 2-3%-ban allergiás reakciók alakulnak ki (bőrkiütés, arc-, nyak-, lábduzzanat, anafilaxiás sokk), ritkábban cholestaticus hepatitis és pszeudomembranosus colitis. A makrolidok legkisebb adagolási gyakorisága, a javult farmakokinetikai paraméterek nem igényelnek dózismódosítást veseelégtelenség esetén, és a betegek jól tolerálják. A legtöbb makrolid (különösen az eritromicin és a klaritromicin) erősen gátolja a citokróm P-450-et (CYP 3A 4, CYP3A5, CYP3A7, CYP 1A 2), ezért használatuk megzavarja a biotranszformációt és növeli az együtt adott gyógyszerek maximális koncentrációját a vérben. Ezt különösen fontos figyelembe venni a használat során Warfarin, ciklosporin, teofillin, digoxin, karbamazepin stb., amelyek a májban metabolizálódnak. Kombinált alkalmazásuk okozhatja a legveszélyesebb szövődményeket (szívritmuszavarok, Q-T intervallum megnyúlása, végtagi ischaemia és gangréna kialakulása). A spiramicin és az azitromicin nincs kitéve a citokróm P-450 általi oxidációnak. A szervezetben a makrolidok enterohepatikus recirkuláción mennek keresztül, főként az epével ürülnek ki, és a gyógyszernek csak 5-10%-a ürül a vesén keresztül.
Eritromicin (Erythromycinum) talajban élő aktinomicéták (sugárzó gombák) termelik, amelyek tenyészfolyadékából 1952-ben izolálták. Jól felszívódik a gyomor-bél traktusból. A gyomor savas környezetében részben elpusztul, ezért az eritromicint csak a bélben oldódó saválló bevonattal bevont tablettákban kell beadni. A gyógyszer könnyen behatol különböző szövetekbe, beleértve. átjut a placenta gáton. Normál körülmények között nem jut be az agyszövetbe. Egyszeri orális adag után a vérben a maximális koncentráció 2 óra elteltével érhető el. Az eritromicin biohasznosulása 2-3 óra, ezért a vér terápiás szintjének fenntartásához naponta négyszer kell beadni. Nagyobb dózisok szájon át: egyszeri - 0,5 g, naponta - 2 g. A széklettel és részben a vizelettel ürül ki. Az eritromicin tablettákat legszélesebb körben tüdőgyulladás, különböző etiológiájú hörghurut, skarlát, mandulagyulladás, gennyes középfülgyulladás, diftéria és sebfertőzések kezelésére használják. A gyógyszert súlyos fertőző betegségekre, szamárköhögés, diftéria kezelésére használják. Újszülöttek kötőhártya-gyulladása esetén intravénásan adják be, egyszeri adagot 250 ml izotóniás nátrium-klorid oldattal hígítanak, lassan, egy óra alatt beadva. Gastroparesisben az eritromicin dózisfüggően serkenti a gyomor motilitását, növeli a pylorus összehúzódások amplitúdóját és javítja az antrális-duodenális koordinációt. Helyileg kenőcs és oldat formájában külső használatra gennyes-gyulladásos bőrbetegségek, fertőzött sebek, trofikus fekélyek, felfekvés és II-III fokú égési sérülések kezelésére. A mikroorganizmusok eritromicinnel szembeni rezisztenciája gyorsan kialakul, a gyógyszer alacsony toxikus és ritkán okoz mellékhatásokat. Néha diszpeptikus rendellenességek (hányinger, hányás) és allergiás reakciók lépnek fel. A biohasznosulás jelentősen csökken, ha az eritromicint étkezés közben vagy után szedik, mert az élelmiszer több mint kétszeresére csökkenti ennek az antibiotikumnak a koncentrációját a vérben. Cső alakú, bevonatos kivitelben kapható. obol. 100 és 250 mg; szemkenőcs 10 g (1 g-ban 10 000 egység); kenőcs külső és helyi használatra 15 mg - 10 ezer egység/g. Kúpok gyermekeknek, 0,05 g és 0,1 g Por injekcióhoz, 0,05, 0,1 és 0,2 g, valamint granulátum szuszpenzióhoz, 0,125 g és 0,2 g 5 ml-es palackokban.