心臓の伝導系とその部分。 心のAV結び目。 伝導系の機能
自然条件下では、心筋細胞はリズミカルな活動 (興奮) 状態にあるため、その静止電位については条件付きでしか話すことができません。 ほとんどの細胞では、これは約 90 mV であり、ほぼ完全に K+ イオンの濃度勾配によって決まります。
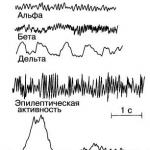
細胞内微小電極を使用して心臓のさまざまな部分で記録された活動電位 (AP) は、形状、振幅、持続時間が大きく異なります (図 7.3、A)。 図では、 図7.3、Bは、心室心筋の単一細胞のPDを概略的に示す。 この電位が発生するには、膜を 30 mV 脱分極する必要がありました。 AP では次のフェーズが区別されます。急速な初期脱分極 - フェーズ 1。 遅い再分極、いわゆるプラトー - フェーズ 2。 急速な再分極 - フェーズ 3; 休止期 - フェーズ4。
心房心筋層、心臓伝導性筋細胞(プルキンエ線維)、および心室心筋層の細胞におけるフェーズ 1 は、神経および骨格筋線維の活動電位の上昇フェーズと同じ性質を持っています。これは、ナトリウム透過性の増加によって引き起こされます。細胞膜の高速ナトリウムチャネルの活性化。 AP ピーク中に、膜電位の符号が変化します (-90 から +30 mV まで)。
膜の脱分極は、遅いナトリウム - カルシウム チャネルの活性化を引き起こします。 これらのチャネルを通って細胞内に Ca2+ イオンが流入すると、AP プラトー (フェーズ 2) が発生します。 プラトー期間中、ナトリウムチャネルは不活性化され、細胞は絶対的な不応状態に入ります。 同時にカリウムチャネルも活性化されます。 細胞から出る K+ イオンの流れは膜の急速な再分極をもたらし (フェーズ 3)、その間にカルシウム チャネルが閉じ、再分極プロセスが加速されます (膜を脱分極させる流入カルシウム流が減少するため)。
膜の再分極により、カリウムチャネルが徐々に閉鎖され、ナトリウムチャネルが再活性化されます。 その結果、心筋細胞の興奮性が回復します。これは、いわゆる相対不応期です。
作動している心筋の細胞(心房、心室)では、膜電位(連続する AP 間の間隔)はほぼ一定のレベルに維持されます。 しかし、心臓のペースメーカーとして機能する洞房結節の細胞では、自発的な拡張期脱分極 (フェーズ 4) が観察され、その臨界レベル (約 -50 mV) に達すると、新しい PD が現れます (図を参照)。 7.3、B)。 これらの心臓細胞の自律リズム活動は、このメカニズムに基づいています。 これらの細胞の生物活性には、他にも重要な特徴があります。1) AP 上昇の傾きが低い。 2) 遅い再分極 (フェーズ 2)、急速な再分極フェーズ (フェーズ 3) にスムーズに移行します。その間、膜電位は (作動中の心筋では -90 mV ではなく) -60 mV のレベルに達し、その後、遅い拡張期が続きます。脱分極段階が再び始まります。 房室結節の細胞の電気活動には同様の特徴がありますが、自発的拡張期脱分極の速度は洞房結節の細胞よりもはるかに低く、したがって潜在的な自動活動のリズムも小さくなります。
ペースメーカー細胞における電位発生のイオン機構は完全には解明されていません。 カルシウムチャネルが、洞房結節の細胞における緩徐拡張期脱分極およびAPの緩徐上昇相の発生において主導的な役割を果たすことが確立されている。 Ca2+イオンだけでなくNa+イオンも透過します。 高速ナトリウムチャネルは、これらの細胞におけるAPの生成には関与しません。
緩徐拡張期脱分極の進行速度は自律神経系によって調節されます。 交感神経部分の影響の場合、伝達物質であるノルアドレナリンが遅いカルシウムチャネルを活性化し、その結果、拡張期脱分極率が増加し、自発的活動のリズムが増加します。 副交感神経部分の影響の場合、ACh伝達物質は膜のカリウム透過性を増加させ、拡張期脱分極の進行を遅らせるか停止させ、さらに膜を過分極させます。 このため、リズムが遅くなったり、自動性が停止したりします。
心筋細胞が生涯を通じて継続的なリズミカルな活動状態にある能力は、これらの細胞のイオンポンプが効果的に動作することによって保証されます。 拡張期には、Na+ イオンが細胞から除去され、K+ イオンが細胞に戻ります。 細胞質に浸透した Ca2+ イオンは小胞体に吸収されます。 心筋への血液供給の悪化(虚血)は、心筋細胞内のATPおよびクレアチンリン酸の貯蔵量の枯渇につながります。 ポンプの動作が中断され、その結果、心筋細胞の電気的および機械的活動が低下します。
心臓伝導系の機能
リズミカルなインパルスの自発的な発生は、洞房結節の多くの細胞の協調した活動の結果であり、これらの細胞の密接な接触 (結合) と電気的相互作用によって確保されています。 洞房結節で生じた興奮は、伝導系を通って収縮性心筋に広がります。
心臓の伝導系の特徴は、各細胞が独立して興奮を生成できることです。 いわゆる自動性の勾配があり、洞房結節から離れるにつれて伝導系のさまざまな部分の自動性の能力が低下することで表され、毎分最大 60 ~ 80 回の周波数のインパルスが生成されます。
通常の状態では、洞房結節から来るより頻繁なインパルスによって、伝導系の下層部分すべての自動性が抑制されます。 このノードが損傷または故障した場合、房室ノードがペースメーカーになる可能性があります。 この場合、インパルスは 1 分あたり 40 ~ 50 回の頻度で発生します。 このノードもオフになると、房室束 (ヒスの束) の繊維がペースメーカーになる可能性があります。 この場合の心拍数は毎分30〜40を超えません。 これらのペースメーカーも故障すると、プルキンエ線維の細胞内で興奮プロセスが自発的に発生する可能性があります。 心拍数は非常にまれになります - 1 分あたり約 20。
心臓の伝導系の特徴は、その細胞内に多数の細胞間接触、つまり結合が存在することです。 これらの接触は、ある細胞から別の細胞への興奮の移行部位です。 伝導系の細胞と作動している心筋層の間にも同じ接触が存在します。 接触の存在のおかげで、個々の細胞からなる心筋は単一の全体として機能します。 多数の細胞間接触の存在により、心筋の興奮の信頼性が高まります。
洞房結節で生じた興奮は心房を通って広がり、房室結節に達します。 温血動物の心臓には、洞房結節と房室結節の間、および右心房と左心房の間に特別な経路があります。 これらの経路における興奮の伝播速度は、作動している心筋全体の興奮の伝播速度よりもそれほど速くはありません。 房室結節では、筋線維の厚みが薄く、筋線維の接続方法が特殊なため、興奮の伝導にある程度の遅れが生じます。 遅延により、心房筋が収縮して心房から心室に血液を送り出す時間ができた後でのみ、興奮が房室束と心臓伝導性筋細胞 (プルキンエ線維) に到達します。
その結果、房室遅延により、心房と心室の収縮に必要な順序 (調整) が行われます。
房室束およびびまん性に位置する心臓伝導性筋細胞における興奮伝播速度は 4.5 ~ 5 m/s に達し、これは作動中の心筋全体にわたる興奮伝播速度の 5 倍です。 このため、心室心筋の細胞はほぼ同時に、つまり同期的に収縮に関与します(図7.2を参照)。 細胞収縮の同時性により、心筋の力と心室のポンプ機能の効率が増加します。 興奮が房室束を介さずに、作動している心筋の細胞を介して、つまり散在的に行われる場合、非同期収縮の期間ははるかに長く続き、心筋細胞は同時に収縮するのではなく、徐々に収縮に関与することになります。心室の力は最大 50% 失われます。
したがって、伝導系の存在は、心臓の多くの重要な生理学的特徴を提供します。1) インパルス (活動電位) のリズミカルな生成。 2)心房と心室の収縮に必要な順序(調整)。 3)収縮の過程における心室心筋細胞の同期的関与(収縮の効率を高める)。
心臓の生理学
心臓の最も重要な機能は、 ポンプハウス。 つまり、静脈から動脈へ、体循環から肺循環へ血液を継続的に送り出す心臓の能力。 このポンプの目的は、酸素と栄養素を運ぶ血液をすべての器官や組織に届けて生命機能を確保し、有害な老廃物を回収して中和器官に届けることです。
心臓は一種の永久機関です。 心臓の生理学に関する今回および後続の号では、心臓が機能する複雑なメカニズムについて説明します。
心臓組織には 4 つの主な特性があります。
- 興奮性– 電気インパルスの形での励起によって刺激に反応する能力。
- 自動化– 自己励起する能力、つまり外部刺激がないときに電気インパルスを生成する能力。
- 導電率– 減衰することなく細胞から細胞へと励起を伝える能力。
- 収縮性– 筋線維がその張力を短縮または増加させる能力。
心臓の中間層である心筋層は、心筋細胞と呼ばれる細胞で構成されています。 心筋細胞は構造がすべて同じではなく、異なる機能を実行します。 次の種類の心筋細胞が区別されます。
- 収縮性(働いている、典型的な)心筋細胞心筋質量の 99% を占め、心臓の収縮機能を直接提供します。
- 伝導性(非定型、特殊)心筋細胞。 心臓の伝導系を形成します。 伝導性心筋細胞には、P 細胞とプルキンエ細胞の 2 種類の細胞があります。 P細胞(英語のペール-ペールに由来)は、電気インパルスを定期的に生成する能力を持ち、自動化機能を提供します。 プルキンエ細胞は心筋のあらゆる部分にインパルスを提供しますが、自動化する能力は弱いです。
- 移行期心筋細胞または T 細胞(英語のtransitional-transitionalから)伝導性心筋細胞と収縮性心筋細胞の間に位置し、それらの相互作用(つまり、伝導性細胞から収縮性心筋細胞へのインパルス伝達)を保証します。
- 分泌型心筋細胞主に心房に位置します。 彼らは、体内の水分と電解質のバランスと血圧を調節するホルモンであるナトリウム利尿ペプチドを心房の内腔に分泌します。
すべての種類の心筋細胞は分裂する能力を持っていません。つまり、再生する能力がありません。 人の心臓への仕事量が増加すると(運動選手など)、心筋細胞の総数(過形成)ではなく、個々の心筋細胞の体積が増加する(肥大)ため、筋肉量が増加します。
ここで、心臓の伝導系の構造を詳しく見てみましょう(図1)。 これには次の主要な構造が含まれます。
- 洞房性(ラテン語のsinus - 洞、atrium - アトリウムから)、または 副鼻腔 , ノード上大静脈の入口近くの右心房の後壁に位置します。 これは、P 細胞によって形成され、P 細胞は T 細胞を介して互いに接続され、心房の収縮性心筋細胞にも接続されます。 3 つの節間束が洞房結節から房室結節に向かって伸びています:前部 (バッハマン束)、中央 (ヴェンケバッハ束)、後部 (トーレル束)。
- 房室(ラテン語の atrium - アトリウム、ventriculum - ventricle から) ノード– 心房心筋細胞からヒス束への移行ゾーンに位置します。 P 細胞が含まれていますが、洞結節、プルキンエ細胞、T 細胞よりも少量です。
- 房室束、または房室束(ドイツの解剖学者 W. ギースが 1893 年に説明した)は、通常、心房から心室に興奮を伝える唯一の方法です。 それは、共通幹を通って房室結節から出発し、心室中隔を貫通する。 ここで、彼の束は右と左の2つの脚に分割され、対応する心室に進みます。 左脚は前上枝と後下枝の2つの枝に分かれています。 彼の束の枝は小さなネットワークの心室で終わります プルキンエ線維(1845年にチェコの生理学者J.プルキンエによって記載)。
1. 洞結節。 2. 房室結節。 3. 枝を束ねます。 4. プルキンエ線維。
一部の人々は、心臓の調律障害(例、心室前興奮症候群)に関与する追加の(異常な)経路(ジェームスの束、ケントの束)を持っています。
通常、興奮は洞結節で発生し、心房心筋に伝わり、房室結節を通過した後、束枝およびプルキンエ線維に沿って心室心筋に広がります。
したがって、心臓の正常なリズムは、洞房結節と呼ばれる活動によって決まります。 一次ペースメーカー、または真のペースメーカー(英語のペースメーカー - 「鼓動ステップ」から)。 自動性は心臓の伝導系の他の構造にも固有のものです。 二次ドライバー房室結節に局在しています。 第 3 層ドライバープルキンエ細胞は心室伝導系の一部です。
つづく。
心臓の伝導系。 洞結節
写真は示す 心臓伝導系の図。 これは以下で構成されます: (1) 洞結節 (洞房結節または SA 結節とも呼ばれます)。インパルスのリズミカルな生成が発生します。 (2)インパルスが洞結節から房室結節まで伝わる心房結節間束。 (3) 房室結節。心房から心室へのインパルスの伝導が遅れます。 (4) 房室束。インパルスが心室に伝達されます。 (5) プルキンエ線維からなる A-B 束の左右の脚。これにより、インパルスが収縮性心筋に到達します。
洞(洞房)結節は、幅 3 mm、長さ 15 mm、厚さ 1 mm の小さな楕円体プレートで、異型の心母細胞から構成されます。 SA 結節は、上大静脈の接合部の右心房の後外側壁の上部に位置します。 C-A 結節を構成する細胞には、実質的に収縮性フィラメントが含まれていません。 その直径はわずか 3 ~ 5 μm です (直径が 10 ~ 15 μm である心房収縮線維とは対照的に)。 洞結節の細胞は収縮筋線維に直接接続されているため、洞結節で発生した活動電位はすぐに心房心筋に広がります。
自動- これは、心臓のリズミカルな収縮を独立して興奮させ、引き起こすいくつかの心線維の能力です。 洞結節の細胞を含む心臓の伝導系の細胞は自動化する能力を持っています。 後で説明するように、心臓のリズムを制御するのは S-A 結節です。 次に、自動化メカニズムについて説明します。
洞結節の自動メカニズム。 この図は、3 つの心周期にわたって記録された洞結節細胞の活動電位と、比較のために心室心筋細胞の単一活動電位を示しています。 洞結節細胞の静止電位は、典型的な心筋細胞 (-85 ~ -90 mV) とは対照的に、小さい値 (-55 ~ -60 mV) を持つことに注意してください。 この違いは、節の細胞膜がナトリウムおよびカルシウムイオンに対してより透過性であるという事実によって説明されます。 これらの陽イオンが細胞に入ると、細胞内の負電荷の一部が中和され、静止電位の値が低下します。
行く前に 自動機構に。 心筋細胞の膜には、活動電位の生成に重要な役割を果たす 3 種類のイオン チャネルがあることを覚えておく必要があります: (1) 高速ナトリウム チャネル、(2) 低速 Na+/Ca2+ チャネル、(3) カリウム チャネル。 心室心筋細胞では、高速ナトリウムチャネルが短期間(1万分の数秒)開き、ナトリウムイオンが細胞内に侵入すると、心筋細胞膜の急速な脱分極と再充電が起こります。 0.3 秒続く活動電位のプラトー段階は、遅い Na+/Ca チャネルの開口によって形成されます。 その後、カリウムチャネルが開き、細胞からのカリウムイオンの拡散が起こり、膜電位は元のレベルに戻ります。
洞結節の細胞内静止電位は収縮性心筋細胞よりも低くなります(-90 mV ではなく -55 mV)。 このような条件下では、イオン チャネルの機能が異なります。 高速ナトリウムチャネルは不活性化され、インパルス生成に関与できません。 実際のところ、膜電位が数ミリ秒を超えて -55 mV まで低下すると、高速ナトリウム チャネルの内側にある不活化ゲートが閉じることになります。 これらのチャネルのほとんどは完全にブロックされています。 このような条件下では、遅い Na+/Ca チャネルのみが開くことができるため、活動電位が発生する原因となるのはこれらのチャネルの活性化です。 さらに、遅い Na/Ca チャネルの活性化は、心室の収縮性心筋の線維とは対照的に、洞結節の細胞における脱分極および再分極プロセスの比較的遅い進行を引き起こします。
自然条件下では、心筋細胞はリズミカルな活動 (興奮) 状態にあるため、その静止電位については条件付きでしか話すことができません。 ほとんどの細胞では、これは約 90 mV であり、ほぼ完全に K+ イオンの濃度勾配によって決まります。
細胞内微小電極を使用して心臓のさまざまな部分で記録された活動電位 (AP) は、形状、振幅、持続時間が大きく異なります (図 7.3、A)。 図では、 図7.3、Bは、心室心筋の単一細胞のPDを概略的に示す。 この電位が発生するには、膜を 30 mV 脱分極する必要がありました。 AP では次のフェーズが区別されます。急速な初期脱分極 - フェーズ 1。 遅い再分極、いわゆるプラトー - フェーズ 2。 急速な再分極 - フェーズ 3; 休止期 - フェーズ4。
心房心筋層、心臓伝導性筋細胞(プルキンエ線維)、および心室心筋層の細胞におけるフェーズ 1 は、神経および骨格筋線維の活動電位の上昇フェーズと同じ性質を持っています。これは、ナトリウム透過性の増加によって引き起こされます。細胞膜の高速ナトリウムチャネルの活性化。 AP ピーク中に、膜電位の符号が変化します (-90 から +30 mV まで)。
膜の脱分極は、遅いナトリウム - カルシウム チャネルの活性化を引き起こします。 これらのチャネルを通って細胞内に Ca2+ イオンが流入すると、AP プラトー (フェーズ 2) が発生します。 プラトー期間中、ナトリウムチャネルは不活性化され、細胞は絶対的な不応状態に入ります。 同時にカリウムチャネルも活性化されます。 細胞から出る K+ イオンの流れは膜の急速な再分極をもたらし (フェーズ 3)、その間にカルシウム チャネルが閉じ、再分極プロセスが加速されます (膜を脱分極させる流入カルシウム流が減少するため)。
膜の再分極により、カリウムチャネルが徐々に閉鎖され、ナトリウムチャネルが再活性化されます。 その結果、心筋細胞の興奮性が回復します。これは、いわゆる相対不応期です。
作動している心筋の細胞(心房、心室)では、膜電位(連続する AP 間の間隔)はほぼ一定のレベルに維持されます。 しかし、心臓のペースメーカーとして機能する洞房結節の細胞では、自発的な拡張期脱分極 (フェーズ 4) が観察され、その臨界レベル (約 -50 mV) に達すると、新しい PD が現れます (図を参照)。 7.3、B)。 これらの心臓細胞の自律リズム活動は、このメカニズムに基づいています。 これらの細胞の生物活性には、他にも重要な特徴があります。1) AP 上昇の傾きが低い。 2) 遅い再分極 (フェーズ 2)、急速な再分極フェーズ (フェーズ 3) にスムーズに移行します。その間、膜電位は (作動中の心筋では -90 mV ではなく) -60 mV のレベルに達し、その後、遅い拡張期が続きます。脱分極段階が再び始まります。 房室結節の細胞の電気活動には同様の特徴がありますが、自発的拡張期脱分極の速度は洞房結節の細胞よりもはるかに低く、したがって潜在的な自動活動のリズムも小さくなります。
ペースメーカー細胞における電位発生のイオン機構は完全には解明されていません。 カルシウムチャネルが、洞房結節の細胞における緩徐拡張期脱分極およびAPの緩徐上昇相の発生において主導的な役割を果たすことが確立されている。 Ca2+イオンだけでなくNa+イオンも透過します。 高速ナトリウムチャネルは、これらの細胞におけるAPの生成には関与しません。
緩徐拡張期脱分極の進行速度は自律神経系によって調節されます。 交感神経部分の影響の場合、伝達物質であるノルアドレナリンが遅いカルシウムチャネルを活性化し、その結果、拡張期脱分極率が増加し、自発的活動のリズムが増加します。 副交感神経部分の影響の場合、ACh伝達物質は膜のカリウム透過性を増加させ、拡張期脱分極の進行を遅らせるか停止させ、さらに膜を過分極させます。 このため、リズムが遅くなったり、自動性が停止したりします。
心筋細胞が生涯を通じて継続的なリズミカルな活動状態にある能力は、これらの細胞のイオンポンプが効果的に動作することによって保証されます。 拡張期には、Na+ イオンが細胞から除去され、K+ イオンが細胞に戻ります。 細胞質に浸透した Ca2+ イオンは小胞体に吸収されます。 心筋への血液供給の悪化(虚血)は、心筋細胞内のATPおよびクレアチンリン酸の貯蔵量の枯渇につながります。 ポンプの動作が中断され、その結果、心筋細胞の電気的および機械的活動が低下します。
心臓伝導系の機能
リズミカルなインパルスの自発的な発生は、洞房結節の多くの細胞の協調した活動の結果であり、これらの細胞の密接な接触 (結合) と電気的相互作用によって確保されています。 洞房結節で生じた興奮は、伝導系を通って収縮性心筋に広がります。
心臓の伝導系の特徴は、各細胞が独立して興奮を生成できることです。 いわゆる自動性の勾配があり、洞房結節から離れるにつれて伝導系のさまざまな部分の自動性の能力が低下することで表され、毎分最大 60 ~ 80 回の周波数のインパルスが生成されます。
通常の状態では、洞房結節から来るより頻繁なインパルスによって、伝導系の下層部分すべての自動性が抑制されます。 このノードが損傷または故障した場合、房室ノードがペースメーカーになる可能性があります。 この場合、インパルスは 1 分あたり 40 ~ 50 回の頻度で発生します。 このノードもオフになると、房室束 (ヒスの束) の繊維がペースメーカーになる可能性があります。 この場合の心拍数は毎分30〜40を超えません。 これらのペースメーカーも故障すると、プルキンエ線維の細胞内で興奮プロセスが自発的に発生する可能性があります。 心拍数は非常にまれになります - 1 分あたり約 20。
心臓の伝導系の特徴は、その細胞内に多数の細胞間接触、つまり結合が存在することです。 これらの接触は、ある細胞から別の細胞への興奮の移行部位です。 伝導系の細胞と作動している心筋層の間にも同じ接触が存在します。 接触の存在のおかげで、個々の細胞からなる心筋は単一の全体として機能します。 多数の細胞間接触の存在により、心筋の興奮の信頼性が高まります。
洞房結節で生じた興奮は心房を通って広がり、房室結節に達します。 温血動物の心臓には、洞房結節と房室結節の間、および右心房と左心房の間に特別な経路があります。 これらの経路における興奮の伝播速度は、作動している心筋全体の興奮の伝播速度よりもそれほど速くはありません。 房室結節では、筋線維の厚みが薄く、筋線維の接続方法が特殊なため、興奮の伝導にある程度の遅れが生じます。 遅延により、心房筋が収縮して心房から心室に血液を送り出す時間ができた後でのみ、興奮が房室束と心臓伝導性筋細胞 (プルキンエ線維) に到達します。
その結果、房室遅延により、心房と心室の収縮に必要な順序 (調整) が行われます。
房室束およびびまん性に位置する心臓伝導性筋細胞における興奮伝播速度は 4.5 ~ 5 m/s に達し、これは作動中の心筋全体にわたる興奮伝播速度の 5 倍です。 このため、心室心筋の細胞はほぼ同時に、つまり同期的に収縮に関与します(図7.2を参照)。 細胞収縮の同時性により、心筋の力と心室のポンプ機能の効率が増加します。 興奮が房室束を介さずに、作動している心筋の細胞を介して、つまり散在的に行われる場合、非同期収縮の期間ははるかに長く続き、心筋細胞は同時に収縮するのではなく、徐々に収縮に関与することになります。心室の力は最大 50% 失われます。
したがって、伝導系の存在は、心臓の多くの重要な生理学的特徴を提供します。1) インパルス (活動電位) のリズミカルな生成。 2)心房と心室の収縮に必要な順序(調整)。 3)収縮の過程における心室心筋細胞の同期的関与(収縮の効率を高める)。
心臓の生理学
心臓の最も重要な機能は、 ポンプハウス。 つまり、静脈から動脈へ、体循環から肺循環へ血液を継続的に送り出す心臓の能力。 このポンプの目的は、酸素と栄養素を運ぶ血液をすべての器官や組織に届けて生命機能を確保し、有害な老廃物を回収して中和器官に届けることです。
心臓は一種の永久機関です。 心臓の生理学に関する今回および後続の号では、心臓が機能する複雑なメカニズムについて説明します。
心臓組織には 4 つの主な特性があります。
- 興奮性– 電気インパルスの形での励起によって刺激に反応する能力。
- 自動化– 自己励起する能力、つまり外部刺激がないときに電気インパルスを生成する能力。
- 導電率– 減衰することなく細胞から細胞へと励起を伝える能力。
- 収縮性– 筋線維がその張力を短縮または増加させる能力。
心臓の中間層である心筋層は、心筋細胞と呼ばれる細胞で構成されています。 心筋細胞は構造がすべて同じではなく、異なる機能を実行します。 次の種類の心筋細胞が区別されます。
- 収縮性(働いている、典型的な)心筋細胞心筋質量の 99% を占め、心臓の収縮機能を直接提供します。
- 伝導性(非定型、特殊)心筋細胞。 心臓の伝導系を形成します。 伝導性心筋細胞には、P 細胞とプルキンエ細胞の 2 種類の細胞があります。 P細胞(英語のペール-ペールに由来)は、電気インパルスを定期的に生成する能力を持ち、自動化機能を提供します。 プルキンエ細胞は心筋のあらゆる部分にインパルスを提供しますが、自動化する能力は弱いです。
- 移行期心筋細胞または T 細胞(英語のtransitional-transitionalから)伝導性心筋細胞と収縮性心筋細胞の間に位置し、それらの相互作用(つまり、伝導性細胞から収縮性心筋細胞へのインパルス伝達)を保証します。
- 分泌型心筋細胞主に心房に位置します。 彼らは、体内の水分と電解質のバランスと血圧を調節するホルモンであるナトリウム利尿ペプチドを心房の内腔に分泌します。
すべての種類の心筋細胞は分裂する能力を持っていません。つまり、再生する能力がありません。 人の心臓への仕事量が増加すると(運動選手など)、心筋細胞の総数(過形成)ではなく、個々の心筋細胞の体積が増加する(肥大)ため、筋肉量が増加します。
ここで、心臓の伝導系の構造を詳しく見てみましょう(図1)。 これには次の主要な構造が含まれます。
- 洞房性(ラテン語のsinus - 洞、atrium - アトリウムから)、または 副鼻腔 , ノード上大静脈の入口近くの右心房の後壁に位置します。 これは、P 細胞によって形成され、P 細胞は T 細胞を介して互いに接続され、心房の収縮性心筋細胞にも接続されます。 3 つの節間束が洞房結節から房室結節に向かって伸びています:前部 (バッハマン束)、中央 (ヴェンケバッハ束)、後部 (トーレル束)。
- 房室(ラテン語の atrium - アトリウム、ventriculum - ventricle から) ノード– 心房心筋細胞からヒス束への移行ゾーンに位置します。 P 細胞が含まれていますが、洞結節、プルキンエ細胞、T 細胞よりも少量です。
- 房室束、または房室束(ドイツの解剖学者 W. ギースが 1893 年に説明した)は、通常、心房から心室に興奮を伝える唯一の方法です。 それは、共通幹を通って房室結節から出発し、心室中隔を貫通する。 ここで、彼の束は右と左の2つの脚に分割され、対応する心室に進みます。 左脚は前上枝と後下枝の2つの枝に分かれています。 彼の束の枝は小さなネットワークの心室で終わります プルキンエ線維(1845年にチェコの生理学者J.プルキンエによって記載)。
1. 洞結節。 2. 房室結節。 3. 枝を束ねます。 4. プルキンエ線維。
一部の人々は、心臓の調律障害(例、心室前興奮症候群)に関与する追加の(異常な)経路(ジェームスの束、ケントの束)を持っています。
通常、興奮は洞結節で発生し、心房心筋に伝わり、房室結節を通過した後、束枝およびプルキンエ線維に沿って心室心筋に広がります。
したがって、心臓の正常なリズムは、洞房結節と呼ばれる活動によって決まります。 一次ペースメーカー、または真のペースメーカー(英語のペースメーカー - 「鼓動ステップ」から)。 自動性は心臓の伝導系の他の構造にも固有のものです。 二次ドライバー房室結節に局在しています。 第 3 層ドライバープルキンエ細胞は心室伝導系の一部です。
つづく。
心臓の伝導系。 洞結節
写真は示す 心臓伝導系の図。 これは以下で構成されます: (1) 洞結節 (洞房結節または SA 結節とも呼ばれます)。インパルスのリズミカルな生成が発生します。 (2)インパルスが洞結節から房室結節まで伝わる心房結節間束。 (3) 房室結節。心房から心室へのインパルスの伝導が遅れます。 (4) 房室束。インパルスが心室に伝達されます。 (5) プルキンエ線維からなる A-B 束の左右の脚。これにより、インパルスが収縮性心筋に到達します。
洞(洞房)結節は、幅 3 mm、長さ 15 mm、厚さ 1 mm の小さな楕円体プレートで、異型の心母細胞から構成されます。 SA 結節は、上大静脈の接合部の右心房の後外側壁の上部に位置します。 C-A 結節を構成する細胞には、実質的に収縮性フィラメントが含まれていません。 その直径はわずか 3 ~ 5 μm です (直径が 10 ~ 15 μm である心房収縮線維とは対照的に)。 洞結節の細胞は収縮筋線維に直接接続されているため、洞結節で発生した活動電位はすぐに心房心筋に広がります。
自動- これは、心臓のリズミカルな収縮を独立して興奮させ、引き起こすいくつかの心線維の能力です。 洞結節の細胞を含む心臓の伝導系の細胞は自動化する能力を持っています。 後で説明するように、心臓のリズムを制御するのは S-A 結節です。 次に、自動化メカニズムについて説明します。
洞結節の自動メカニズム。 この図は、3 つの心周期にわたって記録された洞結節細胞の活動電位と、比較のために心室心筋細胞の単一活動電位を示しています。 洞結節細胞の静止電位は、典型的な心筋細胞 (-85 ~ -90 mV) とは対照的に、小さい値 (-55 ~ -60 mV) を持つことに注意してください。 この違いは、節の細胞膜がナトリウムおよびカルシウムイオンに対してより透過性であるという事実によって説明されます。 これらの陽イオンが細胞に入ると、細胞内の負電荷の一部が中和され、静止電位の値が低下します。
行く前に 自動機構に。 心筋細胞の膜には、活動電位の生成に重要な役割を果たす 3 種類のイオン チャネルがあることを覚えておく必要があります: (1) 高速ナトリウム チャネル、(2) 低速 Na+/Ca2+ チャネル、(3) カリウム チャネル。 心室心筋細胞では、高速ナトリウムチャネルが短期間(1万分の数秒)開き、ナトリウムイオンが細胞内に侵入すると、心筋細胞膜の急速な脱分極と再充電が起こります。 0.3 秒続く活動電位のプラトー段階は、遅い Na+/Ca チャネルの開口によって形成されます。 その後、カリウムチャネルが開き、細胞からのカリウムイオンの拡散が起こり、膜電位は元のレベルに戻ります。
洞結節の細胞内静止電位は収縮性心筋細胞よりも低くなります(-90 mV ではなく -55 mV)。 このような条件下では、イオン チャネルの機能が異なります。 高速ナトリウムチャネルは不活性化され、インパルス生成に関与できません。 実際のところ、膜電位が数ミリ秒を超えて -55 mV まで低下すると、高速ナトリウム チャネルの内側にある不活化ゲートが閉じることになります。 これらのチャネルのほとんどは完全にブロックされています。 このような条件下では、遅い Na+/Ca チャネルのみが開くことができるため、活動電位が発生する原因となるのはこれらのチャネルの活性化です。 さらに、遅い Na/Ca チャネルの活性化は、心室の収縮性心筋の線維とは対照的に、洞結節の細胞における脱分極および再分極プロセスの比較的遅い進行を引き起こします。
心臓の解剖学的構造(節、束、線維)の複合体であり、以下のものからなる。 異型筋線維正常な心臓活動を確保することを目的として、心臓のさまざまな部分(心房と心室)の協調的な働きを確保します。
心房と心室の収縮を調整することにより、PSS は心臓のリズミカルな機能、つまり正常な心臓活動を保証します。 特に、PSS は心臓の自動性を保証します。
ああ 洞房結節(Kies-Fleck 結節) は右心房の壁にあります。 彼は主役であり、リーダーです。 リズムを設定し、衝動を生み出します。
ああ 房室結節(房室; Aschoff-Tavara)は、心室に近い心房中隔に位置します。
- 彼のバンドル(房室束) は房室結節から出発し、心室中隔に続き、そこで心室に向かう 2 本の脚 (右と左) に分かれます。
これらの茎はプルキンエ線維と呼ばれ、心室の壁にあります。
1 – 洞房結節 2 – 房室結節
3 – 彼の束 4 – プルキンエ線維
v それがどのように起こるのか 心臓の伝導系?
興奮のインパルスが洞結節で発生します。 洞結節から心房心筋に到達します。
Ø 興奮は心房を介して接続する 3 つの経路に沿って広がります。 房室結節(AVN)を伴う洞結節(SU)):
・フロントパス( バックマン管) - 右心房の前上壁に沿って走り、心房中隔で2つの枝に分かれます - 1つはAVUに近づき、もう1つは左心房に近づき、その結果、インパルスは左心房に到着します0.2秒の遅延。
・中パス( ヴェンケバッハ地区) - 心房中隔に沿ってAVUまで進みます。
後部パス ( トレル管) - 心房中隔の下部に沿ってAVUに進み、そこから線維が右心房の壁に分岐します。
インパルスから伝わる興奮は、1 m/s の速度で心房心筋全体を即座にカバーします。
心房を通過したインパルスはAVUに到達し、そこから導電性繊維があらゆる方向に広がり、結節の下部がヒス束に入ります。
AVU はフィルターとして機能し、インパルスの通過を遅らせ、心室の興奮が始まる前に心房の興奮と収縮が終了する機会を生み出します。
さらに、励起はヒス束の枝や枝に3〜4 m / sの速度で広がります。 ヒスの束の枝、その枝、およびヒスの束の末端部分には、毎分 15 ~ 40 パルスの自動機能があります。
束の枝の枝はプルキンエ線維に入り、それに沿って興奮が4〜5 m / sの速度で心臓の心室の心筋に広がります。 プルキンエ線維には自動化機能もあります - 毎分15〜30のインパルス。
心室心筋では、興奮波はまず心室中隔を覆い、その後心臓の両心室に広がります。
心室では、興奮のプロセスは心内膜から心外膜に進みます。 この場合、心筋の興奮中に EMF が生成され、これが人体の表面に広がり、心電計によって記録される信号になります。
心臓の伝導系は、正常な心臓機能に必要な心房と心室間の正しい相互作用を担っています。 心臓の操作に失敗すると不整脈を引き起こし、生命を脅かす病気の発症を引き起こす可能性があります。統計によると、心臓病の約 15% は心拍リズム障害に関連しています。
人間の心臓は非常に複雑な構造を持つ筋肉の器官です。 その主な役割には、動脈と静脈を通る血液の継続的な移動を確保すること、心筋が弛緩したときに血液が静脈から右心房に送られた後に二酸化炭素を除去することが含まれます。
右心房から、液体組織は右心室に移動し、そこから肺幹に移動し、その枝のいずれかに沿って左または右の肺に向かいます。 毛細血管を通って肺胞に到達すると、血液から二酸化炭素が除去され、酸素で飽和されます。その後、液体組織は肺静脈を通って左心房に入り、左心室、さらに大動脈に入り、全身に分散します。
心臓の部屋 (心室と心房の両方をそう呼ぶ) が互いにどの程度スムーズに相互作用するかは、心臓伝導系 (CCS) の機能に大きく依存します。 それは、興奮信号が伝達される独特のノードである特別な細胞で構成される複雑な形成の形で提示され、収縮のリズムと頻度を維持することができます。 心臓伝導系は構造生理学において心臓の筋肉組織や神経系とは異なりますが、それらと密接に関連していることは注目に値します。
PSSデバイス
心臓の伝導系はいくつかのノードで構成されています。 その起源は洞房結節 (SA) であり、長さは 10 ~ 20、幅は 3 ~ 5 ミリメートルの繊維の形をした束です。 それは右心房の上部、2つの静脈の合流点近くに位置します。 洞形成の構造の生理学は 2 種類の細胞を提供します。P 細胞は興奮性シグナルを伝達し、T 細胞は興奮波の心房への伝導を確保します。
縫合糸システムにある導電性の糸は、生理学的には心臓の筋細胞に似ていますが、より薄く、波形で、少し軽いです。 洞結節は、心拍数の加速または減速を決定する神経線維に密に囲まれています。

次に、長さ 5 ミリメートル、厚さ 2 ミリメートルの線維である房室結節 (房室、略称 AV) が来ます。 それは、右心房の底部、冠状静脈洞の口近く、心房中隔の右側に位置します。 構造の生理機能も T 型細胞と P 型細胞で構成されます。
次のフォーメーションは、前のフォーメーションと同じくらい複雑な構造の形をしたヒスの束です。 いくつかの部分で構成されています。 形成の開始は心筋には接触せず、心動脈の損傷にはほとんど影響を受けませんが、コラーゲンの弾性糸で構成される周囲の線維組織で発生する病理学的プロセスにすぐに引き込まれます。 その後、彼の繊維は右と左の下腿に分かれ、その後、左の下腿が再び分かれます。
したがって、図では彼の足は次のように表されます。
- 左脚の糸は心室中隔の両側を通っていきます。 図によれば、その前枝から導電性の糸が左心室の左部および側部に伸びています。 後脚から、導電性の糸が左心室の後壁に向かって側壁の底部まで伸びています。
- 右脚の糸が右心室の筋肉まで伸びています。
PSS の構造の生理学は、心室内で徐々に枝分かれしてプルキンエ フィラメントと接続する枝も提供します。 その後、心室心筋に到達し、筋肉を突き刺します。
信号の動き
心筋は、PSS に沿った興奮性インパルスの伝播によって収縮します。興奮性インパルスは縫合系で形成され、伝導系を通って移動します。そのすべての節は自動性を特徴としています。 リズムは洞形成によって設定され、洞形成は通常 1 分間に 60 ~ 90 拍を生成します。 そこに送信された信号は他のノードに広がり、他の編成の同様のインパルスを抑制します。
発生した興奮信号は即座に心房心筋に到達します。 次に、信号は SU と房室を接続する 3 つの経路に沿って伝播します。
- 前方信号経路は右心房の前上壁に沿ってあり、心房中隔で 2 つの導電性分岐に分岐します。1 つは AVU に、もう 1 つは左心房に向かいます。
- インパルスの中間経路は心房中隔に沿ってAVUまで延びます。
- 後部信号経路は心房中隔の底部にある AVU にあり、そこから導電性フィラメントが右心房の壁まで伸びています。
房室形成に到達した後、興奮信号の経路は分岐します。伝導フィラメントはさまざまな方向に広がり、インパルスは下部伝導線維に沿ってヒス束に到達します。 AVU は興奮波の進行をわずかに遅くするため、心室が信号に応答する前に興奮サージと心房収縮が終わるまで待つことができることに注意してください。

興奮の衝動は、一度彼の束に入ると、その枝に沿ってすぐに広がります。 次に、信号はプルキンエ線維に入り、そこから心室心筋に送られ、そこで最初に心室中隔が影響を受け、その後、興奮が両心室に伝わります。
心室では、興奮波の経路は心臓壁の内層 (心内膜) から外層 (心外膜) まで進みます。 この場合、起電力が発生し、人体の表面に到達し、心電計(心筋の電気活動を研究できるいわゆる装置)で記録できます。
不整脈はどのようにして起こるのでしょうか?
心臓にとっての PSS の重要性は非常に重要です。健康な人の場合、心臓の伝導系は 1 分間に 60 ~ 80 回の拍動周波数をもたらします。 その動作が誤動作すると、洞結節の影響が減少し、2次および3次の自動中心(AVUおよびヒス束)によってリズムが設定され始めるため、興奮波のコースの中断につながります。 まず、この機能は房室結節によって引き継がれ、房室結節は 1 分間に 40 ~ 60 個の信号を生成することができます。
二次次数の中心に異常があり、リズム中にその値が減少すると、ビートの周波数はヒスバンドルによって調整され始め、1 分間に 15 ~ 40 のビートが発生する可能性があります。 ペリエファイバーには自動機能もあり、1秒あたり15から30のインパルスを生成することは注目に値します。

心臓の伝導系を通る信号の流れが中断されると、不整脈として知られる心拍リズムの乱れが観察されます。 この病気の特徴は、心臓の鼓動が速すぎたり遅すぎたり、鼓動間の間隔が異なる可能性があり、心臓がしばらく停止してから再び鼓動を始めることもあります。
心房から心室または心室内部への信号の伝導が妨害されると、興奮性信号の経路が「遮断」によって妨害される可能性があります。 このような病気は通常無症候性であり、他の心臓病変の兆候であることがよくあります。
伝導系を通る興奮性信号の流れに障害がある場合、健康な心臓の機能変化は、ストレス、アルコール、過食、便秘、薬の服用、カフェインを含む製品によって引き起こされます。 女性の場合、月経前に衝動の経路が中断されることがあります。
次のような病気も信号の中断に影響を与える可能性があります。
- 心臓病理 - 虚血、心不全、心筋炎、僧帽弁逸脱、心臓病;
- 甲状腺の問題;
- 糖尿病、特に高血圧や肥満との組み合わせ。
- 遺伝;
- 側弯症。
心不全が再発した場合は、必ず医師の診断を受けてください。 治療は信号障害の原因によって異なります。基礎疾患が治癒すると、心拍リズムは正常に戻ります。
不整脈が症状ではなく、本質的に独立したものである場合、治療として抗不整脈薬が処方されます。 個々の伝導枝が遮断された場合、通常は治療は必要ありませんが、医師が特別な薬を処方する場合もあります。
不整脈や閉塞がある場合、医師は外科手術を決定することがあります。その目的は、心臓のリズムを調節するペースメーカーを埋め込むことです。 この後、患者はリハビリテーションを受け、脈拍、血圧、栄養状態を常に監視し、強力な電磁源との接触を避け、さまざまな電気機器を機器から遠ざけるなど、医師の指示に厳密に従う必要があります。
手術後は医師の監督下に置かれなければなりません。 最初は装置を設置してから1か月後、次に3か月後に検査に来る必要があります。 その後、苦情がなければ、年に 1 ~ 2 回経過観察を受けます。
収縮の自動性です。 心房と心室の筋肉組織の連続的な収縮と弛緩に基づく心臓の協調的な働きは、神経インパルスを伝達する複雑な構造を持つ細胞構造によって制御されています。
心臓の伝導系は、人体の重要な機能を確保するための最も重要な機構であり、インパルス発生器(ペースメーカー)と、心筋の活動サイクルを支配するように設計された個々の複雑な構造で構成されています。 P 細胞と T 細胞の働きに基づいた細胞構造で構成され、心拍を開始し、心腔の収縮を調整するように設計されています。 最初のタイプの細胞は、自動性という重要な生理学的機能、つまり外部刺激の影響との明確な関係なしにリズミカルに収縮する能力を持っています。
次に、T 細胞は、P 細胞によって生成された収縮インパルスを心筋に伝達する能力を備えており、これにより心筋の中断のない動作が保証されます。 したがって、これら 2 つの細胞グループの協調的な相互作用に基づく伝導システムは、心臓装置に構造的に含まれる単一の生物学的メカニズムです。

人間の心臓の伝導系は、洞房結節と房室結節、およびプルキンエ線維で終わる左右の枝を持つヒスの束など、いくつかの機能コンポーネントで構成されています。 洞房(洞)結節は、右心房の領域に位置し、楕円形の小さな筋線維の塊です。 心臓全体の収縮反応を引き起こすのは、心臓の伝導系が始まるこの部分からです。 洞房結節の通常の自動化は、毎分 50 ~ 80 のインパルスであると考えられています。
房室コンポーネントは、心房中隔の後部の心内膜の下に位置し、洞房結節によって生成され送信される入力インパルスを遅延、フィルタリング、および再分配するという重要な機能を果たします。 心臓の伝導系は、その構造コンポーネントである房室結節に割り当てられた調節機能と分配機能も実行します。

このような機能が必要なのは、心房系を介して瞬時に広がり、収縮反応を引き起こす神経インパルスの波が、心房心筋が心室から分離されているため、すぐには心臓の心室に到達できないという事実によるものです。神経インパルスの通過を許さない線維組織によるものです。 そして、房室結節の領域にのみ、そのような乗り越えられない障壁はありません。 これにより、出口を求めてインパルスの波がこの重要なコンポーネントに押し寄せ、そこでインパルスは心臓装置全体に均等に分散されます。
心臓の伝導系には、その構造内に心房心筋と心室心筋を接続し、心筋細胞上にシナプスを形成し、筋収縮と神経興奮の必要な結合を提供する機能も含まれています。 これらの線維は、その中心においてヒス束の最後の枝であり、心臓の心室の心内膜下神経叢に付着しています。