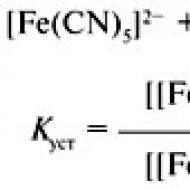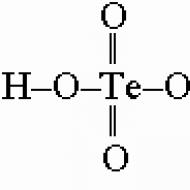
Atšķirība starp adsorbcijas un gēla caurlaidības hromatogrāfiju. Gēla hromatogrāfija kā molekulmasas noteikšanas metode. GPC pamatsistēmas
5. Gēla hromatogrāfija
Gēla filtrēšana (sinonīms gēla hromatogrāfijai) ir metode dažādu molekulmasu vielu maisījuma atdalīšanai, filtrējot caur dažādiem tā sauktajiem šūnu gēliem.
Stacionārā fāze gēla hromatogrāfijā ir šķīdinātājs, kas atrodas gēla porās, un kustīgā fāze ir pats šķīdinātājs, t.i., gan kustīgā, gan stacionārā fāze sastāv no vienas un tās pašas vielas vai viena un tā paša vielu maisījuma. Gēls ir sagatavots, pamatojoties uz, piemēram, dekstrānu, poliakrilamīdu vai citiem dabīgiem un sintētiskiem savienojumiem.
Atšķirībā no citām hromatogrāfijas metodēm, kurās tiek izmantotas atdalāmo vielu ķīmisko īpašību atšķirības, kas izpaužas to sadalīšanās laikā starp stacionāro un kustīgo fāzi, atdalīšanas pamatā ir sieta efekts, kas raksturīgs gēliem ar noteiktu poru rādiusu. Šķīdinātājs (kustīgā fāze) aizpilda gan ārējo tilpumu starp gēla graudiņiem, gan iekšējo poru tilpumu. Šķīdinātāja tilpumu starp gēla graudiņiem - V m sauc par starpproduktu, transporta vai mirušo tilpumu, bet poru iekšējo tilpumu - V p uzskata par stacionārās fāzes objektu. Ja kolonnā tiek ievadīts paraugs, kurā ir vairāku veidu joni vai dažāda izmēra molekulas, tiem ir tendence no kustīgās fāzes iekļūt porās. Šī iespiešanās ir saistīta ar entropijas sadalījumu, jo atdalāmo vielu molekulu koncentrācija ārējā šķīdumā ir augstāka nekā poru telpā. Bet tas kļūst iespējams tikai tad, ja jonu vai molekulu izmēri ir mazāki par poru diametru.
5. attēls. Kalibrēšanas līknes vispārīgs skats gēla hromatogrāfijā:
1 – izslēgšanas apgabals, kur visu molekulu izmērs ir lielāks par m2;
2 – iespiešanās vai atdalīšanas apgabals, kur molekulu izmēri ir robežās no m 1 līdz m 2;
3 - reģions, kurā notiek pilnīga molekulu, kuru izmēri ir mazāki par m 1, iespiešanās.
Gēla hromatogrāfijas procesā lielas molekulas, kuras gēls nesorbē, jo to izmēri pārsniedz poru izmēru, var atdalīt no mazām molekulām, kas iekļūst porās, un pēc tam var eluēt. Tiek veiktas arī smalkākas atdalīšanas, jo poru izmērus var regulēt, mainot, piemēram, šķīdinātāja sastāvu un līdz ar to gēla uzbriestību. Gēla hromatogrāfiju var veikt kolonnas un plānslāņa versijās.
Praksē lietotos želejas parasti iedala mīkstajos, puscietajos un cietajos. Mīkstie gēli ir lielmolekulārie organiskie savienojumi ar nelielu skaitu šķērssaišu. To ietilpības koeficients, kas vienāds ar šķīdinātāja tilpuma attiecību gēlā un tā tilpumu ārpus gēla, ir 3. Uzbriest tie ievērojami palielina savu tilpumu. Tie ir sefadeksa vai dekstrāna gēli, agara gēli, ciete utt. Tos izmanto, lai atdalītu zemas molekulmasas vielu maisījumus, bieži vien plānā slāņa versijā. Hromatogrāfiju uz mīkstiem gēliem sauc par gēla filtrēšanu.
Puscietos gēlus ražo polimerizācijas ceļā. Styrogels, stirola un divinilbenzola kopolimerizācijas produkti ar lielu šķērssavienojumu skaitu, ir kļuvuši plaši izplatīti. Puscieto gēlu kapacitātes koeficients ir robežās no 0,8...1,2, to tilpums uzbriestot nepalielinās īpaši būtiski (1,2...1,8 reizes). Hromatogrāfiju uz puscietiem gēliem sauc par gēla caurlaidības hromatogrāfiju.
Cietie gēli ietver silikagelus un bieži porainas glāzes, lai gan tās nav želejas. Cietajiem gēliem ir mazs ietilpības koeficients (0,8...1,1) un fiksēts poru izmērs. Šos materiālus izmanto augstspiediena gēla hromatogrāfijā.
Gēla hromatogrāfijas šķīdinātājiem jāizšķīdina visas maisījuma sastāvdaļas, jāsamitrina gēla virsma un tie nedrīkst uz tās adsorbēties.
Gēla hromatogrāfijas praktiskā pielietošana galvenokārt ir saistīta ar augstas molekulmasas savienojumu maisījuma atdalīšanu, lai gan tos bieži izmanto zemas molekulmasas savienojumu atdalīšanai, jo atdalīšana ar šo metodi ir iespējama istabas temperatūrā.
6. Augstas izšķirtspējas šķidruma hromatogrāfija (HPLC)
Augstas izšķirtspējas šķidruma hromatogrāfija ir visefektīvākā metode sarežģītu organisko paraugu analīzei. Parauga analīzes process ir sadalīts 2 posmos:
· parauga sadalīšana tā sastāvdaļās;
· katra komponenta satura noteikšana un mērīšana.

Atdalīšanas problēma tiek atrisināta, izmantojot hromatogrāfisko kolonnu, kas ir caurule, kas piepildīta ar sorbentu. Veicot analīzi, caur hromatogrāfijas kolonnu ar nemainīgu ātrumu tiek padots noteikta sastāva šķidrums (eluents). Šajā plūsmā tiek ievadīta precīzi izmērīta parauga deva.
Hromatogrāfijas kolonnā ievadītā parauga sastāvdaļas, ņemot vērā to atšķirīgo afinitāti pret kolonnas sorbentu, pārvietojas pa to dažādos ātrumos un secīgi sasniedz detektoru dažādos laikos.
Tādējādi hromatogrāfijas kolonna ir atbildīga par komponentu atdalīšanas selektivitāti un efektivitāti. Atlasot dažāda veida kolonnas, varat kontrolēt analizējamo vielu atdalīšanas pakāpi. Savienojumus identificē pēc to aiztures laika. Katra komponenta kvantitatīvo noteikšanu aprēķina, pamatojoties uz analītiskā signāla lielumu, kas izmērīts, izmantojot detektoru, kas savienots ar hromatogrāfijas kolonnas izvadi.
Analizējot savienojumus ar zemu MPC (biogēnie amīni, poliaromātiskie ogļūdeņraži, hormoni, toksīni), reālu paraugu sagatavošanas darbietilpības dēļ metodes jutīgums un selektivitāte kļūst par īpaši svarīgu raksturlielumu. Fluorimetriskā detektora izmantošana ļauj ne tikai samazināt noteikšanas robežas, bet arī selektīvi izolēt analizējamās vielas uz matricas un parauga pavadošo komponentu fona.
HPLC metodi izmanto sanitārajā un higiēnas pētniecībā, ekoloģijā, medicīnā, farmācijā, naftas ķīmijā, tiesu ekspertīzē, kvalitātes kontrolei un produktu sertifikācijai.
Kā eluenta padeves bloks tiek izmantots šļirces tipa “Python” sūknis, kam ir šādas īpašības:
· spiediena pulsāciju neesamība, piegādājot šķīdinātāju;
· liels tilpuma plūsmas ātrumu diapazons;
· liels sūkņa kameras tilpums;
· paplašināmība (iespēja apvienot vairākus blokus, lai izveidotu gradientu sistēmu).
Hromatogrāfiskajā sistēmā var izmantot dažāda veida detektorus, piemēram, “Fluorat-02-2M” (spektrālā atlase tiek veikta ar filtriem) vai “Fluorat-02 Panorama” (spektrālo atlasi veic monohromatori).

7. Pieteikums
Šķidruma hromatogrāfija ir vissvarīgākā fizikālās un ķīmiskās pētniecības metode ķīmijā, bioloģijā, bioķīmijā, medicīnā un biotehnoloģijā. To izmanto aminoskābju, peptīdu, olbaltumvielu, fermentu, vīrusu, nukleotīdu, nukleīnskābju, ogļhidrātu, lipīdu, hormonu uc analīzei, atdalīšanai, attīrīšanai un izolēšanai; zāļu metabolisma procesu pētīšana dzīvajos organismos; diagnostika medicīnā; Ķīmiskās un naftas ķīmijas sintēzes produktu, starpproduktu, krāsvielu, degvielu, smērvielu, eļļu, notekūdeņu analīze; šķīduma sorbcijas izotermu izpēte, ķīmisko vielu kinētika un selektivitāte. procesi.
Lielmolekulāro savienojumu ķīmijā un polimēru ražošanā šķidro hromatogrāfiju izmanto, lai analizētu monomēru kvalitāti, pētītu molekulmasu sadalījumu un sadalījumu pēc oligomēru un polimēru funkcionalitātes veidiem, kas nepieciešams produkta kontrolei. Šķidruma hromatogrāfiju izmanto arī parfimērijā, pārtikas rūpniecībā, vides piesārņojuma analīzei un tiesu zinātnē.
Secinājums
20. gadsimta sākums iezīmējās ar hromatogrāfiskās analīzes metodes atklāšanu, kas bagātināja un apvienoja dažādas zinātnes jomas, bez kurām nav iedomājams 21. gadsimta zinātnes progress. Hromatogrāfijas metožu un galvenokārt šķidrumu hromatogrāfijas ieviešana medicīnā ļāva atrisināt daudzas vitāli svarīgas problēmas: pētīt zāļu tīrības pakāpi un stabilitāti, atsevišķu hormonālo zāļu (piemēram, insulīna, interferona) preparātu izolāciju, kvantitatīvu noteikšanu. neirotransmiteri bioloģiskajos objektos: adrenalīns, norepinefrīns. Šo vielu klātbūtne dzīvā organismā ir saistīta ar spēju atcerēties, mācīties un apgūt jebkādas prasmes. Steroīdu, aminoskābju, amīnu un citu savienojumu identificēšana ar HPLC metodēm ir izrādījusies ārkārtīgi svarīga noteiktu iedzimtu slimību diagnostikā: miokarda infarkts, diabēts un dažādas nervu sistēmas slimības. Viens no neatliekamajiem klīniskās medicīnas uzdevumiem ekspresdiagnostikas jomā ir tā sauktā bioloģiskā objekta komponentu profila analīze, kas tiek veikta ar šķidruma hromatogrāfijas metodēm, kas ļauj nevis identificēt katru maksimumu, bet gan salīdzināt hromatogrammas profilus, lai iegūtu secinājums par normālu vai patoloģiju. Milzīga informācijas apjoma apstrāde tiek veikta, tikai izmantojot datoru (metode tiek saukta par "modeļu atpazīšanas metodi").
Bibliogrāfija
1. Vasiļjevs V.P. Analītiskā ķīmija, 2 grāmatas. Grāmata 2 Fizikāli ķīmiskās analīzes metodes: Mācību grāmata. studentiem universitātes, kas studē ķīmijas inženieriju. speciālists. – 4. izd., stereotips. – M.: Bustards, 2004 – 384 lpp.
2. Moskvins L.N., Tsaritsyna L.G. Atdalīšanas un koncentrēšanas metodes analītiskajā ķīmijā. – L.: Ķīmija, 1991. – 256 lpp.
3. http://bibliofond.ru/view.aspx?id=43468
4. http://ru.wikipedia.org/wiki/Paper_chromatography
5. http://referats.qip.ru/referats/preview/93743/6
6. http://www.curemed.ru/medarticle/articles/12186.htm
7. http://www.lumex.ru/method.php?id=16
8. http://www.xumuk.ru/encyklopedia/1544.html
9. http://www.pereplet.ru/obrazovanie/stsoros/1110.html
Apraksts
Kopā ar Vācijas uzņēmumu Polymer Standards Service (PSS), kas ir viens no vadošajiem materiālu un iekārtu ražotājiem gēla caurlaidības hromatogrāfijai (GPC) jeb, citiem vārdiem sakot, izmēru izslēgšanas hromatogrāfijai (SEC), mēs piedāvājam visaptverošus risinājumus vidējās molekulmasas noteikšanai. vērtē polimērus (dabiskos, sintētiskos, biopolimērus), molekulmasu sadalījumu un polimēru makromolekulu īpašības šķīdumā. Šajā metodē analīta atdalīšana notiek nevis adsorbcijas mijiedarbības ar stacionāro fāzi dēļ, bet gan tikai saskaņā ar makromolekulu hidrodinamisko rādiusu.
Lai noteiktu komponentus, kas atdalīti pēc molekulmasas, vismaz vienu koncentrācija detektors (refraktometriskais un spektrofotometriskais, tradicionālais HPLC, iztvaikošanas gaismas izkliedes detektors), kā arī speciāli detektori polimēru analīzei: viskozimetrisks, detektors ar lāzera gaismas izkliede. Kombinācijā ar koncentrācijas detektoriem šie detektori ļauj noteikt absolūto molekulmasu, makromolekulu konformāciju šķīdumā, griešanās rādiusu, hidrodinamisko rādiusu, sazarojuma pakāpi, Marka-Kuhn-Houwink vienādojuma konstantes, un virial koeficienti. Kalibrēšanas atkarību klātbūtnē šī sistēma ļauj iegūt visaptverošu informāciju par lielmolekulāriem objektiem un to uzvedību šķīdumos tikai vienā analīzē (~15 min), savukārt šo raksturlielumu novērtēšana ar tradicionālajām metodēm aizņem vairākas dienas.
Mērījumu rezultātu apstrādei ir nepieciešams izmantot īpašu programmatūru. Mēs piedāvājam elastīgas modulāras HPLC sistēmas gēla caurlaidības hromatogrāfijai (GPC), tostarp Prominence moduļus (sūkņi, kolonnas termostats, autosamplers, refraktometriskais detektors) un īpašus moduļus no Polymer Standards Service (PSS), kas ir autoritatīvs eksperts polimēru HPLC analīzes jomā. . Analīzes rezultātu aprēķināšanai iespējams izmantot gan standarta LabSolution LC programmā integrēto programmatūru Shimadzu GPC Option, gan PSS - WinGPC SW programmatūras produktus, kas atbalsta īpašus detektorus.
Lai strādātu ar agresīvām kustīgajām fāzēm attiecībā pret tradicionāli izmantotajiem kapilāriem un veidgabaliem (heksafluorizopropanols, tetrahidrofurāns), ir iespējams aprīkot HPLC sistēmas ar speciālu degazētāju, sūkņiem un autosampleru, kuru sastāvdaļas ir izturīgas pret šiem šķīdinātājiem.
GPC pamatsistēmas
Pamata HPLC sistēma GPC
Pamata HPLC sistēmu GPC var konfigurēt ar LC-20 Prominence vienībām ar vienu no koncentrācijas detektoriem (spektrofotometrisko/diožu matricu SPD-20A/SPD-M20A UV absorbējošiem polimēriem, universālo refraktometrisko RID-20A un ELSD iztvaikošanas gaismas izkliedes detektoru -LT II). Šī sistēma piemērotu standartu un kalibrēšanas atkarību klātbūtnē ļauj noteikt polimēru relatīvo molekulmasu, kā arī novērtēt makromolekulu hidrodinamiskos izmērus šķīdumā.
| Sūknis LC-20AD | |
|---|---|
| Sūkņa tips | Divkāršs paralēls mikrovirzuļa mehānisms |
| Virzuļa kameru ietilpība | 10 µl |
| Eluenta plūsmas ātruma diapazons | 0,0001 - 10 ml/min |
| Maksimālais spiediens | 40 MPa |
| Plūsmas iestatīšanas precizitāte | 1% vai 0,5 µl (atkarībā no tā, kurš ir labāks) |
| Ripple | 0,1 MPa (ūdenim ar ātrumu 1,0 ml/min un 7 MPa) |
| Darbības režīms | pastāvīga plūsma, pastāvīgs spiediens |
| Sūkņus var aprīkot ar papildu ierīci virzuļa automātiskai skalošanai. Sūkņi ir aprīkoti ar noplūdes sensoru. Sūkņa virzuļa materiāls ir izturīgs pret agresīvu vidi (safīru). | |
| Refraktometriskais detektors RID-20A | |
| Radiācijas avots | Volframa lampa, darbības laiks 20 000 stundas |
| Refrakcijas indeksa diapazons (RIU) | 1,00 - 1,75 |
| Optiskā bloka termiskā kontrole | 30 - 60С° ar optiskās sistēmas dubulto temperatūras kontroli |
| Darbības plūsmas diapazons | Spēja strādāt plašā pielietojuma diapazonā (no analītiskā režīma līdz preparatīvajai hromatogrāfijai), nemainot mērīšanas kameru: no 0,0001 līdz 20 ml/min analītiskā režīmā; līdz 150 ml/min sagatavošanas režīmā |
| Troksnis | 2,5 × 10 -9 RIU |
| Dreifēšana | 1×7 -7 RIU/stundā |
| Linearitātes diapazons | 0,01-500 × 10 -6 analītiskajā režīmā 1,0-5000 × 10 -6 sagatavošanas režīmā |
| Straumēšanas līnijas slēdzis | solenoīda vārsts |
| Maks. darba spiediens | 2 MPa (20 kgf/cm²) |
| Šūnu tilpums | 9 µl |
| Nulles regulēšana | optiskais balanss (optiskā nulle); auto-nulle, precīza nulles noregulēšana, novirzot bāzes līniju |
| Kolonnas termostats ar piespiedu gaisa konvekciju STO-20A | |
| Kontrolējams temperatūras diapazons | no 10°C virs istabas temperatūras līdz 85C° |
| Temperatūras kontroles precizitāte | 0,1C° |
| Termostata iekšējais tilpums | 220 × 365 × 95 mm (7,6 l) |
| Termostata jauda | 6 kolonnas; papildus kolonnām var uzstādīt 2 manuālos inžektorus, gradienta maisītāju, divus augstspiediena pārslēgšanas vārstus (6 vai 7 porti), vadītspējas šūnu |
| Iespējas | lineārā temperatūras programmēšana; kolonnu parametru izmaiņu izsekošana un saglabāšana failā, analīžu skaits, izietās mobilās fāzes daudzums (instalējot papildu CMD ierīci) |
| Darbības parametru uzraudzība | šķīdinātāja noplūdes sensors; pārkaršanas aizsardzības sistēma |
Gaismas izkliedes detektors
SLD7100 MALLS daudzleņķa izkliedes detektors (PSS)

SLD7100 MALLS daudzleņķa izkliedes detektors (PSS) ļauj izmērīt statisko gaismas izkliedi vienlaicīgi septiņos leņķos (35, 50, 75, 90, 105, 130, 145°) un noteikt molekulmasu absolūtās vērtības, tiesa. šķīdumā esošo makromolekulu molekulmasu sadalījuma parametri, aplēses izmēri un konformācija. Šis detektors novērš vajadzību pēc jebkādiem standartiem un var kalpot arī kā kapacitatīvs instruments (bez HPLC sistēmas) bez jebkādām papildu modifikācijām.
Viskozimetra detektors (PSS, Vācija)
DVD1260 viskozimetriskais detektors (PSS)

DVD1260 viskozimetra detektors (PSS), ja to izmanto kā daļu no LC-20 Prominence HPLC sistēmas, ļauj noteikt vidējās molekulmasas un molekulmasu sadalījuma parametri, izmantojot universālo kalibrēšanas metodi, kas ir nepieciešama makromolekulām ar sarežģītu un globulāru arhitektūru, kā arī raksturīgo viskozitāti, Marka-Kuhn-Houwink vienādojuma konstantēm, sazarojuma pakāpi, viriālo koeficientu un makromolekulu konformāciju šķīdumā, pamatojoties uz noteiktiem modeļiem. iekļauts programmatūrā. Detektora unikālā mērīšanas kamera ir četru roku asimetrisks kapilāra tilts, kas atšķirībā no visiem tirgū pieejamajiem analogiem nesatur aiztures kolonnas - salīdzinošajā ķēdē ir iebūvēta īpaša atšķaidīšanas tvertne, kas samazina analīzes laiku. vismaz uz pusi un izvairīties no negatīvu sistēmas pīķu parādīšanās. Kļūda temperatūras uzturēšanā šūnā ir mazāka par 0,01 °C, kas ir galvenais kritiskais faktors viskozimetriskajā analīzē.
| Uzturs | No 110 līdz 260 V; 50/60 Hz; 100 VA |
|---|---|
| Spiediena starpības (DP) diapazons | -0,6 kPa - 10,0 kPa |
| Ieplūdes spiediena (IP) diapazons | 0-150 kPa |
| Šūnu tilpuma mērīšana | 15 µl |
| Atšķaidīšanas kompensācijas tilpums (tvertnē) | 70 ml |
| Bīdes ātrums (1,0 ml/min) | < 2700 с -1 |
| Skaļuma līmenis | 0,2 Pa, diferenciālā spiediena signāls, 5 °C |
| Analogā izeja | 1,0 V / 10 kPa FSD spiediena starpība 1,0 V / 200 kPa FSD ieplūdes spiediens |
| Kopējais detektora skaļums | Apmēram 72 ml (ieskaitot tvertni) |
| Maks. plūsmas ātrums | 1,5 ml/min |
| Temperatūras iestatīšanas precizitāte | ±0,5 °C |
| Temperatūras stabilitāte | Ne zemāka par 0,01 °C |
| Digitālais interfeiss | RS-232C, USB, Ethernet |
| Datu pārsūtīšanas ātrums (baud) | 1200 - 115200 |
| Digitālās ieejas | Skalošana, nulles iestatīšana, iesmidzināšana, kļūda |
| Digitālās izejas | Injekcija, kļūda |
| Svars | Apmēram 4 kg |
| Izmēri (W, H, D) | 160×175×640 mm |
Piederumi

Lai strādātu GPC režīmā un veidotu kalibrēšanas attiecības, mēs piedāvājam plašu izvēli skaļruņi GPC, kas pildīts ar gēliem (stacionārā fāze) un visdažādākās ķīmiskās dabas eluentiem (polāriem un nepolāriem), kas paredzēti gan augstas molekulmasas polimēru, gan oligomēru, kā arī standarta polimēru priekšmeti.
Gēla caurlaidības hromatogrāfijas kolonnas (GPC, SEC):
- jebkuriem organiskajiem eluentiem: PSS SDV, GRAM, PFG, POLEFIN (līdz 200 °C);
- ūdens eluentiem: PSS SUPREMA, NOVEMA, MCX PROTEEMA;
- kolonnas ar monodispersu poru izmēru sadalījumu vai jauktu tipu, lai iegūtu absolūti lineārus kalibrējumus;
- noteikt zemas un augstas MM vērtības;
- gatavie kolonnu komplekti, lai paplašinātu nosakāmo molekulmasu diapazonu;
- sintētiskiem un biopolimēriem;
- risinājumi no mikro GPC līdz sagatavošanas sistēmām;
- kolonnas ātrai dalīšanai.
Kolonnas var piegādāt jebkurā eluentā pēc jūsu izvēles.
Gēla caurlaidības hromatogrāfijas (GPC, SEC) standarti:
- atsevišķus standarta paraugus un gatavus standartu komplektus;
- šķīst organiskajos šķīdinātājos:
- polistirols
- poli(α-metilstirols)
- polimetilmetakrilāts
- poli(n-butilmetakrilāts)
- poli(terc-butilmetakrilāts)
- polibutadiēns-1,4
- poliizoprēns-1,4
- polietilēns
- poli(2-vinilpiridīns)
- polidimetilsiloksāns
- polietilēntereftalāts
- poliizobutilēns
- polilaktīds
- šķīst ūdens sistēmās:
- dekstrāns
- pullulan
- hidroksietilciete
- polietilēnglikoli un polietilēna oksīdi
- Polimetakrilskābes Na-sāls
- Poliakrilskābes Na-sāls
- Poli(p-stirolsulfonskābes) Na-sāls
- Polivinilspirts
- olbaltumvielas
- MALDI standarti, komplekti gaismas izkliedes detektoru (LSD) un viskozimetrijas validācijai;
- deuterēti polimēri;
- pēc pasūtījuma izgatavoti polimēri un standarti.
Izmantojot šo metodi, analizējamo šķīdumu laiž caur kolonnu, kas piepildīta ar uzbriedinātu granulētu želeju (stacionāra fāze). Gēla daļiņas sastāv no augstas molekulmasas savienojuma (HMC), kam ir tīkla struktūra (elastīgās makromolekulas ir savstarpēji saistītas ar ķīmiskām šķērssaistēm). Šī iemesla dēļ pietūkušajam gēlam ir tīkla struktūra, starp kuras mezgliem ir šķīdinātājs.
Gēla intersticiālās telpas radiālais sadalījums- izmantotā gēla galvenā īpašība; tā ir atkarīga no polimēra un šķīdinātāja rakstura, režģa frekvences un temperatūras.
Vielu atdalīšanas efekts gēla hromatogrāfijas gadījumā ir saistīts ar to, ka molekulas, kas atšķiras pēc molārās masas (garuma), spēj iekļūt gēla struktūrā dažādos dziļumos un uzturēties tajā dažādu laiku. Tāpēc eluēšanas laikā lielas molekulas, kas nespēj dziļi iekļūt gēla granulās, vispirms atstāj kolonnu, un mazākās iznāk pēdējās. Tas ir tā, it kā molekulas tiktu izsijātas caur gēla intersticiālo telpu.
Hromatogrāfiju veic šādi. Gēla granulas ievieto stikla kolonnā, ļauj šķīdinātājā uzbriest, un tad analizēto vielu maisījumu ievada kolonnā. Mazās molekulas ir vienmērīgi sadalītas pa visu granulu tilpumu, savukārt lielākas molekulas, nespējot iekļūt iekšā, paliek tikai šķīdinātāja slānī, kas aptver granulas (ārējais tilpums). Tālāk kolonnu mazgā ar šķīdinātāju - eluentu. Kā jau minēts, lielas molekulas pārvietojas pa kolonnu ar lielāku ātrumu nekā mazās, kuru kustību pastāvīgi palēnina difūzija dziļi stacionārās fāzes granulās. Rezultātā maisījuma sastāvdaļas eluē no kolonnas molārās masas samazināšanās secībā. No kolonnas izejošā eluenta paraugus (frakcijas) ņem analīzei. Eksperiments ir ievērojami vienkāršots, ja ir iespējama nepārtraukta automātiska eluenta analīze.
Pētījumiem gēls ir jāizvēlas tā, lai tā afinitāte pret analizējamajām vielām būtu minimāla: šajā gadījumā vielas spēj brīvi sajaukties pa kolonnas slāni atbilstoši to molekulu lielumam. Gēla granulām jābūt optimālie izmēri: pārāk mazs - veicina ātru difūzijas līdzsvara izveidošanos, bet rada augstu kolonnas hidraulisko pretestību. Lielu granulu izmantošana nodrošina zemu hidraulisko pretestību, bet kavē difūziju, palielinot analizējamo vielu izdalīšanās laiku.
Turklāt granulām jābūt ar noteiktu mehānisko izturību, pretējā gadījumā to deformācija kolonnā novedīs pie eluēšanas ātruma samazināšanās.
Gēla hromatogrāfijā visplašāk izmantotā ir Sephadex(dekstrāna gēls - augstas molekulmasas polisaharīds), veidojas, kad noteiktas baktērijas tiek audzētas saharozes vidē. Ir pieejami astoņi Sephadex veidi, kas atšķiras pēc pietūkuma pakāpes, ir izturīgi pret sārmiem un vājām skābēm.
Apskatīsim konkrētu piemēru cietes un glikozes maisījuma atdalīšanai uz Sephadex G- 25. 2 cm 3 cietes un glikozes ūdens šķīduma tika ievietoti kolonnā ar 87 g gela un maisījumu eluēja ar nātrija hlorīda šķīdumu. Filtrāta frakcijas tika savāktas un noteikts cietes un glikozes saturs. Cietes molekulas praktiski neiekļuva gēla granulās, tāpēc ciete tika eluēta vispirms pie eluenta patēriņa 32-44 ml, bet glikoze - otrkārt pie eluenta patēriņa 66-80 ml.
Pamatojoties uz iegūtajiem datiem, tika izveidota hromatogramma. Lai to izdarītu, vielu koncentrācija frakcijās tiek attēlota pa ordinātu asi, un eluenta tilpums (vai frakcijas numurs) tiek attēlots pa abscisu asi. Pēc hromatogrammas tas tika noteikts vielas aiztures tilpumi V/- kopējais savāktā eluenta tilpums, līdz frakcija ar maksimālo vielas koncentrāciju atstāj kolonnu. No konkrētas kolonnas dotā viela vienmēr eluējas vienā un tajā pašā laikā V,. Izskatāmajā gadījumā cietes aiztures tilpums bija 35 ml, bet glikozei - 73 ml.
Vielu aiztures tilpums tiek reproducēts diezgan precīzi. Tāpēc, izmantojot gēla hromatogrāfiju, ir iespējams atrisināt apgriezto problēmu - noteikt nezināmu savienojumu molmasu, nosakot to V,. Lai to izdarītu, vispirms kolonna tiek kalibrēta: tiek noteikti BMC (standarta polimēru) ar zināmu molmasu aiztures tilpumi. Šim nolūkam hidrofilo gēlu kalibrēšanai visbiežāk izmanto proteīnus ar zināmu fiksētu molāro masu. Turklāt vairākiem lodveida proteīniem papildus ķīmiski noteiktajai molārajai masai ir zināms arī to molekulu lielums. Tādējādi, izmantojot kolonnu, kas kalibrēta ar zināmiem proteīniem, var iegūt arī priekšstatu par pētāmo molekulu efektīvo rādiusu.
Gēla caurlaidības hromatogrāfija, iespējams, ir visizplatītākā metode, jo tā ir vienkāršākā metode polisaharīdu atdalīšanai plašā molekulmasu diapazonā. Tajā pašā laikā tas ļauj noteikt polisaharīdu molekulmasu. Ja ir piemērojami viegli noteikšanas apstākļi, šī metode ir īpaši noderīga nestabiliem bioloģiskiem materiāliem.
Ierīce hromatogrāfijai. Gēla caurlaidības hromatogrāfija (GPC) ir metode, kurā polimēru molekulu atdalīšana balstās uz dažādajiem tilpumiem porainās gēla daļiņās, kas ir pieejamas dažāda izmēra izšķīdušās vielas molekulām.
Gēla caurlaidības hromatogrāfija ir kolonnas frakcionēšanas metodes veids, kurā sadalīšanu frakcijās veic, izmantojot molekulārā sieta metodi, pamatojoties uz molekulu spēju iekļūt noteikta izmēra adsorbenta porās. Kā adsorbenti šajā metodē tiek izmantoti materiāli, kuriem nav lādiņu un jonu grupu un kuriem ir precīzi noteikts poru izmērs (skat. nodaļu. Šīs prasības vislabāk atbilst speciāli sagatavotiem stirola kopolimēriem ar divinilbenzolu, kas uzbriest veido želejas.
Darbības shēma pārstrādes režīmā. Gēla caurlaidības hromatogrāfiju galvenokārt izmanto kā metodi polimēru vielu molekulmasu sadalījuma noteikšanai, savukārt gēla filtrācijas hromatogrāfija galvenokārt ir preparatīvā atdalīšanas metode, taču abos gadījumos ir piemērotas abas metodes. Nosakot molekulmasu sadalījumu, ir jānosaka sakarība starp hromatogrammu un molekulāro izmēru vai, pareizāk sakot, molekulmasu.
Gēla caurlaidības hromatogrāfija ar izmēru izslēgšanas hromatogrāfu.
Gēla caurlaidības hromatogrāfija ir rafijas izmēra izslēgšanas hromatogrāfija, kurā stacionārā fāze ir gēls.
Gēla caurlaidības hromatogrāfija ir kolonnas frakcionēšanas metodes veids, kurā atdalīšana balstās uz molekulārā sieta principu. Šis princips bija zināms jau 50. gadu sākumā, taču tikai pēc tam, kad Porats un Flodins no jauna atklāja un plaši izmantoja šo metodi, tā guva atzinību un plašu izmantošanu zinātniskajos pētījumos. Kopš tā laika līdz 1964. gadam tika publicēti vairāk nekā 300 rakstu par šo jauno frakcionēšanas metodi.
Aminoskābju atdalīšana ar jonu apmaiņas hromatogrāfiju. Gēla caurlaidības hromatogrāfija ļauj arī raksturot fenola-formaldehīda sveķus.
Darbības shēma recycle režīmā (10].Gēla caurlaidības hromatogrāfiju izmanto galvenokārt kā metodi polimēru vielu molekulmasu sadalījuma noteikšanai, savukārt gēlfiltrācijas hromatogrāfija galvenokārt ir preparatīvās atdalīšanas metode, bet abos gadījumos ir piemērotas abas metodes, kad nosakot molekulmasas sadalījumu, ir jānosaka sakarība starp hromatogrammu un molekulāro izmēru vai, pareizāk sakot, molekulmasu.
Gēla caurlaidības hromatogrāfija (GPC) ir metode molekulu atdalīšanai, pamatojoties uz to izmēru atšķirībām. Šo metodi sauc par gēla hromatogrāfiju, izmēru izslēgšanas un molekulārā sieta hromatogrāfiju. Uzvārds vispilnīgāk atspoguļo metodes būtību, tomēr literatūrā plašāk tiek lietots termins gēla caurlaidības hromatogrāfija.
Gēla caurlaidības hromatogrāfija (GPC) ir paņēmiens, kurā polimēru molekulu atdalīšana balstās uz dažādajiem tilpumiem porainās gēla daļiņās, kas ir pieejamas dažāda izmēra izšķīdušās vielas molekulām.
Gēla caurlaidības hromatogrāfija (GPC) ir metode, kas izmanto ļoti porainas nejonu gēla lodītes, lai atdalītu polidispersus polimērus šķīdumā. Saskaņā ar izstrādātajām GPC frakcionēšanas teorijām un modeļiem noteicošais atdalīšanas faktors ir nevis molekulmasa, bet gan molekulas hidrodinamiskais tilpums.
Gēla caurlaidības hromatogrāfijas pamatā ir dažāda garuma un līdz ar to arī atšķirīgas molekulmasas makromolekulu spēja iekļūt porainā komponentā dažādos dziļumos. Kolonnu pilda ar porainu stiklu vai ļoti šķērssaistītu uzbriedinātu polimēru gēlu, polimēru pievieno kolonnas augšpusē un pēc tam kolonnu mazgā ar šķīdinātāju. Mazākas molekulas iekļūst daudz dziļāk porās un eluēšanas procesā paliek kolonnā daudz ilgāk nekā lielākās makromolekulas.
Gēla caurlaidības hromatogrāfija ļauj ne tikai frakcionēt oligomēru maisījumus, bet arī noteikt to vidējo molekulmasu un molekulmasu sadalījumu. Šajā gadījumā Marka-Kuhna vienādojuma konstantu skaitliskās vērtības maz atšķiras no Gausa spoles koeficientiem teta šķīdinātājā.
Nukleīnskābju komponentu gēla caurlaidības hromatogrāfija tiek veikta uz šķērssaistītiem dekstrāna gēliem (Sephadex) (Sephadex, Pharmacia, Upsala, Zviedrija) un poliakrilamīda gēliem (biogeliem) (Bio-Gel, Bio-Rad Labs Richmond, Kalifornija. Turklāt gēliem ir jonu apmaiņas un adsorbcijas īpašības, kas uzrāda paaugstinātu afinitāti pret aromātiskiem un heterocikliskiem savienojumiem.
Gēla caurlaidības hromatogrāfijā tiek novērota arī purīna bāzes adsorbcija uz gēla matricas.
Oligobutadiēnu un butadiēna kopolimēru ar akrilskābi un akrilnitrilu RTF saskaņā ar 3. datiem. Gēla caurlaidības hromatogrāfijas (GPC) izmantošana klasiskajā versijā oligomēru RTF novērtēšanai joprojām ir ierobežota. Līdzīgas molekulmasas, bet atšķirīgas funkcionalitātes molekulu atdalīšana ar GPC balstās uz vidējā kvadrāta attāluma izmaiņām starp makromolekulu g / 2 galiem šķīdumā atkarībā no gala grupu rakstura un molekulmasas. R §)/ vērtību īpaši spēcīgi ietekmē molekulu ciklizācija un sazarošanās, kas noved pie tā samazināšanās 1 5 - 2 reizes, salīdzinot ar lineārām molekulām ar vienādu molekulmasu.
Gēla caurlaidības hromatogrāfijas mehānisms būtībā ir vienāds augsta un zema šķērssaites blīvuma gadījumā, lai gan praksē var rasties būtiskas atšķirības. Gēla daļiņas kolonnā ir suspendētas šķīdinātājā. Kanāli starp gēla daļiņām ir daudz lielāki, salīdzinot ar poru izmēru gēla granulu iekšpusē, tāpēc šķīdinātājs plūst tikai telpā starp gēla granulām. Izšķīdušās vielas molekulas atkarībā no to lieluma iekļūst gēla porās dažādos dziļumos un praktiski bez ierobežojumiem pārvietojas gēla granulās esošajā šķīdinātājā.
Gēla caurlaidības hromatogrāfijas mehānisms, kā parādīts šeit, ir balstīts uz pieņēmumu par difūzijas līdzsvaru. Citiem vārdiem sakot, tiek pieņemts, ka izšķīdušo molekulu sadalījuma laiks starp telpu, kas atrodas ārpus gēla daļiņām, un šīm molekulām pieejamo poru tilpumu ir diezgan īss. Laika intervāls, kurā zona, kurā atrodas izšķīdušās vielas, iziet cauri gēla daļiņām, parasti ir daudz garāks nekā pusperiods līdzsvara sasniegšanai, izšķīdušo molekulu difūzijai gēla granulās.
Gēla caurlaidības hromatogrāfijā vielu raksturo tās K a vērtība, tāpat kā parastajā hromatogrāfijā. K vērtība nav atkarīga no kolonnas lieluma, un tāpēc to var izmantot, lai salīdzinātu GPC datus, kas iegūti dažādās kolonnās.
Gēla caurlaidības hromatogrāfijā polimēra šķīdumu ievada šķidrumā (eluentā), kas pārvietojas caur kolonnu, kas piepildīta ar sorbentu. Pie izejas no kolonnas šķīdumu sadala frakcijās (zonās) atbilstoši makromolekulu lielumam. Laiku, kas pagājis no brīža, kad šķīdums tiek ievadīts eluentā, līdz brīdim, kad dotā zona atstāj kolonnu, sauc par aiztures laiku, un eluenta tilpumu, kas šajā laikā šķērso kolonnu, sauc par saglabāto tilpumu.
Poliuretāna pārvietošanas hromatogrāfija. Molekulmasas noteikšana. Molekulāro masu sadalījumu poliuretāna paraugos, kas izšķīdināti tetrahidrofurānā, noteica ar gēla caurlaidības hromatogrāfiju.
Gēla caurlaidības hromatogrāfijas principu var izmantot, lai atdalītu vielas, kas būtiski atšķiras pēc to molekulu izmēriem. Izmantotā sorbenta poru izmēram jābūt samērīgam ar atdalāmo vielu molekulu izmēru. Materiāla atdalīšanas spēja ir atkarīga no poru sadalījuma. Vielas, kuru molekulas ir tik lielas, ka tās nevar iekļūt porās, iziet cauri kolonnai ar tādu pašu ātrumu kā kustīgā fāze. Jo mazākas ir atdalāmo vielu molekulas, jo lielākā poru tilpumā tās var iekļūt, un jo vairāk tās atpaliks no kustīgās fāzes priekšpuses. Gēla caurlaidības hromatogrāfiju galvenokārt izmanto lielmolekulāro vielu analīzei.
Gēla caurlaidības hromatogrāfijā 0 raksturo molekulas un vielas, kas kolonnā nevar iekļūt gela porās; adsorbcijas hromatogrāfijā - vielas, kas, lai arī iekļūst gandrīz visā poru tilpumā, netiek saglabātas mijiedarbības dēļ ar sorbenta virsmu. Jaudas koeficients raksturo atdalāmās vielas mijiedarbības procesus ar kustīgo un stacionāro fāzi, un tāpēc tas ir termodinamisks lielums.
Gēla caurlaidības hromatogrāfijā kā kolonnu pildvielas izmanto makroporainus silikagelus, porainus stiklus un organisko polimēru gelus. Viena veida materiāli, kas atšķiras pēc porainības, ir paredzēti, lai atdalītu vielas ar dažāda izmēra molekulām.
Gēla caurlaidības hromatogrāfijā kustīgā fāze vairumā gadījumu ir vienīgais šķīdinātājs. Šķīdinātāja izvēle jāveic, ņemot vērā polimēra šķīdību tajā un vienlaikus tā, lai izmantotajā kustīgajā fāzē atdalīto vielu mijiedarbība ar stacionāro fāzi būtu minimāla. Tetrahidrofurānu visbiežāk izmanto, lai atdalītu hidrofilos polimērus, kas šķīst ūdenī.
Pietūkušas želejas shematisks attēlojums. Gēla caurlaidības hromatogrāfijā komponentu sorbcijas aktivitāti un ar to saistīto starpfāzu masas pārnesi nosaka tikai makromolekulu difūzijas mobilitāte un to izmēru attiecība pret poru izmēriem.
Gēla caurlaidības hromatogrāfijā tiek izmantoti gēla hromatogrāfi, kas sastāv no hromatogrāfijas kolonnu komplekta, kas piepildīts ar atbilstošu sorbentu (makroporaini stikli, stirogeli utt.).
Papildus vispārējiem hromatogrāfijas principiem, gēla caurlaidības hromatogrāfijai ir savas specifiskās iezīmes, kas galvenokārt saistītas ar polimēru šķīdumu īpašībām, kas ir pētījuma objekts, ar šo objektu daudzveidību, sorbentiem un analīzes apstākļiem. Tas viss, protams, sarežģī vispārējās teorētiskās shēmas izveidi. Līdz ar to GPC jomā strādājošie pētnieki metodes izstrādes pirmajos posmos bija spiesti izstrādāt konkrētas teorētiskas koncepcijas, kuru ietvaros tika noskaidroti atsevišķi eksperimentā novērotie modeļi. Tas ļāva kompetentāk iestatīt eksperimentu, optimizēt tā režīmu un interpretēt rezultātus.
Tika veikta šo polimēru gēla caurlaidības hromatogrāfija un iegūtas kalibrēšanas līknes, lai noteiktu to molekulmasu.
Gēla caurlaidības hromatogrāfijas datu apstrādei ir jānosaka trīs sistēmas raksturlielumi: iegūto datu ticamība, sistēmas kalibrēšana un izšķirtspēja. Šie trīs raksturlielumi ir savstarpēji saistīti, un galu galā tie jānosaka ar tiešiem mērījumiem. Kad tas ir izdarīts, varat izmantot netiešos datus par norādīto sistēmas raksturlielumu nemainīgumu.
Gēla caurlaidības hromatogrāfijas metodē polimēra paraugu atdala atbilstoši tā makromolekulu izmēram. Kamēr mēs runājam par molekulām, kas atšķiras tikai ar molekulmasu, atdalīšanas efektivitāti nosaka tikai un vienīgi molekulmasa. Bet pat tik vienkārša situācija var kļūt sarežģītāka, ja ķīmiski neviendabīga polimēra parauga molekulas satur grupas, kas ir dažādās pakāpēs solvatētas. Tad, neskatoties uz vienādām molekulmasām, dažām ķēdēm var būt liels molārais tilpums.
Gēla caurlaidības hromatogrāfiju izmanto, lai analizētu plašu materiālu klāstu, un tās straujo izplešanos veicināja tās vienkāršības un augstās efektivitātes priekšrocības. Visskaidrāk metodes efektivitāti parāda dabisko vielu analīzē, kuru molekulmasa svārstās plašā diapazonā.
Teorētiskajai plāksnei ekvivalenta augstuma atkarība no sorbenta graudu diametra dažāda veida sorbentiem ar dažādām iepakošanas metodēm. O - virsmas porains sorbents. dK - 2 1 mm, manuāls iepakojums.. - virspusēji porains sorbents, dK 7 9 mm, mašīnas iepakojums. f-virsmas porains sorbents, dK 7 9 mm, manuāls iepakojums. c - silikagels, sabalansēta suspensija. f - mikrosfērisks silikagels. stabilizēta piekare. P - kizelgūrs, tamponu iepakojums. A - mikrosfērisks silikagels, stabilizēta suspensija.| Šauri dispersa polistirola standartu GPC uz kolonnas (250 X 0 20 mm ar silikagelu (Fp 0 20 mm, dp 5 - 6 µm. 1 - Mw 2 - 10. 2 - Mw 5 MO4. 3 - L w 4. Kopš gēla penetrācijas hromatogrāfijā k n ir mazs, šīs hromatogrāfijas metodes F ir mazāks nekā ar adsorbcijas hromatogrāfiju.
Gēla hromatogrāfija (vai gēla caurlaidības hromatogrāfija) ir šķidruma hromatogrāfijas variants, kurā izšķīdinātā viela tiek sadalīta starp brīvo šķīdinātāju, kas ieskauj gēla lodītes, un šķīdinātāju gēla lodītes. Tā kā gēls ir pietūkusi strukturēta sistēma ar dažāda izmēra porām, atdalīšana šāda veida hromatogrāfijā ir atkarīga no atdalāmo vielu molekulāro izmēru un gela poru lieluma attiecības. Papildus molekulu lielumam, ko var uzskatīt par proporcionālu molekulmasai, molekulu formai ir nozīmīga loma gēla hromatogrāfijā. Šis faktors ir īpaši svarīgs polimēru šķīdumiem, kuros ar vienādu molekulmasu molekulas var iegūt dažādas formas (sfēriskas vai citas patvaļīgas) atbilstoši to uzbūvei un rezultātā kolonnā izturēties atšķirīgi. Papildu argumentācija ir derīga molekulām, kurām ir sfēriska forma.
GPC (gela caurlaidības hromatogrāfija), kas kalpo tikai analītiskiem nolūkiem un kuru kopējais garums ir 370 cm. (Šī hromatogrāfa darbības princips, kurā sintētisko polimēru molekulmasas sadalījums tiek noteikts gandrīz pilnībā automātiski, ir aprakstīts lapā Protams, šāda veida instrumentu var izveidot arī darbam ar ūdenī šķīstošiem polimēriem, kas būtiski atvieglos molekulmasas noteikšanas uzdevumu.
Tomēr plašo gēla caurlaidības hromatogrāfijas izmantošanu kavē nelielais poraino gēlu klāsts un neiespējamība atdalīt asfaltēnus, ņemot vērā to ķīmisko raksturu. Saskaņā ar šo metodi, izmantojot jonu apmaiņas sveķus (Amberlite-27 un Amberlite-15), asfaltēnus sadalīja četros skābajos (38-6% no sākotnējā), četros bāziskajos (16-6%) un neitrālajos (41-3%). ) frakcijas. Pēc tam, izmantojot gēla caurlaidības hromatogrāfiju, tās sadala frakcijās ar vienādu molekulu izmēru. Šī metode atklāja ievērojamu no Romaškinskas eļļas izolēto asfaltēnu polaritāti.
Dalgliša trīs punktu mijiedarbības modelis. Principā gēla caurlaidības hromatogrāfijā (ko sauc arī par izmēru izslēgšanas vai sieta hromatogrāfiju), kas ir īpaši svarīga proteīnu ķīmijā, atdalīšana tiek veikta galvenokārt molekulu sterisko izmēru atšķirību dēļ: lielas molekulas, jo tās nespēj izkliedējas matricas mazajās porās, eluē ātrāk nekā mazās molekulas.
Šķiet, ka iepriekš apspriestais gēla caurlaidības hromatogrāfijas mehānisms ir pilnībā apstiprināts ar eksperimentu. Vairumā gadījumu plūsmas ātruma maiņa neietekmē eluēšanas tilpumu, norādot, ka sistēma ir ļoti tuvu līdzsvara apstākļiem. Jāņem vērā arī tas, ka iepriekš zīmētais attēls ir ļoti aptuvens realitātes tuvinājums. Attēlā 5 - 1 norāda uz izšķīdušās vielas molekulām, kuras ar ļoti maziem izmēriem var izkliedēties pa visām matricas porām un pat vietās, kur poras sašaurinās. Tajā pašā laikā starp izšķīdušās vielas molekulām ir molekulas, kuru lielie izmēri ļauj tām iekļūt tikai noteikta izmēra porās, kas atrodas tikai uz gēla granulu ārējā apvalka. Tomēr ir jābūt vidēja izmēra molekulām, kas var iziet cauri sašaurinājumiem porās, lai gan ar daudz mazāku ātrumu mijiedarbības ar kanālu sienām dēļ. Kreigs pārliecinoši parādīja, ka izšķīdušo vielu molekulu caurbraukšanas ātrumi difūzijas laikā caur membrānām, kurām abās pusēs ir atšķirīgas šo molekulu koncentrācijas, daudz neatšķiras, ja membrānu poras ir daudz lielākas par difundējošo molekulu izmēru. Tomēr difūzijas ātrums ir jutīgs molekulu lieluma mērs tām molekulām, kuru izmēri ir tikai nedaudz mazāki par poru diametru. Acīmredzot pēc savas būtības diferenciālās difūzijas un gēla caurlaidības hromatogrāfijas procesi ir tuvu viens otram.
Frakcionējot ar gēla caurlaidības hromatogrāfiju, tiek izmantots vai mēģināts izmantot lielu skaitu dažādu gēlu. Parasti šie gēli ir polimēri ar dažādu šķērssavienojumu pakāpi un parasti uzbriest šķīdinātājos, kuros tie iegūti. Kā piemērus var minēt dekstrānus, ko izmanto ūdens šķīdumos, un polistirolus, ko izmanto, strādājot organiskajos šķīdinātājos. Pretēji ierastajam uzskatam, nav pierādīts, ka pietūkumam būtu nozīmīga loma, taču caurlaidība vai porainības pakāpe ir ļoti svarīgs gela kvalitātes rādītājs. Vona veica plašus dažādu gēlu un citu porainu materiālu pētījumus un parādīja, ka uzbriedināts silikagels (Monsanto's Santocel A) bija ļoti efektīvs polistirola frakcionēšanai benzolā. Silikagels ir hidrofila viela un tāpēc, protams, benzolā neuzbriest.
Neuztraucoties pie gēla caurlaidības hromatogrāfijas teorijas, mēs atzīmējam, ka daļiņu caurlaidība ir atkarīga no porainības un želejas iegūšanas metodes. Pašlaik visplašāk izmantotās želejas ir: ūdens šķīdumiem - dekstrāns, kas šķērssavienots ar epihlorhidrīnu (bioloģiski sintezēts ogļhidrāts) un šķērssaistīts poliakrilamīds, un neūdens šķīdumiem - polistirols, kas šķērssavienots ar divinilbenzolu.
Šajā darbā tika pētīti akrilnitrila un ABS kopolimēri, izmantojot gēla caurlaidības hromatogrāfiju un iegūtas kalibrēšanas līknes dažādiem šķīdinātājiem. Šajā darbā izmantotās metodes ABS kopolimēru analīzei tiks aprakstītas turpmāk. Šajā darbā tika izstrādātas metodes nešķīstošā polimēra (gela), šķīstošā polimēra un nepolimēru piedevu kopējā daudzuma noteikšanai, kā arī metodes saistītā akrilnitrila, butadiēna un stirola noteikšanai gan sākotnējā polimērā, gan izolētajā polimērā. nešķīstošais polimērs (gels) un šķīstošā polimēra frakcijā . Visas šīs metodes ir piemērojamas arī potētā ABS kopolimēra starpparaugu, kā arī šī kopolimēra maisījumu ar zemas molekulmasas stirola-akrilnitrila polimēru, kas tiek izmantoti ABS ražošanā, analīzei.
Šajā darbā ar gēla caurlaidības hromatogrāfijā tika pētīti ar dažādām metodēm sintezēti polikarbonāti. Darba autori secināja, ka šī metode ir vislabākā gala grupu analīzei. Polikarbonāta frakcionēšana tika veikta arī, izmantojot gēla caurlaidības hromatogrāfiju. Polikarbonāti tika frakcionēti no metilēnhlorīda, izmantojot secīgu izgulsnēšanas metodi. Šo kalibrēšanu vēl vairāk apstiprināja membrānas osmometrija un gaismas izkliedes mērījumi. Eksperimentālās viskozitātes vērtības ir pierādījušas, ka Kurata-Stockmayer-Roy attiecība ir piemērota, lai interpretētu polikarbonāta molekulāro stiepšanos metilēnhlorīdā.
Gēla caurlaidības hromatogrāfijas procesa vispārīgam aprakstam jābalstās uz atbilstoši modificētām hromatogrāfijas un sorbcijas dinamikas teorētiskajām koncepcijām, ņemot vērā polimēru šķīdumu specifiku. Hromatogrāfisko sistēmu ir ērti uzskatīt par divu fāžu sistēmu, saprotot mobilo fāzi kā kanālu kopumu, ko veido tukšumi starp sorbenta daļiņām, un stacionāro fāzi kā sorbenta urbumu.
Nosakot MWD ar gēla caurlaidības hromatogrāfiju, polimēra šķīdums tiek izvadīts caur kolonnu ar blīvējumu šķērssaistīta polimēra veidā, kas uzbriedināts šķīdumā. Makromolekulu kustības ātrums kolonnā ir atkarīgs no to mola.
Izmēru izslēgšanas hromatogrāfiju iedala gēla caurlaidības hromatogrāfijā (GPC) un gēla filtrācijas hromatogrāfijā.
Sārmaina ekstrakta frakcionēšana no egles holocelulozes, izmantojot jonu apmaiņas hromatogrāfiju. Frakcionēšanai bieži izmanto gēla caurlaidības hromatogrāfiju.
Šīs metodes fiziskais pamats ir ļoti vienkāršs un skaidrs. Pētāmais polimēra šķīdums plūst caur kolonnu, kas piepildīta ar porainu sorbentu. Komponentu maisījumu atdalīšanas pamatā ir vielas sadalījums starp kustīgo (plūstošo šķīdinātāju) un stacionāro (šķīdinātājs sorbenta porās) fāzi, t.i., uz polimēra makromolekulu atšķirīgo spēju iekļūt gēla granulu porās. , no kurienes cēlies metodes nosaukums.
Sorbenta granulu virsma ir klāta ar daudziem kanāliem, padziļinājumiem un citiem nelīdzenumiem, ko parasti sauc par porām, kuru kopējais tilpums ir V„. Šķīdinātājam nepieejamo tilpumu sauc par mirušo tilpumu. Ļaujiet šķīdumam plūst garām šādai virsmai, kuras izmēri ir samērojami ar poru izmēriem vai mazāki par tiem. Dažas no šīm molekulām iekļūst porās, ja to koncentrācija kustīgajā fāzē ir lielāka nekā porās. Kad izšķīdušās vielas zona atstāj noteiktu sorbenta zonu, molekulu koncentrācija gēla porās kļūst lielāka nekā ārpusē, un molekulas atkal izkliedējas kustīgās fāzes plūsmā. Ja molekulu izmērs ir lielāks par poru izmēru, tad šāda molekula iet garām gēla granulai bez apstājas, t.i., tiek izslēgta no poru telpas. Tādējādi lielākas makromolekulas plūst cauri kolonnai ātrāk. Tas nozīmē, ka dažādas polidispersa parauga molekulas izies no kolonnas dažādos laikos ar atšķirīgu aiztures tilpumu. VR
VR= V0 +kvV„ >
Kur Vo- kustīgās fāzes tilpums (strāvas šķīdinātājs); Kv- poru tilpuma sadalījuma koeficients: lielām makromolekulām, kas pilnībā izslēgtas no porām kv = 0; šķīdinātāja molekulām kv = 1),
Vērtības Vr galvenokārt ir atkarīgi no temperatūras, šķīdinātāja īpašībām un šķīduma koncentrācijas.
Makromolekulas uzvedību šķīdumā var viegli aprakstīt detalizēti, ja tiek noteikta tās Gibsa enerģija A.G.. Ja makromolekula iekļūst porā, tās entropija samazinās. Mijiedarbības klātbūtnē starp makromolekulas segmentiem un poru sienām notiek entalpijas izmaiņas: ar pievilcību entalpija samazinās un otrādi. Tāpēc, ja nav adsorbcijas A.G. > 0, ar spēcīgu makromolekulu adsorbciju uz poru sienām A.G. < 0. Attiecīgi pirmajā gadījumā notiek izmēru izslēgšanas hromatogrāfija (izmēru sadalījums), bet otrajā - adsorbcija; nosacījumi plkst A.G.=0 tiek saukti par kritiskiem. Kopš apgabalā A.G. > 0, makromolekulas tiek atdalītas pēc izmēra, un ir iespējama lineāro polimēru molekulmasas analīze. Ja polimērs ir sazarots, atdalīšanas process kļūst sarežģītāks un atkarīgs no zaru veida un skaita, bet kopolimēru gadījumā arī no ķēdes sastāva un bloķēšanas.
Visplašāk izmantotie sorbenti ir hidrofobu materiālu gēli, piemēram, polistirols, kas šķērssavienots ar divinilbenzolu: Šādos gēlos gandrīz pilnībā nav analizēto paraugu adsorbcijas efekta. Pēdējā laikā ir kļuvuši plaši izplatīti makroporainie stikli, kuriem salīdzinājumā ar polimēru sorbentiem ir vairākas priekšrocības (daļiņu stingrība, poru izmēru izmaiņas, ķīmiskā stabilitāte) un trūkumi (palielināta polimēru sorbcija uz tiem).
Visbiežāk izmantotie šķīdinātāji ir tetrahidrofurāns (THF), hloroforms, toluols, cikloheksāns un to maisījumi. Priekšroka tiek dota THF, kas atšķirībā no toluola neveido micellas vai agregātus ar polimēra makromolekulām un ir caurspīdīgs spektra UV apgabalā. Turklāt 11IX metodes efektivitāte, izmantojot THF, ir maksimāla diezgan zemā temperatūrā (35-45 °C). Tomēr ilgstošas uzglabāšanas laikā THF oksidējas, veidojot sprādzienbīstamus peroksīda savienojumus, tāpēc ir nepieciešams to iepriekš attīrīt. Izmantojot THF kā šķīdinātāju, var analizēt visas gumijas markas, kā arī termoplastiskos elastomērus. Analizējot nitrilbutadiēna gumiju, ieteicams izmantot šķīdinātāju maisījumu, no kuriem vienam ir afinitāte pret gumijas nepolāro daļu, bet otram pret polāro. Ja izmanto refraktometrisko detektoru, nepieciešama prasība šķīdinātājam ir atšķirība starp šķīdinātāja un polimēra refrakcijas koeficientiem.
Pirmo reizi ierīce gēla hromatogrāfijai poli analīze Merovu Voterss atbrīvoja 1964. gadā, vēlāk piecus gadus pēc Metodes atklāšana. Šodien šķidruma hromatogrāfi priekš analīze Polimēru molekulmasas sadalījums (MWD) tiek ražots visās rūpnieciski attīstītajās valstīs, Krievijā ir zināmi KhZh sērijas hromatogrāfi. Starp jaunākajām ārzemju instrumentu modifikācijām ir uzņēmuma "Waters Chem. Div." gēla hromatogrāfs. ar viskozimetru molekulmasas, MWD un makromolekulu orientācijas pakāpes noteikšanai. Ierīces karuseļa dizains ļauj vienlaikus pārbaudīt 16 paraugus.
Hromatogrāfa blokshēma ietver: O Degasser bloks - kalpo gāzu noņemšanai no šķīdinātāja un palīdz uzturēt tādu pašu šķīdinātāja daudzumu ilgā laika periodā.
О Dozatora bloks - ļauj savlaicīgi ieviest noteikta tilpuma paraugu un strādāt automātiskajā režīmā,
О Mūsdienu šķidruma hromatogrāfos hromatogrammas pārvēršana polimēra MWD, ieskaitot ierīces kalibrēšanu pēc molekulmasas un instrumentālās paplašināšanas korekciju, tiek veikta, izmantojot datoru. Tas ļauj aprēķināt diferenciālās un integrālās MWD un vidējās molekulmasas vērtības, izmantojot pieņemtās programmas. Speciāli mikroprocesori kontrolē ierīces bloku darbību saskaņā ar doto programmu.
Eksperimenta apstākļu reģistrēšanas piemērs, kas veikts ar gēla caurlaidības hromatogrāfiju. Instalācija sastāv no šādiem galvenajiem elementiem; sūkņa modelis 6000A, paraugu dozators U 6K un diferenciālais refraktometrs R 401. Instalācijā ietilpst arī 3 atdalīšanas kolonnas, katra 300 mm gara un ar iekšējo diametru 8 mm. Kolonnas ir piepildītas ar SDV-Gel 5, kura poru diametrs ir 103, 104 un 105 Å (Polymer-Standard-Service, PSS, Mainz). Testa temperatūra ir 22°C un plūsmas ātrums ir 1,0 ml/min. Tetrahidrofurānu izmanto kā šķīdinātāju, injekcijas tilpums ir 100 µl pie parauga koncentrācijas 6-10 g/l. Universālā kalibrēšana tiek veikta, izmantojot polistirolu ar molekulmasu 104-106 g/mol.
GPC ļauj izpētīt smalkas izmaiņas polimēru ķīmiskajā struktūrā un nosaka kopējo MWD, un tāpēc to plaši izmanto polimēru ķīmijā. Elastomēru rūpnieciskajā ražošanā GPC metodi var izmantot masveidā ražoto produktu darbības kvalitātes kontrolei un atbilstošai tehnoloģiskā procesa pielāgošanai, kā arī elastomēru ar noteiktām īpašībām ražošanas izstrādē un pilnveidošanā. Gēla hromatogrāfus var iekļaut automatizētās procesa vadības sistēmās, kas ņem paraugus analīzei tieši no reaktora. Analīzes ilgums, ieskaitot parauga sagatavošanu, ir 20-30 minūtes.