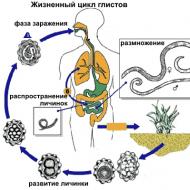
कैंसर के उपचार में अतिताप. कैंसर के उपचार के तरीकों में से एक के रूप में अतिताप
- सीधे ट्यूमर कोशिकाओं को मारें और मेटास्टेसिसजब सबसे प्रभावी कैंसर उपचार के लिए 42.5-43 डिग्री सेल्सियस के तापमान रेंज में गर्म किया जाता है;
- कीमोथेरेपी की खुराक 50% तक कम करेंएंटीट्यूमर प्रभाव में एक साथ वृद्धि और विषाक्त प्रभाव में कमी के साथ;
- असंवेदनशीलता पर काबू पाएंकीमोथेरेपी के लिए ट्यूमर .
- प्रतिरक्षा प्रणाली को उत्तेजित करेंशरीर, ताकि यह कैंसर के खिलाफ लड़ाई से जुड़ा रहे;
- ऑपरेशन को व्यवहार्य बनाएं.स्तन कैंसर, सार्कोमा, डिम्बग्रंथि कैंसर, किडनी कैंसर और अन्य के मामले में, हाइपरथर्मिया के 1-2 सत्र आयोजित करने से आप ट्यूमर के आकार को कम कर सकते हैं और अंग-संरक्षण सहित सर्जिकल उपचार कर सकते हैं।
- पुनरावृत्ति और मेटास्टेसिस के जोखिम को कम करें.
हाइपरथर्मिया कैंसर उपचार योजना:
अतिताप के साथ कैंसर के उपचार के तत्काल परिणाम:
| निदान | नमूने में रोगियों की संख्या | पूर्ण प्रतिगमन | आंशिक प्रतिगमन | स्थिर zation | जीवन की गुणवत्ता में सुधार |
| स्तन कैंसरटी 3-4 एन 0-3 एम 0-1 | 855 | 14,2 % | 38,1 % | 26,4 % | 81,3 % |
| स्थानीय रूप से उन्नत स्तन कैंसरटी 4 एन 2-3 एम 0-1 | 121 | - | 47,6 % | 28,6 % | 76,2 % |
| आमाशय का कैंसरटी2-4 एन0-2 एम 1 | 270 | - | 22,9 % | 51,4 % | 64,3 % |
| पेट का कैंसरटी2-4 एन0-2 एम 1 | 245 | - | 11,1 % | 71,1 % | 48,9 % |
| मलाशय का कैंसरटी2-4 एन0-2 एम 1 | 245 | 4,4 % | 26,7 % | 53,3 % | 64,4 % |
| नरम ऊतक सार्कोमा T2bN0M 1 | 155 | 3,6 % | 36,4 % | 47,3 % | 83,6 % |
| गुर्दे का कैंसरटी1- 3ए एन0 -2 एम 1 | 211 | - | 36,4 % | 54,5 % | 90,9 % |
| अंडाशय, गर्भाशय ग्रीवा, गर्भाशय के शरीर का कैंसर T3a-3cN1M0-1 | 140 | 12,5 % | 35,0 % | 37,5 % | 65,0 % |
| स्वरयंत्र का कैंसर T3-4aN0-2M0-1 | 42 | - | 41,7 % | 50,0 % | 91,7 % |
| थायराइड कैंसर T4a-4bN1M0 | 10 | 10,0 % | 30,0 % | 30,0 % | 80,0 % |
प्रक्रिया के एक महीने बाद मूल्यांकन किया गया। उन्नत कैंसर और व्यापक मेटास्टेसिस वाले मरीजों को ध्यान में रखा गया, जिनमें अन्य अस्पतालों में उपचार की पृष्ठभूमि के मुकाबले प्रगति देखी गई। पहले, मरीजों को कीमोथेरेपी के 17 कोर्स तक मिलते थे।
पूर्ण प्रतिगमन
- सभी घावों का पूरी तरह से गायब हो जाना कैंसर का सबसे अच्छा इलाज है।
आंशिक प्रतिगमन
- सभी या व्यक्तिगत फ़ॉसी के आकार में 50% से अधिक की कमी।
स्थिरीकरण
- नए घावों की अनुपस्थिति में फ़ॉसी में 50% से कम की कमी, या 25% से अधिक की वृद्धि नहीं।
परिणामों के मूल्यांकन के लिए नियंत्रण अध्ययन को ध्यान में रखा गया: रेडियोग्राफी और फ्लोरोस्कोपी; कंप्यूटेड टोमोग्राफी या चुंबकीय अनुनाद इमेजिंग; पीईटी सीटी; अल्ट्रासाउंड, आदि
नश्वरताकीमोथेरेपी के साथ सामान्य हाइपरथर्मिया के सत्र आयोजित करते समय, यह हाइपरथर्मिया सत्रों की संख्या का 0.6% था (यानी हाइपरथर्मिया के 100 सत्रों में से 0.6 लोग मर सकते हैं)। पिछले 12 वर्षों में, क्लिनिक में हाइपरथर्मिया के दौरान कोई घातक मामला सामने नहीं आया है।
कैंसर के उपचार के बाद सामान्य अतिताप के साथ लोग कितने समय तक जीवित रहते हैं?
गणना उन रोगियों के लिए सामान्य अतिताप के पहले सत्र की तारीख से की गई थी जिनमें उपचार के परिणामस्वरूप नैदानिक प्रभाव प्राप्त हुआ था (पूर्ण प्रतिगमन, आंशिक प्रतिगमन, स्थिरीकरण)। जीवित रहने की दर की गणना कपलान-मायर पद्धति के अनुसार की गई थी। परिणाम महत्वपूर्ण हैं (पी<0,01).
सामान्य अतिताप के साथ कैंसर के उपचार में बाधाएँ:
- मस्तिष्क और रीढ़ की हड्डी के ट्यूमर, साथ ही मस्तिष्क में कैंसर मेटास्टेस;
- गंभीर सामान्य स्थिति: गंभीर कैंसर नशा, कैशेक्सिया, श्वसन विफलता III-IV डिग्री, यकृत विफलता, गुर्दे की विफलता, हृदय विफलता, गंभीर हृदय अतालता;
- एनीमिया, ल्यूकोपेनिया, थ्रोम्बोसाइटोपेनिया III-IV गंभीरता।
विधि के बारे में अधिक जानकारी:
तथ्य यह है कि तापमान ट्यूमर कोशिकाओं के लिए हानिकारक है, अधिकांश विशेषज्ञों द्वारा इस पर सवाल नहीं उठाया गया है।
आधारशिला प्रश्न यह है कि यह विधि अभी तक सर्वव्यापी क्यों नहीं है: मानव शरीर को इतने तापमान तक कैसे गर्म किया जाए कि ट्यूमर मर जाए, लेकिन रोगी न मरे?
आधी सदी से भी अधिक समय से विभिन्न देशों के वैज्ञानिकतापमान और गर्म करने की समयावधि के साथ कैंसर के इलाज के तरीकों का प्रयोग करें। गोर्की (अब निज़नी नोवगोरोड) के बंद विज्ञान शहर में 80 के दशक में एक प्रोफेसर की भागीदारी के साथ सोवियत वैज्ञानिक इस मुद्दे को हल किया. सामान्य विद्युत चुम्बकीय अतिताप के लिए एक तकनीक विकसित की गई (आरएफ पेटेंट "घातक नियोप्लाज्म की हाइपरथर्मिक इलेक्ट्रोमैग्नेटिक थेरेपी करने की विधि"क्रमांक 082458 दिनांक 27 जून 1994)। पेटेंट का स्वामी सह-लेखकों के पास है।
कैंसर के उपचार में अतिताप के तापमान क्षेत्र:
1) जब ट्यूमर 38-40 डिग्री सेल्सियस तक गर्म हो जाता है, तो इसकी वृद्धि बढ़ सकती है;
2) 40-42 डिग्री सेल्सियस तक पहुंचने पर, ट्यूमर कीमोथेरेपी दवाओं और आयनकारी विकिरण के प्रति संवेदनशील हो जाता है;
3) 42.5 डिग्री सेल्सियस से ऊपर गर्म करने पर, ट्यूमर कोशिकाओं की मृत्यु देखी जाती है - कैंसर के उपचार में सबसे महत्वपूर्ण प्रभाव।
सामान्य ऊतकों के लिए तापमान व्यवस्था उनकी अधिक तापीय स्थिरता के कारण दोगुनी बड़ी होती है। इसलिए, हाइपरथर्मिया केवल बीमार, ख़राब कैंसर कोशिकाओं के लिए घातक है।
के-टेस्ट क्लिनिक में कीमोथेरेपी के साथ सामान्य हाइपरथर्मिया प्रोफेसर आई.डी. कारेव (आरएफ पेटेंट नंबर 2077348 दिनांक 04/20/1997) की विधि के अनुसार किया जाता है और क्लिनिक विशेषज्ञों की भागीदारी से विकसित घरेलू इंस्टॉलेशन "YUG-VCHG" का उपयोग करके किया जाता है।
सामान्य अतिताप प्रक्रिया का कोर्स:
कैंसर के उपचार के दौरान, रोगी को पानी के गद्दे पर एक इलेक्ट्रोमैग्नेटिक इंस्टालेशन पर लेटी हुई स्थिति में रखा जाता है।
सामान्य अतिताप यांत्रिक वेंटिलेशन के साथ सामान्य संज्ञाहरण के तहत किया जाता है। तापमान नियंत्रण मलाशय में, अन्नप्रणाली में, त्वचा पर, बाहरी श्रवण नहर में स्थापित सेंसर का उपयोग करके किया जाता है।
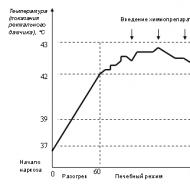
रोगी के शरीर का तापमान 42.5-43 डिग्री सेल्सियस तक बढ़ जाता है और 80 मिनट तक बना रहता है; यह तापमान अंतराल मूल उपचार आहार है।
तापमान शासन का चयन रोगी की प्रारंभिक स्थिति को ध्यान में रखते हुए, जटिलताओं के जोखिम का आकलन करते हुए, कीमोथेरेपी के साथ सामान्य अतिताप के पिछले सत्रों के परिणामों का आकलन करते हुए किया जाता है।
सत्र के दौरान, हृदय, यकृत, मस्तिष्क की गहरी संरचनाओं के ताप के स्तर को नियंत्रित किया जाता है। सेरेब्रल एडिमा को रोकने के लिए इसे ठंडा किया जाता है। यदि सत्र के दौरान रोगी के शरीर को 43 डिग्री सेल्सियस तक गर्म करना संभव है, तो मस्तिष्क का तापमान केवल 41 डिग्री सेल्सियस तक बढ़ाया जा सकता है।

चावल। 2. सामान्य अतिताप के एक सत्र का तापमान शासन
अधिकतम वार्मिंग की पृष्ठभूमि के खिलाफ, हम कीमोथेरेपी दवाएं पेश करते हैं, और यह संभव है प्रभाव में एक साथ वृद्धि के साथ दवाओं की खुराक को 50% तक कम करना.
प्रक्रिया के दौरान, पानी और इलेक्ट्रोलाइट संतुलन का निरंतर समायोजन किया जाता है।
सत्र के अंत में, यूनिट बंद कर दी जाती है, और रोगी शरीर के वजन के आधार पर 40-80 मिनट तक ठंडा हो जाता है। एनेस्थीसिया से निष्कासन 39 डिग्री सेल्सियस के तापमान पर किया जाता है।
सामान्य प्रक्रिया के बादअतिताप :
सत्र की समाप्ति के बाद पहले घंटों में, रोगी को गहन देखभाल इकाई में स्थानांतरित कर दिया जाता है, जहां जल और इलेक्ट्रोलाइट्स के नुकसान की भरपाई करने के उद्देश्य से जलसेक चिकित्सा की जाती है। प्रक्रिया के बाद कुछ घंटों के भीतर रोगी के शरीर का तापमान सामान्य हो जाता है।
अगले 1-7 दिनों में, मरीज़ विषहरण जलसेक चिकित्सा, रक्त मापदंडों की प्रयोगशाला निगरानी से गुजरते हैं।
कीमोथेरेपी के साथ सामान्य अतिताप के कई सत्र आयोजित करते समय, उपचार के पाठ्यक्रमों के बीच का अंतराल तीन सप्ताह है।
उपचार के परिणाम काफी हद तक प्रभावित होते हैं सामान्य अतिताप और तापमान व्यवस्था के सत्रों की संख्या. 42.5-43 डिग्री सेल्सियस के तापमान शासन का उपयोग उपचार के परिणामों में 17-20% तक सुधार करने और 42.3-42.5 डिग्री सेल्सियस के तापमान शासन की तुलना में रोग की प्रगति वाले लोगों की संख्या को कम करने की अनुमति देता है। प्रत्येक रोगी के लिए तापमान शासन का चुनाव सामान्य स्थिति, सहवर्ती रोगों की उपस्थिति आदि से निर्धारित होता है।
कैंसर के उपचार में, सामान्य हाइपरथर्मिया की इष्टतम संख्या 42.5-43 डिग्री सेल्सियस पर 4 प्रक्रियाएं हैं। यह हासिल करने के लिए काफी है अधिकांश ट्यूमर का प्रतिगमन, व्यक्तिपरक प्रभाव प्राप्त करना और रोगियों के जीवन की गुणवत्ता में सुधार करना।
अतिताप के बाद जीवन की गुणवत्ता और कल्याण का आकलन:
- दर्द सिंड्रोम की तीव्रता का गायब होना या कम होना;
- शारीरिक गतिविधि में वृद्धि;
- सांस की तकलीफ़ आदि में कमी
मरीजों को दर्द की तीव्रता में उल्लेखनीय कमी का अनुभव होता है अतिताप के बाद दूसरे दिन ही. हाइपरथर्मिया के 7-14 दिनों के बाद आमतौर पर कमजोरी, सांस लेने में तकलीफ और वजन बढ़ने में कमी देखी जाती है। प्रसारित स्तन कैंसर में, 42.5-43 डिग्री सेल्सियस के तापमान पर अतिताप के व्यक्तिपरक प्रभाव से 95% से अधिक रोगियों में जीवन की गुणवत्ता में सुधार देखा गया।
यह ध्यान दिया जाना चाहिए कि असामान्य ऊतकों पर तापमान का प्रभाव रेडियोफ्रीक्वेंसी एब्लेशन के समूह से संबंधित नहीं है, यह एक पूरी तरह से अलग तकनीक है। विकिरण चिकित्सा के साथ संयोजन में, थर्मल एक्सपोज़र की विधि को थर्मोरेडियोथेरेपी कहा जाता है।
ऑन्कोलॉजी में अतिताप: यह क्या है?
अंतर्राष्ट्रीय ऑन्कोलॉजी ने अभी तक एक आम राय विकसित नहीं की है कि कौन से तापमान संकेतक सबसे सुरक्षित हैं और साथ ही सबसे प्रभावी भी हैं। उपचार के दौरान, शरीर का तापमान आमतौर पर 39.5 और 40.5 डिग्री सेल्सियस के बीच के स्तर तक पहुंच जाता है। हालांकि, अन्य शोधकर्ता हाइपरथर्मिया को 41.8-42 डिग्री सेल्सियस के बीच परिभाषित करते हैं, जो यूरोप और संयुक्त राज्य अमेरिका में आम है। जापान और रूस उच्चतम दर ° C लेते हैं।
तापमान और एक्सपोज़र का समय परस्पर संबंधित हैं। लंबी अवधि और उच्च तापमान कैंसर कोशिकाओं को मारने में बहुत प्रभावी हैं, लेकिन वे विषाक्तता के खतरे को भी काफी गंभीर रूप से बढ़ाते हैं। अव्यवस्थित और सघन संवहनी संरचना वाली ट्यूमर कोशिकाओं में गर्मी को दूर करना बहुत मुश्किल होता है, जो उनके संबंध में एपोप्टोसिस (शारीरिक रूप से क्रमादेशित कोशिका मृत्यु का एक प्रकार) या सामान्य मृत्यु की उत्तेजना में योगदान देता है। जबकि स्वस्थ ऊतकों में बेहतर तापीय चालकता होती है, और इसलिए वे उच्च तापमान को बेहतर ढंग से सहन करते हैं।
भले ही कैंसर कोशिकाएं तुरंत नहीं मरती हैं, फिर भी वे कैंसर थेरेपी या कीमोथेरेपी में आयनीकृत विकिरण के प्रति अधिक संवेदनशील हो सकती हैं। स्थानीय अतिताप के दौरान गर्मी ट्यूमर की रक्त वाहिकाओं को फैला देती है, जिससे ट्यूमर के ऑक्सीजनेशन (ऑक्सीजन संतृप्ति) को बढ़ाने में मदद मिलती है, जिससे विकिरण विरोधी कैंसर चिकित्सा अधिक प्रभावी हो जाती है। ऑक्सीजन एक शक्तिशाली रेडियोसेंसिटाइज़र है, जो डीएनए क्षति के माध्यम से विकिरण की दी गई खुराक की प्रभावशीलता को काफी बढ़ा देता है। ऑक्सीजन की कमी वाली ट्यूमर कोशिकाएं सामान्य ऑक्सीजन वातावरण की तुलना में विकिरण क्षति के प्रति 2-3 गुना अधिक प्रतिरोधी हो सकती हैं।
हाइपरथर्मिया को कीमोथेरेपी के साथ मिलाने पर यह बहुत प्रभावी साबित हुआ है। प्रकाशित अध्ययनों ने हाइपरथर्मिया और कीमोथेरेपी के साथ संयुक्त उपचार प्राप्त करने वाले मूत्राशय कैंसर के रोगियों में 10 साल की पुनरावृत्ति और मेटास्टेसिस-मुक्त अस्तित्व में सुधार दिखाया है। 53% मरीज़ अगले 10 वर्षों तक जीवित रहे, जबकि अकेले कीमोथेरेपी ने केवल 15% मरीज़ों के जीवित रहने को सुनिश्चित किया।
तीव्र ताप से सेलुलर प्रोटीन का विकृतीकरण और जमाव होता है, जो ट्यूमर कोशिकाओं को जल्दी से नष्ट कर देता है। सामान्य से कुछ डिग्री अधिक लंबे समय तक, मध्यम तापन से कोशिकाओं में अधिक सूक्ष्म संरचनात्मक परिवर्तन हो सकते हैं। अन्य तरीकों के साथ हल्के ताप उपचार से जैविक विनाश की उत्तेजना के कारण कोशिका मृत्यु हो सकती है।
कमियों में से, विशेषज्ञ सामान्य कोशिकाओं में हीट शॉक के कई जैव रासायनिक परिणामों पर ध्यान देते हैं, जिनमें विकास मंदता और बाद में आयनीकृत रेडियोधर्मी थेरेपी के प्रति संवेदनशीलता में वृद्धि शामिल है।
हाइपरथर्मिया से गर्म क्षेत्र में रक्त का प्रवाह बढ़ जाता है, जिससे ट्यूमर में रक्त का प्रवाह दोगुना हो सकता है। यह घटना पैथोलॉजिकल क्षेत्रों में कीमोथेराप्यूटिक एजेंटों के सकारात्मक प्रभाव को बढ़ाती है।
हल्का अतिताप, जो कई संक्रामक रोगों में स्वाभाविक रूप से गर्म तापमान प्रदान करता है, ट्यूमर पर प्राकृतिक प्रतिरक्षाविज्ञानी हमलों को उत्तेजित कर सकता है। हालाँकि, यह थर्मोटोलरेंस नामक एक प्राकृतिक शारीरिक प्रतिक्रिया को भी प्रेरित करता है, जो असामान्य कोशिकाओं की रक्षा करता है।
50 डिग्री सेल्सियस से ऊपर, बहुत उच्च तापमान का उपयोग उच्छेदन के लिए किया जाता है - कुछ ट्यूमर का प्रत्यक्ष विनाश। तकनीक सीधे ट्यूमर में एक धातु ट्यूब के रूप में आवेषण का उपयोग करती है, जिसकी नोक गर्म होती है, जिससे इसकी परिधि के आसपास कोशिका मृत्यु हो जाती है।
यह जोर देने योग्य है कि रूस में हाइपरथर्मिक एब्लेशन की तकनीक अभी भी अध्ययन के अधीन है, और व्यावहारिक चिकित्सा में इसका उपयोग शायद ही कभी किया जाता है। हालाँकि, परीक्षणों की प्रभावशीलता हमारे देश सहित इस पद्धति के लिए बहुत अच्छी संभावनाओं की भविष्यवाणी करती है।
स्थानीय, क्षेत्रीय और सामान्य अतिताप के तरीकों के अंतर और विशेषताएं
संकेतों और चिकित्सीय संभावनाओं के आधार पर, उनका उपयोग, एक नियम के रूप में, तीन संस्करणों में किया जाता है।
एक बहुत छोटा क्षेत्र गरम किया जाता है, आमतौर पर ट्यूमर के भीतर ही। कुछ मामलों में, विधि का लक्ष्य आसपास के ऊतकों को नुकसान पहुंचाए बिना असामान्य कोशिकाओं को गर्म करके मारना है। गर्मी को इससे उत्तेजित किया जा सकता है:
- अति लघु तरंगें;
- उच्च रेडियो आवृत्तियाँ;
- अल्ट्रासोनिक ऊर्जा;
- चुंबकीय अतिताप का उपयोग करना।
ट्यूमर के स्थान के आधार पर, सुइयों या जांच के उपयोग के माध्यम से शरीर की सतह, ऊतकों के अंदर या गहरे क्षेत्रों पर गर्मी लागू की जा सकती है। एक अपेक्षाकृत सामान्य प्रकार छोटे ट्यूमर का रेडियोफ्रीक्वेंसी एब्लेशन है। चिकित्सीय लक्ष्य सबसे आसानी से प्राप्त किया जाता है जब ट्यूमर शरीर की सतह पर होता है (सतही हाइपरथर्मिया), या यदि ट्यूमर में सीधे सुई या जांच डालना संभव है (अंतरालीय हाइपरथर्मिया)।
- क्षेत्रीय अतिताप
शरीर का एक बड़ा क्षेत्र गर्म होता है, उदाहरण के लिए, एक संपूर्ण अंग या अंग। आमतौर पर, विधि का लक्ष्य कैंसर कोशिकाओं को इस तरह से कमजोर करना है कि बाद में विकिरण या कीमोथेरेपी दवाओं की कार्रवाई से उनकी मृत्यु हो सके। पिछली विधि की तरह, क्षेत्रीय अतिताप उसी सतही या अंतरालीय तरीकों का उपयोग कर सकता है या रक्त छिड़काव पर निर्भर हो सकता है। छिड़काव प्रक्रिया के दौरान, रोगी के रक्त को शरीर से निकाल लिया जाता है, गर्म किया जाता है और रक्त वाहिकाओं में वापस कर दिया जाता है जो सीधे शरीर के वांछित हिस्से तक ले जाती हैं। एक नियम के रूप में, कीमोथेरेपी दवाओं का उपयोग एक साथ किया जाता है।
इस दृष्टिकोण का एक विशेष प्रकार निरंतर पेरिटोनियल छिड़काव है, जिसका उपयोग प्राथमिक पेट मेसोथेलियोमा और गैस्ट्रिक कैंसर सहित जटिल इंट्रा-पेट के नियोप्लाज्म के इलाज के लिए किया जाता है। कैंसर कोशिकाओं को मारने के लिए गर्म कीमोथेरेपी दवाओं को सीधे पेट में इंजेक्ट किया जाता है।
पूरा शरीर 39 से 43 डिग्री सेल्सियस और उससे अधिक तापमान तक गर्म हो जाता है। इस पद्धति का उपयोग आमतौर पर मेटास्टैटिक कैंसर के इलाज के लिए किया जाता है। इसमें इन्फ्रारेड हाइपरथर्मिक गुंबदों का उपयोग शामिल है, जिसके तहत सिर को छोड़कर रोगी के पूरे शरीर को रखा जाता है। अन्य तरीकों में रोगी को बहुत गर्म कक्ष में रखना या उन्हें गर्म, नम कंबल में लपेटना शामिल है। दुर्लभ तरीकों में से, लगातार गर्म करने या गर्म मोम में डुबाने वाले विशेष वेटसूट का उपयोग किया जाता है।
हाइपरथर्मिया से किस प्रकार के कैंसर का इलाज किया जा सकता है?
अकेले, हाइपरथर्मिया ने घातक बीमारियों का इलाज करने की एक अनूठी क्षमता का प्रदर्शन किया है। यह भी ज्ञात है कि यह तकनीक अन्य उपचारों की प्रभावशीलता को काफी हद तक बढ़ा देती है।
रेडियोधर्मी विकिरण के संयोजन में, हाइपरथर्मिया बड़ी मात्रा में ऑक्सीजन की उपस्थिति में विशेष रूप से प्रभावी होता है, बशर्ते कि एक्सपोज़र कम से कम एक घंटे तक एक साथ हो।
पिछले दस वर्षों में, विकिरण के साथ संयोजन में हाइपरथर्मिया का उपयोग निम्नलिखित निदान वाले रोगियों में चिकित्सीय प्रयोजनों के लिए किया गया है:
- प्रारंभिक चरण का स्तन कैंसर;
- सिर और गर्दन पर कैंसर के स्थानीयकरण के साथ;
- प्रोस्टेट कैंसर।
प्रसिद्ध वैज्ञानिक प्रकाशन अकेले कीमोथेरेपी की तुलना में कीमोथेरेपी के संयोजन से मूत्राशय के कैंसर के 38% रोगियों में सुधार दिखाते हैं। स्तन कैंसर के रोगियों में, परिणाम में 18% रोगियों में बेहतर प्रतिक्रिया देखी गई।
कैंसर के अन्य कौन से प्रकार हैं जिनमें हाइपरथर्मिया उपचार से महत्वपूर्ण सुधार दिखाई देता है?
- मेलेनोमा और त्वचा कैंसर।
- नरम ऊतक सारकोमा.
- मूत्राशय कैंसर।
- ग्रीवा कैंसर।
- मलाशय का कैंसर।
- बगल और छाती की दीवार के घातक ट्यूमर।
- लिम्फ नोड्स में मेटास्टेसिस।
रूस में अध्ययनों ने 43.5-44 डिग्री सेल्सियस पर उच्च हाइपरथर्मिया के साथ दिलचस्प परिणाम दिखाए हैं जब विधि को लागू किया गया है:
- भोजन - नली का कैंसर;
- स्वरयंत्र कैंसर;
- यकृत कैंसर;
- एचआईवी संक्रमण और प्रतिरक्षा प्रणाली के विकारों के साथ।
ट्यूमर का पृथक्करण हाइपरथर्मिया की किस्मों में से एक है।
रेडियोफ्रीक्वेंसी एब्लेशन (आरएफए) संभवतः स्थानीयकृत हाइपरथर्मिया का सबसे अधिक इस्तेमाल किया जाने वाला प्रकार है। तापमान बढ़ाने के लिए उच्च आवृत्ति वाली रेडियो तरंगों का उपयोग किया जाता है।
- ट्यूमर में एक पतली सुई जांच थोड़े समय के लिए डाली जाती है, आमतौर पर 10 से 30 मिनट के लिए।
- अल्ट्रासाउंड, एमआरआई, या सीटी का उपयोग करके जांच प्लेसमेंट को समायोजित किया जाता है।
- जांच की नोक एक उच्च आवृत्ति धारा प्रदान करती है जो 40 और 60 डिग्री सेल्सियस के बीच गर्मी पैदा करने में सक्षम है, जो एक निश्चित क्षेत्र के भीतर कोशिका मृत्यु का कारण बनती है।
- मृत कोशिकाएं हटाई नहीं जातीं, निशान ऊतक बन जाती हैं और समय के साथ घुल जाती हैं।
आरएफए का उपयोग आमतौर पर उन ट्यूमर के इलाज के लिए किया जाता है जिन्हें शल्य चिकित्सा द्वारा हटाया नहीं जा सकता है, या उन रोगियों में जिनका विभिन्न कारणों से इलाज नहीं किया जा सकता है। यह प्रक्रिया बाह्य रोगी के आधार पर की जा सकती है। पुनरावृत्ति में सक्षम ट्यूमर के लिए एब्लेशन पुनरावृत्ति संभव है। इसके अलावा, आरएफए को अन्य चिकित्सीय उपायों में भी जोड़ा जा सकता है, जिसमें नियोप्लाज्म का सर्जिकल निष्कासन, विकिरण चिकित्सा, कीमोथेरेपी, जलसेक थेरेपी, अल्कोहल एब्लेशन, या कीमोएम्बोलाइज़ेशन शामिल है।
आरएफए का उपयोग 5 सेमी व्यास तक के ट्यूमर के इलाज के लिए किया जा सकता है। यह तकनीक यकृत, गुर्दे और फेफड़ों में घावों के इलाज के लिए सबसे प्रभावी है। शरीर के अन्य क्षेत्रों में इसके उपयोग का वर्तमान में अध्ययन किया जा रहा है। हाइपरथर्मिक एब्लेशन उपचार के बाद दीर्घकालिक प्रभावकारिता अभी तक ज्ञात नहीं है, लेकिन शुरुआती परिणाम उत्साहजनक हैं।
अतिताप की संभावित जटिलताएँ और दुष्प्रभाव
उच्च तापमान के उपयोग से ऊतक जल सकते हैं, लक्ष्य अंग को नुकसान हो सकता है, विशेष रूप से क्षेत्रीय उपचार के मामलों में। क्षति की डिग्री एक्सपोज़र के समय, तापमान और ऊतक के प्रकार के आधार पर अलग-अलग होगी। इस विधि के प्रति सबसे अधिक संवेदनशील मस्तिष्क और फेफड़े के ऊतक होते हैं।
- सूजन.
- थ्रोम्बस का गठन।
- आंतरिक रक्तस्त्राव।
- हृदय संबंधी विकार.
रेडियोधर्मी विकिरण या कीमोथेरेपी के साथ संगतता में काफी मजबूत विषाक्तता होती है, जो एक नियम के रूप में, प्रक्रिया के कई घंटों बाद व्यक्त होती है और कभी-कभी काफी गंभीर विकार पैदा कर सकती है।
सामग्री का उपयोग और पुनर्मुद्रण करते समय, साइट पर एक सक्रिय लिंक की आवश्यकता होती है!
सामान्य शारीरिक स्थितियों के तहत, हाइपोथैलेमस लगभग 37ºC का तापमान बनाए रखता है, जो दिन के समय के आधार पर भिन्न हो सकता है। सबसे कम दरें सुबह के समय देखी जाती हैं, और शरीर का तापमान दिन के मध्य में अपने अधिकतम तक पहुंच जाता है। शाम तक शरीर की तापीय अवस्था 36.5 - 37 डिग्री सेल्सियस होती है।
कैंसर में तापमान - लक्षण, कारण
- 38 ºС से अधिक अतिताप।
- अत्यंत थकावट।
- बहुत तेज सिरदर्द।
- तीव्र, गीली खाँसी।
- ट्यूमर में दर्द होता है.
क्या कैंसर में कोई तापमान होता है? ऑन्कोलॉजिकल रोगों में, हाइपरथर्मिया संकेतक मुख्य रूप से सबफ़ेब्राइल संकेतक (37 ºС - 38 ºС) तक बढ़ते हुए देखे जाते हैं। ऐसे तापमान संकेतक तथाकथित "निम्न-श्रेणी बुखार" का संकेत देते हैं। कुछ मामलों में शरीर की इस स्थिति के लिए विशेष उपचार की आवश्यकता नहीं होती है, खासकर यदि अल्प ज्वर संकेतक थोड़े समय के लिए बने रहते हैं।
तापमान कितना होना चाहिए?
चिकित्सीय अतिताप के तरीके
- इंट्राकैवेटरी या इंट्राल्यूमिनल दृष्टिकोण। इन विधियों का उपयोग अन्नप्रणाली के कैंसरयुक्त घावों और "रेक्टल कैंसर" के निदान के लिए किया जाता है। तकनीक को एक विशेष गर्म जांच का उपयोग करके किया जाता है, जिसे संबंधित अंग में डाला जाता है।
संपूर्ण शरीर अतिताप
- क्या आप यहां हैं:
- घर
- कैंसर का उपचार
- कैंसर के लिए तापमान कितना होना चाहिए?
2018 ऑन्कोलॉजी। सभी साइट सामग्री केवल सूचनात्मक उद्देश्यों के लिए पोस्ट की गई हैं और स्व-उपचार सहित कोई भी निर्णय लेने का आधार नहीं हो सकती हैं। सामग्रियों के सभी कॉपीराइट उनके संबंधित स्वामियों के हैं
कैंसर में तापमान
कैंसर में बुखार जैसी स्थिति का मतलब बैक्टीरिया सूक्ष्मजीवों या वायरस से शरीर का संक्रमण हो सकता है। इसके अलावा, कैंसर में तापमान अक्सर ऑन्कोलॉजिकल प्रक्रिया के 3-4 चरणों में देखा जाता है।
सामान्य शारीरिक स्थितियों के तहत, हाइपोथैलेमस लगभग 37ºC का तापमान बनाए रखता है, जो दिन के समय के आधार पर भिन्न हो सकता है। सबसे कम दरें सुबह के समय देखी जाती हैं, और शरीर का तापमान दिन के मध्य में अपने अधिकतम तक पहुंच जाता है। शाम तक शरीर की तापीय अवस्था 36.5 - 37 डिग्री सेल्सियस होती है।
कैंसर में तेज बुखार में शरीर के तापमान में 38ºC से ऊपर की वृद्धि होती है, जो एक आंतरिक रोग प्रक्रिया की उपस्थिति को दर्शाता है। यह स्थिति कई प्रकार के कैंसर के लिए काफी सामान्य लक्षण मानी जाती है।
कैंसर में तापमान - लक्षण, कारण
कैंसर में संक्रामक बुखार, एक नियम के रूप में, निम्नलिखित लक्षणों के साथ होता है:
- 38 ºС से अधिक अतिताप।
- टटोलने पर, रोगियों की त्वचा अक्सर गर्म होती है।
- पूरे शरीर में ठंडक और कंपन महसूस होना।
- ऊपरी और निचले अंगों में दर्द.
- अत्यंत थकावट।
- पेशाब के दौरान जलता दर्द|
- दस्त के रूप में पाचन तंत्र के विकार।
- बहुत तेज सिरदर्द।
- बार-बार चक्कर आना।
- नासॉफरीनक्स और मौखिक गुहा में दर्द।
- तीव्र, गीली खाँसी।
- शरीर के एक हिस्से में स्थानीयकृत दर्द का प्रकट होना।
- ट्यूमर में दर्द होता है.
क्या कैंसर में कोई तापमान होता है? ऑन्कोलॉजिकल रोगों में, हाइपरथर्मिया संकेतक मुख्य रूप से सबफ़ेब्राइल संकेतक (37 ºС - 38 ºС) तक बढ़ते हुए देखे जाते हैं। ऐसे तापमान संकेतक तथाकथित "निम्न-श्रेणी बुखार" का संकेत देते हैं। कुछ मामलों में शरीर की इस स्थिति के लिए विशेष उपचार की आवश्यकता नहीं होती है, खासकर यदि अल्प ज्वर संकेतक थोड़े समय के लिए बने रहते हैं।
कैंसर के साथ, विशिष्ट कैंसर रोधी चिकित्सा की अवधि के दौरान तापमान भी होता है।
कैंसर के लिए तापमान कितना होना चाहिए?
कैंसर के लिए तापमान कितना होना चाहिए? ऑन्कोलॉजी में ज्वर की स्थिति लगातार तीन चरणों से गुजरती है:
- शरीर का तापमान बढ़ाएं. एक जीवाणु और वायरल संक्रमण के प्रवेश या एक रोग प्रक्रिया के गठन के जवाब में, मानव शरीर ल्यूकोसाइट्स की एक बढ़ी हुई संख्या का उत्पादन करता है, जिसका द्रव्यमान धीरे-धीरे संचार और लसीका प्रणालियों में बढ़ जाता है। बड़ी संख्या में श्वेत रक्त कोशिकाएं हाइपोथैलेमस को प्रभावित करती हैं, जो अतिताप को भड़काती है। बुखार की शुरुआती अवस्था में रोगी को अक्सर ठंड और कंपकंपी महसूस होती है। यह शरीर के तापमान में वृद्धि के प्रति त्वचा और मांसपेशियों की सतह परतों की प्रतिक्रिया है। इस घटना का सार एपिडर्मल रक्त वाहिकाओं का संकुचन है, जो आंतरिक थर्मिया के अधिकतम संरक्षण में योगदान देता है। इसके अलावा, प्रतिक्रिया को संवहनी तंत्र के स्टेनोसिस के परिणामस्वरूप आवधिक मांसपेशी संकुचन माना जाता है।
- हाइपरथर्मिया के दूसरे चरण में, गर्मी हस्तांतरण प्रक्रियाएं संतुलित होती हैं, जो चिकित्सकीय रूप से हाइपरथर्मिक अवस्था के स्थिरीकरण से प्रकट होती है। इसलिए, उदाहरण के लिए, फेफड़ों के कैंसर में तापमान महीनों तक 37 ºС - 37.5 ºС की सीमा में हो सकता है, जिससे कैंसर रोगी को विशेष असुविधा नहीं होती।
- शरीर को ठंडा करना. हाइपरथर्मिया के अंतिम चरण में, सतही रक्त वाहिकाएं खुल जाती हैं, जिससे अत्यधिक पसीना आता है और परिणामस्वरूप, शरीर के तापमान में कमी आती है। ऐसी प्रक्रिया को आमतौर पर फार्मास्यूटिकल्स की मदद से उत्तेजित किया जाता है, हालांकि कुछ नैदानिक मामलों में स्व-थर्मोरेग्यूलेशन देखा जाता है।
कैंसर चिकित्सा में हाइपरथर्मिया का उपयोग
घातक घाव वाले कैंसर में अधिकतम चिकित्सीय परिणाम प्राप्त करने के लिए कौन सा तापमान आवश्यक है? कुछ नैदानिक मामलों में, 37.5 ºС - 38.0 ºС के शरीर थर्मोरेग्यूलेशन संकेतक अत्यधिक सक्रिय एक्स-रे विकिरण के प्रभावों के प्रति रोग कोशिकाओं की संवेदनशीलता में वृद्धि में योगदान करते हैं। विकिरण चिकित्सा के साथ संयोजन में शरीर की अतितापीय स्थिति बड़ी संख्या में उत्परिवर्तित ऊतकों के विनाश के रूप में तेजी से कैंसर विरोधी प्रभाव देती है।
चिकित्सीय अतिताप के तरीके
आज तक, शरीर के तापमान को कृत्रिम रूप से बढ़ाने के कुछ तरीके विकास के अधीन हैं।
इस तकनीक में शरीर के उस हिस्से पर स्थानीय थर्मल प्रभाव शामिल होता है जहां कैंसर पहले ही बन चुका है। ट्यूमर के स्थानीयकरण के आधार पर, निम्न प्रकार के स्थानीय हाइपरथर्मिया मौजूद हैं:
- एक बाहरी दृष्टिकोण जिसमें तापीय ऊर्जा या तो त्वचा की सतह पर या उपत्वचीय परत पर लागू की जाती है। ये गतिविधियाँ मुख्यतः अनुप्रयोग प्रकृति की हैं।
- इंट्राकैवेटरी या इंट्राल्यूमिनल दृष्टिकोण। इन विधियों का उपयोग अन्नप्रणाली के कैंसरयुक्त घावों और "रेक्टल कैंसर" के निदान के लिए किया जाता है। तकनीक को एक विशेष गर्म जांच का उपयोग करके किया जाता है, जिसे संबंधित अंग में डाला जाता है।
- मध्यवर्ती तकनीकों को गहराई से स्थानीयकृत अंगों के ऑन्कोलॉजिकल रोगों के लिए संकेत दिया जाता है, जैसे, उदाहरण के लिए, मस्तिष्क और रीढ़ की हड्डी। स्थानीय एनेस्थीसिया के तहत एक विशेष रेडियोफ्रीक्वेंसी सेंसर को पैथोलॉजी के प्राथमिक फोकस में लाया जाता है, जिससे इसमें हाइपरथर्मिक परिवर्तन होते हैं।
इसमें शरीर या अंगों के बड़े क्षेत्रों को गर्म करना शामिल है।
संपूर्ण शरीर अतिताप
इस तकनीक का उपयोग एकाधिक मेटास्टेटिक घावों के लिए किया जाता है। शरीर के तापमान में प्रणालीगत वृद्धि आमतौर पर विशेष तापीय कक्षों में प्राप्त की जाती है।
यह जानना महत्वपूर्ण है:
एक टिप्पणी जोड़ें उत्तर रद्द करें
श्रेणियाँ:
इस साइट पर जानकारी केवल सूचनात्मक उद्देश्यों के लिए प्रदान की गई है! कैंसर के इलाज के लिए वर्णित तरीकों और नुस्खों का उपयोग स्वयं और डॉक्टर की सलाह के बिना करने की अनुशंसा नहीं की जाती है!
कैंसर के लिए सौना
इस मामले ने मुझे एक ऐसी महिला से मिलवाया जो गर्भाशय के कैंसर से ठीक हो गई थी, सचमुच चूल्हे पर लेटी हुई थी। चौथे चरण में इस बीमारी को बेहद नजरअंदाज किया गया। डॉक्टरों का मानना था कि वह एक वर्ष से अधिक जीवित नहीं रह पायेगी। मरीज ने कीमोथेरेपी से इनकार कर दिया और अपने घर गांव चला गया। वह ज्यादातर समय रूसी चूल्हे के पास बैठकर या उस पर लेटकर बिताती थी। लगातार कई घंटों तक, उसने अधिकतम तापमान को झेला, और यहाँ तक कि अपनी पीठ को कंबल में लपेट लिया। चार साल बाद जब हम दोबारा मिले तो वह स्वस्थ महसूस कर रही थी। इस मामले में मेरी बहुत दिलचस्पी थी. आखिरकार, यह सर्वविदित है कि आधिकारिक ऑन्कोलॉजी में किसी भी थर्मल प्रक्रिया को अस्वीकार्य माना जाता है।
हालाँकि, गर्मी से कैंसर का इलाज करने का विचार नया नहीं है, साहित्य में इसकी चर्चा लंबे समय से होती रही है। इस विचार के समर्थक इस तथ्य से आगे बढ़ते हैं कि कैंसर कोशिकाएं ऊंचे तापमान के प्रति बहुत संवेदनशील होती हैं - 40° पर वे विकसित होना बंद कर देती हैं। मरहम लगाने वाले अलेक्जेंडर विनोकुरोव का दावा है कि 10 दिनों तक शरीर पर ऐसे तापमान के संपर्क में रहने पर, कैंसर कोशिकाएं मर जाती हैं, जबकि सामान्य कोशिकाएं नहीं बदलती हैं, पूरी तरह से अपने कार्यों को संरक्षित करती हैं।
हाइपरथर्मिक प्रक्रियाओं की मदद से सर्वोत्तम परिणाम स्तन के ट्यूमर, घातक लिम्फोमा, कोलन, प्रोस्टेट, स्वरयंत्र, थायरॉयड, गुर्दे, पेट और आंतों, सार्कोमा के कैंसर के साथ प्राप्त किए गए थे। किए गए अध्ययनों के अनुसार, पांच वर्षों तक ऐसी प्रक्रियाओं से इलाज किए गए 1400 रोगियों में से, लगभग 80% में उल्लेखनीय सुधार देखा गया - प्राथमिक और मेटास्टेटिक ट्यूमर के विकास की समाप्ति। पहले सत्र के बाद सारा दर्द बंद हो गया। रोग के चरण IV में 60% से अधिक रोगियों में, उपचार के कई सत्रों के बाद, मेटास्टेस और नशा के लक्षण गायब हो गए। रेडिकल सर्जरी के बाद चिकित्सीय उपायों के परिसर में सामान्य हाइपरथर्मिया को शामिल करने से पुनरावृत्ति की संख्या में काफी कमी आती है और कैंसर की पुनरावृत्ति का खतरा कम हो जाता है।
आइए कैंसर कोशिकाओं पर उच्च तापमान के प्रभाव के तंत्र को समझने का प्रयास करें।
एक सिद्धांत के अनुसार, ऑन्कोलॉजिकल रोग कोशिका के जीनोम या साइटोप्लाज्म में वायरल आरएनए की शुरूआत से जुड़े होते हैं। यह मानने का कारण है कि हाइपरथर्मिक प्रक्रियाओं से वायरस और विदेशी आरएनए मातृ कोशिका से अलग हो जाते हैं। बाहर जाने के लिए मजबूर होने पर वे प्रतिरक्षा कोशिकाओं का शिकार बन जाते हैं। उनका आगे का भाग्य प्रतिरक्षा के स्तर पर निर्भर करता है। इसलिए, कैंसर के उपचार में सबसे महत्वपूर्ण क्षेत्रों में से एक प्रतिरक्षा प्रणाली को मजबूत करना है।
लेकिन कोशिकाओं पर उच्च तापमान के प्रभाव पर वापस। यह पाया गया कि 43.5° के तापमान पर कैंसर कोशिकाएं मर जाती हैं। हालाँकि, यह महत्वपूर्ण तापमान केवल अल्प अवधि के लिए ही बनाए रखा जा सकता है। इसलिए, मेरी राय में, 40-42° पर केंद्रित, लेकिन दीर्घकालिक प्रभाव वाली विधियाँ अधिक स्वीकार्य हैं।
हाइपरथर्मिक उपचार विकसित करने वाले वैज्ञानिकों ने ट्यूमर कोशिकाओं की ग्लूकोज का सख्ती से उपभोग करने की क्षमता को भी ध्यान में रखा। लगातार ग्लूकोज की कमी कैंसर कोशिकाओं के विकास और विभाजन में एक प्राकृतिक सीमित कारक है। यह सुझाव दिया गया है कि यदि आप विशेष रूप से रक्त को ग्लूकोज से संतृप्त करते हैं, तो कैंसर कोशिकाएं इसे बिना किसी प्रतिबंध के अवशोषित करना शुरू कर देंगी, और खुद को ऊर्जा की प्रचुरता की स्थिति में ले आएंगी।
बढ़ते तापमान के साथ यह प्रक्रिया बढ़ती है। थर्मल उत्तेजना के बाद सक्रिय रूप से ग्लूकोज का उपभोग करने वाली कोशिकाओं को ग्लूकोज से ऊर्जा उत्पादन के अपशिष्ट उत्पादों के उपयोग में संकट का अनुभव होने लगता है। उनमें जमा होने वाले कार्बनिक अम्लों के अणु माध्यम की अम्लता में तेज बदलाव का कारण बनते हैं, जो कोशिका झिल्ली की प्रतिरोध सीमा के साथ असंगत होता है। यह डेटोनेटर की तरह काम करता है - सक्रिय कैंसर कोशिकाओं का स्वतःस्फूर्त दहन होता है। इसलिए, थर्मल प्रक्रियाओं के दौरान, रोगी को ग्लूकोज (उदाहरण के लिए, शहद के रूप में) देने की सलाह दी जाती है।
हालाँकि, सैद्धांतिक भविष्यवाणियाँ व्यावहारिक अध्ययन के परिणामों से पूरी तरह सहमत नहीं थीं। यह पता चला कि कैंसरग्रस्त ट्यूमर संरचना में विषम है। इसमें सभी कोशिकाएं सक्रिय विभाजन और ग्लूकोज के प्रचुर अवशोषण की स्थिति में नहीं हैं। प्रत्येक ट्यूमर में सक्रिय रूप से बढ़ने वाली कोशिकाओं और परिधीय कोशिकाओं के विशेषाधिकार प्राप्त पूल होते हैं जो लसीका और रक्त वाहिकाओं से अलग हो जाते हैं। फिलहाल, ट्यूमर की परिधीय परतें सापेक्ष आराम में हैं।
प्रायोगिक अभ्यास ने पुष्टि की है कि हाइपरग्लेसेमिया (चीनी की अधिकता) के साथ संयोजन में हाइपरथर्मिया वास्तव में ट्यूमर के ऊतकों के विनाश को सुनिश्चित करता है। लेकिन साथ ही, यह पता चला कि ट्यूमर कोशिकाओं का कुछ छोटा हिस्सा अभी भी नहीं मरता है, इसके थोक के व्यापक परिगलन के बावजूद। इस कारण शीघ्र ही रोग की पुनरावृत्ति उत्पन्न हो गई। पुनरावृत्ति का स्रोत कैंसर कोशिकाओं को पीछे धकेलना निकला, जो पहले निष्क्रिय थीं। अपने धनी पड़ोसियों के विनाश के बाद, ये कोशिकाएँ जाग गईं और बढ़ने लगीं।
इस प्रकार, इष्टतम (43 डिग्री सेल्सियस या अधिक) से अधिक हाइपरथर्मिक एक्सपोज़र, जिससे सक्रिय ऑन्कोसेल्स का परिगलन होता है, आराम करने वाली ट्यूमर परतों को बिल्कुल भी प्रभावित नहीं करता है। इष्टतम (42 डिग्री तक) के भीतर तापमान उन्हें आराम की स्थिति से अधिक सक्रिय और इसलिए अधिक थर्मोसेंसिव में स्थानांतरित कर देता है। यह केवल एक्सपोज़र चक्र के वांछित मोड को चुनने के लिए ही रहता है ताकि ट्यूमर न केवल अपने सक्रिय रूप से बढ़ते केंद्र में, बल्कि परिधि के साथ भी गायब होना शुरू हो जाए।
कई चिकित्सकों का मानना है कि ट्यूमर को नेक्रोटाइज़ (ख़त्म) नहीं होना चाहिए, बल्कि धीरे-धीरे ठीक होना चाहिए। ऐसा करने के लिए, इष्टतम तापमान प्रभाव की बहुत संकीर्ण सीमाओं का पालन करना आवश्यक है। ऊपरी सीमा से परे, ट्यूमर नेक्रोसिस शुरू हो जाता है। इष्टतम सीमा के भीतर, ट्यूमर धीरे-धीरे ठीक हो जाता है, जो प्रतिरक्षा को मजबूत करने से सुगम होता है। इसलिए, हाइपरथर्मल थेरेपी की अवधि के दौरान, टी-एक्टिविन या डायुसिफॉन जैसे प्रभावी इम्युनो-मॉड्यूलेटर का उपयोग करना बहुत उचित है - दवाएं जो प्रतिरक्षा सूत्र को मजबूत करती हैं, रक्त और लिम्फ में लिम्फोसाइटों की संख्या में वृद्धि करती हैं, साथ ही टी-कोशिकाएं, हत्यारी कोशिकाएं जो शरीर के आंतरिक वातावरण में ओंकोसेल और सूक्ष्मजीवों को नष्ट करती हैं। इन सीमाओं से नीचे का तापमान कैंसर कोशिकाओं को दबाता नहीं है, और संभवतः उन्हें उत्तेजित भी करता है। यह वह तापमान है जिसे आधिकारिक चिकित्सा में ऑन्कोलॉजिकल रोगों में वर्जित माना जाता है। जब ऑन्कोलॉजिस्ट कहते हैं कि हीटिंग से ट्यूमर की प्रगति और मेटास्टेसिस बढ़ सकती है, तो वे अति-उच्च तापमान के प्रभावों को ध्यान में नहीं रखते हैं।
हालाँकि, अति-उच्च तापमान, जैसा कि पहले ही उल्लेख किया गया है, बीमारी की पुनरावृत्ति को बाहर नहीं करता है। ऐसा लगता है कि कुछ शोधकर्ताओं की विफलताओं को इस तथ्य से समझाया गया है कि उन्होंने उपचार के दौरान सीमित तापमान निर्धारित किया और ट्यूमर कोशिकाओं के संपर्क की अवधि पर अपर्याप्त ध्यान दिया। मुझे ऐसा लगता है कि ऑन्कोलॉजिकल रोगों के उपचार में सबसे प्रभावी लंबे समय तक हल्के तापमान (40 -42 डिग्री) का उपयोग है, और इसलिए गहरा और अधिक समान प्रभाव है।
इस उद्देश्य के लिए, अलेक्जेंडर विनोकरोव द्वारा प्रस्तावित होम सौना एकदम सही है (चित्र देखें)।
घरेलू सौना में तापमान एक इलेक्ट्रिक हीटर (उदाहरण के लिए, 1.5 किलोवाट की शक्ति वाला एक साधारण घरेलू स्टोव) द्वारा बनाए रखा जाता है, जो पत्थरों से भरे पानी के 2-3 जार को गर्म करता है। पानी उबलता है और वाष्पित हो जाता है, जिससे नरम भाप बनती है। यह सभी सरल उपकरण कुर्सी के पीछे लगे लकड़ी के शेल्फ पर रखे गए हैं। शेल्फ की भीतरी दीवारें एल्युमीनियम शीट से इंसुलेटेड हैं। आप किसी पुराने रेफ्रिजरेटर से एल्युमीनियम फ्रीजर का भी उपयोग कर सकते हैं। बिजली के हीटर के किनारों पर पत्थर लगे होने चाहिए। यह महत्वपूर्ण है कि वह शेल्फ की दीवारों को न छुए।
मरीज को एक कुर्सी पर बैठाया जाता है और कुर्सी के साथ ही कंबल में लपेट दिया जाता है। यह वांछनीय है कि इस "कोकून" के अंदर एक इलेक्ट्रिक थर्मोस्टेट हो, जो एक स्थिर तापमान प्रदान करेगा। तापमान को नियंत्रित करने के लिए एक विशेष थर्मामीटर का उपयोग किया जाता है।
यदि सॉना के लिए आर्मरेस्ट वाली कुर्सी का उपयोग किया जाता है, तो उनके ऊपर विशेष आर्क स्थापित किए जाने चाहिए ताकि हवा के संचलन के लिए "कोकून" के अंदर एक छोटी सी जगह बनी रहे। कुर्सी का पिछला भाग ठोस होना आवश्यक नहीं है।
यदि चाहें तो हाथों को बाहर निकाला जा सकता है, जिसके लिए रोगी के ऊपर कंबल की जगह एक कोट डाला जाता है और बटनों से बांध दिया जाता है, और कमर के नीचे उन्हें कंबल में लपेट दिया जाता है। हाइपरथर्मिक प्रक्रियाओं के दौरान सिर बाहर रहता है। होम स्टीम रूम का एक महत्वपूर्ण लाभ यह है कि पूरा शरीर गर्म हो जाता है (आधे घंटे या एक घंटे में शरीर का तापमान 40 डिग्री तक पहुंच जाता है), लेकिन साथ ही एक व्यक्ति कमरे के तापमान पर हवा में सांस लेता है। वैसे, मेरी राय में, शरीर के अलग-अलग हिस्सों या अंगों का स्थानीय तापन अप्रभावी है। जाहिरा तौर पर, यह स्थानीय वार्मिंग के प्रति विपरीत संवहनी प्रतिक्रियाओं के कारण है।
हाइपरथर्मिक प्रक्रिया के दौरान, पसीना बढ़ाने के लिए शहद के साथ गर्म चाय (हर्बल या हरी) पीने की सलाह दी जाती है। पसीना आसानी से सोखने के लिए सूती अंडरवियर पहनें। प्रक्रिया के अंत के बाद, शरीर को सामान्य तापमान तक ठंडा करने के लिए एक कंट्रास्ट शावर लिया जाता है।
ऑन्कोलॉजिकल रोगों में, प्रति दिन दो हाइपरथर्मिक सत्र (सुबह और दोपहर) किए जाते हैं, जो दो से चार घंटे तक चलते हैं। इष्टतम हवा का तापमान 40-42° है। उपचार का कोर्स 10 दिन है। इसे कुछ दिनों के अंतराल के साथ 6-10 बार दोहराया जाता है।
इसके अतिरिक्त, कोशिका क्षय उत्पादों से रक्त को शुद्ध करने के लिए उपायों की सिफारिश की जाती है: चिकित्सीय उपवास, जूस थेरेपी (उदाहरण के लिए, लाल, पीले और काले रंग की सब्जियों, फलों और जामुनों से रस लेना), अवशोषक लेना, शाकाहारी भोजन, मिट्टी थेरेपी, आदि।
घरेलू सौना के लिए अवरक्त विकिरण वाले विशेष ओवन का उपयोग करना और भी बेहतर है। इसकी किरणें नरम होती हैं, वे ऊतकों में अधिक समान रूप से और गहराई तक प्रवेश करती हैं। ऐसे ओवन घरेलू उपयोग के लिए व्यावसायिक रूप से भी उपलब्ध हैं।
इन्फ्रारेड थर्मल एक्सपोज़र के कई फायदे हैं। सबसे पहले, इसे ले जाना आसान है। यह गंभीर रूप से बीमार और दुर्बल लोगों के लिए विशेष रूप से महत्वपूर्ण है। दूसरे, यह गहरे ट्यूमर और मेटास्टेस के मामलों के लिए अधिक प्रभावी है। दुर्भाग्य से, मुझे इन्फ्रारेड हीटिंग के उपयोग पर विशेष अध्ययन के बारे में जानकारी नहीं मिली है। मुझे यकीन है कि यही भविष्य है.
इस तथ्य के बावजूद कि आधिकारिक चिकित्सा में ऑन्कोलॉजिकल रोगों के मामले में शरीर को गर्म करना वर्जित माना जाता है, रूस और विदेशों में ऐसे क्लीनिक हैं जहां इस बीमारी का इलाज गर्मी से किया जाता है। उदाहरण के लिए, गोर्की में एक ऐसा क्लिनिक है, जहां एक थर्मल चैंबर का उपयोग ताबूत के रूप में किया जाता है (जैसे यहां वर्णित विधि में, सिर बाहर रहता है)। प्रक्रियाएं उपकरणों के नियंत्रण में की जाती हैं।
अंत में, मैं यह कहना चाहता हूं कि शरीर का लंबे समय तक अतिताप एक बहुत ही शारीरिक तरीका है। यह बुखार जैसा दिखता है - रोग के प्रेरक एजेंट के प्रति शरीर की एक प्राकृतिक प्रतिक्रिया, जब शरीर तापमान में वृद्धि की मदद से बीमारी से लड़ता है।
लोकप्रिय लिंक
नवीनतम लेख
लोकप्रिय लेख
हम सोशल नेटवर्क में हैं
लेखों की सामूहिक नकल (प्रति साइट 5 से अधिक) निषिद्ध है.
नकल की अनुमति हैकेवल सक्रिय के साथ, बंद नहीं
. असहनीय दुष्प्रभावों के बारे में चिंता करें (जैसे कि कब्ज, मतली, या चेतना का धुंधलापन। दर्द की दवा की लत के बारे में चिंता। निर्धारित दर्द दवा के नियमों का पालन न करना। वित्तीय बाधाएं। स्वास्थ्य प्रणाली से संबंधित मुद्दे: कैंसर के दर्द प्रबंधन के लिए कम प्राथमिकता। सबसे उपयुक्त उपचार रोगियों और उनके परिवारों के लिए बहुत महंगा हो सकता है। नियंत्रित पदार्थों का सख्त विनियमन। उपलब्ध दवाएं लचीलापन कैंसर दर्द प्रबंधन की कुंजी है। चूंकि रोगी निदान, रोग के चरण, दर्द के प्रति प्रतिक्रिया और व्यक्तिगत प्राथमिकताओं में भिन्न होते हैं, इसलिए इन विशेषताओं को निर्देशित किया जाना चाहिए। 6 कैंसर को ठीक करने या कम से कम उसके विकास को स्थिर करने के लिए। अन्य उपचारों की तरह, किसी विशेष कैंसर के इलाज के लिए विकिरण चिकित्सा का उपयोग करने का विकल्प कई कारकों पर निर्भर करता है। इनमें कैंसर का प्रकार, रोगी की शारीरिक स्थिति, कैंसर का चरण और ट्यूमर का स्थान शामिल है, लेकिन यह इन्हीं तक सीमित नहीं है। विकिरण चिकित्सा (या रेडियोथेरेपी ट्यूमर को सिकुड़ने के लिए एक महत्वपूर्ण तकनीक है। उच्च ऊर्जा तरंगें कैंसरग्रस्त ट्यूमर पर निर्देशित होती हैं। तरंगें सेलुलर प्रक्रियाओं को बाधित करके कोशिकाओं को नुकसान पहुंचाती हैं, कोशिका विभाजन को रोकती हैं, और अंततः घातक कोशिकाओं की मृत्यु का कारण बनती हैं। घातक कोशिकाओं के एक हिस्से की भी मृत्यु ट्यूमर सिकुड़न की ओर ले जाती है। विकिरण चिकित्सा का एक महत्वपूर्ण नुकसान यह है कि विकिरण विशिष्ट नहीं है (अर्थात, यह विशेष रूप से कैंसर कोशिकाओं के लिए कैंसर कोशिकाओं पर निर्देशित नहीं है और स्वस्थ कोशिकाओं को भी नुकसान पहुंचा सकता है। उपचार के लिए सामान्य और कैंसरयुक्त ऊतक प्रतिक्रिया करते हैं। ट्यूमर और सामान्य ऊतकों का विकिरण के प्रति प्रभाव उपचार से पहले और उपचार के दौरान उनके विकास पैटर्न पर निर्भर करता है। विकिरण डीएनए और अन्य लक्ष्य अणुओं के साथ बातचीत के माध्यम से कोशिकाओं को मारता है। मृत्यु तुरंत नहीं होती है, लेकिन तब होती है जब कोशिकाएं विभाजित होने की कोशिश करती हैं, लेकिन विकिरण के संपर्क के परिणामस्वरूप, विभाजन प्रक्रिया में विफलता होती है, जिसे गर्भपात माइटोसिस कहा जाता है। इस कारण से, तेजी से विभाजित होने वाली कोशिकाओं वाले ऊतकों में विकिरण क्षति तेजी से दिखाई देती है, और यह कैंसर कोशिकाएं हैं जो तेजी से विभाजित होती हैं। सामान्य ऊतक बाकी कोशिकाओं के विभाजन को तेज करके विकिरण चिकित्सा के दौरान नष्ट हुई कोशिकाओं की भरपाई करते हैं। इसके विपरीत, विकिरण चिकित्सा के बाद ट्यूमर कोशिकाएं अधिक धीरे-धीरे विभाजित होने लगती हैं, और ट्यूमर आकार में सिकुड़ सकता है। ट्यूमर सिकुड़न की डिग्री कोशिका उत्पादन और कोशिका मृत्यु के बीच संतुलन पर निर्भर करती है। कार्सिनोमा एक प्रकार के कैंसर का उदाहरण है जिसमें अक्सर विभाजन की उच्च दर होती है। इस प्रकार के कैंसर आमतौर पर विकिरण चिकित्सा पर अच्छी प्रतिक्रिया देते हैं। उपयोग किए गए विकिरण की खुराक और व्यक्तिगत ट्यूमर के आधार पर, उपचार रोकने के बाद ट्यूमर फिर से बढ़ना शुरू हो सकता है, लेकिन अक्सर पहले की तुलना में अधिक धीरे-धीरे। ट्यूमर को दोबारा बढ़ने से रोकने के लिए विकिरण को अक्सर सर्जरी और/या कीमोथेरेपी के साथ जोड़ा जाता है। विकिरण थेरेपी उपचारात्मक के लक्ष्य: उपचारात्मक उद्देश्यों के लिए, जोखिम आमतौर पर बढ़ाया जाता है। विकिरण के प्रति प्रतिक्रिया हल्के से लेकर गंभीर तक होती है। लक्षण राहत: इस प्रक्रिया का उद्देश्य कैंसर के लक्षणों से राहत देना और जीवन को लम्बा खींचना, अधिक आरामदायक रहने का वातावरण बनाना है। इस प्रकार का उपचार आवश्यक रूप से रोगी को ठीक करने के इरादे से नहीं किया जाता है। अक्सर इस प्रकार का उपचार हड्डी में मेटास्टेसिस कर चुके कैंसर के कारण होने वाले दर्द को रोकने या ख़त्म करने के लिए दिया जाता है। सर्जरी के बजाय विकिरण: सर्जरी के बजाय विकिरण सीमित संख्या में कैंसर के खिलाफ एक प्रभावी उपकरण है। यदि कैंसर का जल्दी पता चल जाए तो उपचार सबसे प्रभावी होता है, जबकि यह अभी भी छोटा और गैर-मेटास्टेटिक है। यदि कैंसर का स्थान रोगी को गंभीर जोखिम के बिना सर्जरी करना कठिन या असंभव बना देता है तो सर्जरी के बजाय विकिरण चिकित्सा का उपयोग किया जा सकता है। ऐसे क्षेत्र में स्थित घावों के लिए सर्जरी पसंद का उपचार है जहां विकिरण चिकित्सा सर्जरी की तुलना में अधिक नुकसान पहुंचा सकती है। दोनों प्रक्रियाओं में लगने वाला समय भी बहुत अलग-अलग है। एक बार निदान हो जाने पर सर्जरी शीघ्रता से की जा सकती है; विकिरण चिकित्सा को पूरी तरह से प्रभावी होने में कई सप्ताह लग सकते हैं। दोनों प्रक्रियाओं के अपने पक्ष और विपक्ष हैं। विकिरण चिकित्सा का उपयोग अंगों को बचाने और/या सर्जरी और उसके जोखिमों से बचने के लिए किया जा सकता है। विकिरण ट्यूमर में तेजी से विभाजित होने वाली कोशिकाओं को नष्ट कर देता है, जबकि सर्जिकल प्रक्रियाओं में कुछ घातक कोशिकाएं छूट सकती हैं। हालाँकि, बड़े ट्यूमर द्रव्यमान में अक्सर केंद्र में ऑक्सीजन की कमी वाली कोशिकाएं होती हैं जो ट्यूमर की सतह के पास की कोशिकाओं की तरह तेजी से विभाजित नहीं होती हैं। चूँकि ये कोशिकाएँ तेजी से विभाजित नहीं होती हैं, इसलिए ये विकिरण चिकित्सा के प्रति उतनी संवेदनशील नहीं होती हैं। इस कारण से, बड़े ट्यूमर को केवल विकिरण से नष्ट नहीं किया जा सकता है। उपचार के दौरान अक्सर विकिरण और सर्जरी को जोड़ दिया जाता है। रेडियोथेरेपी की बेहतर समझ के लिए उपयोगी लेख: "> विकिरण थेरेपी 5 लक्षित थेरेपी के साथ त्वचा की प्रतिक्रियाएँ त्वचा की समस्याएँ डिस्पेनिया न्यूट्रोपेनिया तंत्रिका तंत्र संबंधी विकार मतली और उल्टी म्यूकोसाइटिस रजोनिवृत्ति के लक्षण संक्रमण हाइपरकैल्सीमिया पुरुष सेक्स हार्मोन सिरदर्द हाथ और पैर सिंड्रोम बालों का झड़ना (खालित्य) लिम्फेडेमा जलोदर फुफ्फुस शोफ अवसाद संज्ञानात्मक समस्याएं रक्तस्राव भूख न लगना बेचैनी और चिंता एनीमिया भ्रम प्रलाप निगलने में कठिनाई डिस्पैगिया मुंह में सूखापन ज़ेरोस्टोमिया न्यूरोपैथी विशिष्ट दुष्प्रभावों के लिए, निम्नलिखित लेख पढ़ें: "> दुष्प्रभाव36 विभिन्न दिशाओं में कोशिका मृत्यु का कारण बनता है। कुछ दवाएं प्राकृतिक यौगिक हैं जिन्हें विभिन्न पौधों में पहचाना गया है, जबकि अन्य प्रयोगशाला में बनाए गए रसायन हैं। कई अलग-अलग प्रकार की कीमोथेरेपी दवाओं का संक्षेप में नीचे वर्णन किया गया है। एंटीमेटाबोलाइट्स: दवाएं जो न्यूक्लियोटाइड्स, डीएनए के निर्माण खंडों सहित कोशिका के भीतर प्रमुख जैव अणुओं के निर्माण में हस्तक्षेप कर सकती हैं। ये कीमोथेराप्यूटिक एजेंट अंततः प्रतिकृति प्रक्रिया (डीएनए बेटी अणु का उत्पादन और इसलिए कोशिका विभाजन) में हस्तक्षेप करते हैं। एंटीमेटाबोलाइट्स के उदाहरणों में निम्नलिखित दवाएं शामिल हैं: फ्लुडारैबिन, 5-फ्लूरोरासिल, 6-थियोगुआनिन, फ्लोरोफुर, साइटाराबिन। जीनोटॉक्सिक दवाएं: दवाएं जो डीएनए को नुकसान पहुंचा सकती हैं। इस तरह की क्षति पहुंचाकर, ये एजेंट डीएनए प्रतिकृति और कोशिका विभाजन की प्रक्रिया में हस्तक्षेप करते हैं। दवाओं के उदाहरण के रूप में: बुसुल्फान, कारमस्टाइन, एपिरुबिसिन, इडारुबिसिन स्पिंडल अवरोधक (या माइटोसिस अवरोधक: इन कीमोथेराप्यूटिक एजेंटों का उद्देश्य साइटोस्केलेटन के घटकों के साथ बातचीत करके उचित कोशिका विभाजन को रोकना है जो एक कोशिका को दो में विभाजित करने की अनुमति देता है। एक उदाहरण दवा पैक्लिटैक्सेल है, जो प्रशांत यू की छाल से और अंग्रेजी यू (टैक्सस बकाटा) से अर्ध-सिंथेटिक रूप से प्राप्त की जाती है। दोनों दवाओं को अंतःशिरा इंजेक्शन की एक श्रृंखला के रूप में दिया जाता है। अन्य कीमोथेरेपी एजेंट: ये एजेंट अवरोध करना (उन तंत्रों द्वारा कोशिका विभाजन को धीमा करना जो ऊपर सूचीबद्ध तीन श्रेणियों में शामिल नहीं हैं। सामान्य कोशिकाएं अधिक प्रतिरोधी होती हैं (दवाओं के प्रति प्रतिरोधी क्योंकि वे अक्सर उन परिस्थितियों में विभाजित होना बंद कर देती हैं जो अनुकूल नहीं हैं। हालांकि, सभी सामान्य विभाजित कोशिकाएं कीमोथेरेपी दवाओं के प्रभाव से बच नहीं पाती हैं, जो इन दवाओं की विषाक्तता का प्रमाण है। कोशिका प्रकार जो तेजी से विभाजित होते हैं, जैसे कि अस्थि मज्जा और आंत की परत में, सबसे अधिक नुकसान होता है। सामान्य कोशिका मृत्यु कीमोथेरेपी के सामान्य दुष्प्रभावों में से एक है। निम्नलिखित लेखों में कीमोथेरेपी की बारीकियों के बारे में अधिक जानें: "> कीमोथेरेपी 6
- और गैर-छोटी कोशिका फेफड़ों का कैंसर। इन प्रकारों का निदान इस आधार पर किया जाता है कि कोशिकाएं माइक्रोस्कोप के नीचे कैसी दिखती हैं। स्थापित प्रकार के आधार पर, उपचार के विकल्प चुने जाते हैं। रोग के पूर्वानुमान और उत्तरजीविता को समझने के लिए, दोनों प्रकार के फेफड़ों के कैंसर के लिए 2014 के यूएस ओपन सोर्स आँकड़े एक साथ दिए गए हैं: नए मामले (अनुमान: 224,210 अनुमानित मौतें: 159,260 आइए दोनों प्रकारों, विशिष्टताओं और उपचार विकल्पों पर करीब से नज़र डालें। "> फेफड़े का कैंसर 4
- 2014 में अमेरिका में: नए मामले: 232,670 मौतें: 40,000 स्तन कैंसर अमेरिका में महिलाओं के बीच सबसे आम गैर-त्वचा कैंसर है (खुले स्रोतों का अनुमान है कि 2014 में अमेरिका में प्री-इनवेसिव बीमारी के 62,570 मामले (इन-सीटू, आक्रामक बीमारी के 232,670 नए मामले और 40,000 मौतें) होने की उम्मीद है। इस प्रकार, छह में से एक महिला में स्तन कैंसर का निदान किया गया है तुलना के लिए, यह अनुमान लगाया गया है कि 2014 में लगभग 72,330 अमेरिकी महिलाएं फेफड़ों के कैंसर से मर जाएंगी। पुरुष स्तन कैंसर (हां, हां, स्तन कैंसर के सभी मामलों और इस बीमारी से होने वाली मौतों का 1% है। व्यापक स्क्रीनिंग ने स्तन कैंसर की घटनाओं में वृद्धि की है और कैंसर का पता लगाने की विशेषताओं को बदल दिया है। सीटू (डीसीआईएस)। अमेरिका और ब्रिटेन में किए गए जनसंख्या अध्ययन से पता चलता है कि 1970 के बाद से डीसीआईएस और आक्रामक स्तन कैंसर की घटनाओं में वृद्धि हुई है। रजोनिवृत्ति के बाद हार्मोन थेरेपी और मैमोग्राफी का व्यापक उपयोग। पिछले दशक में, महिलाओं ने पोस्टमेनोपॉज़ल हार्मोन के उपयोग से परहेज किया है और स्तन कैंसर की घटनाओं में गिरावट आई है, लेकिन उस स्तर तक नहीं जिसे मैमोग्राफी के व्यापक उपयोग से हासिल किया जा सकता है। जोखिम और सुरक्षात्मक कारक बढ़ती उम्र स्तन कैंसर के लिए सबसे महत्वपूर्ण जोखिम कारक है। स्तन कैंसर के अन्य जोखिम कारकों में निम्नलिखित शामिल हैं: पारिवारिक इतिहास 0 अंतर्निहित आनुवंशिक संवेदनशीलता बीआरसीए1 और बीआरसीए2 जीन में लिंग उत्परिवर्तन, और अन्य स्तन कैंसर की संवेदनशीलता वाले जीन शराब का सेवन स्तन ऊतक घनत्व (मैमोग्राफिक) एस्ट्रोजन (अंतर्जात: 0 मासिक धर्म का इतिहास (मासिक धर्म की शुरुआत / देर से रजोनिवृत्ति 0 बच्चे के जन्म का कोई इतिहास नहीं 0 पहले जन्म के समय अधिक उम्र हार्मोनल थेरेपी का इतिहास: 0 संयोजन एस्ट्रोजन और प्रोजेस्टिन (एचआरटी मौखिक गर्भनिरोधक मोटापा की कमी) व्यायाम स्तन कैंसर का व्यक्तिगत इतिहास सौम्य स्तन रोग के प्रसार रूपों का व्यक्तिगत इतिहास स्तन का विकिरण जोखिम स्तन कैंसर से पीड़ित सभी महिलाओं में से 5% से 10% में बीआरसीए1 और बीआरसीए2 जीन में रोगाणु उत्परिवर्तन हो सकता है। अध्ययनों से पता चला है कि बीआरसीए1 और बीआरसीए2 में विशिष्ट उत्परिवर्तन मूल की यहूदी महिलाओं में अधिक आम हैं। जिन पुरुषों में बीआरसीए2 उत्परिवर्तन होता है उनमें भी स्तन कैंसर होने का खतरा बढ़ जाता है। बीआरसीए1 जीन और बीआरसीए2 दोनों में उत्परिवर्तन से डिम्बग्रंथि कैंसर या अन्य प्राथमिक कैंसर विकसित होने का खतरा बढ़ जाता है। एक बार बीआरसीए1 या बीआरसीए2 उत्परिवर्तन की पहचान हो जाने के बाद, परिवार के अन्य सदस्यों के लिए आनुवंशिक परामर्श और परीक्षण कराना वांछनीय है। स्तन कैंसर के विकास के जोखिम को कम करने के लिए सुरक्षात्मक कारकों और उपायों में निम्नलिखित शामिल हैं: एस्ट्रोजेन का उपयोग (विशेष रूप से हिस्टेरेक्टॉमी के बाद व्यायाम की आदत स्थापित करना प्रारंभिक गर्भावस्था स्तनपान चयनात्मक एस्ट्रोजन रिसेप्टर मॉड्यूलेटर (एसईआरएम) एरोमाटेज़ अवरोधक या निष्क्रियकर्ता मास्टेक्टॉमी के जोखिम को कम करना ओओफोरेक्टॉमी या अंडाशय हटाने के जोखिम को कम करना स्क्रीनिंग नैदानिक परीक्षणों से पता चला है कि मैमोग्राफी के साथ स्पर्शोन्मुख महिलाओं की स्क्रीनिंग, नैदानिक परीक्षण के साथ या उसके बिना निदान यदि स्तन कैंसर का संदेह है, तो रोगी को स्तन कैंसर का संदेह है। आमतौर पर निम्नलिखित चरणों से गुजरना चाहिए: निदान की पुष्टि रोग के चरण का मूल्यांकन चिकित्सा का विकल्प स्तन कैंसर के निदान के लिए निम्नलिखित परीक्षण और प्रक्रियाओं का उपयोग किया जाता है: मैमोग्राफी अल्ट्रासाउंड स्तन चुंबकीय अनुनाद इमेजिंग (एमआरआई, यदि चिकित्सकीय रूप से संकेत दिया गया है) बायोप्सी कॉन्ट्रालेटरल स्तन कैंसर घुसपैठ करने वाले फोकल कार्सिनोमा वाले रोगियों में द्विपक्षीय रोग कुछ हद तक आम है। निदान के बाद 10 वर्षों तक, कॉन्ट्रैटरल स्तन में प्राथमिक स्तन कैंसर का जोखिम 3% से 10% तक होता है, हालांकि अंतःस्रावी चिकित्सा इस जोखिम को कम कर सकती है। दूसरे स्तन कैंसर का विकास दीर्घकालिक पुनरावृत्ति के बढ़ते जोखिम से जुड़ा है। ऐसे मामले में जब 40 वर्ष की आयु से पहले बीआरसीए1/बीआरसीए2 जीन उत्परिवर्तन का निदान किया गया था, अगले 25 वर्षों में दूसरे स्तन कैंसर का खतरा लगभग 50% तक पहुंच जाता है। स्तन कैंसर से पीड़ित मरीजों को समकालिक रोग से बचने के लिए निदान के समय द्विपक्षीय मैमोग्राफी करानी चाहिए। गर्भनिरोधक स्तन कैंसर की जांच और स्तन संरक्षण चिकित्सा से उपचारित महिलाओं की निगरानी में एमआरआई की भूमिका लगातार विकसित हो रही है। क्योंकि संभावित बीमारी की मैमोग्राफी पर बढ़ी हुई पहचान दर का प्रदर्शन किया गया है, यादृच्छिक नियंत्रित डेटा की कमी के बावजूद, सहायक स्क्रीनिंग के लिए एमआरआई का चयनात्मक उपयोग अधिक बार हो रहा है। क्योंकि एमआरआई-सकारात्मक निष्कर्षों में से केवल 25% घातकता का प्रतिनिधित्व करते हैं, उपचार शुरू करने से पहले पैथोलॉजिकल पुष्टि की सिफारिश की जाती है। रोग का पता लगाने की दर में इस वृद्धि से उपचार के परिणामों में सुधार होगा या नहीं यह अज्ञात है। पूर्वानुमानित कारक स्तन कैंसर का इलाज आमतौर पर सर्जरी, विकिरण चिकित्सा, कीमोथेरेपी और हार्मोन थेरेपी के विभिन्न संयोजनों से किया जाता है। थेरेपी के निष्कर्ष और चयन निम्नलिखित नैदानिक और रोगविज्ञानी विशेषताओं (पारंपरिक ऊतक विज्ञान और इम्यूनोहिस्टोकेमिस्ट्री के आधार पर) से प्रभावित हो सकते हैं: रोगी की क्लाइमेक्टेरिक स्थिति। रोग का चरण। प्राथमिक ट्यूमर का ग्रेड। एस्ट्रोजेन रिसेप्टर्स (ईआर और प्रोजेस्टेरोन रिसेप्टर्स (पीआर। हिस्टोलॉजिकल प्रकार) की स्थिति के आधार पर ट्यूमर की स्थिति। स्तन कैंसर को विभिन्न हिस्टोलॉजिकल प्रकारों में वर्गीकृत किया जाता है, जिनमें से कुछ पूर्वानुमानित मूल्य के होते हैं। कैंसर में आणविक प्रोफाइलिंग का उपयोग स्तन कैंसर में निम्नलिखित शामिल हैं: ईआर और पीआर स्थिति परीक्षण एचईआर2/न्यू रिसेप्टर स्थिति परीक्षण इन परिणामों के आधार पर, स्तन कैंसर को इस प्रकार वर्गीकृत किया गया है: हार्मोन रिसेप्टर सकारात्मक एचईआर2 सकारात्मक ट्रिपल नकारात्मक (ईआर, पीआर, और एचईआर2/न्यू नकारात्मक हालांकि कुछ दुर्लभ विरासत में मिले उत्परिवर्तन, जैसे बीआरसीए1 और बीआरसीए2, उत्परिवर्ती धनायन के वाहक के लिए स्तन कैंसर का संकेत देते हैं, हालांकि, बीआरसीए1 /बीआरसीए2 उत्परिवर्तन के वाहक पर पूर्वानुमानित डेटा विरोधाभासी हैं; इन महिलाओं में दूसरा स्तन कैंसर विकसित होने का खतरा अधिक होता है। लेकिन ये निश्चित नहीं है कि ऐसा हो पाएगा. हार्मोन रिप्लेसमेंट थेरेपी सावधानीपूर्वक विचार करने के बाद, गंभीर लक्षणों वाले रोगियों का इलाज हार्मोन रिप्लेसमेंट थेरेपी से किया जा सकता है। अनुवर्ती चरण I, चरण II, या चरण III स्तन कैंसर के लिए प्राथमिक उपचार पूरा होने के बाद अनुवर्ती कार्रवाई की आवृत्ति और स्क्रीनिंग की उपयुक्तता विवादास्पद बनी हुई है। यादृच्छिक परीक्षणों के साक्ष्य से पता चलता है कि हड्डी के स्कैन, लीवर अल्ट्रासाउंड, छाती के एक्स-रे और लीवर के कार्य के लिए रक्त परीक्षण के साथ समय-समय पर अनुवर्ती कार्रवाई से नियमित शारीरिक परीक्षाओं की तुलना में जीवित रहने या जीवन की गुणवत्ता में बिल्कुल भी सुधार नहीं होता है। यहां तक कि जब ये परीक्षण रोग की पुनरावृत्ति का शीघ्र पता लगाने की अनुमति देते हैं, तो इससे रोगियों के जीवित रहने पर कोई प्रभाव नहीं पड़ता है। इन आंकड़ों के आधार पर, चरण I से III स्तन कैंसर के इलाज वाले स्पर्शोन्मुख रोगियों के लिए सीमित अनुवर्ती और वार्षिक मैमोग्राफी एक स्वीकार्य अनुवर्ती हो सकती है। लेखों में अधिक जानकारी: "> स्तन कैंसर5
- , मूत्रवाहिनी और समीपस्थ मूत्रमार्ग एक विशेष श्लेष्मा झिल्ली से पंक्तिबद्ध होते हैं जिन्हें ट्रांज़िशनल एपिथेलियम (जिसे यूरोथेलियम भी कहा जाता है। मूत्राशय, वृक्क श्रोणि, मूत्रवाहिनी और समीपस्थ मूत्रमार्ग में बनने वाले अधिकांश कैंसर संक्रमणकालीन कोशिका कार्सिनोमा होते हैं (जिन्हें यूरोटेलियल कार्सिनोमा भी कहा जाता है, जो संक्रमणकालीन उपकला से प्राप्त होते हैं। मूत्राशय के संक्रमणकालीन कोशिका कार्सिनोमा निम्न श्रेणी या उच्च श्रेणी के हो सकते हैं: निम्न श्रेणी का मूत्राशय कैंसर अक्सर होता है। उपचार के बाद मूत्राशय में जमाव हो जाता है, लेकिन शायद ही कभी यह मूत्राशय की मांसपेशियों की दीवारों पर आक्रमण करता है या शरीर के अन्य भागों में फैलता है। निम्न-श्रेणी के मूत्राशय के कैंसर से मरीज़ शायद ही कभी मरते हैं। ललित-श्रेणी का मूत्राशय का कैंसर आमतौर पर मूत्राशय में फिर से उभरता है, और इसमें मूत्राशय की मांसपेशियों की दीवारों पर आक्रमण करने और शरीर के अन्य भागों में फैलने की एक मजबूत प्रवृत्ति होती है। उच्च श्रेणी के मूत्राशय के कैंसर को निम्न-श्रेणी के मूत्राशय के कैंसर की तुलना में अधिक आक्रामक माना जाता है और इसके परिणामस्वरूप मृत्यु होने की अधिक संभावना होती है। मूत्राशय कैंसर से होने वाली लगभग सभी मौतें अत्यधिक घातक कैंसर का परिणाम होती हैं। मूत्राशय के कैंसर को मांसपेशी-आक्रामक और गैर-मांसपेशी-आक्रामक रोगों में भी विभाजित किया जाता है, जो मांसपेशियों की परत पर आक्रमण के आधार पर होता है (जिसे डिट्रसर भी कहा जाता है, जो मूत्राशय की मांसपेशियों की दीवार में गहराई में स्थित होता है। मांसपेशी-आक्रामक रोग के शरीर के अन्य भागों में फैलने की अधिक संभावना होती है और आमतौर पर मूत्राशय को हटाकर या विकिरण और कीमोथेरेपी के साथ मूत्राशय के उपचार द्वारा इलाज किया जाता है। जैसा कि ऊपर उल्लेख किया गया है, उच्च स्तर की घातकता वाला कैंसर मांसपेशी आक्रामक कैंसर होने की अधिक संभावना है। निम्न श्रेणी के कैंसर की तुलना में। इस प्रकार, मांसपेशी आक्रामक कैंसर को आम तौर पर गैर मांसपेशी आक्रामक कैंसर की तुलना में अधिक आक्रामक माना जाता है। गैर मांसपेशी आक्रामक बीमारी का इलाज अक्सर ट्रांसयूरथ्रल दृष्टिकोण का उपयोग करके ट्यूमर को हटाकर किया जा सकता है, और कभी-कभी कीमोथेरेपी या अन्य प्रक्रियाएं जिनमें कैंसर से लड़ने में मदद करने के लिए कैथेटर के माध्यम से मूत्राशय गुहा में दवा इंजेक्ट की जाती है। पुरानी सूजन की स्थितियों में मूत्राशय में कैंसर हो सकता है, जैसे परजीवी हेमेटोबियम शिस्टोसोमा के कारण मूत्राशय में संक्रमण, या स्क्वैमस मेटाप्लासिया के परिणामस्वरूप; स्क्वैमस सेल ब्लैडर कैंसर की घटना क्रोनिकली इंफ्लेमेटरी स्थितियों में अन्य की तुलना में अधिक होती है। संक्रमणकालीन कार्सिनोमा और स्क्वैमस सेल कार्सिनोमा के अलावा, मूत्राशय में एडेनोकार्सिनोमा, छोटे सेल कार्सिनोमा और सार्कोमा बन सकते हैं। संयुक्त राज्य अमेरिका में, संक्रमणकालीन कोशिका कार्सिनोमा विशाल बहुमत (मूत्राशय कैंसर के 90% से अधिक) के लिए जिम्मेदार है। हालांकि, संक्रमणकालीन कार्सिनोमा की एक बड़ी संख्या में स्क्वैमस या अन्य भेदभाव के क्षेत्र होते हैं। कार्सिनोजेनेसिस और जोखिम कारक मूत्राशय के कैंसर की घटना और प्रगति पर कार्सिनोजेन्स के प्रभाव के मजबूत सबूत हैं। सिगरेट धूम्रपान मूत्राशय के कैंसर के लिए सबसे आम जोखिम कारक है। यह अनुमान लगाया गया है कि सभी मूत्राशय कैंसर में से आधे धूम्रपान के कारण होते हैं और धूम्रपान से मूत्र विकसित होने का खतरा बढ़ जाता है। कैंसर। कम कार्यात्मक एन-एसिटाइलट्रांसफेरेज़-2 बहुरूपता (धीमे एसिटिलेटर के रूप में जाना जाता है) वाले धूम्रपान करने वालों में अन्य धूम्रपान करने वालों की तुलना में मूत्राशय कैंसर विकसित होने का अधिक खतरा होता है, जाहिर तौर पर कार्सिनोजेन्स को डिटॉक्सीफाई करने की कम क्षमता के कारण। और टायर उद्योग में रबर; कलाकारों के बीच; चमड़ा प्रसंस्करण उद्योगों के श्रमिक; मोची; और एल्यूमीनियम-, लोहा- और इस्पात श्रमिक। मूत्राशय कार्सिनोजेनेसिस से जुड़े विशिष्ट रसायनों में बीटा-नैफ्थाइलमाइन, 4-एमिनोबिफेनिल और बेंज़िडाइन शामिल हैं। हालाँकि ये रसायन अब आम तौर पर पश्चिमी देशों में प्रतिबंधित हैं, कई अन्य रसायन जो अभी भी उपयोग में हैं, उनमें भी मूत्राशय के कैंसर को ट्रिगर करने का संदेह है। कीमोथेरेपी एजेंट साइक्लोफॉस्फेमाइड के संपर्क में आने से भी मूत्राशय के कैंसर का खतरा बढ़ जाता है। क्रोनिक मूत्र पथ संक्रमण और परजीवी एस हेमेटोबियम के कारण होने वाले संक्रमण भी मूत्राशय के कैंसर और अक्सर स्क्वैमस सेल कार्सिनोमा के बढ़ते जोखिम से जुड़े होते हैं। ऐसा माना जाता है कि इन परिस्थितियों में पुरानी सूजन कार्सिनोजेनेसिस की प्रक्रिया में महत्वपूर्ण भूमिका निभाती है। नैदानिक विशेषताएं मूत्राशय का कैंसर आमतौर पर साधारण या सूक्ष्म रक्तमेह के साथ प्रकट होता है। कम सामान्यतः, मरीज़ बार-बार पेशाब आने, नॉक्टुरिया और डिसुरिया की शिकायत कर सकते हैं, ये लक्षण कार्सिनोमा के रोगियों में अधिक आम हैं। ऊपरी मूत्र पथ के यूरोटेलियल कैंसर के मरीजों को ट्यूमर की रुकावट के कारण दर्द का अनुभव हो सकता है। यह ध्यान रखना महत्वपूर्ण है कि यूरोटेलियल कार्सिनोमा अक्सर मल्टीफोकल होता है, यदि ट्यूमर पाया जाता है तो पूरे यूरोटेलियम की जांच की आवश्यकता होती है। मूत्राशय के कैंसर के रोगियों में, निदान और अनुवर्ती कार्रवाई के लिए ऊपरी मूत्र पथ की इमेजिंग आवश्यक है। इसे यूरेथ्रोस्कोपी, सिस्टोस्कोपी में रेट्रोग्रेड पाइलोग्राम, अंतःशिरा पाइलोग्राम, या कंप्यूटेड टोमोग्राफी (सीटी यूरोग्राम) के साथ प्राप्त किया जा सकता है। इसके अलावा, टीसीसी वाले रोगियों में मूत्राशय के कैंसर के विकास का उच्च जोखिम होता है; इन रोगियों को समय-समय पर सिस्टोस्कोपी और विपरीत ऊपरी मूत्र पथ के अवलोकन की आवश्यकता होती है। निदान जब मूत्राशय के कैंसर का संदेह होता है, तो सिस्टोस्कोपी सबसे उपयोगी नैदानिक परीक्षण है। रेडियोलॉजिकल परीक्षा जैसे कि कंप्यूटेड टोमोग्राफी या अल्ट्रासाउंड में मूत्राशय के कैंसर का पता लगाने में उपयोगी होने के लिए पर्याप्त संवेदनशीलता नहीं होती है। सिस्ट यदि सिस्टोस्कोपी के दौरान कैंसर पाया जाता है, तो रोगी को आमतौर पर एनेस्थीसिया के तहत एक द्वि-मैनुअल परीक्षा के लिए निर्धारित किया जाता है और ऑपरेटिंग रूम में सिस्टोस्कोपी दोहराई जाती है, ताकि ट्यूमर का ट्रांसयूरथ्रल रिसेक्शन और/या बायोप्सी की जा सके। उत्तरजीविता मूत्राशय के कैंसर से मरने वाले मरीजों में लगभग हमेशा मूत्राशय से अन्य अंगों में मेटास्टेसिस होता है। निम्न-श्रेणी का मूत्राशय कैंसर शायद ही कभी मूत्राशय की मांसपेशियों की दीवार में बढ़ता है और शायद ही कभी मेटास्टेसिस करता है, इसलिए निम्न-श्रेणी (स्टेज I मूत्राशय कैंसर) वाले मरीज़ शायद ही कभी कैंसर से मरते हैं। हालांकि, उन्हें कई पुनरावृत्तियों का अनुभव हो सकता है, जिन्हें हटाने की आवश्यकता होती है। मूत्राशय के कैंसर से लगभग सभी मौतें उच्च-श्रेणी की बीमारी वाले रोगियों में होती हैं, जिनमें मूत्र की मांसपेशियों की दीवारों में गहराई से आक्रमण करने की बहुत अधिक क्षमता होती है, नव निदान मूत्राशय कैंसर वाले लगभग 70% से 80% रोगियों में सतही मूत्राशय के ट्यूमर होते हैं (यानी)। । चरण टा, टीआईएस, या टी1)। इन रोगियों का पूर्वानुमान काफी हद तक ट्यूमर के ग्रेड पर निर्भर करता है। ज्यादातर मामलों में आक्रामक मूत्राशय के कैंसर के ठीक होने की संभावना अधिक होती है, और मांसपेशियों में आक्रामक बीमारी के साथ भी, कभी-कभी रोगी को ठीक किया जा सकता है। अध्ययनों से पता चला है कि दूर के मेटास्टेस वाले कुछ रोगियों में, ऑन्कोलॉजिस्ट ने संयोजन कीमोथेरेपी आहार के साथ उपचार के बाद दीर्घकालिक पूर्ण प्रतिक्रिया प्राप्त की है, हालांकि इनमें से अधिकांश रोगियों में, मेटास्टेस उनके लिम्फ नोड्स तक सीमित हैं। माध्यमिक मूत्राशय कैंसर मूत्राशय कैंसर दोबारा होने की प्रवृत्ति रखता है, भले ही निदान के समय यह आक्रामक न हो। इसलिए, मूत्राशय के कैंसर का निदान होने के बाद मूत्र पथ की निगरानी करना मानक अभ्यास है। हालाँकि, यह आकलन करने के लिए अभी तक अध्ययन नहीं किया गया है कि क्या अवलोकन प्रगति दर, उत्तरजीविता या जीवन की गुणवत्ता को प्रभावित करता है; हालाँकि इष्टतम अनुवर्ती कार्यक्रम निर्धारित करने के लिए नैदानिक परीक्षण होते हैं। माना जाता है कि यूरोटेलियल कार्सिनोमा एक तथाकथित क्षेत्र दोष को दर्शाता है जिसमें कैंसर आनुवंशिक उत्परिवर्तन के कारण होता है जो रोगी के मूत्राशय या पूरे यूरोटेलियम में व्यापक रूप से मौजूद होता है। इस प्रकार, जिन लोगों को मूत्राशय का ट्यूमर होता है, उसके बाद अक्सर मूत्राशय में ट्यूमर बना रहता है, अक्सर प्राथमिक ट्यूमर के अलावा अन्य स्थानों पर भी। इसी तरह, लेकिन कम बार, वे ऊपरी मूत्र पथ (यानी, गुर्दे की श्रोणि या मूत्रवाहिनी में) में ट्यूमर विकसित कर सकते हैं। पुनरावृत्ति के इन पैटर्न के लिए एक वैकल्पिक स्पष्टीकरण यह है कि कैंसर कोशिकाएं जो ट्यूमर को हटाने पर नष्ट हो जाती हैं, उन्हें यूरोथेलियम में कहीं और फिर से प्रत्यारोपित किया जा सकता है। इस दूसरे सिद्धांत का समर्थन करते हुए यह है कि मूल कैंसर से पीछे की तुलना में ट्यूमर के दोबारा होने की अधिक संभावना है। ऊपरी मूत्र पथ के कैंसर की मूत्राशय में पुनरावृत्ति होने की अधिक संभावना है, जबकि मूत्राशय का कैंसर ऊपरी मूत्र पथ में पुन: उत्पन्न होगा। . शेष निम्नलिखित लेखों में: "> मूत्राशय कैंसर4
- और मेटास्टैटिक रोग का खतरा बढ़ जाता है। विभेदन की डिग्री (ट्यूमर के विकास के चरण का निर्धारण इस बीमारी के प्राकृतिक इतिहास और उपचार की पसंद पर एक महत्वपूर्ण प्रभाव डालता है। एस्ट्रोजेन के लंबे समय तक, निर्विरोध संपर्क (बढ़े हुए स्तर) के कारण एंडोमेट्रियल कैंसर की घटनाओं में वृद्धि पाई गई है। इसके विपरीत, संयोजन चिकित्सा (एस्ट्रोजन + प्रोजेस्टेरोन) विशिष्ट एस्ट्रोजेन के प्रतिरोध की कमी से जुड़े एंडोमेट्रियल कैंसर के खतरे में वृद्धि को रोकती है। निदान प्राप्त करना सबसे अच्छा क्षण नहीं है। हालांकि, आपको पता होना चाहिए कि एंडोमेट्रियल परीक्षण कैंसर एक इलाज योग्य बीमारी है। लक्षण और सब कुछ ठीक हो जाएगा! कुछ रोगियों में, एटिपिया के साथ जटिल हाइपरप्लासिया का पिछला इतिहास एंडोमेट्रियल कैंसर "एक्टिवेटर" में भूमिका निभा सकता है। टैमोक्सीफेन के साथ स्तन कैंसर के उपचार के साथ एंडोमेट्रियल कैंसर की घटनाओं में भी वृद्धि पाई गई है। शोधकर्ताओं के अनुसार, यह एंडोमेट्रियम पर टैमोक्सीफेन के एस्ट्रोजेनिक प्रभाव के कारण है। इस वृद्धि के कारण, जिन रोगियों को टैमोक्सीफेन थेरेपी निर्धारित की जाती है, उन्हें आवश्यक रूप से नियमित रूप से गुजरना चाहिए। पैल्विक परीक्षण और किसी भी रोग संबंधी गर्भाशय रक्तस्राव पर ध्यान देना चाहिए। हिस्टोपैथोलॉजी घातक एंडोमेट्रियल कैंसर कोशिकाओं का प्रसार आंशिक रूप से सेलुलर भेदभाव की डिग्री पर निर्भर करता है। अच्छी तरह से विभेदित ट्यूमर गर्भाशय म्यूकोसा की सतह तक अपने प्रसार को सीमित करते हैं; मायोमेट्रियल विस्तार कम बार होता है। खराब विभेदित ट्यूमर वाले रोगियों में, मायोमेट्रियम पर आक्रमण बहुत अधिक आम है। मायोमेट्रियम का आक्रमण अक्सर लिम्फ नोड की भागीदारी और दूर के मेटास्टेसिस का अग्रदूत होता है, और अक्सर भेदभाव की डिग्री पर निर्भर करता है। मेटास्टेसिस सामान्य तरीके से होता है। पेल्विक और पैरा-महाधमनी नोड्स तक फैलना आम है। जब दूर के मेटास्टेस होते हैं, तो यह सबसे अधिक बार होता है: फेफड़े। वंक्षण और सुप्राक्लेविकुलर नोड्स। जिगर। हड्डियाँ। दिमाग। प्रजनन नलिका। रोगसूचक कारक एक अन्य कारक जो एक्टोपिक और गांठदार ट्यूमर के प्रसार से जुड़ा है, वह है हिस्टोलॉजिकल परीक्षा में केशिका-लसीका स्थान की भागीदारी। तीन नैदानिक चरण I पूर्वानुमानित समूहों को सावधानीपूर्वक ऑपरेटिव स्टेजिंग द्वारा संभव बनाया गया था। स्टेज 1 ट्यूमर वाले मरीजों में केवल एंडोमेट्रियम शामिल है और इंट्रापेरिटोनियल बीमारी (यानी एडनेक्सल एक्सटेंशन) का कोई सबूत नहीं है, वे कम जोखिम में हैं (">एंडोमेट्रियल कैंसर 4
आधुनिक जीवन की आपाधापी में, हर कोई डॉक्टर के पास जाने के लिए कुछ खाली घंटे नहीं निकाल सकता, भले ही वे अस्वस्थ महसूस करें। हमारी साइट कई बीमारियों के कारणों, उनकी नैदानिक अभिव्यक्तियों, निदान और उपचार के तरीकों के बारे में व्यापक और विश्वसनीय जानकारी से भरी हुई है।
मुख्य पृष्ठ पर एक सुविधाजनक वर्णमाला सूचकांक आपको रुचि की बीमारी, इसके विकास के कारणों और पाठ्यक्रम की विशेषताओं के बारे में पूरी जानकारी तुरंत प्राप्त करने में मदद करेगा।
- निदान
यह अनुभाग आपको उन सामान्य निदान विकल्पों के बारे में बताएगा जिनका उपयोग रोगी परीक्षाओं के लिए किया जाता है। प्रक्रियाओं का वर्णन करने के अलावा, इस अनुभाग में प्रस्तुत लेख आपको प्राप्त परिणामों की प्रतिलेखों से परिचित होने में मदद करेंगे, यह पता लगाएंगे कि ये या वे संकेतक क्या जानकारी रखते हैं।
रूब्रिक उन लोगों के लिए भी उपयोगी होगा जो एक निश्चित निदान प्रक्रिया से गुजरने वाले हैं, क्योंकि यह अध्ययन की तैयारी में मदद करेगा, जिससे संभावित त्रुटियों से बचा जा सकेगा।
- उपचार के तरीके
उपचार विधियों पर अनुभाग आपको ऑन्कोलॉजिकल प्रकृति की बीमारियों, गर्भाशय कैंसर के विकास के लिए वंशानुगत प्रवृत्ति, श्रवण हानि, साथ ही गंभीर पाठ्यक्रम और गंभीर परिणामों की विशेषता वाले कई अन्य रोगों के इलाज के लिए उपयोग की जाने वाली नवीन चिकित्सा के विकल्पों के बारे में विस्तार से परिचित होने में मदद करेगा।
- प्राथमिक चिकित्सा
यह प्रत्येक व्यक्ति के लिए विशेष रूप से उपयोगी रूब्रिक है। यह अनुभाग उन गैर-मानक स्थितियों के विकल्पों का विस्तार से वर्णन करता है जिनका सामना कोई भी कर सकता है। शीतदंश की स्थिति में क्या करें, डूबने, बेहोश होने या फ्रैक्चर होने पर कैसे मदद करें, सांप के काटने की स्थिति में पीड़ित को योग्य चिकित्सा सहायता प्रदान करने से पहले क्या कार्रवाई करें, कई अन्य आपातकालीन स्थितियों पर विचार किया जाता है। प्राथमिक चिकित्सा कौशल का ज्ञान आपको त्वरित और उद्देश्यपूर्ण ढंग से कार्य करने में मदद करेगा, और संभावित भ्रम और देरी को रोकेगा।
- बीमारी
सभी के लिए सबसे व्यापक और उपयोगी रोग संबंधी अनुभाग है। इस अनुभाग की समीक्षा करने के बाद, आप विभिन्न प्रकार की बीमारियों की पहली नैदानिक अभिव्यक्तियों, निदान विधियों, उपचार के मानक और अनूठे तरीकों के बारे में जानेंगे। साथ ही यहां आप कई ज्ञात बीमारियों से बचाव के उपयोगी टिप्स भी पा सकते हैं।
- मिश्रित
यह अनुभाग भी कई लोगों के लिए उपयोगी होगा. यह अनुभाग आपको अक्सर पूछे जाने वाले प्रश्नों के उत्तर पाने में मदद करेगा। उदाहरण के लिए: एलर्जी से पीड़ित किसी व्यक्ति के लिए यात्रा कैसे करें? फ्रैक्चर कैसे ठीक होते हैं, क्या इन प्रक्रियाओं को तेज किया जा सकता है? क्या वेप्स आज इतने लोकप्रिय हैं कि स्वास्थ्य के लिए हानिकारक हैं? हमारे इस अनुभाग के लेख इनके साथ-साथ कई अन्य प्रश्नों के पूर्ण और विस्तृत उत्तर दे सकते हैं।
हमारी साइट युवा माताओं के लिए भी उपयोगी होगी, क्योंकि यह टीकाकरण के लाभ और हानि के बारे में जानकारी प्रदान करती है, प्रतिरक्षा प्रणाली को मजबूत करने और बच्चे को सख्त करने के लिए किन तरीकों का इस्तेमाल किया जा सकता है, बच्चे के व्यवहार में बदलाव के कौन से लक्षण बीमारियों और विकृति के विकास के प्रारंभिक चरणों का संकेत दे सकते हैं? एक शब्द में, हमारे बहुमुखी संसाधन पर, प्रत्येक आगंतुक के पास उस प्रश्न का उत्तर होता है जिसे वे तलाश रहे हैं।
बेशक, हमारी वेबसाइट जैसे सुविधाजनक सहायक की उपस्थिति डॉक्टर के पास पूरी यात्रा की जगह नहीं ले सकती। यह याद रखना महत्वपूर्ण है कि यदि आप अस्वस्थ महसूस करते हैं, तो स्व-दवा से स्थिति में महत्वपूर्ण गिरावट और मौजूदा बीमारियों की प्रगति हो सकती है।
हमारा पोर्टल केवल शैक्षिक और सूचनात्मक उद्देश्यों के लिए है, लेकिन कार्रवाई के लिए मार्गदर्शक नहीं है।
प्रस्तावित उपचार विधियों को स्वयं पर आज़माने से पहले किसी योग्य विशेषज्ञ की सलाह लेना ज़रूरी है।हाइपरथर्मिया को अब बार-बार होने वाले स्तन कैंसर के उपचार के लिए एनसीसीएन क्लिनिकल प्रैक्टिस दिशानिर्देशों में शामिल किया गया है। डॉ. अर्कडी बेसेन्टिन (इज़राइल, तेल अवीव) स्तन कैंसर के रोगियों के उपचार में इस आधुनिक तकनीक का सफलतापूर्वक उपयोग करते हैं।
इस समीक्षा का उद्देश्य- स्तन कैंसर के उपचार के लिए विकिरण चिकित्सा और/या कीमोथेरेपी के संयोजन में हाइपरथर्मिया के उपयोग पर पिछले दशकों में किए गए नैदानिक परीक्षण प्रस्तुत करना। यह लेख एनसीसीएन के मूल सिद्धांतों का विवरण देता है, जिसमें अब स्तन कैंसर में आवर्ती त्वचा घावों के नैदानिक प्रबंधन के लिए हाइपरथर्मिया का उपयोग शामिल है, जो ट्यूमर पुनरावृत्ति के स्थानीय नियंत्रण में हाइपरथर्मिया की संभावित सकारात्मक भूमिका का समर्थन करता है।
हाइपरथर्मिया - अत्यधिक गर्मी, शरीर के तापमान में वृद्धि के साथ मनुष्यों और जानवरों के शरीर में अतिरिक्त गर्मी का संचय, बाहरी कारकों के कारण होता है जो बाहरी वातावरण में गर्मी हस्तांतरण में बाधा डालते हैं या बाहर से गर्मी के प्रवाह को बढ़ाते हैं। (विकिपीडिया)
परिचय
यह कैंसर के सबसे आम प्रकारों में से एक है और एक गंभीर समस्या है, क्योंकि हर साल इस बीमारी के मामलों की संख्या बढ़ती जा रही है। हालाँकि वर्तमान में स्तन कैंसर का शीघ्र पता लगाना संभव है, लेकिन रोग के प्रारंभिक चरण में 30% रोगियों में आगे पुनरावृत्ति होने की संभावना होती है। स्थानीय रूप से उन्नत स्तन कैंसर के रोगियों के उपचार में कीमोथेरेपी के बाद रेडिकल मास्टेक्टॉमी (यह एक ऑपरेशन है जिसमें स्तन का पूर्ण या आंशिक विच्छेदन शामिल होता है) और विकिरण थेरेपी और कुछ मामलों में, हार्मोनल थेरेपी शामिल होती है। यद्यपि यह संयोजन चिकित्सा अभी भी स्थानीय ट्यूमर नियंत्रण के मामले में इष्टतम विकल्प है, फिर भी बेहतर नैदानिक परिणाम के लिए नए उपचारों का चयन करने की आवश्यकता है।
नेशनल एंटीऑक्सीडेंट नेटवर्क 2013 (एनसीसीएन) के सिद्धांतों के अनुसार, बार-बार होने वाले स्तन कैंसर के इलाज के लिए हाइपरथर्मिया को नैदानिक अभ्यास में शामिल किया गया है। हाइपरथर्मिया का लक्ष्य ट्यूमर के तापमान को 42-45 डिग्री सेल्सियस तक बढ़ाना है। ट्यूमर के स्थान के आधार पर हाइपरथर्मिया लगाने के विभिन्न तरीके हैं। स्तन कैंसर में 5 सेमी से कम गहराई वाले ट्यूमर के लिए, सतही हाइपरथर्मिया का मुख्य रूप से उपयोग किया जाता है। रेडियोथेरेपी और/या कीमोथेरेपी के साथ संयोजन में सतही हाइपरथर्मिया अकेले रेडियोथेरेपी या कीमोथेरेपी की तुलना में अधिक प्रभावी साबित हुआ, क्योंकि रेडियोथेरेपी और हाइपरथर्मिया की क्रिया के तंत्र एक दूसरे के पूरक हैं। इसके अलावा, हाइपरथर्मिया का सही नैदानिक अनुप्रयोग बहुत महत्वपूर्ण है, क्योंकि थर्मल पैरामीटर, जैसे थर्मोथेरेपी के दौरान न्यूनतम या अधिकतम ट्यूमर तापमान, उपचार के नैदानिक परिणाम को प्रभावित करते हैं।
इस समीक्षा में शामिल सभी परीक्षण मेडलाइन (मेडलर्स ऑनलाइन मेडलर्स (मेडिकल लिटरेचर एनालिसिस एंड रिट्रीवल सिस्टम) का संक्षिप्त रूप) से प्राप्त किए गए थे, जो दुनिया में प्रकाशित चिकित्सा जानकारी का सबसे बड़ा डेटाबेस है, जो सभी वैश्विक प्रकाशनों का लगभग 75 प्रतिशत कवर करता है।) और 1987 से वर्तमान तक प्रकाशित किए गए हैं।
ये परीक्षण दर्शाते हैं कि रेडिएशन थेरेपी और/या कीमोथेरेपी के साथ हाइपरथर्मिया स्तन कैंसर से पीड़ित रोगियों को कैसे प्रभावित करता है और इस संयोजन उपचार के लाभों का पता लगाता है। प्रत्येक अध्ययन में प्राप्त डेटा प्राथमिक बीमारी या स्तन कैंसर की पुनरावृत्ति वाले रोगियों की संख्या और उनके इलाज के लिए इस्तेमाल की जाने वाली चिकित्सीय विधियों को दर्शाता है। मूल्यांकन किए गए मुख्य पैरामीटर चिकित्सा के प्रति प्रतिक्रिया की दर, पूर्ण और आंशिक प्रतिक्रिया दर, स्थानीय ट्यूमर नियंत्रण और जीवित रहने की दर हैं। अंत में, अतिताप-प्रेरित विषाक्तता पर विचार किया जाता है।
परिणाम और चर्चा
सतही ट्यूमर के लिए थर्मोरेडियोथेरेपी (आरटीएचटी) बनाम रेडियोथेरेपी के तुलनात्मक अध्ययन के पहले नैदानिक परिणाम 1990 से पहले प्रकाशित किए गए थे। 1987 में, एक अध्ययन के नतीजे प्रकाशित हुए थे जिसमें सतही आवर्ती घातकताओं वाले रोगियों को स्थानीय हाइपरथर्मिया (915 या 2450 मेगाहर्ट्ज) के साथ या उसके बिना रेडियोथेरेपी की कम खुराक प्राप्त हुई थी। अधिकांश ट्यूमर (53%) स्तन एडेनोकार्सिनोमा थे। संयोजन समूह में पूर्ण और आंशिक प्रतिक्रिया दर अधिक थी, जिससे पता चलता है कि कम खुराक विकिरण के साथ संयुक्त हाइपरथर्मिया सतही ट्यूमर पुनरावृत्ति के उपचार में उपयोगी हो सकता है, खासकर उन मामलों में जहां पहले विकिरण चिकित्सा की उच्च खुराक का उपयोग किया गया है। उपचार में, कक्षा 3 विषाक्तता (बुलबुले/गीली त्वचा के साथ सतह से कोशिकाओं का विलुप्त होना) क्रमशः 21.2 और 4.2% थी, कक्षा 4 विषाक्तता (छोटी नेक्रोसिस (मरना) या अल्सरेशन/बड़े पैमाने पर अल्सरेशन) क्रमशः 24.2 और 8.3% थी। क्रमशः 3 रोगियों और 1 रोगी में चमड़े के नीचे के वसा ऊतक परिगलन (ग्रेड 4) की सूचना मिली थी।
एक अध्ययन आयोजित किया गया जिसने संयुक्त उपचार की प्रभावशीलता को भी साबित किया:बार-बार होने वाले स्तन कार्सिनोमा वाले 35 रोगियों को विकिरण चिकित्सा के अलावा हाइपरथर्मिया प्राप्त हुआ, जो विकिरण के 30 मिनट के भीतर किया गया था। अकेले रेडियोथेरेपी प्राप्त करने वाले 9 रोगियों और आरटीटी प्राप्त करने वाले 9 रोगियों के बीच तुलना से पता चला कि उपचार प्रतिक्रिया दर क्रमशः 33.3% (3/9) और 77.7% (7/9) थी। अतिताप को शरीर द्वारा गंभीर जटिलताओं के बिना सहन किया गया।
रेडिएशन ऑन्कोलॉजी थेरेपी ग्रुप (आरटीओजी) ने, सतही ट्यूमर (स्तन कैंसर सहित) के हाइपरथर्मिया उपचार का मूल्यांकन करने के लिए, एक यादृच्छिक परीक्षण में एक सहसंबंध स्थापित किया ( परस्पर निर्भरता)ट्यूमर के व्यास और प्रतिक्रिया दर के बीच:अध्ययन के परिणामों ने प्रतिक्रिया में सुधार दिखाया, विशेष रूप से 2 से अधिक हाइपरथर्मिक उपचार (42.5 डिग्री सेल्सियस) प्राप्त करने वाले 3 सेमी से कम व्यास वाले घावों में। अकेले रेडियोथेरेपी से इलाज कराने वाले मरीजों की तुलना में आरटीएचटी से इलाज कराने वाले मरीजों में 12 महीनों में निरंतर प्रतिक्रिया की दर अधिक थी। इन आंकड़ों से पता चलता है कि हाइपरथर्मिया के जुड़ने से उपचार के प्रति लंबी और अधिक संपूर्ण प्रतिक्रिया मिलती है।
उन्नत या स्थानीय रूप से आवर्ती स्तन कार्सिनोमा के लिए हाइपरथर्मिया को रेडियोथेरेपी के साथ जोड़ा गया: 40 रोगियों (10 प्राथमिक मामले और 30 रिलैप्स) में अध्ययन किया गया। यह निर्णय लिया गया कि छोटे घावों वाले रोगियों को अकेले रेडियोथेरेपी प्राप्त होगी, जबकि बड़े घावों वाले रोगियों को आरटीटी प्राप्त होगी। हाइपरथर्मिया से इलाज किए गए ट्यूमर ने अकेले विकिरण चिकित्सा प्राप्त करने वाले नियोप्लाज्म की तुलना में चिकित्सा के प्रति बेहतर प्रतिक्रिया व्यक्त की। यह भी बताया गया है कि विकिरण प्राप्त करने वाले प्राथमिक ट्यूमर वाले रोगियों में पूर्ण और आंशिक प्रतिक्रिया और स्थानीय ट्यूमर नियंत्रण की दर कम थी, जबकि हाइपरथर्मिया के जुड़ने से ये दरें बढ़ गईं। सर्जरी के बाद बार-बार होने वाले ट्यूमर में, हाइपरथर्मिया के जुड़ने से रेडियोथेरेपी के बाद उपचार के प्रति स्थानीय प्रतिक्रिया की दर भी बढ़ गई। यह निष्कर्ष निकाला गया कि संयुक्त उपचार स्थानीयकृत प्राथमिक और आवर्ती स्तन कैंसर से पीड़ित रोगियों में बेहतर नैदानिक परिणाम प्रदान करता है। अध्ययन में यह भी कहा गया है कि ट्यूमर का आकार भी मायने रखता है। सतही ट्यूमर में हाइपरथर्मिया अधिक प्रभावी होता है जब घाव का व्यास 3 सेमी से कम होता है।
हाइपरथर्मिया की प्रभावशीलता का मूल्यांकन करने के लिए सबसे बड़े अध्ययनों में से एक 1996 में प्रकाशित हुआ था:इस विश्लेषण में कुल 306 घावों को शामिल किया गया था। परिणाम आरटीएचटी (चरण III) के साथ स्तन कैंसर के उपचार में 5 अलग-अलग यादृच्छिक परीक्षणों से प्राप्त किए गए थे। अध्ययनों से पता चला है कि हाइपरथर्मिया को विकिरण चिकित्सा में जोड़ने पर एक फायदा होता है, मुख्य रूप से आवर्ती स्तन कैंसर में, जहां, पिछली विकिरण चिकित्सा के कारण, विकिरण की कम खुराक का उपयोग करने की सिफारिश की जाती है। समग्र उपचार प्रतिक्रिया दर आरटीएचटी के लिए 59% और रेडियोथेरेपी के लिए 41% थी।
बार-बार होने वाले स्तन कैंसर से पीड़ित रोगियों में हाइपरथर्मिया के थर्मल मापदंडों और उपचार के परिणाम के बीच संबंध निर्धारित करने के लिए एक अध्ययन: आरटीटीटी प्राप्त करने वाले रोगियों और अकेले विकिरण चिकित्सा प्राप्त करने वाले रोगियों में उपचार की प्रतिक्रिया की तुलना की गई थी। समग्र प्रतिक्रिया दर क्रमशः 61 और 41% थी। एक यादृच्छिक परीक्षण ने स्तन कैंसर सहित सतही घावों के उपचार में गर्मी की खुराक की भूमिका का मूल्यांकन किया। जांचकर्ता उपचार की प्रतिक्रिया और स्थानीय नियंत्रण की अवधि में रुचि रखते थे। मरीजों को 2 समूहों में बांटा गया था। पहले समूह का इलाज अकेले रेडियोथेरेपी से किया गया, और दूसरे समूह का इलाज आरटीटी से किया गया। हाइपरथर्मिया के जुड़ने से थेरेपी और स्थानीय नियंत्रण स्कोर के प्रति समग्र प्रतिक्रिया दर में सुधार हुआ। स्थानीय नियंत्रण में सबसे बड़ा सुधार उन रोगियों में देखा गया जो पहले ही पिछले उपचार में विकिरण चिकित्सा प्राप्त कर चुके थे।
2008 का अध्ययन: इस अध्ययन में 8 विभिन्न चिकित्सा संस्थानों के मरीज़ शामिल थे। उन सभी को बार-बार होने वाला स्तन कार्सिनोमा था और सभी को स्थानीय पुनरावृत्ति के बाद स्तन का पुन: विकिरण प्राप्त हुआ। कुछ रोगियों को विकिरण चिकित्सा के अलावा हाइपोथर्मिया भी प्राप्त हुआ। उपचार के प्रति समग्र प्रतिक्रिया दर हाइपोथर्मिया के साथ 67% और इसके बिना 39% थी।
स्थानीय रूप से आवर्ती स्तन कार्सिनोमा के लिए उपशामक उपचार के रूप में हाइपरथर्मिया की प्रभावशीलता का सत्यापन: अन्य पारंपरिक तरीकों से उपचार के बाद स्तन कैंसर के 30 रोगियों को विकिरण की कम खुराक + 1 घंटे की हाइपरथर्मिया प्राप्त हुई। परिणामों ने स्तन कैंसर की पुनरावृत्ति को कम करने पर हाइपरथर्मिया के प्रभाव की पुष्टि की। इसके अलावा, 5 सेमी से कम व्यास वाले घावों ने संयुक्त उपचार के लिए बेहतर प्रतिक्रिया दी।
आरटीएचटी प्रदान करने में सिद्ध हुआ हैबार-बार होने वाले स्तन कैंसर के उपचार में स्थानीय ट्यूमर नियंत्रण में सुधार: 34 रोगियों को आरटीटी प्राप्त हुआ, 4 रोगियों को कीमोथेरेपी प्लस हाइपरथर्मिया मिला, और 4 रोगियों को केवल हाइपरथर्मिया मिला। यह नोट किया गया कि केवल वे मरीज़ जिन्होंने आरटीटीटी प्राप्त किया था, उन्होंने उपचार पर पूरी तरह से प्रतिक्रिया दी और स्थानीय रोग नियंत्रण में सुधार दिखाया। स्थानीय रूप से आवर्ती स्तन एडेनोकार्सिनोमा से पीड़ित 44 रोगियों को आरटीएचटी प्राप्त हुआ। उपचार पूरा होने के 1 महीने बाद उपचार प्रतिक्रिया दरों का विश्लेषण किया गया। 12 महीनों के बाद, पूर्ण प्रतिक्रिया प्राप्त करने वाले 67% मरीज़ अभी भी सकारात्मक थे। यह पाया गया है कि ट्यूमर का आकार नैदानिक परिणामों को महत्वपूर्ण रूप से प्रभावित करता है।
मेटास्टेस के साथ आवर्ती स्तन कार्सिनोमा के उपचार के लिए विकिरण चिकित्सा के साथ संयोजन में हाइपरथर्मिया का उपयोग: उपचार की प्रभावशीलता का मूल्यांकन करने के लिए, 20 रोगियों में एक अध्ययन किया गया था। अधिकांश रोगियों (95%) ने संयोजन उपचार का पूरी तरह से जवाब दिया, जो स्तन कैंसर में व्यापक फैलने वाले घावों के मामले में प्रभावी था। हालाँकि, उपचारित क्षेत्रों के बाहर मेटास्टेस की उपस्थिति के कारण इन रोगियों की औसत उत्तरजीविता असंतोषजनक थी।
बार-बार होने वाले स्तन कार्सिनोमा वाले रोगियों में सतही आरटीएचटी का उपयोग:अधिकतम प्रतिगमन के दौरान, समग्र प्रतिक्रिया दर 63% थी। 2.5 साल के बाद उत्तरजीविता 21% थी, और 5 साल के बाद - 8%। नीदरलैंड में, आरटीएचटी पहले से उजागर उन रोगियों के लिए मानक उपचार है, जिन्हें दोबारा स्तन कैंसर हुआ है। अध्ययनों से पता चला है कि हाइपरथर्मिया और विकिरण का एक साथ उपयोग अनुक्रमिक उपयोग की तुलना में बेहतर नैदानिक परिणाम देता है। इस पद्धति का उपयोग सतही ट्यूमर वाले रोगियों में किया गया था। हमने मुख्य रूप से सिर और गर्दन के ऑन्कोलॉजिकल रोगों के साथ-साथ स्तन के एडेनोकार्सिनोमा के मामलों पर विचार किया। स्तन एडेनोकार्सिनोमा में चिकित्सा की प्रतिक्रिया 79% पूर्ण प्रतिक्रिया, 14% आंशिक प्रतिक्रिया, और 7% उपचार के प्रति कोई प्रतिक्रिया नहीं थी।
निष्क्रिय आवर्तक स्तन कैंसर वाले रोगियों में आरटीएचटी के साथ कीमोथेरेपी के संयोजन की प्रभावशीलता का अध्ययन: मरीजों को विकिरण के 30 मिनट बाद सप्ताह में एक बार कीमोथेरेपी और हाइपरथर्मिया प्राप्त हुआ। त्वचा की प्रतिक्रिया स्वीकार्य थी, लेकिन ट्रिपल मोडेलिटी के कारण महत्वपूर्ण प्रणालीगत विषाक्तता हुई। यद्यपि चिकित्सा की प्रतिक्रिया दर अधिक थी, स्थानीय नियंत्रण केवल कुछ महीनों तक ही बनाए रखा गया था।
स्थानीय रूप से आवर्ती स्तन कैंसर के लिए अध्ययन: इस मामले में, आरटीएचटी पर ट्यूमर की प्रतिक्रिया सहित संयुक्त उपचार के कई मापदंडों के आधार पर स्थानीय नियंत्रण प्राप्त किया जाता है। बार-बार होने वाले स्तन कैंसर से पीड़ित उनतीस महिलाओं को रेडियोथेरेपी से पहले हाइपरथर्मिया के साथ आरटीएचटी प्राप्त हुई। 1 वर्ष की उत्तरजीविता 71% थी और 2 वर्ष की उत्तरजीविता 54% थी। 2001 में, एथेंस विश्वविद्यालय के मेडिकल स्कूल का अनुभव प्रकाशित हुआ था, जिसमें सतही ट्यूमर के इलाज के लिए आरटीएचटी संयोजन चिकित्सा का उपयोग किया गया था। इस अध्ययन में बार-बार होने वाले मास्टेक्टॉमी स्तन कैंसर वाले 88 मरीज़ और बार-बार होने वाले सुप्राक्लेविक्युलर लिम्फ नोड्स वाले 27 मरीज़ शामिल थे। समग्र उपचार प्रतिक्रिया दर क्रमशः 85.2% और 70.4% थी। वैज्ञानिकों की उसी टीम ने, 1 साल बाद, आरटीएचटी के साथ संयोजन में लिपोसोमल डॉक्सोरूबिसिन की प्रभावशीलता पर पहला अध्ययन प्रकाशित किया। ऐसी 15 महिला मरीज़ थीं जो स्थानीय रूप से उन्नत आवर्तक स्तन कैंसर से पीड़ित थीं। सभी रोगियों ने थेरेपी का जवाब दिया। पूर्ण प्रतिक्रिया दर 20% थी और आंशिक प्रतिक्रिया दर 80% थी। बेन-योसेफ और अन्य ने विकिरण चिकित्सा में जोड़े जाने पर हाइपरथर्मिया के लाभों को पहचाना और स्थानीय रूप से आवर्ती स्तन कैंसर के उपचार में आरटीएचटी के साथ अपने अनुभव का वर्णन किया। 15 महिलाओं को 45 मिनट की हाइपरथर्मिया (45 0C पर) के साथ रेडियोथेरेपी प्राप्त हुई। 15 में से 6 मरीज़ों ने थेरेपी पर पूरी तरह से प्रतिक्रिया दी, 4 मरीज़ों ने आंशिक रूप से प्रतिक्रिया दी, और 3 मरीज़ों ने थेरेपी पर कोई प्रतिक्रिया नहीं दी।
स्थानीय रूप से आवर्ती स्तन कार्सिनोमा वाले मरीजों में आरटीएचटी का उपयोग: 75 घावों में से 41 पहले विकिरणित थे। यह सिद्ध हो चुका है कि विकिरण चिकित्सा के साथ संयोजन में अतिताप का अधिक स्पष्ट नैदानिक प्रभाव होता है। 14% रोगियों में त्वचा पर अल्सर देखा गया।
सीमांत उच्छेदन के साथ स्थानीय रूप से उन्नत या आवर्ती स्तन कैंसर के लिए आवेदन(सीमांत उच्छेदन): इस अध्ययन में 15 मरीजों को 2 समूहों में बांटा गया। पहले समूह को प्राथमिक चिकित्सा के रूप में उच्छेदन के बाद आरटीएचटी प्राप्त हुआ, और दूसरे समूह में आवर्ती ट्यूमर वाले रोगी शामिल थे, जिन्हें एक ही उपचार प्रक्रिया से गुजरना पड़ा - विकिरण चिकित्सा के साथ संयोजन में अतिताप। पहले समूह के लिए कुल मिलाकर जीवित रहने की दर 90% थी और दूसरे समूह के लिए 89% थी, स्थानीय नियंत्रण दर क्रमशः 75 और 81% थी, जबकि रोग-मुक्त जीवित रहने की दर क्रमशः 64 और 69% थी। सभी रोगियों के लिए, उत्तरजीविता, स्थानीय नियंत्रण और रोग-मुक्त उत्तरजीविता क्रमशः 89%, 80% और 68% थी।
सतही ट्यूमर पुनरावृत्ति के लिए विकिरण चिकित्सा के साथ संयोजन में अतिताप का अनुभव:इस अध्ययन में, आरटीएचटी की प्रभावशीलता का मूल्यांकन उन रोगियों में किया गया था, जिन्हें पहले विकिरण प्राप्त हुआ था। 18 महीनों के अनुवर्ती कार्रवाई के बाद, स्थानीय नियंत्रण 72.7% था, रोग स्थिरीकरण 20.5% था, और गैर-नियंत्रण 6.8% था।
अतिताप के साथ संयुक्त पुन: विकिरण की प्रभावकारिता - 2010 अध्ययन:बार-बार होने वाले स्तन कैंसर वाले 78 रोगियों ने संयोजन चिकित्सा का जवाब दिया। 3-वर्षीय बेंचमार्क 78% था और 5-वर्षीय बेंचमार्क 65% था। 3- और 5-वर्षीय रोगी की जीवित रहने की दर क्रमशः 66% और 49% थी। बार-बार होने वाले स्तन कैंसर से पीड़ित 66 वर्षीय महिला के मामले पर विचार किया गया, जिसे रेडियोथेरेपी और कीमोथेरेपी प्राप्त हुई लेकिन उपचार का कोई जवाब नहीं मिला। हालाँकि, जब हाइपरथर्मिया को थेरेपी में जोड़ा गया, तो रोगी ने इलाज पर पूरी तरह से प्रतिक्रिया दी। अंत में, संयुक्त आरटीएचटी उपचार गंभीर विषाक्तता के बिना एक अच्छा परिणाम दे सकता है। आरटीएचटी का उपयोग बार-बार होने वाले स्तन कैंसर से पीड़ित 198 रोगियों में किया गया था। 3-वर्षीय बेंचमार्क 83% था और 5-वर्षीय बेंचमार्क 78% था।
परिणाम और निष्कर्ष
नतीजे बताते हैं कि स्तन कैंसर के इलाज के लिए विकिरण चिकित्सा और/या कीमोथेरेपी के साथ हाइपरथर्मिया का उपयोग उपचार की प्रभावशीलता को बढ़ाता है।
अन्य चिकित्सीय तरीकों के साथ संयोजन में हाइपरथर्मिया का उपयोग आवर्ती स्तन कैंसर के उपचार में एक आशाजनक दिशा है। थेरेपी के लिए दर्ज की गई प्रतिक्रिया दरें उच्च हैं, और उपचार विकल्प के रूप में हाइपरथर्मिया को शामिल करने के साथ या उसके बिना रेडियोथेरेपी की तुलना से संकेत मिलता है कि हाइपरथर्मिया उच्च प्रतिक्रिया दर, स्थानीय नियंत्रण दर और संयोजन चिकित्सा के साथ जीवित रहने की दर के मामले में एक लाभ प्रदान करता है। प्राथमिक स्तन ट्यूमर के उपचार में हाइपरथर्मिया की भूमिका का मूल्यांकन करने के लिए अधिक शोध की आवश्यकता है, क्योंकि वर्तमान में उपलब्ध परिणाम उत्साहजनक हैं। अंत में, सिर और गर्दन के कैंसर के उपचार और घातक मेलेनोमा के उपचार में हाइपरथर्मिया के उपयोग पर कई अध्ययनों के संतोषजनक परिणामों को देखते हुए, हाइपरथर्मिया को अन्य प्रकार के सतही घावों के नैदानिक प्रबंधन में एकीकृत करने पर विचार किया जाना चाहिए। बार-बार होने वाले स्तन कैंसर के इलाज के लिए हाल के एनसीसीएन दिशानिर्देशों में हाइपरथर्मिया को शामिल करने के अलावा, हम स्तन कैंसर में अन्य त्वचा के घावों और प्राथमिक घावों के इलाज के लिए आरटीएचटी के उपयोग का सुझाव देते हैं।