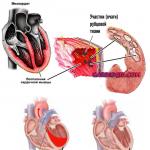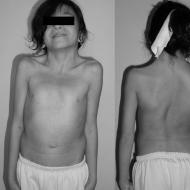
精巣セミノーマの詳細:原因、症状、段階、生命予後。 精巣精上皮腫:原因、症状、治療法 精巣上皮腫の生存期間はどれくらいですか
組織学的には、 WHOの分類によって編集 F.K. モストフィ (1977)、次の点を区別します。
胚細胞腫瘍(精細上皮から発生)
A. 同じ組織構造の腫瘍:
- セミノーマ;
- 精母細胞精上皮腫。
- 胎児がん。
- 卵黄嚢腫瘍。
- 多胚腫;
- 絨毛上皮腫;
- 奇形腫 a) 成熟、b) 未熟、c) 悪性転換を伴う。
B. 複数の組織型の腫瘍。
性索間質腫瘍
A. 明確に区別された形式:
- レイディゴマ。
- セルトリオーマ;
- 顆粒膜細胞腫瘍。
B. 混合形態。
B. 完全に分化していない腫瘍。
生殖細胞および性索間質細胞を含む腫瘍および腫瘍様病変
A. 性腺芽腫;
B. その他。
混合腫瘍
リンパ系および造血組織の腫瘍
二次腫瘍
直管、精巣網、精巣上体、精索、被膜、支持構造、初歩的形成の腫瘍。
未分類の腫瘍
臨床医にとって最も重要なことは、すべての精巣胚細胞腫瘍を精上皮腫と非精上皮腫に分けることであり、これは治療戦術の選択に大きな影響を与えます。 非セミノーマ精巣腫瘍をさらに細分化することは大きな役割を果たしません。 精巣胚細胞腫瘍のさまざまな組織学的変異を詳細に検査した1977年のWHO分類では、それらの起源の統一性や発がんの過程で他の形態学的タイプにさらに分化する可能性が考慮されていなかった。
1992年に提案された新しい組織学的分類は、すべての精巣胚細胞腫瘍の起源は上皮内癌であるという考えに基づいています。 精細胞腫を除くすべての胚細胞腫瘍は、淋細胞腫と呼ばれることが提案されています。 淋細胞腫は、精上皮腫(古典的および未分化、より進行性の経過を特徴とする)、催奇形性腺細胞腫、および精上皮腫と催奇形性腺細胞腫の両方の特徴を有する未分化胚細胞腫瘍に分類されます。 催奇形性淋細胞腫の幹細胞は多能性であり、さまざまな種類の奇形腫(成熟および未熟)、上芽細胞腫(古い分類では胎児がん)、および卵黄嚢腫瘍や絨毛膜がんなどの胚体外要素に分化することができます。
ロシアでは、多くの国と同様に、国際対がん連合が提案した分類が使用されており、治療方針を決定するために腫瘍の進行の範囲をより詳細にカバーしています。 TNM 分類を使用する場合、診断の組織学的確認は必須です。 TNM (1997) のカテゴリーを評価するには、次のような最小限の調査が必要です。T - 臨床検査と精巣摘出術。 N - 超音波検査や尿路造影などの臨床検査および放射線検査。 M - 臨床検査、X 線検査、生化学検査。 S - 腫瘍マーカー。
T - 原発腫瘍
精巣摘出術が行われていない場合は、Tx シンボルを使用する必要があります。
T is - 小管内腫瘍
T1 - 腫瘍は精巣と精巣上体に限定されており、静脈またはリンパ管への浸潤はありません。
T2 - 精巣と精巣上体に限定され、静脈およびリンパ管への浸潤を伴う腫瘍
T3 - 腫瘍が精索まで広がっている
T4 - 腫瘍が白膜に侵入
N - 所属リンパ節および近隣のリンパ節。 睾丸の場合、大静脈傍リンパ節と大動脈傍リンパ節が局所的です。 以前に鼠径部陰嚢領域の手術を受けた場合、鼠径部リンパ節は局所的なものとみなされます。 最も近いものは、骨盤内、縦隔、鎖骨上であると考えられています。
Nx - 所属リンパ節の状態を評価することは不可能です
N0 - プロセスにおける所属リンパ節の関与の兆候なし
N1 - 所属リンパ節が 2 cm 未満
N2 - 2 cm を超え 5 cm 未満の所属リンパ節
N3 - 5cmを超える所属リンパ節
M - 遠隔転移
Mx - 遠隔転移の存在を判断することは不可能
M0 - 遠隔転移の兆候なし
M1a - 横隔膜上のリンパ節および/または肺への転移
M1b - 肝臓、骨、脳への転移
P - 組織病理学的カテゴリー、カテゴリー T、N、および M に対応します。
S - 腫瘍マーカー
Sx - 腫瘍マーカーは測定されませんでした
S0 - 正常範囲内の腫瘍マーカー
S1 - LDH< 1,5 x верхняя граница нормы, ХГ < 5000 Ед/мл, АФП < 1000 нг/мл.
S2 - LDH 1.5-10 x 正常上限値、CG5000 - 50000U/ml、AFP 1000 - 10000 ng/ml
S3 - LDH > 10 x 正常上限、CG > 50,000 U/ml、AFP > 10,000 ng/ml
ロイヤル マースデン病院の分類は、臨床医の間で広く普及しています。
私精巣以外には病気の証拠がない
IMトークンレベルアップのみ
II 横隔膜下のリンパ節の関与
IIA最大サイズ< 2 см
IIB 最大サイズ 2~5cm
IIC
最大サイズ5~10cm
II最大サイズ>10cm
III 横隔膜の上下のリンパ節の関与
縦隔リンパ節 M+
頸部リンパ節 N+
IV内臓転移
後腹膜リンパ節 A、B、C (上記と同様)
縦隔リンパ節 M+
頸部リンパ節 N+
肺、肝臓、その他の臓器への転移
患者の予後を予測し、治療アプローチを標準化するために、病気の広がりの程度に基づいたいくつかの分類が提案されています (MSKCC、IU、NCI、EORTC など)。
1995 年に、播種性精巣胚細胞腫瘍を予後グループに分ける新しい分類である国際生殖細胞癌協力グループ (IGCCCG) 分類が提案されました。この分類は、播種性精巣腫瘍を治療するほとんどの主要施設で受け入れられています。 IGCCCG 分類では、精巣胚細胞腫瘍の予後因子として血清中の腫瘍マーカーの濃度が使用されることに注意してください。
非セミノーマ胚細胞腫瘍
すべての兆候が存在する場合、予後は良好です。
- 血清中のAFPレベルは、<1000 нг/мл;
- 血清hCGレベルは<5000 мМе/мл;
- 血清LDHレベルは<675 Ед/л;
すべての兆候が存在する場合、中等度の予後:
- 血清中のAFPレベルは1000~10,000ng/mlの範囲です。
- 血清中のhCGのレベルは5000から50000 mIU/mlの範囲です。
- 血清LDHレベルは675から4500U/lの範囲です。
- 性腺外縦隔腫瘍がないこと。
- 肝臓、骨、脳への転移がないこと。
少なくとも 1 つの兆候が存在する場合、予後は不良です。
- 血清AFPレベルが10,000ng/mlを超える。
- 血清 hCG レベルが >50,000 mIU/ml;
- 血清LDHレベルが>4500 U/l;
- 縦隔の性腺外腫瘍の存在。
- 肝臓、骨、脳への転移の存在。
セミノーマ
予後良好:肝臓、骨、脳への転移がないこと。
中程度の予測:肝臓、骨、脳に転移の存在。
泌尿器科腫瘍学では悪性精巣腫瘍は非常にまれですが、発生率は着実に増加しています。
それによると、すべての腫瘍学的病理の中で、それが占める割合は2%未満です。 同様の病状は、35 歳未満および 60 歳以上の男性にも見られます。 しかし、10歳未満の少年で精巣の癌性腫瘍が発見されたケースもあります。
このような腫瘍の大部分 (95%) は胚性腫瘍、つまり胚性腺細胞構造で発生します。 それらはセミノーマと非セミノーマに分けられます。 最も一般的な精巣癌は精上皮腫です。
コンセプト
精上皮腫は、精巣の胚細胞から形成される悪性の精巣腫瘍です。
すべての胚細胞腫瘍のうち、精上皮腫は約 40% を占め、他のものよりも一般的です。 通常、この形成は片方の睾丸にのみ影響を及ぼし、痛みのない肥大を引き起こしますが、両側の睾丸病変もあります。
この形態の精巣癌は、リンパ経路を介した早期転移が特徴です。
精上皮腫は壊死領域の形成を引き起こすことがよくありますが、早期に検出されれば予後は非常に良好です。
病気の原因
セミノーマの発生はさまざまな要因によって決まります。
- 多くの場合、睾丸内の生殖細胞形成は、既存の前がん、つまり尿細管内生殖細胞腫瘍プロセスの影響下で形成されます。 組織の変化の過程で異常な変異細胞が形成され、状況によっては悪性腫瘍の形成を引き起こします。
- 多くの場合、セミノーマは原発腫瘍の除去後に再発するものです。
- 遺伝も重要な役割を果たします。 統計によると、病状は血縁者にはるかに頻繁に見られ、近いものだけでなく、数世代の違いがある場合でも遠いものでも見つかります。
- 高エストロゲン症。過剰なレベルのエストロゲンホルモンやその他の形態のホルモンの不均衡によって現れます。
- 精上皮腫の発症のもう一つの理由は、精巣が陰嚢内に下降しない停留精巣です。
- 打撲傷、手術中の損傷、偶発的な打撃などの外傷性要因も、このタイプの精巣がんの発生に影響を与える可能性があります。
男性が先天性または後天性の精巣発達異常を患っている場合、その男性はリスクグループに属します。
分類
セミノーマはいくつかのタイプに分類されます。
- 精母細胞– すべての精上皮腫の 5 ~ 10%、主に高齢患者に見られます。 腫瘍は黄色の粘膜を持ち、内部には嚢胞性封入体、壊死、出血が見られます。
- アナプラスチック– 精上皮腫の男性の 5 ~ 10% に発生します。 それは、攻撃的な経過、明確に定義されていない間質、およびさまざまな形の細胞の存在によって特徴付けられます。
- 典型的な– 症例の 85% で検出されます。 停留精巣のある 20 ~ 35 歳の男性に典型的です。 通常は単一ノードの形式で形成されますが、マルチノード構造もあります。 表面が白く光沢があるように見えます。 結核様肉芽腫が含まれる場合があります。
精上皮腫はいくつかの段階に分かれています。
- ステージ I – 形成は局所的であり、睾丸内にのみ存在します。
- ステージ II では、精上皮腫も精巣内に局在していますが、その形状の変化と膜への腫瘍の成長が観察されます。
- ステージ III – リンパ節転移が出現。
- ステージ IV では、腫瘍プロセスの広がりが離れた臓器に到達します。
精巣精上皮腫の症状
精巣がんは最初はそれ自体がわかりません。 最も注意深い男性は、触診中に偶然睾丸のしこりを発見する可能性があり、それが泌尿器科医を訪れる理由になります。 セミノーマの最初の症状はこれらの圧縮です。
腫瘍がさらに進行すると、影響を受けた睾丸が肥大し始め、痛みを伴い、特に力を入れたり、重いものを持ち上げたりすると激しい痛みを伴います。
睾丸を支える索の損傷により、痛みを伴う症状が発生します。 徐々に、精巣組織は緻密になり、変形します。
痛みや不快感は、腫瘍の過程が影響を受けた精巣の境界を越えて広がった場合にのみ発生します。 リンパ節転移が現れると、臨床像がより顕著になります。
睾丸の腫瘍プロセスは、思春期早発、勃起不全、女性化乳房、ホルモン障害を伴うことがあります。 腹部リンパ節への転移により、周期的な腰痛が発生します。 転移が肺系に浸透している場合、男性は血の混じった分泌物を伴う咳を発症します。
大動脈周囲リンパ節への転移を背景に、腹部に痛みが現れ、脚の腫れが現れます(大静脈が圧迫されている場合)。 尿管が圧迫されると排尿障害が生じ、腹腔内リンパ節への転移を伴う腸閉塞を伴います。
腫瘍の診断
 病理を特定するプロセスは、伝統的な健康診断から始まります。 その後、実験室およびハードウェアの方法を使用した追加の検査が処方されます。
病理を特定するプロセスは、伝統的な健康診断から始まります。 その後、実験室およびハードウェアの方法を使用した追加の検査が処方されます。
通常、男性はまず超音波診断を受け、腫瘍の大きさとその広がりの程度を評価することができます。
転移プロセスを特定するには、磁気共鳴またはコンピューター断層撮影が必要です。
hCG、血清ニューロン特異的エノラーゼ、α-フェトプロテイン、胎盤アルカリホスファターゼなどの腫瘍マーカーの分析は、診断上非常に重要です。
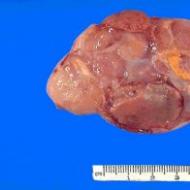
通常、精上皮腫は 5 ~ 10 cm を超えず、精巣組織から分離された 1 つまたはいくつかの小葉結節で構成されます。
セミノーマの治療
このタイプの精巣がんの治療は、慎重な診断と腫瘍の組織学的変異を考慮した上で行われます。
通常、最初のステップは、精上皮腫の影響を受けた精巣の外科的除去 (精巣摘出術) であり、臍帯および場合によっては後腹膜リンパ節構造の除去 (リンパ節切除術) も行われます。
さらなる治療手段は、地層の組織学的性質によって決定されます。
切除した精巣精上皮腫の写真

精上皮腫は、サルコリシンやシクロホスファミドなどの抗腫瘍薬による化学療法の影響を最も受けやすいと考えられています。
治療効果が不十分な場合は、シスプラチン、ブレオマイシン、ビンブラスチンの組み合わせが使用されます。
予後と予防
精巣精上皮腫の治療を精巣がんの第一段階で開始した場合、患者の生存率は最大93.6%、第二段階では約90%、第三段階では57.8%となります。
ステージ 1 ~ 2 のセミノーマの治療完了後、患者の最大 80% が 10 年間生存します。 患者の約 16 ~ 20% が 5 年間で再発を経験し、そのうち約 70% が治療後最初の 2 年以内に再発します。
ほとんどの場合、再発は横隔膜下局在の悪性リンパ節腫瘍の形で検出されます。
精巣における精上皮腫の形成を避けることは、ほとんどの場合、遺伝や遺伝的要因によって引き起こされるため、ほぼ不可能です。 以下の方法で精巣がんの発症リスクを軽減できます。
- 毎月の精巣の触診による定期的な自己検査により、しこりの出現がないか確認します。 何かが検出された場合は、すぐに泌尿器科医に連絡する必要があります。
- さらに、停留精巣を速やかに治療し、ホルモンの不均衡を解消し、不健康な中毒(ニコチン、アルコール、薬物)などを排除することをお勧めします。
セミノーマの再発予防に関しては、治療後最初の12か月間は2か月ごとに検査、腫瘍マーカーの血液検査、X線撮影が行われます。 治療終了後2年目は、患者は上記の予防措置を3か月に1回、3年目は四半期に1回受ける必要があります。
この種のがんでは転移が遅れることが多いため、一般に、このようながん患者のモニタリングは治療終了後5年間実施する必要があります。
治療後4~5年目の通院頻度や予防検査は医師が個別に決定します。
セミノーマは原発性精巣胚細胞腫瘍の約 40% を占めます。 20~40歳で発症することが多く、小児ではほとんど観察されません。 精液腫は精巣の外側(性腺外精液腫)、たとえば前縦隔や後腹膜に発生することがありますが、これは胚発生中の胚上皮の遅れによって説明されます(全知識:奇形腫を参照)。
WHOの分類によれば、定型、未分化、精母細胞性セミノーマが区別されます。
典型的なセミノーマは、主に 20 ~ 40 歳の男性に発生します。 陰嚢内に降りていない精巣で発生することが多いです。 睾丸が拡大しますが、通常のサイズよりも発生する頻度は低くなります。 腫瘍は 1 つのリンパ節から構成され、まれに複数のリンパ節から構成されます。 切り口の表面は光沢があり、白く、裂けています。 顕微鏡的に見ると、典型的なセミノーマは、明確な境界を持ち、グリコーゲンや場合によっては脂質を含む軽い細胞質を備えた、多角形または円形の同じ種類の大きな細胞で構成されています。 腫瘍間質はリンパ系細胞が浸潤した結合組織層で表され、時には肉芽腫性反応が発現することがあります(巨大な多核細胞を含む結核様肉芽腫)。
未分化精上皮腫は、臨床的にはより悪性であると考えられており、顕著な細胞と核の多型、多数の有糸分裂、リンパ球浸潤が乏しい不明瞭な間質、および肉芽腫性反応の欠如を特徴としています。 未分化精上皮腫の領域は、典型的な精上皮腫およびその転移に見られます。
精細胞性精上皮腫は全精上皮腫の約 9% を占め、主に 50 歳以上の人々に発生します。 かなりのサイズに達する可能性があります。 腫瘍は黄色がかった色で、粘液状の外観をしており、わずかに海綿状で、時には嚢胞、小さな壊死領域、および切開部の出血を伴います。 顕微鏡で見ると、それは 3 種類の細胞で構成されています。境界が明確なリンパ球様、丸い好塩基性核、好酸性細胞質です。 巨大 - 1〜3個の核を持つ直径100マイクロメートルまで。 いわゆる中間 - 丸い核と豊富な細胞質を持つ中程度の大きさの細胞。 典型的なセミノーマとは異なり、精母細胞セミノーマ細胞はグリコーゲンを含まず、腫瘍間質にリンパ球浸潤がありません。
セミノーマの転移は、リンパ行性および血行性経路を介して腸骨および傍大動脈リンパ管、リンパ節、肺、肝臓に起こりますが、他の臓器に転移することはまれです。 典型的および未分化精上皮腫の転移は、症例の約65%で精上皮腫の構造を持ち、26% - 胎児がん(全知識を参照)、4% - 奇形腫(全知識を参照)で発生します。 精母細胞性精上皮腫は転移することはほとんどありません。
臨床的には、病気の発症時の症状は、睾丸の拡大と硬化によって特徴付けられます。 これには不快感や痛みが伴うこともあります。 精巣(知識の全文を参照)は大きなサイズ(直径 20 ~ 30 センチメートルまで)に達することがありますが、他の腫瘍ではめったに観察されません。 症例の約 10% では、最初の臨床症状は後腹膜リンパ節、リンパ節、肺への転移によって引き起こされます。 傍大動脈リンパ節が損傷すると、腹部や腰の痛み、下大静脈の圧迫に伴う下肢の腫れが現れ、尿管が圧迫されると乏尿、続いて無尿になります。 重度の痛みや腸閉塞が発生する可能性があります (詳細な知識: 腸閉塞を参照)。
ソ連で採用されたセミノーマの分類によれば、4つの臨床段階が区別されます。 - 白膜に侵入せず、精巣の形状に違反しない小さな腫瘍。 II - 転移のない腫瘍で、白膜を超えて広がり、精巣の形状を破壊する。 III - 所属リンパ節への転移を伴う大きな結節状腫瘍。 IV - ステージ I ~ II と同様の原発腫瘍ですが、所属リンパ節、リンパ節および遠隔臓器への転移を伴います。
セミノーマの推定診断は、他の精巣腫瘍と同様、精巣の徐々に拡大し硬化する証拠に基づいて行うことができます。 原則として、精巣穿刺とその後の細胞学的検査によって確認することができ、場合によっては腫瘍の性質を決定することができます。
尿中のヒト絨毛性ゴナドトロピン(知識の全文を参照)およびα-フェトプロテインの含有量を測定することには、鑑別診断上の重要性があります。 ヒト絨毛性ゴナドトロピンおよびα-フェトプロテインの高い力価は、絨毛膜上皮腫(詳細な知識:栄養膜疾患を参照)および胎児がんの特徴です。 セミノーマ患者では、α-フェトプロテインのレベルと同様に、セミノーマの含有量の増加が観察されることはほとんどありません。 肺および局所転移領域の X 線検査は重要な役割を果たします。国際対がん連合が提案した分類によれば、リンパ節、大動脈および下大静脈に沿って位置するリンパ節、鼠径リンパ節が含まれます。 、リンパ節(陰嚢または鼠径部に手術が行われた場合)、骨盤内リンパ節、縦隔リンパ節、鎖骨上リンパ節も含まれます。 鎖骨上リンパ節が腫れている場合は穿刺し、細胞診検査を行います。 はるかに難しいのは後腹膜リンパ節の検査で、通常は排泄性尿路造影検査から始まります (知識全体を参照)。 腹膜リンパ節に大きな転移がある場合、尿路造影では尿管の変位、場合によってはその圧迫が明らかになり、尿路の拡張につながり、場合によっては腎機能の停止に至ることもあります。 特に右睾丸のセミノーマでは、キャボグラフィーを使用すると、より多くの情報が得られます。完全な遮断に至るまで、下大静脈の変位と圧縮が検出されます。 側方投影で行われるカボグラフィーにより、リンパ節の前群または後群の転移性病変を区別することが可能になります。 さらに、場合によっては、下大静脈の影に重なっているため、直接投影では検出できない転移が検出されることもあります。 小さな転移の場合、直接リンパ造影は後腹膜リンパ節、重いリンパ節の状態に関する貴重な情報を提供します(知識の全文を参照)が、リンパ節転移によって完全に置き換えられたリンパ節はリンパ像では検出されません。
現在、コンピューター断層撮影法 (全知識: コンピューター断層撮影法を参照) は、後腹膜転移の診断において重要になってきており、リンパ節の拡大、主要な血管 (大動脈、下大静脈、腎血管) および隣接臓器との関係を明らかにしています。そしてティッシュ。 この方法では、セミノーマの転移が検出されることが多い肝臓、腎臓、副腎、膵臓の層ごとの画像を同時に取得できます。
治療は複雑です。 彼らは睾丸摘出術から始まります。 精巣摘出術のみを行うことは受け入れられません (知識の全文: 去勢を参照)。精索を除去する必要があります (知識の全文を参照)。 さらなる治療の性質は、腫瘍の組織学的検査の結果を受けた後に決定されます。
典型的な精上皮腫のステージ I および II では、精巣摘出術後、局所転移領域への放射線療法または一連の予防化学療法が行われます。 リンパ管および流出経路に加えて、精索の断端も照射の対象となります。
疾患のIII期およびIV期では、併用療法(化学療法と放射線療法)が最もよく使用されます。 放射線療法は、単一の大量転移が存在する場合に優先されます。 化学療法は主に多発性転移患者や、後腹膜転移による尿管圧迫による乏尿や無尿などの即効性が必要な場合に処方されます。 このような場合、サルコリシンのいわゆる負荷用量(一度に100~120ミリグラム)を投与することが許容されます。 典型的なセミノーマには、放射線療法と抗腫瘍剤による治療が非常に効果的であるため、原則として、後腹膜リンパ節郭清術(全知識:Chevassus-Gregoire手術を参照)は行われません。
原発腫瘍の放射線療法は、原発腫瘍が手術不能な場合、または患者が手術を拒否した場合に行われます。
放射線療法の禁忌は、広範な腫瘍の播種、悪液質、重度の貧血、白血球減少症による患者の重篤な全身状態です。
大量の組織を照射する必要があるため、メガボルトの電離放射線源を使用する体外照射療法 (知識全体を参照) の使用が決定されます。 根治的放射線療法では、総焦点線量は 3000 ~ 4000 rad (30 ~ 40 Gy) になります。 放射線照射は 4 ~ 5 週間行われ、緩和目的の放射線療法では、総局所線量は 2000 ~ 3000 rad (20 ~ 30 Gy) になります。 放射線場の領域での皮膚の充血、白血球減少症、胃や腸の機能不全の可能性があります。 晩期放射線障害 (詳細情報を参照) には、腎臓への放射線照射中の慢性胃腸炎 (詳細情報を参照) および放射線腎硬化症 (詳細情報を参照) が含まれます。
セミノーマの治療に最も効果的な抗腫瘍剤はサルコリシンとシクロホスファミドです。 サルコリシンは通常、週に 1 回 50 ミリグラムを静脈内に処方され、総用量は 200 ~ 250 ミリグラムになります。 シクロホスファミドは、1日おきに0.4グラムを合計6~8年間静脈内投与され、化学療法コースは3~4か月に1回、2年間実施されます。
精母細胞と未分化精上皮腫は、典型的な精上皮腫よりも治療に対する反応性が低く、未分化精上皮腫は放射線療法や抗腫瘍剤に耐性があります。 腫瘍が治療に抵抗性がある場合、または効果が不完全な場合は、胚胚細胞腫などの他の悪性精巣腫瘍に使用される治療計画および治療法に切り替える必要があります(知識全体を参照)。 これは、セミノーマの要素を含む複数の組織型の精巣腫瘍にも当てはまります。
予報。 D. E. Johnson と共著者 (1976) によると、典型的なセミノーマのステージ 1.11 および III の 5 年生存率は、それぞれ 93.7%、90%、および 57.9% です。 Percarpio (B. Percarpio) ら (1979) によれば、未分化セミノーマのステージ I および II では、5 年生存率は 96%、10 年生存率は 87% です。 放射線療法または化学療法中のヒト絨毛性ゴナドトロピン含有量の減少は治療の有効性を示し、治療中および追跡調査中のヒト絨毛性ゴナドトロピン含有量の増加は予後不良の兆候であることが確立されています。
あなたは、この世界から永久に消えるという見通しに断固として不満を持っていますか? あなたは、その中に群がる墓虫に食い荒らされた、おぞましい腐った有機物の塊の形で自分の人生を終えたくないですか? 青春時代に戻って別の人生を生きてみませんか? 最初からやり直します? 犯した間違いを修正しますか? 果たせなかった夢を叶えますか? このリンクに従ってください:
精巣精上皮腫は、男性の生殖器(精巣)の悪性腫瘍の一種です。 精巣組織を形成する胚細胞から発生し、精巣がんとも呼ばれます。
精巣セミノーマは精巣癌の一種です。
 現代の護身手段は、その動作原理が異なる驚くべきリストです。 最も人気のあるものは、購入や使用にライセンスや許可を必要としないものです。 で オンラインストア Tesakov.com, 護身用品はライセンスがなくても購入できます。
現代の護身手段は、その動作原理が異なる驚くべきリストです。 最も人気のあるものは、購入や使用にライセンスや許可を必要としないものです。 で オンラインストア Tesakov.com, 護身用品はライセンスがなくても購入できます。
この病気はまれです。 精巣がんは、男性が罹患する悪性腫瘍の約 2% を占めます。 しかし、過去数十年にわたって増加傾向にあり、医師の間で深刻な懸念を引き起こしています。
主に20~40歳の男性が罹患します。 60歳以上の患者はセミノーマに罹患する可能性は低くなりますが、小児にセミノーマが発生することがあります。
精巣精上皮腫の発症の理由は、他の悪性腫瘍と同様、完全に不明です。 素因の中で、最も重要なものは遺伝と(胎児発育中の陰嚢内への停留精巣)です。 多くの患者には性器外傷や内分泌疾患の病歴があった。
症状と経過

セミノーマでは、痛み、腫れ、睾丸のサイズの増加が見られます。
精巣精上皮腫の臨床症状は病気の段階によって異なります。
初期段階では、患者は睾丸の圧縮とその上の硬い形成の存在を独立して検出します。 その後、睾丸の腫れとサイズの増加が現れます。
病気が進行すると背中に痛みが現れます。 これは所属リンパ節への転移の広がりによるものです。 静脈の圧迫により発症することがあります。 鼠径部の著しく肥大した転移性集塊が尿管を圧迫し、次のような症状が起こることがあります。 遠隔転移は通常、肺に影響を及ぼします。 吐血や息切れを伴います。 転移が肝臓に広がると、黄疸、右季肋部の痛み、腹水(腹腔内の液体)が発生します。 転移が骨に局在すると、骨に激しいうずくような痛みが現れます。
あらゆる種類の腫瘍に特徴的な、癌中毒の典型的な症状である全身衰弱、体重減少、無力症、嗜眠も、精巣精上皮腫の場合、特に進行すると典型的です。
精巣精上皮腫の病期別分類
- ステージ 1 - 腫瘍は局在しており、精巣は拡大しておらず、圧縮や腫れもありません。
- ステージ2 - 精巣組織への損傷が腫瘍に加わり、浮腫が発生し、硬化し、精巣の形状が変化します。
- ステージ 3 - 上記の変化には、局所リンパ節の損傷が伴います。
- ステージ 4 - 離れた臓器や体のシステムへの転移損傷。
診断

精巣の触診では、精上皮腫は密な形成として定義されます。
セミノーマの診断は、患者の訴えを正しく解釈し、医師が検査することから始まります。 触診すると、精巣組織と融合した密な形成が確認されます。
通常、精上皮腫のサイズは 5 ~ 8 cm で、腫瘍は超音波を使用するとよく視覚化できます。 腫瘍の形態学的要素を確認します。
特別な血液検査では、α-フェトプロテインやβ-絨毛性ゴナドトロピンなどの特定の腫瘍マーカーが見つかります。これは、腫瘍がほとんど見えない非常に小さな腫瘍にとって重要です。
がんが所属リンパ節に転移し、さらに重要な臓器に転移しているかどうかを理解するには、さらに多くの研究を実施する必要があります。 最も有益なのはコンピューター断層撮影法で、転移によって影響を受けた鼠径部、腹膜、縦隔のリンパ節を示します。 診断は、腹腔および胸腔の単純X線撮影によっても行うことができます。 後者は肺の転移を見つけるのに役立ちます。
最も感度の高い診断方法は陽電子放射断層撮影法であり、病気の段階を正確に決定します。
処理
精巣セミノーマの治療では、腫瘍疾患の治療に使用される基本原則が遵守されます。
最初のステップは腫瘍を除去する手術です。 ほとんどの場合、精索とともに睾丸全体が切除されます。 所属リンパ節および後腹膜リンパ節が影響を受けている場合は、それらも切除されます。 次に、放射線療法と化学療法が行われ、最終的に腫瘍細胞の増殖が抑制されます。 術後療法の選択は、プロセスの程度と臓器やシステムへの損傷の深さに応じて異なります。

病気の初期段階では、鼠径部および後腹膜領域への放射線療法は完全に限定される可能性があります。 がんが広範囲に進行し、治療が無効な場合(転移がさらに進行する恐れがある場合)には、数コースの化学療法が使用されます。
場合によっては、腫瘍が第 2 精巣に広がることもあります。 この場合、外科医は使用します。 その結果、患者は睾丸で生成されるテストステロンのレベルが低下し、テストステロンのレベルを一定に保つ必要があります。
すでに述べたように、精巣セミノーマは、まだ自分の子供を持たない若い患者に発生することがよくあります。 さらに、セミノーマは小児期でも発生する可能性があります。 このような場合、病気が早期に発見され、腫瘍の局在が明らかな場合には、精巣を温存したまま腫瘍を切除する臓器温存手術が行われます。 この場合、再発の可能性について患者を監視する際には、さらに警戒する必要があります。
睾丸の摘出を恐れる必要はありません。 残りの睾丸は、原則として、の機能を引き受けます。 ほとんどの患者は手術後も通常の性生活を送り、精子は生殖能力を維持します。
防止

停留精巣のタイムリーな治療は癌の発症を予防することです。
原発性精巣精上皮腫の予防について言えば、停留精巣のタイムリーな治療に注意を払う必要があります。 統計によれば、精巣を陰嚢内に下降させる手術を受けた患者は、腫瘍を発症することが最も多い患者であるため、生涯を通じて注意深く観察する必要があります。 また、生殖器への損傷を避け、生殖器領域の炎症性疾患を適時に治療する必要があります。
精上皮腫を除去する手術を受けた患者は、継続的なモニタリングが必要です。 退院後1年目は2ヶ月に1回、腫瘍マーカーの血液検査を含む一般検査が必要です。 2年目は少なくとも3か月に1回患者を観察します。 来年は四半期に1回。 今後は患者の状態に応じて半年に1回以下の頻度で検査を実施する。
予報
ステージ1。早期診断とタイムリーな包括的な治療により、予後は非常に良好です。 手術後の病気の第一段階の患者は、原則として完全に回復し(最大95%)、子供を産むことも含めて完全な生活を送ります。
ステージ2。病気の第 2 段階では、一般に良好な転帰にもかかわらず、依然として再発のリスクが高くなります (患者の 15 ~ 20% が今後 5 年間で再び病気になるリスクがあります)。 このような患者は、この期間中、注意深く監視する必要があります。
ステージ3-4。第 3 期と第 4 期の予後は、腫瘍のサイズ、転移の有病率、重要な器官や身体システムへの損傷の程度によって異なります。
したがって、患者の回復の鍵は、病気を早期に診断し、適切な時期に適切な治療を行うことです。
コメントを追加する