Nátrium-tioszulfát. Nátrium-tioszulfát Nátrium-tioszulfát kémiai képlete
A nátrium-tioszulfát halogénekkel, nehézfémsókkal és cianidokkal alacsony toxikus vagy nem toxikus vegyületeket képez. A nátrium-tioszulfát benzol, anilin, jód, higany, réz, hidrogén-cianid, fenolok, szublimát ellenszere. Ólom-, higany- és arzénvegyületekkel történő mérgezés esetén nem mérgező szulfitok keletkeznek. Hidrociánsavval és sóival történő mérgezés esetén a fő méregtelenítési mechanizmus a tiocianát ion képződése (amely viszonylag nem mérgező) cianidból a rodonáz - tioszulfát-cianid szeratranszferáz enzim részvételével (ez az enzim számos szövetben jelen van) , de a májban a legaktívabb). A szervezet maga is képes a cianid méregtelenítésére, de a rodonáz rendszer lassan működik, és ciánmérgezés esetén aktivitása nem elegendő a méregtelenítéshez. Ebben az esetben a reakció felgyorsításához exogén kéndonorokra, általában nátrium-tioszulfátra van szükség, amelyet a rodonáz katalizál.
A nátrium-tioszulfát rüh elleni hatása annak a képességének köszönhető, hogy savas környezetben kén-dioxidot és ként képződik, amelyek káros hatással vannak a rühes atkára és annak tojásaira.
A nátrium-tioszulfátot alkoholos delíriumban szenvedő betegeknél alkalmazzák a méregtelenítő szerek komplexének részeként.
Intravénás beadáskor a nátrium-tioszulfát eloszlik az extracelluláris folyadékban, és változatlan formában ürül a vizelettel. A biológiai felezési idő 0,65 óra. A nátrium-tioszulfát nem mérgező. Kutyákon végzett vizsgálatokban hipovolémiát figyeltek meg nátrium-tioszulfát krónikus adagolásakor, ami nagy valószínűséggel a diuretikus ozmotikus hatásának köszönhető.
Javallatok
Arzén, higany, ólom, jód sói, bróm, cianid és hidrogén-cianid mérgezése; ízületi gyulladás; neuralgia; allergiás betegségek; rüh.
A nátrium-tioszulfát alkalmazásának módja és adagja
A nátrium-tioszulfátot intravénásan, orálisan, külsőleg alkalmazzák. Mérgezés: intravénásan - 5-50 ml (a mérgezés súlyosságától és típusától függően) 30% -os oldat vagy orálisan - 10% -os oldat formájában, 2-3 g adagonként. Rüh: dörzsölje be 60%-os oldattal a végtagok és a törzs bőrét, majd szárítás után nedvesítse be 6%-os sósavoldattal.
Ciánmérgezés során az ellenszer beadásakor kerülni kell a késleltetést (mivel lehetséges a gyors halál). A beteg gondos megfigyelése 1-2 napig szükséges, mivel a cianidmérgezés jelei visszatérhetnek. Ha a cianidmérgezés tünetei visszatérnek, a nátrium-tioszulfátot a dózis felével kell újra beadni.
A használat ellenjavallatai
Túlérzékenység.
Használati korlátozások
Nincs adat.
Használata terhesség és szoptatás alatt
A nátrium-tioszulfát alkalmazása terhesség és szoptatás alatt csak akkor lehetséges, ha feltétlenül szükséges. Nátrium-tioszulfáttal állatokon nem végeztek szaporodási vizsgálatokat. Nem ismert, hogy a nátrium-tioszulfát befolyásolhatja-e a reprodukciót és káros magzati hatásokat okoz-e, ha terhes nők szedik.
Gyógyszerelemek VI És IV az elemek periódusos rendszerének csoportjai.
KÉNVEGYÜLETEK ELEMZÉSE. 6 CSOPORT PSE.
Az emberi szervezetben a kén az epidermiszben, a bőrben, az izmokban, a hasnyálmirigyben és a hajban található. Egyes aminosavak (metionin, cisztein), peptidek része, amelyek részt vesznek a szöveti légzés folyamataiban és katalizálják az enzimatikus folyamatokat.
Az orvostudományban magát a ként kenőcsök és nátrium-tioszulfát formájában használják.
Nátrium-tioszulfát Natrii tioszulfák (ln)
Na 2 S 2 O 3 5 H 2 ONátriumtioszulfát (MHH)
A tiokénsav nátriumsója
Szerkezeti képlet:
A kénatomok különböző oxidációs állapotúak. Az S 2 miatt - LB helyreállító tulajdonságokkal rendelkezik.
Nyugta
Nátrium-szulfit és kén melegítésekor ( először 1799-ben szerezték be):
Na 2 SO 3 + S → Na 2 S 2 O 3
Nátrium-szulfid oxidációja kén-dioxiddal:
2Na 2 S+ 3S0 2 → 2Na 2 S 2 0 3 +S↓
Jelenleg felhasználásával nyerik hidrogén-szulfidot tartalmazó gáztermelési hulladék. A módszer többlépcsős jellege ellenére gazdaságilag előnyös:
A hidrogén-szulfidot egy abszorber - kalcium-hidroxid - rögzíti:
Ca(OH) 2 + H 2 S → CaS + 2H 2 S
azonban a kalcium-szulfid hidrolízise következtében a következő reakciók lépnek fel:
CaS + 2H 2 O → Ca(OH) 2 + H 2 S
2Ca(OH)2 + 3H2S → CaS + Ca(SH)2 + 4H2O
A kalcium-hidroszulfidot a légköri oxigén kalcium-tioszulfáttá oxidálja:
Ca(SH) 2 + 2O 2 → CaS 2 O 3 + H 2 O
a kalcium-tioszulfát kalcium-karbonáttal van összeolvasztva:
CaS 2 O 3 + Na 2 CO 3 → Na 2 S 2 O 3 + CaCO 3 ↓
Leírás és oldhatóság
Színtelen átlátszó kristályok, szagtalanok. Meleg, száraz levegőben kristályvizet veszít (erózus). Nedves levegőn szétterül (folyékony halmazállapotúvá válik). +50 0 C hőmérsékleten kristályosodási vízben megolvad.
Vízben nagyon könnyen oldódik, alkoholban gyakorlatilag nem oldódik.
Kémiai tulajdonságok
A képletből látható, hogy a kén oxidációs állapota eltérő (6+ és 2-). Mivel a molekulában S2- van, a gyógyszer helyreállító tulajdonságokat mutat.
A nátrium-tioszulfát, akárcsak a tiokénsav, amelynek sója, nem erős vegyület, könnyen lebomlanak savak hatására, akár szénsavas (levegőnedvesség + szén-dioxid):
Na 2 S 2 O 3 + CO 2 + H 2 O → Na 2 CO 3 + H 2 S 2 O 3
H 2 S 2 O 3 → S↓ + SO 2 + H 2 O
sárga szag
üledék (zavarosság)
Ezt a tulajdonságot hitelességi reakciókban használják:
Hitelesség
Reakciók nátriumionra(lásd katin anionok).
Reakciók tioszulfát ionra:
Bomlási reakció hígított sósavval ha híg sósavat adunk a gyógyszer oldatához, az oldat fokozatosan zavarossá válik - szabad kén szabadul fel (ellentétben a kénsav sóival), majd a kén-dioxid SO 2 sajátos szaga jelenik meg:
Na 2 S 2 O 3 + 2HCl → 2NaCl + SO 2 + S↓+ H 2 O
sárga szaga
üledék (zavarosság)
S 2 O 3 2- + H 2 O - 2ē → 2SO 2 + 2H +
S 2 O 3 2- + 6H + + 4ē → 2S↓ + 3H 2 O
Reakció ezüst-nitrát oldattal.
Ha több ezüst-nitrátot adunk hozzá, fehér csapadék szabadul fel, amely gyorsan sárgul, állás közben megbarnul, végül az ezüst-szulfid képződése miatt feketévé válik.
Először fehér ezüst-tioszulfát csapadék képződik:
Na 2 S 2 O 3 + 2AgN0 3 → Ag 2 S 2 O 3 ↓ + 2NaN0 3
Az ezüst-tioszulfát gyorsan lebomlik (intramolekuláris redox reakció), ezüst-szulfit és kén képződik (sárga csapadék):
Ag 2 S 2 O 3 → Ag 2 SO 3 ↓ + S↓
Állás közben fekete ezüst-szulfid csapadék képződik:
Ag 2 SO 3 + S + H 2 O → Ag 2 S↓ + H 2 SO 4
Ha a reakcióeljárást megváltoztatjuk - nátrium-tioszulfátot adunk az ezüst-nitrát oldathoz, akkor az ezüst-tioszulfát fehér csapadéka feloldódik a nátrium-tioszulfát feleslegében:
Ag 2 S 2 O 3 + 3Na 2 S 2 O 3 → 2Na 3
A nátrium-tioszulfát egy szintetikus vegyület, amely a kémiában nátrium-szulfátként, az élelmiszeriparban pedig E539 adalékanyagként ismert, élelmiszergyártásban való felhasználásra engedélyezett.
A nátrium-tioszulfát savasságot szabályozó (antioxidáns), csomósodást gátló vagy tartósítószerként funkcionál. A tioszulfát élelmiszer-adalékanyagként történő használata lehetővé teszi az eltarthatóság és a termék minőségének növelését, valamint a rothadás, savanyúság és erjedés megelőzését. Ez az anyag tiszta formájában részt vesz az étkezési jódozott só előállításának technológiai folyamataiban, mint jódstabilizátor, és sütőliszt feldolgozására használják, amely hajlamos a csomósodásra és csomósodásra.
Az E539 élelmiszer-adalékanyag használata kizárólag az ipari szférára korlátozódik, az anyag kiskereskedelmi forgalomba nem kerül. Orvosi célokra a nátrium-tioszulfátot súlyos mérgezés ellenszereként, külső használatra pedig gyulladáscsökkentő szerként használják.
Általános információ
A tioszulfát (hiposzulfit) egy szervetlen vegyület, amely a tiokénsav nátriumsója. Az anyag színtelen, szagtalan por, mely alaposabb vizsgálat után átlátszó monoklin kristályoknak bizonyul.
A hiposzulfit instabil vegyület, amely a természetben nem fordul elő. Az anyag kristályos hidrátot képez, amely 40 °C fölé melegítve saját kristályos vizében megolvad és feloldódik. Az olvadt nátrium-tioszulfát túlhűl, és körülbelül 220 ° C-on a vegyület teljesen megsemmisül.
Nátrium-tioszulfát: szintézis
A nátrium-szulfátot először mesterségesen, a laboratóriumban, a Leblanc-módszerrel állították elő. Ez a vegyület a szódagyártás mellékterméke, amely a kalcium-szulfid oxidációjával képződik. Oxigénnel kölcsönhatásba lépve a kalcium-szulfid részben tioszulfáttá oxidálódik, amelyből nátrium-szulfát segítségével Na 2 S 2 O 3 -ot nyernek.
 A modern kémia számos módszert kínál a nátrium-szulfát szintézisére:
A modern kémia számos módszert kínál a nátrium-szulfát szintézisére:
- nátrium-szulfidok oxidációja;
- forrásban lévő kén nátrium-szulfittal;
- hidrogén-szulfid és kén-oxid kölcsönhatása nátrium-hidroxiddal;
- forrásban lévő ként nátrium-hidroxiddal.
A fenti módszerekkel a reakció melléktermékeként vagy vizes oldat formájában nátrium-tioszulfát állítható elő, amelyből a folyadékot el kell párologtatni. A nátrium-szulfát lúgos oldatát úgy állíthatjuk elő, hogy szulfidját oxigénes vízben oldjuk.
A tiszta, vízmentes tioszulfát vegyület nátriumsó és salétromsav és kén reakciójának eredménye egy formamid néven ismert anyagban. A szintézis reakciója 80 °C hőmérsékleten megy végbe, és körülbelül fél óráig tart, termékei a tioszulfát és annak oxidjai.
A hiposzulfit minden kémiai reakcióban erős redukálószerként működik. Erős oxidálószerekkel való reakciók során a Na 2 S 2 O 3 szulfáttá vagy kénsavvá oxidálódik, gyenge anyagokkal pedig tetrationsóvá. A tioszulfát oxidációs reakciója az anyagok meghatározására szolgáló jodometriás módszer alapja.
Külön figyelmet érdemel a nátrium-tioszulfát kölcsönhatása a szabad klórral, amely erős oxidálószer és mérgező anyag. A hiposzulfitot a klór könnyen oxidálja, és ártalmatlan vízoldható vegyületekké alakítja. Így ez a vegyület megakadályozza a klór pusztító és mérgező hatását.
Ipari körülmények között a tioszulfátot a gáztermelési hulladékból vonják ki. A legelterjedtebb nyersanyag a világítógáz, amely a szén kokszolása során szabadul fel, és hidrogén-szulfid szennyeződéseket tartalmaz. Kalcium-szulfidot szintetizálnak belőle, amelyet hidrolízisnek és oxidációnak vetnek alá, majd nátrium-szulfáttal kombinálva tioszulfátot állítanak elő. A többlépcsős eljárás ellenére ezt a módszert tartják a leginkább költséghatékony és környezetbarát módszernek a hiposzulfit kinyerésére.
| Szisztematikus név | Nátrium-tioszulfát |
|---|---|
| Hagyományos nevek | Nátrium-diszulfid, nátrium-hiposzulfit (nátrium) szóda, antiklór |
| Nemzetközi jelölés | E539 |
| Kémiai formula | Na2S2O3 |
| Csoport | Szervetlen tioszulfátok (sók) |
| Az összesítés állapota | Színtelen monoklin kristályok (por) |
| Oldhatóság | Benne oldódik, benne oldhatatlan |
| Olvadási hőmérséklet | 50 °C |
| Kritikus hőmérséklet | 220 °C |
| Tulajdonságok | Reduktív (antioxidáns), komplexképző |
| Étrend-kiegészítő kategória | Savanyúságot szabályozó szerek, csomósodást gátló szerek (csomósodásgátlók) |
| Eredet | Szintetikus |
| Toxicitás | Nem vizsgálták, az anyag feltételesen biztonságos |
| Felhasználási területek | Élelmiszer-, textil-, bőripar, fényképezés, gyógyszeripar, analitikai kémia |
Nátrium-tioszulfát: alkalmazás
 A nátrium-diszulfidot sokféle célra használták jóval azelőtt, hogy a vegyületet étrend-kiegészítőkbe és gyógyszerekbe foglalták volna. Az antiklórt gézkötések és gázmaszkszűrők impregnálására használták, hogy megvédjék a légzőrendszert a mérgező klórtól az első világháború idején.
A nátrium-diszulfidot sokféle célra használták jóval azelőtt, hogy a vegyületet étrend-kiegészítőkbe és gyógyszerekbe foglalták volna. Az antiklórt gézkötések és gázmaszkszűrők impregnálására használták, hogy megvédjék a légzőrendszert a mérgező klórtól az első világháború idején.
A hiposzulfit modern alkalmazási területei az iparban:
- fényképészeti film feldolgozása és képek fényképészeti papírra történő rögzítése;
- ivóvíz klórmentesítése és bakteriológiai elemzése;
- klórfoltok eltávolítása szövetek fehérítése során;
- aranyérc kilúgozás;
- rézötvözetek és patina gyártása;
- bőrcserzés.
A nátrium-szulfátot az analitikai és szerves kémiában reagensként használják, semlegesíti az erős savakat, semlegesíti a nehézfémeket és azok mérgező vegyületeit. A tioszulfát reakciói különböző anyagokkal a jodometria és a bromometria alapját képezik.
Élelmiszer-adalékanyag E539
A nátrium-tioszulfát nem széles körben használt élelmiszer-adalékanyag, és a vegyület instabilitása és bomlástermékeinek toxicitása miatt nem hozzáférhető szabadon. A hiposzulfit az étkezési jódozott só és sütőipari termékek előállításának technológiai folyamataiban, mint savtartalom-szabályozó és csomósodást gátló anyag.
Az E539 adalékanyag antioxidánsként és tartósítószerként működik a zöldség- és halkonzerv, desszertek és alkoholos italok gyártásában. Ez az anyag része a friss, szárított és fagyasztott zöldségek és gyümölcsök felületének kezelésére használt vegyszereknek is.
Az E539 tartósítószert és antioxidánst az ilyen termékek minőségének javítására és eltarthatóságának növelésére használják:
- friss és fagyasztott zöldségek, gyümölcsök, tenger gyümölcsei;
- , diófélék, magvak;
- Zöldségek, gombák és hínár, olajban vagy olajban konzerválva;
- lekvárok, zselék, kandírozott gyümölcsök, gyümölcspürék és töltelékek;
- friss, fagyasztott, füstölt és szárított hal, tenger gyümölcsei, konzervek;
- liszt, keményítők, szószok, fűszerek, ecet, ;
- fehér és cukornád, édesítőszerek (dextróz és), cukorszirupok;
- gyümölcs- és zöldséglevek, édes víz, alacsony alkoholtartalmú italok, szőlőitalok.
Az étkezési jódozott só előállítása során az E539 élelmiszer-adalékanyagot használják a jód stabilizálására, amely jelentősen meghosszabbíthatja a termék eltarthatóságát és megőrzi tápértékét. A konyhasóban az E539 maximális megengedett koncentrációja 250 mg/1 kg.
A sütés során a nátrium-tioszulfátot aktívan használják különféle adalékanyagok részeként a termék minőségének javítása érdekében. A sütést javító szerek vagy oxidatívak vagy reduktívak. Az E539 csomósodásgátló egy helyreállító javítószer, amely lehetővé teszi a tulajdonságok megváltoztatását.
A sűrű lisztből készült, rövidre szakadó glutént tartalmazó tészta nehezen feldolgozható, megsül, nem éri el a kívánt térfogatot és sütés közben megreped. Az E539 csomósodást gátló szer tönkreteszi a diszulfid kötéseket és strukturálja a sikérfehérjéket, aminek következtében a tészta jól megkel, a morzsa laza és rugalmas lesz, a kéreg nem reped meg sütés közben.
A vállalkozásoknál csomósodásgátló szert adnak a liszthez az élesztővel együtt közvetlenül a tészta dagasztása előtt. A liszt tioszulfát tartalma a pékáru gyártási technológiájától függően tömegének 0,001-0,002%-a. Az E539 adalék egészségügyi szabványa 50 mg/1 kg búzaliszt.
Az E539 csomósodásgátlót technológiai folyamatokban szigorú adagolásban alkalmazzák, így a liszttermékek fogyasztása során nem áll fenn a tioszulfát-mérgezés veszélye. A kiskereskedelmi értékesítésre szánt lisztet értékesítés előtt nem dolgozzák fel. A normál határokon belül a kiegészítő biztonságos és nincs mérgező hatása a szervezetre.
Használata az orvostudományban és hatása a szervezetre
A szóda-hiposzulfit az egyik leghatékonyabb és legbiztonságosabb gyógyszerként szerepel az Egészségügyi Világszervezet alapvető gyógyszerek listáján. Szubkután, intramuszkulárisan és intravénásan injekciós oldat formájában vagy külső szerként alkalmazzák.
A huszadik század elején a nátrium-tioszulfátot először a hidrogén-cianid-mérgezés ellenszereként használták. Nátrium-nitrittel kombinálva a tioszulfát különösen súlyos cianidmérgezés esetén javasolt, és intravénásan adják be, hogy a cianidot nem mérgező tiocianátokká alakítsák, amelyek biztonságosan kiürülhetnek a szervezetből.
A nátrium-szulfát orvosi felhasználása:
A hiposzulfit emberi szervezetre gyakorolt hatását szájon át fogyasztva nem vizsgálták, ezért lehetetlen megítélni az anyag előnyeit és ártalmait tiszta formában vagy élelmiszerek részeként. Az E539 adalékanyaggal nem történt mérgezés, ezért általában nem mérgezőnek tartják.
A nátrium-tioszulfát és a jogszabályok
A nátrium-tioszulfát szerepel azon élelmiszer-adalékanyagok listáján, amelyeket Oroszországban és Ukrajnában élelmiszergyártásra engedélyeztek. Az E539 csomósodásgátlót és savanyúságot szabályozó anyagot a megállapított egészségügyi és higiéniai szabványoknak megfelelően kizárólag ipari célokra használják.
Tekintettel arra, hogy a vegyi anyag emberi szervezetre gyakorolt hatását szájon át adva még nem vizsgálták, az E539 adalékanyag nem engedélyezett az EU-ban és az USA-ban.
Az orvosi gyakorlatban injekciós oldat formájában méregtelenítő és érzéketlenítő szerként vagy külsőleg rovarölő szerként, állatgyógyászatban bőrbetegségek elleni szerként, gyógyszeriparban gyógyszergyártásban; 30%-os nátrium-tioszulfát injekciós oldatok készítéséhez.Nátrium-tioszulfátot is használnak
- klórnyomok eltávolítására a szövetek fehérítése után
- ezüst ércekből való kinyerésére;
- rögzítő a fotózásban;
- reagens a jodometriában
- mérgezés ellenszere: As, Br, Hg és más nehézfémek, cianidok (tiocianáttá alakítja) stb.
- bélfertőtlenítéshez;
- rüh kezelésére (sósavval együtt);
- gyulladásgátló és égésgátló szer;
- molekulatömeg-meghatározási közegként használható a fagyáspont csökkentésével (krioszkópiai állandó 4,26°)
- az élelmiszeriparban E539 élelmiszer-adalékanyagként van bejegyezve.
- adalékok betonhoz.
- a szövetek jódtól való tisztítására
Leírás
Fizikai-kémiai jellemzők
Színtelen, átlátszó, szagtalan kristályokCsomagolás
Zsák 40 kg. Kiszerelés 1 kg. Zsák 35 kg. Zsák 0,5 kg. 1 kg-os zsák. 5 kg-os zsák. Zsák 10 kg.
Tárolás
Kiszerelés: egyenként 0,5 kg; 1 kg; 5 kg; 10 kg; 35 kg; 40 kg; 45 kg polietilén fóliából vagy polimer bevonatú csomagolópapírból készült zacskóban vagy zacskóban.
Tárolás: Száraz helyen, jól csomagolt edényekben. Felhasználhatósági idő - 5 év.
Gyógyszerkönyvi nátrium-tioszulfát, amelyet a róla elnevezett vegyi üzem állít elő. L.Ya. Karpova
| Tömegtört, % | Norma | |
|---|---|---|
| Na2S2O3*5H2O | 99,0-102,0 | |
| kalcium | nincs reakció | |
| szulfidok | kiállod a próbát | |
| szulfitok és szulfátok | Max. | 0,01 |
| kloridok | Max. | 0,005 |
| nehéz fémek | Max. | 0,001 |
| arzén, szelén | nincs reakció | |
| mirigy | Max. | 0,002 |
| lúgosság | a fenolftalein rózsaszín elszíneződésének hiánya | |
| Mikrobiológiai tisztaság | megfelel az Állami Alap XI. számának 2. számának 193. o |
- Termékkód: 264-01
- Elérhetőség: raktáron
Termikusan nagyon instabil:
Kénsav jelenlétében lebomlik:
Reagál lúgokkal:
Halogénekkel reagál:
Tiokénsav
Ha nátrium-szulfit vizes oldatát kénnel forraljuk, és a felesleges kén kiszűrése után hagyjuk kihűlni, akkor az oldatból színtelen átlátszó kristályok szabadulnak fel, amelyek összetételét a képlet fejezi ki. Ez az anyag a tiokénsav nátriumsója.
A tiokénsav instabil. Már szobahőmérsékleten szétesik. Sói, tioszulfátjai sokkal stabilabbak. Ezek közül a leggyakrabban használt nátrium-tioszulfát, más néven hiposzulfit.
Ha némi savat, például sósavat adunk a nátrium-tioszulfát oldatához, kén-dioxid szaga jelenik meg, és egy idő után a folyadék zavarossá válik a felszabaduló kéntől.
A nátrium-tioszulfát tulajdonságainak vizsgálata arra a következtetésre jut, hogy az összetételében lévő kénatomok eltérő oxidációs szinttel rendelkeznek: az egyik oxidációs foka +4, a másik 0. . Nátrium-tioszulfát - redukálószer . A klór, bróm és más erős oxidálószerek kénsavvá vagy sójává oxidálják.
Tioszulf, te vagy- tiokénsav sói és észterei, H2S2O3. A tioszulfátok instabilak, ezért a természetben nem fordulnak elő. A legszélesebb körben használt nátrium-tioszulfát és ammónium-tioszulfát.
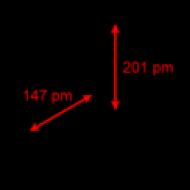
Szerkezet. A tioszulfát ion szerkezete

A tioszulfátion szerkezetében közel áll a szulfátionhoz. A 2− tetraéderben az S-S kötés (1,97A) hosszabb, mint az S-O kötések
Nátrium-tioszulfát meglehetősen instabil anyagok közé sorolhatók. A nátrium-tioszulfát 220°C-ra melegítve bomlik: A nátrium-tioszulfát hőbomlási reakciójában nátrium-poliszulfidot kapunk, amely szintén tovább bomlik nátrium-szulfiddá és elemi kénné. Kölcsönhatás savakkal: a tiokénsavat (hidrogén-tioszulfátot) nem lehet izolálni nátrium-tioszulfát és erős sav reakciójával, mivel instabil és azonnal lebomlik: A sósav és a salétromsav is ugyanazon a reakción megy keresztül. A bomlást kellemetlen szagú váladék kíséri.
A nátrium-tioszulfát redox tulajdonságai: a 0 oxidációs állapotú kénatomok jelenléte miatt a tioszulfát ion redukáló tulajdonságokkal rendelkezik, például gyenge oxidálószerekkel (I2, Fe3+) a tioszulfát tetrationát ionná oxidálódik: Lúgos környezetben az oxidáció nátrium-tioszulfát jóddal szulfáttá alakulhat.
Az erősebb oxidálószerek pedig szulfátionokká oxidálják :
Erős redukálószerek Az ion S2-származékokká redukálódik: A körülményektől függően a nátrium-tioszulfát oxidáló és redukáló tulajdonságokat is mutathat.
A tioszulfátok komplexképző tulajdonságai:
A tioszulfát ion erős komplexképző szer , a fényképezésben a redukálatlan ezüst-bromid fotófilmről való eltávolítására használják: Az S2O32 iont fémek koordinálják egy kénatomon keresztül, így a tioszulfát komplexek könnyen átalakulnak a megfelelő szulfidokká.
A nátrium-tioszulfát alkalmazásai
A nátrium-tioszulfátot meglehetősen széles körben használják mind a mindennapi életben, mind az iparban. A nátrium-tioszulfát fő alkalmazási területei az orvostudomány, a textilipar és a bányászat, valamint a fotózás lesz.
A nátrium-tioszulfátot a textil- és papíriparban használják a klórnyomok eltávolítására a szövetek és a papír fehérítése után, a bőrgyártásban pedig krómsav-csökkentőként.
A bányászatban nátrium-tioszulfátot használnak az ezüst kinyerésére alacsony ezüstkoncentrációjú ércekből. Az ezüst tioszulfátokkal alkotott összetett vegyületei meglehetősen stabilak, legalábbis stabilabbak, mint a fluorral, klórral, bromidokkal és tiocianátokkal alkotott összetett vegyületek. Ezért az ezüst izolálása a készítmény oldható komplex vegyülete formájában vagy iparilag jövedelmező. Dolgoznak az aranykitermelésben való felhasználásán. De ebben az esetben a komplex vegyület instabilitási állandója sokkal magasabb, és a komplexek kevésbé stabilak az ezüsthöz képest.
A nátrium-tioszulfátot először az orvostudományban használták fel. És a mai napig nem veszítette el jelentőségét az orvostudományban. Igaz, számos betegség kezelésére találtak már más, hatékonyabb gyógyszereket, így a nátrium-tioszulfátot szélesebb körben kezdték alkalmazni az állatgyógyászatban. A nátrium-tioszulfátot az orvostudományban ellenszerként használják arzénnal, higannyal és más nehézfémekkel, cianidokkal való mérgezés ellen (tiocianátokká alakítja őket):
Mint fentebb említettük, a tioszulfát ion sok fémmel, köztük sok mérgező nehézfémmel, stabil komplex vegyületeket hoz létre. A létrejövő komplex vegyületek alacsony toxikusak és kiürülnek a szervezetből. A nátrium-tioszulfát ezen tulajdonsága az alapja a toxikológiában és a mérgezések kezelésében való alkalmazásának.
A nátrium-tioszulfátot ételmérgezés esetén a belek fertőtlenítésére, a rüh kezelésére is használják (sósavval együtt), gyulladáscsökkentő és égésgátló szerként.
A nátrium-tioszulfátot széles körben használják az analitikai kémiában, mivel reagens a jodometriában. A jodometria az anyagok koncentrációjának kvantitatív meghatározásának és a jódkoncentráció meghatározásának egyik módszere, redox reakciót alkalmaznak nátrium-tioszulfáttal:
A nátrium-tioszulfát végső, meglehetősen gyakori felhasználási módja a fényképezésben történő rögzítés. És bár a közönséges fekete-fehér fényképezés már átadta helyét a színesnek, és a hétköznapi fényképezőfilmet meglehetősen ritkán, sok tekintetben elmaradva a digitális képrögzítéstől, jó néhány helyen még mindig használnak fotólemezeket és fotófilmet. Ilyenek például az orvosi és ipari röntgengépek, a tudományos berendezések és a fototeleszkópok.
Ahhoz, hogy fényképes képet kapjunk, elegendő, ha a fotófilmben lévő ezüst-bromid körülbelül 25%-a kifejlődik. A többi része pedig a fotófilmben marad, és megőrzi fényérzékenységét. Ha a fotófilmet előhívás után kivesszük a fényre, akkor a benne maradó előhívatlan halogénezüstet az előhívó előhívja és a negatív elsötétül. Még ha az összes előhívót ki is mossuk, a negatív valahogy elsötétül a fényben az ezüsthalogenid bomlása miatt.
A kép megőrzéséhez a filmen el kell távolítani róla a fejletlen ezüst halogént. Ehhez képrögzítési eljárást alkalmaznak, melynek során az ezüsthalogenideket oldható vegyületekké alakítják, és kimossák a filmről vagy fényképről. A kép rögzítésére nátrium-tioszulfátot használnak.
Az oldatban lévő nátrium-tioszulfát koncentrációjától függően különféle vegyületek képződnek. Ha a fixáló oldat kis mennyiségű tioszulfátot tartalmaz, akkor a reakció a következő egyenlet szerint megy végbe:
A keletkező ezüst-tioszulfát vízben nem oldódik, ezért nehéz elkülöníteni a fotorétegtől, meglehetősen instabil és kénsav felszabadulásával bomlik:
Az ezüst-szulfid elfeketíti a képet, és nem távolítható el a fotórétegről.
Ha az oldatban feleslegben van nátrium-tioszulfát, összetett ezüstsók képződnek:
A kapott komplex só, a nátrium-tioszulfát-argentát meglehetősen stabil, de vízben rosszul oldódik.
Ha az oldatban nagy feleslegben van tioszulfát, akkor vízben jól oldódó összetett ezüst komplex sók képződnek:
A nátrium-tioszulfát ezen tulajdonságai az alapja annak, hogy fixálószerként használják a fényképezésben.
Tetratnopinsav a polinoid savak csoportjába tartozik. Ezek általános képletű kétbázisú savak, ahol 2 és 6 közötti értékeket vehetnek fel, és esetleg többet is. Polnitionsavak instabil és csak vizes oldatokban ismert. A politiosavak sói – a politionátok – stabilabbak; egy részüket kristályok formájában kapják meg.
Politionsavak - H2SnO6 általános képletű kénvegyületek, ahol n>=2. Sóikat politionátoknak nevezik.

Tetrationát ion a tioszulfát ion jóddal történő oxidációjával nyerhető (a reakciót a jodometriában használják):
Pentationate ion SCl2 hatásával a tioszulfát ionra és Wackenroder-féle folyadékból kálium-acetát hozzáadásával nyerik. Először a kálium-tetrationát prizmás kristályai hullanak ki, majd a kálium-pentationát lemezszerű kristályai, amelyekből borkősav hatására pentationsav vizes oldata keletkezik.
Kálium-hexationát K2S6O6 a legjobban a KNO2 K2S2O3-on történő hatására szintetizálható tömény sósavban alacsony hőmérsékleten.