महिलाओं, पुरुषों और बच्चों में डायबिटीज इन्सिपिडस। बच्चों में मधुमेह मेलिटस इडियोपैथिक मधुमेह मेलिटस
7.1. मधुमेह मेलिटस का वर्गीकरण
मधुमेह(डीएम) बिगड़ा हुआ स्राव और/या इंसुलिन क्रिया की दक्षता के कारण हाइपरग्लेसेमिया द्वारा विशेषता चयापचय रोगों का एक समूह है। क्रोनिक हाइपरग्लेसेमिया, जो मधुमेह के साथ विकसित होता है, कई अंगों और प्रणालियों से जटिलताओं के विकास के साथ होता है, मुख्य रूप से हृदय, रक्त वाहिकाओं, आंखों, गुर्दे और तंत्रिकाओं से। कुल मिलाकर 5-6% आबादी मधुमेह से पीड़ित है। दुनिया के आर्थिक रूप से विकसित देशों में हर 10-15 साल में मधुमेह के रोगियों की संख्या दोगुनी हो जाती है। मधुमेह के साथ जीवन प्रत्याशा 10-15% कम हो जाती है।
मधुमेह के कारण व्यापक रूप से भिन्न होते हैं। अधिकांश मामलों में, मधुमेह या तो इंसुलिन की पूर्ण कमी के कारण विकसित होता है (मधुमेह मेलिटस प्रकार 1 -डीएम-1), या अग्नाशयी β-कोशिकाओं के स्रावी शिथिलता के साथ संयोजन में इंसुलिन के प्रति परिधीय ऊतकों की संवेदनशीलता में कमी के कारण (मधुमेह मेलिटस प्रकार 2 -एसडी-2). कुछ मामलों में, किसी मरीज को डीएम-1 या डीएम-2 के रूप में वर्गीकृत करना मुश्किल है; हालांकि, व्यवहार में, इसके प्रकार की सटीक पहचान करने के बजाय, डीएम के लिए मुआवजा अधिक महत्वपूर्ण है। एटिऑलॉजिकल वर्गीकरण मधुमेह के चार मुख्य नैदानिक वर्गों की पहचान करता है (तालिका 7.1)।
सबसे आम डीएम-1 (खंड 7.5), डीएम-2 (खंड 7.6) और गर्भकालीन डीएम (खंड 7.9) पर अलग-अलग अध्यायों में चर्चा की गई है। पर अन्य विशिष्ट प्रकारयह मधुमेह के केवल 1% मामलों के लिए जिम्मेदार है। इस प्रकार के मधुमेह के एटियलजि और रोगजनन का मधुमेह 1 और विशेष रूप से मधुमेह 2 की तुलना में अधिक अध्ययन किया गया प्रतीत होता है। कई डीएम प्रकार मोनोजेनिक रूप से विरासत में मिले कारणों से होते हैं कार्य में आनुवंशिक दोषβ -कोशिकाएं।इसमें ऑटोसोमल प्रमुखता से विरासत में मिले MODY सिंड्रोम के विभिन्न प्रकार शामिल हैं। जवान की परिपक्वता शुरुआत मधुमेह- युवा लोगों में वयस्क प्रकार का मधुमेह), जो उल्लंघन की विशेषता है, लेकिन परिधीय ऊतकों की सामान्य संवेदनशीलता के साथ इंसुलिन स्राव की अनुपस्थिति नहीं है।
मेज़ 7.1.मधुमेह मेलिटस का वर्गीकरण
आकस्मिक रूप से दुर्लभ इंसुलिन क्रिया में आनुवंशिक दोष,इंसुलिन रिसेप्टर (कुष्ठ रोग, रबसन-मैंडेहॉल सिंड्रोम) के उत्परिवर्तन के साथ जुड़ा हुआ है। डीएम स्वाभाविक रूप से विकसित होता है एक्सोक्राइन अग्न्याशय के रोग,β-कोशिकाओं (अग्नाशयशोथ, अग्नाशयशोथ, सिस्टिक फाइब्रोसिस, हेमोक्रोमैटोसिस) के विनाश के साथ-साथ कई अंतःस्रावी रोगों में, जिनमें काउंटरिनसुलर हार्मोन का अत्यधिक उत्पादन होता है (एक्रोमेगाली, कुशिंग सिंड्रोम)। औषधियाँ एवं रसायन(वैकोर, पेंटामिडाइन, निकोटिनिक एसिड, डायज़ॉक्साइड, आदि) शायद ही कभी मधुमेह का कारण बनते हैं, लेकिन इंसुलिन प्रतिरोध वाले व्यक्तियों में रोग की अभिव्यक्ति और विघटन में योगदान कर सकते हैं। पंक्ति संक्रामक रोग(रूबेला, साइटोमेगाली, कॉक्ससैकीवायरस और एडेनोवायरस संक्रमण) के साथ β-कोशिकाएं नष्ट हो सकती हैं, जबकि अधिकांश रोगियों में डीएम-1 के इम्युनोजेनेटिक मार्कर पाए जाते हैं। को प्रतिरक्षा-मध्यस्थता मधुमेह के दुर्लभ रूपइसमें "स्टिफ-आरएन" सिंड्रोम (एक ऑटोइम्यून न्यूरोलॉजिकल बीमारी) वाले रोगियों में विकसित होने वाली मधुमेह, साथ ही इंसुलिन रिसेप्टर्स के लिए ऑटोएंटीबॉडी के संपर्क के कारण मधुमेह शामिल है। बढ़ती आवृत्ति के साथ मधुमेह के विभिन्न रूप सामने आते हैं
कई आनुवंशिक सिंड्रोम, विशेष रूप से, डाउन सिंड्रोम, क्लाइनफेल्टर सिंड्रोम, टर्नर सिंड्रोम, वोल्फ्राम सिंड्रोम, प्रेडर-विली सिंड्रोम और कई अन्य।
7.2. कार्बोहाइड्रेट चयापचय के शरीर क्रिया विज्ञान के नैदानिक पहलू
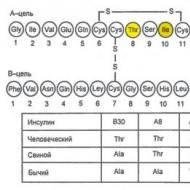
इंसुलिनअग्न्याशय (पीएलआई) के लैंगरहैंस के आइलेट्स की β-कोशिकाओं द्वारा संश्लेषित और स्रावित किया जाता है। इसके अलावा, लैंगरहैंस के आइलेट्स ग्लूकागन (α कोशिकाएं), सोमैटोस्टैटिन (δ कोशिकाएं) और अग्नाशयी पॉलीपेप्टाइड (पीपी कोशिकाएं) का स्राव करते हैं। आइलेट सेल हार्मोन एक दूसरे के साथ परस्पर क्रिया करते हैं: ग्लूकागन सामान्य रूप से इंसुलिन स्राव को उत्तेजित करता है, और सोमैटोस्टैटिन इंसुलिन और ग्लूकागन के स्राव को दबा देता है। इंसुलिन अणु में दो पॉलीपेप्टाइड श्रृंखलाएं होती हैं (ए श्रृंखला - 21 अमीनो एसिड; बी श्रृंखला - 30 अमीनो एसिड) (चित्र 7.1)। इंसुलिन संश्लेषण प्रीप्रोइन्सुलिन के निर्माण के साथ शुरू होता है, जो प्रोटीज़ द्वारा विखंडित होकर बनता है प्रोइंसुलिनगोल्गी तंत्र के स्रावी कणिकाओं में, प्रोइन्सुलिन इंसुलिन में टूट जाता है और सी-पेप्टाइड,जो एक्सोसाइटोसिस की प्रक्रिया के दौरान रक्त में छोड़े जाते हैं (चित्र 7.2)।
इंसुलिन स्राव का मुख्य उत्प्रेरक ग्लूकोज है। रक्त शर्करा के स्तर में वृद्धि की प्रतिक्रिया में इंसुलिन जारी होता है दो चरण(चित्र 7.3)। पहला, या तीव्र, चरण कई मिनटों तक चलता है, और संचित की रिहाई से जुड़ा होता है
 चावल। 7.1.इंसुलिन अणु की प्राथमिक संरचना का आरेख
चावल। 7.1.इंसुलिन अणु की प्राथमिक संरचना का आरेख
 चावल। 7.2.इंसुलिन जैवसंश्लेषण योजना
चावल। 7.2.इंसुलिन जैवसंश्लेषण योजना
भोजन के बीच की अवधि के दौरान β-कोशिका में मौजूद इंसुलिन। दूसरा चरण तब तक जारी रहता है जब तक ग्लाइसेमिक स्तर सामान्य उपवास स्तर (3.3-5.5 mmol/l) तक नहीं पहुंच जाता। सल्फोनीलुरिया का β-कोशिका पर समान प्रभाव पड़ता है।
पोर्टल प्रणाली के माध्यम से इंसुलिन पहुंचता है जिगर- इसका मुख्य लक्ष्य अंग. लीवर रिसेप्टर्स स्रावित हार्मोन के आधे हिस्से को बांधते हैं। दूसरा आधा हिस्सा, प्रणालीगत परिसंचरण में प्रवेश करके, मांसपेशियों और वसा ऊतक तक पहुंचता है। अधिकांश इंसुलिन (80%) यकृत में प्रोटियोलिटिक टूटने से गुजरता है, बाकी गुर्दे में, और केवल थोड़ी मात्रा सीधे मांसपेशियों और वसा कोशिकाओं द्वारा चयापचय की जाती है। जीवनकाल सामान्य है
 चावल। 7.3.ग्लूकोज के प्रभाव में इंसुलिन का द्विचरणीय स्राव
चावल। 7.3.ग्लूकोज के प्रभाव में इंसुलिन का द्विचरणीय स्राव
एक वयस्क व्यक्ति प्रतिदिन 35-50 यूनिट इंसुलिन स्रावित करता है, जो शरीर के वजन के प्रति 1 किलोग्राम पर 0.6-1.2 यूनिट है। इस स्राव को पोषणीय और बेसल में विभाजित किया गया है। भोजन स्रावइंसुलिन ग्लूकोज के स्तर में भोजन के बाद वृद्धि से मेल खाता है, यानी। इससे भोजन का हाइपरग्लेसेमिक प्रभाव निष्प्रभावी हो जाता है। आहार इंसुलिन की मात्रा लगभग ली गई कार्बोहाइड्रेट की मात्रा से मेल खाती है - लगभग 1-2.5 इकाइयाँ
10-12 ग्राम कार्बोहाइड्रेट के लिए (1 ब्रेड यूनिट - XE)। बेसल इंसुलिन स्रावभोजन के बीच और नींद के दौरान ग्लाइसेमिया और उपचय का इष्टतम स्तर प्रदान करता है। बेसल इंसुलिन लगभग 1 यू/एच की दर से स्रावित होता है; लंबे समय तक शारीरिक गतिविधि या लंबे समय तक उपवास के साथ, यह काफी कम हो जाता है। आहार इंसुलिन दैनिक इंसुलिन उत्पादन का कम से कम 50-70% होता है (चित्र 7.4)।
इंसुलिन का स्राव सिर्फ भोजन से ही नहीं, बल्कि इससे भी प्रभावित होता है दैनिक
 चावल। 7 .4.
सामान्य दैनिक इंसुलिन उत्पादन पैटर्न
चावल। 7 .4.
सामान्य दैनिक इंसुलिन उत्पादन पैटर्न
कोई उतार-चढ़ाव:सुबह के समय इंसुलिन की आवश्यकता बढ़ जाती है और फिर पूरे दिन धीरे-धीरे कम होती जाती है। तो, नाश्ते में प्रति 1 XE में 2.0-2.5 यूनिट इंसुलिन स्रावित होता है, दोपहर के भोजन के लिए - 1.0-1.5 यूनिट, और रात के खाने के लिए - 1.0 यूनिट। इंसुलिन संवेदनशीलता में इस बदलाव का एक कारण सुबह के समय कई काउंटर-इंसुलर हार्मोन (मुख्य रूप से कोर्टिसोल) का उच्च स्तर है, जो रात की शुरुआत में धीरे-धीरे न्यूनतम हो जाता है।
मुख्य इंसुलिन के शारीरिक प्रभावइंसुलिन पर निर्भर ऊतकों की कोशिका झिल्लियों में ग्लूकोज स्थानांतरण की उत्तेजना होती है। इंसुलिन के लिए मुख्य लक्ष्य अंग यकृत, वसा ऊतक और मांसपेशियां हैं। इंसुलिन-स्वतंत्र ऊतक, जिसमें ग्लूकोज की आपूर्ति इंसुलिन के प्रभाव पर निर्भर नहीं होती है, में मुख्य रूप से केंद्रीय और परिधीय तंत्रिका तंत्र, संवहनी एंडोथेलियम, रक्त कोशिकाएं आदि शामिल हैं। इंसुलिन यकृत और मांसपेशियों में ग्लाइकोजन के संश्लेषण को उत्तेजित करता है, यकृत और वसा ऊतक में वसा का संश्लेषण, यकृत, मांसपेशियों और अन्य अंगों में संश्लेषण प्रोटीन। इन सभी परिवर्तनों का उद्देश्य ग्लूकोज का उपयोग करना है, जिससे रक्त में इसके स्तर में कमी आती है। इंसुलिन का एक शारीरिक प्रतिपक्षी है ग्लूकागन,जो डिपो से ग्लाइकोजन और वसा के एकत्रीकरण को उत्तेजित करता है; आम तौर पर, ग्लूकागन का स्तर इंसुलिन उत्पादन के साथ पारस्परिक रूप से बदलता है।
इंसुलिन के जैविक प्रभाव इसके द्वारा मध्यस्थ होते हैं रिसेप्टर्सजो लक्ष्य कोशिकाओं पर स्थित होते हैं। इंसुलिन रिसेप्टर एक ग्लाइकोप्रोटीन है जिसमें चार सबयूनिट होते हैं। रक्त में इंसुलिन के उच्च स्तर के साथ, डाउन रेगुलेशन के सिद्धांत के अनुसार इसके रिसेप्टर्स की संख्या कम हो जाती है, जिसके साथ इंसुलिन के प्रति कोशिका की संवेदनशीलता में कमी आती है। इंसुलिन सेलुलर रिसेप्टर से बंधने के बाद, परिणामी कॉम्प्लेक्स कोशिका में प्रवेश करता है। मांसपेशियों और वसा कोशिकाओं के अंदर, इंसुलिन इंट्रासेल्युलर पुटिकाओं की गतिशीलता का कारण बनता है ग्लूकोज ट्रांसपोर्टरग्लूट-4. परिणामस्वरूप, पुटिकाएं कोशिका की सतह पर चली जाती हैं, जहां GLUT-4 ग्लूकोज के लिए प्रवेश बिंदु के रूप में कार्य करता है। शारीरिक गतिविधि का GLUT-4 पर समान प्रभाव पड़ता है।
7.3. मधुमेह मेलेटस के लिए प्रयोगशाला निदान और मुआवजा मानदंड
मधुमेह का प्रयोगशाला निदान रक्त शर्करा के स्तर को निर्धारित करने पर आधारित है, और निदान मानदंड सभी के लिए समान हैं
एसडी के प्रकार और प्रकार (तालिका 7.2)। मधुमेह के निदान को सत्यापित करने के लिए अन्य प्रयोगशाला परीक्षणों (ग्लूकोसुरिया स्तर, ग्लाइकेटेड हीमोग्लोबिन स्तर का निर्धारण) के डेटा का उपयोग नहीं किया जाना चाहिए। मधुमेह का निदान किसी एक की दोहरी पहचान के आधार पर स्थापित किया जा सकता है तीन मानदंड:
1. मधुमेह (पॉलीयूरिया, पॉलीडिप्सिया) के स्पष्ट लक्षणों के साथ और पूरे केशिका रक्त में ग्लूकोज का स्तर 11.1 mmol/l से अधिक है, दिन के समय और पिछले भोजन की परवाह किए बिना।
2. जब उपवास करने वाले पूरे केशिका रक्त में ग्लूकोज का स्तर 6.1 mmol/l से अधिक हो।
3. जब 75 ग्राम ग्लूकोज (मौखिक ग्लूकोज सहिष्णुता परीक्षण) लेने के 2 घंटे बाद पूरे केशिका रक्त में ग्लूकोज का स्तर 11.1 mmol/l से अधिक हो।
मेज़ 7.2.मधुमेह मेलेटस के निदान के लिए मानदंड
 मधुमेह के निदान में सबसे महत्वपूर्ण और महत्वपूर्ण परीक्षण उपवास ग्लाइसेमिया के स्तर (न्यूनतम 8 घंटे का उपवास) निर्धारित करना है। रूसी संघ में, ग्लाइसेमिक स्तर का मूल्यांकन आमतौर पर पूरे रक्त में किया जाता है। कई देशों में ग्लूकोज परीक्षण का व्यापक रूप से उपयोग किया जाता है
मधुमेह के निदान में सबसे महत्वपूर्ण और महत्वपूर्ण परीक्षण उपवास ग्लाइसेमिया के स्तर (न्यूनतम 8 घंटे का उपवास) निर्धारित करना है। रूसी संघ में, ग्लाइसेमिक स्तर का मूल्यांकन आमतौर पर पूरे रक्त में किया जाता है। कई देशों में ग्लूकोज परीक्षण का व्यापक रूप से उपयोग किया जाता है
रक्त प्लाज्मा में. मौखिक ग्लूकोज सहनशीलता परीक्षण(ओजीटीटी; पानी में घुले 75 ग्राम ग्लूकोज के सेवन के 2 घंटे बाद ग्लूकोज के स्तर का निर्धारण) को इस संबंध में कम महत्व दिया जाता है। हालाँकि, OGTT के आधार पर इसका निदान किया जाता है क्षीण ग्लूकोज सहनशीलता(एनटीजी)। आईजीटी का निदान तब किया जाता है जब उपवास वाले पूरे केशिका रक्त का ग्लूकोज स्तर 6.1 mmol/l से अधिक न हो, और ग्लूकोज लोड के 2 घंटे बाद यह 7.8 mmol/l से ऊपर हो, लेकिन 11.1 mmol/l से नीचे हो। कार्बोहाइड्रेट चयापचय विकार का एक अन्य प्रकार है खाली पेट होने के समय शर्करा में खराबी(एनजीएनटी)। उत्तरार्द्ध स्थापित किया गया है यदि खाली पेट पर पूरे केशिका रक्त के ग्लाइसेमिया का स्तर 5.6-6.0 mmol/l की सीमा में है, और ग्लूकोज लोड के 2 घंटे बाद 7.8 mmol/l से कम है)। एनटीजी और एनजीएनटी वर्तमान में इस शब्द के तहत संयुक्त हैं प्रीडायबिटीज,चूँकि दोनों श्रेणियों के रोगियों में मधुमेह प्रकट होने और मधुमेह मैक्रोएंगियोपैथी विकसित होने का उच्च जोखिम होता है।
मधुमेह का निदान करने के लिए, ग्लाइसेमिक स्तर को मानक प्रयोगशाला विधियों द्वारा निर्धारित किया जाना चाहिए। ग्लाइसेमिक मूल्यों की व्याख्या करते समय, यह ध्यान में रखा जाना चाहिए कि पूरे शिरापरक रक्त में ग्लूकोज का उपवास स्तर पूरे केशिका रक्त में इसके स्तर से मेल खाता है। भोजन या ओजीटीटी के बाद, शिरापरक रक्त में इसका स्तर केशिका रक्त की तुलना में लगभग 1.1 mmol/l कम होता है। प्लाज्मा में ग्लूकोज की मात्रा पूरे रक्त की तुलना में लगभग 0.84 mmol/l अधिक है। मधुमेह चिकित्सा की क्षतिपूर्ति और पर्याप्तता का आकलन करने के लिए, पोर्टेबल का उपयोग करके केशिका रक्त में ग्लाइसेमिया के स्तर का आकलन किया जाता है ग्लूकोमीटरस्वयं रोगियों, उनके रिश्तेदारों या चिकित्सा कर्मचारियों द्वारा।
किसी भी प्रकार के मधुमेह के साथ-साथ महत्वपूर्ण ग्लूकोज भार के साथ, यह विकसित हो सकता है ग्लूकोसुरिया,जो प्राथमिक मूत्र से ग्लूकोज पुनर्अवशोषण की सीमा से अधिक होने का परिणाम है। ग्लूकोज पुनर्अवशोषण की सीमा व्यक्तिगत रूप से काफी भिन्न होती है (≈ 9-10 mmol/l)। मधुमेह के निदान के लिए ग्लूकोसुरिया को एक अलग संकेतक के रूप में उपयोग नहीं किया जाना चाहिए। आम तौर पर, परिष्कृत कार्बोहाइड्रेट के महत्वपूर्ण आहार भार के मामलों को छोड़कर, ग्लूकोसुरिया नहीं होता है।
उत्पादों कीटोन निकाय(एसीटोन, एसीटोएसीटेट, β-हाइड्रॉक्सीब्यूटाइरेट) पूर्ण इंसुलिन की कमी के साथ काफी तीव्र हो जाता है। डीएम-1 के विघटन के साथ, उच्चारण किया गया ketonuria(परीक्षण स्ट्रिप्स का उपयोग करके परीक्षण किया जाता है जिन्हें मूत्र में डुबोया जाता है)। स्वस्थ लोगों में उपवास और कम कार्बोहाइड्रेट वाले आहार के दौरान हल्के (ट्रेस) कीटोनुरिया का पता लगाया जा सकता है।
एक महत्वपूर्ण प्रयोगशाला संकेतक जिसका उपयोग मधुमेह के प्रकारों के विभेदक निदान के लिए किया जाता है, साथ ही मधुमेह -2 के रोगियों में इंसुलिन की कमी के गठन की पहचान करने के लिए किया जाता है, स्तर है सी-पेप्टाइड।रक्त में सी-पेप्टाइड का स्तर अप्रत्यक्ष रूप से अग्न्याशय की β-कोशिकाओं की इंसुलिन-स्रावित क्षमता का अनुमान लगा सकता है। उत्तरार्द्ध प्रोइन्सुलिन का उत्पादन करता है, जिसमें से सी-पेप्टाइड स्राव से पहले टूट जाता है, इंसुलिन के साथ समान मात्रा में रक्त में प्रवेश करता है। इंसुलिन 50% यकृत में बंधा होता है और परिधीय रक्त में इसका आधा जीवन लगभग 4 मिनट का होता है। सी-पेप्टाइड को यकृत द्वारा रक्तप्रवाह से नहीं हटाया जाता है और रक्त में इसका आधा जीवन लगभग 30 मिनट का होता है। इसके अलावा, यह परिधि में सेलुलर रिसेप्टर्स से बंधता नहीं है। इसलिए, सी-पेप्टाइड के स्तर का निर्धारण द्वीपीय उपकरण के कार्य का आकलन करने के लिए एक अधिक विश्वसनीय परीक्षण है। उत्तेजना परीक्षणों (ग्लूकागन खाने या प्रशासित करने के बाद) की पृष्ठभूमि के खिलाफ सी-पेप्टाइड के स्तर का अध्ययन करना सबसे अधिक जानकारीपूर्ण है। यह परीक्षण जानकारीपूर्ण नहीं है यदि यह मधुमेह के गंभीर विघटन की पृष्ठभूमि के खिलाफ किया जाता है, क्योंकि गंभीर हाइपरग्लेसेमिया का β-कोशिकाओं (ग्लूकोटॉक्सिसिटी) पर विषाक्त प्रभाव पड़ता है। पिछले कुछ दिनों में इंसुलिन थेरेपी परीक्षण के परिणामों को प्रभावित नहीं करेगी।
बुनियादी उपचार का उद्देश्यकिसी भी प्रकार के मधुमेह की रोकथाम इसकी देर से होने वाली जटिलताओं की रोकथाम है, जिसे कई मापदंडों के लिए इसके स्थिर मुआवजे की पृष्ठभूमि के खिलाफ हासिल किया जा सकता है (तालिका 7.3)। मधुमेह में कार्बोहाइड्रेट चयापचय के मुआवजे की गुणवत्ता का मुख्य मानदंड स्तर है ग्लाइकेटेड (ग्लाइकोसिलेटेड) हीमोग्लोबिन (HbA1c)।उत्तरार्द्ध हीमोग्लोबिन है जो ग्लूकोज से गैर-सहसंयोजक रूप से बंधा होता है। ग्लूकोज इंसुलिन से स्वतंत्र रूप से एरिथ्रोसाइट्स में प्रवेश करता है, और हीमोग्लोबिन का ग्लाइकोसिलेशन एक अपरिवर्तनीय प्रक्रिया है, और इसकी डिग्री ग्लूकोज की एकाग्रता के सीधे आनुपातिक है जिसके साथ यह अपने अस्तित्व के 120 दिनों के दौरान संपर्क में था। हीमोग्लोबिन का एक छोटा सा हिस्सा ग्लाइकोसिलेटेड होता है और सामान्य होता है; मधुमेह में यह काफी बढ़ सकता है। HbA1c स्तर, ग्लूकोज स्तर के विपरीत, जो लगातार बदल रहा है, पिछले 3-4 महीनों में ग्लाइसेमिया को एकीकृत रूप से दर्शाता है। इसी अंतराल पर मधुमेह क्षतिपूर्ति का आकलन करने के लिए एचबीए1सी स्तर निर्धारित करने की सिफारिश की जाती है।
मधुमेह की देर से होने वाली जटिलताओं के विकास और प्रगति के लिए क्रोनिक हाइपरग्लेसेमिया एकमात्र जोखिम कारक नहीं है। इसकी वजह डीएम मुआवजे का आकलनएक कॉम्प्लेक्स पर आधारित
प्रयोगशाला और वाद्य अनुसंधान विधियां (तालिका 7.3)। कार्बोहाइड्रेट चयापचय की स्थिति को दर्शाने वाले संकेतकों के अलावा, सबसे महत्वपूर्ण हैं रक्तचाप का स्तर और रक्त का लिपिड स्पेक्ट्रम।
मेज़ 7.3.मधुमेह मेलेटस के मुआवजे के लिए मानदंड
 उपरोक्त मुआवजे के मानदंडों के अलावा, मधुमेह के इलाज के लिए लक्ष्य की योजना बनाते समय एक व्यक्तिगत दृष्टिकोण की आवश्यकता होती है। रोग की अवधि बढ़ने के साथ मधुमेह (विशेष रूप से माइक्रोएंगियोपैथी) की देर से जटिलताओं के विकास और प्रगति की संभावना बढ़ जाती है। इस प्रकार, यदि बच्चों और युवा रोगियों में, जिनका मधुमेह का इतिहास बाद में कई दशकों तक पहुंच सकता है, इष्टतम ग्लाइसेमिक संकेतक प्राप्त करना आवश्यक है, तो जिन रोगियों में मधुमेह बुढ़ापे में प्रकट हुआ, उन्हें सख्त यूग्लाइसेमिक मुआवजा दिया जाना चाहिए, जिससे जोखिम काफी बढ़ जाता है। हाइपोग्लाइसीमिया, हमेशा उचित नहीं।
उपरोक्त मुआवजे के मानदंडों के अलावा, मधुमेह के इलाज के लिए लक्ष्य की योजना बनाते समय एक व्यक्तिगत दृष्टिकोण की आवश्यकता होती है। रोग की अवधि बढ़ने के साथ मधुमेह (विशेष रूप से माइक्रोएंगियोपैथी) की देर से जटिलताओं के विकास और प्रगति की संभावना बढ़ जाती है। इस प्रकार, यदि बच्चों और युवा रोगियों में, जिनका मधुमेह का इतिहास बाद में कई दशकों तक पहुंच सकता है, इष्टतम ग्लाइसेमिक संकेतक प्राप्त करना आवश्यक है, तो जिन रोगियों में मधुमेह बुढ़ापे में प्रकट हुआ, उन्हें सख्त यूग्लाइसेमिक मुआवजा दिया जाना चाहिए, जिससे जोखिम काफी बढ़ जाता है। हाइपोग्लाइसीमिया, हमेशा उचित नहीं।
7.4. इंसुलिन की तैयारी और इंसुलिन थेरेपी
टाइप 1 मधुमेह वाले रोगियों के लिए इंसुलिन की तैयारी महत्वपूर्ण है; इसके अलावा, T2DM वाले 40% मरीज़ इन्हें प्राप्त करते हैं। सामान्य को मधुमेह के लिए इंसुलिन थेरेपी निर्धारित करने के संकेत,जिनमें से कई वास्तव में एक दूसरे को ओवरलैप करते हैं उनमें शामिल हैं:
1. मधुमेह मेलेटस प्रकार 1
2. अग्न्याशय
3. केटोएसिडोटिक और हाइपरोस्मोलर कोमा
4. टाइप 2 मधुमेह मेलिटस के लिए:
इंसुलिन की कमी के स्पष्ट संकेत, जैसे प्रगतिशील वजन घटाने और केटोसिस, गंभीर हाइपरग्लेसेमिया;
प्रमुख सर्जिकल हस्तक्षेप;
तीव्र मैक्रोवास्कुलर जटिलताएं (स्ट्रोक, मायोकार्डियल रोधगलन, गैंग्रीन, आदि) और कार्बोहाइड्रेट चयापचय के विघटन के साथ गंभीर संक्रामक रोग;
उपवास ग्लूकोज स्तर 15-18 mmol/l से अधिक है;
विभिन्न टैबलेट हाइपोग्लाइसेमिक दवाओं की अधिकतम दैनिक खुराक निर्धारित करने के बावजूद, स्थिर मुआवजे का अभाव;
मधुमेह की देर से जटिलताओं के अंतिम चरण (गंभीर पोलीन्यूरोपैथी और रेटिनोपैथी, क्रोनिक रीनल फेल्योर)।
5. आहार चिकित्सा के साथ गर्भकालीन मधुमेह के लिए मुआवजा प्राप्त करने में असमर्थता।
मूलतःइंसुलिन की तैयारियों को तीन समूहों में वर्गीकृत किया जा सकता है:
पशु इंसुलिन (सूअर का मांस);
मानव इंसुलिन (अर्ध-सिंथेटिक, आनुवंशिक रूप से इंजीनियर);
इंसुलिन एनालॉग्स (लिस्प्रो, एस्पार्ट, ग्लार्गिन, डिटेमिर)।
मानव इंसुलिन उत्पादन प्रौद्योगिकी में प्रगति के कारण इसका उपयोग शुरू हो गया है पोर्क इंसुलिन(एक अमीनो एसिड में मानव से भिन्न) हाल ही में काफी कमी आई है। मानव इंसुलिन का उत्पादन करने के लिए पोर्सिन इंसुलिन का उपयोग किया जा सकता है अर्ध-सिंथेटिक विधि,जिसमें इसके अणु में एक अलग अमीनो एसिड को प्रतिस्थापित करना शामिल है। उच्चतम गुणवत्ता जेनेटिक इंजीनियरिंगमानव इंसुलिन. उन्हें प्राप्त करने के लिए, इंसुलिन संश्लेषण के लिए जिम्मेदार मानव जीनोम का क्षेत्र जीनोम से जुड़ा होता है ई कोलाईया यीस्ट कल्चर, जिसके परिणामस्वरूप बाद वाला मानव इंसुलिन का उत्पादन शुरू कर देता है। निर्माण इंसुलिन एनालॉग्सविभिन्न अमीनो एसिड की पुनर्व्यवस्था का उपयोग करके, लक्ष्य वांछित और सबसे अनुकूल फार्माकोकाइनेटिक्स वाली दवाएं प्राप्त करना था। इस प्रकार, इंसुलिन लिस्प्रो (हमलोग) एक एनालॉग है
अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन, जिसका हाइपोग्लाइसेमिक प्रभाव इंजेक्शन के 15 मिनट के भीतर विकसित होता है। इसके विपरीत, इंसुलिन एनालॉग ग्लार्गिन (लैंटस) की विशेषता एक दीर्घकालिक प्रभाव है जो पूरे दिन रहता है, जबकि दवा के कैनेटीक्स की एक विशेषता प्लाज्मा एकाग्रता में स्पष्ट चोटियों की अनुपस्थिति है। वर्तमान में उपयोग की जाने वाली अधिकांश इंसुलिन तैयारियां और इसके एनालॉग्स का उत्पादन किया जाता है सांद्रता 100 यू/एमएल. द्वारा कार्रवाई की अवधिइंसुलिन को 4 मुख्य समूहों में विभाजित किया गया है (तालिका 7.4):
मेज़ 7.4.दवाओं और इंसुलिन एनालॉग्स के फार्माकोकाइनेटिक्स
 1.
अल्ट्रा-शॉर्ट-एक्टिंग (लिस्प्रो, एस्पार्ट)।
1.
अल्ट्रा-शॉर्ट-एक्टिंग (लिस्प्रो, एस्पार्ट)।
2. लघु-अभिनय (सरल मानव इंसुलिन)।
3. मध्यम-अभिनय (तटस्थ प्रोटामाइन हेजडॉर्न इंसुलिन)।
4. लंबे समय तक काम करने वाला (ग्लार्जिन, डिटेमिर)।
5. क्रिया की अलग-अलग अवधि के इंसुलिन का मिश्रण (नोवोमिक्स-30, ह्यूमुलिन-एमजेड, ह्यूमलोग-मिक्स-25)।
ड्रग्स अति लघु क्रिया[लिस्प्रो (हमलोग), एस्पार्ट (नोवोरैपिड)] इंसुलिन एनालॉग हैं। उनके फायदे इंजेक्शन के बाद (15 मिनट के बाद) हाइपोग्लाइसेमिक प्रभाव का तेजी से विकास है, जो भोजन से तुरंत पहले या भोजन के तुरंत बाद भी इंजेक्शन लगाने की अनुमति देता है, साथ ही कार्रवाई की एक छोटी अवधि (3 घंटे से कम), जो जोखिम को कम करता है। हाइपोग्लाइसीमिया। ड्रग्स छोटा अभिनय(सरल इंसुलिन, नियमित इंसुलिन) 100 यू/एमएल की सांद्रता पर इंसुलिन युक्त एक समाधान है। साधारण इंसुलिन का एक इंजेक्शन भोजन से 30 मिनट पहले दिया जाता है; कार्रवाई की अवधि लगभग 4-6 घंटे है। अल्ट्रा-शॉर्ट और लघु-अभिनय दवाओं को चमड़े के नीचे, इंट्रामस्क्युलर और अंतःशिरा रूप से प्रशासित किया जा सकता है।
दवाओं के बीच कार्रवाई की औसत अवधिसबसे अधिक इस्तेमाल की जाने वाली दवाएं न्यूट्रल प्रोटामाइन हेजडॉर्न (एनपीएच) हैं। एनपीएच एक प्रोटीन है जो गैर-सहसंयोजक रूप से इंसुलिन को सोख लेता है, जिससे चमड़े के नीचे के डिपो से इसका अवशोषण धीमा हो जाता है। एनपीएच इंसुलिन की कार्रवाई की प्रभावी अवधि आमतौर पर लगभग 12 घंटे होती है; उन्हें केवल चमड़े के नीचे प्रशासित किया जाता है। एनपीएच इंसुलिन एक सस्पेंशन है, और इसलिए, साधारण इंसुलिन के विपरीत, यह शीशी में बादल जैसा होता है, और जब इसे लंबे समय तक खड़ा छोड़ दिया जाता है, तो एक सस्पेंशन बनता है, जिसे इंजेक्शन से पहले अच्छी तरह मिलाया जाना चाहिए। एनपीएच इंसुलिन, अन्य लंबी-अभिनय दवाओं के विपरीत, लघु-अभिनय इंसुलिन (सरल इंसुलिन) के साथ किसी भी अनुपात में मिलाया जा सकता है, और मिश्रण के घटकों के फार्माकोकाइनेटिक्स में बदलाव नहीं होगा, क्योंकि एनपीएच सरल इंसुलिन की अतिरिक्त मात्रा को बांध नहीं पाएगा ( चित्र 7.5). इसके अलावा, प्रोटामाइन का उपयोग इंसुलिन एनालॉग्स (नोवोमिक्स-30, ह्यूमलोग-मिक्स-25) के मानक मिश्रण तैयार करने के लिए किया जाता है।
लंबे समय तक काम करने वाली दवाओं में, इंसुलिन एनालॉग्स का वर्तमान में सक्रिय रूप से उपयोग किया जाता है। ग्लेरगीन(लैंटस) और Detemir(लेवेमीर)। इन दवाओं के फार्माकोकाइनेटिक्स की एक अनुकूल विशेषता यह है कि, एनपीएच इंसुलिन के विपरीत, वे चमड़े के नीचे के डिपो से दवा की अधिक समान और लंबे समय तक आपूर्ति प्रदान करते हैं। इस संबंध में, ग्लार्गिन को दिन में केवल एक बार निर्धारित किया जा सकता है, व्यावहारिक रूप से दिन के समय की परवाह किए बिना।
 चावल। 7.5.विभिन्न इंसुलिन तैयारियों के फार्माकोकाइनेटिक्स:
चावल। 7.5.विभिन्न इंसुलिन तैयारियों के फार्माकोकाइनेटिक्स:
ए) मोनोकंपोनेंट; बी) मानक इंसुलिन मिश्रण
मोनोकंपोनेंट इंसुलिन तैयारियों के अलावा, उनका व्यापक रूप से नैदानिक अभ्यास में उपयोग किया जाता है। मानक मिश्रण.एक नियम के रूप में, हम इंटरमीडिएट-एक्टिंग इंसुलिन के साथ शॉर्ट-एक्टिंग या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन के मिश्रण के बारे में बात कर रहे हैं। उदाहरण के लिए, दवा "ह्यूमुलिन-एमजेड" में एक बोतल में 30% सरल इंसुलिन और 70% एनपीएच इंसुलिन होता है; दवा "नोवोमिक्स-30" में 30% इंसुलिन एस्पार्टर और 70% इंसुलिन एस्पार्टर का क्रिस्टलीय प्रोटामाइन सस्पेंशन होता है; दवा "हमलोग-मिक्स-25" में 25% इंसुलिन लिस्प्रो और इंसुलिन लिस्प्रो का 75% प्रोटामाइन सस्पेंशन होता है। फ़ायदा
मानक इंसुलिन मिश्रण एक के साथ दो इंजेक्शनों का प्रतिस्थापन है और मिश्रण के घटकों की खुराक में कुछ हद तक अधिक सटीकता है; नुकसान मिश्रण के व्यक्तिगत घटकों की व्यक्तिगत खुराक की असंभवता है। यह T2DM या तथाकथित के उपचार के लिए मानक इंसुलिन मिश्रण का उपयोग करने की प्राथमिकता निर्धारित करता है पारंपरिक इंसुलिन थेरेपी(इंसुलिन की निश्चित खुराक निर्धारित करना), जबकि के लिए गहन इंसुलिन थेरेपी(ग्लाइसेमिक संकेतकों और भोजन में कार्बोहाइड्रेट की मात्रा के आधार पर लचीली खुराक का चयन) मोनोकंपोनेंट दवाओं का उपयोग बेहतर है।
सफल इंसुलिन थेरेपी की कुंजी इसका कड़ाई से पालन करना है इंजेक्शन तकनीक.इंसुलिन देने के कई तरीके हैं। सबसे सरल और सबसे विश्वसनीय तरीका इंसुलिन का उपयोग करके इंजेक्शन है। सिरिंज।इंसुलिन देने का एक अधिक सुविधाजनक तरीका इंजेक्शन का उपयोग करना है सिरिंज पेन,जो एक संयुक्त उपकरण है जिसमें एक इंसुलिन भंडार (कारतूस), एक खुराक प्रणाली और एक इंजेक्टर के साथ एक सुई होती है।
रखरखाव चिकित्सा के लिए (जब हम मधुमेह या गंभीर स्थितियों के गंभीर विघटन के बारे में बात नहीं कर रहे हैं), इंसुलिन को चमड़े के नीचे प्रशासित किया जाता है। शॉर्ट-एक्टिंग इंसुलिन के इंजेक्शन को पेट के चमड़े के नीचे के वसायुक्त ऊतक में, लंबे समय तक काम करने वाले इंसुलिन को जांघ या कंधे के ऊतकों में लगाने की सलाह दी जाती है (चित्र 7.6 ए)। 45° के कोण पर व्यापक रूप से संपीड़ित त्वचा के माध्यम से चमड़े के नीचे के ऊतक में इंजेक्शन लगाए जाते हैं (चित्र 7.6 बी)। लिपोडिस्ट्रोफी के विकास को रोकने के लिए रोगी को प्रतिदिन उसी क्षेत्र में इंसुलिन इंजेक्शन साइट बदलने की सलाह दी जानी चाहिए।
को इंसुलिन अवशोषण की दर को प्रभावित करने वाले कारकचमड़े के नीचे के डिपो से, इंसुलिन की खुराक को ध्यान में रखा जाना चाहिए (खुराक बढ़ाने से अवशोषण की अवधि बढ़ जाती है), इंजेक्शन साइट (पेट के ऊतकों से अवशोषण तेज होता है), और परिवेश का तापमान (इंजेक्शन साइट को गर्म करने और मालिश करने से अवशोषण में तेजी आती है) ).
प्रशासन की एक अधिक जटिल विधि, जो फिर भी कई रोगियों में अच्छे उपचार परिणाम प्राप्त करने की अनुमति देती है, का उपयोग है इंसुलिन डिस्पेंसर,या निरंतर चमड़े के नीचे इंसुलिन प्रशासन के लिए सिस्टम। डिस्पेंसर एक पोर्टेबल डिवाइस है जिसमें एक कंप्यूटर होता है जो इंसुलिन आपूर्ति मोड सेट करता है, साथ ही एक कैथेटर और चमड़े के नीचे एक छोटी सुई के माध्यम से इंसुलिन आपूर्ति प्रणाली भी सेट करता है।
 चावल। 7.6.इंसुलिन इंजेक्शन: ए) विशिष्ट इंजेक्शन साइटें; बी) इंजेक्शन के दौरान इंसुलिन सिरिंज सुई की स्थिति
चावल। 7.6.इंसुलिन इंजेक्शन: ए) विशिष्ट इंजेक्शन साइटें; बी) इंजेक्शन के दौरान इंसुलिन सिरिंज सुई की स्थिति
मोटा टिश्यू। एक डिस्पेंसर का उपयोग करके, शॉर्ट-एक्टिंग या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन का निरंतर बेसल इंजेक्शन (लगभग 0.5-1 यू/घंटा की दर से) किया जाता है, और खाने से पहले, कार्बोहाइड्रेट सामग्री और ग्लाइसेमिक स्तर के आधार पर, रोगी को उसी लघु-अभिनय इंसुलिन की आवश्यक बोलस खुराक दी जाती है। एक डिस्पेंसर का उपयोग करके इंसुलिन थेरेपी का लाभ अकेले लघु-अभिनय (या यहां तक कि अल्ट्रा-शॉर्ट) इंसुलिन का प्रशासन है, जो अपने आप में कुछ हद तक अधिक शारीरिक है, क्योंकि लंबे समय तक अभिनय इंसुलिन की तैयारी का अवशोषण बड़े उतार-चढ़ाव के अधीन है; इस संबंध में, लघु-अभिनय इंसुलिन का निरंतर प्रशासन एक अधिक प्रबंधनीय प्रक्रिया प्रतीत होती है। डिस्पेंसर का उपयोग करके इंसुलिन थेरेपी का नुकसान डिवाइस को लगातार पहनने की आवश्यकता है, साथ ही चमड़े के नीचे के ऊतक में इंजेक्शन सुई की दीर्घकालिक उपस्थिति है, जिसके लिए इंसुलिन आपूर्ति प्रक्रिया की आवधिक निगरानी की आवश्यकता होती है। डिस्पेंसर का उपयोग करके इंसुलिन थेरेपी मुख्य रूप से टाइप 1 मधुमेह वाले रोगियों के लिए संकेतित है जो इसके प्रबंधन की तकनीक में महारत हासिल करने के लिए तैयार हैं। विशेष रूप से इस संबंध में, स्पष्ट "प्रभात" घटना वाले रोगियों के साथ-साथ गर्भवती और गर्भावस्था की योजना बना रहे टी1डीएम वाले रोगियों और रोगियों पर ध्यान दिया जाना चाहिए।
अव्यवस्थित जीवनशैली (अधिक लचीले आहार की संभावना) वाले लोग।
7.5. टाइप 1 मधुमेह
सीडी-1 - अंग-विशिष्ट स्व-प्रतिरक्षितएक बीमारी जिसके कारण अग्न्याशय के आइलेट्स की इंसुलिन-उत्पादक β-कोशिकाएं नष्ट हो जाती हैं, जो इंसुलिन की पूर्ण कमी से प्रकट होती है। कुछ मामलों में, प्रत्यक्ष T1DM वाले रोगियों में β-कोशिकाओं में ऑटोइम्यून क्षति के मार्करों की कमी होती है (अज्ञातहेतुक डीएम-1)।
एटियलजि
डीएम-1 एक वंशानुगत प्रवृत्ति वाली बीमारी है, लेकिन बीमारी के विकास में इसका योगदान छोटा है (इसके विकास को लगभग 1/3 निर्धारित करता है)। एक जैसे जुड़वाँ बच्चों में T1DM की समवर्ती दर केवल 36% है। बीमार मां वाले बच्चे में टी1डी विकसित होने की संभावना 1-2%, पिता के लिए 3-6%, भाई या बहन के लिए 6% होती है। ऑटोइम्यून β-कोशिका क्षति के एक या अधिक ह्यूमरल मार्कर, जिनमें अग्नाशयी आइलेट्स के लिए एंटीबॉडी, ग्लूटामेट डिकार्बोक्सिलेज (GAD65) के लिए एंटीबॉडी और टायरोसिन फॉस्फेट (IA-2 और ΙΑ-2β) के लिए एंटीबॉडी शामिल हैं, 85-90% रोगियों में पाए जाते हैं। . फिर भी, β-कोशिकाओं के विनाश में मुख्य भूमिका सेलुलर प्रतिरक्षा कारकों को दी जाती है। T1DM ऐसे HLA हैप्लोटाइप्स से जुड़ा है डीक्यूएऔर डीक्यूबीजबकि केवल एलील्स एचएलए-डीआर/डीक्यूरोग के विकास के लिए पूर्वसूचक हो सकते हैं, जबकि अन्य सुरक्षात्मक हैं। बढ़ी हुई आवृत्ति के साथ, डीएम-1 को अन्य ऑटोइम्यून एंडोक्राइन (ऑटोइम्यून थायरॉयडिटिस, एडिसन रोग) और गैर-एंडोक्राइन रोगों, जैसे खालित्य, विटिलिगो, क्रोहन रोग, आमवाती रोगों (तालिका 7.5) के साथ जोड़ा जाता है।
रोगजनन
डीएम-1 तब प्रकट होता है जब 80-90% β-कोशिकाएं एक ऑटोइम्यून प्रक्रिया द्वारा नष्ट हो जाती हैं। इस प्रक्रिया की गति और तीव्रता काफी भिन्न हो सकती है। बहुधा जब विशिष्ट पाठ्यक्रमबच्चों और युवाओं में रोग, यह प्रक्रिया काफी तेजी से आगे बढ़ती है, इसके बाद रोग तेजी से प्रकट होता है, जिसमें पहले नैदानिक लक्षणों की उपस्थिति से लेकर केटोएसिडोसिस (कीटोएसिडोटिक कोमा तक) के विकास तक केवल कुछ सप्ताह ही बीत सकते हैं।
मेज़ 7.5.मधुमेह मेलेटस प्रकार 1
 तालिका की निरंतरता. 7.5
तालिका की निरंतरता. 7.5
 अन्य, बहुत दुर्लभ मामलों में, आमतौर पर 40 वर्ष से अधिक उम्र के वयस्कों में, रोग गुप्त हो सकता है। (वयस्कों का अव्यक्त ऑटोइम्यून मधुमेह - LADA),वहीं, बीमारी की शुरुआत में, ऐसे रोगियों में अक्सर मधुमेह मेलिटस -2 का निदान किया जाता है, और कई वर्षों तक, सल्फोनील्यूरिया दवाएं निर्धारित करके मधुमेह के लिए मुआवजा प्राप्त किया जा सकता है। लेकिन बाद में, आमतौर पर 3 साल के बाद, पूर्ण इंसुलिन की कमी के लक्षण दिखाई देते हैं (वजन में कमी, केटोनुरिया, गंभीर हाइपरग्लेसेमिया, टैबलेट वाली हाइपोग्लाइसेमिक दवाएं लेने के बावजूद)।
अन्य, बहुत दुर्लभ मामलों में, आमतौर पर 40 वर्ष से अधिक उम्र के वयस्कों में, रोग गुप्त हो सकता है। (वयस्कों का अव्यक्त ऑटोइम्यून मधुमेह - LADA),वहीं, बीमारी की शुरुआत में, ऐसे रोगियों में अक्सर मधुमेह मेलिटस -2 का निदान किया जाता है, और कई वर्षों तक, सल्फोनील्यूरिया दवाएं निर्धारित करके मधुमेह के लिए मुआवजा प्राप्त किया जा सकता है। लेकिन बाद में, आमतौर पर 3 साल के बाद, पूर्ण इंसुलिन की कमी के लक्षण दिखाई देते हैं (वजन में कमी, केटोनुरिया, गंभीर हाइपरग्लेसेमिया, टैबलेट वाली हाइपोग्लाइसेमिक दवाएं लेने के बावजूद)।
जैसा कि संकेत दिया गया है, T1DM का रोगजनन पूर्ण इंसुलिन की कमी पर आधारित है। ग्लूकोज की इंसुलिन-निर्भर ऊतकों (वसा और मांसपेशियों) में प्रवेश करने में असमर्थता से ऊर्जा की कमी हो जाती है, जिसके परिणामस्वरूप तीव्र लिपोलिसिस और प्रोटियोलिसिस होता है, जो वजन घटाने से जुड़ा होता है। ग्लाइसेमिक स्तर में वृद्धि हाइपरोस्मोलैरिटी का कारण बनती है, जो ऑस्मोटिक ड्यूरिसिस और गंभीर निर्जलीकरण के साथ होती है। इंसुलिन की कमी और ऊर्जा की कमी की स्थिति में, गर्भनिरोधक हार्मोन (ग्लूकागन, कोर्टिसोल, ग्रोथ हार्मोन) का उत्पादन बाधित होता है, जो ग्लाइसेमिया में वृद्धि के बावजूद, ग्लूकोनियोजेनेसिस की उत्तेजना का कारण बनता है। वसा ऊतक में लिपोलिसिस बढ़ने से मुक्त फैटी एसिड की सांद्रता में उल्लेखनीय वृद्धि होती है। इंसुलिन की कमी से लीवर की लिपोसिंथेटिक क्षमता दब जाती है और मुक्त हो जाती है
केटोजेनेसिस में फैटी एसिड शामिल होने लगते हैं। कीटोन निकायों के संचय से मधुमेह कीटोसिस और बाद में कीटोएसिडोसिस का विकास होता है। निर्जलीकरण और एसिडोसिस में प्रगतिशील वृद्धि के साथ, कोमा विकसित होता है (धारा 7.7.1 देखें), जो इंसुलिन थेरेपी और पुनर्जलीकरण की अनुपस्थिति में अनिवार्य रूप से मृत्यु में समाप्त होता है।
महामारी विज्ञान
T1DM मधुमेह के सभी मामलों का लगभग 1.5-2% है, और T2DM की घटनाओं में तेजी से वृद्धि के कारण यह सापेक्ष आंकड़ा और भी कम हो जाएगा। कोकेशियान व्यक्ति में T1DM विकसित होने का जीवनकाल जोखिम लगभग 0.4% है। टाइप 1 मधुमेह की घटनाएँ प्रति वर्ष 3% बढ़ रही हैं: नए मामलों के कारण 1.5% और रोगियों की जीवन प्रत्याशा में वृद्धि के कारण अन्य 1.5%। T1DM की व्यापकता जनसंख्या की जातीय संरचना के आधार पर भिन्न होती है। 2000 तक, यह अफ्रीका में 0.02%, दक्षिण एशिया और दक्षिण और मध्य अमेरिका में 0.1% और यूरोप और उत्तरी अमेरिका में 0.2% थी। डीएम-1 की घटना फिनलैंड और स्वीडन में सबसे अधिक है (प्रति वर्ष प्रति 100 हजार जनसंख्या पर 30-35 मामले), और जापान, चीन और कोरिया में सबसे कम (क्रमशः 0.5-2.0 मामले)। T1DM के प्रकट होने की चरम आयु लगभग 10-13 वर्ष है। अधिकांश मामलों में, T1DM 40 वर्ष की आयु से पहले ही प्रकट होता है।
नैदानिक अभिव्यक्तियाँ
में विशिष्ट मामले,विशेष रूप से बच्चों और युवाओं में, T1DM एक ज्वलंत नैदानिक तस्वीर के साथ शुरू होता है जो कई महीनों या हफ्तों में विकसित होता है। T1DM की अभिव्यक्ति संक्रामक और अन्य सहवर्ती बीमारियों से शुरू हो सकती है। विशेषता सभी प्रकार के मधुमेह के सामान्य लक्षण,हाइपरग्लेसेमिया से जुड़े: पॉलीडिप्सिया, पॉलीयूरिया, त्वचा की खुजली, लेकिन टाइप 1 मधुमेह के साथ वे बहुत स्पष्ट हैं। तो, दिन भर में, मरीज़ 5-10 लीटर तक तरल पदार्थ पी सकते हैं और उत्सर्जित कर सकते हैं। विशिष्टटाइप 1 मधुमेह के लिए, लक्षण, जो इंसुलिन की पूर्ण कमी के कारण होता है, 1-2 महीनों में वजन का 10-15 किलोग्राम तक कम होना है। गंभीर सामान्य और मांसपेशियों की कमजोरी, प्रदर्शन में कमी और उनींदापन इसकी विशेषता है। रोग की शुरुआत में, कुछ रोगियों को भूख में वृद्धि का अनुभव हो सकता है, जो कीटोएसिडोसिस विकसित होने पर एनोरेक्सिया का मार्ग प्रशस्त करता है। उत्तरार्द्ध को मुंह से एसीटोन गंध (या फल गंध) की उपस्थिति, मतली की विशेषता है
टिप्पणियाँ, उल्टी, अक्सर पेट में दर्द (स्यूडोपेरिटोनिटिस), गंभीर निर्जलीकरण और कोमा के विकास में समाप्त होता है (धारा 7.7.1 देखें)। कुछ मामलों में, बच्चों में T1DM की पहली अभिव्यक्ति सहवर्ती रोगों, आमतौर पर संक्रामक या तीव्र सर्जिकल विकृति के कारण कोमा तक की चेतना की प्रगतिशील हानि है।
35-40 वर्ष से अधिक उम्र के लोगों में टी1डीएम के विकास के अपेक्षाकृत दुर्लभ मामले (वयस्कों का अव्यक्त ऑटोइम्यून मधुमेह)रोग स्वयं इतने स्पष्ट रूप से प्रकट नहीं हो सकता है (मध्यम पॉलीडिप्सिया और पॉलीयूरिया, शरीर के वजन में कोई कमी नहीं) और ग्लाइसेमिक स्तर के नियमित निर्धारण के दौरान संयोग से इसका पता भी चल सकता है। इन मामलों में, रोगी को अक्सर शुरू में मधुमेह मेलिटस -2 का निदान किया जाता है और टैबलेट हाइपोग्लाइसेमिक दवाएं (टीजीडी) निर्धारित की जाती हैं, जो कुछ समय के लिए मधुमेह के लिए स्वीकार्य मुआवजा प्रदान करती हैं। हालांकि, कई वर्षों में (अक्सर एक वर्ष के भीतर), रोगी में इंसुलिन की बढ़ती पूर्ण कमी के कारण लक्षण विकसित होते हैं: वजन में कमी, टीएसपी, केटोसिस, केटोएसिडोसिस की पृष्ठभूमि के खिलाफ सामान्य ग्लाइसेमिया बनाए रखने में असमर्थता।
निदान
यह ध्यान में रखते हुए कि DM-1 की एक स्पष्ट नैदानिक तस्वीर है और यह एक अपेक्षाकृत दुर्लभ बीमारी भी है, DM-1 के निदान के उद्देश्य से ग्लाइसेमिक स्तर के स्क्रीनिंग निर्धारण का संकेत नहीं दिया गया है। रोगियों के निकटतम रिश्तेदारों में रोग विकसित होने की संभावना कम है, जो T1DM की प्राथमिक रोकथाम के लिए प्रभावी तरीकों की कमी के साथ, उनमें रोग के इम्यूनोजेनेटिक मार्करों का अध्ययन करने की अनुपयुक्तता को निर्धारित करता है। अधिकांश मामलों में T1DM का निदान पूर्ण इंसुलिन की कमी के गंभीर नैदानिक अभिव्यक्तियों वाले रोगियों में महत्वपूर्ण हाइपरग्लेसेमिया का पता लगाने पर आधारित है। T1DM के निदान के उद्देश्य से OGTT का प्रदर्शन बहुत ही कम करना पड़ता है।
क्रमानुसार रोग का निदान
संदिग्ध मामलों में (स्पष्ट नैदानिक अभिव्यक्तियों की अनुपस्थिति में मध्यम हाइपरग्लेसेमिया का पता लगाना, अपेक्षाकृत उन्नत उम्र में अभिव्यक्ति), साथ ही साथ अन्य प्रकार के मधुमेह के साथ विभेदक निदान के उद्देश्य से, स्तर निर्धारण का उपयोग किया जाता है सी पेप्टाइड(बेसल और भोजन के 2 घंटे बाद)। संदिग्ध मामलों में अप्रत्यक्ष निदान मूल्य में, परिभाषा हो सकती है इम्यूनोलॉजिकल मार्करसीडी-1 - आइलेट्स के प्रति एंटीबॉडी
PZH, ग्लूटामेट डिकार्बोक्सिलेज (GAD65) और टायरोसिन फॉस्फेट (IA-2 और IA-2β) के लिए। डीएम-1 और डीएम-2 का विभेदक निदान तालिका में प्रस्तुत किया गया है। 7.6.
मेज़ 7.6.डीएम-1 और डीएम-2 के बीच विभेदक निदान और अंतर
 इलाज
इलाज
किसी भी प्रकार के मधुमेह का उपचार तीन मुख्य सिद्धांतों पर आधारित है: ग्लूकोज कम करने वाली चिकित्सा (मधुमेह -1 के लिए - इंसुलिन थेरेपी), आहार और रोगी शिक्षा। इंसुलिन थेरेपी DM-1 पहनने के साथ स्थानापन्न प्रकृतिऔर इसका लक्ष्य स्वीकृत क्षतिपूर्ति मानदंड (तालिका 7.3) को प्राप्त करने के लिए हार्मोन के शारीरिक उत्पादन का अधिकतम अनुकरण करना है। शारीरिक इंसुलिन स्राव के सबसे करीब गहन इंसुलिन थेरेपी.इसके अनुरूप इंसुलिन की आवश्यकता होती है बेसल स्रावइंटरमीडिएट-एक्टिंग इंसुलिन (सुबह और शाम) के दो इंजेक्शन या लंबे समय तक काम करने वाले इंसुलिन (ग्लार्गिन) के एक इंजेक्शन द्वारा प्रदान किया जाता है। बेसल इंसुलिन की कुल खुराक
यह मात्रा दवा की कुल दैनिक आवश्यकता के आधे से अधिक नहीं होनी चाहिए। भोजन या बोलस इंसुलिन स्रावप्रत्येक भोजन से पहले शॉर्ट-एक्टिंग या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन के इंजेक्शन द्वारा प्रतिस्थापित किया जाता है, और इसकी खुराक की गणना आगामी भोजन के दौरान ली जाने वाली कार्बोहाइड्रेट की मात्रा और ग्लाइसेमिया के मौजूदा स्तर के आधार पर की जाती है, जो रोगी द्वारा निर्धारित किया जाता है। प्रत्येक इंसुलिन इंजेक्शन से पहले एक ग्लूकोमीटर (चित्र 7.7)।
अनुमानित गहन इंसुलिन थेरेपी आहार,जो लगभग हर दिन बदलेगा, इसे इस प्रकार दर्शाया जा सकता है। यह माना जाता है कि इंसुलिन की दैनिक आवश्यकता शरीर के वजन के प्रति 1 किलोग्राम पर लगभग 0.5-0.7 यूनिट है (70 किलोग्राम वजन वाले रोगी के लिए, लगभग 35-50 यूनिट)। इस खुराक का लगभग 1/3 - 1/2 लंबे समय तक काम करने वाला इंसुलिन (20-25 यू), 1/2 - 2/3 लघु- या अति-लघु-अभिनय इंसुलिन होगा। एनपीएच इंसुलिन की खुराक को 2 इंजेक्शनों में विभाजित किया गया है: सुबह में इसकी खुराक का 2/3 (12 यूनिट), शाम को - 1/3 (8-10 यूनिट)।
उद्देश्य प्रथम चरणइंसुलिन थेरेपी का चयन फास्टिंग ग्लूकोज स्तर को सामान्य करने के लिए है। एनपीएच इंसुलिन की शाम की खुराक आमतौर पर 22-23 घंटे पर दी जाती है, सुबह की खुराक नाश्ते से पहले लघु-अभिनय इंसुलिन के इंजेक्शन के साथ दी जाती है। एनपीएच इंसुलिन की शाम की खुराक का चयन करते समय, कई विकसित होने की संभावना को ध्यान में रखना आवश्यक है
 चावल। 7.7.गहन इंसुलिन थेरेपी आहार
चावल। 7.7.गहन इंसुलिन थेरेपी आहार
काफी विशिष्ट घटना. सुबह हाइपरग्लेसेमिया का कारण लंबे समय तक काम करने वाले इंसुलिन की अपर्याप्त खुराक हो सकता है, क्योंकि सुबह तक इंसुलिन की आवश्यकता काफी बढ़ जाती है ("भोर" घटना)।अपर्याप्त खुराक के अलावा, सुबह हाइपरग्लेसेमिया इसकी अधिकता के कारण हो सकता है - सोमोगी घटना(सोमोगी), पोस्ट-हाइपोग्लाइसेमिक हाइपरग्लेसेमिया। इस घटना को इस तथ्य से समझाया गया है कि इंसुलिन के प्रति ऊतकों की अधिकतम संवेदनशीलता सुबह 2 से 4 बजे के बीच देखी जाती है। यह इस समय है कि मुख्य गर्भनिरोधक हार्मोन (कोर्टिसोल, ग्रोथ हार्मोन, आदि) का स्तर सामान्य रूप से सबसे कम होता है। यदि लंबे समय तक काम करने वाले इंसुलिन की शाम की खुराक अत्यधिक है, तो इस समय हाइपोग्लाइसीमिया।चिकित्सकीय रूप से, यह बुरे सपने के साथ खराब नींद, नींद में अचेतन क्रियाएं, सुबह सिरदर्द और थकान के रूप में प्रकट हो सकता है। इस समय हाइपोग्लाइसीमिया का विकास ग्लूकागन और अन्य गर्भनिरोधक हार्मोनों के एक महत्वपूर्ण प्रतिपूरक रिलीज का कारण बनता है, जिसके बाद सुबह हाइपरग्लेसेमिया।यदि इस स्थिति में शाम को प्रशासित लंबे समय तक काम करने वाले इंसुलिन की खुराक कम नहीं की जाती है, बल्कि बढ़ा दी जाती है, तो रात में हाइपोग्लाइसीमिया और सुबह हाइपरग्लेसेमिया खराब हो जाएगा, जो अंततः क्रोनिक इंसुलिन ओवरडोज सिंड्रोम (सोमोगी सिंड्रोम) का कारण बन सकता है, जो मोटापे का एक संयोजन है। मधुमेह के दीर्घकालिक विघटन, बार-बार हाइपोग्लाइसीमिया और प्रगतिशील देर से जटिलताओं के साथ। सोमोगी घटना का निदान करने के लिए, लगभग 3 बजे ग्लाइसेमिक स्तर का अध्ययन करना आवश्यक है, जो इंसुलिन थेरेपी के चयन का एक अभिन्न अंग है। यदि सुरक्षित रात्रि हाइपोग्लाइसीमिया के लिए एनपीएच की शाम की खुराक में कमी सुबह (भोर की घटना) में हाइपरग्लाइसीमिया के साथ होती है, तो रोगी को पहले (6-7 बजे) उठने की सलाह दी जानी चाहिए, जबकि रात में प्रशासित इंसुलिन सामान्य बनाए रखना जारी रखता है ग्लाइसेमिक स्तर.
एनपीएच इंसुलिन का दूसरा इंजेक्शन आमतौर पर सुबह नाश्ते से पहले शॉर्ट-एक्टिंग (अल्ट्रा-शॉर्ट-एक्टिंग) इंसुलिन के इंजेक्शन के साथ दिया जाता है। इस मामले में, खुराक का चयन मुख्य रूप से मुख्य दैनिक भोजन (दोपहर का भोजन, रात का खाना) से पहले ग्लाइसेमिक स्तर के आधार पर किया जाता है; इसके अलावा, इसे भोजन के बीच के अंतराल में हाइपोग्लाइसीमिया के विकास से सीमित किया जा सकता है, उदाहरण के लिए दोपहर में, नाश्ते और दोपहर के भोजन के बीच।
इंसुलिन की पूरी खुराक लंबे समय से अभिनय(ग्लार्जिन) दिन में एक बार दी जाती है, और इससे कोई फर्क नहीं पड़ता कि किस समय। कैनेटीक्स
रात के समय हाइपोग्लाइसीमिया सहित हाइपोग्लाइसीमिया विकसित होने के जोखिम के मामले में इंसुलिन ग्लार्गिन और डिटेमिर अधिक अनुकूल हैं।
शॉर्ट-एक्टिंग या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन की खुराक, यहां तक कि रोगी के लिए इंसुलिन प्रिस्क्रिप्शन के पहले दिन भी, खपत किए गए कार्बोहाइड्रेट की मात्रा (ब्रेड यूनिट) और इंजेक्शन से पहले ग्लाइसेमिया के स्तर पर निर्भर करेगी। परंपरागत रूप से, इंसुलिन स्राव की सामान्य दैनिक लय के आधार पर, लघु-अभिनय इंसुलिन की लगभग 1/4 खुराक (6-8 इकाइयाँ) रात के खाने के लिए आवंटित की जाती है, शेष खुराक को लगभग समान रूप से नाश्ते और दोपहर के भोजन (10-12) में विभाजित किया जाता है। इकाइयाँ)। प्रारंभिक ग्लाइसेमिक स्तर जितना अधिक होगा, प्रशासित इंसुलिन की प्रति यूनिट यह उतना ही कम होगा। शॉर्ट-एक्टिंग इंसुलिन इंजेक्शन भोजन से 30 मिनट पहले दिया जाता है, अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन इंजेक्शन भोजन से तुरंत पहले या भोजन के तुरंत बाद भी दिया जाता है। लघु-अभिनय इंसुलिन की खुराक की पर्याप्तता का आकलन भोजन के 2 घंटे बाद और अगले भोजन से पहले ग्लाइसेमिक संकेतकों द्वारा किया जाता है।
गहन इंसुलिन थेरेपी के दौरान इंसुलिन की खुराक की गणना करने के लिए, केवल कार्बोहाइड्रेट घटक के आधार पर एक्सई की संख्या की गणना करना पर्याप्त है। इस मामले में, सभी कार्बोहाइड्रेट युक्त उत्पादों को ध्यान में नहीं रखा जाता है, बल्कि केवल तथाकथित गणनीय उत्पादों को ध्यान में रखा जाता है। उत्तरार्द्ध में आलू, अनाज उत्पाद, फल, तरल डेयरी और मीठे उत्पाद शामिल हैं। अपाच्य कार्बोहाइड्रेट (अधिकांश सब्जियां) वाले उत्पादों को ध्यान में नहीं रखा जाता है। विशेष विनिमय तालिकाएँ विकसित की गई हैं जिनकी सहायता से, XE में कार्बोहाइड्रेट की मात्रा व्यक्त करके, आप इंसुलिन की आवश्यक खुराक की गणना कर सकते हैं। एक XE 10-12 ग्राम कार्बोहाइड्रेट से मेल खाता है (सारणी 10.7)।
1 XE युक्त भोजन खाने के बाद, ग्लाइसेमिक स्तर 1.6-2.2 mmol/l तक बढ़ जाता है, यानी। लगभग उतना ही जितना कि 1 यूनिट इंसुलिन देने पर ग्लूकोज का स्तर कम हो जाता है। दूसरे शब्दों में, जिस भोजन को आप खाने की योजना बना रहे हैं उसमें शामिल प्रत्येक एक्सई के लिए, आपको पहले से लगभग 1 यूनिट इंसुलिन का प्रबंध करना होगा (दिन के समय के आधार पर)। इसके अलावा, ग्लाइसेमिक स्तर की स्व-निगरानी के परिणामों को ध्यान में रखना आवश्यक है, जो प्रत्येक इंजेक्शन से पहले किया जाता है, और दिन का समय (सुबह में 1 एक्सई प्रति 2 यू इंसुलिन और दोपहर के भोजन के समय, 1 यू) रात के खाने में प्रति 1 XE)। इसलिए, यदि हाइपरग्लेसेमिया का पता चलता है, तो आगामी भोजन (एक्सई की संख्या के आधार पर) के अनुसार गणना की जाने वाली इंसुलिन की खुराक को बढ़ाने की आवश्यकता होती है, और इसके विपरीत, यदि हाइपोग्लाइसीमिया का पता चलता है, तो कम इंसुलिन प्रशासित किया जाता है।
मेज़ 7.7. 1 XE बनाने वाले उत्पादों का समतुल्य प्रतिस्थापन
 उदाहरण के लिए, यदि किसी मरीज का ग्लाइसेमिक स्तर 5 XE वाले नियोजित रात्रिभोज से 30 मिनट पहले 7 mmol/l है, तो उसे 1 यूनिट इंसुलिन इंजेक्ट करने की आवश्यकता है ताकि ग्लाइसेमिया सामान्य स्तर तक कम हो जाए: 7 mmol/l से लगभग 5 एमएमओएल/एल. इसके अलावा, 5 एक्सई को कवर करने के लिए 5 यूनिट इंसुलिन का प्रबंध किया जाना चाहिए। इस प्रकार, इस मामले में, रोगी को 6 यूनिट शॉर्ट-एक्टिंग या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन इंजेक्ट किया जाएगा।
उदाहरण के लिए, यदि किसी मरीज का ग्लाइसेमिक स्तर 5 XE वाले नियोजित रात्रिभोज से 30 मिनट पहले 7 mmol/l है, तो उसे 1 यूनिट इंसुलिन इंजेक्ट करने की आवश्यकता है ताकि ग्लाइसेमिया सामान्य स्तर तक कम हो जाए: 7 mmol/l से लगभग 5 एमएमओएल/एल. इसके अलावा, 5 एक्सई को कवर करने के लिए 5 यूनिट इंसुलिन का प्रबंध किया जाना चाहिए। इस प्रकार, इस मामले में, रोगी को 6 यूनिट शॉर्ट-एक्टिंग या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन इंजेक्ट किया जाएगा।
टी1डीएम के प्रकट होने और पर्याप्त लंबे समय तक इंसुलिन थेरेपी शुरू करने के बाद, इंसुलिन की आवश्यकता छोटी हो सकती है और 0.3-0.4 यू/किग्रा से कम हो सकती है। इस अवधि को छूट चरण के रूप में जाना जाता है, या "हनीमून"।हाइपरग्लेसेमिया और कीटोएसिडोसिस की अवधि के बाद, जो शेष β-कोशिकाओं के 10-15% द्वारा इंसुलिन स्राव को दबा देता है, इंसुलिन के प्रशासन द्वारा हार्मोनल-चयापचय संबंधी विकारों की भरपाई इन कोशिकाओं के कार्य को बहाल करती है, जो फिर शरीर को इंसुलिन प्रदान करने का काम करती हैं। न्यूनतम स्तर पर. यह अवधि कई हफ्तों से लेकर कई वर्षों तक रह सकती है, लेकिन अंततः, शेष β-कोशिकाओं के ऑटोइम्यून विनाश के कारण, "हनीमून" समाप्त हो जाता है।
आहारप्रशिक्षित रोगियों में T1DM के लिए जिनके पास आत्म-नियंत्रण और इंसुलिन खुराक के चयन का कौशल है, इसे उदार बनाया जा सकता है, अर्थात। मुक्त आ रहा हूँ. यदि रोगी का वजन अधिक या कम नहीं है तो उसे आहार देना चाहिए
आइसोकैलोरिक. T1DM के लिए भोजन का मुख्य घटक कार्बोहाइड्रेट है, जो दैनिक कैलोरी का लगभग 65% होना चाहिए। जटिल, धीरे-धीरे अवशोषित कार्बोहाइड्रेट वाले उत्पादों के साथ-साथ आहार फाइबर से भरपूर उत्पादों को प्राथमिकता दी जानी चाहिए। आसानी से पचने योग्य कार्बोहाइड्रेट (आटा, मिठाई) वाले उत्पादों से बचना चाहिए। प्रोटीन का अनुपात 10-35% तक कम किया जाना चाहिए, जो माइक्रोएंगियोपैथी के विकास के जोखिम को कम करने में मदद करता है, और वसा का अनुपात 25-35% तक कम किया जाना चाहिए, जबकि वसा को सीमित करना 7% कैलोरी तक होना चाहिए, जो एथेरोस्क्लेरोसिस के विकास के जोखिम को कम करता है। इसके अलावा, मादक पेय, विशेष रूप से मजबूत पेय पीने से बचना आवश्यक है।
T1DM वाले रोगी के साथ काम करने का एक अभिन्न अंग और प्रभावी मुआवजे की कुंजी है रोगी शिक्षा।अपने पूरे जीवन में, रोगी को कई कारकों के आधार पर, हर दिन स्वतंत्र रूप से इंसुलिन की खुराक बदलनी होगी। जाहिर है, इसके लिए कुछ कौशलों में निपुणता की आवश्यकता होती है जिन्हें रोगी को सिखाया जाना आवश्यक है। "डीएम-1 के साथ रोगी स्कूल" एंडोक्रिनोलॉजी अस्पतालों में या बाह्य रोगी के आधार पर आयोजित किया जाता है और इसमें 5-7 संरचित सत्र होते हैं जिसमें एक डॉक्टर या विशेष रूप से प्रशिक्षित नर्स, विभिन्न दृश्य सहायता का उपयोग करके, रोगियों को सिद्धांत सिखाते हैं। आत्म - संयम।
पूर्वानुमान
इंसुलिन थेरेपी के अभाव में, टाइप 1 मधुमेह वाले रोगी कीटोएसिडोटिक कोमा से अनिवार्य रूप से मृत्यु हो जाती है। अपर्याप्त इंसुलिन थेरेपी के साथ, जिसकी पृष्ठभूमि के खिलाफ मधुमेह के मुआवजे के मानदंड हासिल नहीं किए गए हैं और रोगी क्रोनिक हाइपरग्लेसेमिया (तालिका 7.3) की स्थिति में है, देर से जटिलताएं विकसित होने लगती हैं और प्रगति होती है (खंड 7.8)। T1DM में, डायबिटिक माइक्रोएंगियोपैथी (नेफ्रोपैथी और रेटिनोपैथी) और न्यूरोपैथी (डायबिटिक फुट सिंड्रोम) की अभिव्यक्तियाँ इस संबंध में सबसे बड़ा नैदानिक महत्व रखती हैं। टाइप 1 मधुमेह में मैक्रोएंगियोपैथी अपेक्षाकृत कम ही सामने आती है।
7.6. टाइप 2 मधुमेह मेलिटस
मधुमेह मेलेटस प्रकार 2- इंसुलिन प्रतिरोध और β-कोशिकाओं की स्रावी शिथिलता के कारण हाइपरग्लेसेमिया के विकास के साथ बिगड़ा हुआ कार्बोहाइड्रेट चयापचय द्वारा प्रकट एक पुरानी बीमारी,
साथ ही एथेरोस्क्लेरोसिस के विकास के साथ लिपिड चयापचय। चूँकि रोगियों में मृत्यु और विकलांगता का मुख्य कारण प्रणालीगत एथेरोस्क्लेरोसिस की जटिलताएँ हैं, T2DM को कभी-कभी हृदय रोग भी कहा जाता है।
मेज़ 7.8.मधुमेह मेलेटस प्रकार 2
 एटियलजि
एटियलजि
T2DM वंशानुगत प्रवृत्ति वाली एक बहुक्रियात्मक बीमारी है। एक जैसे जुड़वाँ बच्चों में T2DM के लिए सहमति 80% या उससे अधिक तक पहुँच जाती है। T2DM वाले अधिकांश मरीज़ अपने निकटतम परिवार में T2DM की उपस्थिति का संकेत देते हैं; यदि माता-पिता में से किसी एक को T2DM है, तो जीवन भर वंशज में इसके विकसित होने की संभावना 40% है। कोई एकल जीन, जिसकी बहुरूपता T2DM के प्रति पूर्वसूचना निर्धारित करती है, नहीं पाया गया है। पर्यावरणीय कारक, मुख्य रूप से जीवनशैली की विशेषताएं, T2DM के लिए वंशानुगत प्रवृत्ति की प्राप्ति में एक महान भूमिका निभाते हैं। T2DM विकसित होने के जोखिम कारक हैं:
मोटापा, विशेष रूप से आंत संबंधी (पैराग्राफ 11.2 देखें);
जातीयता (विशेषकर जब पारंपरिक जीवनशैली को पश्चिमी जीवनशैली में बदल रहे हों);
आसीन जीवन शैली;
आहार संबंधी विशेषताएं (परिष्कृत कार्बोहाइड्रेट की अधिक खपत और कम फाइबर सामग्री);
धमनी का उच्च रक्तचाप।
रोगजनन
रोगजनक रूप से, T2DM चयापचय संबंधी विकारों का एक विषम समूह है, जो इसकी महत्वपूर्ण नैदानिक विविधता को निर्धारित करता है। इसका रोगजनन इंसुलिन प्रतिरोध (ऊतकों द्वारा इंसुलिन-मध्यस्थ ग्लूकोज उपयोग में कमी) पर आधारित है, जो β-कोशिकाओं के स्रावी शिथिलता की पृष्ठभूमि के खिलाफ होता है। इस प्रकार, इंसुलिन संवेदनशीलता और इंसुलिन स्राव में असंतुलन होता है। स्रावी शिथिलताβ -कोशिकाएंइसमें रक्त शर्करा के स्तर में वृद्धि के जवाब में इंसुलिन के "प्रारंभिक" स्रावी रिलीज को धीमा करना शामिल है। इस मामले में, स्राव का पहला (तेज़) चरण, जिसमें संचित इंसुलिन के साथ पुटिकाओं को खाली करना शामिल है, वस्तुतः अनुपस्थित है; स्राव का दूसरा (धीमा) चरण टॉनिक मोड में लगातार हाइपरग्लेसेमिया को स्थिर करने की प्रतिक्रिया में होता है, और, अतिरिक्त इंसुलिन स्राव के बावजूद, इंसुलिन प्रतिरोध की पृष्ठभूमि के खिलाफ ग्लाइसेमिया का स्तर सामान्य नहीं होता है (चित्र 7.8)।
हाइपरइन्सुलिनमिया का परिणाम संवेदनशीलता और इंसुलिन रिसेप्टर्स की संख्या में कमी, साथ ही दमन है
पोस्ट-रिसेप्टर तंत्र इंसुलिन के प्रभाव की मध्यस्थता करता है (इंसुलिन प्रतिरोध)।मांसपेशियों और वसा कोशिकाओं (जीएलयूटी-4) में मुख्य ग्लूकोज ट्रांसपोर्टर की सामग्री आंत के मोटापे वाले व्यक्तियों में 40% और टाइप 2 मधुमेह वाले व्यक्तियों में 80% कम हो जाती है। हेपेटोसाइट्स और पोर्टल के इंसुलिन प्रतिरोध के कारण हाइपरइंसुलिनमिया होता है यकृत द्वारा ग्लूकोज का अत्यधिक उत्पादन,और फास्टिंग हाइपरग्लेसेमिया विकसित हो जाता है, जिसका पता रोग के प्रारंभिक चरण सहित टी2डीएम वाले अधिकांश रोगियों में लगाया जाता है।
हाइपरग्लेसेमिया स्वयं β-कोशिकाओं (ग्लूकोटॉक्सिसिटी) की स्रावी गतिविधि की प्रकृति और स्तर पर प्रतिकूल प्रभाव डालता है। लंबे समय तक, कई वर्षों और दशकों तक, मौजूदा हाइपरग्लेसेमिया अंततः β-सेल इंसुलिन उत्पादन में कमी का कारण बनता है और रोगी को कुछ लक्षणों का अनुभव हो सकता है इंसुलिन की कमी- वजन में कमी, सहवर्ती संक्रामक रोगों के साथ कीटोसिस। हालाँकि, अवशिष्ट इंसुलिन उत्पादन, जो किटोएसिडोसिस को रोकने के लिए पर्याप्त है, लगभग हमेशा T2DM में संरक्षित रहता है।
महामारी विज्ञान
T2DM समग्र रूप से मधुमेह की महामारी विज्ञान को निर्धारित करता है, क्योंकि यह इस बीमारी के लगभग 98% मामलों का कारण बनता है। T2DM की व्यापकता देशों और जातीय समूहों के बीच भिन्न-भिन्न है। यूरोपीय में
 चावल। 7.8.टाइप 2 मधुमेह मेलेटस में β-कोशिकाओं की स्रावी शिथिलता (इंसुलिन स्राव के पहले तेज़ चरण का नुकसान)
चावल। 7.8.टाइप 2 मधुमेह मेलेटस में β-कोशिकाओं की स्रावी शिथिलता (इंसुलिन स्राव के पहले तेज़ चरण का नुकसान)
देशों, संयुक्त राज्य अमेरिका और रूसी संघ में, यह जनसंख्या का लगभग 5-6% है। T2DM की घटना उम्र के साथ बढ़ती है: वयस्कों में, T2DM की व्यापकता 10% है, और 65 वर्ष से अधिक उम्र के लोगों में यह 20% तक पहुँच जाती है। मूल अमेरिकियों और हवाईवासियों में T2DM की घटना 2.5 गुना अधिक है; पीमा इंडियंस (एरिज़ोना) में यह 50% तक पहुँच जाता है। भारत, चीन, चिली और अफ्रीकी देशों की पारंपरिक जीवनशैली जीने वाली ग्रामीण आबादी में T2DM का प्रचलन बहुत कम (1% से कम) है। दूसरी ओर, पश्चिमी औद्योगिक देशों में अप्रवासियों के बीच यह एक महत्वपूर्ण स्तर तक पहुँच जाता है। इस प्रकार, संयुक्त राज्य अमेरिका और ग्रेट ब्रिटेन में रहने वाले भारत और चीन के अप्रवासियों के बीच, T2DM की व्यापकता 12-15% तक पहुँच जाती है।
डब्ल्यूएचओ का अनुमान है कि अगले 20 वर्षों में दुनिया में मधुमेह से पीड़ित लोगों की संख्या 122% (135 से 300 मिलियन तक) बढ़ जाएगी। यह जनसंख्या की प्रगतिशील उम्र बढ़ने और शहरी जीवनशैली के फैलने और बिगड़ने दोनों के कारण है। हाल के वर्षों में, T2DM का एक महत्वपूर्ण "कायाकल्प" हुआ है और बच्चों में इसकी घटनाओं में वृद्धि हुई है।
नैदानिक अभिव्यक्तियाँ
अधिकतर परिस्थितियों में, कोई स्पष्ट नैदानिक अभिव्यक्तियाँ नहीं हैं,और निदान ग्लाइसेमिक स्तरों के नियमित निर्धारण द्वारा स्थापित किया जाता है। यह रोग आम तौर पर 40 वर्ष की आयु में प्रकट होता है, जबकि अधिकांश रोगियों में मोटापा और चयापचय सिंड्रोम के अन्य घटक होते हैं (धारा 11.2 देखें)। यदि इसके लिए कोई अन्य कारण न हों तो मरीज़ प्रदर्शन में कमी की शिकायत नहीं करते हैं। प्यास और बहुमूत्र की शिकायतें शायद ही कभी महत्वपूर्ण गंभीरता तक पहुँचती हैं। अक्सर, रोगी त्वचा और योनि की खुजली से परेशान होते हैं, और इसलिए वे त्वचा विशेषज्ञों और स्त्री रोग विशेषज्ञों के पास जाते हैं। चूँकि T2DM की वास्तविक अभिव्यक्ति से लेकर निदान तक कई वर्ष (औसतन लगभग 7 वर्ष) बीत जाते हैं, कई रोगियों में नैदानिक तस्वीर हावी रहती है मधुमेह की देर से होने वाली जटिलताओं के लक्षण और अभिव्यक्तियाँ।इसके अलावा, T2DM वाले रोगी की चिकित्सा देखभाल के लिए पहली यात्रा अक्सर देर से होने वाली जटिलताओं के कारण होती है। इस प्रकार, पैरों के अल्सरेटिव घावों वाले रोगियों को सर्जिकल अस्पतालों में अस्पताल में भर्ती कराया जा सकता है (मधुमेह पैर सिंड्रोम),प्रगतिशील दृष्टि हानि के कारण नेत्र रोग विशेषज्ञों से संपर्क करें (मधुमेह संबंधी रेटिनोपैथी),दिल का दौरा पड़ने, स्ट्रोक होने पर अस्पताल में भर्ती होना
टैमी, उन संस्थानों में पैरों की वाहिकाओं के घावों को मिटाना जहां हाइपरग्लेसेमिया का पहली बार पता चला है।
निदान
सभी प्रकार के मधुमेह के लिए सामान्य नैदानिक मानदंड पैराग्राफ 7.3 में प्रस्तुत किए गए हैं। अधिकांश मामलों में डीएम-2 का निदान डीएम-2 के विशिष्ट नैदानिक लक्षणों (मोटापा, 40-45 वर्ष से अधिक आयु, डीएम-2 का सकारात्मक पारिवारिक इतिहास, डीएम-2 के अन्य घटक) वाले व्यक्तियों में हाइपरग्लेसेमिया की पहचान पर आधारित है। मेटाबोलिक सिंड्रोम), नैदानिक और प्रयोगशाला संकेतों की अनुपस्थिति में पूर्ण इंसुलिन की कमी (स्पष्ट वजन घटाने, केटोसिस)। T2DM के उच्च प्रसार का संयोजन, इसकी विशेषता दीर्घकालिक स्पर्शोन्मुख पाठ्यक्रम और शीघ्र निदान के साथ इसकी गंभीर जटिलताओं को रोकने की संभावना आवश्यकता को पूर्व निर्धारित करती है स्क्रीनिंग,वे। रोग के किसी भी लक्षण के बिना व्यक्तियों में T2DM को बाहर करने के लिए एक परीक्षा आयोजित करना। मुख्य परीक्षण, जैसा कि संकेत दिया गया है, दृढ़ संकल्प है उपवास रक्त शर्करा का स्तर।यह निम्नलिखित स्थितियों में दर्शाया गया है:
1. 45 वर्ष से अधिक आयु के सभी लोगों में, विशेष रूप से अतिरिक्त शरीर के वजन (बीएमआई 25 किग्रा/एम2 से अधिक) के साथ हर 3 साल के अंतराल पर।
2. कम उम्र में शरीर का अतिरिक्त वजन (बीएमआई 25 किग्रा/एम2 से अधिक) और अतिरिक्त जोखिम कारकों की उपस्थिति में, जिनमें शामिल हैं:
आसीन जीवन शैली;
करीबी रिश्तेदारों में सीडी-2;
T2DM विकसित होने के उच्च जोखिम वाली राष्ट्रीयताओं से संबंधित (अफ्रीकी अमेरिकी, हिस्पैनिक, मूल अमेरिकी, आदि);
जिन महिलाओं ने 4 किलोग्राम से अधिक वजन वाले बच्चे को जन्म दिया है और/या गर्भकालीन मधुमेह का इतिहास है;
धमनी उच्च रक्तचाप (≥ 140/90 मिमी एचजी);
एचडीएल स्तर > 0.9 mmol/l और/या ट्राइग्लिसराइड्स > 2.8 mmol/l;
बहुगंठिय अंडाशय लक्षण;
एनटीजी और एनजीएनटी;
हृदय रोग।
बच्चों में T2DM की घटनाओं में उल्लेखनीय वृद्धि ग्लाइसेमिक स्तर के स्क्रीनिंग निर्धारण की आवश्यकता को निर्धारित करती है बच्चों और किशोरों के बीच(10 वर्ष से शुरू होकर 2 वर्ष के अंतराल के साथ या शुरुआत के साथ
यौवन, यदि यह पहले की उम्र में हुआ हो), उच्च जोखिम वाले समूहों से संबंधित है, जिसमें बच्चे भी शामिल हैं शरीर के अतिरिक्त वजन के साथ(बीएमआई और/या वजन > उम्र के लिए 85वां प्रतिशत या आदर्श वजन के 120% से अधिक वजन) निम्नलिखित अतिरिक्त जोखिम कारकों में से किन्हीं दो के संयोजन में:
प्रथम या द्वितीय श्रेणी के रिश्तेदारों के बीच सीडी-2;
उच्च जोखिम वाली राष्ट्रीयताओं से संबंधित;
इंसुलिन प्रतिरोध से जुड़ी नैदानिक अभिव्यक्तियाँ (अकन्थोसिस निगरिकन्स,धमनी उच्च रक्तचाप, डिस्लिपिडेमिया);
माँ में गर्भकालीन मधुमेह सहित मधुमेह।
क्रमानुसार रोग का निदान
डीएम-2 और डीएम-1 का विभेदक निदान सबसे बड़ा नैदानिक महत्व है, जिसके सिद्धांत पैराग्राफ 7.5 (तालिका 7.6) में वर्णित हैं। जैसा कि संकेत दिया गया है, ज्यादातर मामलों में यह नैदानिक डेटा पर आधारित है। ऐसे मामलों में जहां मधुमेह के प्रकार को स्थापित करना मुश्किल है, या वंशानुगत सिंड्रोम के ढांचे सहित मधुमेह के कुछ दुर्लभ प्रकार का संदेह है, सबसे महत्वपूर्ण व्यावहारिक प्रश्न जिसका उत्तर दिया जाना चाहिए वह यह है कि क्या रोगी को इंसुलिन थेरेपी की आवश्यकता है।
इलाज
DM2 के उपचार के मुख्य घटक हैं: आहार चिकित्सा, बढ़ी हुई शारीरिक गतिविधि, हाइपोग्लाइसेमिक थेरेपी, DM की देर से होने वाली जटिलताओं की रोकथाम और उपचार। चूंकि T2DM वाले अधिकांश रोगी मोटापे से ग्रस्त हैं, इसलिए आहार का उद्देश्य वजन कम करना (हाइपोकैलोरिक) और देर से होने वाली जटिलताओं, मुख्य रूप से मैक्रोएंगियोपैथी (एथेरोस्क्लेरोसिस) की रोकथाम करना होना चाहिए। हाइपोकैलोरिक आहारअतिरिक्त शरीर के वजन (बीएमआई 25-29 किग्रा/एम2) या मोटापे (बीएमआई > 30 किग्रा/एम2) वाले सभी रोगियों के लिए आवश्यक है। ज्यादातर मामलों में, महिलाओं के लिए दैनिक कैलोरी सेवन को 1000-1200 किलो कैलोरी और पुरुषों के लिए 1200-1600 किलो कैलोरी तक कम करने की सिफारिश की जानी चाहिए। डीएम-2 के लिए मुख्य खाद्य घटकों का अनुशंसित अनुपात डीएम-1 (कार्बोहाइड्रेट - 65%, प्रोटीन 10-35%, वसा 25-35% तक) के समान है। उपयोग शराबइस तथ्य के कारण इसे सीमित किया जाना चाहिए कि यह अतिरिक्त कैलोरी का एक महत्वपूर्ण स्रोत है; इसके अलावा, उपचार के दौरान शराब का सेवन
सल्फोनीलुरिया और इंसुलिन का अंतर्ग्रहण हाइपोग्लाइसीमिया के विकास को भड़का सकता है (धारा 7.7.3 देखें)।
के लिए सिफ़ारिशें बढ़ती शारीरिक गतिविधिव्यक्तिगत होना चाहिए. शुरुआत में, दिन में 3-5 बार (प्रति सप्ताह लगभग 150 मिनट) 30-45 मिनट तक चलने वाले मध्यम तीव्रता के एरोबिक व्यायाम (चलना, तैरना) की सिफारिश की जाती है। भविष्य में, शारीरिक गतिविधि में क्रमिक वृद्धि आवश्यक है, जो शरीर के वजन को कम करने और सामान्य करने में महत्वपूर्ण योगदान देती है। इसके अलावा, शारीरिक गतिविधि इंसुलिन प्रतिरोध को कम करने में मदद करती है और हाइपोग्लाइसेमिक प्रभाव डालती है। ग्लूकोज कम करने वाली दवाओं को निर्धारित किए बिना आहार चिकित्सा और बढ़ी हुई शारीरिक गतिविधि का संयोजन T2DM वाले लगभग 5% रोगियों में स्थापित लक्ष्यों (तालिका 7.3) के अनुसार मधुमेह क्षतिपूर्ति को बनाए रखना संभव बनाता है।
के लिए औषधियाँ हाइपोग्लाइसेमिक थेरेपी T2DM को चार मुख्य समूहों में विभाजित किया जा सकता है।
I. दवाएं जो इंसुलिन प्रतिरोध (सेंसिटाइज़र) को कम करने में मदद करती हैं।इस समूह में मेटफॉर्मिन और थियाज़ोलिडाइनायड्स शामिल हैं। मेटफोर्मिनवर्तमान में उपयोग में आने वाली समूह की एकमात्र दवा है बिगुआनाइड्स.इसकी क्रियाविधि के मुख्य घटक हैं:
1. यकृत में ग्लूकोनियोजेनेसिस का दमन (यकृत द्वारा ग्लूकोज उत्पादन में कमी), जिससे तेजी से रक्त शर्करा के स्तर में कमी आती है।
2. इंसुलिन प्रतिरोध में कमी (परिधीय ऊतकों, मुख्य रूप से मांसपेशियों द्वारा ग्लूकोज का उपयोग में वृद्धि)।
3. अवायवीय ग्लाइकोलाइसिस का सक्रियण और छोटी आंत में ग्लूकोज अवशोषण में कमी।
मेटफोर्मिनटाइप 2 मधुमेह, मोटापा और फास्टिंग हाइपरग्लेसेमिया वाले रोगियों में ग्लूकोज कम करने वाली चिकित्सा के लिए पहली पसंद की दवा है। शुरुआती खुराक रात में या रात के खाने के साथ 500 मिलीग्राम है। इसके बाद, खुराक को धीरे-धीरे 2-3 खुराक में 2-3 ग्राम तक बढ़ाया जाता है। दुष्प्रभावों में, अपच (दस्त) अपेक्षाकृत आम है, जो, एक नियम के रूप में, क्षणिक है और दवा लेने के 1-2 सप्ताह के बाद अपने आप ठीक हो जाता है। चूंकि मेटफॉर्मिन का इंसुलिन उत्पादन पर उत्तेजक प्रभाव नहीं पड़ता है, इसलिए इस दवा के साथ मोनोथेरेपी के दौरान हाइपोग्लाइसीमिया नहीं होता है।
विकसित करें (इसकी क्रिया को एंटीहाइपरग्लाइसेमिक के रूप में नामित किया जाएगा, न कि हाइपोग्लाइसेमिक के रूप में)। मेटफॉर्मिन के उपयोग में बाधाएं गर्भावस्था, गंभीर हृदय, यकृत, गुर्दे और अन्य अंग विफलता, साथ ही अन्य मूल की हाइपोक्सिक स्थितियां हैं। एक अत्यंत दुर्लभ जटिलता जो तब होती है जब उपरोक्त मतभेदों को ध्यान में रखे बिना मेटफॉर्मिन निर्धारित किया जाता है, लैक्टिक एसिडोसिस है, जो एनारोबिक ग्लाइकोलाइसिस के अतिसक्रियण का परिणाम है।
थियाजोलिडाइनायड्स(पियोग्लिटाज़ोन, रोसिग्लिटाज़ोन) पेरोक्सीसोम प्रोलिफ़रेटर-सक्रिय रिसेप्टर γ (PPAR-γ) एगोनिस्ट हैं। थियाजोलिडाइनायड्स मांसपेशियों और वसा ऊतकों में ग्लूकोज और लिपिड के चयापचय को सक्रिय करता है, जिससे अंतर्जात इंसुलिन की गतिविधि में वृद्धि होती है, अर्थात। इंसुलिन प्रतिरोध (इंसुलिन सेंसिटाइज़र) को खत्म करने के लिए। पियोग्लिटाज़ोन की दैनिक खुराक 15-30 मिलीग्राम/दिन है, रोसिग्लिटाज़ोन - 4-8 मिलीग्राम (1-2 खुराक के लिए)। मेटफॉर्मिन के साथ थियाज़ोलिडाइनायड्स का संयोजन बहुत प्रभावी है। थियाजोलिडाइनायड्स के उपयोग के लिए एक विपरीत संकेत यकृत ट्रांसएमिनेस के स्तर में वृद्धि (2.5 गुना या अधिक) है। हेपेटोटॉक्सिसिटी के अलावा, थियाजोलिडाइनायड्स के दुष्प्रभावों में द्रव प्रतिधारण और एडिमा शामिल हैं, जो अक्सर तब विकसित होते हैं जब दवाओं को इंसुलिन के साथ जोड़ा जाता है।
द्वितीय. दवाएँ असर कर रही हैंβ -सेल और बढ़े हुए इंसुलिन स्राव को बढ़ावा देता है।इस समूह में सल्फोनीलुरिया और ग्लिनाइड्स (प्रांडियल ग्लाइसेमिक रेगुलेटर) शामिल हैं, जिनका उपयोग मुख्य रूप से भोजन के बाद ग्लाइसेमिक स्तर को सामान्य करने के लिए किया जाता है। मुख्य लक्ष्य सल्फोनिलयूरिया(पीएसएम) अग्नाशयी आइलेट्स की β-कोशिकाएं हैं। पीएसएम β-सेल झिल्ली पर विशिष्ट रिसेप्टर्स से जुड़ते हैं। इससे एटीपी-निर्भर पोटेशियम चैनल बंद हो जाते हैं और कोशिका झिल्ली का विध्रुवण होता है, जो बदले में कैल्शियम चैनलों के खुलने को बढ़ावा देता है। β-कोशिकाओं में कैल्शियम के प्रवेश से उनका क्षरण होता है और रक्त में इंसुलिन का स्राव होता है। नैदानिक अभ्यास में, बहुत सारे पीएसएम का उपयोग किया जाता है, जो ग्लूकोज कम करने वाले प्रभाव की अवधि और गंभीरता में भिन्न होते हैं (तालिका 7.9)।
मेज़ 7.9.सल्फोनिलयूरिया
 पीएसएम का मुख्य और काफी सामान्य दुष्प्रभाव हाइपोग्लाइसीमिया है (धारा 7.7.3 देखें)। यह दवा की अधिक मात्रा, इसके संचय (गुर्दे की विफलता) के साथ हो सकता है।
पीएसएम का मुख्य और काफी सामान्य दुष्प्रभाव हाइपोग्लाइसीमिया है (धारा 7.7.3 देखें)। यह दवा की अधिक मात्रा, इसके संचय (गुर्दे की विफलता) के साथ हो सकता है।
आहार का अनुपालन न करना (भोजन छोड़ना, शराब पीना) या आहार (महत्वपूर्ण शारीरिक गतिविधि, जिसके पहले पीएसएम की खुराक कम नहीं की गई थी या कार्बोहाइड्रेट नहीं लिया गया था)।
समूह को glinides(प्रैंडियल ग्लाइसेमिक रेगुलेटर) शामिल हैं repaglinide(बेंजोइक एसिड व्युत्पन्न; दैनिक खुराक 0.5-16 मिलीग्राम/दिन) और Nateglinide(डी-फेनिलएलनिन व्युत्पन्न; दैनिक खुराक 180-540 मिलीग्राम/दिन)। एक बार प्रशासित होने के बाद, दवाएं तेजी से और विपरीत रूप से β-सेल पर सल्फोनील्यूरिया रिसेप्टर के साथ बातचीत करती हैं, जिसके परिणामस्वरूप इंसुलिन के स्तर में थोड़ी वृद्धि होती है जो सामान्य इंसुलिन स्राव के पहले चरण की नकल करती है। दवाएं मुख्य भोजन से 10-20 मिनट पहले ली जाती हैं, आमतौर पर दिन में 3 बार।
तृतीय. दवाएं जो आंत में ग्लूकोज के अवशोषण को कम करती हैं।
इस समूह में एकरबोस और ग्वार गम शामिल हैं। एकरबोस की क्रिया का तंत्र छोटी आंत में α-ग्लाइकोसिडेस की प्रतिवर्ती नाकाबंदी है, जिसके परिणामस्वरूप अनुक्रमिक किण्वन और कार्बोहाइड्रेट के अवशोषण की प्रक्रिया धीमी हो जाती है, पुनर्वसन की दर और यकृत में ग्लूकोज का प्रवेश कम हो जाता है। , और भोजन के बाद ग्लाइसेमिया का स्तर कम हो जाता है। एकरबोस की प्रारंभिक खुराक दिन में 3 बार 50 मिलीग्राम है, बाद में खुराक को दिन में 3 बार 100 मिलीग्राम तक बढ़ाया जा सकता है; दवा भोजन से तुरंत पहले या भोजन के दौरान ली जाती है। एकरबोस का मुख्य दुष्प्रभाव आंतों की अपच (दस्त, पेट फूलना) है, जो बृहदान्त्र में अनवशोषित कार्बोहाइड्रेट के प्रवेश से जुड़ा है। एकरबोस का ग्लूकोज कम करने वाला प्रभाव बहुत मध्यम है (तालिका 7.10)।
नैदानिक अभ्यास में, टैबलेट वाली हाइपोग्लाइसेमिक दवाओं को एक दूसरे के साथ और इंसुलिन दवाओं के साथ प्रभावी ढंग से जोड़ा जाता है, क्योंकि अधिकांश रोगियों में उपवास और भोजन के बाद हाइपरग्लेसेमिया दोनों का एक साथ पता लगाया जाता है। असंख्य हैं निश्चित संयोजनएक गोली में दवा. अक्सर, मेटफ़ॉर्मिन को एक टैबलेट में विभिन्न पीएसएम के साथ जोड़ा जाता है, साथ ही मेटफ़ॉर्मिन को थियाज़ोलिडाइनायड्स के साथ जोड़ा जाता है।
मेज़ 7.10.टेबलेटयुक्त हाइपोग्लाइसेमिक दवाओं की क्रिया का तंत्र और संभावित प्रभावशीलता
 चतुर्थ. इंसुलिन और इंसुलिन एनालॉग्स
चतुर्थ. इंसुलिन और इंसुलिन एनालॉग्स
एक निश्चित चरण में, T2DM वाले 30-40% रोगियों को इंसुलिन की तैयारी मिलनी शुरू हो जाती है। टाइप 2 मधुमेह के लिए इंसुलिन थेरेपी के संकेत खंड 7.4 की शुरुआत में दिए गए हैं। T2DM वाले रोगियों को इंसुलिन थेरेपी में स्थानांतरित करने का सबसे आम विकल्प ग्लूकोज कम करने वाली दवाओं की गोलियों के साथ लंबे समय तक काम करने वाले इंसुलिन (एनपीएच इंसुलिन, ग्लार्गिन या डिटेमिर) को निर्धारित करना है। ऐसी स्थिति में जहां उपवास रक्त शर्करा के स्तर को मेटफॉर्मिन निर्धारित करके नियंत्रित नहीं किया जा सकता है या बाद वाला वर्जित है, रोगी को शाम (रात में) इंसुलिन इंजेक्शन निर्धारित किया जाता है। यदि टैबलेट दवाओं का उपयोग करके उपवास और भोजन के बाद ग्लाइसेमिया दोनों को नियंत्रित करना असंभव है, तो रोगी को मोनोइंसुलिन थेरेपी में स्थानांतरित किया जाता है। आमतौर पर, T2DM के लिए, तथाकथित के अनुसार इंसुलिन थेरेपी की जाती है "पारंपरिक" योजनाजिसमें लंबी-अभिनय और लघु-अभिनय इंसुलिन की निश्चित खुराक निर्धारित करना शामिल है। इस योजना में
एक बोतल में लघु (अल्ट्रा-शॉर्ट) और लंबे समय तक काम करने वाले इंसुलिन वाले मानक इंसुलिन मिश्रण सुविधाजनक होते हैं। पारंपरिक इंसुलिन थेरेपी का विकल्प इस तथ्य से निर्धारित होता है कि टी2डीएम के मामले में, इसे अक्सर बुजुर्ग रोगियों को निर्धारित किया जाता है, जिन्हें इंसुलिन की खुराक को स्वतंत्र रूप से बदलना सिखाना मुश्किल होता है। इसके अलावा, गहन इंसुलिन थेरेपी, जिसका लक्ष्य नॉर्मोग्लाइसीमिया के करीब पहुंचने वाले स्तर पर कार्बोहाइड्रेट चयापचय के मुआवजे को बनाए रखना है, हाइपोग्लाइसीमिया का खतरा बढ़ जाता है। जबकि हल्का हाइपोग्लाइसीमिया युवा रोगियों में गंभीर खतरा पैदा नहीं करता है, हाइपोग्लाइसीमिया का अनुभव करने की कम सीमा वाले वृद्ध रोगियों में इसके हृदय संबंधी बहुत प्रतिकूल परिणाम हो सकते हैं। टी2डीएम वाले युवा रोगियों, साथ ही प्रभावी सीखने के आशाजनक अवसरों वाले रोगियों को इंसुलिन थेरेपी का एक गहन संस्करण निर्धारित किया जा सकता है।
पूर्वानुमान
T2DM वाले रोगियों में विकलांगता और मृत्यु का मुख्य कारण देर से होने वाली जटिलताएँ हैं (धारा 7.8 देखें), सबसे अधिक बार मधुमेह संबंधी मैक्रोएंगियोपैथी। देर से आने वाली कुछ जटिलताओं के विकसित होने का जोखिम कई कारकों द्वारा निर्धारित होता है जिनकी चर्चा संबंधित अध्यायों में की गई है। उनके विकास के लिए एक सार्वभौमिक जोखिम कारक क्रोनिक हाइपरग्लेसेमिया है। इस प्रकार, टाइप 2 मधुमेह वाले रोगियों में एचबीए1सी के स्तर में 1% की कमी से समग्र मृत्यु दर में क्रमशः लगभग 20%, 2% और 3% - लगभग 40% की कमी आती है।
7.7. मधुमेह मेलिटस की गंभीर जटिलताएँ
7.7.1. डायबिटीज़ संबंधी कीटोएसिडोसिस
मधुमेह कीटोएसिडोसिस (डीकेए)- डीएम-1 का विघटन, इंसुलिन की पूर्ण कमी के कारण होता है, जो समय पर उपचार के अभाव में कीटोएसिडोटिक कोमा (केसी) और मृत्यु में समाप्त होता है।
एटियलजि
डीकेए इंसुलिन की पूर्ण कमी के कारण होता है। टी1डीएम (डीकेए के सभी मामलों में 10-20%) के प्रकट होने के समय अधिकांश रोगियों में अलग-अलग गंभीरता का डीकेए निर्धारित होता है।
टी1डीएम के स्थापित निदान वाले रोगी में, डीकेए तब विकसित हो सकता है जब इंसुलिन प्रशासन बंद कर दिया जाता है, अक्सर रोगी द्वारा स्वयं (डीकेए मामलों का 13%), सहवर्ती रोगों की पृष्ठभूमि के खिलाफ, मुख्य रूप से संक्रामक, वृद्धि की अनुपस्थिति में इंसुलिन की खुराक
मेज़ 7.11.डायबिटीज़ संबंधी कीटोएसिडोसिस
 टी1डीएम वाले युवा रोगियों में डीकेए विकास के 20% तक मामले मनोवैज्ञानिक समस्याओं और/या खाने के विकारों (वजन बढ़ने का डर, हाइपोग्लाइसीमिया का डर, किशोर समस्याएं) से जुड़े होते हैं। कई देशों में डीकेए का एक सामान्य कारण है
टी1डीएम वाले युवा रोगियों में डीकेए विकास के 20% तक मामले मनोवैज्ञानिक समस्याओं और/या खाने के विकारों (वजन बढ़ने का डर, हाइपोग्लाइसीमिया का डर, किशोर समस्याएं) से जुड़े होते हैं। कई देशों में डीकेए का एक सामान्य कारण है
जनसंख्या के कुछ वर्गों के लिए दवाओं की उच्च लागत के कारण रोगी द्वारा स्वयं इंसुलिन की निकासी (तालिका 7.11)।
रोगजनन
डीकेए का रोगजनन ग्लूकागन, कैटेकोलामाइन और कोर्टिसोल जैसे काउंटर-इंसुलर हार्मोन के उत्पादन में वृद्धि के साथ संयुक्त इंसुलिन की पूर्ण कमी पर आधारित है। नतीजतन, यकृत द्वारा ग्लूकोज के उत्पादन में उल्लेखनीय वृद्धि और परिधीय ऊतकों द्वारा इसके उपयोग का उल्लंघन, हाइपरग्लेसेमिया में वृद्धि और बाह्य कोशिकीय स्थान की ऑस्मोलैरिटी का उल्लंघन होता है। डीकेए में कॉन्ट्रेन्सुलर हार्मोन की सापेक्ष अधिकता के साथ संयोजन में इंसुलिन की कमी से परिसंचरण (लिपोलिसिस) में मुक्त फैटी एसिड की रिहाई होती है और यकृत में कीटोन बॉडी (β-हाइड्रॉक्सीब्यूटाइरेट, एसीटोएसिटेट, एसीटोन) में उनका अनियंत्रित ऑक्सीकरण होता है, जिसके परिणामस्वरूप हाइपरकेटोनमिया का विकास, और बाद में मेटाबोलिक एसिडोसिस। गंभीर ग्लाइकोसुरिया के परिणामस्वरूप, आसमाटिक ड्यूरिसिस, निर्जलीकरण, सोडियम, पोटेशियम और अन्य इलेक्ट्रोलाइट्स की हानि विकसित होती है (चित्र 7.9)।
महामारी विज्ञान
डीकेए के नए मामलों की घटना प्रति वर्ष टाइप 1 मधुमेह वाले प्रति 1000 रोगियों में 5-8 है और यह सीधे मधुमेह के रोगियों के लिए चिकित्सा देखभाल के संगठन के स्तर पर निर्भर करता है। संयुक्त राज्य अमेरिका में हर साल डीकेए के लिए लगभग 100,000 अस्पताल में भर्ती होते हैं, और प्रति मरीज 13,000 डॉलर प्रति अस्पताल की लागत के साथ, डीकेए के लिए आंतरिक रोगी देखभाल पर प्रति वर्ष 1 अरब डॉलर से अधिक खर्च किया जाता है। 2005 में रूसी संघ में, DKA 4.31% बच्चों, 4.75% किशोरों और 0.33% T1DM वाले वयस्क रोगियों में दर्ज किया गया था।
नैदानिक अभिव्यक्तियाँ
डीकेए के विकास में, इसके कारण के आधार पर, कई सप्ताह से लेकर एक दिन तक का समय लग सकता है। ज्यादातर मामलों में, डीकेए विघटित मधुमेह के लक्षणों से पहले होता है, लेकिन कभी-कभी उन्हें विकसित होने का समय नहीं मिल पाता है। डीकेए के नैदानिक लक्षणों में बहुमूत्रता, बहुमूत्रता, वजन घटना, फैला हुआ पेट दर्द ("मधुमेह स्यूडोपेरिटोनिटिस"), निर्जलीकरण, गंभीर कमजोरी, सांस से एसीटोन की गंध (या फल की गंध), और चेतना का धीरे-धीरे धुंधला होना शामिल हैं। प्रारंभिक निदान के कारण डीकेए के साथ सच्चा कोमा हाल ही में अपेक्षाकृत कम विकसित हुआ है। शारीरिक परीक्षण से निर्जलीकरण के लक्षणों का पता चलता है: कमी आई
 चावल। 7.9. कीटोएसिडोटिक कोमा का रोगजनन
चावल। 7.9. कीटोएसिडोटिक कोमा का रोगजनन
त्वचा का मरोड़ और नेत्रगोलक का घनत्व, क्षिप्रहृदयता, हाइपोटेंशन। उन्नत मामलों में, कुसमौल श्वास विकसित होती है। डीकेए के 25% से अधिक रोगियों में उल्टी विकसित होती है, जिसका रंग कॉफी के मैदान जैसा हो सकता है।
निदान
नैदानिक चित्र डेटा के आधार पर, संकेत मिलता है कि रोगी को टाइप 1 मधुमेह है, साथ ही प्रयोगशाला परीक्षण डेटा भी। डीकेए की विशेषता हाइपरग्लेसेमिया (कुछ मामलों में मामूली), केटोनुरिया, मेटाबोलिक एसिडोसिस, हाइपरोस्मोलैरिटी (तालिका 7.12) है।
मेज़ 7.12.मधुमेह मेलेटस की तीव्र जटिलताओं का प्रयोगशाला निदान
 मधुमेह के तीव्र विघटन वाले रोगियों की जांच करते समय, ग्लाइसेमिया, क्रिएटिनिन और यूरिया और इलेक्ट्रोलाइट्स के स्तर को निर्धारित करना आवश्यक है, जिसके आधार पर प्रभावी ऑस्मोलैरिटी की गणना की जाती है। इसके अलावा, एसिड-बेस स्थिति का आकलन आवश्यक है। प्रभावी ऑस्मोलेरिटी(ईओ) की गणना निम्नलिखित सूत्र का उपयोग करके की जाती है: 2 *। आम तौर पर, EO 285 - 295 mOsm/l है।
मधुमेह के तीव्र विघटन वाले रोगियों की जांच करते समय, ग्लाइसेमिया, क्रिएटिनिन और यूरिया और इलेक्ट्रोलाइट्स के स्तर को निर्धारित करना आवश्यक है, जिसके आधार पर प्रभावी ऑस्मोलैरिटी की गणना की जाती है। इसके अलावा, एसिड-बेस स्थिति का आकलन आवश्यक है। प्रभावी ऑस्मोलेरिटी(ईओ) की गणना निम्नलिखित सूत्र का उपयोग करके की जाती है: 2 *। आम तौर पर, EO 285 - 295 mOsm/l है।
डीकेए वाले अधिकांश रोगियों में, ल्यूकोसाइटोसिस,जिसकी गंभीरता रक्त में कीटोन बॉडी के स्तर के समानुपाती होती है। स्तर सोडियम,एक नियम के रूप में, यह हाइपरग्लेसेमिया के जवाब में इंट्रासेल्युलर स्थानों से बाह्य कोशिकीय स्थानों में तरल पदार्थ के आसमाटिक बहिर्वाह के कारण कम हो जाता है। आमतौर पर, गंभीर हाइपर- के परिणामस्वरूप सोडियम का स्तर गलत तरीके से कम हो सकता है।
ट्राइग्लिसराइडिमिया। स्तर पोटैशियमसीरम स्तर शुरू में बाह्य कोशिकीय स्थानों से इसकी गति के कारण बढ़ सकता है।
क्रमानुसार रोग का निदान
मधुमेह के रोगियों में चेतना की हानि के अन्य कारण। हाइपरोस्मोलर कोमा के साथ विभेदक निदान, एक नियम के रूप में, कठिनाइयों का कारण नहीं बनता है (T2DM वाले बुजुर्ग रोगियों में विकसित होता है) और इसका अधिक नैदानिक महत्व नहीं है, क्योंकि दोनों स्थितियों के उपचार सिद्धांत समान हैं। यदि मधुमेह के रोगी में चेतना के नुकसान का कारण तुरंत निर्धारित करना असंभव है, तो उसे ग्लूकोज देने की सलाह दी जाती है, क्योंकि हाइपोग्लाइसेमिक स्थितियां बहुत अधिक सामान्य हैं, और ग्लूकोज प्रशासन की पृष्ठभूमि के खिलाफ तेजी से सकारात्मक गतिशीलता चेतना के नुकसान के कारण का पता लगाना संभव बनाती है।
इलाज
डीकेए के उपचार में पुनर्जलीकरण, हाइपरग्लेसेमिया का सुधार, इलेक्ट्रोलाइट विकार, साथ ही उन बीमारियों का उपचार शामिल है जो मधुमेह के विघटन का कारण बने हैं। किसी विशेष चिकित्सा संस्थान की गहन देखभाल इकाई में उपचार सबसे बेहतर तरीके से किया जाता है। गंभीर सहवर्ती हृदय रोगविज्ञान के बिना वयस्क रोगियों में, यहां तक कि प्रीहॉस्पिटल चरण में भी पहली प्राथमिकता वाले उपाय के रूप में पुनर्जलीकरणलगभग एक लीटर प्रति घंटे (लगभग 15-20 मिलीलीटर प्रति किलोग्राम शरीर के वजन प्रति घंटे) की दर से एक आइसोटोनिक समाधान (0.9% NaCl) देने की सिफारिश की जाती है। तरल पदार्थ की कमी का पूरा मुआवजा, जो डीकेए में 100-200 मिलीलीटर प्रति किलोग्राम वजन है, उपचार के पहले दिन के भीतर प्राप्त किया जाना चाहिए। सहवर्ती हृदय या गुर्दे की विफलता के मामले में, समय की इस अवधि को बढ़ाया जाना चाहिए। बच्चों के लिए, पुनर्जलीकरण चिकित्सा के लिए आइसोटोनिक समाधान की अनुशंसित मात्रा प्रति घंटे शरीर के वजन के प्रति किलोग्राम 10-20 मिलीलीटर है, जबकि पहले 4 घंटों में यह शरीर के वजन के प्रति किलोग्राम 50 मिलीलीटर से अधिक नहीं होनी चाहिए। लगभग 48 घंटों के बाद पूर्ण पुनर्जलीकरण प्राप्त करने की अनुशंसा की जाती है। समानांतर इंसुलिन थेरेपी की पृष्ठभूमि के मुकाबले ग्लाइसेमिया का स्तर लगभग 14 mmol/l तक कम हो जाने के बाद, वे 10% ग्लूकोज समाधान के आधान पर स्विच करते हैं, जो पुनर्जलीकरण जारी रखता है।
"छोटी खुराक" की अवधारणा वर्तमान में स्वीकार की गई है इंसुलिनडीकेए के उपचार में. केवल लघु-अभिनय इंसुलिन का उपयोग किया जाता है। अंतःशिरा इंसुलिन का सबसे इष्टतम उपयोग है
लीना. इंसुलिन का इंट्रामस्क्युलर प्रशासन, जो कम प्रभावी है, केवल डीकेए की मध्यम गंभीरता के साथ, स्थिर हेमोडायनामिक्स के साथ और जब अंतःशिरा चिकित्सा संभव नहीं है, संभव है। बाद के मामले में, इंजेक्शन रेक्टस एब्डोमिनिस मांसपेशी में लगाए जाते हैं, जबकि एक इंट्रामस्क्युलर इंजेक्शन सुई को इंसुलिन सिरिंज (विश्वसनीय इंट्रामस्क्युलर इंजेक्शन के लिए) पर रखा जाता है, और इस सुई का उपयोग करके इंसुलिन को शीशी से सिरिंज में खींचा जाता है।
अंतःशिरा इंसुलिन प्रशासन के लिए कई विकल्प हैं। सबसे पहले, इंसुलिन को जलसेक प्रणाली के "रबर बैंड में" इंजेक्ट किया जा सकता है, जबकि इंसुलिन की आवश्यक मात्रा को इंसुलिन सिरिंज में खींचा जाता है, जिसके बाद इसमें 1 मिलीलीटर आइसोटोनिक समाधान जोड़ा जाता है। जब तक ग्लाइसेमिक स्तर 14 mmol/l तक नहीं पहुंच जाता, तब तक रोगी को हर घंटे 6-10 यूनिट लघु-अभिनय इंसुलिन दिया जाता है; आगे (आइसोटोनिक से 10% ग्लूकोज तक पुनर्जलीकरण समाधान को बदलने के समानांतर)प्रति घंटा निर्धारित ग्लाइसेमिक संकेतकों के आधार पर, इंसुलिन की खुराक प्रति घंटे 4-8 यूनिट तक कम हो जाती है। ग्लाइसेमिक स्तर में कमी की अनुशंसित दर 5 mmol/l प्रति घंटे से अधिक नहीं होनी चाहिए। अंतःशिरा इंसुलिन थेरेपी के एक अन्य विकल्प में परफ्यूज़र का उपयोग शामिल है। परफ्यूज़र के लिए एक समाधान तैयार करने के लिए, निम्नलिखित अनुपात का उपयोग किया जाता है: लघु-अभिनय इंसुलिन के 50 यू में, मानव एल्ब्यूमिन के 20% समाधान के 2 मिलीलीटर को जोड़ा जाता है, जिसके बाद 0.9% आइसोटोनिक समाधान के 50 मिलीग्राम को जोड़ा जाता है। यदि इंसुलिन प्रशासन के इंट्रामस्क्युलर मार्ग को चुना जाता है, तो शुरू में लघु-अभिनय इंसुलिन की 20 इकाइयां प्रशासित की जाती हैं, इसके बाद प्रति घंटे 6 इकाइयां दी जाती हैं, और ग्लाइसेमिक स्तर 14 मिमीओल / एल तक पहुंचने के बाद, खुराक प्रति घंटे 4 इकाइयों तक कम हो जाती है। हेमोडायनामिक्स के पूर्ण स्थिरीकरण और एसिड-बेस विकारों के मुआवजे के बाद, रोगी को चमड़े के नीचे इंसुलिन इंजेक्शन में स्थानांतरित किया जाता है।
जैसा कि संकेत दिया गया है, महत्वपूर्ण होने के बावजूद पोटेशियम की कमीशरीर में (कुल हानि 3-6 mmol/kg), DKA के साथ इंसुलिन थेरेपी शुरू होने से पहले इसका स्तर थोड़ा बढ़ सकता है। हालाँकि, यदि प्लाज्मा पोटेशियम का स्तर 5.5 mmol/L से कम है, तो इंसुलिन थेरेपी शुरू करने के साथ ही पोटेशियम क्लोराइड समाधान का आधान शुरू करने की सिफारिश की जाती है। पोटेशियम की कमी का सफल सुधार पीएच के सामान्यीकरण की पृष्ठभूमि के खिलाफ ही होता है। कम पीएच पर, कोशिका में पोटेशियम का प्रवाह काफी कम हो जाता है; इसलिए, यदि संभव हो, तो ट्रांसफ़्यूज़ किए गए पोटेशियम क्लोराइड की खुराक को एक विशिष्ट पीएच मान (तालिका 7.13) के अनुसार अनुकूलित करने की सलाह दी जाती है।
मेज़ 7.13.पोटेशियम की कमी सुधार योजना
 * गणना के लिए निम्नलिखित डेटा का उपयोग किया जाता है:
* गणना के लिए निम्नलिखित डेटा का उपयोग किया जाता है:
1 ग्राम KCl = 13.4 mmol; 1 mmol KCl = 0.075 ग्राम। KS1 के 4% घोल में: 100 मिली में - KS1 का 4 ग्राम, 25 मिली में - KS1 का 1 ग्राम, 10 मिली में KS1 का 0.4 ग्राम।
मधुमेह विघटन अक्सर किसके कारण होता है? संक्रामक रोग(पायलोनेफ्राइटिस, डायबिटिक फुट सिंड्रोम में संक्रमित अल्सर, निमोनिया, साइनसाइटिस, आदि)। एक नियम है जिसके अनुसार, डीकेए के मामले में, निम्न-श्रेणी के बुखार या बुखार वाले लगभग सभी रोगियों को एंटीबायोटिक चिकित्सा निर्धारित की जाती है, यहां तक कि संक्रमण के दृश्य स्रोत की अनुपस्थिति में भी, क्योंकि शरीर के तापमान में वृद्धि सामान्य नहीं है। डीकेए.
पूर्वानुमान
डीकेए के लिए मृत्यु दर 0.5-5% है, ज्यादातर मामले देर से और अयोग्य चिकित्सा देखभाल के कारण होते हैं। बुजुर्ग रोगियों में मृत्यु दर सबसे अधिक (50% तक) है।
7.7.2. हाइपरोस्मोलर कोमा
हाइपरोस्मोलर कोमा(जीओसी) टी2डीएम की एक दुर्लभ तीव्र जटिलता है, जो उच्च मृत्यु दर (तालिका 7.14) के साथ पूर्ण इंसुलिन की कमी के अभाव में गंभीर निर्जलीकरण और हाइपरग्लेसेमिया के परिणामस्वरूप विकसित होती है।
एटियलजि
GOC आमतौर पर T2DM वाले वृद्ध रोगियों में विकसित होता है। ऐसे मरीज अक्सर अकेले होते हैं, बिना देखभाल के रहते हैं, अपनी स्थिति और आत्म-नियंत्रण की उपेक्षा करते हैं और अपर्याप्त तरल पदार्थ लेते हैं। अक्सर विघटन संक्रमण (मधुमेह पैर सिंड्रोम, निमोनिया, तीव्र पायलोनेफ्राइटिस), मस्तिष्क विकारों के कारण होता है
रक्त परिसंचरण और अन्य स्थितियाँ, जिसके परिणामस्वरूप मरीज़ खराब तरीके से चलते हैं, ग्लूकोज कम करने वाली दवाएं और तरल पदार्थ नहीं लेते हैं।
मेज़ 7.14.हाइपरोस्मोलर कोमा (HOC)
 रोगजनन
रोगजनन
हाइपरग्लेसेमिया और ऑस्मोटिक ड्यूरेसिस बढ़ने से गंभीर निर्जलीकरण होता है, जो उपरोक्त कारणों से, बाहर से पूरा नहीं होता है। हाइपरग्लेसेमिया और निर्जलीकरण का परिणाम प्लाज्मा हाइपरोस्मोलैरिटी है। जीओसी के रोगजनन का एक अभिन्न घटक इंसुलिन की सापेक्ष कमी और गर्भनिरोधक हार्मोन की अधिकता है; हालांकि, टी2डीएम में बना रहने वाला अवशिष्ट इंसुलिन स्राव लिपोलिसिस और केटोजेनेसिस को दबाने के लिए पर्याप्त है, जिसके परिणामस्वरूप कीटोएसिडोसिस का विकास नहीं होता है। घटित होना।
कुछ मामलों में, ऊतक हाइपोपरफ्यूजन की पृष्ठभूमि के खिलाफ हाइपरलैक्टेटेमिया के परिणामस्वरूप मध्यम एसिडोसिस का पता लगाया जा सकता है। गंभीर हाइपरग्लेसेमिया के साथ, मस्तिष्कमेरु द्रव में आसमाटिक संतुलन बनाए रखने के लिए, मस्तिष्क कोशिकाओं से आने वाली सोडियम सामग्री बढ़ जाती है, जहां बदले में पोटेशियम प्रवेश करता है। तंत्रिका कोशिकाओं की ट्रांसमेम्ब्रेन क्षमता बाधित हो जाती है। प्रगतिशील मूर्खता ऐंठन सिंड्रोम के साथ संयोजन में विकसित होती है (चित्र 7.10)।
महामारी विज्ञान
टी2डीएम वाले वयस्कों और बुजुर्ग रोगियों में जीओसी 10-30% तीव्र हाइपरग्लाइसेमिक स्थितियों के लिए जिम्मेदार है। लगभग 2/3 मामलों में, जीओसी पहले से अज्ञात मधुमेह वाले व्यक्तियों में विकसित होता है।
नैदानिक अभिव्यक्तियाँ
हाइपरोस्मोलर कोमा की नैदानिक तस्वीर की विशेषताएं हैं:
निर्जलीकरण और हाइपोपरफ्यूजन के संकेतों और जटिलताओं का एक सेट: प्यास, शुष्क श्लेष्मा झिल्ली, टैचीकार्डिया, धमनी हाइपोटेंशन, मतली, कमजोरी, सदमा;
फोकल और सामान्यीकृत दौरे;
बुखार, मतली और उल्टी (40-65% मामले);
सहवर्ती रोगों और जटिलताओं में अक्सर गहरी शिरा घनास्त्रता, निमोनिया, सेरेब्रोवास्कुलर दुर्घटनाएं और गैस्ट्रोपेरेसिस शामिल हैं।
निदान
नैदानिक तस्वीर के आधार पर, रोगी की उम्र और टाइप 2 मधुमेह का इतिहास, केटोनुरिया और केटोएसिडोसिस की अनुपस्थिति में गंभीर हाइपरग्लेसेमिया। जीओसी के विशिष्ट प्रयोगशाला संकेत तालिका में प्रस्तुत किए गए हैं। 7.12.
 चावल। 7 .10.
हाइपरोस्मोलर कोमा का रोगजनन
चावल। 7 .10.
हाइपरोस्मोलर कोमा का रोगजनन
क्रमानुसार रोग का निदान
मधुमेह के रोगियों में विकसित होने वाली अन्य तीव्र स्थितियाँ, अक्सर सहवर्ती विकृति के साथ, मधुमेह के गंभीर विघटन की ओर ले जाती हैं।
इलाज
जीओसी के लिए उपचार और निगरानी, कुछ विशेषताओं के अपवाद के साथ, कीटोएसिडोटिक डायबिटिक कोमा (धारा 7.7.1) के लिए वर्णित उपचारों से भिन्न नहीं है:
प्रारंभिक पुनर्जलीकरण की बड़ी मात्रा 1.5-2 लीटर प्रति 1 घंटा; 1 एल - दूसरे और तीसरे घंटे में, फिर 500 मिलीलीटर/घंटा आइसोटोनिक सोडियम क्लोराइड समाधान;
पोटेशियम युक्त समाधानों के प्रशासन की आवश्यकता, एक नियम के रूप में, कीटोएसिडोटिक कोमा की तुलना में अधिक है;
इंसुलिन थेरेपी सीसी के समान है, लेकिन इंसुलिन की आवश्यकता कम होती है और सेरेब्रल एडिमा के विकास से बचने के लिए ग्लाइसेमिक स्तर को 5 mmol/l प्रति घंटे से अधिक तेजी से कम नहीं किया जाना चाहिए;
हाइपोटोनिक समाधान (NaCl 0.45%) के प्रशासन से बचना सबसे अच्छा है (केवल गंभीर हाइपरनाट्रेमिया के साथ: > 155 mmol/L और/या प्रभावी ऑस्मोलैरिटी > 320 mOsm/L);
बाइकार्बोनेट देने की कोई आवश्यकता नहीं है (केवल पीएच के साथ एसिडोसिस के लिए विशेष गहन देखभाल इकाइयों में)।< 7,1).
पूर्वानुमान
जीओसी के साथ मृत्यु दर अधिक है और 15-60% के बीच है। गंभीर सहवर्ती विकृति वाले बुजुर्ग रोगियों में सबसे खराब पूर्वानुमान है, जो अक्सर मधुमेह के विघटन और जीओसी के विकास का कारण होता है।
7.7.3. हाइपोग्लाइसीमिया
हाइपोग्लाइसीमिया- सीरम ग्लूकोज स्तर में कमी (<2,2- 2,8 ммоль/л), сопровождающее клинический синдром, характеризующийся признаками активации симпатической нервной системы и/или дисфункцией центральной нервной системы. Гипогликемия как лабораторный феномен не тождественен понятию «гипогликемическая симптоматика», поскольку лабораторные данные и клиническая картина не всегда совпадают.
एटियलजि
इंसुलिन और इसके एनालॉग्स, साथ ही सल्फोनीलुरिया की अधिक मात्रा;
अपरिवर्तित ग्लूकोज-कम करने वाली चिकित्सा की पृष्ठभूमि के खिलाफ अपर्याप्त भोजन का सेवन;
मादक पेय पीना;
निरंतर ग्लूकोज-कम करने वाली चिकित्सा की पृष्ठभूमि के खिलाफ और/या कार्बोहाइड्रेट के अतिरिक्त सेवन के बिना शारीरिक गतिविधि;
मधुमेह की देर से जटिलताओं का विकास (गैस्ट्रोपैसिस, गुर्दे की विफलता के साथ स्वायत्त न्यूरोपैथी) और कई अन्य बीमारियों (अधिवृक्क अपर्याप्तता, हाइपोथायरायडिज्म, यकृत विफलता, घातक ट्यूमर) अपरिवर्तित ग्लूकोज-कम करने वाली थेरेपी (पृष्ठभूमि के खिलाफ टीएसपी लेने और संचय की निरंतरता) के साथ गुर्दे की विफलता के कारण, इंसुलिन की समान खुराक बनाए रखना);
इंसुलिन प्रशासन तकनीक का उल्लंघन (चमड़े के नीचे के बजाय इंट्रामस्क्युलर इंजेक्शन);
कृत्रिम हाइपोग्लाइसीमिया (रोगी द्वारा स्वयं ग्लूकोज कम करने वाली दवाओं का जानबूझकर ओवरडोज़);
कार्बनिक हाइपरिन्सुलिनिज्म - इंसुलिनोमा (पैराग्राफ 10.3 देखें)।
रोगजनन
हाइपोग्लाइसीमिया का रोगजनन रक्त में ग्लूकोज के प्रवेश, उसके उपयोग, इंसुलिन के स्तर और काउंटर-इंसुलर हार्मोन के बीच असंतुलन है। आम तौर पर, 4.2-4.7 mmol/l की सीमा में ग्लाइसेमिक स्तर पर, β-कोशिकाओं से इंसुलिन का उत्पादन और रिलीज दबा दिया जाता है। 3.9 mmol/l से नीचे ग्लाइसेमिक स्तर में कमी के साथ-साथ काउंटर-इंसुलर हार्मोन (ग्लूकागन, कोर्टिसोल, ग्रोथ हार्मोन, एड्रेनालाईन) के उत्पादन में उत्तेजना होती है। न्यूरोग्लाइकोपेनिक लक्षण तब विकसित होते हैं जब ग्लाइसेमिक स्तर 2.5-2.8 mmol/l से कम हो जाता है। ओवरडोज़ के मामले में इंसुलिनऔर/या दवाएं सल्फोनिलयूरियाहाइपोग्लाइसीमिया किसी बहिर्जात या अंतर्जात हार्मोन के प्रत्यक्ष हाइपोग्लाइसेमिक प्रभाव के कारण विकसित होता है। सल्फोनील्यूरिया दवाओं की अधिक मात्रा के मामले में, हमले के रुकने के बाद हाइपोग्लाइसेमिक लक्षण कई बार दोबारा हो सकते हैं, इस तथ्य के कारण कि कुछ दवाओं की कार्रवाई की अवधि एक दिन या उससे अधिक तक पहुंच सकती है। टीएसपी जिनका इंसुलिन उत्पादन (मेटफोर्मिन, थियाजोलिडाइनायड्स) पर उत्तेजक प्रभाव नहीं पड़ता है, वे अपने आप हाइपोग्लाइसीमिया का कारण नहीं बन सकते हैं, लेकिन जब उन्हें सल्फोनीलुरिया या इंसुलिन में जोड़ा जाता है, तो उसी खुराक में बाद वाले को लेने से हाइपोग्लाइसेमिक के संचय के कारण हाइपोग्लाइसीमिया हो सकता है। संयोजन चिकित्सा का प्रभाव (तालिका 7.15)।
मेज़ 7.15.हाइपोग्लाइसीमिया
 तालिका का अंत. 7.15
तालिका का अंत. 7.15
 प्रवेश पर शराबयकृत में ग्लूकोनियोजेनेसिस दबा हुआ है, जो हाइपोग्लाइसीमिया का प्रतिकार करने वाला सबसे महत्वपूर्ण कारक है। शारीरिक व्यायामग्लूकोज के इंसुलिन-स्वतंत्र उपयोग को बढ़ावा देना, जिसके कारण, अपरिवर्तित ग्लूकोज-कम करने वाली चिकित्सा की पृष्ठभूमि के खिलाफ और/या अतिरिक्त कार्बोहाइड्रेट सेवन की अनुपस्थिति में, वे हाइपोग्लाइसीमिया का कारण बन सकते हैं।
प्रवेश पर शराबयकृत में ग्लूकोनियोजेनेसिस दबा हुआ है, जो हाइपोग्लाइसीमिया का प्रतिकार करने वाला सबसे महत्वपूर्ण कारक है। शारीरिक व्यायामग्लूकोज के इंसुलिन-स्वतंत्र उपयोग को बढ़ावा देना, जिसके कारण, अपरिवर्तित ग्लूकोज-कम करने वाली चिकित्सा की पृष्ठभूमि के खिलाफ और/या अतिरिक्त कार्बोहाइड्रेट सेवन की अनुपस्थिति में, वे हाइपोग्लाइसीमिया का कारण बन सकते हैं।
महामारी विज्ञान
गहन इंसुलिन थेरेपी प्राप्त करने वाले टाइप 1 मधुमेह वाले रोगियों में हल्का, शीघ्र प्रतिवर्ती हाइपोग्लाइसीमिया सप्ताह में कई बार हो सकता है और अपेक्षाकृत हानिरहित है। गहन इंसुलिन थेरेपी लेने वाले प्रत्येक रोगी के लिए, प्रति वर्ष गंभीर हाइपोग्लाइसीमिया का 1 मामला होता है। ज्यादातर मामलों में, हाइपोग्लाइसीमिया रात में विकसित होता है। टाइप 2 मधुमेह में, इंसुलिन प्राप्त करने वाले 20% रोगियों और सल्फोनीलुरिया प्राप्त करने वाले 6% रोगियों में 10 वर्षों में गंभीर हाइपोग्लाइसीमिया का कम से कम एक प्रकरण विकसित होता है।
नैदानिक अभिव्यक्तियाँ
लक्षणों के दो मुख्य समूह हैं: एड्रीनर्जिक, सहानुभूति तंत्रिका तंत्र के सक्रियण और अधिवृक्क ग्रंथियों द्वारा एड्रेनालाईन की रिहाई से जुड़ा हुआ है, और न्यूरोग्लाइकोपेनिक, इसके मुख्य ऊर्जा सब्सट्रेट की कमी की पृष्ठभूमि के खिलाफ केंद्रीय तंत्रिका तंत्र की शिथिलता से जुड़ा हुआ है। . को एड्रीनर्जिकलक्षणों में शामिल हैं: टैचीकार्डिया, मायड्रायसिस; चिंता, आक्रामकता; कांपना, ठंडा पसीना, पेरेस्टेसिया; मतली, गंभीर भूख, अत्यधिक लार; दस्त, अत्यधिक पेशाब आना। को न्यूरोग्लाइकोपेनिकलक्षणों में अस्थेनिया शामिल है,
एकाग्रता में कमी, सिरदर्द, भय, भ्रम, भटकाव, मतिभ्रम; भाषण, दृश्य, व्यवहार संबंधी विकार, भूलने की बीमारी, बिगड़ा हुआ चेतना, आक्षेप, क्षणिक पक्षाघात, कोमा। हाइपोग्लाइसीमिया अधिक गंभीर हो जाने पर लक्षणों की गंभीरता और अनुक्रम के बीच कोई स्पष्ट संबंध नहीं हो सकता है। केवल एड्रीनर्जिक या केवल न्यूरोग्लाइकोनिक लक्षण हो सकते हैं। कुछ मामलों में, नॉर्मोग्लाइसीमिया की बहाली और चल रही चिकित्सा के बावजूद, मरीज़ कई घंटों या यहां तक कि दिनों तक बेहोश या बेहोशी की स्थिति में रह सकते हैं। लंबे समय तक हाइपोग्लाइसीमिया या इसके बार-बार होने वाले एपिसोड से केंद्रीय तंत्रिका तंत्र (मुख्य रूप से सेरेब्रल कॉर्टेक्स में) में अपरिवर्तनीय परिवर्तन हो सकते हैं, जिनकी अभिव्यक्तियाँ प्रलाप और मतिभ्रम-पागल एपिसोड से लेकर विशिष्ट मिर्गी के दौरे तक काफी भिन्न होती हैं, जिसका अपरिहार्य परिणाम लगातार मनोभ्रंश है। .
हाइपरग्लेसेमिया को हल्के हाइपोग्लाइसीमिया के एपिसोड की तुलना में रोगियों द्वारा अधिक आसानी से सहन किया जाता है। इसलिए, कई मरीज़, हाइपोग्लाइसीमिया के डर के कारण, ग्लाइसेमिया को अपेक्षाकृत उच्च स्तर पर बनाए रखना आवश्यक मानते हैं, जो वास्तव में रोग के विघटन से मेल खाता है। इस रूढ़िवादिता पर काबू पाने के लिए कभी-कभी डॉक्टरों और प्रशिक्षण कर्मचारियों को काफी प्रयास की आवश्यकता होती है।
निदान
प्रयोगशाला में (आमतौर पर ग्लूकोमीटर का उपयोग करके) निम्न रक्त शर्करा के स्तर का पता लगाने के साथ मधुमेह के रोगी में हाइपोग्लाइसीमिया की नैदानिक तस्वीर।
क्रमानुसार रोग का निदान
चेतना की हानि के अन्य कारण। यदि मधुमेह के रोगी की चेतना के नुकसान का कारण अज्ञात है और ग्लाइसेमिक स्तर का तेजी से विश्लेषण करना असंभव है, तो ग्लूकोज प्रशासन का संकेत दिया जाता है। मधुमेह के रोगियों में बार-बार होने वाले हाइपोग्लाइसीमिया के विकास का कारण निर्धारित करने की अक्सर आवश्यकता होती है। अक्सर ये अपर्याप्त ग्लूकोज-कम करने वाली चिकित्सा और रोगी के अपने रोग के बारे में ज्ञान के निम्न स्तर का परिणाम होते हैं। यह याद रखना चाहिए कि घातक ट्यूमर सहित कई बीमारियाँ (अधिवृक्क अपर्याप्तता, हाइपोथायरायडिज्म, गुर्दे और यकृत की विफलता), ग्लूकोज कम करने वाली चिकित्सा की आवश्यकता में कमी ला सकती है, इसके पूर्ण उन्मूलन तक ("गायब मधुमेह") .
इलाज
हल्के हाइपोग्लाइसीमिया का इलाज करने के लिए, जिसमें रोगी सचेत है और खुद की मदद कर सकता है, आमतौर पर 1-2 ब्रेड यूनिट (10-20 ग्राम ग्लूकोज) की मात्रा में कार्बोहाइड्रेट युक्त भोजन या तरल पदार्थ लेना पर्याप्त होता है। यह मात्रा, उदाहरण के लिए, 200 मिलीलीटर मीठे फलों के रस में निहित होती है। पेय हाइपोग्लाइसीमिया से अधिक प्रभावी ढंग से राहत देते हैं, क्योंकि तरल रूप में ग्लूकोज बहुत तेजी से अवशोषित होता है। यदि लगातार कार्बोहाइड्रेट सेवन के बावजूद लक्षण बिगड़ते रहें, तो अंतःशिरा ग्लूकोज या इंट्रामस्क्युलर ग्लूकागन आवश्यक है। चेतना की हानि के साथ होने वाले गंभीर हाइपोग्लाइसीमिया का इलाज इसी तरह किया जाता है। इस मामले में, रोगी को लगभग 50 मिलीलीटर दिया जाता है 40% ग्लूकोज समाधान अंतःशिरा द्वारा।ग्लूकोज का प्रशासन तब तक जारी रखा जाना चाहिए जब तक कि हमला बंद न हो जाए और ग्लाइसेमिया सामान्य न हो जाए, हालांकि एक नियम के रूप में, बड़ी खुराक - 100 मिलीलीटर या उससे अधिक की आवश्यकता नहीं होती है। ग्लूकागनप्रशासित किया जाता है (आमतौर पर फैक्ट्री-तैयार भरी हुई सिरिंज के साथ) इंट्रामस्क्युलर या चमड़े के नीचे। कुछ मिनटों के बाद, ग्लूकागन द्वारा ग्लाइकोजेनोलिसिस को प्रेरित करने के कारण ग्लाइसेमिक स्तर सामान्य हो जाता है। हालाँकि, ऐसा हमेशा नहीं होता है: जब रक्त में इंसुलिन का स्तर अधिक होता है, तो ग्लूकागन अप्रभावी होता है। ग्लूकागन का आधा जीवन इंसुलिन की तुलना में कम होता है। शराब और यकृत रोग में, ग्लाइकोजन संश्लेषण ख़राब हो जाता है, और ग्लूकागन प्रशासन अप्रभावी हो सकता है। ग्लूकागन प्रशासन का एक दुष्प्रभाव उल्टी हो सकता है, जिससे आकांक्षा का खतरा पैदा हो सकता है। रोगी के रिश्तेदारों को ग्लूकागन इंजेक्शन की तकनीक में महारत हासिल करने की सलाह दी जाती है।
पूर्वानुमान
रोग की अच्छी क्षतिपूर्ति की पृष्ठभूमि में प्रशिक्षित रोगियों में हल्का हाइपोग्लाइसीमिया सुरक्षित है। बार-बार हाइपोग्लाइसीमिया मधुमेह की खराब क्षतिपूर्ति का संकेत है; ज्यादातर मामलों में, ऐसे रोगियों में दिन के बाकी समय में कम या ज्यादा गंभीर हाइपरग्लेसेमिया और ग्लाइकेटेड हीमोग्लोबिन का उच्च स्तर होता है। मधुमेह की देर से जटिलताओं वाले बुजुर्ग रोगियों में, हाइपोग्लाइसीमिया संवहनी जटिलताओं जैसे मायोकार्डियल रोधगलन, स्ट्रोक और रेटिना रक्तस्राव को भड़का सकता है। एक नियम के रूप में, पर्याप्त उपचार और चेतना की तीव्र वापसी के साथ हाइपोग्लाइसेमिक कोमा 30 मिनट तक रहता है, इसमें कोई जटिलता या परिणाम नहीं होता है।
7.8. मधुमेह मेलिटस की देर से होने वाली जटिलताएँ
दोनों प्रकार के मधुमेह में देर से जटिलताएँ विकसित होती हैं। चिकित्सकीय रूप से, मधुमेह की पाँच मुख्य देर से होने वाली जटिलताएँ हैं: मैक्रोएंगियोपैथी, नेफ्रोपैथी, रेटिनोपैथी, न्यूरोपैथी और डायबिटिक फ़ुट सिंड्रोम। कुछ प्रकार के मधुमेह के लिए देर से होने वाली जटिलताओं की गैर-विशिष्टता इस तथ्य से निर्धारित होती है कि उनका मुख्य रोगजनक लिंक क्रोनिक हाइपरग्लेसेमिया है। इस संबंध में, टी1डीएम की अभिव्यक्ति के समय, रोगियों में देर से जटिलताएं लगभग कभी नहीं होती हैं, जो चिकित्सा की प्रभावशीलता के आधार पर वर्षों और दशकों में विकसित होती हैं। एक नियम के रूप में, T1DM के लिए सबसे बड़ा नैदानिक महत्व है मधुमेह माइक्रोएन्जियोपैथी(नेफ्रोपैथी, रेटिनोपैथी) और न्यूरोपैथी (मधुमेह पैर सिंड्रोम)। इसके विपरीत, T2DM के साथ, देर से आने वाली जटिलताओं का अक्सर निदान के समय ही पता चल जाता है। सबसे पहले, यह इस तथ्य के कारण है कि T2DM निदान होने से बहुत पहले ही प्रकट हो जाता है। दूसरे, एथेरोस्क्लेरोसिस, जो चिकित्सकीय रूप से मैक्रोएंगियोपैथी द्वारा प्रकट होता है, में मधुमेह के साथ कई रोगजन्य संबंध हैं। T2DM में, सबसे बड़ा नैदानिक महत्व, एक नियम के रूप में, मधुमेह द्वारा प्राप्त किया जाता है मैक्रोएंगियोपैथी,जो निदान के समय अधिकांश रोगियों में पाया जाता है। प्रत्येक विशिष्ट मामले में, व्यक्तिगत देर से जटिलताओं का सेट और गंभीरता, बीमारी की महत्वपूर्ण अवधि के बावजूद, उनकी विरोधाभासी पूर्ण अनुपस्थिति से लेकर गंभीर रूप में सभी संभावित विकल्पों के संयोजन तक भिन्न होती है।
देर से जटिलताएँ हैं मौत का मुख्य कारणमधुमेह के रोगी, और इसकी व्यापकता को ध्यान में रखते हुए, यह अधिकांश देशों में सबसे महत्वपूर्ण चिकित्सा और सामाजिक स्वास्थ्य समस्या है। इसकी वजह उपचार का मुख्य लक्ष्यऔर मधुमेह के रोगियों का अवलोकन इसकी देर से होने वाली जटिलताओं की रोकथाम (प्राथमिक, माध्यमिक, तृतीयक) है।
7.8.1. मधुमेह मैक्रोएंगियोपैथी
मधुमेह मैक्रोएंगियोपैथी- एक सामूहिक अवधारणा जो मधुमेह में बड़ी धमनियों के एथेरोस्क्लोरोटिक घावों को एकजुट करती है,
नैदानिक रूप से कोरोनरी हृदय रोग (सीएचडी) द्वारा प्रकट, मस्तिष्क, निचले छोरों, आंतरिक अंगों और धमनी उच्च रक्तचाप (तालिका 7.16) के जहाजों के एथेरोस्क्लेरोसिस को नष्ट कर देता है।
मेज़ 7.16.मधुमेह मैक्रोएंगियोपैथी
 एटियलजि और रोगजनन
एटियलजि और रोगजनन
संभवतः मधुमेह रहित व्यक्तियों में एथेरोस्क्लेरोसिस के एटियलजि और रोगजनन के समान। मधुमेह वाले और मधुमेह रहित व्यक्तियों में एथेरोस्क्लोरोटिक सजीले टुकड़े सूक्ष्म संरचना में भिन्न नहीं होते हैं। हालाँकि, मधुमेह में, अतिरिक्त जोखिम कारक सामने आ सकते हैं, या मधुमेह ज्ञात गैर-विशिष्ट कारकों को बढ़ा सकता है। मधुमेह के लिए इनमें शामिल हैं:
1. हाइपरग्लेसेमिया।यह एथेरोस्क्लेरोसिस के विकास के लिए एक जोखिम कारक है। T2DM वाले रोगियों में HbA1c के स्तर में 1% की वृद्धि होती है
मायोकार्डियल रोधगलन विकसित होने का 15% जोखिम है। हाइपरग्लेसेमिया के एथेरोजेनिक प्रभाव का तंत्र पूरी तरह से स्पष्ट नहीं है; शायद यह एलडीएल चयापचय के अंतिम उत्पादों और संवहनी दीवार के कोलेजन के ग्लाइकोसिलेशन से जुड़ा हुआ है।
2. धमनी का उच्च रक्तचाप(एजी). रोगजनन में, गुर्दे के घटक को बहुत महत्व दिया जाता है (मधुमेह अपवृक्कता)।टाइप 2 मधुमेह में उच्च रक्तचाप दिल के दौरे और स्ट्रोक के लिए हाइपरग्लेसेमिया से कम महत्वपूर्ण जोखिम कारक नहीं है।
3. डिस्लिपिडेमिया।हाइपरइंसुलिनमिया, जो टाइप 2 मधुमेह में इंसुलिन प्रतिरोध का एक अभिन्न घटक है, एचडीएल स्तर में कमी, ट्राइग्लिसराइड स्तर में वृद्धि और घनत्व में कमी का कारण बनता है, अर्थात। एलडीएल की एथेरोजेनेसिस में वृद्धि।
4. मोटापा,टी2डीएम वाले अधिकांश रोगी इससे पीड़ित होते हैं, जो एथेरोस्क्लेरोसिस, मायोकार्डियल रोधगलन और स्ट्रोक के लिए एक स्वतंत्र जोखिम कारक है (धारा 11.2 देखें)।
5. इंसुलिन प्रतिरोध।हाइपरइंसुलिनिमिया और इंसुलिन-प्रोइन्सुलिन जैसे अणुओं के उच्च स्तर से एथेरोस्क्लेरोसिस विकसित होने का खतरा बढ़ जाता है, जो एंडोथेलियल डिसफंक्शन से जुड़ा हो सकता है।
6. रक्त जमाव विकार.मधुमेह में, फाइब्रिनोजेन, प्लेटलेट इनहिबिटर एक्टिवेटर और वॉन विलेब्रांड कारक के स्तर में वृद्धि निर्धारित की जाती है, जिसके परिणामस्वरूप रक्त जमावट प्रणाली की प्रोथ्रोम्बोटिक अवस्था का निर्माण होता है।
7. एंडोथेलियल डिसफंक्शन,प्लास्मिनोजेन इनहिबिटर एक्टिवेटर और सेल आसंजन अणुओं की बढ़ी हुई अभिव्यक्ति की विशेषता।
8. ऑक्सीडेटिव तनाव,जिससे ऑक्सीकृत एलडीएल और एफ2-आइसोप्रोस्टेन की सांद्रता में वृद्धि हुई।
9. प्रणालीगत सूजनजिसमें फाइब्रिनोजेन और सी-रिएक्टिव प्रोटीन की अभिव्यक्ति में वृद्धि होती है।
टाइप 2 मधुमेह में कोरोनरी धमनी रोग के विकास के लिए सबसे महत्वपूर्ण जोखिम कारक एलडीएल स्तर में वृद्धि, एचडीएल स्तर में कमी, धमनी उच्च रक्तचाप, हाइपरग्लेसेमिया और धूम्रपान हैं। मधुमेह में एथेरोस्क्लोरोटिक प्रक्रिया के बीच एक अंतर इसका अधिक व्यापक होना है पश्चकपाल घाव की दूरस्थ प्रकृति,वे। इस प्रक्रिया में अक्सर अपेक्षाकृत छोटी धमनियां शामिल होती हैं, जो सर्जिकल उपचार को जटिल बनाती हैं और रोग का पूर्वानुमान खराब कर देती हैं।
महामारी विज्ञान
टाइप 2 मधुमेह वाले लोगों में कोरोनरी हृदय रोग विकसित होने का जोखिम बिना मधुमेह वाले लोगों की तुलना में 6 गुना अधिक है, जबकि पुरुषों और महिलाओं के लिए यह समान है। टाइप 1 मधुमेह वाले 20% रोगियों में और टाइप 2 मधुमेह वाले 75% रोगियों में धमनी उच्च रक्तचाप पाया जाता है। सामान्य तौर पर, मधुमेह के रोगियों में यह बिना मधुमेह वाले लोगों की तुलना में 2 गुना अधिक बार होता है। मधुमेह के 10% रोगियों में परिधीय वाहिकाओं का एथेरोस्क्लेरोसिस विकसित होता है। मस्तिष्क वाहिकाओं का थ्रोम्बोएम्बोलिज़्म मधुमेह वाले 8% रोगियों में विकसित होता है (मधुमेह के बिना व्यक्तियों की तुलना में 2-4 गुना अधिक)।
नैदानिक अभिव्यक्तियाँ
मूलतः वे मधुमेह रहित व्यक्तियों से भिन्न नहीं हैं। टी2डीएम की नैदानिक तस्वीर में, मैक्रोवास्कुलर जटिलताएं (मायोकार्डियल इंफार्क्शन, स्ट्रोक, पैरों के जहाजों के रोड़ेदार घाव) अक्सर सामने आती हैं, और यह उनके विकास के साथ होता है कि रोगी में हाइपरग्लेसेमिया का पहली बार पता लगाया जाता है। शायद सहवर्ती स्वायत्त न्यूरोपैथी के कारण, मधुमेह वाले लोगों में 30% तक मायोकार्डियल रोधगलन एक विशिष्ट एंजाइनल अटैक (दर्द रहित रोधगलन) के बिना होता है।
निदान
एथेरोस्क्लेरोसिस (कोरोनरी हृदय रोग, सेरेब्रोवास्कुलर दुर्घटना, पैरों की धमनियों के अवरोधी घाव) की जटिलताओं के निदान के सिद्धांत मधुमेह रहित व्यक्तियों से भिन्न नहीं हैं। माप रक्तचाप(बीपी) मधुमेह के रोगी के हर बार डॉक्टर के पास जाने पर और संकेतकों का निर्धारण करने के लिए किया जाना चाहिए लिपिड स्पेक्ट्रममधुमेह के लिए रक्त परीक्षण (कुल कोलेस्ट्रॉल, ट्राइग्लिसराइड्स, एलडीएल, एचडीएल) वर्ष में कम से कम एक बार किया जाना चाहिए।
क्रमानुसार रोग का निदान
अन्य हृदय रोग, रोगसूचक धमनी उच्च रक्तचाप, माध्यमिक डिस्लिपिडेमिया।
इलाज
♦ रक्तचाप नियंत्रण.मधुमेह में सिस्टोलिक रक्तचाप का उचित स्तर 130 mmHg से कम है, और डायस्टोलिक रक्तचाप 80 mmHg है (तालिका 7.3)। इस लक्ष्य को प्राप्त करने के लिए अधिकांश रोगियों को कई उच्चरक्तचापरोधी दवाओं की आवश्यकता होती है। मधुमेह के लिए एंटीहाइपरटेंसिव थेरेपी के लिए पसंद की दवाएं एसीई अवरोधक और एंजियोटेंसिन रिसेप्टर ब्लॉकर्स हैं, जो यदि आवश्यक हो, तो थियाजाइड मूत्रवर्धक के साथ पूरक हैं। मधुमेह के जिन रोगियों को मायोकार्डियल रोधगलन हुआ है, उनकी पसंद की दवाएं β-ब्लॉकर्स हैं।
♦ डिस्लिपिडेमिया का सुधार.लिपिड स्पेक्ट्रम संकेतकों के लक्ष्य स्तर तालिका में प्रस्तुत किए गए हैं। 7.3. लिपिड कम करने वाली चिकित्सा के लिए पसंद की दवाएं 3-हाइड्रॉक्सी-3-मिथाइलग्लुटरीएल-सीओए रिडक्टेस इनहिबिटर (स्टैटिन) हैं।
♦ एंटीप्लेटलेट थेरेपी.एस्पिरिन थेरेपी (75-100 मिलीग्राम/दिन) 40 वर्ष से अधिक उम्र के मधुमेह वाले रोगियों के लिए संकेत दिया गया है, जिनमें कार्डियोवैस्कुलर पैथोलॉजी (जटिल पारिवारिक इतिहास, धमनी उच्च रक्तचाप, धूम्रपान, डिस्लिपिडेमिया, माइक्रोएल्ब्यूमिन्यूरिया) विकसित होने का खतरा है, साथ ही साथ सभी रोगियों के लिए भी। द्वितीयक रोकथाम के रूप में एथेरोस्क्लेरोसिस की नैदानिक अभिव्यक्तियाँ।
♦ कोरोनरी धमनी रोग की जांच और उपचार।कोरोनरी धमनी रोग को बाहर करने के लिए तनाव परीक्षणों को हृदय रोगों के लक्षणों वाले रोगियों के लिए संकेत दिया जाता है, साथ ही जब ईसीजी द्वारा विकृति का पता लगाया जाता है।
पूर्वानुमान
T2DM वाले 75% मरीज़ और T1DM वाले 35% मरीज़ हृदय रोगों से मरते हैं। T2DM वाले लगभग 50% मरीज़ कोरोनरी धमनी रोग की जटिलताओं से मरते हैं, 15% सेरेब्रल थ्रोम्बोम्बोलिज्म से मरते हैं। मधुमेह से पीड़ित लोगों में रोधगलन से मृत्यु दर 50% से अधिक है।
7.8.2. मधुमेह संबंधी रेटिनोपैथी
मधुमेह संबंधी रेटिनोपैथी(डीआर) - रेटिनल वाहिकाओं की माइक्रोएंगियोपैथी, जिसमें माइक्रोएन्यूरिज्म, रक्तस्राव, एक्सयूडेटिव परिवर्तन और नवगठित वाहिकाओं के प्रसार का विकास होता है, जिससे दृष्टि का आंशिक या पूर्ण नुकसान होता है (तालिका 7.17)।
एटियलजि
डीआर के विकास में मुख्य एटियलॉजिकल कारक क्रोनिक हाइपरग्लेसेमिया है। अन्य कारक (धमनी उच्च रक्तचाप, डिस्लिपिडेमिया, धूम्रपान, गर्भावस्था, आदि) कम महत्व के हैं।
रोगजनन
डीआर के रोगजनन में मुख्य लिंक हैं:
रेटिनल वाहिकाओं की माइक्रोएंगियोपैथी, जिससे हाइपोपरफ्यूज़न के विकास के साथ रक्त वाहिकाओं के लुमेन का संकुचन होता है;
माइक्रोएन्यूरिज्म के गठन के साथ संवहनी अध: पतन;
प्रगतिशील हाइपोक्सिया, संवहनी प्रसार को उत्तेजित करता है और रेटिना में फैटी अध: पतन और कैल्शियम लवण के जमाव का कारण बनता है;
मेज़ 7.17.मधुमेह संबंधी रेटिनोपैथी
 स्राव के साथ सूक्ष्म रोधगलन, जिससे नरम "कपास-ऊनी धब्बे" का निर्माण होता है;
स्राव के साथ सूक्ष्म रोधगलन, जिससे नरम "कपास-ऊनी धब्बे" का निर्माण होता है;
घने एक्सयूडेट के निर्माण के साथ लिपिड का जमाव;
शंट और एन्यूरिज्म के गठन के साथ रेटिना में फैलने वाली वाहिकाओं का प्रसार, जिससे नसों का फैलाव होता है और रेटिना हाइपोपरफ्यूज़न बिगड़ जाता है;
इस्किमिया की आगे की प्रगति के साथ चोरी की घटना, जो घुसपैठ और निशान के गठन का कारण बनती है;
इसके इस्केमिक विघटन और विटेरोरेटिनल ट्रैक्शन के गठन के परिणामस्वरूप रेटिना टुकड़ी;
रक्तस्रावी रोधगलन, बड़े पैमाने पर संवहनी आक्रमण और धमनीविस्फार के टूटने के परिणामस्वरूप होने वाला कांच का रक्तस्राव;
आईरिस (मधुमेह रूबियोसिस) के जहाजों का प्रसार, जिससे माध्यमिक मोतियाबिंद का विकास होता है;
रेटिनल एडिमा के साथ मैकुलोपैथी।
महामारी विज्ञान
विकसित देशों की कामकाजी आबादी में डीआर अंधेपन का सबसे आम कारण है, और डीएम के रोगियों में अंधापन विकसित होने का जोखिम सामान्य आबादी की तुलना में 10-20 गुना अधिक है। T1DM के निदान के समय, लगभग किसी भी रोगी में DR का पता नहीं चलता है; 5 वर्षों के बाद, 8% रोगियों में रोग का पता चलता है, और तीस वर्षों के मधुमेह के अनुभव के साथ - 98% रोगियों में। टी2डीएम के निदान के समय, 20-40% रोगियों में डीआर का पता लगाया जाता है, और पंद्रह वर्षों के टी2डीएम अनुभव वाले रोगियों में - 85% में। डीएम-1 में, प्रोलिफ़ेरेटिव रेटिनोपैथी अपेक्षाकृत अधिक आम है, और डीएम-2 में - मैकुलोपैथी (मैकुलोपैथी के 75%) मामले।
नैदानिक अभिव्यक्तियाँ
आम तौर पर स्वीकृत वर्गीकरण के अनुसार, डीआर के 3 चरण होते हैं
(सारणी 7.18).
निदान
रोग की शुरुआत के 3-5 साल बाद टी1डीएम वाले रोगियों के लिए, और इसके निदान के तुरंत बाद टी2डीएम वाले रोगियों के लिए, रेटिना फोटोग्राफी के साथ प्रत्यक्ष ऑप्थाल्मोस्कोपी सहित एक संपूर्ण नेत्र विज्ञान परीक्षा का संकेत दिया जाता है। भविष्य में, ऐसे अध्ययन प्रतिवर्ष दोहराए जाने चाहिए।
मेज़ 7.18.मधुमेह संबंधी रेटिनोपैथी का वर्गीकरण
 क्रमानुसार रोग का निदान
क्रमानुसार रोग का निदान
मधुमेह के रोगियों में अन्य नेत्र रोग।
इलाज
मधुमेह संबंधी रेटिनोपैथी, साथ ही अन्य देर से आने वाली जटिलताओं के उपचार का मूल सिद्धांत मधुमेह का इष्टतम मुआवजा है। डायबिटिक रेटिनोपैथी के इलाज और अंधापन को रोकने के लिए सबसे प्रभावी तरीका है लेजर फोटोकैग्यूलेशन।उद्देश्य
 चावल। 7.11.मधुमेह संबंधी रेटिनोपैथी:
चावल। 7.11.मधुमेह संबंधी रेटिनोपैथी:
क) अप्रसार; बी) प्रीप्रोलिफेरेटिव; ग) प्रजननशील
लेजर फोटोकैग्यूलेशन नवगठित वाहिकाओं के कामकाज की समाप्ति है, जो हेमोफथाल्मोस, ट्रैक्शन रेटिनल डिटेचमेंट, आईरिस रुबियोसिस और माध्यमिक ग्लूकोमा जैसी गंभीर जटिलताओं के विकास का मुख्य खतरा पैदा करता है।
पूर्वानुमान
मधुमेह के 2% रोगियों में अंधापन दर्ज किया गया है (टाइप 1 मधुमेह के 3-4% रोगियों और टाइप 2 मधुमेह के 1.5-2% रोगियों में)। डीआर से जुड़े अंधेपन के नए मामलों की अनुमानित घटना प्रति वर्ष प्रति 100,000 जनसंख्या पर 3.3 मामले हैं। टाइप 1 मधुमेह में, एचबीए1सी को 7.0% तक कम करने से डीआर विकसित होने का जोखिम 75% कम हो जाता है और डीआर बढ़ने का जोखिम 60% कम हो जाता है। टाइप 2 मधुमेह में, एचबीए1सी में 1% की कमी से डीआर विकसित होने का जोखिम 20% कम हो जाता है।
7.8.3. मधुमेह अपवृक्कता
मधुमेह अपवृक्कता(डीएनएफ) को एल्ब्यूमिन्यूरिया (प्रति दिन 300 मिलीग्राम से अधिक एल्ब्यूमिन या प्रति दिन 0.5 ग्राम से अधिक प्रोटीनमेह) और/या मूत्र संक्रमण, हृदय विफलता या अन्य की अनुपस्थिति में मधुमेह वाले व्यक्तियों में गुर्दे के निस्पंदन कार्य में कमी के रूप में परिभाषित किया गया है। गुर्दे की बीमारियाँ. माइक्रोएल्ब्यूमिन्यूरिया को 30-300 मिलीग्राम/दिन या 20-200 एमसीजी/मिनट के एल्ब्यूमिन उत्सर्जन के रूप में परिभाषित किया गया है।
एटियलजि और रोगजनन
डीएनएफ के लिए मुख्य जोखिम कारक मधुमेह की अवधि, क्रोनिक हाइपरग्लेसेमिया, धमनी उच्च रक्तचाप, डिस्लिपिडेमिया और माता-पिता में गुर्दे की बीमारी हैं। DNF में सबसे पहले जो चीज़ प्रभावित होती है ग्लोमेरुलर उपकरणगुर्दे
1. जिसके द्वारा संभावित तंत्रों में से एक hyperglycemiaग्लोमेरुलर क्षति के विकास को बढ़ावा देता है, ग्लूकोज चयापचय के पॉलीओल मार्ग के सक्रियण के साथ-साथ कई उन्नत ग्लाइकेशन अंत उत्पादों के कारण सोर्बिटोल का संचय होता है।
2. हेमोडायनामिक विकार, अर्थात् इंट्राग्लोमेरुलर उच्च रक्तचाप(गुर्दे के ग्लोमेरुली के अंदर रक्तचाप में वृद्धि) रोगजनन का एक आवश्यक घटक है
इंट्राग्लोमेरुलर उच्च रक्तचाप का कारण धमनियों के स्वर का उल्लंघन है: अभिवाही का फैलाव और अपवाही का संकुचन।
मेज़ 7.19.मधुमेह अपवृक्कता
 यह, बदले में, कई हास्य कारकों के प्रभाव में होता है, जैसे कि एंजियोटेंसिन -2 और एंडोटिलिन, साथ ही ग्लोमेरुलर बेसमेंट झिल्ली के इलेक्ट्रोलाइट गुणों के उल्लंघन के कारण। इसके अलावा, इंट्राग्लोमेरुलर उच्च रक्तचाप को प्रणालीगत उच्च रक्तचाप द्वारा बढ़ावा दिया जाता है, जो डीएनएफ वाले अधिकांश रोगियों में पाया जाता है। इंट्राग्लोमेरुलर उच्च रक्तचाप के कारण, बेसमेंट झिल्ली और निस्पंदन छिद्रों को नुकसान होता है,
यह, बदले में, कई हास्य कारकों के प्रभाव में होता है, जैसे कि एंजियोटेंसिन -2 और एंडोटिलिन, साथ ही ग्लोमेरुलर बेसमेंट झिल्ली के इलेक्ट्रोलाइट गुणों के उल्लंघन के कारण। इसके अलावा, इंट्राग्लोमेरुलर उच्च रक्तचाप को प्रणालीगत उच्च रक्तचाप द्वारा बढ़ावा दिया जाता है, जो डीएनएफ वाले अधिकांश रोगियों में पाया जाता है। इंट्राग्लोमेरुलर उच्च रक्तचाप के कारण, बेसमेंट झिल्ली और निस्पंदन छिद्रों को नुकसान होता है,
जिसके माध्यम से निशान घुसना शुरू हो जाते हैं (माइक्रोएल्ब्यूमिन्यूरिया),और फिर एल्ब्यूमिन की महत्वपूर्ण मात्रा (प्रोटीन्यूरिया)।बेसमेंट झिल्लियों के मोटे होने से उनके इलेक्ट्रोलाइट गुणों में बदलाव होता है, जिससे निस्पंदन छिद्रों के आकार में बदलाव के अभाव में भी अधिक एल्ब्यूमिन अल्ट्राफिल्ट्रेट में प्रवेश करता है।
3. आनुवंशिक प्रवृत्ति.डीएनएफ वाले रोगियों के रिश्तेदारों में धमनी उच्च रक्तचाप बढ़ी हुई आवृत्ति के साथ होता है। डीएनएफ और एसीई जीन बहुरूपता के बीच संबंध का प्रमाण है। सूक्ष्मदर्शी रूप से, डीएनएफ के साथ, ग्लोमेरुलर बेसमेंट झिल्ली का मोटा होना, मेसेजियम का विस्तार, साथ ही अभिवाही और अपवाही धमनियों में रेशेदार परिवर्तन का पता लगाया जाता है। अंतिम चरण में, जो चिकित्सकीय रूप से क्रोनिक रीनल फेल्योर (सीआरएफ) से मेल खाता है, फोकल (किमेलस्टील-विल्सन) और फिर फैलाना ग्लोमेरुलोस्केलेरोसिस निर्धारित किया जाता है।
महामारी विज्ञान
T1DM वाले 6-60% रोगियों में इसके प्रकट होने के 5-15 साल बाद माइक्रोएल्ब्यूमिन्यूरिया का पता चलता है। T1DM वाले 35% लोगों में DNF पाया जाता है, अधिक बार पुरुषों में और उन लोगों में जिनमें 15 वर्ष की आयु से पहले T1DM विकसित हुआ था। T2DM में, DNF 25% कॉकेशियन और 50% एशियाई लोगों में विकसित होता है। T2DM में DNF का समग्र प्रसार 4-30% है।
नैदानिक अभिव्यक्तियाँ
एक अपेक्षाकृत प्रारंभिक नैदानिक अभिव्यक्ति जो अप्रत्यक्ष रूप से डीएनएफ से जुड़ी है वह धमनी उच्च रक्तचाप है। अन्य चिकित्सीय रूप से स्पष्ट अभिव्यक्तियाँ देर से होती हैं। इनमें नेफ्रोटिक सिंड्रोम और क्रोनिक रीनल फेल्योर की अभिव्यक्तियाँ शामिल हैं।
निदान
मधुमेह से पीड़ित लोगों में डीएनएफ की जांच के लिए वार्षिक परीक्षण शामिल होता है माइक्रोएल्ब्यूमिन्यूरियाडीएम-1 के लिए, रोग प्रकट होने के 5 साल बाद, और डीएम-2 के लिए, इसका पता चलने के तुरंत बाद। इसके अलावा, गणना के लिए कम से कम वार्षिक क्रिएटिनिन स्तर की आवश्यकता होती है ग्लोमेरुलर निस्पंदन दर (जीएफआर)।जीएफआर की गणना विभिन्न सूत्रों का उपयोग करके की जा सकती है, उदाहरण के लिए, कॉकक्रॉफ्ट-गॉल्ट फॉर्मूला:
पुरुषों के लिए: ए = 1.23 (सामान्य जीएफआर 100 - 150 मिली/मिनट) महिलाओं के लिए: ए = 1.05 (सामान्य जीएफआर 85 - 130 मिली/मिनट)
डीएनएफ के शुरुआती चरणों में, जीएफआर में वृद्धि का पता लगाया जा सकता है, जो क्रोनिक रीनल फेल्योर विकसित होने पर धीरे-धीरे कम हो जाती है। डीएम-1 के प्रकट होने के 5-15 साल बाद माइक्रोएल्ब्यूमिन्यूरिया का पता चलना शुरू हो जाता है; 8-10% मामलों में टी2डीएम के साथ इसका पता लगने के तुरंत बाद पता चल जाता है, संभवतः निदान से पहले रोग के लंबे स्पर्शोन्मुख पाठ्यक्रम के कारण। T1DM में प्रत्यक्ष प्रोटीनुरिया या एल्बुमिनुरिया का चरम विकास शुरुआत के 15 से 20 साल के बीच होता है। प्रोटीनुरिया इंगित करता है अपरिवर्तनीयताडीएनएफ, जो देर-सबेर दीर्घकालिक गुर्दे की विफलता का कारण बनेगा। प्रत्यक्ष प्रोटीनमेह की शुरुआत के बाद औसतन 7-10 वर्षों में यूरेमिया विकसित होता है। यह ध्यान दिया जाना चाहिए कि जीएफआर प्रोटीनुरिया से संबंधित नहीं है।
क्रमानुसार रोग का निदान
मधुमेह वाले लोगों में प्रोटीनूरिया और गुर्दे की विफलता के अन्य कारण। ज्यादातर मामलों में, डीएनएफ को धमनी उच्च रक्तचाप, मधुमेह संबंधी रेटिनोपैथी या न्यूरोपैथी के साथ जोड़ा जाता है, जिसके अभाव में विभेदक निदान में विशेष रूप से सावधानी बरतनी चाहिए। डीएम-1 के 10% मामलों में और डीएम-2 के 30% मामलों में, प्रोटीनूरिया डीएनएफ से जुड़ा नहीं है।
इलाज
♦ प्राथमिक एवं माध्यमिक की बुनियादी शर्तें रोकथाम
डीएनएफमधुमेह का मुआवजा और सामान्य प्रणालीगत रक्तचाप बनाए रखना है। इसके अलावा, डीएनएफ की प्राथमिक रोकथाम में प्रोटीन खाद्य पदार्थों की खपत को कम करना शामिल है - दैनिक कैलोरी का 35% से कम।
♦ चरणों में माइक्रोएल्ब्यूमिन्यूरियाऔर प्रोटीनमेहमरीजों को एसीई इनहिबिटर या एंजियोटेंसिन रिसेप्टर ब्लॉकर्स निर्धारित किए जाते हैं। सहवर्ती धमनी उच्च रक्तचाप के साथ, यदि आवश्यक हो तो अन्य एंटीहाइपरटेंसिव दवाओं के साथ संयोजन में, उन्हें एंटीहाइपरटेंसिव खुराक में निर्धारित किया जाता है। सामान्य रक्तचाप के साथ, ये दवाएं खुराक में निर्धारित की जाती हैं जिससे हाइपोटेंशन का विकास नहीं होता है। एसीई अवरोधक (डीएम-1 और डीएम-2 के लिए) और एंजियोटेंसिन रिसेप्टर ब्लॉकर्स (डीएम-2 के लिए) दोनों माइक्रोएल्ब्यूमिन्यूरिया के प्रोटीनूरिया में संक्रमण को रोकने में मदद करते हैं। कुछ मामलों में, अन्य मापदंडों द्वारा मधुमेह के मुआवजे के संयोजन में इस चिकित्सा की पृष्ठभूमि के खिलाफ, माइक्रोएल्ब्यूमिन्यूरिया समाप्त हो जाता है। इसके अलावा, माइक्रोएल्ब्यूमिन्यूरिया के चरण से शुरू करना आवश्यक है
प्रोटीन का सेवन दैनिक कैलोरी के 10% से कम (या प्रति किलोग्राम वजन 0.8 ग्राम से कम) और नमक का सेवन 3 ग्राम से कम करना।
♦ मंच पर चिरकालिक गुर्दा निष्क्रियता,एक नियम के रूप में, ग्लूकोज कम करने वाली चिकित्सा के समायोजन की आवश्यकता होती है। T2DM वाले अधिकांश रोगियों को इंसुलिन थेरेपी पर स्विच करने की आवश्यकता होती है, क्योंकि TSP के संचय से गंभीर हाइपोग्लाइसीमिया विकसित होने का खतरा होता है। T1DM वाले अधिकांश रोगियों को इंसुलिन आवश्यकताओं में कमी का अनुभव होता है, क्योंकि किडनी इंसुलिन चयापचय की मुख्य साइटों में से एक है। जब सीरम क्रिएटिनिन का स्तर 500 μmol/L या अधिक तक बढ़ जाता है, तो रोगी को एक्स्ट्राकोर्पोरियल (हेमोडायलिसिस, पेरिटोनियल डायलिसिस) या सर्जिकल (किडनी प्रत्यारोपण) उपचार पद्धति के लिए तैयार करने का प्रश्न उठाना आवश्यक है। किडनी प्रत्यारोपण का संकेत तब दिया जाता है जब क्रिएटिनिन का स्तर 600-700 μmol/l तक पहुंच जाता है और ग्लोमेरुलर निस्पंदन दर क्रमशः 25 ml/min, हेमोडायलिसिस - 1000-1200 µmol/l और 10 ml/min से कम हो जाती है।
पूर्वानुमान
टाइप 1 डायबिटीज़ वाले 50% मरीज़ और टाइप 2 डायबिटीज़ वाले 10% मरीज़ जिन्हें प्रोटीनमेह होता है, उनमें अगले 10 वर्षों में क्रोनिक रीनल फेल्योर विकसित हो जाता है। 50 वर्ष से कम आयु के टाइप 1 मधुमेह के रोगियों में होने वाली सभी मौतों में से 15% डीएनएफ के कारण क्रोनिक रीनल फेल्योर से जुड़ी हैं।
7.8.4. मधुमेही न्यूरोपैथी
मधुमेही न्यूरोपैथी(डीएनई) तंत्रिका तंत्र को नुकसान के सिंड्रोम का एक संयोजन है, जिसे प्रक्रिया में इसके विभिन्न भागों (सेंसरिमोटर, ऑटोनोमिक) की प्रमुख भागीदारी के साथ-साथ क्षति की व्यापकता और गंभीरता के आधार पर वर्गीकृत किया जा सकता है (तालिका 7.20) ).
मैं। सेंसोरिमोटर न्यूरोपैथी:
सममित;
फोकल (मोनोन्यूरोपैथी) या पॉलीफोकल (कपाल, समीपस्थ मोटर, अंगों और धड़ की मोनोन्यूरोपैथी)।
द्वितीय. स्वायत्त (स्वायत्त) न्यूरोपैथी:
कार्डियोवैस्कुलर (ऑर्थोस्टैटिक हाइपोटेंशन, कार्डियक डिनेरवेशन सिंड्रोम);
गैस्ट्रोइंटेस्टाइनल (गैस्ट्रिक प्रायश्चित, पित्त संबंधी डिस्केनेसिया, मधुमेह एंटरोपैथी);
मूत्रजननांगी (मूत्राशय और यौन क्रिया की शिथिलता के साथ);
रोगी की हाइपोग्लाइसीमिया को पहचानने की क्षमता क्षीण होती है;
बिगड़ा हुआ पुतली समारोह;
पसीने की ग्रंथियों की शिथिलता (डिस्टल एनहाइड्रोसिस, भोजन करते समय हाइपरहाइड्रोसिस)।
मेज़ 7.20.मधुमेही न्यूरोपैथी
 एटियलजि और रोगजनन
एटियलजि और रोगजनन
डीएनई का मुख्य कारण हाइपरग्लेसेमिया है। इसके रोगजनन के कई तंत्र सुझाए गए हैं:
ग्लूकोज चयापचय के पॉलीओल मार्ग का सक्रियण, जिसके परिणामस्वरूप सोर्बिटोल, फ्रुक्टोज का संचय होता है और तंत्रिका कोशिकाओं में मायोइनोसिटोल और ग्लूटाथियोन की सामग्री में कमी आती है। यह, बदले में, मुक्त कण प्रक्रियाओं की सक्रियता और नाइट्रिक ऑक्साइड के स्तर में कमी की ओर जाता है;
तंत्रिका कोशिकाओं की झिल्ली और साइटोप्लाज्मिक प्रोटीन का गैर-एंजाइमी ग्लाइकोसिलेशन;
माइक्रोएन्जियोपैथी वासा तंत्रिकाजिससे केशिका रक्त प्रवाह और तंत्रिका हाइपोक्सिया में मंदी आती है।
महामारी विज्ञान
दोनों प्रकार के मधुमेह में डीएनई का प्रसार लगभग 30% है। T1DM के साथ, बीमारी की शुरुआत के 5 साल बाद, 10% रोगियों में इसका पता चलना शुरू हो जाता है। T2DM में DNE के नए मामलों की घटना प्रति वर्ष लगभग 6% रोगियों की है। सबसे आम प्रकार डिस्टल सिमेट्रिक सेंसरिमोटर डीएनई है।
नैदानिक अभिव्यक्तियाँ
सेंसरिमोटर दिवसमोटर और संवेदी विकारों के एक जटिल रूप में प्रकट होता है। डीएनई के डिस्टल रूप का एक सामान्य लक्षण है पेरेस्टेसिया,जो "रेंगने वाले रोंगटे खड़े होने", स्तब्ध हो जाने की भावना से प्रकट होते हैं। मरीज़ अक्सर ठंडे पैरों की शिकायत करते हैं, हालांकि स्पर्श करने पर वे गर्म रहते हैं, जो एक संकेत है जो पॉलीन्यूरोपैथी को इस्कीमिक परिवर्तनों से अलग करता है, जब पैर छूने पर ठंडे होते हैं। संवेदी न्यूरोपैथी की प्रारंभिक अभिव्यक्ति कंपन संवेदनशीलता का उल्लंघन है। इसकी विशेषता "रेस्टलेस लेग्स" सिंड्रोम है, जो रात्रिकालीन पेरेस्टेसिया और बढ़ी हुई संवेदनशीलता का एक संयोजन है। पैर में दर्दअक्सर रात में परेशानी होती है, और कभी-कभी रोगी कंबल का स्पर्श भी सहन नहीं कर पाता है। एक विशिष्ट मामले में, दर्द, अवरोधी धमनी रोगों के विपरीत, चलने पर कम हो सकता है। वर्षों से, दर्द संवेदनशीलता के लिए जिम्मेदार छोटे तंत्रिका तंतुओं की मृत्यु के कारण दर्द अपने आप बंद हो सकता है। हाइपोएस्थेसिया"मोज़ा" और "दस्ताने" के तरीके में संवेदनशीलता की हानि से प्रकट होता है। गहरी, प्रोप्रियोसेप्टिव संवेदनशीलता के उल्लंघन से बिगड़ा हुआ समन्वय और चलने में कठिनाई (संवेदी गतिभंग) होती है। रोगी "विदेशी पैर", "रूई पर खड़े होने" की भावना की शिकायत करता है। ट्रॉफिक संक्रमण के उल्लंघन से त्वचा, हड्डियों और टेंडन में अपक्षयी परिवर्तन होते हैं। दर्द संवेदनशीलता के क्षीण होने से बार-बार, रोगी द्वारा ध्यान न दिए जाने पर, पैरों में सूक्ष्म आघात हो जाते हैं, जो आसानी से संक्रमित हो जाते हैं। बिगड़ा समन्वय और चलने से पैर के जोड़ों पर भार का गैर-शारीरिक पुनर्वितरण होता है। परिणामस्वरूप, पैर की मस्कुलोस्केलेटल प्रणाली में शारीरिक संबंध बाधित हो जाते हैं।
पैर का आर्च विकृत हो जाता है, सूजन, फ्रैक्चर और पुरानी पीप प्रक्रियाएं विकसित होती हैं (धारा 7.8.5 देखें)।
स्वायत्त दिन के उजाले के कई रूप हैं। कारण हृदय संबंधी रूप- कार्डियोपल्मोनरी कॉम्प्लेक्स और बड़े जहाजों के संक्रमण का उल्लंघन। वेगस तंत्रिका सबसे लंबी तंत्रिका है, और इसलिए दूसरों की तुलना में पहले प्रभावित होती है। सहानुभूतिपूर्ण प्रभावों की प्रबलता के परिणामस्वरूप, विश्राम क्षिप्रहृदयता.ऑर्थोस्टेसिस के प्रति अपर्याप्त प्रतिक्रिया प्रकट होती है ऑर्थोस्टैटिक हाइपोटेंशनऔर बेहोशी. फुफ्फुसीय-हृदय परिसर के स्वायत्त निषेध से हृदय गति परिवर्तनशीलता का अभाव होता है। ऑटोनोमिक न्यूरोपैथी मधुमेह के रोगियों में साइलेंट मायोकार्डियल रोधगलन के बढ़ते प्रसार से जुड़ी है।
लक्षण जठरांत्र रूपडीएनई धीमी गति से या, इसके विपरीत, तेजी से गैस्ट्रिक खाली करने वाला गैस्ट्रोपैरेसिस है, जो इंसुलिन थेरेपी के चयन में कठिनाइयां पैदा कर सकता है, क्योंकि कार्बोहाइड्रेट अवशोषण का समय और मात्रा अनिश्चित काल तक बदलती रहती है; ग्रासनली प्रायश्चित, भाटा ग्रासनलीशोथ, डिस्पैगिया; पतली दस्त। के लिए मूत्रजननांगी रूपडीएनई की विशेषता मूत्रवाहिनी और मूत्राशय की शिथिलता है, जिससे मूत्र संक्रमण की प्रवृत्ति होती है; स्तंभन दोष (मधुमेह के लगभग 50% रोगी); प्रतिगामी स्खलन।
वनस्पति डीएनई की अन्य संभावित अभिव्यक्तियाँ हाइपोग्लाइसीमिया, बिगड़ा हुआ पुतली समारोह, बिगड़ा हुआ पसीना ग्रंथि समारोह (एनहाइड्रोसिस), और डायबिटिक एमियोट्रॉफी को पहचानने की क्षमता में कमी है।
निदान
मधुमेह के रोगियों की न्यूरोलॉजिकल जांच हर साल करानी चाहिए। कम से कम, इसमें डिस्टल सेंसरिमोटर न्यूरोपैथी की पहचान करने के उद्देश्य से परीक्षण करना शामिल है। यह एक स्नातक ट्यूनिंग कांटा का उपयोग करके कंपन संवेदनशीलता, एक मोनोफिलामेंट का उपयोग करके स्पर्श संवेदनशीलता, साथ ही तापमान और दर्द संवेदनशीलता का आकलन करके किया जाता है। संकेतों के अनुसार, स्वायत्त तंत्रिका तंत्र की स्थिति का अध्ययन किया जाता है: हृदय के पैरासिम्पेथेटिक संक्रमण की अपर्याप्तता का निदान करने के लिए, कई कार्यात्मक परीक्षणों का उपयोग किया जाता है, जैसे कि परिवर्तनशीलता के आकलन के साथ गहरी सांस लेने के दौरान हृदय गति को मापना।
हृदय गति और वलसाल्वा पैंतरेबाज़ी; हृदय की सहानुभूतिपूर्ण संक्रमण की अपर्याप्तता का निदान करने के लिए, एक ऑर्थोस्टेटिक परीक्षण का उपयोग किया जाता है।
क्रमानुसार रोग का निदान
अन्य मूल की न्यूरोपैथी (अल्कोहल, यूरीमिक, बी 12 की कमी वाले एनीमिया, आदि के साथ)। स्वायत्त न्यूरोपैथी के परिणामस्वरूप किसी विशेष अंग की शिथिलता का निदान अंग विकृति को छोड़कर ही स्थापित किया जाता है।
इलाज
1. ग्लूकोज कम करने वाली चिकित्सा का अनुकूलन।
2. पैरों की देखभाल (खंड 7.8.5 देखें)।
3. सभी अध्ययनों में न्यूरोट्रोपिक दवाओं (α-लिपोइक एसिड) की प्रभावशीलता की पुष्टि नहीं की गई है।
4. रोगसूचक चिकित्सा (दर्द से राहत, स्तंभन दोष के लिए सिल्डेनाफिल, ऑर्थोस्टेटिक हाइपोटेंशन के लिए फ्लूड्रोकार्टिसोन, आदि)।
पूर्वानुमान
शुरुआती चरणों में, मधुमेह की लगातार क्षतिपूर्ति की पृष्ठभूमि के खिलाफ डीएनई को उलटा किया जा सकता है। डीएनई अल्सरेटिव घावों वाले 80% रोगियों में पाया जाता है और पैर विच्छेदन के लिए मुख्य जोखिम कारक है
7.8.5. मधुमेह पैर सिंड्रोम
मधुमेह पैर सिंड्रोम(एसडीएस) मधुमेह में पैर की एक रोग संबंधी स्थिति है, जो परिधीय नसों, त्वचा और नरम ऊतकों, हड्डियों और जोड़ों को नुकसान की पृष्ठभूमि के खिलाफ उत्पन्न होती है और तीव्र और पुरानी अल्सर, ऑस्टियोआर्टिकुलर घावों और प्युलुलेंट-नेक्रोटिक प्रक्रियाओं द्वारा प्रकट होती है (तालिका 7.21) .
एटियलजि और रोगजनन
डीएफएस का रोगजनन बहुघटक है और संक्रमण की स्पष्ट प्रवृत्ति के साथ न्यूरोपैथिक और छिड़काव विकारों के संयोजन द्वारा दर्शाया जाता है। रोगजनन में सूचीबद्ध कारकों में से एक या किसी अन्य की प्रबलता के आधार पर, 3 मुख्य रूपों को प्रतिष्ठित किया जाता है
मेज़ 7.21.मधुमेह पैर सिंड्रोम
 I. न्यूरोपैथिक रूप(60-70 %):
I. न्यूरोपैथिक रूप(60-70 %):
ऑस्टियोआर्थ्रोपैथी के बिना;
मधुमेह ऑस्टियोआर्थ्रोपैथी के साथ।
द्वितीय. न्यूरोइस्केमिक (मिश्रित) रूप(15-20 %).
तृतीय. इस्केमिक रूप(3-7 %).
एसडीएस का न्यूरोपैथिक रूप। मधुमेह न्यूरोपैथी में, सबसे लंबी नसों के दूरस्थ भाग मुख्य रूप से प्रभावित होते हैं। पोषी आवेगों की लंबे समय तक कमी से त्वचा, हड्डियों, स्नायुबंधन, टेंडन और मांसपेशियों की हाइपोट्रॉफी होती है। संयोजी संरचनाओं की हाइपोट्रॉफी का परिणाम सहायक भार के गैर-शारीरिक पुनर्वितरण और कुछ क्षेत्रों में इसकी अत्यधिक वृद्धि के साथ पैर की विकृति है। इन स्थानों में, उदाहरण के लिए मेटाटार्सल हड्डियों के सिर के प्रक्षेपण के क्षेत्र में, त्वचा का मोटा होना और हाइपरकेराटोज़ का गठन नोट किया जाता है। इन क्षेत्रों पर लगातार दबाव से अंतर्निहित नरम ऊतकों की सूजन ऑटोलिसिस होती है, जो अल्सरेटिव दोष के गठन के लिए पूर्व शर्त बनाती है। शोष और खराब पसीने के परिणामस्वरूप, त्वचा शुष्क हो जाती है और आसानी से फट जाती है। दर्द संवेदनशीलता कम होने के कारण रोगी अक्सर होने वाले परिवर्तनों पर ध्यान नहीं देता है। वह जूते की असुविधा का तुरंत पता नहीं लगा सकता है, जिससे खरोंच और कॉलस का निर्माण होता है, और दरार के स्थानों में विदेशी निकायों या छोटे घावों की शुरूआत पर ध्यान नहीं देता है। स्थिति गहरी संवेदनशीलता के उल्लंघन से बढ़ जाती है, जो चाल में गड़बड़ी और पैरों की गलत स्थिति में प्रकट होती है। अक्सर, अल्सरेटिव दोष स्टेफिलोकोसी, स्ट्रेप्टोकोकी और आंतों के बैक्टीरिया से संक्रमित होता है; अवायवीय वनस्पतियाँ अक्सर मिलती हैं। न्यूरोपैथिक ऑस्टियोआर्थ्रोपैथी पैर के ऑस्टियोआर्टिकुलर तंत्र (ऑस्टियोपोरोसिस, ऑस्टियोलाइसिस, हाइपरोस्टोसिस) में स्पष्ट डिस्ट्रोफिक परिवर्तनों का परिणाम है।
एसडीएस का इस्केमिक रूप निचले छोरों की धमनियों के एथेरोस्क्लेरोसिस का परिणाम है, जिससे मुख्य रक्त प्रवाह में व्यवधान होता है, अर्थात। डायबिटिक मैक्रोएंगियोपैथी के प्रकारों में से एक है।
महामारी विज्ञान
डीडीएस 10-25% में देखा जाता है, और कुछ आंकड़ों के अनुसार, मधुमेह के 30-80% रोगियों में किसी न किसी रूप में देखा जाता है। संयुक्त राज्य अमेरिका में, डीडीएस के साथ मधुमेह के रोगियों के इलाज की वार्षिक लागत $1 बिलियन है।
नैदानिक अभिव्यक्तियाँ
पर न्यूरोपैथिक रूपएसडीएस दो सबसे सामान्य प्रकार के घावों को अलग करता है: न्यूरोपैथिक अल्सर और ऑस्टियोआर्थ्रोपैथी (विकास के साथ)।
 चावल। 7.12.डायबिटिक फुट सिंड्रोम में न्यूरोपैथिक अल्सर
चावल। 7.12.डायबिटिक फुट सिंड्रोम में न्यूरोपैथिक अल्सर
 चावल। 7.13.डायबिटिक फुट सिंड्रोम में चारकोट जोड़
चावल। 7.13.डायबिटिक फुट सिंड्रोम में चारकोट जोड़
चारकोट जोड़)। न्यूरोपैथिक अल्सर,एक नियम के रूप में, वे एकमात्र और इंटरडिजिटल रिक्त स्थान के क्षेत्र में स्थानीयकृत होते हैं, अर्थात। सबसे अधिक दबाव महसूस करने वाले पैर के क्षेत्रों पर (चित्र 7.12)।
पैर की लिगामेंटस प्रणाली में विनाशकारी परिवर्तन कई महीनों में बढ़ सकते हैं और गंभीर हड्डी विकृति का कारण बन सकते हैं - मधुमेह ऑस्टियोआर्थ्रोपैथीऔर गठन चारकोट जोड़,इस मामले में, पैर की तुलना लाक्षणिक रूप से "हड्डियों के थैले" से की जाती है
पर एसडीएस का इस्केमिक रूप
पैरों की त्वचा ठंडी, पीली या सियानोटिक है; इस्कीमिया की प्रतिक्रिया में सतही केशिकाओं के फैलाव के कारण अक्सर इसका रंग गुलाबी-लाल हो जाता है। अल्सरेटिव दोष एक्रल नेक्रोसिस के रूप में होते हैं - उंगलियों की युक्तियों पर, एड़ी की सीमांत सतह पर (चित्र 7.14)।
पैर की धमनियों, पोपलीटल और ऊरु धमनियों में नाड़ी कमजोर हो जाती है या दिखाई नहीं देती है।
विशिष्ट मामलों में, मरीज़ "आंतरायिक खंजता" की शिकायत करते हैं। इस्केमिक अंग क्षति की गंभीरता तीन मुख्य कारकों द्वारा निर्धारित की जाती है: स्टेनोसिस की गंभीरता, संपार्श्विक रक्त प्रवाह का विकास, और रक्त जमावट प्रणाली की स्थिति।
निदान
मधुमेह से पीड़ित रोगी के पैरों की जांच हर छह महीने में कम से कम एक बार डॉक्टर से मिलने के दौरान की जानी चाहिए। एसडीएस के निदान में शामिल हैं:
 चावल। 7.14.डायबिटिक फुट सिंड्रोम के इस्केमिक रूप में एक्रल नेक्रोसिस
चावल। 7.14.डायबिटिक फुट सिंड्रोम के इस्केमिक रूप में एक्रल नेक्रोसिस
पैरों की जांच;
न्यूरोलॉजिकल स्थिति का आकलन - विभिन्न प्रकार की संवेदनशीलता, कण्डरा सजगता, इलेक्ट्रोमोग्राफी;
धमनी रक्त प्रवाह की स्थिति का आकलन - एंजियोग्राफी, डॉपलर अल्ट्रासाउंड, डॉपलर सोनोग्राफी;
पैरों और टखने के जोड़ों का एक्स-रे;
घाव स्राव की बैक्टीरियोलॉजिकल जांच।
क्रमानुसार रोग का निदान
यह एक अलग मूल के पैरों पर घाव की प्रक्रियाओं के साथ-साथ निचले छोरों के जहाजों के अन्य रोड़ा रोगों और पैर के जोड़ों की विकृति के साथ किया जाता है। इसके अलावा, डीएफएस के नैदानिक रूपों में अंतर करना आवश्यक है (तालिका 7.22)।
इलाज
इलाज न्यूरोपैथिक रूप से संक्रमितवीटीएस फॉर्म में निम्नलिखित गतिविधियों का एक सेट शामिल है:
मधुमेह के लिए मुआवजे के अनुकूलन में आमतौर पर इंसुलिन की खुराक बढ़ाना शामिल है, और मधुमेह -2 के मामले में - इसे पर स्विच करना;
प्रणालीगत एंटीबायोटिक चिकित्सा;
पैर को पूरी तरह से उतारना (इससे वर्षों से मौजूद अल्सर कुछ ही हफ्तों में ठीक हो सकते हैं);
हाइपरकेराटोसिस के क्षेत्रों को हटाने के साथ घाव का स्थानीय उपचार;
पैरों की देखभाल, उचित चयन और विशेष जूते पहनना। समय पर रूढ़िवादी चिकित्सा की अनुमति देता है
95% मामलों में सर्जरी से बचें।
मेज़ 7.22.डीएफएस के नैदानिक रूपों का विभेदक निदान
 इलाज इस्कीमिकवीटीएस फॉर्म में शामिल हैं:
इलाज इस्कीमिकवीटीएस फॉर्म में शामिल हैं:
मधुमेह के लिए मुआवजे के अनुकूलन में आमतौर पर इंसुलिन की खुराक बढ़ाना शामिल है, और मधुमेह -2 के मामले में - इसे पर स्विच करना;
अल्सरेटिव-नेक्रोटिक घावों की अनुपस्थिति में, एर्गोथेरेपी (दिन में 1-2 घंटे चलना, संपार्श्विक रक्त प्रवाह के विकास को बढ़ावा देना);
प्रभावित वाहिकाओं पर पुनरोद्धार संचालन;
रूढ़िवादी चिकित्सा: थक्कारोधी, एस्पिरिन (100 मिलीग्राम/दिन तक), यदि आवश्यक हो, फाइब्रिनोलिटिक्स, प्रोस्टाग्लैंडीन ई1 और प्रोस्टेसाइक्लिन तैयारी।
सभी प्रकार के डीएफएस में व्यापक प्युलुलेंट-नेक्रोटिक घावों के विकास के साथ, विच्छेदन का प्रश्न उठाया जाता है।
पूर्वानुमान
पैर विच्छेदन की कुल संख्या में से 50 से 70% मधुमेह के रोगियों में होते हैं। मधुमेह के रोगियों में पैर का विच्छेदन मधुमेह रहित लोगों की तुलना में 20-40 गुना अधिक होता है।
7.9. मधुमेह और गर्भावस्था
गर्भकालीन मधुमेह(जीडीएम) ग्लूकोज सहनशीलता का एक विकार है जिसे सबसे पहले गर्भावस्था के दौरान पहचाना गया (तालिका 7.23)। यह परिभाषा इस संभावना को बाहर नहीं करती है कि कार्बोहाइड्रेट चयापचय की विकृति गर्भावस्था से पहले हो सकती है। जीडीएम को उन स्थितियों से अलग किया जाना चाहिए जब पहले से निदान मधुमेह (उम्र के कारण, अक्सर टी1डीएम) से पीड़ित महिला गर्भवती हो जाती है।
एटियलजि और रोगजनन
GDM में वे T2DM के समान हैं। डिम्बग्रंथि और प्लेसेंटल स्टेरॉयड के उच्च स्तर, साथ ही अधिवृक्क प्रांतस्था द्वारा कोर्टिसोल के उत्पादन में वृद्धि से गर्भावस्था के दौरान शारीरिक इंसुलिन प्रतिरोध का विकास होता है। जीडीएम का विकास इस तथ्य से जुड़ा है कि इंसुलिन प्रतिरोध, जो स्वाभाविक रूप से गर्भावस्था के दौरान विकसित होता है, और इसके परिणामस्वरूप, पूर्वनिर्धारित व्यक्तियों में इंसुलिन की बढ़ती आवश्यकता अग्न्याशय की β-कोशिकाओं की कार्यात्मक क्षमता से अधिक हो जाती है। बच्चे के जन्म के बाद, हार्मोनल और चयापचय संबंधों के मूल स्तर पर लौटने के साथ, यह आमतौर पर दूर हो जाता है।
मेज़ 7.23.गर्भकालीन मधुमेह
 जीडीएम आमतौर पर गर्भावस्था के 4 से 8 महीने के बीच, दूसरी तिमाही के मध्य में विकसित होता है। अधिकांश मरीज़ अधिक वजन वाले हैं और उनमें मधुमेह मेलिटस-2 का इतिहास है। जीडीएम विकसित होने के जोखिम कारक, साथ ही जीडीएम विकसित होने के कम जोखिम वाली महिलाओं के समूह तालिका में दिए गए हैं। 7.24.
जीडीएम आमतौर पर गर्भावस्था के 4 से 8 महीने के बीच, दूसरी तिमाही के मध्य में विकसित होता है। अधिकांश मरीज़ अधिक वजन वाले हैं और उनमें मधुमेह मेलिटस-2 का इतिहास है। जीडीएम विकसित होने के जोखिम कारक, साथ ही जीडीएम विकसित होने के कम जोखिम वाली महिलाओं के समूह तालिका में दिए गए हैं। 7.24.
मेज़ 7.24.गर्भावधि मधुमेह के विकास के लिए जोखिम कारक
 मातृ हाइपरग्लेसेमिया से बच्चे के संचार तंत्र में हाइपरग्लेसेमिया हो जाता है। ग्लूकोज आसानी से प्लेसेंटा में प्रवेश कर जाता है और मां के रक्त से लगातार भ्रूण तक पहुंचता रहता है। अमीनो एसिड का सक्रिय परिवहन और भ्रूण में कीटोन निकायों का स्थानांतरण भी होता है। इसके विपरीत, इंसुलिन, ग्लूकागन और मातृ मुक्त फैटी एसिड भ्रूण के रक्त में प्रवेश नहीं करते हैं। गर्भावस्था के पहले 9-12 सप्ताह में, भ्रूण का अग्न्याशय अभी तक अपना इंसुलिन उत्पन्न नहीं करता है। यह समय भ्रूण के ऑर्गोजेनेसिस के चरण से मेल खाता है, जब निरंतर हाइपरग्लेसेमिया के साथ, मां में विभिन्न विकासात्मक दोष (हृदय, रीढ़, रीढ़ की हड्डी, जठरांत्र संबंधी मार्ग) बन सकते हैं। गर्भावस्था के 12वें सप्ताह से, भ्रूण का अग्न्याशय इंसुलिन को संश्लेषित करना शुरू कर देता है, और हाइपरग्लेसेमिया के जवाब में, भ्रूण के अग्न्याशय की β-कोशिकाओं की प्रतिक्रियाशील अतिवृद्धि और हाइपरप्लासिया विकसित होती है। हाइपरइन्सुलिनमिया के कारण, भ्रूण का मैक्रोसोमिया विकसित होता है, साथ ही लेसिथिन संश्लेषण का निषेध होता है, जो नवजात शिशुओं में श्वसन संकट सिंड्रोम की उच्च घटनाओं की व्याख्या करता है। β-सेल हाइपरप्लासिया और हाइपरिन्सुलिनमिया के परिणामस्वरूप, गंभीर और लंबे समय तक हाइपोग्लाइसीमिया की प्रवृत्ति होती है।
मातृ हाइपरग्लेसेमिया से बच्चे के संचार तंत्र में हाइपरग्लेसेमिया हो जाता है। ग्लूकोज आसानी से प्लेसेंटा में प्रवेश कर जाता है और मां के रक्त से लगातार भ्रूण तक पहुंचता रहता है। अमीनो एसिड का सक्रिय परिवहन और भ्रूण में कीटोन निकायों का स्थानांतरण भी होता है। इसके विपरीत, इंसुलिन, ग्लूकागन और मातृ मुक्त फैटी एसिड भ्रूण के रक्त में प्रवेश नहीं करते हैं। गर्भावस्था के पहले 9-12 सप्ताह में, भ्रूण का अग्न्याशय अभी तक अपना इंसुलिन उत्पन्न नहीं करता है। यह समय भ्रूण के ऑर्गोजेनेसिस के चरण से मेल खाता है, जब निरंतर हाइपरग्लेसेमिया के साथ, मां में विभिन्न विकासात्मक दोष (हृदय, रीढ़, रीढ़ की हड्डी, जठरांत्र संबंधी मार्ग) बन सकते हैं। गर्भावस्था के 12वें सप्ताह से, भ्रूण का अग्न्याशय इंसुलिन को संश्लेषित करना शुरू कर देता है, और हाइपरग्लेसेमिया के जवाब में, भ्रूण के अग्न्याशय की β-कोशिकाओं की प्रतिक्रियाशील अतिवृद्धि और हाइपरप्लासिया विकसित होती है। हाइपरइन्सुलिनमिया के कारण, भ्रूण का मैक्रोसोमिया विकसित होता है, साथ ही लेसिथिन संश्लेषण का निषेध होता है, जो नवजात शिशुओं में श्वसन संकट सिंड्रोम की उच्च घटनाओं की व्याख्या करता है। β-सेल हाइपरप्लासिया और हाइपरिन्सुलिनमिया के परिणामस्वरूप, गंभीर और लंबे समय तक हाइपोग्लाइसीमिया की प्रवृत्ति होती है।
महामारी विज्ञान
मधुमेह प्रजनन आयु की सभी महिलाओं में से 0.3% को प्रभावित करता है, 0.2-0.3% गर्भवती महिलाएं पहले से ही मधुमेह से पीड़ित हैं, और 1-14% गर्भधारण में जीडीएम वास्तविक मधुमेह विकसित या प्रकट होता है। जीडीएम की व्यापकता अलग-अलग आबादी में अलग-अलग होती है, उदाहरण के लिए, संयुक्त राज्य अमेरिका में यह लगभग 4% गर्भवती महिलाओं (प्रति वर्ष 135 हजार मामले) में पाई जाती है।
नैदानिक अभिव्यक्तियाँ
जीडीएम में अनुपस्थित। विघटित मधुमेह के गैर-विशिष्ट लक्षण हो सकते हैं।
निदान
जैव रासायनिक रक्त परीक्षण के भाग के रूप में सभी गर्भवती महिलाओं के लिए उपवास रक्त शर्करा के स्तर का निर्धारण किया जाता है। जो महिलाएं जोखिम में हैं (तालिका 7.24) उन्हें सलाह दी जाती है मौखिक ग्लूकोज सहिष्णुता परीक्षण(ओजीटीटी)। गर्भवती महिलाओं में इसके कार्यान्वयन के लिए कई विकल्प बताए गए हैं। उनमें से सबसे सरल में निम्नलिखित नियम शामिल हैं:
परीक्षा से 3 दिन पहले, महिला सामान्य आहार खाती है और अपनी सामान्य शारीरिक गतिविधि बनाए रखती है;
परीक्षण सुबह खाली पेट, रात भर कम से कम 8 घंटे के उपवास के बाद किया जाता है;
खाली पेट रक्त का नमूना लेने के बाद, 5 मिनट के भीतर महिला 250-300 मिलीलीटर पानी में 75 ग्राम सूखा ग्लूकोज घोलकर पीती है; रक्त शर्करा का स्तर 2 घंटे के बाद फिर से निर्धारित होता है।
जीडीएम का निदान निम्नलिखित द्वारा स्थापित किया गया है मानदंड:
उपवास संपूर्ण रक्त ग्लूकोज (शिरापरक, केशिका) > 6.1 mmol/l या
शिरापरक रक्त प्लाज्मा ग्लूकोज ≥ 7 mmol/l या
75 ग्राम ग्लूकोज ≥ 7.8 mmol/l के भार के 2 घंटे बाद संपूर्ण केशिका रक्त ग्लूकोज या शिरापरक रक्त प्लाज्मा।
यदि जोखिम वाली महिला के परीक्षण के परिणाम सामान्य हैं, तो गर्भावस्था के 24-28 सप्ताह में परीक्षण दोहराया जाता है।
क्रमानुसार रोग का निदान
जीडीएम और सच्चा मधुमेह; गर्भवती महिलाओं में ग्लूकोसुरिया।
इलाज
मां और भ्रूण के लिए जोखिम, साथ ही मधुमेह के उपचार के दृष्टिकोण और जीडीएम और वास्तविक मधुमेह में इसके नियंत्रण की विशेषताएं समान हैं। गर्भावस्था के दौरान मधुमेह की देर से जटिलताएँ काफी बढ़ सकती हैं, लेकिन मधुमेह की उच्च गुणवत्ता वाली क्षतिपूर्ति के साथ गर्भावस्था की समाप्ति के कोई संकेत नहीं हैं। मधुमेह (आमतौर पर टाइप 1 मधुमेह) से पीड़ित महिला को कम उम्र में गर्भावस्था की योजना बनानी चाहिए, जब जटिलताओं का जोखिम सबसे कम होता है। यदि गर्भावस्था की योजना बनाई गई है, तो इसे रद्द करने की सिफारिश की जाती है
इष्टतम मुआवजा प्राप्त करने के कई महीनों बाद रिसेप्शन। गर्भावस्था की योजना बनाने में बाधाएं प्रगतिशील गुर्दे की विफलता के साथ गंभीर नेफ्रोपैथी, गंभीर इस्केमिक हृदय रोग, गंभीर प्रोलिफेरेटिव रेटिनोपैथी जिसे ठीक नहीं किया जा सकता है, प्रारंभिक गर्भावस्था में केटोएसिडोसिस (कीटोन बॉडी टेराटोजेनिक कारक हैं) हैं।
उपचार का उद्देश्यगर्भावस्था के दौरान जीडीएम और सच्चा मधुमेह निम्नलिखित प्रयोगशाला मापदंडों की उपलब्धि है:
उपवास ग्लाइसेमिया< 5-5,8 ммоль/л;
खाने के 1 घंटे बाद ग्लाइसेमिया< 7,8 ммоль/л;
खाने के 2 घंटे बाद ग्लाइसेमिया< 6,7 ммоль/л;
औसत दैनिक ग्लाइसेमिक प्रोफ़ाइल< 5,5 ммоль/л;
मासिक निगरानी के साथ HbA1c का स्तर स्वस्थ लोगों (4-6%) के समान है।
टाइप 1 मधुमेह के साथ-साथ गर्भावस्था के बाहर भी, एक महिला को गहन इंसुलिन थेरेपी मिलनी चाहिए, हालांकि, गर्भावस्था के दौरान ग्लाइसेमिया के स्तर का दिन में 7-8 बार आकलन करने की सिफारिश की जाती है। यदि पारंपरिक इंजेक्शन के साथ नॉर्मोग्लाइसेमिक क्षतिपूर्ति प्राप्त करना असंभव है, तो रोगी को इंसुलिन डिस्पेंसर का उपयोग करके इंसुलिन थेरेपी में स्थानांतरित करने पर विचार करना आवश्यक है।
पहले चरण में जीडीएम का उपचारआहार चिकित्सा निर्धारित की जाती है, जिसमें दैनिक कैलोरी सेवन को वास्तविक वजन के लगभग 25 किलो कैलोरी/किलोग्राम तक सीमित करना शामिल है, मुख्य रूप से आसानी से पचने योग्य कार्बोहाइड्रेट और पशु मूल के वसा के साथ-साथ शारीरिक गतिविधि का विस्तार करना। यदि आहार चिकित्सा उपचार के लक्ष्यों को प्राप्त करने में विफल रहती है, तो रोगी को गहन इंसुलिन थेरेपी निर्धारित की जानी चाहिए। गर्भावस्था के दौरान ग्लूकोज कम करने वाली कोई भी गोली (टीडीएल)। विपरीत।यह पता चला है कि लगभग 15% महिलाओं को इंसुलिन थेरेपी पर स्विच करने की आवश्यकता है।
पूर्वानुमान
गर्भावस्था के दौरान जीडीएम और मधुमेह के असंतोषजनक मुआवजे के साथ, भ्रूण में विभिन्न विकृति विकसित होने की संभावना 30% है (जोखिम सामान्य आबादी की तुलना में 12 गुना अधिक है)। गर्भावस्था के दौरान जीडीएम का निदान करने वाली 50% से अधिक महिलाओं में अगले 15 वर्षों में टी2डीएम विकसित होगा।
"मधुमेह" शब्द ग्रीक "आई लीक" से आया है; प्राचीन समय में यह माना जाता था कि इस बीमारी के दौरान शरीर में प्रवेश करने वाला तरल बिना अवशोषित हुए शरीर से गुजर जाता है। डायबिटीज इन्सिपिडस एक दुर्लभ पुरानी विकृति है जो पूरी तरह से प्राचीन परिभाषा से मेल खाती है। इसका कारण एक हार्मोन की कमी है जो किडनी द्वारा पानी के उत्सर्जन को नियंत्रित करता है। परिणामस्वरूप, मूत्र उत्पादन कई गुना बढ़ जाता है, जिससे व्यक्ति व्यावहारिक रूप से सामान्य जीवन से वंचित हो जाता है।
रोगी को लगातार प्यास लगती है और निर्जलीकरण को रोकने के लिए उसे कई लीटर तरल पदार्थ पीने के लिए मजबूर किया जाता है। डायबिटीज मेलिटस के विपरीत, डायबिटीज इन्सिपिडस रक्त शर्करा में वृद्धि नहीं करता है, अग्न्याशय के प्रदर्शन से जुड़ा नहीं है, और विशिष्ट मधुमेह संबंधी जटिलताओं का कारण नहीं बनता है। इन दोनों रोगों में एक ही सामान्य लक्षण है - गंभीर बहुमूत्रता।
डायबिटीज इन्सिपिडस - यह क्या है?
हमारी किडनी में प्रवेश करने वाला सारा तरल पदार्थ मूत्र नहीं बनता है। प्राथमिक मूत्र की लगभग पूरी मात्रा, निस्पंदन के बाद, वृक्क नलिकाओं के माध्यम से वापस रक्त में अवशोषित हो जाती है, इस प्रक्रिया को पुनर्अवशोषण कहा जाता है। गुर्दे स्वयं से जो 150 लीटर पानी प्रवाहित करते हैं, उसमें से केवल 1% ही सांद्रित द्वितीयक मूत्र के रूप में उत्सर्जित होता है। पुनर्अवशोषण एक्वापोरिन के कारण संभव है - प्रोटीन पदार्थ जो कोशिका झिल्ली में छिद्र बनाते हैं। गुर्दे में स्थित एक प्रकार का एक्वापोरिन, वैसोप्रेसिन की उपस्थिति में ही अपना कार्य करता है।
वैसोप्रेसिन एक हार्मोन है जो हाइपोथैलेमस (मस्तिष्क का एक हिस्सा) में संश्लेषित होता है और पिट्यूटरी ग्रंथि (मस्तिष्क के निचले भाग में स्थित एक विशेष ग्रंथि) में संग्रहीत होता है। इसका मुख्य कार्य जल चयापचय को विनियमित करना है। यदि रक्त घनत्व बढ़ जाता है या शरीर में पर्याप्त तरल पदार्थ नहीं है, तो वैसोप्रेसिन का स्राव बढ़ जाता है।
यदि किसी कारण से हार्मोन का संश्लेषण कम हो जाता है, या गुर्दे की कोशिकाएं वैसोप्रेसिन का अनुभव नहीं करती हैं, तो डायबिटीज इन्सिपिडस विकसित होता है। इसका पहला लक्षण है बहुमूत्र, अधिक पेशाब आना। गुर्दे प्रतिदिन 20 लीटर तक तरल पदार्थ उत्सर्जित कर सकते हैं। रोगी लगातार पानी पीता रहता है और पेशाब करता रहता है। जीवन की यह लय व्यक्ति को थका देती है और उसके जीवन की गुणवत्ता को काफी खराब कर देती है। इस बीमारी का दूसरा नाम डायबिटीज इन्सिपिडस है। डायबिटीज इन्सिपिडस से पीड़ित लोगों को विकलांगता समूह 3, मुफ्त उपचार और निर्धारित दवाएं प्राप्त करने का अवसर मिलता है।
यह बीमारी दुर्लभ है, जो 10 लाख में से 2-3 लोगों को प्रभावित करती है। अधिकतर, यह बीमारी वयस्कता में शुरू होती है, 25 से 40 साल की उम्र में - प्रति 10 लाख जनसंख्या पर 6 लोग। बच्चों में डायबिटीज इन्सिपिडस बहुत कम विकसित होता है।
एनडी के विभिन्न रूप और प्रकार क्या हैं?
पॉल्यूरिया के कारण के आधार पर, डायबिटीज इन्सिपिडस को रूपों में विभाजित किया गया है:
- सेंट्रल डायबिटीज इन्सिपिडस- तब शुरू होता है जब मस्तिष्क क्षतिग्रस्त हो जाता है और रक्तप्रवाह में वैसोप्रेसिन का निकलना बंद हो जाता है। यह रूप न्यूरोसर्जरी, चोट, ट्यूमर, मेनिनजाइटिस और मस्तिष्क की अन्य सूजन के बाद विकसित हो सकता है। बच्चों में, केंद्रीय रूप अक्सर तीव्र या दीर्घकालिक संक्रमण या आनुवंशिक विकारों का परिणाम होता है। रोगियों में गंभीर लक्षण तब प्रकट होते हैं जब हाइपोथैलेमिक नाभिक का लगभग 80% कार्य करना बंद कर देता है; इससे पहले, हार्मोन संश्लेषण का कार्य अप्रभावित क्षेत्रों द्वारा ले लिया जाता है।
- नेफ्रोजेनिक डायबिटीज इन्सिपिडस- तब विकसित होता है जब गुर्दे की नलिकाओं में रिसेप्टर्स वैसोप्रेसिन पर प्रतिक्रिया करना बंद कर देते हैं। मधुमेह के इस रूप में, मूत्र आमतौर पर केंद्रीय मधुमेह की तुलना में कम बनता है। गुर्दे में इस तरह के विकार मूत्र के रुकने, सिस्टिक संरचनाओं और ट्यूमर और दीर्घकालिक सूजन प्रक्रिया के कारण हो सकते हैं। रीनल डायबिटीज इन्सिपिडस का एक जन्मजात रूप भी होता है, जो भ्रूण में गुर्दे की विकृतियों के कारण होता है।
- इडियोपैथिक डायबिटीज इन्सिपिडस- निदान अक्सर अपर्याप्त वैसोप्रेसिन होने पर किया जाता है, लेकिन इस समय इसकी कमी का कारण पहचाना नहीं जा सकता है। यह आमतौर पर एक छोटा ट्यूमर होता है। जैसे-जैसे यह बढ़ता है, आधुनिक दृश्य विधियों का उपयोग करके गठन का पता लगाया जाता है: एमआरआई या सीटी। हार्मोन का स्तर ऊंचा होने पर इडियोपैथिक डायबिटीज इन्सिपिडस का भी निदान किया जा सकता है, लेकिन किडनी में होने वाले बदलावों का पता नहीं लगाया जा सकता है। इसे आमतौर पर जीन उत्परिवर्तन द्वारा समझाया जाता है। लक्षण केवल पुरुषों में ही देखे जाते हैं। महिलाएं क्षतिग्रस्त जीन की वाहक होती हैं; उनमें रोग के लक्षण केवल प्रयोगशाला विधियों द्वारा ही पता लगाए जा सकते हैं; कोई स्पष्ट बहुमूत्रता नहीं होती है।
- गर्भावधि मधुमेह इन्सिपिडस- केवल गर्भवती महिलाओं में ही संभव है, क्योंकि इसका कारण प्लेसेंटा द्वारा संश्लेषित हार्मोन वैसोप्रेसिनेज़ है, जो वैसोप्रेसिन को नष्ट कर देता है। बीमारी का यह रूप बच्चे के जन्म के तुरंत बाद गायब हो जाता है - इस बारे में हमारा लेख।
रक्त में वैसोप्रेसिन की उपस्थिति के अलावा, डायबिटीज इन्सिपिडस को अन्य मानदंडों के अनुसार वर्गीकृत किया जाता है:
| वर्गीकरण मानदंड | मधुमेह के प्रकार | विशेषता |
| समय शुरू | जन्मजात | दुर्लभ रूप से देखा गया, आमतौर पर नेफ्रोजेनिक। |
| अधिग्रहीत | जीवन के दौरान अन्य बीमारियों या चोटों के कारण हुआ। | |
| निदान पर मधुमेह की गंभीरता | आसान | पॉल्यूरिया प्रति दिन 8 लीटर तक। |
| औसत | 8-14 ली | |
| भारी | > 14 ली | |
| इलाज शुरू होने के बाद मरीज की हालत | मुआवज़ा | बहुमूत्रता नहीं होती. |
| उपमुआवजा | दिन में कई बार मूत्र उत्पादन और प्यास बढ़ जाती है। | |
| क्षति | उपचार के बाद बहुमूत्रता का बने रहना। |
एनडी के विकास के कारण
मधुमेह का केंद्रीय रूप निम्नलिखित स्थितियों में विकसित हो सकता है:
- हाइपोथैलेमस और पिट्यूटरी ग्रंथि की चोटें - इन क्षेत्रों को नुकसान, आस-पास के क्षेत्र में सूजन, अन्य ऊतकों द्वारा संपीड़न;
- मस्तिष्क में ट्यूमर और मेटास्टेस;
- हाइपोथैलेमस और पिट्यूटरी ग्रंथि के करीब मस्तिष्क संरचनाओं में सर्जिकल या रेडियोथेराप्यूटिक हस्तक्षेप के परिणामस्वरूप। इस तरह के ऑपरेशन मरीज की जान बचाते हैं, लेकिन दुर्लभ मामलों में (डायबिटीज इन्सिपिडस की कुल घटनाओं का 20%) वे हार्मोन के उत्पादन को प्रभावित करते हैं। स्व-उपचार मधुमेह के मामले हैं, जो सर्जरी के तुरंत बाद शुरू होता है और कुछ दिनों में ठीक हो जाता है;
- मस्तिष्क ट्यूमर के इलाज के लिए दी जाने वाली विकिरण चिकित्सा;
- घनास्त्रता, धमनीविस्फार या स्ट्रोक के परिणामस्वरूप सिर की वाहिकाओं में संचार संबंधी विकार;
- न्यूरोसंक्रामक रोग - एन्सेफलाइटिस, मेनिनजाइटिस;
- तीव्र संक्रमण - काली खांसी, इन्फ्लूएंजा, चिकनपॉक्स। बच्चों में संक्रामक रोग वयस्कों की तुलना में अधिक बार डायबिटीज इन्सिपिडस का कारण बनते हैं। यह बचपन में मस्तिष्क की शारीरिक रचना की ख़ासियत के कारण है: नई वाहिकाओं का तेजी से विकास, मौजूदा जहाजों की पारगम्यता, और अपूर्ण रूप से गठित रक्त-मस्तिष्क बाधा;
- फुफ्फुसीय ग्रैनुलोमैटोसिस, तपेदिक;
- क्लोनिडाइन लेना;
- जन्मजात दोष - माइक्रोसेफली, मस्तिष्क के कुछ हिस्सों का अविकसित होना;
- अंतर्गर्भाशयी संक्रमण द्वारा हाइपोथैलेमस को क्षति। इस मामले में मधुमेह के लक्षण तनाव, चोट या हार्मोनल परिवर्तन के कारण वर्षों बाद दिखाई दे सकते हैं।
- एक जीन दोष जो वैसोप्रेसिन संश्लेषण को असंभव बना देता है;
- वोल्फ्राम सिंड्रोम एक जटिल वंशानुगत विकार है जिसमें मधुमेह मेलिटस और मधुमेह इंसिपिडस, खराब दृष्टि और सुनवाई शामिल है।

नेफ्रोजेनिक मधुमेह के संभावित कारण:
- क्रोनिक किडनी रोग, पॉलीसिस्टिक रोग, यूरोलिथियासिस के कारण गुर्दे की विफलता का विकास;
- गुर्दे के ऊतकों में अमाइलॉइड के जमाव के साथ प्रोटीन चयापचय में गड़बड़ी;
- मायलोमा या गुर्दे का सार्कोमा;
- गुर्दे में वैसोप्रेसिन के लिए रिसेप्टर्स की आनुवंशिक हीनता;
- कुछ दवाओं के गुर्दे पर विषाक्त प्रभाव:
डायबिटीज इन्सिपिडस के लक्षण
किसी भी रूप में डायबिटीज इन्सिपिडस का पहला संकेत पेशाब में तेजी से वृद्धि (4 लीटर से) है, जो रात में नहीं रुकता है। रोगी सामान्य नींद से वंचित हो जाता है, और धीरे-धीरे तंत्रिका संबंधी थकावट विकसित होने लगती है। बच्चों में, रात्रि और फिर दिन के समय स्फूर्ति शुरू हो जाती है। मूत्र साफ है, लगभग बिना नमक के, इसका हिस्सा आधा लीटर से बड़ा है। उपचार के बिना, मूत्र की इतनी मात्रा के कारण, गुर्दे की श्रोणि और मूत्राशय धीरे-धीरे फैलते हैं।
शरीर से तरल पदार्थ के निष्कासन के जवाब में, गंभीर प्यास शुरू हो जाती है; मरीज़ कई लीटर पानी पीते हैं। आमतौर पर बहुत ठंडे पेय को प्राथमिकता दी जाती है, क्योंकि गर्म पेय अधिक प्यास बुझाते हैं। पाचन क्रिया ख़राब हो जाती है, पेट खिंच जाता है और सिकुड़ जाता है तथा आंतों में जलन होने लगती है।
सबसे पहले, पिया गया पानी शरीर में इसकी कमी को पूरा करने के लिए पर्याप्त होता है, फिर धीरे-धीरे निर्जलीकरण शुरू हो जाता है। इसके लक्षण थकान, सिरदर्द और चक्कर आना, निम्न रक्तचाप, अतालता हैं। डायबिटीज इन्सिपिडस के रोगी में लार की मात्रा कम हो जाती है, त्वचा सूख जाती है और आंसू द्रव का स्राव नहीं होता है।
पुरुषों में लक्षण - महिलाओं में मासिक धर्म का न आना, बच्चों में शारीरिक और बौद्धिक विकास में देरी।
निदान और परीक्षा
पॉल्यूरिया के सभी रोगियों को डायबिटीज इन्सिपिडस की जांच करानी चाहिए। निदान प्रक्रिया:
- इतिहास लेना - रोगी से बीमारी की अवधि, उत्सर्जित मूत्र की मात्रा, अन्य लक्षण, करीबी रिश्तेदारों में डायबिटीज इन्सिपिडस के मामले, पिछले ऑपरेशन या मस्तिष्क की चोटों के बारे में पूछना। प्यास की प्रकृति का निर्धारण: यदि यह रात में अनुपस्थित है या जब रोगी किसी दिलचस्प गतिविधि में व्यस्त है, तो पॉल्यूरिया का कारण डायबिटीज इन्सिपिडस नहीं, बल्कि साइकोजेनिक पॉलीडिप्सिया हो सकता है।
- मधुमेह मेलेटस को बाहर करने के लिए रक्त शर्करा का निर्धारण - और इसे सही तरीके से कैसे करें।
- इसके घनत्व और परासारिता की गणना के साथ मूत्र विश्लेषण। 1005 से कम घनत्व और 300 से कम ऑस्मोलैरिटी डायबिटीज इन्सिपिडस के पक्ष में बोलते हैं।
- जल अभाव परीक्षण - रोगी को 8 घंटे तक किसी भी पेय और तरल भोजन से वंचित रखा जाता है। इस पूरे समय वह डॉक्टरों की निगरानी में हैं। यदि खतरनाक निर्जलीकरण होता है, तो परीक्षण जल्दी रोक दिया जाता है। डायबिटीज इन्सिपिडस की पुष्टि तब मानी जाती है जब इस दौरान रोगी का वजन 5% या उससे अधिक कम हो गया हो, और मूत्र परासरणता और घनत्व में वृद्धि नहीं हुई हो।
- रोग के रूप को निर्धारित करने के लिए परीक्षण के तुरंत बाद रक्त में वैसोप्रेसिन की मात्रा का विश्लेषण किया जाता है। केंद्रीय मधुमेह में इसका स्तर कम रहता है, नेफ्रोजेनिक रूप में यह बहुत बढ़ जाता है।
- यदि केंद्रीय मधुमेह में मस्तिष्क में ट्यूमर का पता चलने का संदेह हो तो एमआरआई करें।
- नेफ्रोजेनिक रूप की उच्च संभावना के साथ गुर्दे का अल्ट्रासाउंड।
- संदिग्ध वंशानुगत मधुमेह के लिए आनुवंशिक जांच।
डायबिटीज इन्सिपिडस का उपचार
बीमारी के कारण की पहचान करने के बाद, डॉक्टरों के सभी प्रयासों का उद्देश्य इसे खत्म करना है: ट्यूमर को हटाना, गुर्दे में सूजन से राहत देना। यदि केंद्रीय रूप की पहचान की जाती है, और संभावित कारण के उपचार के बाद मधुमेह बंद नहीं होता है, तो प्रतिस्थापन चिकित्सा निर्धारित की जाती है। इसमें रक्त में रोगी में गायब हार्मोन का एक सिंथेटिक एनालॉग पेश करना शामिल है - डेस्पोप्रेसिन (गोलियाँ मिनिरिन, नूरेम, नेटिवा)। स्वयं के वैसोप्रेसिन के संश्लेषण की उपस्थिति और इसकी आवश्यकता के आधार पर खुराक का चयन व्यक्तिगत रूप से किया जाता है। यदि डायबिटीज इन्सिपिडस के लक्षण गायब हो जाएं तो खुराक को पर्याप्त माना जाता है।

जब आपका स्वयं का हार्मोन उत्पादित होता है लेकिन पर्याप्त नहीं होता है, तो क्लोफाइब्रेट, कार्बामाज़ेपाइन या क्लोरप्रोपामाइड निर्धारित किया जा सकता है। कुछ रोगियों में वे वैसोप्रेसिन संश्लेषण में वृद्धि का कारण बन सकते हैं। बच्चों के लिए, इन दवाओं में से केवल क्लोरप्रोपामाइड की अनुमति है, लेकिन इसका उपयोग करते समय, रक्त शर्करा को नियंत्रित करना आवश्यक है, क्योंकि इसमें हाइपोग्लाइसेमिक प्रभाव होता है।
नेफ्रोजेनिक मधुमेह के लिए कोई सिद्ध प्रभावी उपचार नहीं हैं। थियाज़ाइड्स समूह के मूत्रवर्धक द्रव हानि को 25-50% तक कम कर सकते हैं। डायबिटीज इन्सिपिडस में, वे स्वस्थ लोगों की तरह मूत्र उत्सर्जन को उत्तेजित नहीं करते हैं, बल्कि, इसके विपरीत, इसके पुनर्अवशोषण को बढ़ाते हैं।
दवाओं के अलावा, मरीजों को सीमित मात्रा में प्रोटीन वाला आहार दिया जाता है ताकि किडनी पर अधिक भार न पड़े। निर्जलीकरण को रोकने के लिए, आपको धुले हुए विटामिन और सूक्ष्म तत्वों को बहाल करने के लिए पर्याप्त तरल पदार्थ, अधिमानतः जूस या कॉम्पोट्स पीने की ज़रूरत है।
यदि उपचार ने डायबिटीज इन्सिपिडस के मुआवजे के चरण तक पहुंचने में मदद की है, तो रोगी काम करने की क्षमता बनाए रखते हुए सामान्य जीवन जी सकता है। यदि रोग का कारण समाप्त हो गया है तो पूर्ण पुनर्प्राप्ति संभव है। अक्सर, मधुमेह गायब हो जाता है यदि यह चोट, ट्यूमर और सर्जरी के कारण हुआ हो। अन्य मामलों में, रोगियों को आजीवन उपचार की आवश्यकता होती है।
मधुमेह मेलिटस का संदेह करने वाले प्रमुख लक्षणों में से एक लगातार प्यास और अत्यधिक पेशाब है, जो प्रति दिन 5 और 10 लीटर तक पहुंच सकता है।
यही लक्षण डायबिटीज इन्सिपिडस या डायबिटीज इन्सिपिडस के साथ भी देखे जाते हैं। यह दुर्लभ बीमारी एंटीडाययूरेटिक हार्मोन वैसोप्रेसिन की कमी से जुड़ी है।
वैसोप्रेसिन को कम मात्रा में संश्लेषित किया जा सकता है, या गुर्दे में रिसेप्टर्स अब इस पर प्रतिक्रिया नहीं कर सकते हैं। इसके अलावा, दवाएँ लेने पर, गर्भावस्था के दूसरे या अंतिम तिमाही में, एक वर्ष से कम उम्र के बच्चों में डायबिटीज इन्सिपिडस विकसित हो सकता है। केंद्रीय और वृक्क रूपों के विपरीत, बाद के रूपों में अनुकूल पूर्वानुमान और हल्का कोर्स होता है।
डायबिटीज इन्सिपिडस का विकास: कारण और तंत्र
प्राथमिक मूत्र से द्रव को रक्त में वापस लाने के लिए वैसोप्रेसिन की आवश्यकता होती है। यह मानव शरीर का एकमात्र हार्मोन है जो ऐसा कार्य कर सकता है। यदि यह काम नहीं करता है, तो एक गंभीर चयापचय विकार विकसित हो जाएगा - डायबिटीज इन्सिपिडस।
वैसोप्रेसिन का उत्पादन हाइपोथैलेमस के न्यूरॉन्स में होता है - सुप्राऑप्टिक न्यूक्लियस में। फिर यह न्यूरॉन्स की प्रक्रियाओं के साथ पिट्यूटरी ग्रंथि में प्रवेश करता है, जहां यह जमा होता है और रक्त में छोड़ दिया जाता है। इसके जारी होने का संकेत प्लाज्मा ऑस्मोलैरिटी (एकाग्रता) में वृद्धि और परिसंचारी रक्त की मात्रा में कमी है।
ऑस्मोलैरिटी सभी घुले हुए लवणों की सांद्रता को दर्शाती है। आम तौर पर, यह 280 से 300 mOsm/l तक होता है। इस मामले में, शरीर शारीरिक स्थितियों के तहत काम करता है। यदि यह बढ़ता है, तो हाइपोथैलेमस, यकृत और मस्तिष्क के तीसरे वेंट्रिकल की दीवार में रिसेप्टर्स मूत्र से तरल पदार्थ लेकर उसे बनाए रखने की आवश्यकता के बारे में संकेत भेजते हैं।
यदि परिसंचारी रक्त की मात्रा सामान्य से कम है, तो पिट्यूटरी ग्रंथि अटरिया और छाती के अंदर स्थित नसों में वॉल्यूम रिसेप्टर्स से समान संकेत प्राप्त करती है। सामान्य मात्रा बनाए रखने से ऊतकों को पोषक तत्व और ऑक्सीजन की आपूर्ति हो पाती है। जब रक्त की मात्रा कम हो जाती है, तो वाहिकाओं में दबाव कम हो जाता है और माइक्रोसिरिक्युलेशन बाधित हो जाता है।
तरल पदार्थ की कमी और अतिरिक्त नमक के परिणामों को खत्म करने के लिए वैसोप्रेसिन जारी किया जाता है। एंटीडाययूरेटिक हार्मोन के स्तर में वृद्धि निम्नलिखित कारणों से होती है: चोट के दौरान दर्द का झटका, खून की कमी, निर्जलीकरण, मनोविकृति।
वैसोप्रेसिन की क्रिया निम्नलिखित दिशाओं में होती है:
- मूत्र उत्पादन कम हो जाता है।
- मूत्र से पानी रक्त में प्रवेश करता है, जिससे इसकी मात्रा बढ़ जाती है।
- सोडियम और क्लोरीन के स्तर सहित, प्लाज्मा ऑस्मोलैरिटी कम हो जाती है।
- चिकनी मांसपेशियों की टोन बढ़ती है, खासकर पाचन तंत्र और रक्त वाहिकाओं में।
- धमनियों में दबाव बढ़ जाता है और वे एड्रेनालाईन और नॉरपेनेफ्रिन के प्रति अधिक संवेदनशील हो जाती हैं।
- खून बहना बंद हो जाता है.
इसके अलावा, वैसोप्रेसिन मानव व्यवहार को प्रभावित करता है, आंशिक रूप से सामाजिक व्यवहार, आक्रामक प्रतिक्रियाओं और पिता में बच्चों के लिए प्यार का निर्धारण करता है।
यदि हार्मोन रक्त में प्रवेश करना बंद कर देता है या उसके प्रति संवेदनशीलता खत्म हो जाती है, तो डायबिटीज इन्सिपिडस विकसित हो जाता है।
डायबिटीज इन्सिपिडस के रूप
शर्करा स्तर
 केंद्रीय प्रकार का डायबिटीज इन्सिपिडस चोटों और मस्तिष्क ट्यूमर के साथ-साथ हाइपोथैलेमस या पिट्यूटरी ग्रंथि को खराब रक्त आपूर्ति के साथ विकसित होता है। अक्सर बीमारी की घटना न्यूरोइन्फेक्शन से जुड़ी होती है।
केंद्रीय प्रकार का डायबिटीज इन्सिपिडस चोटों और मस्तिष्क ट्यूमर के साथ-साथ हाइपोथैलेमस या पिट्यूटरी ग्रंथि को खराब रक्त आपूर्ति के साथ विकसित होता है। अक्सर बीमारी की घटना न्यूरोइन्फेक्शन से जुड़ी होती है।
पिट्यूटरी एडेनोमा का सर्जिकल उपचार या उपचार के दौरान विकिरण मधुमेह इन्सिपिडस के लक्षणों के विकास का कारण बन सकता है। जेनेटिक वोल्फ्राम सिंड्रोम वैसोप्रेसिन के अपर्याप्त उत्पादन के साथ होता है, जो इस विकृति की घटना को उत्तेजित करता है।
जब कारण स्थापित करना मुश्किल होता है, जो कि डायबिटीज इन्सिपिडस के केंद्रीय रूप वाले सभी रोगियों के एक महत्वपूर्ण अनुपात में देखा जाता है, तो रोग के इस प्रकार को इडियोपैथिक कहा जाता है।
गुर्दे के रूप में, वैसोप्रेसिन के रिसेप्टर्स रक्त में इसकी उपस्थिति पर प्रतिक्रिया नहीं करते हैं। ऐसा निम्नलिखित कारणों से हो सकता है:
- रिसेप्टर संरचना का जन्मजात विकार।
- किडनी खराब।
- प्लाज्मा की आयन संरचना में गड़बड़ी।
- लिथियम दवाएँ लेना।
- अंतिम चरणों में मधुमेह संबंधी नेफ्रोपैथी।
गर्भवती महिलाओं में डायबिटीज इन्सिपिडस को क्षणिक (पासिंग) के रूप में वर्गीकृत किया गया है, यह इस तथ्य से जुड़ा है कि प्लेसेंटा द्वारा उत्पादित एंजाइम वैसोप्रेसिन को नष्ट कर देते हैं। बच्चे के जन्म के बाद, गर्भकालीन मधुमेह इन्सिपिडस दूर हो जाता है।
इसके अलावा, जीवन के पहले वर्ष में बच्चे क्षणिक मधुमेह इन्सिपिडस से पीड़ित होते हैं, जो पिट्यूटरी ग्रंथि और हाइपोथैलेमस के गठन से जुड़ा होता है।
रोग की गंभीरता और जल-इलेक्ट्रोलाइट चयापचय में गड़बड़ी का स्तर शरीर के निर्जलीकरण की डिग्री पर निर्भर करता है। डायबिटीज इन्सिपिडस के निम्नलिखित रूप हैं:
- गंभीर - प्रति दिन 14 लीटर पेशाब।
- औसत - प्रति दिन 8 से 14 लीटर तक मूत्राधिक्य।
- हल्के - मरीज़ प्रति दिन 8 लीटर तक मलत्याग करते हैं।
- यदि आप प्रतिदिन 4 लीटर से कम वजन कम करते हैं - आंशिक (आंशिक) डायबिटीज इन्सिपिडस।
बच्चों और गर्भवती महिलाओं में क्षणिक मधुमेह अक्सर हल्के रूप में होता है। दवाएँ लेते समय (आईट्रोजेनिक) - मध्यम गंभीरता। केंद्रीय और वृक्क रूपों में, डायबिटीज इन्सिपिडस का सबसे गंभीर कोर्स देखा जाता है।
डायबिटीज इन्सिपिडस को एक दुर्लभ विकृति माना जाता है। लेकिन हाल ही में, दर्दनाक मस्तिष्क की चोटों और मस्तिष्क रोगों के लिए सर्जिकल हस्तक्षेप में वृद्धि के कारण केंद्रीय रूपों में लगातार वृद्धि दर्ज की गई है।
अधिकतर, डायबिटीज इन्सिपिडस और इसके लक्षण 10 से 30 वर्ष की आयु के पुरुषों में पाए जाते हैं।
डायबिटीज इन्सिपिडस का निदान
डायबिटीज इन्सिपिडस के लक्षण बड़ी मात्रा में मूत्र उत्पन्न होने और निर्जलीकरण के विकास से जुड़े हैं। इसके अलावा, रक्त में इलेक्ट्रोलाइट्स का असंतुलन और रक्तचाप में गिरावट विकसित होती है।
गंभीरता की डिग्री रोग की गंभीरता और उसके होने के कारण से निर्धारित होती है। मधुमेह की तरह रोगियों की मुख्य शिकायत अत्यधिक प्यास, लगातार शुष्क मुँह, शुष्क, निर्जलित त्वचा और श्लेष्मा झिल्ली, साथ ही बार-बार और प्रचुर मात्रा में पेशाब आना है।
मरीज़ प्रति दिन 6 लीटर से अधिक तरल पदार्थ पी सकते हैं और उत्सर्जित मूत्र की मात्रा 10 - 20 लीटर तक बढ़ जाती है। रात्रिकालीन मूत्राधिक्य काफी बढ़ जाता है।
डायबिटीज इन्सिपिडस के विशिष्ट लक्षण हैं:
- गंभीर थकान, शक्तिहीनता.
- अनिद्रा या अधिक नींद आना।
- लार उत्पादन में कमी.
- लगातार कब्ज रहना.
- खाने के बाद पेट में भारीपन, डकारें आना।
- समुद्री बीमारी और उल्टी।
- शरीर का तापमान बढ़ना.
हृदय प्रणाली से, बिगड़ा हुआ संवहनी विनियमन के लक्षणों का एक जटिल विकास होता है - रक्तचाप में गिरावट, तेजी से नाड़ी, हृदय समारोह में रुकावट। शरीर का वजन कम हो जाता है, 4 साल की उम्र के बाद बच्चों में मूत्र असंयम विकसित हो जाता है और रोगी त्वचा की लगातार खुजली से परेशान रहते हैं।
मूत्र में इलेक्ट्रोलाइट्स की कमी के परिणामस्वरूप न्यूरोलॉजिकल लक्षण विकसित होते हैं - सिरदर्द, ऐंठन या मांसपेशियों और शरीर के अन्य हिस्सों में ऐंठन। पुरुष डायबिटीज इन्सिपिडस में कामेच्छा में कमी और स्तंभन दोष के विकास जैसी विशिष्ट अभिव्यक्ति होती है।
डायबिटीज इन्सिपिडस के निदान की पुष्टि करने के लिए, डायबिटीज इन्सिपिडस की उत्पत्ति को स्पष्ट करने के लिए प्रयोगशाला निदान और विशेष परीक्षण किए जाते हैं। रोग के गुर्दे और केंद्रीय रूपों का विभेदक निदान किया जाता है, और मधुमेह मेलेटस को भी बाहर रखा जाता है।
पहले चरण में मूत्र की मात्रा, उसके घनत्व और परासरणीयता की जांच की जाती है। डायबिटीज इन्सिपिडस की विशेषता निम्नलिखित मूल्यों से होती है:
- शरीर के प्रत्येक किलोग्राम वजन के लिए प्रतिदिन 40 मिलीलीटर से अधिक मूत्र उत्सर्जित होता है।
- मूत्र के सापेक्ष घनत्व में 1005 ग्राम/लीटर से कम कमी
- मूत्र परासरणशीलता 300 mOsm/kg से कम
डायबिटीज इन्सिपिडस के गुर्दे के रूप में, निम्नलिखित लक्षण दिखाई देते हैं: हाइपरकैल्सीमिया, हाइपरकेलेमिया, रक्त में क्रिएटिनिन में वृद्धि, गुर्दे की विफलता के लक्षण या मूत्र पथ में एक संक्रामक प्रक्रिया। मधुमेह अपवृक्कता में, नैदानिक संकेतक रक्त शर्करा में वृद्धि है।
सूखा भोजन परीक्षण करते समय, रोगियों को जल्दी ही निर्जलीकरण के लक्षण और वजन घटाने का अनुभव होता है। डेस्मोप्रेसिन के साथ परीक्षण करने पर डायबिटीज इन्सिपिडस का केंद्रीय रूप जल्दी से उलट जाता है।
यदि निदान अस्पष्ट है, तो मस्तिष्क टोमोग्राफी, साथ ही आनुवंशिक अध्ययन करना आवश्यक है।
डायबिटीज इन्सिपिडस का उपचार
डायबिटीज इन्सिपिडस के उपचार में रणनीति का चुनाव रोग के रूप पर निर्भर करता है। हाइपोथैलेमस या पिट्यूटरी ग्रंथि को नुकसान के कारण केंद्रीय रूप का इलाज करने के लिए, कृत्रिम रूप से उत्पादित वैसोप्रेसिन एनालॉग का उपयोग किया जाता है।
डेस्मोप्रेसिन पर आधारित दवा टैबलेट या नेज़ल स्प्रे के रूप में उपलब्ध है। व्यापारिक नाम: वाज़ोमिरिन, मिनिरिन, प्रेसेनेक्स और नेटिवा। यह किडनी में पानी के पुनर्अवशोषण को बढ़ावा देता है। इसलिए, इसका उपयोग करते समय, आपको केवल तभी पीना चाहिए जब आपको प्यास लगे, ताकि पानी का नशा न हो।
यदि आप डेस्मोप्रेसिन की अधिक मात्रा लेते हैं या इसका उपयोग करते समय बड़ी मात्रा में तरल का सेवन करते हैं, तो निम्नलिखित हो सकता है:
- रक्तचाप में वृद्धि.
- ऊतक शोफ का विकास.
- रक्त में सोडियम की मात्रा कम होना।
- क्षीण चेतना.
खुराक प्रति दिन 10 से 40 एमसीजी तक व्यक्तिगत रूप से चुनी जाती है। इसे एक बार लिया जा सकता है या दो खुराक में विभाजित किया जा सकता है। आमतौर पर दवा अच्छी तरह से सहन की जाती है, लेकिन सिरदर्द और चक्कर आना, आंतों में दर्द, मतली और रक्तचाप में मध्यम वृद्धि के रूप में दुष्प्रभाव संभव हैं।
डेस्मोप्रेसिन स्प्रे या ड्रॉप्स का उपयोग करते समय, आपको यह याद रखना होगा कि जब श्लेष्म झिल्ली की सूजन के कारण आपकी नाक बहती है, तो दवा का अवशोषण धीमा हो जाता है, इसलिए ऐसे मामलों में इसे जीभ के नीचे टपकाया जा सकता है।
डायबिटीज इन्सिपिडस के केंद्रीय रूप में, वैसोप्रेसिन के उत्पादन को प्रोत्साहित करने के लिए कार्बामाज़ेपाइन (फिनलेप्सिन, ज़ेप्टोल) और क्लोरोप्रोपामाइड पर आधारित दवाओं का भी उपयोग किया जाता है।
नेफ्रोजेनिक डायबिटीज इन्सिपिडस वैसोप्रेसिन पर प्रतिक्रिया करने में गुर्दे की अक्षमता से जुड़ा है, जो रक्त में पर्याप्त मात्रा में हो सकता है। हालाँकि, जब डेस्मोप्रेसिन के साथ परीक्षण किया जाता है, तो कोई प्रतिक्रिया प्रकट नहीं होती है।
इस रूप का इलाज करने के लिए, थियाजाइड मूत्रवर्धक और गैर-स्टेरायडल विरोधी भड़काऊ दवाओं का उपयोग किया जाता है - इंडोमेथेसिन, निमेसुलाइड, वोल्टेरेन। आहार में नमक की मात्रा सीमित है।
जेस्टेशनल डायबिटीज इन्सिपिडस का इलाज डेस्मोप्रेसिन दवाओं से किया जाता है; उपचार केवल गर्भावस्था के दौरान किया जाता है; बच्चे के जन्म के बाद ऐसी चिकित्सा की कोई आवश्यकता नहीं होती है।
हल्के या आंशिक मधुमेह इन्सिपिडस के लिए, निर्जलीकरण को रोकने के लिए गैर-दवा चिकित्सा का उपयोग पर्याप्त पीने के आहार के रूप में किया जा सकता है।
गुर्दे पर भार को कम करने के लिए आहार पोषण निर्धारित किया जाता है। इसके मुख्य सिद्धांत:
- प्रोटीन को सीमित करना, विशेषकर मांस को।
- पर्याप्त मात्रा में वसा और कार्बोहाइड्रेट.
- बार-बार छोटे भोजन करना।
- ताजी सब्जियों और फलों का समावेश।
- अपनी प्यास बुझाने के लिए फलों के पेय, जूस या कॉम्पोट्स का उपयोग करें।
उपचार की प्रभावशीलता का आकलन रोगियों की भलाई और उत्सर्जित मूत्र की मात्रा में कमी से किया जाता है।
डायबिटीज इन्सिपिडस किडनी द्वारा तरल पदार्थ के खराब अवशोषण से जुड़ी एक काफी दुर्लभ बीमारी है। इस बीमारी को मधुमेह भी कहा जाता है, क्योंकि इसके विकास से यह तथ्य सामने आता है कि मूत्र केंद्रित होना बंद हो जाता है और बड़ी मात्रा में पतला होकर शरीर से बाहर निकल जाता है।इसी तरह की बीमारी जानवरों में होती है, अक्सर कुत्तों और लोगों में, और किसी भी उम्र में। स्वाभाविक रूप से, गुर्दे की इतनी गंभीर खराबी पूरे शरीर की कार्यक्षमता पर नकारात्मक प्रभाव डालती है। रोग कैसे प्रकट होता है और इसका इलाज कैसे होता है?
यह क्या है?
डायबिटीज इन्सिपिडस हाइपोथैलेमस या पिट्यूटरी ग्रंथि की शिथिलता से जुड़ी एक दुर्लभ बीमारी (प्रति 100,000 में लगभग 3) है, जो पॉल्यूरिया (प्रति दिन 6-15 लीटर मूत्र का उत्सर्जन) और पॉलीडिप्सिया (प्यास) की विशेषता है।
यह दोनों लिंगों, वयस्कों और बच्चों दोनों में होता है। अक्सर, युवा लोग - 18 से 25 वर्ष की आयु तक - बीमार पड़ते हैं। जीवन के पहले वर्ष में बच्चों में बीमारी के ज्ञात मामले हैं (ए.डी. अर्बुज़ोव, 1959, शारापोव वी.एस. 1992)।
डायबिटीज इन्सिपिडस के कारण
डायबिटीज इन्सिपिडस एक विकृति है जो वैसोप्रेसिन की कमी, इसकी पूर्ण या सापेक्ष कमी के कारण होती है। वैसोप्रेसिन (एंटीडाययूरेटिक हार्मोन) हाइपोथैलेमस में स्रावित होता है और अन्य कार्यों के अलावा, पेशाब की प्रक्रिया को सामान्य करने के लिए जिम्मेदार होता है। उत्पत्ति के कारणों के अनुसार, इस बीमारी के तीन प्रकारों को अलग करने की प्रथा है: आनुवंशिक, अधिग्रहित, अज्ञातहेतुक।
इस दुर्लभ बीमारी वाले अधिकांश रोगियों के लिए, इसका कारण अभी भी अज्ञात है। इस प्रकार के मधुमेह को इडियोपैथिक कहा जाता है और यह 70 प्रतिशत रोगियों को प्रभावित करता है। आनुवंशिक एक वंशानुगत कारक है। इस मामले में, डायबिटीज इन्सिपिडस कभी-कभी परिवार के कई सदस्यों और कई पीढ़ियों को प्रभावित करता है।
दवा इसे जीनोटाइप में गंभीर परिवर्तनों द्वारा समझाती है, जो एंटीडाययूरेटिक हार्मोन के कामकाज में गड़बड़ी की घटना में योगदान करती है। इस बीमारी की वंशानुगत प्रकृति को डाइएनसेफेलॉन और मिडब्रेन की संरचना में जन्मजात दोष द्वारा समझाया गया है।
डायबिटीज इन्सिपिडस के कारणों पर विचार करते समय, इसके विकास के तंत्र को ध्यान में रखा जाना चाहिए:
1) सेंट्रल डायबिटीज इन्सिपिडस - तब होता है जब हाइपोथैलेमस में वैसोप्रेसिन का अपर्याप्त स्राव होता है या जब पिट्यूटरी ग्रंथि से रक्त में इसकी रिहाई बाधित होती है, संभवतः इसके कारण हैं:
- हाइपोथैलेमस की विकृति, चूंकि यह मूत्र उत्सर्जन के नियमन और एंटीडाययूरेटिक हार्मोन के संश्लेषण के लिए जिम्मेदार है, इसके कामकाज में व्यवधान से यह रोग होता है। हाइपोथैलेमस की शिथिलता के कारण और उत्तेजक कारक तीव्र या पुरानी संक्रामक रोग हो सकते हैं: गले में खराश, इन्फ्लूएंजा, यौन संचारित रोग, तपेदिक।
- मस्तिष्क पर सर्जिकल हस्तक्षेप और मस्तिष्क की सूजन संबंधी विकृति।
- आघात, दर्दनाक मस्तिष्क की चोट।
- स्व - प्रतिरक्षित रोग।
- सिस्टिक, अपक्षयी, सूजन संबंधी गुर्दे के घाव जो वैसोप्रेसिन धारणा को ख़राब करते हैं।
- हाइपोथैलेमस और पिट्यूटरी ग्रंथि की ट्यूमर प्रक्रियाएं।
- इसके अलावा, उच्च रक्तचाप की उपस्थिति डायबिटीज इन्सिपिडस के दौरान गंभीर कारकों में से एक है।
- हाइपोथैलेमस-पिट्यूटरी प्रणाली के संवहनी घाव, जिससे हाइपोथैलेमस और पिट्यूटरी ग्रंथि को आपूर्ति करने वाले जहाजों में मस्तिष्क परिसंचरण में समस्याएं पैदा होती हैं।
2) रीनल डायबिटीज इन्सिपिडस - इस मामले में, वैसोप्रेसिन का उत्पादन सामान्य मात्रा में होता है, लेकिन किडनी के ऊतक इस पर ठीक से प्रतिक्रिया नहीं करते हैं। कारण इस प्रकार हो सकते हैं:
- नेफ्रॉन या वृक्क मज्जा की मूत्र नलिकाओं को नुकसान;
- वंशानुगत कारक - जन्मजात विकृति विज्ञान;
- दरांती कोशिका अरक्तता;
- रक्त में पोटेशियम का बढ़ना या कैल्शियम का स्तर कम होना;
- चिरकालिक गुर्दा निष्क्रियता;
- गुर्दे की अमाइलॉइडोसिस (ऊतकों में अमाइलॉइड का जमाव) या पॉलीसिस्टिक रोग (कई सिस्ट का बनना);
- ऐसी दवाएं लेना जो गुर्दे के ऊतकों पर विषाक्त प्रभाव डाल सकती हैं (डेमेक्लोसिलिन, एम्फोटेरिसिन बी, लिथियम);
- कभी-कभी विकृति बुढ़ापे में या किसी अन्य विकृति द्वारा कमजोर होने की पृष्ठभूमि में होती है।
कभी-कभी तनाव के कारण अधिक प्यास लग सकती है (साइकोजेनिक पॉलीडिप्सिया)। या गर्भावस्था के दौरान डायबिटीज इन्सिपिडस, जो प्लेसेंटा द्वारा उत्पादित एंजाइमों द्वारा वैसोप्रेसिन के विनाश के कारण तीसरी तिमाही में विकसित होता है। मूल कारण समाप्त होने के बाद दोनों प्रकार के उल्लंघन अपने आप समाप्त हो जाते हैं।
वर्गीकरण
इस रोग के 2 नैदानिक रूपों में अंतर करने की प्रथा है:
- नेफ्रोजेनिक डायबिटीज इन्सिपिडस (परिधीय)। रोग का यह रूप वैसोप्रेसिन के जैविक प्रभावों के प्रति दूरस्थ वृक्क नलिकाओं की संवेदनशीलता में कमी या पूर्ण अनुपस्थिति का परिणाम है। एक नियम के रूप में, यह क्रोनिक किडनी पैथोलॉजी (पायलोनेफ्राइटिस के साथ या पॉलीसिस्टिक किडनी रोग की पृष्ठभूमि के खिलाफ) के मामले में देखा जाता है, रक्त में पोटेशियम सामग्री में दीर्घकालिक कमी और अपर्याप्त प्रोटीन सेवन के साथ कैल्शियम के स्तर में वृद्धि होती है। भोजन से - प्रोटीन भुखमरी, स्जोग्रेन सिंड्रोम, और कुछ जन्म दोष। कुछ मामलों में, बीमारी पारिवारिक होती है।
- न्यूरोजेनिक डायबिटीज इन्सिपिडस (केंद्रीय)। तंत्रिका तंत्र में पैथोलॉजिकल परिवर्तनों के परिणामस्वरूप विकसित होता है, विशेष रूप से हाइपोथैलेमस या पश्च पिट्यूटरी ग्रंथि में। एक नियम के रूप में, इस मामले में बीमारी का कारण पिट्यूटरी ग्रंथि को पूरी तरह या आंशिक रूप से हटाने के लिए सर्जरी, इस क्षेत्र की घुसपैठ विकृति (हेमोक्रोमैटोसिस, सारकॉइडोसिस), आघात या सूजन प्रकृति के परिवर्तन हैं। कुछ मामलों में, न्यूरोजेनिक डायबिटीज इन्सिपिडस अज्ञातहेतुक होता है, जो एक ही परिवार के कई सदस्यों में एक साथ होता है।

डायबिटीज इन्सिपिडस के लक्षण
डायबिटीज इन्सिपिडस के सबसे पहले लक्षण गंभीर, दर्दनाक प्यास (पॉलीडिप्सिया) और बार-बार अत्यधिक पेशाब (पॉलीयूरिया) हैं, जो रात में भी रोगियों को परेशान करते हैं। प्रति दिन 3 से 15 लीटर तक मूत्र निकल सकता है और कभी-कभी इसकी मात्रा 20 लीटर प्रति दिन तक पहुंच जाती है। अत: रोगी को तेज प्यास सताती है।
- पुरुषों में डायबिटीज इन्सिपिडस के लक्षण कामेच्छा और शक्ति में कमी है।
- महिलाओं में डायबिटीज इन्सिपिडस के लक्षण: एमेनोरिया तक मासिक धर्म की अनियमितता, संबंधित बांझपन, और यदि गर्भावस्था होती है, तो सहज गर्भपात का खतरा बढ़ जाता है।
- बच्चों में मधुमेह के लक्षण स्पष्ट होते हैं। नवजात शिशुओं और छोटे बच्चों में इस बीमारी की स्थिति आमतौर पर गंभीर होती है। शरीर के तापमान में वृद्धि होती है, अस्पष्ट उल्टी होती है और तंत्रिका तंत्र के विकार विकसित होते हैं। किशोरावस्था तक के बड़े बच्चों में, डायबिटीज इन्सिपिडस का एक लक्षण बिस्तर गीला करना या एन्यूरिसिस है।
बाद में, जैसे-जैसे यह बढ़ता है, निम्नलिखित लक्षण प्रकट होते हैं:
- बड़ी मात्रा में तरल पदार्थ के सेवन से पेट खिंच जाता है और कभी-कभी गिर भी जाता है;
- निर्जलीकरण (शरीर में पानी की कमी) के लक्षण दिखाई देते हैं: शुष्क त्वचा और श्लेष्मा झिल्ली (शुष्क मुँह), शरीर के वजन में कमी;
- अधिक मात्रा में मूत्र निकलने के कारण मूत्राशय में खिंचाव होता है;
- शरीर में पानी की कमी के कारण पेट और आंतों में पाचन एंजाइमों का उत्पादन बाधित होता है। इसलिए, रोगी की भूख कम हो जाती है, गैस्ट्रिटिस या कोलाइटिस विकसित होता है, और कब्ज की प्रवृत्ति होती है;
- रक्तचाप अक्सर कम हो जाता है और हृदय गति बढ़ जाती है;
- चूंकि शरीर में पर्याप्त पानी नहीं है, पसीना आना कम हो जाता है;
- रोगी जल्दी थक जाता है;
- कभी-कभी अस्पष्ट मतली और उल्टी होती है;
- शरीर का तापमान बढ़ सकता है.
- कभी-कभी बिस्तर गीला करना (एन्यूरिसिस) हो जाता है।
चूंकि रात में प्यास और अत्यधिक पेशाब जारी रहता है, इसलिए रोगी को मानसिक और भावनात्मक विकार विकसित हो जाते हैं:
- भावनात्मक विकलांगता (कभी-कभी मनोविकृति भी विकसित हो जाती है) और चिड़चिड़ापन;
- अनिद्रा और सिरदर्द;
- मानसिक गतिविधि में कमी.
ये सामान्य मामलों में डायबिटीज इन्सिपिडस के लक्षण हैं। हालाँकि, पुरुषों और महिलाओं के साथ-साथ बच्चों में भी रोग की अभिव्यक्तियाँ थोड़ी भिन्न हो सकती हैं।
निदान
विशिष्ट मामलों में, डायबिटीज इन्सिपिडस का निदान मुश्किल नहीं है और यह इस पर आधारित है:
- स्पष्ट प्यास
- दैनिक मूत्र की मात्रा प्रति दिन 3 लीटर से अधिक है
- प्लाज्मा हाइपरऑस्मोलैलिटी (290 mOsm/kg से अधिक, तरल पदार्थ के सेवन पर निर्भर करता है)
- उच्च सोडियम सामग्री
- मूत्र की हाइपोऑस्मोलैलिटी (100-200 mOsm/किग्रा)
- मूत्र का कम सापेक्ष घनत्व (<1010)
रोग का कारण निर्धारित करने के लिए, एक्स-रे, नेत्र विज्ञान और न्यूरोसाइकिएट्रिक परीक्षाओं के परिणामों का सावधानीपूर्वक विश्लेषण किया जाता है। मस्तिष्क की चुंबकीय अनुनाद इमेजिंग आवश्यक है।

डायबिटीज इन्सिपिडस का इलाज कैसे करें?
इस विकृति के लिए चिकित्सा का सफल परिणाम मुख्य कारण की सटीक पहचान करने और उसे समाप्त करने में निहित है जो वैसोप्रेसिन के उत्पादन में विफलता का कारण बनता है, उदाहरण के लिए, मधुमेह इन्सिपिडस के केंद्रीय रूप में मस्तिष्क में एक ट्यूमर या मेटास्टेस।
डायबिटीज इन्सिपिडस के लिए दवाओं का चयन उपस्थित चिकित्सक द्वारा किया जाता है; ये सभी एंटीडाययूरेटिक हार्मोन के सिंथेटिक एनालॉग हैं। दवा की कार्रवाई की अवधि के आधार पर, दवा को दिन में कई बार या हर कुछ दिनों में एक बार लिया जाना चाहिए (लंबे समय तक काम करने वाली दवाएं)।
केंद्रीय रूप के डायबिटीज इन्सिपिडस के लिए, कार्बामाज़ेपाइन या क्लोरप्रोपामाइड दवाओं का सबसे अधिक उपयोग किया जाता है - ये दवाएं वैसोप्रेसिन के उत्पादन और रिलीज को उत्तेजित करती हैं। प्रचुर मात्रा में और बार-बार पेशाब आने की पृष्ठभूमि में शरीर में पानी की कमी को रोकने के लिए, रोगी को अंतःशिरा में खारा घोल दिया जाता है।
महिलाओं में डायबिटीज इन्सिपिडस के उपचार में स्त्री रोग विशेषज्ञ के साथ अतिरिक्त परामर्श और मासिक धर्म चक्र में सुधार शामिल है।
पोषण नियम
हर कोई जानता है कि मधुमेह के रोगियों का शर्करा के साथ एक "विशेष" संबंध होता है। लेकिन अगर बीमारी शुगर इन्सिपिडस है तो पोषण के बारे में क्या कहा जा सकता है? इस मामले में, प्रतिबंध एक अन्य उत्पाद - नमक - को प्रभावित करेगा। यदि रोगी गुर्दे की विफलता से पीड़ित नहीं है, तो नमक को आहार अनुपूरक के साथ बदलना संभव है, उदाहरण के लिए, सनासोल।
इस बीमारी के लिए आहार में प्रोटीन खाद्य पदार्थों की खपत को सीमित करना शामिल है (प्रति दिन 70 ग्राम से अधिक नहीं)। रोगी को आहार तालिका क्रमांक 7 की अनुशंसा की जाती है।
आहार में निम्नलिखित खाद्य पदार्थ और पेय शामिल हैं:
- खट्टे-मीठे स्वाद वाले जामुन और फल।
- ताज़ी सब्जियां।
- ताजा निचोड़ा हुआ रस, क्वास, चाय - हर्बल और हरा।
- नींबू के रस के साथ पानी.
- किण्वित दूध उत्पाद और पेय।
- दुबले प्रकार के मांस.
- कम वसा वाली मछली और समुद्री भोजन।
पूर्वानुमान
इडियोपैथिक डायबिटीज इन्सिपिडस, पर्याप्त प्रतिस्थापन चिकित्सा के अधीन, रोगी के जीवन के लिए खतरा पैदा नहीं करता है, हालांकि, इस रूप से उबरना असंभव है।
डायबिटीज इन्सिपिडस, जो किसी अन्य बीमारी की पृष्ठभूमि पर होता है, कुछ मामलों में उस कारण के ख़त्म होने के बाद अपने आप दूर हो जाता है जिसके कारण यह हुआ है।
टाइप 1 डायबिटीज मेलिटस एक अंग-विशिष्ट ऑटोइम्यून बीमारी है जो अग्न्याशय के आइलेट्स की इंसुलिन-उत्पादक बीटा कोशिकाओं के विनाश की ओर ले जाती है, जो इंसुलिन की पूर्ण कमी से प्रकट होती है। कुछ मामलों में, प्रत्यक्ष प्रकार 1 मधुमेह वाले रोगियों में बीटा कोशिकाओं में ऑटोइम्यून क्षति के मार्करों की कमी होती है (इडियोपैथिक डायबिटीज मेलिटस टाइप 1)।
एटियलजि
टाइप 1 मधुमेह एक वंशानुगत प्रवृत्ति वाली बीमारी है, लेकिन रोग के विकास में इसका योगदान छोटा है (यह इसके विकास को लगभग 1/3 निर्धारित करता है)। बीमार मां वाले बच्चे में टाइप 1 मधुमेह विकसित होने की संभावना 1-2%, पिता में 3-6%, भाई या बहन में 6% होती है। ऑटोइम्यून बीटा सेल क्षति के एक या अधिक ह्यूमरल मार्कर, जिनमें एंटी-अग्नाशय आइलेट एंटीबॉडीज, एंटी-ग्लूटामेट डिकार्बोक्सिलेज एंटीबॉडीज (जीएडी 65) और एंटी-टायरोसिन फॉस्फेट एंटीबॉडीज (आईए-2 और आईए-2बीटा) शामिल हैं, 85-90 में पाए जाते हैं। रोगियों का %. फिर भी, बीटा कोशिकाओं के विनाश में मुख्य महत्व सेलुलर प्रतिरक्षा कारकों को दिया जाता है। टाइप 1 डायबिटीज मेलिटस HLA हैप्लोटाइप्स DQA और DQB से जुड़ा है। बढ़ी हुई आवृत्ति के साथ, टाइप 1 मधुमेह मेलेटस को अन्य ऑटोइम्यून एंडोक्राइन (ऑटोइम्यून थायरॉयडिटिस, एडिसन रोग) और गैर-एंडोक्राइन रोगों, जैसे खालित्य, विटिलिगो, क्रोहन रोग, आमवाती रोगों के साथ जोड़ा जाता है।
रोगजनन
टाइप 1 मधुमेह तब प्रकट होता है जब 80-90% बीटा कोशिकाएं एक ऑटोइम्यून प्रक्रिया द्वारा नष्ट हो जाती हैं। इस प्रक्रिया की गति और तीव्रता काफी भिन्न हो सकती है। बहुधा जब विशिष्ट पाठ्यक्रमबच्चों और युवाओं में रोग, यह प्रक्रिया काफी तेजी से आगे बढ़ती है, इसके बाद रोग तेजी से प्रकट होता है, जिसमें पहले नैदानिक लक्षणों की उपस्थिति से लेकर केटोएसिडोसिस (कीटोएसिडोटिक कोमा तक) के विकास तक केवल कुछ सप्ताह ही बीत सकते हैं।
अन्य, बहुत दुर्लभ मामलों में, आमतौर पर 40 वर्ष से अधिक उम्र के वयस्कों में, रोग गुप्त हो सकता है। (वयस्कों का अव्यक्त ऑटोइम्यून मधुमेह - LADA),इसके अलावा, बीमारी की शुरुआत में, ऐसे रोगियों को अक्सर टाइप 2 मधुमेह मेलिटस का निदान किया जाता है, और कई वर्षों तक, सल्फोनील्यूरिया दवाओं को निर्धारित करके मधुमेह मेलिटस के लिए मुआवजा प्राप्त किया जा सकता है। लेकिन बाद में, आमतौर पर 3 साल के बाद, पूर्ण इंसुलिन की कमी के लक्षण दिखाई देते हैं (वजन में कमी, केटोनुरिया, गंभीर हाइपरग्लेसेमिया, टैबलेट वाली हाइपोग्लाइसेमिक दवाएं लेने के बावजूद)।
टाइप 1 मधुमेह मेलेटस का रोगजनन पूर्ण इंसुलिन की कमी पर आधारित है। ग्लूकोज की इंसुलिन-निर्भर ऊतकों (वसा और मांसपेशियों) में प्रवेश करने में असमर्थता से ऊर्जा की कमी हो जाती है, जिसके परिणामस्वरूप तीव्र लिपोलिसिस और प्रोटियोलिसिस होता है, जो वजन घटाने से जुड़ा होता है। ग्लाइसेमिक स्तर में वृद्धि हाइपरोस्मोलैरिटी का कारण बनती है, जो ऑस्मोटिक ड्यूरिसिस और गंभीर निर्जलीकरण के साथ होती है। इंसुलिन की कमी और ऊर्जा की कमी की स्थिति में, गर्भनिरोधक हार्मोन (ग्लूकागन, कोर्टिसोल, ग्रोथ हार्मोन) का उत्पादन बाधित होता है, जो ग्लाइसेमिया में वृद्धि के बावजूद, ग्लूकोनियोजेनेसिस की उत्तेजना का कारण बनता है। वसा ऊतक में लिपोलिसिस बढ़ने से मुक्त फैटी एसिड की सांद्रता में उल्लेखनीय वृद्धि होती है। इंसुलिन की कमी के साथ, यकृत की लिपोसिंथेटिक क्षमता दब जाती है, और मुक्त फैटी एसिड केटोजेनेसिस में शामिल होने लगते हैं। कीटोन निकायों के संचय से मधुमेह कीटोसिस और बाद में कीटोएसिडोसिस का विकास होता है। निर्जलीकरण और एसिडोसिस में प्रगतिशील वृद्धि के साथ, कोमा विकसित होता है, जो इंसुलिन थेरेपी और पुनर्जलीकरण की अनुपस्थिति में अनिवार्य रूप से मृत्यु में समाप्त होता है।
महामारी विज्ञान
मधुमेह के सभी मामलों में टाइप 1 मधुमेह मेलिटस 1.5-2% है। कोकेशियान व्यक्ति में टाइप 1 मधुमेह विकसित होने का जीवनकाल जोखिम लगभग 0.4% है। टाइप 1 मधुमेह मेलिटस के प्रकट होने की चरम आयु लगभग 10-13 वर्ष है। अधिकांश मामलों में, टाइप 1 मधुमेह 40 वर्ष की आयु से पहले ही प्रकट होता है।
नैदानिक अभिव्यक्तियाँ
सामान्य मामलों में,विशेष रूप से बच्चों और युवाओं में, टाइप 1 मधुमेह एक स्पष्ट नैदानिक तस्वीर के साथ शुरू होता है जो कई महीनों या हफ्तों में विकसित होता है। टाइप 1 मधुमेह मेलिटस की अभिव्यक्ति संक्रामक और अन्य सहवर्ती बीमारियों से शुरू हो सकती है। विशेषता सभी प्रकार के मधुमेह के सामान्य लक्षण,हाइपरग्लेसेमिया से जुड़े: पॉलीडिप्सिया, पॉलीयूरिया, खुजली, लेकिन टाइप 1 डायबिटीज मेलिटस में वे बहुत स्पष्ट होते हैं। तो, दिन भर में, मरीज़ 5-10 लीटर तक तरल पदार्थ पी सकते हैं और उत्सर्जित कर सकते हैं। विशिष्टटाइप 1 मधुमेह के लिए, लक्षण, जो इंसुलिन की पूर्ण कमी के कारण होता है, 1-2 महीनों में वजन का 10-15 किलोग्राम तक कम होना है। गंभीर सामान्य और मांसपेशियों की कमजोरी, प्रदर्शन में कमी और उनींदापन इसकी विशेषता है। रोग की शुरुआत में, कुछ रोगियों को भूख में वृद्धि का अनुभव हो सकता है, जो कीटोएसिडोसिस विकसित होने पर एनोरेक्सिया का मार्ग प्रशस्त करता है। उत्तरार्द्ध को मुंह से एसीटोन गंध (या फल गंध) की उपस्थिति, मतली, उल्टी, अक्सर पेट में दर्द (स्यूडोपेरिटोनिटिस), गंभीर निर्जलीकरण और कोमा के विकास में समाप्त होने की विशेषता है। कुछ मामलों में, बच्चों में टाइप 1 मधुमेह मेलेटस की पहली अभिव्यक्ति सहवर्ती रोगों, आमतौर पर संक्रामक या तीव्र सर्जिकल विकृति के कारण कोमा तक चेतना की प्रगतिशील हानि है।
35-40 वर्ष से अधिक उम्र के लोगों में टाइप 1 मधुमेह के विकास के दुर्लभ मामलों में (वयस्कों का अव्यक्त ऑटोइम्यून मधुमेह)रोग स्वयं इतने स्पष्ट रूप से प्रकट नहीं हो सकता है (मध्यम पॉलीडिप्सिया और पॉलीयूरिया, शरीर के वजन में कोई कमी नहीं) और ग्लाइसेमिक स्तर के नियमित निर्धारण के दौरान संयोग से इसका पता भी चल सकता है। इन मामलों में, रोगी को अक्सर पहले टाइप 2 डायबिटीज मेलिटस का निदान किया जाता है और टैबलेट वाली हाइपोग्लाइसेमिक दवाएं दी जाती हैं, जो कुछ समय के लिए डायबिटीज मेलिटस के लिए स्वीकार्य मुआवजा प्रदान करती हैं। हालाँकि, कई वर्षों के दौरान (अक्सर एक वर्ष के भीतर), रोगी में इंसुलिन की बढ़ती पूर्ण कमी के कारण लक्षण विकसित होते हैं: वजन में कमी, टैबलेट ग्लूकोज कम करने वाली दवाओं की पृष्ठभूमि पर सामान्य ग्लाइसेमिया बनाए रखने में असमर्थता, केटोसिस, केटोएसिडोसिस।
निदान
यह ध्यान में रखते हुए कि टाइप 1 डायबिटीज मेलिटस की एक स्पष्ट नैदानिक तस्वीर है और यह एक अपेक्षाकृत दुर्लभ बीमारी भी है, टाइप 1 डायबिटीज मेलिटस के निदान के लिए ग्लाइसेमिक स्तर के स्क्रीनिंग निर्धारण का संकेत नहीं दिया गया है। रोगियों के करीबी रिश्तेदारों में रोग विकसित होने की संभावना कम है, जो टाइप 1 मधुमेह की प्राथमिक रोकथाम के लिए प्रभावी तरीकों की कमी के साथ-साथ उनमें रोग के इम्यूनोजेनेटिक मार्करों का अध्ययन करने की अनुपयुक्तता को निर्धारित करता है। अधिकांश मामलों में टाइप 1 मधुमेह मेलेटस का निदान पूर्ण इंसुलिन की कमी के गंभीर नैदानिक अभिव्यक्तियों वाले रोगियों में महत्वपूर्ण हाइपरग्लेसेमिया की पहचान पर आधारित है। मौखिक ग्लूकोज सहनशीलता परीक्षणटाइप 1 मधुमेह मेलिटस का निदान करने के उद्देश्य से इसे बहुत ही कम करना आवश्यक है।
क्रमानुसार रोग का निदान
संदिग्ध मामलों में (स्पष्ट नैदानिक अभिव्यक्तियों की अनुपस्थिति में मध्यम हाइपरग्लेसेमिया का पता लगाना, अपेक्षाकृत उन्नत उम्र में अभिव्यक्ति), साथ ही साथ अन्य प्रकार के मधुमेह मेलिटस के साथ विभेदक निदान के उद्देश्य से, स्तर निर्धारण का उपयोग किया जाता है सी पेप्टाइड(बेसल और भोजन के 2 घंटे बाद)। संदिग्ध मामलों में अप्रत्यक्ष निदान मूल्य में, परिभाषा हो सकती है इम्यूनोलॉजिकल मार्करटाइप 1 मधुमेह मेलिटस - अग्नाशयी आइलेट्स, ग्लूटामेट डिकार्बोक्सिलेज (जीएडी65) और टायरोसिन फॉस्फेट (आईए-2 और आईए-2पी) के प्रति एंटीबॉडी।
इलाजकिसी भी प्रकार का मधुमेह मेलिटस तीन मुख्य सिद्धांतों पर आधारित है: हाइपोग्लाइसेमिक थेरेपी (टाइप 1 डायबिटीज मेलिटस के लिए - इंसुलिन थेरेपी), आहार और रोगी शिक्षा। टाइप 1 मधुमेह के लिए इंसुलिन थेरेपी है स्थानापन्न प्रकृतिऔर इसका लक्ष्य स्वीकृत क्षतिपूर्ति मानदंडों को प्राप्त करने के लिए यथासंभव शारीरिक हार्मोन उत्पादन की नकल करना है। गहन इंसुलिन थेरेपी शारीरिक इंसुलिन स्राव के सबसे करीब है। इसके अनुरूप इंसुलिन की आवश्यकता होती है बेसल स्रावइंटरमीडिएट-एक्टिंग इंसुलिन (सुबह और शाम) के दो इंजेक्शन या लंबे समय तक काम करने वाले इंसुलिन (ग्लार्गिन) के एक इंजेक्शन द्वारा प्रदान किया जाता है। बेसल इंसुलिन की कुल खुराक दवा की कुल दैनिक आवश्यकता के आधे से अधिक नहीं होनी चाहिए।
भोजन या बोलस इंसुलिन स्रावप्रत्येक भोजन से पहले शॉर्ट- या अल्ट्रा-शॉर्ट-एक्टिंग इंसुलिन के इंजेक्शन द्वारा प्रतिस्थापित किया जाता है, और इसकी खुराक की गणना आगामी भोजन के दौरान ली जाने वाली कार्बोहाइड्रेट की मात्रा और ग्लाइसेमिया के मौजूदा स्तर के आधार पर की जाती है, जो रोगी द्वारा निर्धारित किया जाता है। प्रत्येक इंसुलिन इंजेक्शन से पहले ग्लूकोमीटर।
टाइप 1 मधुमेह के प्रकट होने और काफी लंबे समय तक इंसुलिन थेरेपी की शुरुआत के बाद, इंसुलिन की आवश्यकता छोटी हो सकती है और 0.3-0.4 यू/किग्रा से कम हो सकती है। इस अवधि को छूट चरण के रूप में जाना जाता है, या "हनीमून"।हाइपरग्लेसेमिया और कीटोएसिडोसिस की अवधि के बाद, जो शेष 10-15% बीटा कोशिकाओं द्वारा इंसुलिन स्राव को दबा देता है, इंसुलिन का प्रशासन करके हार्मोनल-चयापचय विकारों के लिए क्षतिपूर्ति इन कोशिकाओं के कार्य को बहाल करती है, जो तब शरीर को न्यूनतम इंसुलिन प्रदान करने का काम करती हैं। स्तर। यह अवधि कई हफ्तों से लेकर कई वर्षों तक रह सकती है, लेकिन अंततः, शेष बीटा कोशिकाओं के ऑटोइम्यून विनाश के कारण, हनीमून समाप्त हो जाता है।