新しい生殖技術に対する宗教的評価。 要約: 生殖補助技術。 I.はじめに
現代の生物学と医学の成果により、女性が遭遇する病状を補う技術の開発が可能になり、その結果生殖が困難、さらには不可能となっています。 現在では、代理母の助けを借りて、受精、胎児の保存、妊娠をバイオテクノロジー的に確実に行うことが可能になっています。 これらのテクノロジーのおかげで、多くの夫婦が新しい命を出産し、子育ての幸せを実感することができています。 しかし、新しい生殖技術にはリスクがあります。 したがって、体外受精では、いくつかの卵子が授精され、得られたいくつかの細胞の段階の胚が病状についての細胞学的分析に供されます。 すべての検査に合格した胚は子宮に移植されます。 問題は、残りをどうするか、生殖細胞として扱うべきか、それともヒト胚として扱うべきかということです。 この質問自体は、人間の胎児が単なる「生物学的物質」ではなく、社会によって保障されなければならない特定の権利、主に生きる権利を持っている可能性があることを示唆しています。 このようなテクノロジーを使用する可能性が生じたすべての社会、およびすでに使用されている社会では、その合法性と倫理的許容性に関して公的議論が生じます。
新たな社会的不一致は、談話的かつ実践的な手段を通じて解決できます。 特定の社会で発展した倫理体制 (自由主義*民主主義*、権威主義*、共同体主義*、または保守*伝統主義) に応じて、異なる社会倫理的、政治的および法的手法が適切な場合があります。 しかし、いずれにせよ、これは一般的な道徳的実践です - いくつかの利益を言説的に擁護し、他の利益を制限し、利益のバランスを維持し、それらの調和を目指して努力し、このためにそれらを高めるために行われる努力。 調整、調和、相互認識、利益の受容(相互的または一方的)のプロセスは、コミュニケーション的、社会政治的、法律的など、さまざまな社会的ツールの助けを借りて社会で継続的に実行されます。 利益について議論するとき、結局のところ、道徳的価値観に言及する道徳的議論が使用されます。
ただし、これらのツールは常に機能するとは限りません。 議論上の意見の相違が、社会政治的対立の形をとった対立に変わると、国家は利益を区切るために行政的、政治的、法的手段を使用します。 原則として、これは国益の形で提示される「一般利益」の立場から行われます。 権威主義的または寡頭制の政府が存在する社会では、三権分立制度の未発達または脆弱さ、政治的抑制と均衡のシステムの不作動、国家利益を装った政治的および市民的自由の抑圧が見られる。 すべての人の利益が満たされれば、支配グループの特定の利益も実現されます。 利益相反は、刑事的および強制的な手段によって解決されることもあります。 これらすべてが公の場での議論の可能性を狭め、さらには排除し、それが社会の道徳的可能性を弱める要因となっていることが判明しています。
通常の社会の社会的実践においては、さまざまな手段によって利益を調整するという課題は、原則として異なる方法で解決されるため、道徳は伝統などの多かれ少なかれ似た他の手段とともに手段の1つとして認識されています。 、法律、法律、行政、企業機関。 さらに、道徳は規律、したがって抑圧性(抑圧)と関連付けられる可能性があります。 ただし、ここではしつけについて話す方が正確です。 制限性(ラテン語のresctrictio - 制限から)、つまり 抑圧ではなく、制限についてです。 社会的規律は、その重要な側面において、個人との関係において制限的です。 制限が、パートナーシップ、協力、友情などの人々の相互作用において、私的利益の存在とその実現の可能性を提供する場合、その制限は道徳的に正当である、または合法的です。 これは、道徳と、制限の程度が異なる他の社会規律の仕組み(法律、習慣)の両方に当てはまります。
他の形態の社会規律と同様に、道徳は、一部の私的利益が他の私的利益または一般的利益に対して不当に支配されるのを防ぐために、私的な利益を制限することを目的としています。 教訓的で道徳的なジャンルの歴史上最も古い作品に反映されている道徳の初期の形式の分析によって証明されているように、美徳の指導の形でそれらの作品に現れた道徳は、最初は主に警告し、人の犯罪を抑制します。他者の利益、尊厳、自己同一性を侵害し、個々のコミュニティに反する行為。 ただし、分析 知恵の文学*、そこから、道徳主義、つまり道徳を啓発する文学や倫理(道徳哲学として)が徐々に現れ、思想の発展(特に、コミュニケーションや社会的経験の豊かさを反映)とともに、禁欲には美徳がますます見なされなくなっていることを示しています。自己抑制など、意図的な行動、ポジティブな(道徳的な意味での)結果を求める意識的な欲求、他の人々、グループ、社会にとって重要な活動がますます増えています。
道徳の積極的な性質は、ロシア語の「徳」という言葉の中に明らかに「聞こえ」ます。 言葉の構成からわかるように、徳は善行を保証するものです。 一般に、警告による制限だけでは善行には不十分であることは明らかです。 肯定的なものは必要です、つまり 生産的な行動。 道徳は制限に限定されず、禁止にまで引き下げることもできないため、法律を超えます。
彼女は、禁止されていることを避けることに加えて、何をする必要があるかを促し、指示します。 既存の現状を維持するという問題を解決する法律とは異なり、道徳では建設的な戦略がはるかに重要です。つまり、どのようにして人間と社会が物事の状態を改善し、日常生活を超えて、それによって完璧に近づくことができるのでしょうか? 理解することは大切ですが、 してはいけないこと、道徳の主体としての人間にとって、他の問題も非常に重要です。何をすべきか、どのように行うべきか、最善を尽くすためにはどうあるべきか?
しかし、利害を調和させ、共同体を維持し、他人の善を促進し、共通善を促進するという課題が、他人の弱みや悪徳を甘んじることによって解決できる場合には背景に追いやられる状況、さらには人生の全期間においてさえも存在する。間接的ではあるが、それに近い、適合または参加のコスト。 自分の原則や最高の価値観に忠実であるためには、自分には何の共通点もないと信じているものから断固として距離を置く必要があるかもしれません。
« 嘘をついて生きるなよ!」 - アレクサンドル・ソルジェニーツィンは1974年にソビエト国民にそのような訴えをした。 もし私たちに積極的に悪に抵抗する力がないのなら、道はただ一つ、悪に加担しないことです。自分!" 嘘は人を通して保たれるので、人は嘘をやめなければなりません。 嘘は暴力と結びつき、暴力は嘘と結びつきます。暴力は、自分自身を秘密にし、身を隠し、保護的で思いやりのあるふりをするために嘘を必要とします。 ソルジェニーツィンは、「暴力が平和な人間生活に突入すると、その顔は自信に満ちて輝き、旗を掲げて叫びます。『私は暴力だ!』と叫びます。」 解散せよ、道を譲れ――潰してやる!』 しかし、暴力は数年と急速に老化します。暴力はもはや自信を失い、まともに見えるために、それは確かに嘘を同盟者として求めます。 なぜなら、暴力には嘘以外に隠すものは何もなく、嘘は暴力によってのみ維持できるからです。 そして、暴力は毎日、すべての肩に重い足を置くわけではありません。暴力が私たちに要求するのは、嘘への服従、嘘への毎日の参加だけです - そしてこれがすべての忠誠です。」
嘘をつかないで生きるとは、決して良心に反することを言わないこと、誰かが吐いた嘘を繰り返さないこと、特にそれを支持しないこと、嘘に耳を貸さないこと(情報を隠して歪曲した新聞を読まないこと)、そして嘘が真実として受け入れられているふりをしないことを意味します。 。
嘘に頼らずに生きることは、偽善、嘘、不正義、暴力が支配する社会で人ができる最も簡単な事です。 いずれにせよ、これを決断しなければなりません。それは簡単なことではありません。真実に生きたいという願望のために、自分のキャリアと地位で代価を支払い、仕事を失い、自分と家族の平和を奪うこともできます。
真実か嘘かの選択は、精神的な自立か精神的な隷属かの選択である、とソルジェニーツィンは確信している。
原則的な道徳的立場は常に独立性、独立性で表現されます。 しかし、他人の意見に流されないことと、道徳的根拠に基づいて当局、直属の上司、集団の利己主義などの不当な決定に抵抗することは別のことです。 このような状況では、優先事項は非行動の原則、つまり悪を避けること、悪に参加しないことです。
これを認識することは、近代になってようやく具体化された道徳の哲学的概念における重要な点であり、「善(善)と悪」という言葉で表されるコミュニケーション的、社会的、精神的実践の側面の一般化を表しています。 「徳と悪」、「正義とわがまま」、「善悪」、そして「性格」、「行動規範」、「責任」、「友情」、「愛」など。 精神的および規範的な経験、習慣、行動、性格における「道徳」の概念の助けを借りて、最高の価値を表現し、それを通じて人が知的に、自由に、責任を持って自分自身を表現する機会を持つことが特定されます。 社会的慣習と人間関係における秩序、恣意性の限界、正しい行動、個人の尊厳と完全さ - これが道徳の一般的な概念の内容です。 上記からわかるように、この概念は異種混合です。 次の 3 つの次元を組み合わせています。 A)社会の状態(国家としての社会と民間の地域社会実体としてのコミュニティの両方を含む広い意味で)。 b)社会的役割の遂行者としての人々と私的な個人としての人々の間の関係、つまり社会的つながりに依存せず、相互理解、交流、思いやり、愛ができる個人の能力で行動する個人間の関係。 V)人格の質、それは正気としても現れます。 他者の要求への応答性、他者の期待への敏感さ、そして自分自身を理解しコントロールする能力、一貫性を持って自分に忠実であること、そして自分自身と他者に対する自分の考えや行動に責任を持つ能力として。 後者の責任は、完全ではありませんが、何らかの形で道徳のさまざまな側面を結びつけます。
倫理学、または道徳哲学は、この多様な内容の何が特別なのかを理解し、それに基づいて道徳に関する特別な考え方を構築しようと努めています。 同時に、道徳の一般的な概念の形成に伴い、「善と悪」、「美徳と悪徳」、「正義」、「義務」など、特定の倫理的カテゴリーの仕様が発生します。 道徳の文脈におけるそれらに特徴的な特別な内容の特定と明確化。
テストの問題と課題
- 1. 道徳の定義に対する主なアプローチを挙げ、それらをどのように分類できるかを確立します。
- 2. 決定手順の内容を展開します。 この定義を使用するとどのような理論上の問題が解決されますか?
- 3. 道徳の異質性はどのように表現されますか? 道徳の内部的に異質な要素の統一性は何によって決まるのでしょうか?
- 4. この章で与えられた道徳の予備的な定義から始めて、道徳のどのような社会文化的機能を特定できますか?
1. 体外受精(IVF)。
2. 配偶子および胚の卵管への移植 (GIFT、ZIFT)。
3. 男性不妊治療における配偶子の顕微操作:
透明帯ゾーンの部分解剖。
帯下受精。
細胞質内精子注入 (ICIS)。
4. ドナーの卵母細胞および胚を使用した生殖補助方法。
5. 代理出産(女性ドナーが顧客家族の遺伝的子供を宿す)。
6. 精子、卵子、胚の凍結保存。
7. 夫またはドナーの精子による人工授精(ISM、ISD)。
正当化
ロシアにおける不妊婚の頻度は15%を超えており、WHOによれば、これは重大なレベルであると考えられている。 国内には500万人以上の不妊カップルが登録されており、その半数以上がART法の使用を必要としている。 専門家の推計によると、女性の不妊率だけでも過去5年間で14%増加したという。
現在 ART という一般用語にまとめられている多くのアプローチの開発の基礎は、子宮腔内での IVF と ET という古典的な方法でした。 この場合、卵母細胞は特別な栄養培地で培養された後、精子と受精し、精子は事前に遠心分離され、栄養培地中で処理されます。
アートの種類:
- その後の遺伝的親への子(子供)の移植のために、ボランティアの女性(「代理母」)によって胚を運ぶ。
- 卵子と胚の提供。
- ICSI;
- 卵母細胞と胚の冷凍保存。
- 遺伝性疾患の着床前診断。
- 多胎妊娠における胚の減少。
- 実際には体外受精とPEです。
エコこの方法は、1978 年以来世界の不妊治療に使用されています。ロシアでは、1986 年にロシア医学アカデミーの産科、婦人科、周産期科学センターでこの方法が初めて成功裏に実施されました。 B.V. レオノフにとって最初の試験管の子供が誕生した。 体外受精法の開発により、卵管性不妊症の治療の問題が袋小路から抜け出し、これまでは子供を産めない運命にあった膨大な数の女性が妊娠できるようになりました。
体外受精プログラムの患者に関しては、夫婦全体の不妊症について話し合う必要があります。 これにより、患者を選択してプログラムに備えるためのアプローチが根本的に変わり、女性と男性の両方の生殖器系の状態の事前評価が義務付けられます。
夫婦間の不妊症の約40%は男性不妊が原因です。 ICSI 法では、重度の不妊症(乏精子症、無力症、重度の奇形精子症)を持つ男性でも、場合によっては精巣生検で得られた点状の中に単一の精子が存在する場合に限り、子孫を残すことができます。 ドナー卵母細胞を使用する体外受精は、女性が自分の卵母細胞を入手できない場合、または受精および完全な妊娠の発達ができない低品質の卵母細胞を受け取った場合に、不妊症を克服するために使用されます。
「代理母」プログラムは、子宮を欠いている女性、または重度の生殖器外病変を抱えている女性が、妊娠が不可能または禁忌である場合に、遺伝的に子供を得る唯一の方法です。
着床前診断も体外受精法に基づいています。 その目的は、着床前発育の初期段階で胚を取得し、遺伝的病理と子宮腔内のPEを検査することです。 縮小手術は、胚が 3 つ以上ある場合に実行されます。 これは強制的な処置ですが、多胎妊娠を成功させるためには必要です。 合理的かつ科学に基づいた削減の使用、および多胎妊娠における削減の実施技術の改善により、そのような妊娠の臨床経過を最適化し、健康な子孫の誕生を予測し、周産期損失の頻度を減らすことが可能になります。
※夫の精子による授精(ISM)
夫の精子による授精(ISM)は、a)少量の新鮮な精子を膣および子宮頸部に、または b)実験室で浮遊またはパーコール勾配で濾過することによって調製された精子の子宮腔に直接注入することです。 ISMは、女性が完全に健康であり、管が通過できる場合に実行されます。
ISM の使用の適応:
♦ 膣内射精の不能(心因性または器質的インポテンス、重度の尿道下裂、逆行性射精、膣機能不全)。
♦ 男性因子不妊 - 精子の数の欠如(乏精子症)、運動性(無力精子症)、または構造の障害(奇形精子症)。
♦ 子宮頸部の不利な因子。従来の治療法では克服できません。
■ 妊娠誘発のための凍結保存精子の使用(精子は癌治療または精管切除術の前に採取されます)。
ISM手順の有効性 - 20 %.
ドナー精子による授精(ISD)
凍結保存されたドナー精子を解凍して使用します。 ISDは、夫の精子が無効である場合、または不適合の壁を克服できない場合に実行されます。 ISM 技術と ISD 技術は同じです。
ISDの効率- 50% (試行することをお勧めする最大サイクル数は 4 です)。
贈り物- 卵子と精子の卵管への移動。 女性からは 1 つ以上の卵子が、夫からは精子が採取され、混合されて卵管に挿入されます。
ジフト- 卵管への胚(接合子)の移植。
ZIFTの場合、GIFTよりも妊娠の確率が大幅に高くなります。 GIFT と ZIFT は、腹腔鏡検査中および超音波制御下の両方で実行できます。
最初のケースでは、配偶子または接合子は腹腔からチューブに導入され、2番目のケースでは子宮頸部を通って導入されます。 GIFT と ZIFT は診断用腹腔鏡検査と組み合わせて 1 回で実行されます。 最大 30% の効率。
体外受精(IVF) - 実験室条件で卵母細胞と精子を混合するプロセス。 卵巣刺激は、血漿エストラジオールレベルの測定および卵胞の成長の超音波測定によって監視されます。 卵胞に穴を開け、内容物を吸引します。 得られた卵母細胞は、夫からの受精能を獲得した精子と培養され、その後、自然受精の場合と同様に、卵胞の穿刺から2日から6日後に、得られた胚が子宮腔に移植されます。
IV の実施の適応:
炎症過程または手術中の卵管への不可逆的な損傷。
♦ 男性不妊。
♦ 免疫学的不妊症。
♦ 子宮内膜症による不妊症。
♦ 原因不明の不妊症。
ドナー胚を用いた体外受精法
卵巣が機能していない女性(「早期閉経」または卵巣摘出後)に使用されます。 この方法の本質は、ドナー卵子と夫の精子の受精の結果形成された胚を患者に移植することです。 場合によっては、卵子の代わりにドナー胚がこの目的に使用されます。 続いて、通常の生理学的妊娠中の女性の状態をシミュレートする HRT が実行されます。
代理出産
このタイプの体外受精は子宮のない患者に対して行われます。 この方法の本質は、女性から得た卵子に夫の精子を授精し、得られた胚を別の女性、つまり子供を産むことに同意した「代理母」の子宮に移植し、出産後にその子供を与えることである。卵の「所有者」、つまり 遺伝的な母親。
精子と胚の凍結
この方法の利点:
♦ いつでもどこでも精子を使用できる機能。
■エイズウイルスによる精子の汚染に関してドナーを監視し、女性と胎児の両方への感染リスクを排除する。
♦ 移植に必要な数よりも多くの卵子と胚が得られた場合(通常は 3 ~ 4 個以上)、体外受精の失敗後の周期で胚を使用する可能性。
芸術の目的
不妊のカップルから健康な子孫を得る。
アートの表示
- 卵管またはその閉塞がない完全な卵管性不妊症。
- 原因不明の不妊症。
- 治療できない不妊症、または他の方法よりも体外受精の方が克服できる可能性が高い不妊症。
- 免疫学的形態の不妊症(MAP検査による抗精子抗体の存在≧50%)。
- ICSI法の使用を必要とする、さまざまな形態の男性不妊症(乏症、無力症、奇形精子症)。
- PCOS;
- 子宮内膜症。
アートの禁忌
- 胚の着床や妊娠が不可能な子宮腔の先天奇形または後天的変形。
- 外科的治療が必要な子宮の良性腫瘍。
- あらゆる場所の悪性新生物(病歴を含む)。
- 卵巣腫瘍;
- あらゆる局在性の急性炎症性疾患;
- 妊娠や出産に禁忌とされる身体疾患および精神疾患。
アートの準備
体外受精前の夫婦の検査範囲は、2003 年 2 月 26 日付けのロシア連邦保健省令第 67 号「女性および男性の不妊治療における ART の使用について」によって規定されています。
女性の場合は以下のことが必要です。
- 健康状態と妊娠の可能性に関する医師の報告書。
- 尿道と子宮頸管の微生物叢と膣の清潔度の検査。
- 血液凝固時間の測定を含む臨床血液検査 (1 か月間有効)。
- 一般および特殊な婦人科検査。
- 血液型とRh因子の決定。
- 骨盤臓器の超音波検査。
指示に従って、次のことが追加で実行されます。
- 尿道および子宮頸管からの物質の細菌学的検査。
- 子宮内膜生検。
- 感染症検査(クラミジア、ウレアプラズマ、マイコプラズマ、HSV、CMV、トキソプラズマ、風疹ウイルス)。
- 子宮と卵管の状態の検査(HSGまたは子宮卵管鏡検査と腹腔鏡検査)。
- 抗精子抗体および抗リン脂質抗体の存在の検査。
- FSH、LH、エストラジオール、プロラクチン、テストステロン、コルチゾール、プロゲステロン、甲状腺ホルモン、TSH、STHの血漿濃度の測定。
- 子宮頸部塗抹標本の細胞学的検査。
必要に応じて、他の専門家との相談が処方されます。
男性の場合は以下のことが求められます。
- 梅毒、HIV、B型肝炎およびC型肝炎の血液検査(3か月間有効)。
- スペルモグラム。 兆候によると:
- 感染症検査(クラミジア、ウレアプラズマ、マイコプラズマ、HSV、CMV)。
- 精子のFISH診断(蛍光in situハイブリダイゼーション法)。
- 血液型とRh因子の決定。
アンドロロジストによる診察も予定されています。 35 歳以上の夫婦の場合、医学的遺伝カウンセリングが必要です。
アート方法論
IVF 手順は次の段階で構成されます。
- 患者の選択、検査、および逸脱が検出された場合の事前準備。
- 卵胞形成および子宮内膜発達のモニタリングを含む、過排卵の刺激(制御された卵巣刺激)。
- 排卵前の卵母細胞を取得するための卵胞の穿刺。
- 卵母細胞の授精と体外受精の結果として発生した胚の培養。
- 子宮腔内へのPEの注入。
- PE後の期間のサポート。
- 初期段階での妊娠の診断。
アートの有効性
欧州生殖医学会によると、現在ヨーロッパでは年間 290,000 サイクル以上の ART サイクルが実施されており、そのうち 25.5% が出産につながっています。 米国では年間 110,000 周期以上、平均妊娠率は 32.5% です。
ロシアの ART クリニックでは年間 10,000 サイクルが実行され、妊娠率は約 26% です。
アートの効果に影響を与える要因
薬学産業の発展により、卵胞形成を刺激する新薬、卵母細胞を採取するための新しい使い捨て穿刺針、子宮腔内に挿入するための最新の非外傷性カテーテルが開発されました。 これにより、より多くの良質の卵母細胞を採取することが可能となり、TVP 中に起こり得る合併症のリスクが軽減され、その結果、子宮腔内の ET 1 人あたり体外受精プログラムの効率が 36 ~ 39% に向上しました。
IVF および ET プログラムにおいて、最も効果的なスキームは、生殖系の GnRH 脱感作を背景に、組換えゴナドトロピン製剤で過剰排卵を刺激することです。 我々の観点からは、組換えゴナドトロピンとGnRHアンタゴニストの薬剤を使用した過排卵刺激療法の使用は効果は低いですが、OHSSの発生率をほぼ2分の1に減らすことができます。
2 回以上の IVF および PE の失敗歴があり、女性の精子形成が正常で生殖機能が障害されている夫婦に ICSI 法を使用すると、症例の 52% で妊娠が可能になります。
無精子症患者において、精巣および/または精巣上体の生検とそれに続く組織学的検査とホルモンおよび遺伝子スクリーニングを組み合わせることで、診断を確立し、夫婦の不妊治療のためのさらなる戦略を決定することが可能になります。 非閉塞性無精子症の患者グループは、体外受精/ICSIプログラムで精子を獲得し妊娠するという点で予後的に最も不利です。 この患者グループの妊娠率は 14.3% です。
今日の ART における凍結保存は、ほぼあらゆる種類の生物学的材料に使用されています。 この方法により、精子、精巣組織、卵母細胞、胚の長期保存が可能になります。 解凍後、精子の 95% と胚の 80% が生存しています。 OHSS を発症するリスクが高いために刺激サイクル中に ET 処置がキャンセルされ、「良好な」品質の胚がすべて凍結保存された場合、患者の妊娠率は刺激サイクルに基づいて 37.1% になります。 試みが失敗した女性のARTプログラムにおいて、凍結保存後に解凍した胚盤胞を使用する有効性は29.5%でした。
IVFおよびETプログラムにおける出生前診断は、両親の一方が染色体異常保因者であるカップルの自然中絶の発生率を13%に減少させました。これと比較して、同様の問題を抱え、出生前診断サービスを利用しなかった患者の自然中絶の頻度は減少しました。 。 胚の染色体病理を検出し、遺伝的に正常な胚のみを移植することで、着床率が向上し、自然流産のリスクが軽減され、体外受精プログラム患者における遺伝的病理をもつ子供の誕生が防止されます。 出生前診断の助けを借りて、胎児の性別に関連する染色体疾患(血友病AおよびB、デュシェンヌ筋症、マーティン・ベル症候群など)、21番目の染色体のトリソミー(ダウン症候群)、13番目の染色体上の染色体疾患を回避することが可能です。染色体(パトー症候群)、18番染色体(エドワーズ症候群)、モノソミー(シェレシェフスキー・ターナー)など。
出生前診断は、遺伝性および先天性病理の病歴、核型におけるバランスのとれた染色体異常の存在、過去に体外受精の試みが2回以上失敗したこと、胞状奇胎の病歴、異常の増加を伴う子供の出生の場合に適応されます。女性が35歳以上の場合、配偶者の射精液中の異なる染色体異数性(X、Y染色体>0.25%)を持つ精子の割合を調べて胎児の性別を判定する。 この方法を使用した胚の性別決定の精度は 95 ~ 97% です。 2006 年に ART 部門の連邦州機関「NTs AGiP Rosmedtekhnologii」で出生前診断を使用した後の妊娠率は 32% でした。
三つ子を妊娠した場合の流産および超未熟児出産のリスクは 70% に達するため、減胎手術は多胎妊娠における合併症の発生率を減らすことができます。 初めて、経子宮頚管アクセスと下にある卵子の除去を使用して、妊娠第 1 期の多胎妊娠の減少が実施されました。 この方法は非常に外傷性が高く、多くの合併症を伴うことが判明したため、実際には使用されませんでした。 現在、経腹腔または経膣アクセスが使用されています。
経膣アクセスでは、膣円蓋の後部または前部を通して特別にマークされた針を使用して子宮内介入が行われます。 針の進行状況を視覚的に監視するために、子宮腔内の針の動きを高精度で視覚化できる特別な生検アダプターが使用されます。
経腹アクセスによって胚を減らすために、生検アダプターと、自己固定マンドレルを備えた、遠位端に 1 cm のエコー源面を備えた長さ 15 cm の針を備えたセンサーを経腹スキャンに使用します。
両方の方法を使用して整復を実行する場合、センサーの電子マーキングが胚の胸部に向けられ、針が胎児卵の腔に素早く挿入され、画像上のビデオ画像を使用して操作の精度を制御します。超音波診断装置のモニター画面。 針の貫通の深さは視覚的に制御されます。 胎児の卵の腔に侵入した後、針の先端が縮小した胚の胸部に運ばれ、心臓の活動が停止するまで胸部臓器を機械的に破壊します。 減胎胚の心拍が残っている場合は、2~4日後に再度減胎を行います。
芸術の複雑さ
- 排卵を刺激する薬に対するアレルギー反応。
- 炎症過程。
- 出血;
- 多胎妊娠。
- OHSS は通常、PE 後に発生し、卵巣のサイズの増大と卵巣内での嚢胞の形成を特徴とする医原性疾患です。 この状態には、血管透過性の増加、血液量減少、血液濃縮、凝固亢進、腹水、胸水および心膜水腫、電解質の不均衡、血漿中のエストラジオールおよび腫瘍マーカー CA125 の濃度の増加が伴います(詳細は「卵巣過剰刺激症候群」のセクションを参照)。
- 異所性子宮外妊娠。 ART 使用時の子宮外妊娠の発生率は 3% ~ 5% です。
導入
人口減少が進む状況では、出生率を高めるためにあらゆる資源を活用することが重要になります。 不妊症を減らすことが特に重要視されており、どの国でもその最低レベルは 10% であり、この問題に国家的重要性を与える臨界レベルは 15% です。 不妊症の増加はさまざまな要因によって説明されますが、最も多くの場合、人間の生殖機能に対する外部環境(化学、放射線、ライフスタイル、仕事の性質など)の影響に関連しています。 不妊症の本当の程度を判断するのは次の理由から困難です。
1. 避妊法の普及により、子供のいないすべての人が不妊であるとは考えられなくなりました。
2. 社会学的調査を行う場合、回答者は不妊の「偏見」を理由に自分の不妊を隠す傾向があります。
3. 公式統計には、不妊症および初診に関する医療機関の受診のみが記録されている。 患者が一度に複数の診療所に同時に連絡できることは考慮されておらず(これにより合計が増加します)、州外の診療所では登録を制限したり、登録を完全に拒否したりすることができます(これにより合計が減少します)。
4. 生殖問題を抱えている人全員が医療援助を求めているわけではありません。
さまざまな推定によると、現在、ロシアの生殖可能年齢の人口の 10 ~ 20% が不妊です。 これはヨーロッパ先進国の水準にほぼ相当する最大500万組のカップルがいる。2007年にはフランスでは女性の約15%が不妊症に関連して医師の相談を受け、イタリアでは5組に1組のカップルが不妊、英国では7組に1組が不妊症だった。
カップルの不妊症の原因は、女性 (カップルの最大 80%) または男性 (最大 45%) の生殖機能の障害である可能性があり、約 3 分の 1 のカップルでは複合不妊症、つまり不妊症が原因である可能性があります。 男性的要因と女性的要因の両方によって同時に引き起こされます。
不妊症は長い間、よく言えば解決できる問題ですが、解決するのはほぼ不可能です。 効果的な治療法がなかったため、生殖障害を抱えた不妊カップルは10組中3組しか自分の子供を産むことができなかったという事実が生じました。 ルイーズ・ブラウンが英国で生まれた1978年以降、体外受精(「体外」)に基づく生殖補助医療が臨床現場に導入されて初めて、不妊問題の根本的な解決策があると結論付けることができた。社会に。 生殖補助医療 (ART) を使用した場合の 1 回の妊娠確率は 30 ~ 40% ですが、自然妊娠では 8 ~ 25% です。
現代の ART には 10 を超える手法が含まれており、その数は常に拡大しており、実際の応用は特定の国の国内法や伝統によって規制されています。 最も効果的で人気のあるものは次のとおりです。
1. 体外受精(IVF、その後の子宮腔への胚の移植を伴う「体外受胎」)。
2. ICSI(男性不妊症の場合 - インビトロでの個々の精子と卵子の「強制的」結合)。
3. 代理出産(体外受精/顕微授精によって得られた遺伝的母親の胚を別の女性が運ぶ)。
4. 遺伝性および遺伝性疾患の着床前診断(子供の遺伝性疾患を除外し、妊娠後期の医学的理由による中絶を避けるために胎児期に実施されます)。
5. ドナー生殖細胞の使用(受精可能な自分の卵子と精子が存在しない場合)。
6. 凍結保存(将来の使用目的のために胚および生殖細胞を凍結する)。
ART の拡大解釈には、内分泌性不妊症や加齢に伴う個人の生殖能力の低下に使用され、「自然な」方法での妊娠を可能にする排卵のホルモン刺激も含まれます。 ホルモン刺激の必要性は、「出産の延期」の後期への広がりによって増加しており、多くの場合、卵巣予備能の生理的減少が始まる年齢制限(27歳)を超えています。
ART に関する情報は、公式の医療統計の必須指標のリストには含まれていませんが、任意です。 は、ART 実施のライセンスを持ち、その結果の公表を希望するクリニックから全国の専門家団体によって収集されます。 1995 年以来、ロシア人類生殖協会 (RAHR) は、他国との比較を可能にする形式を使用して ART の登録簿を維持しています。
ART は社会の「生殖基盤」を拡大し、受胎と妊娠を妨げるさまざまな性質の生殖能力の制限を克服します (図 1 を参照)。 現代の不妊治療のイデオロギーは、どんな犠牲を払ってでも妊娠することではなく、母親の健康を維持しながら健康な子供を一人出産することです(多胎やARTの合併症は医療ミスとみなされます)。
図 1. 社会の再生産基盤の拡大
生殖医療は、効果的で需要があり、市場変動に強い、収益性の高い新しい産業です。 不完全なデータによると、21世紀初頭までに。 世界ですでに200万人以上がARTを利用して誕生しています。 人口動態の個別化(初産の延期、「自然発生的」子育てではなく「意識的」子育ての普及など)は、一方ではARTに対する国民の需要の絶え間ない増加につながり、他方では新たな問題を引き起こす。 これ:
・不妊治療の効果をさらに高め、治療期間が数年を超えないようにし、繰り返し適用できる可能性を残す。 現代の ART プロトコルは、最初の適用から子供の誕生までの期間は 2 年を超えてはならないという事実に基づいています。 伝統的な不妊治療は診断と治療に少なくとも10年を要し、生殖年齢の終わりまで続く可能性がありました。
・生殖学、男性学、ヒト発生学などの新しい専門分野における高度な資格を持つ人材の研修。
・問題の社会化(哲学(倫理)、法律、経済学の主題分野に含める)。 コスタリカだけが、ART が国家憲法に違反するものとして公式に違法である(人工授精で人間の生命が始まり、その後、非移植または削減により生命が破壊されるため)。 他の国には、ART を明確に全面的に禁止する法律はありません。
ロシアの臨床現場への ART の導入は、革新的な産業の形成の一例です。 国内初の ART 出産は 1986 年に行われましたが、国内における生殖医療のさらなる発展は、集中計画の伝統によって複雑になりました。 1990年代初頭の過渡期のロシア経済の状況において。 革新的な生殖技術は、実績のある開発アルゴリズムを備えた「模倣」イノベーションとなっています。 1996 年、モスクワ、サンクトペテルブルク、ソチ、キスロヴォツク、ウラル山脈、シベリアにある 12 の生殖センターが国内 ART 登録に正式に登録され、2005 年にはすでに 51 の生殖センターがあり、それらはほぼ全土にありました。極東を含む国。 最も効果的な組織的および技術的スキームの使用、共同医療センターの創設、ノウハウなど。 これにより、ロシアの生殖クリニックは、提供されるサービスの必要な質を達成することができ、国内のニッチ市場を迅速に埋め、世界市場に参入することができました。 ロシアのセンターにおけるARTの有効性はすぐに世界レベルに達し、開始されたサイクルの約30%が出産で終了します。
現在、多くの主要な国内生殖医療センターはヨーロッパやアメリカの診療所と提携して外国人患者、特にARTを禁止する制限的な法律がある国からの患者を受け入れている。 ART に対する最も厳しい制限は、ドイツの法律「養子縁組の調停について」(1989 年) および「ヒト胎児の保護について」(1990 年)、イタリアの「出産における医療援助に関する基準」(2004 年) に含まれています。配偶子および胚の提供、着床前診断、胚の凍結保存、代理出産、および多胎妊娠の軽減(部分的中絶)を完全に禁止します。 こうした過剰な非経済的規制の試みは、いわゆる「リプロダクティブ・ツーリズム」の発展につながりました。不妊カップルは、より自由な法律がありながらも質の高いARTを備えた国に治療のために旅行します。 ロシアは「生殖を目的とした観光客」も受け入れている。 さらに、価格と品質のバランスが良いため、海外に永住する多くのロシア人女性がロシアのクリニックを選択しています。
ART に関する主な種類の経済関係は、市場主体を通じて実装されます。
・消費者(患者)。
・生殖クリニック。
· 機器と医薬品のサプライヤー。
· 金融機関、信用機関、保険機関。
· 近年 - 国家は、医療と人口開発に関する優先国家プロジェクトの枠組みの中で。
しかし、これらの市場主体の目標と目的は、ほぼ相互に矛盾しています。
・患者は、たとえ複雑な診断であっても、できるだけ安価にサービスを受けたいと考えている。
· 国家は、「人口統計への投資」の利益を増やすことに関心があり、実際に出生数を増やすことができるのは彼らなので、チャンスが最も大きい人々に資金を提供しようとしている。
· クリニックは、州予算から無料体外受精の割り当てを自分たちに有利になるように再配分しようと努めています。
o 公式には、州立診療所は自らの優先順位を主張し、州は州の機関でのみ治療に資金を提供すべきであると信じている。
公式には、私立診療所はさまざまな政府機関に対し、出生証明書の制度と同様に「患者に金銭(つまり、この場合は国が割り当てた割り当て)」を支給できる法律の制定を求めてロビー活動を行っている。 成功し人気のある私立クリニックの代表者らは、この場合、患者の選択は明らかに自社に有利になると確信しており、一般に、商業患者にとっての魅力はさらに高まるだろう。
製薬会社や機器メーカーは、ターゲット市場の規模拡大に関心を持っており、新しい診療所、患者団体、政府の人口統計プログラムなど、すべての人をサポートしようと努めています。なぜなら、彼らの観点からすると、これらすべてが自社製品の売上増加につながるからです。
ART は商品市場と資源市場の両方を同時に作成します。 ここでの製品は単なる医療ではなく、患者消費者が製造クリニックから購入する有料サービスです。 資源市場としての ART の具体的な役割は、合法的な生殖労働 (代理出産、生殖提供など) の機会を創出することです。 このようなリソースの必要性は、医療および社会的要素によって決定される ART の需要によって決まります。 医療は人々のリプロダクティブ・ヘルスの不良と関連しており、社会は人間の生殖方法としてのARTの基本的な可能性と関連している(例えば、法律で定められた独身女性のARTへの権利、ARTへの経済的および地域的アクセスのしやすさ)。 ロシアでは、他の大多数の国と同様に、法律により医療上の理由でのみ ART の使用が許可されています。
生殖クリニックのファイルやインターネットのテーマ別サイトのユーザー分析を通じてARTの潜在的な消費者を明らかにしたところ、主に若い生殖年齢(20~35歳)の患者の間で、医学的動機が絶対的に優勢であることが示された。 IVF と ICSI の主な消費者は同じ年齢層です。 ART の全体構造におけるこれらのプログラムの割合が 75% を超えていることを考慮すると、得られた結果は人口全体の傾向に対応していると推測できます (表 1 を参照)。
表 1. IVF および ICSI プログラムに参加する女性の年齢分布 (2004 年)、%
ソース : ヨーロッパにおける生殖補助医療、2004 年: ESHRE Human Reproduction によるヨーロッパの登録からの結果、2008 年。 23. No. 4. P. 758。
ヘルスケア管理の市場手法と政府の直接規制手法を組み合わせることで、ART 市場を予算セグメントと商業セグメントに条件付きで分割することが可能になります。 セグメントの財務上の境界は、最終的には ART に対する国の関心の程度に依存し、治療に対する予算割り当てを通じて商業需要が減少し、サービスのコストが削減されます。
予算セグメントは予算融資の枠組みによって決定され、割り当ての量は地域および連邦予算の財政能力、医療費およびARTのその他の要素(薬剤や設備、医師やその他の専門家の仕事、建物の賃貸料など)、割り当て数とその目標は、不妊症克服への投資の最も効率的なパラメータ(患者の年齢と医学的状態)に基づいて決定されます。
商業セグメントには、予算基金以外の資金(個人、スポンサーシップ、保険など)を使用してARTの支払いが含まれるため、快適性の向上に関連する追加の非医療サービスを提供し、より幅広い患者向けに設計されています(非医療的サービスとの関連で)。経済的可能性のみが考慮されますが、病歴にはより複雑な診断が存在します)。 生殖クリニックはあらゆるマーケティング ツールを使用し、独自のデータベースを作成し、交通機関やホテルのサービス、福利厚生、割引、さらには「ターンキー IVF」(体外受精を何度試みても、カップルの出産を保証する非常に高価なサービス)を提供しています。ドナーの遺伝物質と代理出産を使用する可能性があります)。
不妊症は生命への差し迫った脅威を伴うものではないため、その治療費は通常有料であり、強制健康保険の対象にはなりません。 しかし、ロシアの任意健康保険の基準では、不妊症はほぼ完全に除外されている。これは、保険会社の見解では、成功率が不十分であることによる商業上のリスクが高いためである。
こうした状況により ART 市場の商業化が促進され、主に小規模クリニック (体外受精の試行回数が年間 1000 ~ 1500 回以下) にとって魅力的なものとなり、相応の価格で「エリート」セグメントに位置することになります。 このような診療所の一般的なプロジェクトには 2,550 万ルーブルかかります。 24 か月の投資回収期間と医師と患者を通じたサービスの促進。 これにより中小企業にとって手頃な価格になります 11 。 その結果、ART 法を使用して不妊治療を提供する医療機関の数は増え続けており、2009 年初頭の時点で、ロシアのさまざまな地域から 90 以上のそのような診療所がメディアやインターネットで積極的にサービスを宣伝しています。
この活動の強化は、ロシアにおけるART出生数の大幅な増加の前提条件を生み出し、観察期間全体を通じてその割合は総出生数の0.5%を超えませんでした。 12 ; これは最大値である 4.2% よりも大幅に低いです (デンマーク、2002、2004) 13 。 排卵のホルモン刺激が ART 複合体で考慮される場合、結果はさらに印象的になります。いくつかの推定によると、ベルギーでは出生の最大 25%、フランスでは出生の 5 ~ 10% が ART の助けを借りて発生しています。 。
ロシアでこれを可能にするためには、生殖医療の公共部門と商業部門の関係を変える必要がある。 障害には、不十分な予算資金、地域のニーズとARTの利用可能性の違いを考慮していない予算割り当ての配分、割り当てを特定の診療所や不妊カップルの医学的および人口統計的特徴に「結び付ける」ことが含まれます。 「患者を追跡」する「生殖証明書」(「出生証明書」と同様)の導入により、夫婦が割り当て枠をどこに使用するかを独自に決定できるようになり、年齢、診断、子供の有無などに関する制限が緩和されます。ロシアの出生率におけるART出生の割合がさらに大きくなる可能性がある。
この問題には定性的な側面もあります。 不妊の問題に直面している人の生殖目標は2人、3人、4人に増加しますが、ARTは原則として病状を治すものではなく、その背景に対して出産の可能性を生み出すだけです。 したがって、2人目以降の子供の誕生にはほぼ確実に再びARTが必要となるが、夫婦はもはや国家からの経済的支援を当てにできなくなる。 さらに、ART はまさに望ましい子どもの誕生のためのリソースであり、誕生前からケアが始まります。 自ら進んで出産を拒否する「チャイルドフリー」の人気が高まる中、こうしたARTチルドレンの社会的価値は高まっている。
一部の国の実践が示すように、現在の不利な人口動態においては、出生率を高めるための資源を一つも無視することはできません。 避妊革命により、「自発的」親になることを受け入れない人々も確実にそれを回避できるようになりました。 社会の均衡のとれた発展の論理には、たとえ生物学的障害があっても、子供を持ちたい人全員が産むことを可能にする生殖技術という、避妊に反する制度の出現、普及、強化が必要である。
体外受精 (IVF)
標準的な体外受精プログラムの主な適応症は次のとおりです。
1 。 絶対 卵管性不妊症、両方の卵管の欠如に関連しています。
2 。 持続的 卵管および卵管腹膜不妊症さらなる保存的治療または外科的治療の見込みがない場合。
3. 内分泌性不妊症 6~12か月間ホルモン療法を行っても妊娠できない場合。
4. 原因となる不妊症 子宮内膜症骨盤臓器、2年間治療失敗。
5. 男性因子不妊症(乏精子症、無力症、奇形精子症、1〜2度)。
6. 原因不明の不妊症腹腔鏡検査を含むすべての最新の治療法を使用した後、確立された持続期間は2年以上です。
体外受精の主な手順
1. 過排卵の誘発 (ISO)。
過排卵を刺激する薬
卵胞刺激ホルモン含有製剤
女性の体内では、卵胞刺激ホルモン(FSH)が卵胞の成熟に関与しているため、過排卵を刺激するためにFSHを含む薬剤が使用されます。 現在、組換え医薬品が最も効果的であると考えられています。 これらは、閉経後の女性の尿から単離されたヒト尿中ゴナドトロピンをベースにした従来の薬剤の使用と比較して、妊娠率を高め、治療費を削減します。 そのような組換え FSH の 1 つが、遺伝子工学によって作成された Puregon です。 現在、女性の利便性と快適性を最大限に高めるため、インジェクターペン「ピュアゴンペン」が使用されています。 ピュアゴン ペン インジェクター ペン: 在宅患者によるピュアゴンの自己皮下投与用に設計され、再利用可能に設計されており、既製のピュアゴン ソリューションのカートリッジを使用し、マイクロニードルのおかげで操作の痛みを軽減します。 ピュアゴン ペンは新しい投与方法です。 FSH - Puregon は次の利点を提供します: 医師が処方した Puregon の用量を最大限に正確に投与できること、患者の個々の特性に応じて用量を調整できる最大限の可能性、最大限のシンプルさと使いやすさ、治療に伴う追加のストレスの軽減治療プロセスそのものを評価することで、肯定的な結果に対する信頼感が高まります。
下垂体自身のホルモンの産生を抑制する薬(ホルモンアゴニストおよびアンタゴニスト)
女性自身の下垂体ホルモンが過剰排卵の刺激を妨げないように、その産生はアンタゴニストとアゴニストによってブロックされます。 オルガルトランは、下垂体を瞬時に遮断し、その機能を迅速に回復させる新しい拮抗薬であり、従来の薬(作動薬)と比較して治療期間をほぼ半分に短縮できます。 アゴニスト(トリプトレリン、ゴセレリン、リュープロレリン、ブセレリン)は、かなり長期の投与を必要とします。 それらは20〜30日間毎日投与するか、少なくとも1か月間吸収される大量の投与量の形で1回投与する必要があります。
ヒト絨毛性性腺刺激ホルモン(hCG)を含む製剤
卵胞の穿刺は、成熟卵胞の排卵を開始する hCG の注射の 36 時間後に行われます。 hCG を使用すると、受精の準備ができた成熟した卵子を得ることができます。 hCGを含む薬剤の一つにプレグニルがあります。
過排卵刺激プロトコル
VECO はさまざまな種類のプロトコルを使用します。 厳格な治療計画はなく、以下の各プロトコルには個人差があり得ることを覚えておいてください。
「クリーンプロトコル」
下垂体を遮断せずに刺激療法を行う女性もいます。 このためには、ピュアゴンパンなどのFSHを含む薬剤のみが使用されます。 このスキームは「純粋」と呼ばれます。 欠点は、穿刺前であっても卵胞の早期排卵(破裂)の可能性があり、卵子を得ることが不可能になることです。 これは 15 ~ 20% のケースで発生します。 このプロトコルでは、興奮剤の投与は月経の 2 ~ 3 日目に開始され、9 ~ 14 日間継続されます。 1 日の投与量は超音波データに応じて医師によって調整され、通常は刺激期間全体で 4 ~ 5 回実行されます。 卵胞の最終成熟のために、hCG、たとえばプレグニルが投与され、35 ~ 36 時間後に卵胞に穴が開けられます。
「長いプロトコル」
このプロトコルは、原則として刺激前の月経周期の 21 ~ 23 日目 (まれに 2 ~ 3 日目) に開始されるため、「ロング」と呼ばれます。 下垂体をブロックするには、治療の開始時にアゴニストのみを5日間服用します。 下垂体の遮断が達成された後、月経が始まり、その開始から2〜3日から、「純粋な」レジメンと同じようにFSHを含む薬物で刺激が実行されますが、アゴニストの継続投与も併用されます。 。
「最適なプロトコル」
新しいアンタゴニストであるオルガルトランを使用すると、下垂体の明白で容易に可逆的な遮断を維持しながら、刺激プロトコルが大幅に短縮されます。 「純粋な」レジメンと同様に、月経周期の 2 ~ 3 日目に FSH を含む薬剤を毎日投与することによって刺激が始まります。 その後、刺激5~6日目から刺激を継続しながらオルガルトランを毎日注射します。 したがって、「最適プロトコル」は、「純粋な」スキームのように短くなり、「長い」スキームのように効率的になります。 新世代薬ピュアゴンとオルガルトラン(拮抗薬)の組み合わせは次のとおりです。
- 治療時間の短縮。
- 注射に対する耐性が向上します。
- 実証済みの有効性。
このおかげで、ピュレゴンとオルガルトランの併用は「不妊治療の期待の2成分」と言えます。
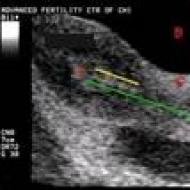
図 1 は、多くの卵胞を持つ刺激された卵巣の超音波写真を示しています。 赤い点は、直径 18 mm の最大の卵胞を示しています。
体外受精を可能にするためにはいくつの卵胞が必要ですか?
IVF に必要な卵胞の最小数は、いくつかの要因によって異なります。
1. 卵胞のサイズ。
2. 女性の年齢。
3.排卵を刺激するためのこれまでの試みの回数と結果。
一部の専門家は、刺激プロセス中に 14 mm の卵胞を少なくとも 5 つ取得する必要があると考えています。 しかし、この理論に反対する人たちは、十分な大きさの卵胞が少なくとも 1 つある場合でもこの手術を行うことは可能であると主張しています。
米国のほとんどのクリニックでは、この手術が成功したとみなされるには少なくとも 3 ~ 4 個の優勢卵胞が必要であると考えています。
以下の場合は排卵誘発はできません。
1. 卵管が通過できるという確信はありません。
2. 卵胞の成長を超音波でモニタリングすることはできません。
3. 無月経を背景に FSH レベルが 20 IU/l を超える場合。
4. 不妊治療期間がすでに2年を超えている。
人工授精(AI)- これは、夫またはドナーからの特別に処理された精子を子宮腔に導入する手順です。 AI と排卵誘発を組み合わせることで、治療の有効性が大幅に向上します。
AIは、ヒト絨毛性ゴナドトロピン(この薬は36~42時間後に排卵をプログラムします)の投与後12時間後と36時間後(いくつかのデータによると、最適には38~42時間後)の排卵予定日に1回または2回実施されます。
体外受精プログラムに直接の適応がある場合、体外受精の代替として AI を実施することは容認できません。
図 2 は、準備された精子の子宮腔への導入を概略的に示しています。
子宮内授精の有効性を決定する要因は何ですか?
文献によると、次の場合にこの手順の有効性が低下することが知られています。
1. 38歳以上の女性。
2. 卵巣予備力が低下している女性。
3. 精子の質が低い。
4. 中等度および重度の子宮内膜症が存在する場合。
5. 骨盤内に顕著な癒着がある女性。
子宮内授精にはどのような精子が使用できますか?
授精には、1mlあたり1000万個以上の運動精子を含む配偶者またはドナーの精子を使用する必要があります。 別の基準は、正常な形態の少なくとも 400 万個の精子が授精することを目的とした材料中に存在することです。
受精は何回まで行うことができますか?
授精による妊娠のほとんどは最初の 3 周期以内に起こることが知られています。 3 回の試行の後、この方法の可能性と有効性は減少し、4 ~ 6 回の操作が失敗すると確実に低くなります。
1周期中に子宮内授精は何回行う必要がありますか?
この問題は今日に至るまで物議を醸している。 一部の研究では、周期の対応する日に 2 回の授精を行った場合と、1 回の授精を行った場合に有効性が有意に増加しないことが示されています。 いくつかのデータによると、二重授精の使用により妊娠率が大幅に増加します。
確率論によれば、特に女性の体内での精子の寿命は約 2 ~ 5 日であるため、二重授精を使用すると、適切なタイミングで精子が導入される可能性が高まります。
成熟卵母細胞の採取(卵巣穿刺)
卵巣穿刺は、超音波制御と最新の薬剤による短期間の麻酔下で後部膣円蓋を通して行われ、副作用は最小限に抑えられます。
女性は眠っていて何も感じていません。 図 1 は、成熟卵母細胞を取得するために特殊な針で卵胞液を採取する超音波画像を示しています。
必要な卵胞がすべて穿刺された後、女性は1時間観察され、その後家に送られます。 図 2 は、25 歳の女性からの卵胞穿刺の結果として得られた良質の卵子を示しています。
比較のために、図 3 に、43 歳の女性の卵胞を穿刺して得られた低品質の卵母細胞を示します。 これらの卵母細胞の違いは、肉眼でも確認できます。
胚培養
発生学の研究室では、精子が卵子に受精します。 この段階には 3 ~ 5 日かかります。 図4は受精卵を示しています。 中央には男性と女性の2つの前核があり、右上隅には受精がすでに起こっていることを示す極体があります。
図4.受精卵。
手順の発生学的部分の重要な段階の 1 つは評価です。 "品質"胚の取得は、専門の発生学者によってさまざまな兆候に基づいて行われます。
セルの数。
同じサイズ;
断片化の程度。
発生学者は、多核の存在、空胞化の出現、粒度などに注意する必要があります。 通常、胚の「品質」を判断できるのは、受精後 48 時間以内です。
原則として 2 日後、少なくとも 3 個の細胞からなる胚を少なくとも 1 つ取得する必要があります。 72時間後、胚は少なくとも6個以上の細胞で構成されていなければなりません。
断片化がほとんどまたはまったくなく、規則的な形状とサイズの細胞を多く含む胚は、これらの要件を満たさない胚よりも着床する可能性が高くなります。
比較のために、「高品質」と「低品質」の胚を以下に示します。
顕微鏡を使用して検査した際の胚の「品質」を評価することは、移植後の特定の胚の推定着床確率を評価するための基礎を与えます。 しかし、統計によると、3 つの「見た目の良い」胚を移植するとプログラムは失敗し、「質の悪い」胚を移植すると非常に美しい子供が生まれることが示されています。
残念ながら、さらなる発育や子宮腔内への着床に必要な真の遺伝的可能性を評価することはできません。 多くの発生学研究室は胚の状態を評価するためにスコアスケールを使用していますが、統一されたスキームはまだ存在していません。 現在、この分野は世界中の発生学者によって集中的に研究されています。
非常に多くの場合、患者は発生学者に質問します。それは、「低品質の」胚がなんとか子宮に着床し発育を始めたとしても、最終的には「低品質の」子供になってしまうのではないかということです。 世界中の多くの研究室の経験が示しています。 そのような胚の移植から生まれた子供たちは、「高品質」の胚の移植から生まれた子供と同じくらい賢く、知的で、美しいです。 このような胚を移植する際に注意すべき唯一の点は、子宮内での発育と出産の可能性が低いことです。
子宮腔への胚の移植
実験室で得られた良質の胚は、非常に注意深く、最小限の外傷で子宮腔の子宮底部のほぼ中央まで移植する必要があるため、この段階は重要なポイントの 1 つです。
女性の場合、この手順は痛みがなく、追加の麻酔も必要ありません。 胚が入った特殊なカテーテルが子宮頸部から子宮腔に挿入され、超音波によって子宮腔が制御されます。
カテーテルが目的の位置に到達したら、胚を子宮腔に移し、カテーテルを取り外し、顕微鏡を使用して確認します(子宮腔への目的の胚の完全な導入を監視します)。 胚がまだカテーテル内に残っている場合は、この手順がすぐに繰り返され、その後カテーテルの状態が再チェックされます。
図 8 は、胚移植の超音波画像を示しています: 緑色 - 子宮頸部を通って子宮腔内へのカテーテルの移動:

図8。胚移植の超音波画像*
次の 1 時間、女性は横になり、身体活動をある程度制限する必要があります。 胚移植後 9 ~ 11 日後に、妊娠の存在を確認するために女性の血液中のヒト絨毛性ゴナドトロピンの含有量を検査することが推奨されます。
卵子の細胞質への精子の注入 (ICSI)
ICSI– 英語の略語 ICSI のロシア語音訳 – – マイクロマニピュレーターを使用して単一の精子を卵子の細胞質に注入(細胞質内精子注入)して受精させる。 x200~x400の倍率の顕微鏡下で実施されます。
下の写真は、卵子に精子を注入するために針を挿入するプロセスを示しています。



写真1。針を刺して卵子に精子を注入します。 この手順を実行すると、70〜85%のケースで体外受精が行われます。
ICSI の適応
1 つ以上のスペルモグラムパラメータの大幅な劣化。
抗精子抗体の存在;
精巣 (TESA) または精巣上体 (PESA) から外科的に精子を採取する場合、射精液中に精子が存在しない (無精子症)。
逆行性射精中に尿から精子を採取する。
標準的な体外受精手順の過去 2 回の試みで受精が不足している。
標準的な体外受精では受精率が低いと想定できる状況。たとえば、重度の子宮内膜症や原因不明の不妊症の患者などです。
この手順にはいくつかの段階が含まれます。
1. 卵母細胞を得るために過排卵を刺激した後の卵胞の穿刺;
2. 非常に細く鋭い針で 1 個の精子を採取します。
3. 顕微鏡下での卵子の細胞質への精子の導入。
4. 翌朝、受精を確認します。
多くの研究によると、ICSI 手順を使用した妊娠率は、標準的な体外受精プログラムを使用した妊娠率よりも大幅に高くなっています。
おそらくこれは、原則として、このプログラムに参加する女性は若くて生殖能力が高く(ICSIの適応が主に男性要因であるため)、結果として得られる卵子の品質の向上につながるという事実によるものと考えられます。パンクの。
また、顕微授精は、場合によっては「女性の適応」のためにも行われること、つまり、採卵できる卵子の数が少なく、卵巣予備能の減少に伴う品質があまり良くない場合にも実施されることにも留意すべきである。 。
精巣上体 (MESA) または精巣組織 (TESE) からの精子の抽出
残念ながら、一部の男性には射精液中に精子が含まれていないため、体外受精や顕微授精などの従来の方法では、必要な精子を取得するために追加の予備的な「ステップ」が必要です。 精子を取得する方法には次のようなものがあります。
-TESE(精巣精子採取)- 卵巣組織からの精子の抽出(回収)。
-MESA (顕微手術による精巣上体精子吸引術)– 精巣上体からの精子の顕微手術吸引。
-PESA(経皮的精巣上体精子吸引法)– 精巣上体からの精子の経皮的吸引。
MESA 手順を使用すると、他の技術と比較して最高の品質と十分な量の精子を取得することができます。 この手順は最も穏やかで、合併症も最小限に抑えられます。
これらの方法を実行する場合、原則として、体外受精が失敗した場合に備えて、凍結して次のサイクルで使用できる精子を最大数取得するよう努めます。
可用性 無精子症男性の場合(射精液中の精子の欠如)はいくつかの要因と関連している可能性があり、それが無精子症には 2 つのタイプがある理由です。
1) 閉塞性無精子症。
これは、精子が放出される管がある程度のレベルで遮断される、つまり射精が起こることを意味します。 この状態の原因は、手術(精管切除術)または先天性病理のいずれかである可能性があります。
つまり、このカテゴリーの男性では、精子自体は良好ですが、これらの「健康な」精子を得るには何らかの操作を行う必要があります。 この目的のために、次のいずれかのテクニックを使用できます。 ペザ、精巣上体から細い針で精子を採取する方法、または テセこの方法では、生検によって精巣そのものから精子が採取されます。 どちらの手術も局所麻酔下で外来で行われます。
閉塞性無精子症の患者では、予備診断生検で精子形成の存在が確認されていれば、TESE中の精子採取効率は100%になる傾向があります。
2) 非閉塞性無精子症。
これは、何かが精子の侵入を妨げるのではなく、精子の数が著しく減少するために、射精液中に精子が存在しない病態です。 一般に、これらの男性のほとんどは、精巣内に精子の生成が行われる小さな領域を持っているため、これらの男性は、精子形成が活発に行われている領域(TESE)を検出するために、いくつかの場所から精巣生検を受けます。
最近、そのような場合には、新しい技術であるmicroTESEが使用されています。microTESEでは、特別な手術用顕微鏡を使用して精巣生検が実行され、この操作中にすでに精巣のどのゾーンから採取する必要があるかを正確に決定できます。最大限の精子を得るために。
精巣マッピングと呼ばれる方法も使用される場合があります。 生検を行う前に、細い針を使用して睾丸の領域を検査し、その針で数か所から液体を採取し、すぐに精子の内容を検査します。 この方法により、TESE 手順を実行するときに「考慮する」必要がある睾丸の領域を特定することもできます。 原則として、受精に必要な精子は70%の確率で得られます。
上記の方法を使用する場合は、その後、受精の可能性を高めるためにICSI手順を使用することをお勧めします。
ゲームと受精卵の卵管への移動
これらは、胚 (英語、TET)、接合子 (英語、ZIFT)、または配偶子の卵管への移植 (GIFT) を含む ART 方法です。 いくつかの考えによれば、従来の胚移植のように子宮腔ではなく、卵管に細胞を「送達」するということです。 自然の受精プロセスに可能な限り近い、通常は卵管で発生します。

写真1。配偶子と受精卵の卵管への移動のメカニズム。
これらの手順には何が含まれますか?
TET では、卵子を取得し、研究室で夫の精子と「体外」で受精させ、受精から 2 日後に胚を卵管に移植します。
ZIFTは、受精後1日、つまり受精卵の段階での胚移植です。 どちらの手順も腹腔鏡検査の形式での手術を必要とし、その間に細胞を卵管に移します。
これらのメソッドは誰のためのものですか?
TETとZIFTは、卵管が通過可能で正常な機能状態にあり、子宮内癒着(癒着)がない場合、つまり子宮腔の状態が良好な場合、どの不妊カップルにも実施できます。
これらの処置は、子宮内授精処置が 4 ~ 6 サイクル以内に効果がない場合にも適応となることがあります。

図2.配偶子と接合子を卵管に移すプロセス。
TET/ZIFT (配偶子、接合子、または胚の卵管への移植) それとも従来の IVF (胚の子宮腔への直接移植)?
何がより良いのか、どのような場合に、何をすべきなのかという疑問が常に生じます。 現代医学における戦術は、医学的適応だけでなく、女性の希望によっても決定されます。 たとえば、他のすべての条件が同じであれば、卵管への配偶子または胚の移植に対する禁忌がない場合、女性は受精プロセスをできるだけ自然に近づけるためにこの特定の操作を実行することを主張します。 あるいは、腹腔鏡検査、つまり外科的介入に関連してそれを断固として拒否します。 さらに、各クリニックには独自の能力があり、何らかの方法に関して特定の立場に立っています。
ただし、以下に、あなた自身の意見を形成するのに役立ついくつかの事実を示します。
1. いくつかの研究によると、卵管に移動する場合の着床(つまり妊娠)の頻度は、子宮腔に移動する場合よりも大幅に高くなります。
2. ただし、ランダム化研究によると、卵管または子宮腔への移植を使用した場合に有意な差は見つかりませんでした。
3. TET プログラムなどに患者を含めるためのより正確な適応を決定するには、さらなる研究が必要です。
4. 特定の方法の有効性は、医師の資格だけでなく、特定の方法を使用した経験によっても決まると考えられています。
5. 卵管移植法の使用は、腹腔鏡検査の費用を含めてプログラム全体の費用を大幅に増加させます。
したがって、 サポーター これらの方法について彼らは言う
a) 高い効率について。
b) 自然のプロセスに最大限に近づくこと。
対戦相手 卵管への移行は次のように主張します
a) 卵管移植プログラムの効率が高いのは、このプログラムには実質的に健康な患者が含まれており(彼らは理想的な卵管と子宮腔を持っている)、不妊の主因はもっぱら男性であるという事実によるものです。これが理由です。高い妊娠率。
b) 配偶子または胚を移植する場合、腹腔鏡検査が使用されます。これは侵襲性が低い方法ではありますが、費用がかかることは言うまでもなく、外科的介入になります。
c) 子宮腔への移植に長年携わってきた不妊治療の医師は、当然のことながらより優れた治療を行います(子宮腔への移植のみに限定することもできます)。
d) 研究室で受精卵移植を使用する場合、受精卵はわずか 1 日で残りますが、卵管への胚移植を使用する場合は 2 日以内です。
卵管への移植に反対する人々によれば、この期間では、子宮腔に移植する場合(実験室での3〜5日目)に行われるような最良の胚の選択は不可能である。
一般に、データは矛盾しているため、特定の方法の選択は、さまざまな要因を考慮して毎回個別に決定されます。
ゲームと胚の冷凍保存
配偶子と胚の凍結保存 –精子、卵子、胚を特殊な低温環境で保存する技術です。
卵子凍結の技術は比較的新しいものですが、2007 年までに、解凍した卵子の受精と胚移植を経て、すでに世界中で 200 人の子供が誕生しています。
場合によっては、特に男性および女性のがんの場合、卵巣または精巣の切除が計画されている場合、および化学療法または放射線治療が必要な場合には、事前に生殖細胞を取得して凍結する必要があります。別々に、または受精後に。 このような患者さんのために、これらのプログラムが提供されています。 世界中のさまざまな研究室によると、凍結胚を移植した場合の平均妊娠率は約50%です。
胚は発生のどの段階でも凍結できます。 生後 1 日から始まり、胚盤胞期 (5 ~ 6 日) で終了しますが、「古い」胚を凍結することで、最高品質の胚を選択することができます。
凍結はどのようにして起こり、どのようにして起こり得るのでしょうか?
現在、摂氏マイナス 196 度の温度まで超急速冷凍し、液体窒素中でこの温度で保存するプロセスが使用されています。
物理的には、このプロセスはガラス化、つまり結晶化段階を迂回して液体がガラス状態に移行することです。 この効果は、セル温度を非常に急速に下げることによってのみ達成できます。 凍結中に形成される結晶は胚に損傷を与える可能性があるため、これは非常に重要な条件です。
この操作を実行する場合、「細胞内に漏出する」もの(プロパンジオールなど)と細胞外のもの(スクロースやリポタンパク質など)の 2 種類の凍結保護剤が必ず使用されます。 これらの物質により次のことが可能になります。
1. 凝固点を下げ、細胞内結晶(「氷塊」)の形成を防ぎます。
2. 細胞が状態を変化させ、密度が高くなったり硬くなったりするときに、細胞膜と相互作用することで細胞を保護します。
その後、胚は特別な容器に入れられ、解凍されるまで液体窒素中で適切な温度で保管されます。
胚はどのように解凍されるのですか?
女性の適切な準備の後、凍結胚の標識遵守の完全なチェックが実行され、その後室温で解凍されます。 このプロセスで最も重要なことは、解凍の時間ではなく、凍結保護剤を注意深く希釈することと、解凍後の胚による元の特性の保存です。
米国生殖医学会の倫理委員会は、胚凍結技術を使用した場合に妊娠率を高める以下の要因を特定しました。
1. 三つ子や四つ子が発生する可能性を減らすために最適な数の胚を移植する。
2. エストロゲンとプロゲステロンの含有量が正常値を超えない、刺激された周期ではなく自然な周期で胚を移植する。
3. 妊娠の可能性を高めるために、排卵誘発剤の量を可能な限り減らす。
リスクと失敗
胚凍結技術の最も重要な点は、急激な温度変化によるストレスの結果、一部の健康な胚が生存できない可能性があるという事実です。 平均して、原則として約 25 ~ 50% の胚が生存しません。
一方、冷凍保存はダーウィンの自然選択とみなすことができ、その過程で「最強」が生き残り、それが将来移転されることになります。
このテクノロジーを使用する際のもう 1 つの重要な問題は、子供が何らかの欠陥を持って生まれる可能性があることです。 多くの動物実験により、冷凍/解凍技術が欠陥のある動物の誕生をもたらさないことが示されています。 人間を対象とした研究では、集団内の他の小児と比較して、解凍胚の移植の結果として生まれた小児の異常の数に有意な増加はないことが示されています。 しかし、問題のこれらの側面は、妊娠率を高める機会と同様に、引き続き集中的に研究されています。
解凍された胚の移植の結果として妊娠が生じた場合、夫婦には残りの胚の運命を決定する権利が与えられます。 それらは凍結したままにすることも(最新のデータによると5〜10年間)、解凍することも、寄付して別の不妊の女性に移すこともできます。
代理出産
代理出産 -これは、卵子と精子の受精によって「体外」で得られた妊娠を代理母、つまり別の女性が運ぶART法の1つです。
これは、女性が卵子を取得し、男性が精子を取得する機会がある場合に必要ですが、子宮の状態(先天性または後天性の病状)または外科的介入後の子宮の欠如により妊娠が不可能な場合に必要です。
代理母を選ぶ際には、包括的な検査が実施され、医療文書が作成され、体外受精の結果得られた胚の移植に備えて代理母の体を準備するために、代理母の月経周期が不妊女性の周期と同期します。またはICSI。
代理出産プログラムとその法的根拠は、現在世界中で集中的に議論されている。なぜなら、この問題には医学的側面(特に、女性が代理出産に適しているかどうか)だけでなく、さまざまな問題も含まれているからである。合法化と明確化を必要とする倫理的問題について。
たとえば、オーストリア、ドイツ、ノルウェー、スウェーデン、フランス、および米国の一部の州では、代理出産が依然として禁止されています。 このプログラムはベルギー、ギリシャ、アイルランド、フィンランドで使用されているという事実にもかかわらず、その使用には法的根拠がありません。
代理母になることを計画している女性の要件は何ですか?
年齢 23 ~ 35 歳。
自分の子供が少なくとも 1 人いる。
もう自分の子供を持ちたくない人。
既婚またはシビルパートナーシップを結んでいる。
財政的に安定した財務状況。
この役割を果たすために愛する人のサポートと承認を得ること。
妊娠前少なくとも6か月間非喫煙者であること。
妊娠の状態を楽しむ。
不妊のカップルを助けたいという真剣な願望がある。
正常な身長と体重の女性。
彼女が妊娠している子供を持つ夫婦から要求された場合、中絶に同意する。 多胎妊娠における胚の減少も同様です。
一部の国には、代理母を選定する機関があります。
たとえば、以下は、ある代理店が提供するサービスの全範囲です。 25,000人形。
代理母センターのデータベースから代理母の候補を提供する。
代理母候補者の心理的適合性と代理母プログラムへの参加準備の心理的診断。
体外受精、妊娠、健康な子供の誕生に適しているかどうかを確認するための、代理母候補者の包括的な健康診断。
最初の法律相談。遺伝的親と代理母との間の合意書を作成し、顧客の個々の状況のあらゆるニュアンスを考慮し、「子供の出産に関する」合意書に必要な条項を導入します。
遺伝的親と代理母の間の最初の協議と合意書の作成の過程で翻訳者サービスを提供します。
子供の誕生と必要な書類の受領までのプログラムの調整と管理。
妊娠期間全体にわたる代理母への補償(段階的に支払い - 妊娠時に 10%、出産の 4 ~ 6 週間前に 90% - 資金が代理母の銀行口座に振り込まれます。
複数の子供が生まれた場合の代理母への補償。
妊娠 9 か月間の毎月の維持費 - 毎月支払われます。 妊娠中の医療監督 - クリニックサービスと必要なすべての検査の費用。
代理母のための事故に対する医療保険。
大使館にさらに提出するための子供のための書類の準備;
代理母と遺伝的親(顧客)との間で契約が締結された瞬間から、胚が代理母に移植されるまでのプログラムの管理およびサポートの費用。
代理母と遺伝的親(顧客)との間で契約を締結した瞬間から、妊娠の有無が確認されるまでのプログラムの管理およびサポートの費用。
ドナーへの補償、健康診断、当センターのサービスにかかる費用。
代理母の保護者による 24 時間の監視、すべての宿題の実施、医師への付き添い、行われた作業に関する完全な報告書、および別の住居の提供。
医療費は追加で支払われます。
ロシア連邦の現在の家族法(1995 年 12 月 8 日付け、第 2 部第 10 章第 4 節第 51 条第 4 項第 2 部)によれば、「互いに結婚しており、書面で同意を与えた者」胎児を産む目的で他の女性に胚を移植する場合、その子の両親は、その子を産んだ女性(代理母)の同意があった場合にのみ登録することができる。」
医療機関では、両当事者(代理母と将来の親)が必要な医療文書にのみ署名しますが、我が国の問題の法的側面は、適切なサービスの助けを借りて、このプロセスの参加者が独自に解決する必要があります(結論)合意の)。
オボドネーション
オボドネーション、または 卵子提供、ドナー卵子を受精に利用するART法の一つです。
この方法は 1982 年に初めて使用に成功し、現在まで、例えば米国では毎年約 15,000 個のドナー卵子が受精に使用されています。 この技術を使用した体外受精の平均効率は約 50% です。
この方法を使用する場合の適応は何ですか?
1. この方法の使用の主な適応症は、女性に卵母細胞(卵子を含む)が存在しないことであり、これは次のことに関連します。
自然閉経。
卵巣予備能の減少(発育異常、早発卵巣不全症候群、卵巣の除去または切除後の状態、放射線療法または化学療法)。
2. 正常な数の卵子に遺伝子異常があり、受精に使用できない。
通常、卵子提供者は次のいずれかです。
1. 妊娠を希望する患者の親族。
2. 専門の医療機関から職業、容姿、血液型等を記載した名簿を入手できる特別なドナー。
卵子提供者は、34 歳未満で、健康な子供がおり、目立った身体的特徴を持たない必要があります。
卵子提供者は排卵刺激を受け(その周期は妊婦の周期と同期しています)、続いて卵胞を穿刺して卵子を採取し、体外受精プロセスのすべての段階を経ます。
免疫疾患が原因で流産を繰り返す女性における体外受精後の妊娠の管理
P反復流産に苦しむ女性は、妊娠第 1 学期における着床障害および胎盤形成障害のリスクグループとなります。 このような障害は、ほとんどの場合、子宮内膜と発達中の栄養膜細胞との間の免疫相互作用によって引き起こされます。
体外受精(IVF)を受ける女性は通常、ホルモンの問題を抱え、慢性炎症性疾患を患い、その結果、骨盤領域に癒着が生じ、子宮、卵巣、卵管に対して 1 回以上の外科的介入を受けていることがよくあります。 同時に、生殖補助医療の使用によって解決できる妊娠達成の困難は免疫学的問題と組み合わされ、場合によっては早期の生殖喪失を繰り返すことになります。 胎児喪失を繰り返す患者では、免疫病理学的プロセスが妊娠の初期段階から活性化されると、いわゆる悪循環が形成されます。
子宮内膜のナチュラルキラー細胞の活性の抑制や母体による遮断因子の産生といった、妊娠初期における免疫系の保護機能は、主にホルモンに依存するさまざまなメカニズムによって提供されます。これに違反すると、着床不全や早期の自然流産が引き起こされます。
自己免疫プロセスでは、免疫系の攻撃の標的は母親自身の組織です。 抗体応答はそれ自身の抗原に対して向けられます。 発育中の卵子は、栄養膜血管の血栓症の結果として影響を受け、その侵入が制限されますが、場合によっては、発育中の胎盤のリン脂質に対する自己抗体の直接的な損傷効果の結果として影響を受けます。 同種免疫反応では、女性の免疫反応は父親から受け取った胎児抗原に対して向けられ、これにより子宮内膜での完全な防御反応の形成も妨げられます。
この点において、子宮内膜における免疫相互作用を正常化し、一連の病理学的変化を防ぐことができる妊娠前の準備の問題は、特に体外受精プログラムに参加している夫婦にとって非常に重要になります。
さらに、高用量のホルモン剤を使用して排卵を刺激する計画は、女性の免疫学的、ホルモン学的、止血学的状態の変化を引き起こすため、タイムリーな診断と修正が必要です。 体外受精後の妊娠管理には、自然流産を防ぐために妊娠の初期段階から高度な医療の提供が必要です。
上記を踏まえると 研究の目的は、体外受精前の反復性流産、自己免疫病理および同種異系免疫病理を患う女性の診断と治療のためのアルゴリズムの開発でした。
材料と研究方法
私たちは、2 回以上の流産歴があり、体外受精を計画している 60 組の夫婦を検査、治療し、前向きに観察しました。 すべての患者は、ロシア医学アカデミー産科・婦人科・周産期科学センターのONBスキームに従って、機能診断検査、ホルモン状態の研究、狼瘡抗凝固物質の測定、ヒト絨毛性ゴナドトロピンに対する抗体、生化学的パラメータ、細菌学的検査、ウイルス学的検査、超音波診断およびX線診断、遺伝カウンセリング、および夫の精子検査。
上記に加えて、以下のことを実施しました。
夫婦における主要組織適合性複合体 (HLA) クラス I および II の抗原産物の研究 - 遺伝子座 A、B、C、DR、DQa、DQb。
b 2 -糖タンパク質、アネキシン、プロトロンビン、ホスファチジルコリン、ホスファチジルセリン、ホスファチジルイノシトール、スフィンゴミエリン、カルジオリピンに対する抗体の循環の研究。
自己免疫病理が特定された女性における天然抗凝固剤 - アンチトロンビン III、プロテイン C および S の活性の測定。
妊娠前およびヒト絨毛性ゴナドトロピンの b サブユニットの最初の陽性指標を受け取った後の経時的な血管内血栓形成マーカー (D ダイマー、フィブリンモノマーの可溶性複合体) の研究による止血学的制御。
研究結果と考察
詳細な検査の後、免疫疾患と診断された60組の夫婦が観察グループに選ばれ、そのうち32組が同種免疫病理、28組が自己免疫問題を抱えていた。 女性の平均年齢は32.0±4.2歳で、女性の66.7%が30歳以上であった。
このグループの女性の体細胞性罹患率を分析したところ、4.5±0.21 という高い感染指数が認められました。 心血管系の疾患は主に低緊張型または高血圧型の栄養血管ジストニアで代表され、1 人の患者は逆流のないグレード I の僧帽弁逸脱を患っていた。 呼吸器疾患は慢性気管支炎として現れました。 消化管の疾患としては、胃炎、胃潰瘍、胆道ジスキネジアなどが挙げられます。 このグループの患者の 25% は、慢性腎盂腎炎および膀胱炎の形で泌尿器系の疾患を患っていました。 5 人 (8.3%) の女性の甲状腺の病状は、潜在性甲状腺機能低下症の症状を伴う自己免疫性甲状腺炎でした。
婦人科病理の構造を分析したところ、女性の 30% に子宮頸部異視症の病歴があることが明らかになりました。 生殖器の炎症性疾患は46.7%が慢性子宮内膜炎と慢性卵管卵巣炎であった。 希発月経は女性の10%に観察されました。
婦人科手術は腹腔鏡アクセスを使用してすべての患者に実施されました。3 例 (5.0%) の患者で筋腫切除術が行われました。 1 例 (1.7%) の患者で子宮内中隔の切除。 6人(10%)が卵管妊娠のための卵管切除術。 類内膜嚢胞の存在による卵巣切除 1 例 (1.7%)。 1人(1.7%)の女性で両卵巣の焼灼、4人(6.7%)の女性で外生殖器子宮内膜症の病巣の凝固。
高アンドロゲン症の形でのホルモン障害が女性の 20% に発生し、以前の妊娠の喪失はグルココルチコイドの服用中に発生しました。 高プロラクチン血症は女性の8.3%で観察され、黄体期欠乏症は40%で観察されました。
検査を受けた女性の妊娠の大部分 (全妊娠の 179 ~ 84%) は、妊娠第 1 期に自然に終了しました。
このうち、流産は妊娠 5 ~ 8 週目に最も多く観察されます (50.7%)。 9~12週目での流産は、全妊娠の11.7%で21.6%、無胎芽症とやや頻度が低かった。
研究では、HLAシステムの3つ以上の共通対立遺伝子を持ち、習慣的流産の同種免疫因子を持つ32組の夫婦が選ばれた。
HLA クラス I システムの抗原を分析すると、反復流産グループの男性では B35 抗原の発生頻度の統計的に有意な増加が認められました。遺伝子頻度は集団の 0.071 と比較して 0.162 でした (p<0,05).
流産を繰り返したグループでは、男性と女性の両方で、A11 抗原が検出される頻度が集団よりも有意に低かった (p<0,05 и p<0,01 сооответственно), у женщин достоверно реже отмечены антигены В7 (p<0,05), Cw4 (p<0,01), у мужчин – Cw2 (p<0,05).
HLA クラス I 互換性を持つカップルでは、A 遺伝子座の抗原の一致がはるかに一般的です (87.7%)。 しかし、史上最も多くの流産が発生するのは、HLA クラス II システムの 3 つの対立遺伝子に適合するカップルです。 したがって、ペアの 50% が 3 つの遺伝子座すべてに共通の対立遺伝子を持っていました。 2 つの遺伝子座で対立遺伝子を共有する残りの 16 対のうち、DQA1 と DQB1 の組み合わせが優勢でした。
遺伝子座内の共通対立遺伝子の出現に関しては、DQA1 遺伝子座が 81.3% で優勢です。 DQA1 および DQB1 遺伝子座における 0201 対立遺伝子の出現の定量的分析では、男性における 0201 対立遺伝子の優位性が、症例の 28.1% で DQA1 遺伝子座で、症例の 31.3% で DQB1 遺伝子座で認められました。 女性では、対立遺伝子 0201 の出現率はそれぞれ 9.4 % と 12.5% と大幅に低かった。 私たちは、集団のデータと比較して、男性の DQA1 遺伝子座における対立遺伝子 0201 の出現頻度が大幅に増加していることを発見しました (p<0,001).
HLA適合性が確認されたカップルは、能動免疫と受動免疫からなる受胎前の準備コースを受けました。 能動免疫の場合、目的の体外受精の 1 か月前、月経周期の 5 ~ 8 日目にドナー細胞を用いたリンパ球免疫療法 (LIT) が使用されました。 4 週間後、IVF を背景に LIT を繰り返しました。 胚移植後、10%免疫グロブリン製剤(Gamimun-N 50ml、Gamunex 50ml)または5%イントラグロビン製剤 50mlによる受動免疫の形で免疫グロブリン点滴療法が処方されました。 妊娠が起こった場合、初期段階から血管内凝固マーカーの測定および必要に応じて低分子量ヘパリンによる補正を伴う止血学的モニタリングが実施された。 免疫調節の目的で、胎児拒絶反応を抑制するために、妊娠初期から妊娠 16 週までジドロゲステロンが 30 mg/日の用量で使用されました。 LIT手順は妊娠16週まで4週間間隔で繰り返されました。
自己免疫病理を患う28人の女性の妊娠の準備には、自己免疫の重症度を軽減するために骨盤臓器の慢性炎症過程の特定と強制的な治療が含まれ、その後、抗凝固薬、抗血小板薬、コルチコステロイド療法が処方されました。
自己免疫病理のマーカーの中で最も有益なのは、抗リン脂質抗体の補因子である b 2 - 糖タンパク質、アネキシン、プロトロンビンに対する自己抗体であり、これは文献データと一致しています。 したがって、すでに妊娠期間外で、トロンボエラストグラフィーによる凝固亢進、血管内血栓形成マーカー(Dダイマー、フィブリンモノマーの可溶性複合体)の存在によって現れる止血系の障害が女性の64.3%で記録され、陽性反応を示した。ループス抗凝固物質の検査は 21.4% の女性にのみ認められました。 抗カルジオリピン自己抗体を検出するための検査はより感度が高く、症例の 75% で中力価および高力価で検出されました。 特定の補因子に対する自己抗体の存在を調べる検査では、89.3%の女性が陽性反応を示しました。これはおそらく、妊娠の初期段階から自己免疫プロセスが進行する素因を示していると考えられます。
体外受精の即時準備プログラムには、凝固検査および止血図パラメーターの変化によって明らかな自己免疫プロセスの活動性が顕著な女性の 25% に対する治療的血漿交換 (PA) が含まれていました。 治療用 PA は体外受精の 1 か月前に処方され、循環血液から免疫複合体や自己抗体を除去し、内因性物質や薬用物質に対する感受性を高めることが可能になりました。 他のケースでは、胚移植後の体外受精プログラムで低分子量ヘパリン(ナドロパリン、エノキサパリン、ダルテパリン)が処方され、妊娠後も治療が継続されました。 免疫調節のために、低用量のコルチコステロイド (メチプレド 2 ~ 4 mg) とジドロゲステロン (1 日あたり 30 mg) が処方されました。 3 人の患者では、妊娠の第 1 学期に反復的な治療的 PA が必要でした。
一般に、体外受精後、同種免疫病理を有する女性 12 名 (37.5%) と自己免疫疾患を有する女性 11 名 (39.3%) で妊娠が起こりました。
すべての女性の妊娠初期の管理には、慎重な止血学的モニタリングとその後の指標の修正が含まれており、自己免疫疾患のあるグループでは症例の90.9%に低分子量ヘパリンが使用され、同種免疫病理のあるグループでは症例の25%に低分子量ヘパリンが使用されました。
免疫調節の目的で、すべての患者にジドロゲステロンが 30 mg/日の用量で使用されました。 近年、免疫担当子宮内膜細胞上のプロゲステロン受容体の活性化によるこの薬剤の免疫矯正効果が証明されています。 次のリンクは、プロゲステロン誘導性遮断因子の影響下での防御免疫調節です。これは、ナチュラルキラー細胞とリンホカイン活性化細胞の活性を低下させ、調節サイトカイン (インターロイキン 4、10) の合成を誘導し、胚の成長過程を抑制します。拒絶反応と正常な栄養膜侵入の確保。 一方で、炎症反応や血栓形成反応を引き起こすサイトカイン(腫瘍壊死因子、インターロイキン1、γ-インターフェロンなど)の産生は抑制されます。
メチプレド(メチルプレドニゾロン)は、自己免疫プロセスのある患者に、2~6 mg/日の用量で、妊娠初期に免疫グロブリンの点滴静注と組み合わせて、5 g(10% ガミムン 50 ml)の用量で少なくとも 1 回処方されました。溶液または100mlの5%イントラグロビン溶液)。 同種免疫疾患のある女性は、LIT および免疫グロブリン療法を継続しました。
体外受精後の免疫障害のある女性 23 人のうち、21 人(91.3%)は妊娠を第 2 学期まで延長しました。 2つの観察では、同種免疫疾患のある女性で無胎児症が認められました。 データを分析したところ、ある症例では患者の夫が DQA1 遺伝子座に対立遺伝子 0201 を持っていたことが判明しました。これは、多くの著者が、無胎児症の発症にとって好ましくない予後兆候であると考えています。 自己免疫病理のあるグループでは、妊娠第 1 期に妊娠喪失はありませんでした。
したがって、妊娠以外の免疫病理学的プロセスの性質を研究することは、体外受精前の個々の治療計画の選択において幅広い展望を開き、明らかに、妊娠の開始と延長を目的とした対策の有効性を高めることになるでしょう。
考えられる合併症。 多胎妊娠
この方法を使用して妊娠の可能性を高めるには エコ、原則として、複数の胚(最大3つ)が女性の子宮に移植されます。 場合によっては、これが多胎妊娠の発症につながる可能性があります。
子宮内で 2 つ以上の胎児が発育する場合、そのような妊娠を行うのは非常に困難になる可能性があります。 他の胚に影響を与えることなく、1 つの胚の発育を停止する方法があります。 この手術は減胎と呼ばれ、超音波ガイド下で行われます。 通常、2つの胚が残ります。 減胎後、妊娠を出産まで無事に継続できる可能性は、三つ子を残す場合よりも高くなります。
子宮外妊娠
胚を子宮腔に移植した後、衰弱、めまい、妊娠の初期の兆候、下腹部の漠然としたまたは鋭い痛みなどが現れた場合、おそらくこれは子宮内で胎児が発育しない子宮外妊娠である可能性があります。 、ただし、たとえば卵管内です。 この場合、パイプが破裂して重度の出血を引き起こす可能性があるため、この状態は生命を脅かすため、すぐに医師に相談してください。 4週間以上の子宮外妊娠の場合、子宮腔内の胎児卵子は超音波検査で見えませんが、妊娠検査薬(hCG)は陽性になります。 子宮外妊娠は通常、穏やかな腹腔鏡手術で治療されます。 上記の症状が発生した場合は、すぐに医師の診察を受けてください。 このパンフレットの最後のページにクリニックの電話番号と医師の名前を書き留めてください。 緊急電話番号も調べておきましょう。 医師の推奨事項にすべて従うことで、合併症のリスクが軽減され、幸せな妊娠の可能性が高まります。
卵巣過剰刺激症候群
生殖補助医療の目標は健康な子どもを生むことですが、生殖補助医療による妊娠の産科転帰は、卵巣過剰刺激症候群 (OHSS) によって複雑になりますが、このことについては依然として十分に理解されていません。
OHSS は、生殖補助医療で使用する卵子と胚の数を増やすために行われる超生理学的卵巣刺激の合併症です。 イスラエルからの 10 年間のデータの最近の分析では、OHSS の発生率が増加していることが判明し、この合併症の「流行」の存在が示唆されました。 驚くべきことに、同じ著者らは、1987年1月から1996年12月の間にイスラエルで重度または重度のOHSSを合併した104件の体外妊娠で有害な転帰の発生率が高かったことも報告した。流産、早産、低出生体重、妊娠糖尿病、高血圧の発生率。さまざまな国の報告によると、そのような妊娠では胎盤早期剥離がより多く発生しました。
この記事では、OHSS と妊娠の有害転帰との関連性を予想する根拠を検討します。
好ましくない産科転帰との関連メカニズム 超生理学的卵巣刺激
自然妊娠と補助妊娠の間の流産の相対リスクに関するさまざまな研究で得られたデータの解釈を困難にする要因 (カップルの臨床的特徴、女性の年齢、妊娠検出の精度) が多数あります。 生殖補助医療は、明らかな OHSS がない場合でも、卵巣の超生理学的刺激と関連しており、その結果、「自然な」周期よりも高いレベルのエストラジオールが生じます。 OHSS は、刺激に対する卵巣の反応が最大の場合に発生する可能性が高くなります。 アッシュら。 彼らは、ピークエストラジオール濃度と卵子数が流産率にほとんど影響を及ぼさないことを発見しました。 これは、卵巣反応の程度自体は、合併症のない体外受精周期と比較して、OHSS合併症の場合の流産のリスクを増加させないことを示唆しています。
病態生理学
重度の OHSS の病態生理学には、血管透過性の増加を伴う重度の全身血管機能不全、第 3 空間への体液の漏出、および血管内脱水症が含まれます。 重篤な場合には、血栓塞栓症、腎不全、およびその後の低血圧、低酸素血症、電解質不均衡を伴う成人呼吸窮迫症候群が発生する可能性があります。
これらの現象は妊娠初期に悪影響を与える可能性があります。 重度の OHSS の一部の症例で認められる全身性凝固障害は、移植プロセスに影響を与える可能性があります。
着床障害は流産につながったり、その後子癇前症や胎盤機能不全として現れたりする可能性があります。 OHSS における免疫系と免疫メディエーターの役割はますます明らかになりつつあります。 重度の OHSS は、血清および腹水中の高レベルの炎症誘発性サイトカインおよび血管内皮増殖因子と関連しています。
着床時の主に炎症促進性の Th-1 反応が自然流産と関連していることが示唆されています。 重度の OHSS は、流産のリスクが増加する可能性が最も高い状態と言えます。
典型的なやりとり。 OHSS と妊娠の有害転帰との関係は、それらに共通する危険因子によって説明されます。 多嚢胞性卵巣症候群の患者は、性腺刺激刺激に対して過剰反応する可能性が高く、OHSSを発症するリスクが高くなります。 また、それらの場合、ゴナドトロピン放出ホルモン作動薬(AGTRH)を使用しないその後の生殖補助治療は効果がない可能性があります。 多嚢胞性卵巣症候群の女性における流産のリスクの増加は、OHSSのリスクの増加ではなく、黄体形成ホルモンの過剰分泌と関連しており、これはAGTRHを使用して下垂体を抑制することで修正できます。
正常な卵巣形態を持つ女性の 332 周期と女性の 97 周期の比較研究が行われました。 治療の一環としてAGTRHを受けており、臨床症状はないが超音波検査で確認された多嚢胞性卵巣を患っている。 卵巣の形態が変化したグループでは、OHSS がより頻繁に発症しましたが (10.3 対 0.3%)、流産のリスクには差がありませんでした (6.9 対 11.1%)。
一部の女性は、サイトカインプロファイルの異常により、サイトカイン産生や非炎症性サイトカインと炎症性サイトカインのバランスが変化するために、OHSS と不良な産科転帰の両方を発症する遺伝的に決定された素因を持っている可能性があります。 TNF-α 遺伝子については遺伝子多型が報告されており、その一部の対立遺伝子はこの炎症誘発性サイトカインの発現増加に関連しています。 TNF 1 対立遺伝子の優位性は、子癇前症における TNF-α mRNA の発現増加を説明できる可能性があります。 OHSS の女性では血清および腹水中の TNF-α レベルが増加しましたが、OHSS の女性における TNF-α 遺伝子多型の有病率は研究されていません。
黄体期の後半に発症する OHSS (「後期」OHSS) は、移植された胚によるヒト絨毛性ゴナドトロピンの放出を特徴とし、受胎と関連しています。 多胎妊娠におけるヒト絨毛性性腺刺激ホルモンのレベルは単胎妊娠よりも高く、このことが、このような女性では初期 OHSS よりも後期 OHSS の発生率が高い、またはそのような女性が存在しないことを説明しています。 多胎妊娠がより頻繁に発生することも、OHSS という合併症が存在する場合には、そうでない場合よりも好ましくない結果が予想されるもう 1 つの理由です。 多胎妊娠は単胎に比べて早産や低出生体重児のリスクが最も高くなります。
妊娠転帰研究。 明らかに、OHSS と妊娠の有害転帰との関連には理論的根拠があります。 しかし、このテーマに関する文献は限られており、明確な結論は得られていません。 アブラモフらによる研究に加えて、 、他の2つは、OHSSによって複雑化された体外受精周期中の流産の頻度の研究に専念しています。 そしてそのうちの 1 つだけが OHSS ありとなしのサイクルを比較しています (対照グループ)。 チェンら。 OHSSを伴う周期と伴わない周期の間で流産率に有意差は見られなかった(それぞれ15回中4回(26.7%)対110回中19回(17.2%))。 マクドゥーガルら。 は、OHSS を合併した体外妊娠 14 件 (28.6%) のうち 4 件が流産したと報告しました。 OHSS を伴わない一期妊娠に関するデータは、Caspi et al. によってのみ得られました。 彼らは、OHSSを伴うHHTサイクルでは流産率が高いことを指摘しました(それぞれ29人中10人(34.5%)対114人中20人(17.5%))。 他の 2 つの研究では、ゴナドトロピン療法後の OHSS 患者の流産の発生率を調査しました。 シェンカーとワインスタインは流産率40%(10人中4人)と報告し、Rabauらは流産率40%(10人中4人)であると報告した。 – 約 25% (4 人に 1 人)。 これらの研究のほとんどが流産率を主要評価項目として報告していないことは注目に値します。 これらの研究のうち 2 つを除くすべての研究は管理が不十分であり、Abramov らの研究を除いては行われませんでした。 少数の患者から得られたデータを提示します。 1995年1月1日から1998年9月30日までに、中等度または重度のOHSSを合併した41件の妊娠がブリストル大学の体外受精サービスによって実施された。 流産率は、このグループと、卵管水腫またはOHSSのない40歳未満の女性の補助妊娠501人の対照グループとの間で有意な差はなかった。 自然胎児死亡率は 2 つのグループ間で有意な差はありませんでした (表 1)。
文献では、OHSS を合併した妊娠の in vitro 周産期転帰を記載した Abramov らを除いて、単一の研究は見つかりませんでした。 私たちのセンターでは、OHSS を合併した妊娠 36 件と合併症のない 546 件の出産 (女性は 40 歳未満) を同時に検査しました。 OHSS のグループでは、多胎妊娠と早産がより一般的でしたが、その差は統計的に有意ではありませんでした (表 2)。
OHSS を持つ母親から生まれた新生児の体重中央値は、対照と比較して有意に低かったが、単胎妊娠の場合、その差は有意ではなかった。
アブラモフらのデータは、 彼らはOHSSと流産との関連性を示しているが、OHSSのない妊娠における流産率に関するイスラエルのデータと比較していない。 彼らの患者の流産のリスクは、過去 10 年間のさまざまな時期のさまざまな国の一般的な体外集団と比較して高くなります。 しかし、既存の偏見、患者の年齢、妊娠の診断基準、多嚢胞性卵巣症候群の存在、多胎妊娠のケースなどの要因により、同等の対照群が存在しないため、データの評価が困難になります。 対照群を含む体外妊娠を調べた唯一の研究では、OHSSありとなしの周期で流産率に有意差は見られず、これは我々のデータと一致している。 私たちの対照研究の結果とアブラモフらによる研究の違いは次のとおりです。 アブラモフグループでは多胎妊娠の発生率が高いこと、あるいはおそらくOHSSの重症度が高いことと関連している可能性がある。 最後に、我々の研究でOHSS患者の低出生体重児と早産の発生率が高いのは、このグループの多胎妊娠の数が多いためである可能性があります。
結論
OHSS自体が妊娠の進行に悪影響を与えるかどうかについては、未解決の疑問が残っています。 OHSS が生殖補助医療による妊娠の結果に悪影響を与えることが証明できれば、産科に影響を与えるだけでなく、生殖補助医療で使用されている一般的な卵巣過剰刺激療法にも大きな影響を与えることになるでしょう。 プロセスをより生理学的にし、超生理学的卵巣刺激による即時的および長期的な結果のリスクを軽減するために、最大の卵巣反応を引き起こさない「より穏やかな」刺激レジメンが実行されました。 OHSSを合併した妊娠の産科転帰がOHSSを伴わない妊娠よりも悪いことが研究で示されれば、これは最大限の卵巣刺激を避けるための議論となるだろう。 現在までのところ、OHSS と不良な産科転帰との関連性を裏付ける唯一の管理されたデータはありません。 しかし、この問題は未解決のままであり、生殖補助医療の使用により発生し、OHSSにより複雑化した妊娠を同等の対照群と比較する研究が必要である。
妊娠– 新しい個体の受胎によって引き起こされる生物学的状態。
不妊– 出産適齢期の人が子孫を残すことができないこと。 女性が避妊手段や方法を使用せずに通常の性交から1年以内に妊娠しない場合、その結婚は不妊とみなされます。
不妊は、かなり広範な医学的、心理社会的、倫理的な概念です。 このような場合は、医師の診察を受け、妊娠しない理由を特定する必要があります。
女性の不妊症の原因は非常に多様ですが、主な要因は次の 3 つです。
子宮。
卵管腹膜(卵管の閉塞、癒着)。
神経内分泌(多嚢胞性卵巣症候群(PCOS)または高プロラクチン血症に関連する排卵障害)。
免疫学的障害、例えば、抗精子抗体の存在や、目に見える原因が存在しない原因不明の不妊症も注目されています。
これらの形態の女性不妊症の治療の最初の段階は、治療または外科的矯正です。 これでも結果が得られない場合は、体外受精および PE プログラムが問題の解決策になる可能性があります。
さらに複雑な条件は次のとおりです。
卵巣に自分の卵子がない。
生殖腺の形成不全、例えばシェレシェフスキー・ターナー症候群。
がんの化学療法。
卵巣の外科的除去。
遺伝子異常。
男性不妊の原因には次のようなものがあります。
生殖器官の発達の先天異常(停留精巣など)。
有害な環境要因の影響;
アレルギーと免疫システムの低下。
薬物の管理されていない使用(アナボリックステロイドや麻薬を含む)。
性感染症;
ストレス要因;
体を動かさない生活;
アルコール依存症と喫煙。
生殖器の損傷;
さまざまなホルモン障害、たとえば、FSH レベルの低下、副腎の形成不全および過形成、糖尿病、甲状腺疾患など。
高FSHレベルを背景とした精子形成の欠如;
クラインフェルター症候群(XXY核型)などの先天性遺伝子異常。
がんの化学療法。
VRT- 生殖補助技術。 生殖補助医療とは次のことを意味します。
夫の精子による子宮内授精
体外受精で
顕微操作ICSIを用いた体外受精(ICSI)
ART におけるドナー精子の使用。
ART の主なメソッドとプログラムの名前の略語のリスト:
エコ- 体外受精で
PE- 子宮腔への胚の移植
贈り物- 配偶子の卵管への移動
ジフト- 卵管への受精卵の移動
AI- 人工授精
IISD- ドナー精子による人工授精
IISM・夫の精子を使った人工授精
ICSI- 卵母細胞の細胞質への精子の注入
ISO- 過排卵の誘発
メサ- 精巣上体からの精子の吸引
ペザ- 精巣上体からの経皮的精子吸引
論文- 精巣組織からの精子の吸引
テセ- 精巣組織からの精子の抽出
EIFT- 卵管への胚の移植。
夫(ドナー)の精子による授精 - ISM (ISD))。 人工授精は最も古い不妊治療法です。 種子が導入されるプロセスを描いたフレスコ画が私たちに届きました。 人工授精は、卵管開通がある内分泌性不妊症、免疫性不妊症、男性不妊症の一部のケースで行われます。 妊娠に適した日に、女性の精子は夫またはドナーから子宮腔に注入されます。
子宮腔への直接精子の導入には、子宮頸部に精子が人工的に通過することが含まれますが、自然妊娠を試みる場合、子宮頸部不妊症により死亡する可能性があります。 この手順を実行するには、少なくとも 1 つの卵管開存があることが前提条件です。
体外受精(ラテン語で体外受精) -この手順の本質は、女性の卵巣から成熟した卵子を採取し、夫の精子(または配偶者双方の希望に応じてドナーの精子)で受精させ、得られた胚を保育器で48~72時間成長させ、胚を患者の子宮に移植(再移植)します。
IVF 手順は次の段階で構成されます。
患者の選択と検査;
卵胞形成および子宮内膜発達のモニタリング(超音波を使用した卵胞成熟および子宮内膜成長のモニタリング)を含む、過排卵の誘発。 刺激の目的は、妊娠の可能性を高めるために両方の卵巣に多数の成熟卵子を採取することです。 SSOは、事前検査の結果に基づいて、夫婦ごとに個別に選択されるさまざまな現代のホルモン剤を使用して実行されます。
卵胞の穿刺(卵胞の穿刺は、静脈麻酔と超音波制御下で膣の外側円蓋を通して行われます)。 この日、患者の夫は精子を提供し、特別な治療を受けます。
インビトロでの卵母細胞の授精と胚の培養。
子宮腔への胚の移植。 胚移植は、卵胞穿刺後2、3、または5日目に子宮頸部を介して特別なカテーテルを使用して行われます。 原則として、これには特別な準備は必要ありません。 通常は2個の胚を移植します。 患者が何度も移植を試みた場合、または胚の品質が悪い場合は、2 つ以上の胚の移植が可能です。 残った良質な胚は冷凍保存されます。 試みが失敗した場合、これらの胚はその後の移植に使用されます。
刺激された月経周期の黄体期をサポートします。 胚移植後は、妊娠をサポートするための薬が 2 週間処方されます。
妊娠初期の診断。 2週間後、女性は妊娠しているかどうかを判断するためにβhCGのために献血します。 研究の結果に応じて、患者を管理するためのさらなる戦術が決定されます。
体外受精は、過排卵を誘発せずに自然な月経周期でも可能です。
体外受精の適応:
治療できない不妊症、または他の方法よりも体外受精の方が克服できる可能性が高い不妊症。 禁忌がない限り、あらゆる形態の不妊症に対して夫婦(未婚女性)の希望に応じて体外受精を行うことができます。
体外受精の禁忌:
妊娠および出産の禁忌となる身体疾患および精神疾患。
胚の着床や妊娠が不可能な子宮腔の先天奇形または後天的変形。
卵巣腫瘍;
外科的治療が必要な子宮の良性腫瘍。
あらゆる局在性の急性炎症性疾患。
病歴を含むあらゆる場所の悪性新生物。
不妊婚に対する有能かつ効果的な治療は、泌尿器科医、婦人科医、体外受精の専門家間の明確な相互作用によってのみ可能です。 妊孕性を回復するために考えられるすべての方法について患者に十分に知らせ、成功した手段の割合と自分と妻の合併症のリスクを示すことが義務付けられています。
卵子の細胞質への精子の注入 (ICSI)。 ICSI プログラムは、重度の男性不妊症に対して実施されるだけでなく、夫婦の生殖に関する健康の個々の特性に関連する場合もあります。 妻から得た卵子の受精は、卵子の細胞質に精子を導入することによって行われます。
体外受精で卵子の受精が不可能な場合には、顕微操作法ICSIが使用されます。
細胞質内精子注入 (ICSI) 技術の本質は、顕微鏡下で、微細な顕微手術手順を使用して、単一の精子を成熟卵子の細胞質に注入することです。 これは、通常、重度の男性不妊症のカップルに子供がいない理由である自然受精の不可能性の壁を克服します。 ICSI の使用適応は最近拡大しました。 この方法は、以前の体外受精プログラムで受精しなかった場合、卵子の数が少ない場合、卵の殻が厚い場合などにも使用されます。
ICSI は、次のタイプの男性の病理に使用されます。
重い 乏精子症(射精液中の精子の濃度は1mlあたり1,000万未満、つまり卵子の自然受精が実質的に不可能になるほど低い)。
無力精子症あらゆる形で 乏精子症(射精液中の総精子濃度が 1 ml あたり 2,000 万個未満であるにもかかわらず、活発に運動する精子は 30% 未満)。
無精子症精巣または精巣上体の穿刺中に運動精子が検出された場合、さまざまな原因の(射精液中に成熟精子が欠如している)可能性があります。
生殖補助医療プログラムで ICSI 技術を使用した世界の経験は、この手順が生まれた子供の健康に影響を与えないことを示しています。 ただし、男性不妊の原因が遺伝的疾患に関連している場合、ICSIを使用すると、これらの疾患が精子の染色体とともに息子に受け継がれることに留意する必要があります。 重度の精子形成障害を持つ男性の予備検査は、先天性病状をもつ子孫の誕生を避けるのに役立ちます ICIS - 細胞質内精子注入。
卵子提供。 卵子提供プログラムにより、卵巣に卵子がない女性や、胎児に遺伝性疾患のリスクが高い女性も、健康な子どもを妊娠・出産することができます。 このような場合、卵子は健康な女性のドナーから採取されます。
代理出産。「代理出産」プログラムは、さまざまな理由で子宮を摘出した女性や、重篤な病気により妊娠を禁忌とされている女性に子供を産む機会を与えるものである。 このような場合には、不妊のカップルの卵子と精子が使用されます。 得られた胚は、健康な女性、つまり「代理母」の子宮腔に移植されます。
代理母から生まれた子供の登録に関連する法的問題が数多くあるため、妊娠の開始と胎児の妊娠は背景に消えてしまうことがあります。
すべての国で実の親が子どもに対する権利を保持しているわけではありません。 そして、「代理母」は、家族が法律で保護されていない場合、いわゆる「代理」訴訟に訴えることができます。 子どもが生まれた後、両親は子どもを引き渡すことを拒否し、養育費などのすべての費用を子どもに負担させる。
代理母の要件:
年齢は20歳から35歳まで。
自分自身の健康な子供を持つこと。
精神的および身体的健康。
胚の凍結。このプログラムは、IVF (体外受精) プログラムで順調に発育している胚を保管し、その後使用するために作成されています。 必要に応じて、これらの胚は完全な体外受精サイクルを繰り返すことなく解凍され、子宮腔に移植されます。
ドナー精子バンク。ドナー精子は、完全な男性不妊症の場合、または性的パートナーがいない場合に使用されます。
化学療法の前に、がん患者は精子サンプルを凍結し、後で ICIS 法を使用して妊娠するために使用できます。