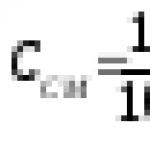Az új reprodukciós technológiák vallási értékelései. Absztrakt: Asszisztált reprodukciós technológiák. I. Bevezetés
A modern biológia és orvostudomány vívmányai lehetővé tették olyan technológiák megalkotását, amelyek kompenzálják a nőknél előforduló patológiákat, amelyek következtében a szaporodás nehézkes, sőt lehetetlen. A megtermékenyítés, a magzat és a terhesség megőrzése biotechnológiai úton ma már megoldható, akár béranya segítségével is. Ezeknek a technológiáknak köszönhetően sok házaspár képes új életet szülni és megtalálni a szülői boldogságot. Az új reprodukciós technológiáknak azonban megvannak a maga kockázatai. Így az in vitro megtermékenyítés során több tojást megtermékenyítenek, és a keletkező embriókat több sejt állapotában citológiai elemzésnek vetik alá patológiák kimutatására. Az összes vizsgálat után az embriót átültetik a méhbe. A kérdés az: mit kezdjünk a többivel – csírasejtként vagy emberi embrióként kezeljük? A kérdés önmagában is azt sugallja, hogy az emberi embriók nem csupán „biológiai anyag”, hanem bizonyos jogokkal, elsősorban az élethez való joggal rendelkezhetnek, amelyet a társadalomnak kell biztosítania. Minden társadalomban, ahol felmerül az ilyen technológiák alkalmazásának lehetősége, és ahol már használatban vannak, nyilvános vita alakul ki jogszerűségükről és etikai megengedhetőségükről.
A kialakuló társadalmi nézeteltérések diszkurzív és gyakorlati eszközökkel feloldhatók. Az adott társadalomban kialakult etikai rezsimtől függően (liberális*-demokrata*, tekintélyelvű*, kommunitárius* vagy konzervatív*-tradicionalista) különböző társadalmi-etikai, politikai és jogi módszerek lehetnek megfelelőek. De mindenesetre ez egy bevett erkölcsi gyakorlat - egyes érdekek diszkurzív védelme, mások korlátozása, érdekegyensúly fenntartása, összhangra törekvés, ezek felemelése ennek érdekében. Az érdekek összehangolásának, harmonizációjának, kölcsönös elismerésének és elfogadásának (kölcsönös vagy egyoldalú) folyamatai a társadalomban folyamatosan zajlanak, különféle – kommunikációs, társadalompolitikai, jogi – társadalmi eszközök segítségével. Az érdekek megvitatásakor, amikor arról van szó, olyan erkölcsi érveket használnak, amelyek erkölcsi értékekre utalnak.
Ezek az eszközök azonban nem mindig működnek. Amikor a diszkurzív nézeteltérések konfrontációvá alakulnak, amely társadalmi-politikai konfliktus formáját ölti, az állam adminisztratív, politikai és jogi módszereket alkalmaz az érdekek elhatárolására. Ez általában az „általános érdek” pozíciójából történik, amely állami érdek formájában jelenik meg. A tekintélyelvű vagy oligarchikus kormányzattal rendelkező társadalmakban a hatalmi ágak szétválasztásának intézményének fejletlensége vagy gyengesége, a politikai fékek és ellensúlyok rendszerének tétlensége, a politikai és polgári szabadságjogok állami érdekek leple alatt való elnyomása, i.e. mindenki érdekeit kielégítve megvalósulnak az uralkodó csoport sajátos érdekei. Az összeférhetetlenség büntetőjogi és erőszakos módszerekkel is feloldható. Mindez beszűkíti, sőt megszünteti a közbeszéd lehetőségeit, és ezáltal a társadalom morális potenciálját gyengítő tényezővé válik.
Egy normális társadalom társadalmi gyakorlatában az érdekek különböző eszközökkel történő összehangolásának feladatait általában eltérően oldják meg, olyannyira, hogy az erkölcsöt az egyik eszköznek tekintik a többé-kevésbé hasonló eszközökkel, például a hagyományokkal együtt. , jog, jog, közigazgatási és társasági intézmények. Ezen túlmenően, az erkölcs társítható a fegyelemhez, és ennek következtében az elfojtottsághoz (elnyomáshoz). Itt azonban pontosabb fegyelmezésről beszélni korlátozás(a latin resctrictio - korlátozásból), i.e. a korlátozásról, nem az elnyomásról. A társadalmi fegyelem a maga jelentős aspektusaiban korlátozó az egyén vonatkozásában. A korlátozások erkölcsileg indokoltak, vagy jogosak, ha a magánérdekek fennállásának lehetőségét és azok megvalósulását az emberek interakciójában – partnerségben, együttműködésben vagy barátságban – biztosítják. Ez vonatkozik mind az erkölcsre, mind a társadalmi fegyelem egyéb eszközeire (jog, szokás), amelyek a korlátozóság mértékében különböznek egymástól.
A társadalmi fegyelem más formáihoz hasonlóan az erkölcs célja a magánérdek korlátozása annak érdekében, hogy megakadályozza egyes magánérdekek indokolatlan dominanciáját más magánérdekekkel vagy általános érdekekkel szemben. Amint azt az erkölcs korai formáinak elemzése bizonyítja, amely a tanulságos és moralista műfaj történetileg legősibb alkotásaiban tükröződik, az erkölcs, amely az erényre való tanítás formájában jelent meg bennük, eleinte főként figyelmeztet, visszatartja az embert az elkövetéstől. mások érdekeit, méltóságát, önazonosságát sértő, az egyéni közösséggel szembehelyezkedő cselekmények. Azonban elemzés a bölcsesség irodalma*, amelyből a moralizmus, vagyis a morálisan építkező irodalom és etika (mint erkölcsfilozófia) fokozatosan kialakult, azt mutatja, hogy a gondolkodás fejlődésével (különösen a kommunikációs és társadalmi tapasztalat gazdagodását tükrözve) az erény egyre kevésbé látszik az absztinenciában, ( ön-)visszafogottság és egyre inkább - szándékos cselekvésben tudatos vágy egy pozitív (erkölcsi értelemben vett) eredményre, más emberek, csoportok, társadalom számára jelentős tevékenységre.
Az erkölcs aktív természete egyértelműen „hallható” az orosz „erény” szóban. Amint a szó összetételéből kiderül, az erény az, ami biztosítja a jó cselekedetet. Nyilvánvaló, hogy a figyelmeztető korlátozás általában nem elég a jó cselekedethez. A pozitívum szükséges, pl. produktív cselekvés. Az erkölcs meghaladja a törvényt, hiszen nem korlátozódik a korlátozásokra és nem redukálható tiltásokra.
Kéri és jelzi, hogy mit kell tenni amellett, hogy tartózkodik a tilos elkövetésétől. Ellentétben a joggal, amely a fennálló állapotok megőrzésének problémáját oldja meg, az erkölcsben sokkal fontosabb a konstruktivitás stratégiája: hogyan javíthatja az ember és a társadalom a dolgok állapotát, hogyan emelkedhet felül a mindennapi életen, és ezáltal közelebb kerülhet a tökéletességhez? Miközben fontos megérteni mit ne tegyünk, Az ember, mint az erkölcs alanya számára más kérdések is rendkívül fontosak: mit tegyen, hogyan tegye, milyennek kell lennie ahhoz, hogy a legjobbat tegye?
Vannak azonban olyan helyzetek, sőt egész életszakaszok, amikor az érdekharmonizáció, a közösség megőrzése, a mások javának, a közjó előmozdításának feladatai háttérbe szorulnak, ha megoldásuk mások gyengeségeinek, hibáinak kényeztetésével lehetséges. a megfelelés vagy részvétel költsége, bár közvetett, de közel. Az elvekhez és a legmagasabb értékekhez való hűség megkövetelheti az embertől, hogy határozottan elhatárolódjon valamitől, amiről úgy gondolja, hogy nincs közös vonása.
« Ne élj hazugságból!” - Alekszandr Szolzsenyicin 1974-ben ilyen felhívást intézett a szovjet néphez. Ha nincs erőnk a gonosznak tevőlegesen ellenállni, csak egy út van – nem veszünk részt benne: „A hazugság borítson mindent, a hazugság irányítson mindent, de legyünk makacsok a legkisebb dolgokkal szemben: ne uralkodjon el rajta. nekem!" A hazugság az embereken keresztül megmarad, ami azt jelenti, hogy az embereknek fel kell adniuk a hazugságokat. A hazugság az erőszakhoz kapcsolódik, az erőszak pedig a hazugságokhoz: az erőszaknak hazugságra van szüksége, hogy titokban tartsa magát, elrejtse magát, és úgy tegyen, mintha védelmező és gondoskodó lenne. „Amikor az erőszak – írja Szolzsenyicin – betör a békés emberi életbe, arca ragyog az önbizalomtól, viszi a zászlót és azt kiáltja: „Én vagyok az erőszak!” Szétoszlanak, engedjenek utat – összetörlek!" De az erőszak gyorsan elöregszik, néhány évvel – már nem magabiztos, és hogy kitartson, tisztességesnek tűnjön, minden bizonnyal a Hazugságokat hívja szövetségeseinek. Mert: az erőszaknak nincs más mögé bújva, mint a hazugságon, és a hazugságot csak erőszakkal lehet fenntartani. És nem minden nap, nem minden vállra teszi nehéz mancsát az erőszak: csak a hazugságnak való engedelmességet, a hazugságban való napi részvételt követeli meg tőlünk – és ez mind hűség.”
Nem hazugságban élni azt jelenti, hogy soha nem mondasz semmit a lelkiismereted ellen, nem ismételsz meg és különösen nem támogatsz valaki által kifejtett hazugságot, nem hallgatsz hazugságra (nem olvasol újságokat, amelyek elrejtik és elferdítik az információkat), és nem teszel úgy, mintha a hazugságot elfogadnák az igazságnak. .
Nem hazugság szerint élni a legegyszerűbb dolog, amit az ember megtehet egy olyan társadalomban, amelyet a képmutatás, a hazugság, az igazságtalanság és az erőszak ural. Bárhogy is legyen, döntenie kell erről, mert nem lesz könnyű: az igazságban való életvágyért karrierjével és pozíciójával fizethet, elveszítheti állását, megfoszthatja magát és családját a békétől.
Szolzsenyicin meg van győződve arról, hogy az igazság és a hazugság közötti választás a lelki függetlenség és a spirituális szervilizmus közötti választás.
Az elvi erkölcsi álláspont mindig a függetlenségben, függetlenségben fejeződik ki. De egy dolog nem mások véleménye vezérelni, más pedig erkölcsi okokból ellenállni a hatóságok, közvetlen felettesek tisztességtelen döntéseinek, csoportos önérdeknek stb. Ilyen körülmények között a prioritás a nem cselekvés elve – a gonosztól való tartózkodás, a rosszban való részvétel.
Ennek felismerése fontos pontja az erkölcsfilozófiai koncepciónak, amely végül a modern időkben öltött formát, és a kommunikációs, társadalmi, spirituális gyakorlat azon aspektusainak általánosítását jelenti, amelyeket a „jó (jó) és rossz” szavakkal jelöltek meg. „erény és hamisság”, „igazságosság és félrevezetés”, „helyes és helytelen”, valamint „jellem”, „viselkedési szabályok”, „felelősség”, „barátság”, „szeretet” stb. Az „erkölcs” fogalmának segítségével a mentális és normatív tapasztalatokban azonosítják azokat a szokásokat, cselekvéseket, karaktereket, amelyek a legmagasabb értékeket fejezik ki, és amelyeken keresztül az embernek lehetősége van arra, hogy intelligensen, szabadon és felelősségteljesen kifejezze magát. Rend a társadalmi erkölcsökben és az emberi kapcsolatokban, az önkény határai, a helyes viselkedés, az egyén méltósága és tökéletessége - ez az általános erkölcsi koncepció tartalma. A fentiekből következően ez a fogalom heterogén. Három dimenziót egyesít: A) a társadalom állapota (a szó tág értelmében, ideértve mind a társadalmat mint nemzetet, mind a közösségeket mint privát, helyi társadalmi entitásokat); b) az emberek, mint társadalmi szerepeket betöltők és magánszemélyek közötti kapcsolatok - olyan egyének, akik saját minőségükben cselekszenek, amely nem függ társadalmi kapcsolataitól, képes kölcsönös megértésre, interakcióra, gondoskodásra és szeretetre; V) személyiségminőség, ami józanságként is megnyilvánul, i.e. mások igényeire való reagálás, elvárásaik iránti érzékenység, önmaga megértésének és ellenőrzésének képessége, önmaga iránti következetes és hűség, valamint a gondolataiért és tetteiért önmaga és mások iránti felelősségvállalás képessége. Ez utóbbi - a felelősség - valamilyen módon, bár nem teljesen, de összekapcsolja az erkölcs különböző dimenzióit.
Az etika vagy erkölcsfilozófia arra törekszik, hogy megértse, mi a különleges ebben a sokrétű tartalomban, és ennek alapján sajátos erkölcsi elképzelést épít. Ugyanakkor az erkölcs általános fogalmának kialakításával együtt megtörténik bizonyos etikai kategóriák meghatározása - „jó és rossz”, „erény és bűn”, „igazságosság”, „kötelesség” stb., azaz. a rájuk jellemző sajátos tartalom azonosítása és tisztázása az erkölcs összefüggésében.
Tesztkérdések és feladatok
- 1. Nevezze meg az erkölcs definíciójának főbb megközelítéseit, és határozza meg, hogyan lehetne őket besorolni!
- 2. Bővítse ki a meghatározási eljárás tartalmát. Milyen elméleti problémákat old meg a definíció segítségével?
- 3. Hogyan fejeződik ki az erkölcs heterogenitása? Mi határozza meg az erkölcs belsőleg heterogén elemeinek egységét?
- 4. Az erkölcsnek milyen szociokulturális funkciói azonosíthatók a fejezetben szereplő előzetes moráldefinícióból kiindulva?
1. In vitro megtermékenyítés (IVF).
2. Ivarsejtek és embriók átvitele a petevezetékbe (GIFT, ZIFT).
3. Az ivarsejtek mikromanipulációja a férfi meddőség kezelésében:
a zona pellucida zóna részleges disszekciója;
szubzonális műtrágyázás;
intracitoplazmatikus spermium injekció (ICIS).
4. Segített szaporodási módszerek donor petesejtek és embriók felhasználásával.
5. Béranyaság (női donor az ügyfélcsalád genetikai gyermekét hordozza).
6. A spermiumok, petesejtek és embriók mélyhűtése.
7. Mesterséges megtermékenyítés a férj vagy donor spermájával (ISM, ISD).
INDOKOLÁS
A terméketlen házasságok gyakorisága Oroszországban meghaladja a 15%-ot, ami a WHO szerint kritikus szintnek számít. Az országban több mint 5 millió meddő házaspárt tartanak nyilván, ezek több mint fele igényli az ART módszerek alkalmazását. Szakértői becslések szerint csak a női meddőség aránya 14%-kal nőtt az elmúlt 5 évben.
Számos, jelenleg az ART általános elnevezés alatt egyesített megközelítés kidolgozásának alapja a méhüregben végzett IVF és ET klasszikus módszere volt. Ebben az esetben a petesejteket speciális tápközegben történő tenyésztés után spermával megtermékenyítik, amelyet előcentrifugálnak és tápközegben dolgoznak fel.
Az ART típusai:
- embrióhordozás egy önkéntes nő által ("helyettes anyaság") a gyermek (gyermekek) későbbi átadása céljából genetikai szülőkhöz;
- petesejtek és embriók adományozása;
- ICSI;
- petesejtek és embriók mélyhűtése;
- örökletes betegségek preimplantációs diagnózisa;
- az embriók számának csökkentése többes terhességben;
- valójában IVF és PE.
ECO 1978 óta alkalmazzák a meddőségi terápia világgyakorlatában. Oroszországban ezt a módszert először az Orosz Orvostudományi Akadémia Szülészeti, Nőgyógyászati és Perinatológiai Tudományos Központjában alkalmazták sikeresen, ahol 1986-ban professzor munkájának köszönhetően B.V. Megszületett Leonov első kémcső gyermeke. Az IVF módszer kifejlesztése kihozta a zsákutcából a petevezeték meddőség kezelésének problémáját, és lehetővé tette a terhesség elérését rengeteg olyan nőnél, akik korábban gyermektelenségre voltak ítélve.
Az IVF programban részt vevő betegekkel kapcsolatban szükséges, hogy a pár egészének meddőségéről beszéljünk. Ez alapjaiban változtatja meg a betegek kiválasztásának és a programra való felkészítésének szemléletét – kötelezővé teszi mind a nők, mind a férfiak reproduktív rendszerének állapotának előzetes felmérését.
A házaspárok meddőségi eseteinek hozzávetőleg 40%-a férfi meddőségre vezethető vissza. Az ICSI-módszer lehetővé teszi a meddőség súlyos formáiban (oligo, astheno, súlyos teratozoospermia) szenvedő férfiaknak utódokat, esetenként csak akkor, ha a herebiopsziával nyert pontban egyetlen spermium található. A donor petesejteket használó IVF-et a meddőség leküzdésére használják olyan esetekben, amikor egy nő nem tud saját petesejteket beszerezni, vagy gyenge minőségű petesejteket kap, amelyek nem képesek megtermékenyítésre és teljes terhesség kialakulására.
A „helyettesítő anyasági program” az egyetlen módja annak, hogy genetikailag gyermeket szülhessenek a méhhiányban szenvedő vagy súlyos extragenitális patológiás nők számára, amikor a terhesség lehetetlen vagy ellenjavallt.
A preimplantációs diagnózis is IVF módszeren alapul. Célja, hogy a preimplantációs fejlődés korai szakaszában embriót nyerjenek, genetikai patológiát és PE-t vizsgáljanak a méhüregben. A redukciós műveletet háromnál több embrió esetén hajtják végre. Ez egy kényszerű eljárás, de szükséges a többes terhesség sikeres lefolyásához. A redukció racionális és tudományosan megalapozott alkalmazása, valamint a többes terhességben történő végrehajtás technikájának javítása lehetővé teszi az ilyen terhességek klinikai lefolyásának optimalizálását, az egészséges utódok születésének előrejelzését és a perinatális veszteségek gyakoriságának csökkentését.
* Megtermékenyítés a férj spermájával (ISM)
A férj spermájával történő megtermékenyítés (ISM) azt jelenti, hogy a) kis mennyiségű friss spermát juttatnak a hüvelybe és a méhnyakba, vagy b) közvetlenül a laboratóriumban előállított spermiumok méhüregébe, lebegtetéssel vagy Percoll gradiens segítségével. Az ISM-et olyan esetekben végezzük, amikor a nő teljesen egészséges és a csövek átjárhatók.
Az ISM használatára vonatkozó javallatok:
♦ a hüvelyi magömlés lehetetlensége (pszichogén vagy organikus impotencia, súlyos hypospadia, retrográd ejakuláció, hüvelyi diszfunkció);
♦ férfifaktor meddőség - a spermiumok számának hiánya (oligospermia), motilitása (asthenospermia) vagy szerkezeti zavara (teratospermia);
♦ kedvezőtlen nyaki faktor, amely hagyományos kezeléssel nem küszöbölhető ki;
♦ mélyhűtött spermiumok alkalmazása terhesség indukálására (a spermiumot rákkezelés vagy vazektómia előtt nyerik ki).
Az eljárás hatékonysága az ISM-re - 20 %.
Megtermékenyítés donor spermával (ISD)
Felolvasztott, mélyhűtött donor spermát használnak. Az ISD-t akkor hajtják végre, ha a férj spermája hatástalan, vagy ha az összeférhetetlenség akadályát nem lehet leküzdeni. Az ISM és az ISD technikák megegyeznek.
Az ISD hatékonysága- 50% (a kísérletek maximális száma 4).
AJÁNDÉK- a petesejt a spermával együtt a petevezetékekbe. A nőtől egy vagy több petesejtet, a férjtől spermát vesznek, összekevernek és behelyezik a petevezetékbe.
ZIFT- embrió (zigóta) átvitele a petevezetékekbe.
A ZIFT-tel lényegesen nagyobb a terhesség valószínűsége, mint az AJÁNDÉK esetében. A GIFT és ZIFT laparoszkópia során és ultrahangos kontroll mellett is elvégezhető.
Az első esetben ivarsejteket vagy zigótákat vezetnek be a csőbe a hasüregből, a másodikban a méhnyakon keresztül. A GIFT és a ZIFT diagnosztikai laparoszkópiával kombinálva egyszer kerül végrehajtásra. Hatékonyság akár 30%.
In vitro megtermékenyítés (IVF) - a petesejtek és a spermiumok keveredésének folyamata laboratóriumi körülmények között. A petefészek-stimulációt a plazma ösztradiolszint mérésével és a tüszőnövekedés ultrahangos mérésével követik nyomon. A tüszőket átszúrják és tartalmukat leszívják. Az így létrejött petesejteket a férjtől származó kapacitált spermiumokkal inkubálják, majd az így létrejött embriókat a tüszőszúrás után 2-6 nappal a méh üregébe juttatják, ahogyan ez természetes megtermékenyítés esetén is történik.
A IV lebonyolításának indikációi:
♦ a petevezetékek visszafordíthatatlan károsodása gyulladásos folyamat következtében vagy műtét során;
♦ férfi meddőség;
♦ immunológiai meddőség;
♦ endometriózis miatti meddőség;
♦ ismeretlen eredetű meddőség.
IVF módszer donor embriók felhasználásával
Nem működő petefészkekben ("korai menopauzában" vagy azok eltávolítása után) szenvedő nőknél alkalmazzák. A módszer lényege: a donor petesejtjének férje spermájával történő megtermékenyítésének eredményeként létrejött embriót átvisszük a betegbe. Néha a tojások helyett donorembriókat használnak erre a célra. Ezt követően HRT-t végeznek, szimulálva a nő állapotát a normál fiziológiás terhesség alatt.
Béranyaság
Az ilyen típusú IVF-et méh nélküli betegeken végzik. A módszer lényege: egy nőtől kapott petesejtet megtermékenyítenek a férje spermájával, majd a keletkezett embriót egy másik nő méhébe juttatják – egy „pótmanya”, aki vállalta, hogy kihordja a gyermeket, és születése után odaadja. a tojások „tulajdonosa”, azaz. genetikai anya.
A spermiumok és az embriók lefagyasztása
A módszer előnyei:
♦ a sperma felhasználásának lehetősége bármikor és bárhol;
♦ a donorok megfigyelése spermájuk AIDS-vírussal való fertőződése tekintetében, ami kizárja mind a nő, mind a magzat fertőzésének kockázatát;
♦ sikertelen IVF-kísérletet követő ciklusokban történő embriófelhasználás lehetősége, ha az átvitelhez szükségesnél több petesejt és embrió került elő (általában 3-4-nél több).
A MŰVÉSZET CÉLJA
Egészséges utódok szerzése meddő pároktól.
MŰVÉSZETI JELZÉSEK
- abszolút petevezeték meddőség petevezeték hiányában vagy elzáródása esetén;
- ismeretlen eredetű meddőség;
- meddőség, amelyet nem lehet kezelni, vagy olyan meddőség, amelyet nagyobb valószínűséggel lehet legyőzni IVF-el, mint más módszerekkel;
- a meddőség immunológiai formái (az antispermium antitestek jelenléte a MAP teszt szerint ≥50%);
- a férfi meddőség különböző formái (oligo, astheno vagy teratozoospermia), amelyek az ICSI módszer alkalmazását igénylik;
- PCOS;
- endometriózis.
ELLENJAVALLATOK ART
- a méh üregének veleszületett rendellenességei vagy szerzett deformációi, amelyekben az embriók beültetése vagy terhesség lehetetlen;
- a méh jóindulatú daganatai, amelyek műtéti kezelést igényelnek;
- bármely hely rosszindulatú daganatai (beleértve az anamnézist is);
- petefészek daganatok;
- bármilyen lokalizációjú akut gyulladásos betegségek;
- szomatikus és mentális betegségek, amelyek ellenjavallt terhesség és szülés.
FELKÉSZÜLÉS A MŰVÉSZETRE
A házaspár IVF előtti vizsgálatának körét az Orosz Föderáció Egészségügyi Minisztériumának 2003. február 26-i 67. számú, „Az ART alkalmazásáról a női és férfi meddőség kezelésében” című rendelete szabályozza.
Egy nő számára a következők szükségesek:
- orvosi jelentés az egészségi állapotról és a terhesség lehetőségéről;
- a húgycső és a nyaki csatorna mikroflórájának és a hüvely tisztaságának mértékének vizsgálata;
- klinikai vérvizsgálat, beleértve a véralvadási idő meghatározását (1 hónapig érvényes);
- általános és speciális nőgyógyászati vizsgálat;
- a vércsoport és az Rh faktor meghatározása;
- A kismedencei szervek ultrahangja.
A jelzések szerint a következőket is elvégzik:
- a húgycsőből és a nyaki csatornából származó anyag bakteriológiai vizsgálata;
- endometrium biopszia;
- fertőző vizsgálat (chlamydia, ureaplasma, mycoplasma, HSV, CMV, toxoplasma, rubeola vírus);
- a méh és a petevezetékek állapotának vizsgálata (HSG vagy hysterosalpingoscopia és laparoszkópia);
- antisperma és antifoszfolipid antitestek jelenlétének vizsgálata;
- FSH, LH, ösztradiol, prolaktin, tesztoszteron, kortizol, progeszteron, pajzsmirigyhormonok, TSH, STH vérplazma koncentrációjának meghatározása;
- méhnyakkenetek citológiai vizsgálata.
Szükség esetén más szakemberekkel való konzultációt írnak elő.
Egy férfi számára a következők szükségesek:
- vérvizsgálat szifiliszre, HIV-re, hepatitis B-re és C-re (3 hónapig érvényes);
- spermogram. A jelzések szerint:
- fertőző vizsgálat (chlamydia, ureaplasma, mycoplasma, HSV, CMV);
- spermiumok FISH diagnosztikája (fluoreszcens in situ hibridizációs módszer);
- vércsoport és Rh faktor meghatározása.
Egy andrológus konzultációt is előírnak. A 35 év feletti házaspárok esetében orvosi genetikai tanácsadás szükséges.
MŰVÉSZETI MÓDSZERTAN
Az IVF eljárás a következő szakaszokból áll:
- a betegek kiválasztása, kivizsgálása, eltérések észlelése esetén előzetes felkészítés;
- a szuperovuláció stimulálása (kontrollált petefészek-stimuláció), beleértve a folliculogenezis és az endometrium fejlődésének nyomon követését;
- petefészek tüszők átszúrása az ovuláció előtti petesejtek kinyerésére;
- petesejtek megtermékenyítése és in vitro megtermékenyítés eredményeként kialakult embriók tenyésztése;
- PE a méh üregébe;
- PE utáni időszak támogatása;
- a terhesség diagnosztizálása a korai szakaszban.
A MŰVÉSZET HATÉKONYSÁGA
Az Európai Reproduktív Medicina Szövetség adatai szerint Európában jelenleg több mint 290 000 ART ciklust végeznek évente, amelyek 25,5%-a szülést eredményez; az USA-ban - több mint 110 000 ciklus évente, átlagos terhességi arány 32,5%.
Az orosz ART klinikákon évente 10 000 ciklust végeznek, a terhességi arány körülbelül 26%.
A MŰVÉSZET HATÉKONYSÁGÁT BEFOLYÁSOLÓ TÉNYEZŐK
A farmakológiai ipar fejlődése új, tüszőképződést serkentő gyógyszerek, új, eldobható szúró tűk létrehozásához vezetett a petesejtek kinyeréséhez, valamint modern atraumás katéterek létrehozásához a PE méhüregbe juttatására. Ez lehetővé tette nagyobb számú, jó minőségű petesejtek kinyerését, csökkenti a TVP során fellépő lehetséges szövődmények kockázatát, és ennek megfelelően az IVF program hatékonyságát 36-39%-ra növelte egy ET-re a méhüregben.
Az IVF és ET programban a leghatékonyabb séma a szuperovuláció stimulálása rekombináns gonadotropin készítményekkel a reproduktív rendszer GnRH deszenzitizálásának hátterében. Meglátásunk szerint a rekombináns gonadotropinokat és GnRH-antagonistákat tartalmazó szuperovulációs stimulációs sémák alkalmazása kevésbé hatékony, de közel 2-szeresére csökkentheti az OHSS előfordulását.
Az ICSI módszer alkalmazása olyan házaspároknál, akiknek a kórtörténetében két vagy több sikertelen IVF és PE kísérlet történt, normális spermatogenezissel és károsodott reproduktív funkcióval a nőknél, az esetek 52%-ában lehetővé teszi a terhesség elérését.
Azoospermiás betegek here- és/vagy mellékhere biopsziája, majd szövettani vizsgálata hormonális és genetikai szűréssel kombinálva lehetővé teszi a diagnózis felállítását és a meddőség kezelésének további taktikáinak meghatározását egy házaspárban. A nem obstruktív azoospermia formájú betegek csoportja prognosztikailag a legkedvezőtlenebb az IVF/ICSI programban a spermium megszerzése és a terhesség szempontjából. A terhességi arány ebben a betegcsoportban 14,3%.
Az ART-ban ma már szinte bármilyen típusú biológiai anyag esetében alkalmazzák a mélyhűtést. Ez a módszer lehetővé teszi a spermiumok, a hereszövetek, a petesejtek és az embriók hosszú távú tárolását. Felolvasztás után a spermiumok 95%-a és az embriók 80%-a életképes. Ha az ET eljárást a stimulált ciklusban az OHSS kialakulásának magas kockázata miatt megszakítják, és ha minden „jó” minőségű embriót mélyhűtöttek, a betegek terhességi aránya 37,1% a stimulációs ciklus alapján. A krioprezerváció után felolvasztott blasztociszták alkalmazásának hatékonysága az ART programokban a sikertelen próbálkozású nőknél 29,5% volt.
Az IVF és ET programokban végzett prenatális diagnosztika 13%-ra csökkentette a spontán abortuszok előfordulását azokban a párokban, ahol az egyik szülő kromoszóma-rendellenesség hordozója, összehasonlítva a spontán abortuszok gyakoriságával azoknál a hasonló problémákkal küzdő betegeknél, akik nem vettek igénybe prenatális diagnosztikai szolgáltatásokat. . Az embriók kromoszómapatológiájának kimutatása és a csak genetikailag normális embriók átvitele növeli a beágyazódási arányt, csökkenti a spontán vetélés kockázatát és megakadályozza a genetikai patológiás gyermek születését az IVF programban részt vevő betegeknél. A prenatális diagnosztika segítségével elkerülhetők a magzat neméhez kötődő kromoszómabetegségek (A és B hemofília, Duchenne myopathia, Martin-Bell szindróma stb.), a 21. kromoszóma triszómiája (Down-szindróma), a 13. sz. kromoszóma (Patau-szindróma), 18. kromoszóma (Edwards-szindróma), monoszómia (Shereshevsky-Turner) stb.
A prenatális diagnózis olyan gyermekek születése esetén javasolt, akiknek a kórtörténetében örökletes és veleszületett patológia szerepel, kiegyensúlyozott kromoszóma-rendellenességek jelenléte a kariotípusban, a kórtörténetben kétszer vagy több sikertelen IVF-kísérlet, a kórelőzményben hydatidiform anyajegy, megnövekedett a különböző kromoszómák aneuploidia (X, Y kromoszómákon > 0,25%) spermiumok százalékos aránya a házastárs ejakulátumában, ha a nő 35 évesnél idősebb, a magzat nemének meghatározásához. Az embrió nemének ezzel a módszerrel történő meghatározásának pontossága 95-97%. A terhességi ráta a prenatális diagnosztika alkalmazása után az „NTs AGiP Rosmedtekhnologii” szövetségi állami intézménynél az ART osztályon 2006-ban 32% volt.
Az embriócsökkentő műtét csökkentheti a többes terhesség szövődményeinek előfordulását, hiszen a vetélés és a rendkívül koraszülött gyermekek születésének kockázata hármasikrek hordozásakor eléri a 70%-ot. Az első trimeszterben a többes terhesség csökkentését először végezték transzcervikális hozzáféréssel és a mögöttes petesejt eltávolításával. A módszer rendkívül traumatikusnak bizonyult, és számos szövődmény kísérte, ezért a gyakorlatban nem alkalmazták. Jelenleg transzabdominális vagy transzvaginális hozzáférést alkalmaznak.
Transzvaginális hozzáférés esetén az intrauterin beavatkozás speciálisan megjelölt tűvel történik a hüvely hátsó vagy elülső fornixén keresztül. A tű előrehaladásának vizuális követésére speciális biopsziás adaptereket használnak, amelyek lehetővé teszik a tű mozgásának nagy pontosságú megjelenítését a méh üregében.
Az embriók transzabdominális hozzáférés révén történő csökkentésére a transzabdominális szkenneléshez egy biopsziás adapterrel ellátott szenzort és egy 15 cm hosszú tűt használnak, amelynek echogén felülete 1 cm a disztális végén, önrögzítő tüskével.
Ha mindkét módszerrel redukciót hajtanak végre, az érzékelő elektronikus jelölése az embrió mellkasi területére irányul, és a tűt gyorsan behelyezik a magzati tojás üregébe, szabályozva a manipulációk pontosságát a videokép segítségével. az ultrahang diagnosztikai készülék monitor képernyője. A tű behatolási mélysége vizuálisan szabályozható. A magzati petesejt üregébe való behatolás után a tű hegye a lecsökkent embrió mellkasához kerül, és mechanikusan elpusztítja a mellkasi szerveket, amíg a szívműködés le nem áll. Ha a lecsökkent embrió szívverése megmarad, 2-4 nap múlva ismételt redukciót kell végezni.
A MŰVÉSZET SZÖVŐDÉSE
- allergiás reakciók az ovulációt serkentő gyógyszerekre;
- gyulladásos folyamatok;
- vérzés;
- többes terhesség;
- Az OHSS, amely általában a PE után jelentkezik, egy iatrogén állapot, amelyet a petefészkek méretének növekedése és ciszták képződése jellemez. Ezt az állapotot fokozott vaszkuláris permeabilitás, hipovolémia, hemokoncentráció, hiperkoaguláció, ascites, hidrothorax és hidropericardium, elektrolit-egyensúlyzavar, az ösztradiol és a CA125 tumormarker megnövekedett koncentrációja kíséri a vérplazmában (további részletek a „Pefetefészek hiperstimulációs szindróma” részben);
- méhen kívüli méhen kívüli terhesség. Az ART alkalmazása során a méhen kívüli terhesség előfordulása 3% és 5% között van.
Bevezetés
Az elnéptelenedés körülményei között fontossá válik, hogy minden erőforrást felhasználjunk a születésszám növelésére. Kiemelt jelentőséget tulajdonítanak a meddőség visszaszorításának, amelynek minimális szintje minden nemzetben 10%, a problémát országos jelentőségűvé adó kritikus szint pedig 15%. A meddőség növekedését különféle tényezők magyarázzák, amelyek leggyakrabban a külső környezet (kémia, sugárzás, életmód, munka jellege stb.) emberi reproduktív funkcióra gyakorolt hatásával függnek össze. A meddőség valódi mértékét nehéz meghatározni, mert:
1. a fogamzásgátlás széles körű elterjedésével nem tekinthető minden gyermektelen ember meddőnek;
2. A szociológiai felmérések során a válaszadók hajlamosak eltitkolni meddőségüket annak „stigmatizáló” vonatkozásai miatt;
3. a hivatalos statisztika csak a meddőség és az első alkalommal diagnosztizált egészségügyi intézményi látogatásokat rögzíti; nem veszi figyelembe, hogy a betegek egyszerre több klinikával is felvehetik a kapcsolatot (ez növeli az összlétszámot), a nem állami klinikák pedig korlátozhatják a regisztrációt vagy teljesen megtagadhatják azt (ez csökkenti az összlétszámot);
4. Nem mindenki kér orvosi segítséget, akinek szaporodási problémái vannak.
Különféle becslések szerint Oroszországban a reproduktív korú lakosság 10-20%-a jelenleg terméketlen, i.e. akár 5 millió pár, ami megközelítőleg megfelel a fejlett európai országok szintjének: 2007-ben Franciaországban a nők mintegy 15%-a fordult orvoshoz meddőséggel kapcsolatban, Olaszországban minden ötödik pár meddő, az Egyesült Királyságban - minden hetedik.
A meddőség oka egy párban a női (a párok 80%-a) vagy a férfi (legfeljebb 45%-a) szaporodási funkció zavara, a párok mintegy harmadában pedig a kombinált meddőség, i.e. férfi és női tényezők egyszerre okozzák.
A meddőség már régóta olyan probléma, amely a legjobb esetben is kijelenthető, de szinte lehetetlen megoldani. A hatékony kezelési módszerek hiánya oda vezetett, hogy tíz reproduktív rendellenességgel küzdő meddő párból legfeljebb három számíthatott saját gyermekvállalásra. Csak az in vitro megtermékenyítésen („testen kívüli”) alapuló asszisztált reprodukciós módszerek klinikai gyakorlatba történő bevezetése 1978 után, amikor Louise Brown Nagy-Britanniában született, tette lehetővé azt a következtetést, hogy létezik alapvető megoldás a meddőség problémájára. a társadalomban. Az asszisztált reprodukciós technológiák (ART) alkalmazásával kísérletenkénti terhesség valószínűsége 30-40%, szemben a természetes fogantatással 8-25%-kal.
A modern ART több mint 10 módszert tartalmaz, amelyek száma folyamatosan bővül, és a gyakorlati alkalmazást az adott ország nemzeti jogszabályai vagy hagyományai szabályozzák. A leghatékonyabb és legnépszerűbb a következők:
1. in vitro megtermékenyítés (IVF, „in vitro fogantatás” az embriók későbbi áthelyezésével a méhüregbe);
2. ICSI (férfi meddőség esetén – az egyéni spermium „kényszer” összekapcsolása egy petesejttel in vitro);
3. béranyaság (a genetikai anya IVF/ICSI-vel nyert embrióit egy másik nő hordozza);
4. örökletes és genetikai betegségek preimplantációs diagnózisa (az embrionális stádiumban a gyermekek örökletes betegségeinek kizárása és a terhesség késői szakaszában az orvosi okokból történő abortusz elkerülése érdekében);
5. donor csírasejtek felhasználása (saját pete és megtermékenyítésre képes hímivarsejt hiányában);
6. mélyhűtés (az embriók és csírasejtek lefagyasztása a jövőbeni felhasználás céljából).
Az ART kiterjesztett értelmezése magában foglalja az ovuláció hormonális stimulálását is, amelyet endokrin meddőségre, valamint az egyéni szaporodási képességek életkorral összefüggő csökkenésére használnak, és lehetővé teszik a „természetes” fogantatást. A hormonális stimuláció iránti igény megnő a „szülés elhalasztásának” egy későbbi időszakra való átterjedése miatt, amely gyakran meghaladja a petefészek-tartalék fiziológiás csökkenésének kezdetére vonatkozó korhatárt (27 év).
Az ART-ra vonatkozó információk nem szerepelnek a hivatalos orvosi statisztika kötelező mutatóinak listáján, hanem önkéntesek, pl. nemzeti szakmai szövetségek gyűjtik össze azoktól a klinikáktól, amelyek rendelkeznek engedéllyel az ART elvégzésére, és közzé kívánják tenni eredményeiket. 1995 óta az Orosz Emberi Reprodukciós Szövetség (RAHR) nyilvántartást vezet az ART-ról, olyan űrlapok használatával, amelyek lehetővé teszik az összehasonlítást más országokkal.
Az ART kiterjeszti a társadalom „reproduktív bázisát”, leküzdve a fogantatást és a terhességet akadályozó, sokféle termékenységi korlátozást (lásd 1. ábra). A meddőségi kezelés modern ideológiája nem a bármi áron történő teherbeesés, hanem egy egészséges gyermek születése az anya egészségének megőrzése mellett (a többszörös szülés és az ART szövődményei orvosi hibának számítanak).
1. ábra A társadalom reproduktív bázisának bővítése
A reproduktív gyógyászat egy új, rendkívül jövedelmező iparág, hatékony, keresett és ellenáll a piaci ingadozásoknak. Hiányos adatok szerint a 21. század elejére. Már több mint 2 millió ember született a világon, akik ART segítségével fogantak. A demográfiai magatartás individualizálódása (az elsőszülések elhalasztása, a „tudatos” nem „spontán” szülői lét terjedése stb.) egyrészt az ART iránti lakossági igény folyamatos növekedéséhez vezet, másrészt új problémákat okoz. . Ez:
· a meddőségi kezelés hatékonyságának további növelése, hogy a kezelés időtartama ne haladja meg a több évet, lehetőséget adva az ismételt alkalmazásra. A modern ART protokollok azon a tényen alapulnak, hogy az első alkalmazástól a gyermek születéséig tartó időszak nem haladhatja meg a két évet; a hagyományos meddőségkezelési gyakorlatok legalább 10 éves diagnózison és kezelésen alapultak, és a reproduktív kor végéig tarthattak;
· magasan képzett személyzet képzése új szakterületeken - reproduktológia, andrológia, humán embriológia;
· a kérdés társadalmasítása (beillesztése a filozófia (etika), jog, közgazdaságtan tárgykörébe). Csak Costa Ricában hivatalosan az ART-ok illegálisak, mivel sértik a nemzeti alkotmányt (mivel mesterséges megtermékenyítéssel kezdik az emberi életet, majd az átvitel hiánya vagy csökkentése miatt megsemmisítik). Más országokban nincsenek olyan törvények, amelyek kifejezetten tiltják az ART-t.
Az ART bevezetése az orosz klinikai gyakorlatba az innovatív ipar kialakulásának példája. Az első hazai ART-szülés 1986-ban történt, és a reproduktív medicina továbbfejlesztését az országban a központosított tervezés hagyományai nehezítették. Az 1990-es évek eleji átmeneti orosz gazdaság körülményei között. Az innovatív reprodukciós technológiák „utánzati” innovációkká váltak, bevált fejlesztési algoritmussal. 1996-ban Moszkvában, Szentpéterváron, Szocsiban, Kiszlovodszkban, az Urálban és Szibériában található 12 reproduktív központ hivatalosan bejelentette magát a hazai ART nyilvántartásba, 2005-ben pedig már 51 volt belőlük, és szinte az egész ország területén helyezkedtek el. ország, beleértve a Távol-Keletet is. A leghatékonyabb szervezeti és technológiai sémák alkalmazása, közös orvosi központok létrehozása, know-how stb. lehetővé tette az orosz reproduktív klinikák számára, hogy elérjék a kínált szolgáltatások szükséges minőségét, ami lehetővé tette számukra, hogy gyorsan betöltsék az országon belüli rést, és belépjenek a világpiacra. Az ART hatékonysága az orosz központokban gyorsan elérte a világszintet, amikor a megkezdett ciklusok körülbelül 30%-a születéssel végződik.
Jelenleg számos vezető hazai reprodukciós központ működik partnerségben európai és amerikai klinikákkal, és fogadnak külföldi betegeket, különösen olyan országokból, ahol korlátozó törvények tiltják az ART-t. Az ART-ra vonatkozó legszigorúbb korlátozásokat az örökbefogadás közbeni közvetítésről (1989) és az emberi embrió védelméről szóló (1990) német törvény, az olasz „Szülési orvosi segítségnyújtásra vonatkozó szabványok” (2004) tartalmazza, amelyek majdnem teljes mértékben megtiltja az ivarsejtek és embriók adományozását, a preimplantációs diagnosztikát, az embriók mélyhűtését, a béranyaságot, valamint a többes terhességek csökkentését (részleges abortuszt). Ezek a túlzott, nem gazdasági szabályozásra tett kísérletek az úgynevezett „reproduktív turizmus” kialakulásához vezettek, amelyben a meddő párok olyan országokba utaznak kezelésre, ahol liberálisabb szabályozás, de jó minőségű ART; Oroszország „reproduktív turistákat” is fogad. Ráadásul a kedvező ár-minőség arány miatt sok, tartósan külföldön élő orosz nő választja az orosz klinikákat.
Az ART-ra vonatkozó gazdasági kapcsolatok fő típusait piaci entitásokon keresztül valósítják meg:
· fogyasztók (betegek);
· reproduktív klinikák;
· berendezések és gyógyszerek szállítói;
· pénzügyi, hitel- és biztosítási intézmények;
· az elmúlt években - az állam, kiemelt nemzeti egészségügyi és demográfiai fejlesztési projektek keretében.
E piaci entitások céljai és célkitűzései azonban nagymértékben ellentmondanak egymásnak.
· A betegek a lehető legolcsóbban szeretnének szolgáltatáshoz jutni, még összetett diagnózis esetén is.
· A „demográfiai befektetések” megtérülésében érdekelt állam azokat igyekszik finanszírozni, akiknek a legnagyobbak az esélyei, hiszen ők tudják ténylegesen növelni a születések számát.
· A klinikák arra törekszenek, hogy az állami költségvetésből az ingyenes IVF kvótáját a maguk javára osztsák el:
o Formálisan az állami klinikák ragaszkodnak prioritásukhoz, és úgy vélik, hogy az államnak csak állami intézményekben kell finanszíroznia a kezelést;
o Formálisan a magánklinikák lobbiznak a különböző állami szerveknél egy olyan törvény elfogadásáért, amely szerint a születési anyakönyvi kivonatok rendszeréhez hasonlóan „a pénz (azaz jelen esetben az állam által kiosztott kvóták) követhetné a beteget”. A sikeres és népszerű magánklinikák képviselői meg vannak győződve arról, hogy ebben az esetben a betegek választása egyértelműen nekik kedvez, ami általánosságban tovább növelné vonzerejüket a kereskedelmi betegek számára.
A célpiac méretének növelésében érdekelt gyógyszergyártók és eszközgyártók mindenkit támogatni igyekeznek: új klinikákat, betegszervezeteket, állami demográfiai programokat, mert szempontjuk szerint mindez termékeik értékesítésének növekedéséhez vezet.
Az ART egyszerre hoz létre áru- és erőforráspiacot. A termék itt nem csak orvosi ellátás, hanem fizetős szolgáltatás, amelyet a beteg-fogyasztó a gyártó klinikákon vásárol meg. Az ART mint erőforráspiac sajátos szerepe az, hogy lehetőséget teremtsen a legális reproduktív munkára (béranyaságban, reproduktív adományozásban stb.). Az ilyen erőforrások iránti igény az ART iránti kereslettől függ, amelyet az orvosi és társadalmi összetevők határoznak meg. Az orvostudomány a lakosság rossz reproduktív egészségével, a szociális - az ART, mint az emberi reprodukciós módszer alapvető lehetőségeivel (például egyedülálló nők ART-hoz való törvényileg rögzített joga; az ART anyagi és területi elérhetősége) társul. Oroszországban, csakúgy, mint a többi ország túlnyomó többségében, a törvények csak orvosi okokból engedélyezik az ART alkalmazását.
Az ART potenciális fogyasztóinak számbavétele a reproduktív klinikák aktáin és a tematikus internetes oldalak felhasználóinak elemzésén keresztül az orvosi motivációk abszolút túlsúlyát mutatják, főként a fiatal reproduktív korú (20-35 éves) betegek körében. Ugyanez a korosztály az IVF és az ICSI fő fogyasztója. Tekintettel arra, hogy ezeknek a programoknak a részaránya az ART teljes szerkezetében meghaladja a 75%-ot, feltételezhetjük, hogy a kapott eredmények megfelelnek a teljes populációra jellemző trendeknek (lásd 1. táblázat).
1. táblázat A nők életkor szerinti megoszlása IVF és ICSI programokban (2004), %
Forrás : Assisted Reproductive Technology in Europe, 2004: eredmények az ESHRE Human Reproduction európai regisztereiből, 2008. évf. 23. No. 4. P. 758.
Az egészségügyi menedzsment piaci módszereinek és a közvetlen kormányzati szabályozás módszereinek kombinációja lehetővé teszi az ART piac feltételes felosztását költségvetési és kereskedelmi szegmensekre. A szegmensek pénzügyi határai végső soron az ART iránti állami érdeklődés mértékétől függenek, ami a kezelésre szánt költségvetési kvóták révén csökkenti a kereskedelmi keresletet és csökkenti a szolgáltatás költségeit.
A költségvetési szegmenst a költségvetési finanszírozás keretei határozzák meg, ahol a kvóták nagysága a regionális és szövetségi költségvetések pénzügyi lehetőségeitől, az ART orvosi és egyéb összetevőinek (gyógyszerek és felszerelések, orvosok és más szakemberek munkája, épületek bérbeadása stb.), valamint a kvóták száma és megcélzása - a meddőség leküzdésére irányuló beruházások legnagyobb hatékonyságának paraméterei alapján (a betegek életkora és egészségügyi állapota).
A kereskedelmi szegmens magában foglalja az ART kifizetését a költségvetési forrásokon kívül bármilyen pénzeszközből - személyi, szponzorálási, biztosítási stb. -, ezért további nem orvosi szolgáltatásokat kínál a kényelem növelésével kapcsolatban, és a betegek szélesebb köre számára készült (nem viszonyítva). csak anyagi lehetőségeikre, hanem összetettebb diagnózisok jelenléte kórtörténetükben). A reproduktív klinikák minden marketingeszközt felhasználnak, saját adatbázisokat alakítanak ki, szállítási és szállodai szolgáltatásokat, kedvezményeket, kedvezményeket, akár „kulcsrakész IVF-et” is kínálnak (egy nagyon drága szolgáltatás, amely garantálja a gyermek születését egy párban, akárhány IVF-kísérlet is történik vele). vesz, a donor genetikai anyag felhasználásának és a béranyaság lehetőségével).
A meddőség nem jár közvetlen életveszéllyel, így kezelése általában fizetős, és nem fedezi a kötelező egészségbiztosítás. De az önkéntes egészségbiztosítás normái Oroszországban szinte teljesen kizárják a meddőséget a magas kereskedelmi kockázat miatt, amelyet a biztosítók véleménye szerint a sikeres kimenetelek nem kellően magas aránya okoz.
Ezek a körülmények elősegítik az ART piac kommercializálódását, és elsősorban a kis klinikák számára teszik vonzóvá (évente legfeljebb 1000-1500 IVF-kísérlet), amelyek megfelelő árakkal az „elit” szegmensbe pozícionálják magukat. Egy ilyen klinika tipikus projektje 25,5 millió rubelbe kerül. 24 hónapos megtérülési idejű beruházások, valamint a szolgáltatások orvosokon és betegeken keresztül történő népszerűsítése; ez megfizethetővé teszi a kisvállalkozások számára 11 . Ennek eredményeként folyamatosan növekszik az ART módszerekkel meddőségi kezelést nyújtó egészségügyi intézmények száma - 2009 elején Oroszország különböző régióiból több mint 90 ilyen klinika hirdette aktívan szolgáltatásait a médiában és az interneten.
Az aktivitás fokozódása megteremti az előfeltételeket az ART születések számának jelentős növekedéséhez Oroszországban, amelynek aránya a teljes megfigyelési időszak alatt nem haladta meg a születések teljes számának 0,5%-át 12 ; ez lényegesen alacsonyabb, mint a maximum - 4,2% (Dánia, 2002, 2004) 13 . Ha az ART komplexben figyelembe vesszük az ovuláció hormonális stimulációját, az eredmény még lenyűgözőbb lesz: egyes becslések szerint Belgiumban a születések 25%-a, Franciaországban pedig 5-10%-a történik ART segítségével. .
Ahhoz, hogy ez Oroszországban lehetséges legyen, meg kell változtatni a reproduktív gyógyászat állami és kereskedelmi szektora közötti kapcsolatot. Az akadályok közé tartozik az elégtelen költségvetési finanszírozás, a költségvetési kvóták olyan elosztása, amely nem veszi figyelembe a regionális szükségletek és az ART elérhetősége közötti különbségeket, valamint a kvóták „összekapcsolása” konkrét klinikákkal, valamint a meddő párok egészségügyi és demográfiai jellemzőivel. A „születési anyakönyvi kivonatokhoz hasonlóan” „reprodukciós anyakönyvi kivonatok” bevezetése, amelyek „követnék a beteget”, lehetővé téve a párnak, hogy önállóan döntsék el, hol használják fel a kvótát, enyhítve a korhatárokat, a diagnózisokat, a gyermekek jelenlétét stb. az ART-születések jelentősebb részét tehetné ki az orosz születési arányban.
A kérdésnek van egy minőségi oldala is. A meddőség problémájával szembesülők reproduktív céljai 2, 3, 4 gyermekre nőnek, azonban az ART általában nem gyógyítja meg a patológiát, hanem csak a gyermekvállalás lehetőségét teremti meg annak hátterében. Ezért a második és az azt követő gyermekek megszületéséhez szinte biztosan újra ART-ra lesz szükség, de a házaspár már nem számíthat az állam anyagi támogatására. Emellett az ART egy erőforrás a pontosan kívánt gyermekek megszületéséhez, amelyek gondozása már születésük előtt megkezdődik. A gyermekvállalást önként megtagadó „gyermekmentes” emberek népszerűségének növekedésével az ilyen ART gyerekek társadalmi értéke növekszik.
Amint azt egyes országok gyakorlata mutatja, a jelenlegi kedvezőtlen demográfiai helyzetben egyetlen forrás sem elhanyagolható a születésszám növelésére. A fogamzásgátló forradalom lehetővé tette, hogy azok, akik nem fogadják el a „spontán” szülőséget, megbízhatóan elkerüljék azt. A társadalom kiegyensúlyozott fejlődésének logikája megkívánja a fogamzásgátlással ellentétes intézmény kialakulását, elterjedését és megerősödését - olyan reproduktív technológiákat, amelyek lehetővé teszik mindenkinek, hogy gyermeket vállaljon, még akkor is, ha ennek biológiai akadályai vannak.
IN VITRO MŰTERMÉKEZÉS (IVF)
A standard IVF program főbb jelzései a következők:
1 . Abszolút petevezeték meddőség, mindkét petevezeték hiányával jár.
2 . Kitartó petevezeték és tubo-peritoneális meddőségés ha nincs kilátás további konzervatív vagy műtéti kezelésre.
3. Endokrin meddőség ha 6-12 hónapos hormonterápiával nem lehet terhességet elérni.
4. által okozott meddőség endometriózis kismedencei szervek, 2 évig tartó sikertelen kezeléssel.
5. Férfi faktor meddőség(oligo-, astheno-, teratozoospermia 1-2 fok).
6. Ismeretlen eredetű meddőség több mint 2 évig tartó, minden modern kezelési módszer, beleértve a laparoszkópiát, felhasználásával megállapított.
AZ IVF FŐ LÉPÉSEI
1. Szuperovuláció indukciója (ISO).
Szuperovulációt serkentő gyógyszerek
Tüszőstimuláló hormont tartalmazó készítmények
A nő szervezetében a tüszőserkentő hormon (FSH) felelős a tüszők éréséért, ezért az FSH-t tartalmazó gyógyszereket a szuperovuláció serkentésére használják. A rekombináns gyógyszereket ma a leghatékonyabbnak tekintik. Növelik a terhesség arányát és csökkentik a kezelési költségeket a posztmenopauzás nők vizeletéből izolált humán vizeletgonadotropinokon alapuló klasszikus gyógyszerekhez képest. Az egyik ilyen rekombináns FSH a Puregon, amelyet géntechnológiával hoztak létre. Jelenleg a nők maximális kényelme és kényelme érdekében a Puregon Pen injekciós tollat használják. Puregon Pen injektoros toll: a Puregon páciensek általi, otthoni szubkután beadására tervezték, újrafelhasználható, kész Puregon oldattal ellátott patronokat használ, a mikrotűnek köszönhetően csökkenti a manipuláció fájdalmát A Puregon Pen egy új beadási módszer FSH - Puregon, amely a következő előnyöket nyújtja: az orvos által felírt Puregon adag maximális pontossága, maximális lehetőség a dózis beállítására a beteg egyéni jellemzőinek megfelelően, maximális egyszerűség és könnyű használat, csökkenti a kezeléssel járó további stresszt. magát a kezelési folyamatot, ami növeli a pozitív eredménybe vetett bizalmat.
Olyan gyógyszerek, amelyek elnyomják az agyalapi mirigy saját hormonjainak termelését (hormonagonisták és antagonisták)
Annak megakadályozása érdekében, hogy a nők saját agyalapi mirigyhormonjai megzavarják a szuperovuláció stimulálását, termelésüket blokkolják antagonisták és agonisták. Az Orgalutran egy új antagonista, amely lehetővé teszi az agyalapi mirigy azonnali blokkolását, majd működésének gyors helyreállítását, ami majdnem felére csökkenti a kezelés időtartamát a hagyományos gyógyszerekhez (agonistákhoz) képest. Az agonisták (triptorelin, goserelin, leuprorelin, buserelin) meglehetősen hosszú távú alkalmazást igényelnek. Naponta kell beadni 20-30 napig, vagy egyszer, nagy adag formájában, amely legalább egy hónapig felszívódik.
Humán koriongonadotropint (hCG) tartalmazó készítmények
A tüszők punkcióját 36 órával a hCG injekció beadása után hajtják végre, ami elindítja az érett tüszők ovulációját. A hCG használata lehetővé teszi, hogy érett tojást kapjon, amely készen áll a megtermékenyítésre. A hCG-t tartalmazó gyógyszerek egyike a Pregnil.
Szuperovulációs stimulációs protokollok
A VECO különböző típusú protokollokat használ. Emlékeztetni kell arra, hogy nincsenek merev kezelési rendek, és az alábbi protokollok mindegyikéhez egyéni eltérések lehetségesek.
"Tiszta protokoll"
Egyes nők stimulációs kezeléseket alkalmaznak anélkül, hogy az agyalapi mirigyet blokkolnák. Ehhez csak FSH-t tartalmazó gyógyszereket használnak, például a Puregon Pan-t. Ezt a sémát „tisztának” nevezik. Hátránya a tüsző korai peteérésének (repedésének) valószínűsége már a szúrás előtt, ami lehetetlenné teszi a peteszerzést. Ez az esetek 15-20% -ában fordul elő. Ebben a protokollban a stimuláns gyógyszerek beadása a menstruáció 2–3. napján kezdődik és 9–14 napig tart. A napi adagot az orvos az ultrahang adatok függvényében állítja be, amit általában 4-5 alkalommal végeznek el a teljes stimulációs időszak alatt. A tüszők végső éréséhez hCG-t, például Pregnilt adnak be, majd 35-36 óra elteltével a tüszőket átszúrják.
"Hosszú Protokoll"
A protokollt „hosszúnak” nevezik, mert általában a stimulációt megelőző menstruációs ciklus 21–23. (ritkán a 2.–3.) napján kezdődik. Az agyalapi mirigy blokkolására a kezelés kezdetén csak az agonistát kell bevenni 5 napig. Az agyalapi mirigy blokádjának elérése után megkezdődik a menstruáció, és annak kezdetétől számított 2-3 napon belül a stimulációt FSH-t tartalmazó gyógyszerekkel végezzük, ugyanúgy, mint a „tiszta” kezelésben, de az agonista folyamatos adagolásával együtt. .
"Optimális protokoll"
Az új antagonista Orgalutran alkalmazásakor a stimulációs protokoll jelentősen lerövidül, miközben az agyalapi mirigy kifejezett és könnyen visszafordítható blokádja megmarad. A stimuláció a „tiszta” kezeléshez hasonlóan a menstruációs ciklus 2–3. napján kezdődik FSH-t tartalmazó gyógyszer napi adagolásával. Ezután a stimuláció 5. vagy 6. napjától az Orgalutran napi injekcióit adják be, miközben a stimuláció folytatódik. Így az „Optimális Protokoll” rövid lesz, mint a „tiszta” sémában, és hatékony, mint a „hosszú” sémában. Az új generációs Puregon és Orgalutran (antagonista) gyógyszerek kombinációja:
- a kezelési idő csökkentése;
- az injekciók jobb toleranciája;
- bizonyított hatékonyság.
Ennek köszönhetően a Puregon és az Orgalutran együttes alkalmazása „a remény két összetevője a meddőség kezelésében” nevezhető.
Az 1. ábra egy stimulált petefészek ultrahangos képe látható sok tüszővel. A piros pontok a maximális tüszőt jelölik 18 mm átmérővel:
Hány tüszőre van szükség az IVF-hez?
Az IVF-hez szükséges minimális tüszők száma több tényezőtől függ:
1. tüszőméretek;
2. a nő életkora;
3. az ovuláció stimulálására tett korábbi kísérletek száma és eredményei;
Egyes szakértők úgy vélik, hogy a stimulációs folyamat során legalább 5, 14 mm-es tüszőt kell szerezni. és többen azonban az elmélet ellenzői azzal érvelnek, hogy az eljárás akkor is elvégezhető, ha van legalább egy megfelelő méretű tüsző.
A legtöbb amerikai klinika azon a véleményen van, hogy legalább 3-4 domináns tüszőre van szükség ahhoz, hogy az eljárás sikeres legyen.
Az ovuláció indukciója nem hajtható végre, ha:
1. Nem biztos, hogy a petevezetékek átjárhatók;
2. A tüszők növekedésének ultrahangos monitorozására nincs lehetőség;
3. Ha az FSH szint meghaladja a 20 NE/l-t amenorrhoea hátterében;
4. A meddőségi kezelés időtartama már meghaladta a 2 évet.
Mesterséges megtermékenyítés (AI)- ez egy olyan eljárás, amelynek során a férj vagy a donor speciálisan feldolgozott spermáját juttatják be a méh üregébe. Az AI és az ovuláció indukció kombinációja jelentősen növeli a kezelés hatékonyságát.
Az AI-t a humán koriongonadotropin (ez a gyógyszer 36-42 óra elteltével programozza be az ovulációt) beadása után 12 és 36 óra után (egyes adatok szerint optimálisan 38-42 óra múlva) a várható ovuláció napjain végezzük egyszer/kétszer.
Elfogadhatatlan a mesterséges intelligencia elvégzése az IVF helyettesítéseként, ha az IVF-program közvetlen jelzése van.
A 2. ábra vázlatosan mutatja be az előkészített spermiumok méhüregbe történő bevezetését.
Milyen tényezők határozzák meg az intrauterin megtermékenyítés hatékonyságát?
A szakirodalom szerint ismert, hogy az eljárás hatékonysága csökken, ha:
1. 38 év feletti nőknél;
2. Csökkent petefészek-tartalékkal rendelkező nőknél;
3. Alacsony spermaminőséggel;
4. Az endometriózis mérsékelt és súlyos formáinak jelenlétében;
5. Azoknál a nőknél, akiknek kifejezett összenövése van a medencében.
Milyen spermiumok használhatók méhen belüli megtermékenyítéshez?
A megtermékenyítéshez házastárs vagy donor spermáját kell használni, amely 1 ml-enként több mint 10 millió mozgékony spermiumot tartalmaz. Egy másik kritérium az, hogy a megtermékenyítésre szánt anyagban legalább 4 millió normál morfológiájú spermium jelen legyen.
Hány megtermékenyítési kísérlet tehető?
Ismeretes, hogy a legtöbb megtermékenyítésből származó terhesség az első 3 ciklusban következik be. 3 próbálkozás után ennek a módszernek az esélye, valamint a hatékonysága csökken, és 4-6 sikertelen manipuláció után megbízhatóan alacsony.
Hány méhen belüli inszeminációt kell elvégezni egy ciklus alatt?
Ez a kérdés a mai napig ellentmondásos. Egyes tanulmányok kimutatták, hogy nincs szignifikáns hatékonyságnövekedés, ha két termékenyítést végeznek a ciklus megfelelő napjain az egyhez képest. Egyes adatok szerint a kettős megtermékenyítés alkalmazása jelentősen növeli a vemhesség arányát.
A valószínűségi elmélet szerint a kettős megtermékenyítés növeli annak esélyét, hogy a spermiumok pontosan a megfelelő időben kerüljenek be, különösen, mivel a spermiumok élettartama a nő szervezetében körülbelül 2-5 nap.
Érett petesejtek gyűjtése (petefészek-punkció)
A petefészek-punkciót a hátsó hüvelyi fornixon keresztül végezzük ultrahangos ellenőrzés mellett, rövid távú érzéstelenítésben, modern gyógyszerekkel, minimális mellékhatásokkal.
A nő alszik, és nem érez semmit. Az 1. ábra egy ultrahangos képet mutat arról, hogy a follikuláris folyadékot speciális tűvel gyűjtik, hogy érett petesejteket nyerjenek.
Miután az összes szükséges tüszőt átszúrták, a nőt egy órán keresztül megfigyelik, majd hazaküldik. A 2. ábra egy 25 éves nőtől follikuláris punkció eredményeként kapott jó minőségű petesejteket mutat be.
Összehasonlításképpen a 3. ábrán egy rossz minőségű petesejt látható, amelyet egy 43 éves nő tüszőinek átszúrásával nyertek. A petesejtek közötti különbségek még szabad szemmel is láthatók.
Embriótenyésztés
Az embriológiai laboratóriumban a spermium megtermékenyíti a tojást. Ez a szakasz 3-5 napig tart. A 4. ábra egy megtermékenyített tojást mutat. A központban 2 pronukleus található - férfi és nő, a jobb felső sarokban pedig egy sarki test - a megtermékenyítés már megtörtént jele.
4. ábra. Megtermékenyített tojás.
Az eljárás embriológiai részének egyik fontos szakasza a felmérés "minőség" kapott embriókat, amelyet egy speciális embriológus végez számos jel alapján:
cellák száma;
Ugyanaz a méret;
A töredezettség mértéke.
Az embriológusnak meg kell jegyeznie a multinukleáció jelenlétét, a vakuolizáció megjelenését, a granularitást stb. Általában az embrió „minőségének” meghatározása legkorábban 48 órával a megtermékenyítés után lehetséges.
2 nap elteltével rendszerint legalább egy embriót kell szerezni, amely legalább 3 sejtből áll. 72 óra elteltével az embriónak legalább 6 vagy több sejtből kell állnia.
Azok az embriók, amelyekben több szabályos alakú és méretű, csekély vagy egyáltalán nem töredezett sejt található, nagyobb eséllyel kerül beágyazódásba, mint azoknak, amelyek nem felelnek meg ezeknek a követelményeknek.
Összehasonlításképpen az alábbiakban egy „jó” és „alacsony” minőségű embriót mutatunk be.
Az embrió „minőségének” mikroszkópos vizsgálata némi alapot ad ahhoz, hogy felmérjük egy adott embrió beültetésének becsült esélyét az átültetés után. A statisztikák azonban azt mutatják, hogy a program 3 „nagyszerű” embrió átvitelekor sikertelen, míg a „rossz minőségű” embriók átvitele nagyon szép gyermekeket eredményez.
Sajnos a további fejlődéshez, valamint a méhüregbe történő beültetéshez szükséges valódi genetikai potenciált nem lehet felmérni. Sok embriológiai laboratórium pontozási skálát használ az embriók állapotának felmérésére, de egységes séma még mindig nem létezik. Most ezt a területet intenzíven tanulmányozzák az embriológusok világszerte.
A betegek gyakran feltesznek egy kérdést az embriológusnak, attól tartva, hogy az „alacsony minőségű” embriók, amelyeknek mégis sikerült beültetniük a méhbe és megkezdték fejlődésüket, végül „rossz minőségű” gyermekekké válhatnak. A világ számos laboratóriumának tapasztalata ezt mutatja Az ilyen embriók átültetéséből született gyermekek ugyanolyan okosak, intelligensek és szépek, mint a „kiváló minőségű” embriók átviteléből született gyermekek. Az egyetlen szempont, amelyre figyelni kell az ilyen embriók átültetésekor, az a méhen belüli fejlődés és születés alacsonyabb esélye.
Az embriók átvitele a méh üregébe
Ez a szakasz az egyik fontos pont, hiszen a laboratóriumban nyert jó minőségű embriókat nagyon óvatosan és minimális traumával kell átvinni a méhüregbe, körülbelül a méhfenék közepéig.
Egy nő számára ez az eljárás fájdalommentes, és nem igényel további érzéstelenítést. Az embriót tartalmazó speciális katétert a méhnyakon keresztül vezetik be a méh üregébe, amelyet ultrahanggal vezérelnek.
Miután a katéter elérte a kívánt pontot, az embriót bevisszük a méhüregbe, a katétert eltávolítjuk, és mikroszkóppal ellenőrizzük (figyeljük a kívánt embriók teljes bejutását a méhüregbe). Ha az embriók továbbra is a katéterben maradnak, az eljárást azonnal meg kell ismételni, majd a katéter állapotának újbóli ellenőrzése következik.
A 8. ábra ultrahangos képet mutat az embriótranszferről: zöld – a katéter mozgása a méhüregbe a méhnyakon keresztül:

8. ábra. Az embriótranszfer ultrahangképe*
A következő órában a nőnek le kell feküdnie, majd némileg korlátoznia kell a fizikai aktivitást. Az embrió átültetése után 9-11 nappal javasolt a humán koriongonadotropin tartalmának vizsgálata a nő vérében a terhesség jelenlétének megállapítása érdekében.
SPERMÁK INJEKCIÓJA A PEJÉS CITOPLAZMÁBA (ICSI)
ICSI– az ICSI angol rövidítés orosz átírása – – egyetlen spermium mikromanipulátoraival történő befecskendezése a petesejt citoplazmájába (intracitoplazmatikus spermiuminjekció) a megtermékenyítéshez; mikroszkóp alatt, 200-x400-as nagyítással végezzük.
Az alábbi képen egy tű beszúrásának folyamata látható, hogy a spermát a tojásba fecskendezzék.



1. kép Tű beszúrása a spermium tojásba való befecskendezéséhez. Ennek az eljárásnak a végrehajtása során az esetek 70-85% -ában in vitro megtermékenyítés történik.
Az ICSI indikációi
Egy vagy több spermogram paraméter jelentős romlása;
Antisperma antitestek jelenléte;
A spermium hiánya az ejakulátumban (azoospermia), amikor a spermát sebészeti úton nyerik ki a heréből (TESA) vagy mellékhereből (PESA);
Sperma kinyerése a vizeletből retrográd ejakuláció során;
A megtermékenyítés hiánya a standard IVF eljárás előző 2 kísérletében;
Olyan helyzetek, amikor standard IVF-el alacsony megtermékenyítési arányt feltételezhetünk, például súlyos endometriózisban vagy ismeretlen eredetű meddőségben szenvedő betegeknél.
Ez az eljárás több szakaszból áll:
1. Tüszők punkciója a szuperovuláció stimulálása után petesejtek kinyerése céljából;
2. Egy spermium összegyűjtése nagyon vékony és éles tűvel;
3. A spermiumok mikroszkóp alatt történő bejuttatása a petesejt citoplazmájába;
4. Másnap reggel ellenőrizze a megtermékenyítést.
Számos tanulmány szerint a terhességi ráta az ICSI eljárást alkalmazva lényegesen magasabb, mint a standard IVF program esetén.
Valószínűleg ez annak a ténynek köszönhető, hogy a programban részt vevő nők általában fiatalabbak és termékenyek (mivel az ICSI indikációja elsősorban a férfi tényező), ami az eredményeként kapott tojások minőségének javulásához vezet. a defekt.
Azt is meg kell jegyezni, hogy az ICSI-t bizonyos esetekben „nőstény indikációkra” is elvégzik, olyan esetekben, amikor csak kis számú és nem túl jó minőségű pete beszerzése lehetséges, ami a petefészek-tartalék csökkenésével jár. .
A spermiumok extrahálása a mellékhereből (MESA) VAGY a hereszövetből (TESE)
Sajnos néhány férfi ejakulátumában nincs spermium, így a hagyományos módszerek, mint például az IVF és az ICSI további előzetes „lépéseket” igényelnek a szükséges sperma megszerzéséhez. A sperma megszerzésének ezek a módszerei a következők:
-TESE (herék sperma kivonása)- spermiumok kinyerése (kinyerése) a petefészekszövetből;
-MESA (mikrosebészeti epididimális spermium aspiráció)– a spermiumok mikrosebészeti aspirációja a mellékhereből;
-PESA (perkután epididimális spermium aspiráció)– spermiumok perkután aspirációja a mellékhereből.
A MESA eljárás segítségével más technológiákkal összehasonlítva a legjobb minőségű és elegendő mennyiségű spermát nyerhet. Ez az eljárás a legkíméletesebb is, és minimális számú szövődményt okoz.
Ezeknek a módszereknek a végrehajtása során általában arra törekszenek, hogy a spermiumok maximális számát megszerezzék, amelyeket azután lefagyaszthatnak és a következő ciklusokban felhasználhatnak sikertelen IVF-kísérletek esetén.
Elérhetőség azoospermia férfiaknál (a spermiumok hiánya az ejakulátumban) több tényező is összefüggésbe hozható, ezért az azoospermiának két típusa van:
1) Obstruktív azoospermia.
Ez azt jelenti, hogy bizonyos szinten elzáródnak azok a csatornák, amelyeken keresztül a spermiumok felszabadulnak, vagyis megtörténik a magömlés. Ennek az állapotnak az okai lehetnek műtét (vazektómia) vagy veleszületett patológia.
Vagyis ebben a férfikategóriában maga a spermium jó, azonban néhány manipulációt kell végrehajtani az „egészséges” spermiumok megszerzéséhez. Erre a célra bármelyik technika használható PEZA, amelyben vékony tűvel gyűjtik össze a spermiumot a mellékhereből, ill TESE amelyben magából a heréből nyerik ki a spermát biopsziával. Mindkét eljárást helyi érzéstelenítésben, ambulánsan végezzük.
Az obstruktív azoospermiában szenvedő betegeknél a spermiumfelvétel hatékonysága a TESE során általában 100%-os, ha az előzetes diagnosztikai biopszia megerősítette a spermatogenezis jelenlétét.
2) Nem obstruktív azoospermia.
Ez egy olyan patológia, amelyben a spermiumok nem azért hiányoznak az ejakulátumból, mert valami megakadályozza a bejutást, hanem azért, mert számuk kritikusan lecsökkent. Általában ezeknek a férfiaknak a herében kis területei vannak, ahol a spermatermelés megtörténik, ezért ezeknél a férfiaknál több helyről herebiopsziát vesznek át az aktív spermatogenezis (TESE) területeinek kimutatása érdekében.
A közelmúltban ilyen esetekben egy új technikát alkalmaznak - a microTESE-t, amelyben egy speciális műtőmikroszkóp segítségével herebiopsziát végeznek, amely lehetővé teszi, hogy már a manipuláció során pontosan meghatározza, melyik zónából kell kivenni a herék egy darabját. a spermiumok maximális számának eléréséhez.
A heretérképezésnek nevezett módszer is használható. A biopszia elvégzése előtt vékony tűvel megvizsgálják a here területeit, amellyel több helyről folyadékot nyernek, amelyet azonnal megvizsgálnak a spermiumtartalom szempontjából. Ez a módszer lehetővé teszi a here azon területeinek azonosítását is, amelyeket „figyelembe kell venni” a TESE eljárás végrehajtása során. A megtermékenyítéshez szükséges spermiumok általában az esetek 70%-ában beszerezhetők.
A fent leírt módszerek alkalmazásakor utólag javasolt az ICSI eljárás alkalmazása a megtermékenyítés valószínűségének növelése érdekében.
JÁTÉKOK ÉS ZIGÓTÁK ÁTSZÁLLÍTÁSA A PETECSÖVEKBE
Ezek olyan ART módszerek, amelyek során embriókat (angol, TET), zigótákat (angol, ZIFT) vagy ivarsejteket visznek át a petevezetőkbe (GIFT). Egyes elképzelések szerint a sejtek „bejuttatása” a petevezetékbe, nem pedig a méh üregébe, mint a hagyományos embriótranszfernél, a lehető legközelebb áll a természetes megtermékenyítés folyamatához, amely normál esetben a petevezetékben fordul elő.

1. kép Az ivarsejtek és zigóták petevezetékekbe történő átvitelének mechanizmusa.
Mit tartalmaznak ezek az eljárások?
A TET magában foglalja a petesejtek beszerzését, laboratóriumi megtermékenyítését a férj spermájával „in vitro”, majd az embriót a megtermékenyítés után 2 nappal a petevezetékbe juttatják.
A ZIFT egy embriótranszfer 1 nappal a megtermékenyítés után, vagyis a zigóta stádiumban. Mindkét eljárás sebészeti beavatkozást igényel laparoszkópia formájában, melynek során a sejteket a petevezetékekbe juttatják.
Kinek szólnak ezek a módszerek?
A TET és a ZIFT bármely meddő páron elvégezhető, ha a petevezetékek átjárhatóak és normál működési állapotban vannak, valamint méhen belüli synechia (összenövés) hiányában, vagyis ha a méhüreg állapota kielégítő.
Ezek az eljárások akkor is javallhatók, ha az intrauterin megtermékenyítési eljárás 4-6 cikluson belül hatástalan.

2. ábra. Az ivarsejtek és zigóták petevezetékekbe történő átvitelének folyamata.
TET/ZIFT (ivarsejtek, zigóták vagy embriók átvitele a petevezetékbe) vagy hagyományos IVF (az embriók közvetlenül a méhüregbe történő átvitele)?
Mindig felmerül a kérdés: mi a jobb, és milyen esetben, és mit kell tenni? A modern orvoslás taktikáját nemcsak az orvosi indikációk, hanem a nő kívánságai is meghatározzák. Például, ha minden más dolog egyenlő, az ivarsejtek vagy embriók petevezetékbe történő átvitelének ellenjavallatai hiányában a nő ragaszkodik ehhez a manipulációhoz, hogy a megtermékenyítési folyamatot a lehető legközelebb hozza a természeteshez. Illetve kategorikusan elutasítja a laparoszkópia, vagyis a műtéti beavatkozás kapcsán. Sőt, minden klinikának megvannak a saját képességei, és bizonyos pozíciókat foglal el egyik vagy másik módszerrel kapcsolatban.
Az alábbiakban azonban felsorolunk néhány tényt, amelyek segíthetnek a saját vélemény kialakításában.
1. Egyes tanulmányok szerint a beágyazódás (tehát a terhesség) gyakorisága a petevezetékbe történő áthelyezéskor lényegesen magasabb, mint a méhüregbe történő áthelyezéskor.
2. Randomizált vizsgálatok szerint azonban nem találtunk szignifikáns különbséget a petevezetékbe vagy a méh üregébe történő transzfer alkalmazásakor.
3. További kutatások szükségesek a betegek TET programba való bevonásának pontosabb indikációinak meghatározásához stb.
4. Úgy gondolják, hogy egy adott módszer hatékonyságát nemcsak az orvos képzettsége határozza meg, hanem az adott módszer alkalmazásában szerzett tapasztalata is.
5. A petevezeték transzfer módszerek alkalmazása jelentősen megnöveli a teljes program költségét a laparoszkópia költségének beszámításával.
És így, támogatói ezekről a módszerekről azt mondják
a) nagy hatékonyságukról;
b) a természetes folyamathoz való maximális közelség.
Ellenfelek átvitel a petevezetékbe azzal érvelnek
a) a petevezeték átültetési program nagy hatékonysága annak köszönhető, hogy gyakorlatilag egészséges betegek vesznek részt ebben a programban (ideális petevezetékkel és méhüreggel rendelkeznek), és a meddőség vezető tényezője kizárólag a férfi - ez az oka annak, magas terhességi arány;
b) ivarsejtek vagy embriók átültetésekor laparoszkópiát alkalmaznak, amely bár minimálisan invazív módszer, mégis műtéti beavatkozás, a költségekről nem is beszélve;
c) a termékenységi orvosok, akik már régóta részt vesznek a méhüregbe történő áthelyezésben, természetesen jobban teszik ezt (és korlátozhatja magát a méhüregbe történő átvitelre);
d) laboratóriumi zigóta transzfer esetén a megtermékenyített petesejt mindössze egy napon belül, az embrió petevezetékbe történő átvitele esetén 2 napon belül marad meg.
A petevezetékbe való áthelyezés ellenzői szerint ezek az időszakok nem teszik lehetővé a legjobb embrió kiválasztását, ahogyan a méhüregbe történő áthelyezéskor (a laboratóriumban a 3-5. napon) meg lehet tenni.
Általánosságban elmondható, hogy az adatok ellentmondásosak, és az adott módszer kiválasztását minden alkalommal egyedileg, számos tényező figyelembevételével határozzák meg.
JÁTÉKOK ÉS EMBRIÓK KRIOKONERVÁCIÓJA
Ivarsejtek és embriók mélyhűtése – Ez egy olyan technológia, amely lehetővé teszi a spermiumok, petesejtek és embriók megőrzését speciális alacsony hőmérsékleti körülmények között.
A petefagyasztás technológiája viszonylag új, azonban 2007-re már 200 gyermek született világszerte egy felengedett petesejt megtermékenyítését és embriótranszfert követően.
Egyes esetekben, különösen férfiak és nők daganatos megbetegedései esetén, amikor a petefészkek vagy a herék eltávolítását tervezik, valamint olyan esetekben, amikor kemoterápia vagy sugárkezelés szükséges, előzetesen szükséges a csírasejtek beszerzése és lefagyasztása. külön-külön vagy megtermékenyítés után. Ezeket a programokat az ilyen betegek számára kínálják. A világ különböző laboratóriumai szerint az átlagos terhességi arány a fagyasztott embriók átvitelekor körülbelül 50%.
Az embriók fejlődésük bármely szakaszában lefagyaszthatók: egynapos koruktól kezdve a blasztociszta stádiumig (5-6 nap), míg az „öregebb” embriók lefagyasztása lehetővé teszi a legjobb minőségű embriók kiválasztását.
Hogyan történik a fagyás és hogyan lehetséges?
Jelenleg az alkalmazott eljárás ultragyors fagyasztás -196 Celsius fokig, majd ezen a hőmérsékleten történő tárolás folyékony nitrogénben.
Fizikailag ez a folyamat az üvegesedés, vagyis a folyadék üveges állapotba kerülése, a kristályosodási szakasz megkerülésével. Ez a hatás csak a cella hőmérsékletének nagyon gyors csökkentésével érhető el. Ez nagyon fontos feltétel, mivel a fagyasztás során keletkező kristályok egyszerűen károsíthatják az embriókat.
Ennek a manipulációnak a végrehajtása során szükségszerűen kétféle krioprotektort használnak - „a sejtbe szivárgó” (például propándiol) és extracelluláris (például szacharóz és lipoprotein). Ezek az anyagok lehetővé teszik:
1. Csökkentse a fagyáspontot és akadályozza meg az intracelluláris kristályok („jégtömbök”) képződését;
2. Védje a sejteket azáltal, hogy kölcsönhatásba lép a membránjaikkal, miközben megváltoztatják állapotukat és sűrűvé vagy merevevé válnak.
Ezt követően az embriókat speciális tartályokba helyezik, ahol a megfelelő hőmérsékleten, folyékony nitrogénben tárolják őket a kiolvasztásig.
Hogyan olvasztják fel az embriókat?
A nő megfelelő előkészítése után teljes körűen ellenőrizzük a fagyasztott embriók címkézésének megfelelőségét, majd szobahőmérsékleten leolvasztják. Ebben a folyamatban nem a kiolvasztás ideje a legfontosabb, hanem a fagyvédő szerek gondos hígítása és eredeti tulajdonságaik megőrzése az embriók által a felolvasztás után.
Az Amerikai Reproduktív Orvostudományi Társaság Etikai Bizottsága a következő tényezőket azonosította, amelyek növelik a terhesség arányát az embriófagyasztási technológia alkalmazásakor:
1. az optimális számú embrió átültetése a hármasikrek és négyesek kialakulásának valószínűségének csökkentése érdekében;
2. embriók átvitele természetes ciklusban, és nem stimulált ciklusban, amelyben az ösztrogén és progeszteron tartalma nem haladja meg a normál értéket;
3. az ovulációt serkentő gyógyszerek mennyiségének maximális lehetséges csökkentése a terhesség valószínűségének növelése érdekében.
Kockázatok és kudarcok
Az embriófagyasztás technológiájának legfontosabb szempontja az, hogy egyes egészséges embriók nem maradnak életben a gyors hőmérséklet-változások miatti stressz következtében. Átlagosan az embriók 25-50%-a nem él túl.
Másrészt a mélyhűtést darwini természetes szelekciónak tekinthetjük, amelynek során a „legerősebbek” maradnak életben, amelyek a jövőben átkerülnek.
Egy másik fontos kérdés ennek a technológiának a használatakor annak valószínűsége, hogy egy gyermek valamilyen hibával születik. Számos állatkísérlet kimutatta, hogy a fagyasztás/olvasztás technológia nem eredményez hibás állatok születését. Embereken végzett vizsgálatok kimutatták, hogy a felolvasztott embriók átvitele következtében született gyermekeknél nem nőtt jelentős mértékben a rendellenességek száma a populáció más gyermekeihez képest. A probléma ezen aspektusait azonban továbbra is intenzíven tanulmányozzák, csakúgy, mint a terhességi arány növelésének lehetőségeit.
Ha a terhesség felolvasztott embrió áthelyezése következtében következik be, a házaspárnak joga van dönteni a megmaradt embriók sorsáról. Lefagyva maradhatnak (a mai adatok szerint 5-10 évig), felolvaszthatók, vagy adományozhatók és átvihetők egy másik meddő nőnek.
BERESKÁNYZAT
Béranyaság - Ez az egyik olyan ART módszer, amelyben a petesejt spermával történő megtermékenyítésével „in vitro” létrejött terhességet egy béranya, azaz egy másik nő hordozza.
Erre olyan esetekben van szükség, amikor egy nőnek lehetősége van tojást, a férfiaknak pedig spermát szerezni, de a méh állapota (veleszületett vagy szerzett patológia) vagy hiánya sebészeti beavatkozások után nem teszi lehetővé a terhességet.
A béranya kiválasztásakor átfogó vizsgálatot végeznek, orvosi dokumentációt készítenek, és menstruációs ciklusát szinkronizálják a meddő nő ciklusával, hogy felkészítsék testét az IVF eredményeként kapott embrió átültetésére. vagy ICSI.
A béranyasági programokról, valamint ennek a módszernek a jogi alapjáról ma már világszerte intenzíven vitatkoznak, hiszen ennek a problémának nemcsak orvosi vonatkozásai (különösen a nők béranyaságra való alkalmassága), hanem számos legalizálást és tisztázást igénylő etikai kérdésekről.
Például a béranyaság továbbra is tilos Ausztriában, Németországban, Norvégiában, Svédországban, Franciaországban és néhány amerikai államban. Annak ellenére, hogy ezt a programot Belgiumban, Görögországban, Írországban és Finnországban használják, használatának nincs jogalapja.
Milyen követelményeket támasztanak azon nők számára, akik béranya akarnak lenni?
Életkor 23-35 év;
legalább egy saját gyermeke van;
Akik már nem akarnak saját gyereket vállalni;
Házas vagy élettársi kapcsolatban él;
Pénzügyileg stabil pénzügyi helyzet;
Szerettei támogatása és jóváhagyása e szerep betöltéséhez;
Nemdohányzók legalább 6 hónappal a fogantatás előtt;
Élvezze a terhesség állapotát;
Komoly vágy, hogy segítsen egy meddő párnak;
Normál magasságú és súlyú nők;
beleegyezés az abortuszba, ha azt olyan házaspár kéri, akinek gyermeke van; valamint az embrió csökkenése többes terhességben.
Egyes országokban vannak ügynökségek a béranyák kiválasztására.
Az alábbiakban például az egyik ügynökség által nyújtott szolgáltatások teljes skálája látható, melynek költsége kb 25 ezer Baba.
Béranya jelöltség biztosítása a béranyaközpont adatbázisából;
Potenciális béranya pszichológiai diagnosztikája a béranya béranya programban való részvételre való pszichológiai alkalmasságára és felkészültségére;
A potenciális béranya átfogó orvosi vizsgálata az in vitro megtermékenyítésre, terhességre és egészséges gyermek születésére való alkalmasság igazolására;
Kezdeti jogi egyeztetés, megállapodás készítése a genetikai szülők és a béranya között, figyelembe véve a vásárlók egyéni helyzetének minden lehetséges árnyalatát és a szükséges kitételeket a „gyermekvállalásról” szóló megállapodásba;
Fordítói szolgáltatások a kezdeti konzultáció és a genetikai szülők és a béranya közötti megállapodás megkötése során.
A program koordinálása, ellenőrzése a gyermek születéséig és minden szükséges dokumentum átvétele.
Kompenzáció a béranya részére a terhesség teljes időtartamára (szakaszos fizetés - 10% terhességkor, 90% 4-6 héttel a gyermek születése előtt - a pénzeszközöket a béranya bankszámlájára utalják);
Kártérítés a béranya számára, ha egynél több gyermek születik;
Havi tartásdíj a terhesség 9 hónapjára - havonta fizetendő; Terhesség alatti orvosi felügyelet – a klinikai szolgáltatások és az összes szükséges vizsgálat költsége;
Egészségbiztosítás a béranya számára balesetek ellen;
Dokumentumok elkészítése a gyermek számára a nagykövetségen történő további benyújtáshoz;
A program ellenőrzésének és támogatásának költsége a béranya és a genetikai szülők (Vásárlók) közötti szerződés megkötésétől az embrió béranya számára történő átültetéséig;
A program ellenőrzésének és támogatásának költsége a béranya és a genetikai szülők (Vásárlók) közötti megállapodás megkötésétől a terhesség bekövetkezésének vagy elmaradásának igazolásáig;
A donor kompenzáció, orvosi vizsgálat, központunk szolgáltatásainak költsége.
A béranya gondozójának 24 órás felügyelete, az összes házi feladat elvégzése, az orvoshoz való elkísérés és az elvégzett munkáról szóló teljes jelentés, külön lakhatás biztosításával;
Az orvosi szolgáltatások költsége külön fizetendő.
Az Orosz Föderáció jelenlegi családjogi törvénykönyve (1995. december 8-i keltezésű, 4. szakasz 10. fejezet 51. cikk (4) bekezdés második rész) értelmében: „Azok a személyek, akik házasságban élnek egymással és írásban hozzájárultak embrió beültetése másik nőbe annak kihordása céljából, a gyermek szülei csak a gyermeket világra hozó nő (béranya) beleegyezésével regisztrálhatják.”
Az egészségügyi intézményben mindkét fél (helyettes anya és leendő szülők) csak a szükséges orvosi dokumentációt írja alá, azonban a kérdés jogi oldalát hazánkban ennek a folyamatnak a résztvevőinek önállóan, megfelelő szolgáltatások segítségével kell megoldaniuk (következtetés). megállapodás).
OVODONATION
Ovodonáció, vagy tojás adományozás, Ez az egyik olyan ART módszer, amelyben a donor petesejteket megtermékenyítésre használják.
Ezt a módszert először 1982-ben alkalmazták sikeresen, és a mai napig például az Egyesült Államokban évente mintegy 15 000 donor petesejteket használnak fel megtermékenyítésre. Az IVF átlagos hatékonysága ezzel a technológiával körülbelül 50%.
Mik a javallatok ennek a módszernek a használatára?
1. A módszer alkalmazásának fő javallata a petesejtek (petéket tartalmazó) hiánya egy nőben, ami a következőkhöz kapcsolódik:
Természetes menopauza;
Csökkent petefészek-tartalék (fejlődési rendellenességek, korai petefészek-elégtelenség szindróma, petefészkek eltávolítása vagy reszekciója, sugárkezelés vagy kemoterápia utáni állapot).
2. Normál számú petesejtek genetikai rendellenességeinek jelenléte, ami lehetetlenné teszi a megtermékenyítéshez való felhasználásukat.
Általában a petesejt donorok a következők:
1. a terhességet kívánó beteg hozzátartozói;
2. speciális donorok, amelyek listája foglalkozásuk, megjelenésük, vércsoportjuk stb. leírásával szakorvosi intézményben beszerezhető.
A petedonoroknak 34 év alattinak kell lenniük, egészséges gyermekük van, és nem lehet semmilyen feltűnő fizikai tulajdonsága.
A petesejt donorok ovulációs stimuláción esnek át (ciklusuk szinkronizálódik a várandós anya ciklusával), majd a tüszők szúrásával petesejteket nyernek, amelyek azután az IVF-folyamat minden szakaszán átmennek.
Az in vitro megtermékenyítés után fellépő terhességek kezelése immunológiai rendellenességek által okozott visszatérő vetélésben
P A visszatérő vetélésben szenvedő nők a terhesség első trimeszterében az implantációs és placentációs rendellenességek kockázati csoportját képezik. Az ilyen rendellenességeket leggyakrabban az endometrium és a fejlődő trofoblasztsejtek közötti immunkölcsönhatások okozzák.
Az in vitro megtermékenyítésen (IVF) átesett nők általában hormonális problémákkal küzdenek, krónikus gyulladásos betegségekben szenvednek, és ennek következtében összenövések a medence területén, és gyakran estek át egy vagy több sebészeti beavatkozást a méhen, a petefészkeken és a csövekben. Ugyanakkor az asszisztált reprodukciós technológiák alkalmazásával megoldható terhességi nehézségek immunológiai problémákkal párosulnak, ami esetenként ismétlődő korai reprodukciós veszteségekhez vezet. Az ismétlődő magzati veszteségekben szenvedő betegeknél egy úgynevezett ördögi kör alakul ki, amikor az immunpatológiai folyamat a terhesség legkorábbi szakaszától beindul.
Az immunrendszer védekező funkcióit a terhesség korai szakaszában a méhnyálkahártya természetes ölősejtek aktivitásának visszaszorítása és az anyai szervezet által blokkoló faktorok termelődése formájában különböző, nagyrészt hormonfüggő mechanizmusok biztosítják, a amelyek megsértése beültetési kudarcokat vagy korai spontán vetélést okoz.
Az autoimmun folyamatokban az immunrendszer agressziójának célpontja az anya saját szövetei, azaz. az antitest válasz a saját antigénjei ellen irányul. A fejlődő petesejt a trofoblaszt erek trombózisa, korlátozva invázióját, esetenként pedig az autoantitestek a fejlődő méhlepény foszfolipidjeire gyakorolt közvetlen károsító hatása következtében érintett. Az alloimmun reakciókban a nő immunválasza az apától kapott embrionális antigének ellen irányul, ami szintén megakadályozza a teljes védőreakció kialakulását az endometriumban.
Ebben a vonatkozásban a pregesztációs felkészítés kérdései, amelyek normalizálhatják az endometrium immunkölcsönhatásait, és megakadályozhatják a kóros elváltozások sorozatát, rendkívüli fontossággal bírnak, különösen az IVF programban részt vevő házaspárok számára.
Ezenkívül az ovuláció stimulálására szolgáló rendszerek nagy dózisú hormonális gyógyszerek alkalmazásával a nő immunológiai, hormonális, hemosztatikus állapotának megváltozásához vezetnek, ami időben történő diagnózist és korrekciót igényel. Az IVF utáni terhesség kezelése csúcstechnológiás orvosi ellátást igényel a terhesség legkorábbi szakaszától a spontán abortusz megelőzése érdekében.
A fentiekre tekintettel a tanulmány célja egy algoritmus kidolgozása volt az IVF előtt visszatérő vetélésben, auto- és alloimmun patológiás nők diagnosztizálására és terápiájára.
Anyagok és kutatási módszerek
60 olyan házaspárt vizsgáltunk, kezeltünk és prospektíven figyeltünk meg, akiknek a kórtörténetében két vagy több terhességi veszteség szerepel, és IVF-et terveztek. Minden beteg átfogó klinikai és laboratóriumi vizsgálaton esett át a terhességen kívül az Orosz Orvostudományi Akadémia Szülészeti, Nőgyógyászati és Perinatológiai Tudományos Központja ONB-sémája szerint, beleértve: funkcionális diagnosztikai teszteket, hormonális állapotvizsgálatokat, lupus antikoaguláns meghatározását, humán koriongonadotropin elleni antitestek, biokémiai paraméterek, bakteriológiai, virológiai vizsgálat, ultrahang és röntgen diagnosztika, genetikai tanácsadás, férj spermogram vizsgálata.
A fentieken kívül a következőket hajtották végre:
A fő hisztokompatibilitási komplex (HLA) I. és II. osztályába tartozó antigéntermékek vizsgálata házaspárokban - A, B, C, DR, DQa, DQb lókuszokban;
b 2 -glikoprotein, annexin, protrombin, foszfatidil-kolin, foszfatidil-szerin, foszfatidil-inozit, szfingomielin, kardiolipin elleni antitestek keringésének vizsgálata;
Természetes antikoagulánsok - antitrombin III, C és S fehérjék - aktivitásának meghatározása azonosított autoimmun patológiás nőknél;
Hemostaziológiai kontroll az intravaszkuláris trombusképződés markereinek (D-dimerek, fibrinmonomerek oldható komplexei) vizsgálatával a terhesség előtt és idővel a humán koriongonadotropin b-alegységének első pozitív mutatóinak megérkezése után.
Kutatási eredmények és megbeszélés
Részletes vizsgálat után 60 diagnosztizált immunológiai rendellenességgel rendelkező házaspárt választottunk a megfigyelési csoportba, ebből 32 fő alloimmun patológiás és 28 fő autoimmun betegségben szenvedett. A nők átlagéletkora 32,0±4,2 év volt, a nők 66,7%-a 30 év feletti volt.
A szomatikus morbiditás elemzése után a nők e csoportjában magas, 4,5±0,21-es fertőzőképességi indexet állapítottunk meg. A szív- és érrendszeri betegségeket túlnyomórészt a hipotóniás vagy hipertóniás típusú vegetatív-vaszkuláris dystonia jelentette, egy betegnél I. fokozatú mitrális billentyű prolapsus volt regurgitáció nélkül; légúti betegségek krónikus hörghurutként nyilvánultak meg; a gyomorhurut, gyomorfekély és epeúti diszkinézia a gyomor-bél traktus betegségei között volt megfigyelhető. Az ebbe a csoportba tartozó betegek 25%-ának volt húgyúti betegsége krónikus pyelonephritis és cystitis formájában. A pajzsmirigy patológiáját 5 (8,3%) nő esetében autoimmun pajzsmirigygyulladás jellemezte, szubklinikai hypothyreosis tüneteivel.
A nőgyógyászati patológia szerkezetének elemzése során kiderült, hogy a nők 30%-ának volt a kórtörténetében méhnyak ectopia; a nemi szervek gyulladásos betegségei 46,7%-ban krónikus endometritis és krónikus salpingoophoritis voltak; Oligomenorrhoeát a nők 10%-ánál figyeltek meg.
Nőgyógyászati műtétet minden betegnél végeztek laparoszkópos hozzáféréssel: myomectomia 3 betegnél (5,0%); az intrauterin septum kimetszése 1 (1,7%) betegnél; tubectomia petevezetékes terhesség miatt 6-ban (10%); a petefészek reszekciója endometrioid ciszta jelenléte miatt 1 esetben (1,7%); mindkét petefészek cauterizációja 1 (1,7%), külső nemi endometriózis gócainak koagulációja 4 (6,7%) nőnél.
Hormonális rendellenességek hiperandrogenizmus formájában a nők 20% -ánál fordultak elő, és a korábbi terhesség elvesztése a glükokortikoidok szedése közben következett be; hiperprolaktinémia a nők 8,3%-ánál, luteális fázis hiánya 40%-nál volt megfigyelhető.
A vizsgált nőknél a terhességek túlnyomó többsége (az összes terhesség 179-84%-a) az első trimeszterben spontán megszakadt.
Ezek közül a vetéléseket leggyakrabban a terhesség 5-8 hetében figyelik meg - 50,7%. A 9-12 hetes vetélések valamivel ritkábban fordultak elő - 21,6%, anembryonia - az összes terhesség 11,7%-ában.
A vizsgálat során 32 olyan házaspárt választottak ki, akiknél alloimmun tényező a szokásos terhességi veszteség – három vagy több HLA-rendszer közös alléljával.
A HLA I. osztályú rendszer antigénjeinek elemzésekor a B35 antigén előfordulási gyakoriságának statisztikailag szignifikáns növekedését figyelték meg a visszatérő vetélést szenvedő férfiak körében - a gén gyakorisága 0,162 volt, szemben a populáció 0,071-ével (p<0,05).
A visszatérő vetélésben szenvedő csoportban az A11 antigént szignifikánsan ritkábban találták meg mind a férfiaknál, mind a nőknél, mint a populációban (p<0,05 и p<0,01 сооответственно), у женщин достоверно реже отмечены антигены В7 (p<0,05), Cw4 (p<0,01), у мужчин – Cw2 (p<0,05).
A HLA I. osztályú kompatibilitással rendelkező párokban az A lókusz antigénjei sokkal gyakoribbak – 87,7%. A történelem során azonban a legtöbb terhességi veszteség azoknál a pároknál fordult elő, akik kompatibilisek a HLA II. osztályú rendszer három alléljával. Így a párok 50%-ának volt közös allélja mindhárom lókuszban. A fennmaradó 16 pár közül, amelyek két lókuszban osztoznak az allélokon, a DQA1 és DQB1 kombináció dominált.
A gyakori allélok lokuszban való előfordulását tekintve a DQA1 lókusz dominál - 81,3%. A 0201 allélok DQA1 és DQB1 lókuszokban való előfordulásának kvantitatív elemzése során a 0201 allél túlsúlyát férfiaknál a DQA1 lókusznál az esetek 28,1%-ában, a DQB1 lókusznál pedig az esetek 31,3%-ában észlelték. A nőknél a 0201 allél előfordulása szignifikánsan alacsonyabb volt – 9,4 és 12,5%. Szignifikánsan szignifikáns növekedést tapasztaltunk a 0201 allél előfordulási gyakoriságában a DQA1 lókuszban férfiakban a populáció adataihoz képest (p<0,001).
Az azonosított HLA-kompatibilitású párok prekoncepciós felkészítésen estek át, amely aktív és passzív immunizálásból állt. Az aktív immunizáláshoz limfocitoimmunterápiát (LIT) alkalmaztak donorsejtekkel a menstruációs ciklus 5–8. napján, 1 hónappal a tervezett IVF előtt. 4 hét elteltével a LIT-t megismételték az IVF hátterében. Az embriótranszfer után intravénás csepegtető immunglobulin terápiát írtak elő passzív immunizálás formájában 10% immunglobulin készítményekkel - Gamimun-N 50 ml, Gamunex 50 ml - vagy 5% intraglobin készítmény 50 ml. Terhesség bekövetkeztekor a hemosztatikus monitorozást a legkorábbi stádiumban végeztük intravaszkuláris koagulációs markerek meghatározásával, és szükség esetén kis molekulatömegű heparinokkal történő korrekcióval. Immunmodulációs célokra a didrogeszteront a terhesség korai szakaszától 30 mg/nap dózisban alkalmazták a magzati kilökődési reakciók elnyomására a terhesség 16. hétéig. A LIT eljárásokat 4 hetes időközönként megismételtük a terhesség 16. hetéig.
28 autoimmun patológiás nőnél a terhességre való felkészítés része volt a kismedencei szervek krónikus gyulladásos folyamatainak azonosítása és kötelező kezelése az autoimmunizáció súlyosságának csökkentése érdekében, majd antikoaguláns, thrombocyta-aggregáció és kortikoszteroid terápia felírása.
Az autoimmun patológia markerei közül a leginformatívabbak az antifoszfolipid antitestek kofaktorai – b 2 -glikoprotein, annexin, protrombin – elleni autoantitestek voltak, ami megfelel az irodalmi adatoknak. Így már a terhességen kívül a nők 64,3%-ánál észleltek vérzéscsillapító rendszeri rendellenességeket, amelyek a thromboelastográfia szerint hiperkoagulációval, az intravaszkuláris trombusképződés markereinek jelenlétével (D-dimer, oldható fibrinmonomer komplexek) nyilvánultak meg, és pozitív eredményt mutattak. lupus antikoaguláns tesztet csak a nők 21,4%-ánál figyeltek meg. Az antikardiolipin autoantitestek kimutatására szolgáló teszt érzékenyebb volt - az esetek 75%-ában közepes és magas titerben mutatták ki őket. Az egyes kofaktorok elleni autoantitestek jelenlétére vonatkozó tesztek a nők 89,3%-ánál pozitívnak bizonyultak, ami valószínűleg a terhesség legkorábbi szakaszától fogva az autoimmun folyamat megvalósítására való hajlamra utal.
Az IVF-re való azonnali felkészítés programja terápiás plazmaferézist (PA) tartalmazott azon nők 25%-ánál, akiknél az autoimmun folyamat kifejezett aktivitása volt, ami a véralvadási tesztek és a hemostasiogram paramétereinek változásában nyilvánult meg. A terápiás PA-t 1 hónappal az IVF előtt írták fel, ami lehetővé tette az immunkomplexek és autoantitestek eltávolítását a keringő vérből, valamint az endogén és gyógyászati anyagokkal szembeni érzékenység növelését. Más esetekben az IVF programban kis molekulatömegű heparint írtak fel embriótranszfer után (nadroparin, enoxaparin, dalteparin), a terhesség utáni kezelés folytatása mellett. Az immunmodulációhoz alacsony dózisú kortikoszteroidokat (2-4 mg metipred) és didrogeszteront (30 mg/nap) írtak elő. Három betegnél volt szükség ismételt terápiás PA-ra a terhesség első trimeszterében.
Általánosságban elmondható, hogy az IVF után 12 (37,5%) alloimmun patológiás és 11 (39,3%) autoimmun betegségben szenvedő nőnél következett be terhesség.
A terhesség első trimeszterében minden nő esetében gondos hemosztatikus monitorozást, majd az indikátorok korrekcióját foglalta magában; az autoimmun betegségekben szenvedő csoportban az esetek 90,9% -ában, az alloimmun patológiás csoportban - 25% -ban alacsony molekulatömegű heparint alkalmaztak.
Immunmoduláló célokra a didrogeszteront minden betegnél 30 mg/nap dózisban alkalmazták. Az elmúlt években igazolták ennek a gyógyszernek az immunkorrekciós hatását a progeszteron receptorok aktiválása révén az immunkompetens endometrium sejteken. A következő láncszem a protektív immunmoduláció a progeszteron által kiváltott blokkoló faktor hatására, amely a természetes ölősejtek és a limfokin-aktivált sejtek aktivitásának csökkentésében, a szabályozó citokinek (interleukinek 4, 10) szintézisének indukálásában, az embrió folyamatainak elnyomásában áll. elutasítása és a normál trofoblaszt invázió biztosítása. Ezzel szemben a gyulladásos és thrombophiliás reakciókat kiváltó citokinek (tumornekrózis faktorok, interleukin 1, g-interferon stb.) termelődése visszaszorul.
A Metypredet (metilprednizolont) autoimmun folyamatban szenvedő betegeknek napi 2-6 mg dózisban írták fel, immunglobulin intravénás csepegtető adagolásával kombinálva az első trimeszterben, legalább egyszer 5 g-os dózisban (50 ml 10%-os gamimun). oldat vagy 100 ml 5%-os intraglobin oldat) . Az alloimmun betegségekben szenvedő nők folytatták a LIT- és immunglobulin-terápiát.
Az immunrendszeri zavarokkal küzdő IVF után 23 nő közül 21 (91,3%) hosszabbította meg a terhességet a második trimeszterig. Két megfigyelésben anembryoniát figyeltek meg alloimmun betegségekben szenvedő nőknél. Az adatok elemzése során kiderült, hogy egy esetben a páciens férjének 0201-es allélja volt a DQA1 lókuszban, amit sok szerző az anembryonia kialakulásának kedvezőtlen prognosztikai jelének tart. Az autoimmun patológiás csoportban az első trimeszterben nem volt terhességi veszteség.
Így az immunpatológiai folyamatok terhességen kívüli természetének tanulmányozása széles távlatokat nyit az egyéni kezelési rendek kiválasztásában az IVF előtt, ami nyilvánvalóan növeli a terhesség kialakulását és meghosszabbítását célzó intézkedések hatékonyságát.
Lehetséges szövődmények. Többszörös terhesség
A terhesség valószínűségének növelése a módszer segítségével ECO, általában több embriót (legfeljebb három) helyeznek át egy nő méhébe. Néha ez többes terhesség kialakulásához vezethet.
Ha kettőnél több magzat fejlődik ki a méhben, akkor egy ilyen terhesség kihordása meglehetősen nehéz lehet. Léteznek módszerek az egyik embrió fejlődésének megállítására anélkül, hogy a többit érintené. Ezt a műveletet magzati redukciónak nevezik, és ultrahangos irányítás mellett hajtják végre. Általában két embrió marad. A terhesség sikeres kihordásának valószínűsége az embriócsökkentés után nagyobb, mintha hármasikret hagynánk.
Méhen kívüli terhesség
Ha az embriók méhüregbe történő átvitele után gyengeség, szédülés, terhesség korai jelei, homályos vagy éles fájdalom jelentkezik az alhasban stb., akkor valószínűleg méhen kívüli terhességről van szó, amelyben a magzat nem fejlődik ki a méhben. , hanem például a petevezetékben. Ebben az esetben azonnal forduljon orvoshoz, mivel ez az állapot életveszélyes, mivel a csőszakadás súlyos vérzést okozhat. 4 hetes vagy annál hosszabb méhen kívüli terhesség esetén a méh üregében lévő magzati petesejt ultrahangon nem látható, de a terhességi teszt (hCG-re) pozitív. A méhen kívüli terhességet általában kíméletes laparoszkópos műtéttel kezelik. Ha a fenti tünetek bármelyike jelentkezik, azonnal forduljon orvosához. A prospektus utolsó oldalára írja fel a klinika telefonszámát és orvosa nevét. Tudja meg a segélyhívó telefonszámokat is. Az orvos összes ajánlásának betartásával csökkenti a szövődmények kockázatát és növeli a boldog fogantatás esélyét.
Petefészek hiperstimulációs szindróma
Bár az asszisztált reprodukciós technológia célja az egészséges gyermek, az asszisztált reprodukciós technológiával járó terhességek szülészeti kimenetelét bonyolítja a petefészek hiperstimulációs szindróma (OHSS), amely továbbra is kevéssé ismert.
Az OHSS a petefészek szuperfiziológiás stimulációjának szövődménye, amelyet a petesejtek és az embriók számának növelése érdekében végeznek az asszisztált reprodukciós technológiában. Egy közelmúltbeli, 10 éves izraeli adatok elemzése az OHSS előfordulási gyakoriságának növekedését mutatta ki, és ennek a szövődménynek a „járvány” létezését feltételezte. Riasztó, hogy ugyanezek a szerzők a káros kimenetelek magas előfordulásáról számoltak be 104 súlyos vagy kritikus OHSS-sel szövődött in vitro terhesség között Izraelben 1987 januárja és 1996 decembere között. Vetélés, koraszülés, alacsony születési súly, terhességi cukorbetegség és magas vérnyomás, Különböző országokból származó jelentések szerint az ilyen terhességeknél magasabb volt a placenta-leválás.
Ebben a cikkben áttekintjük az OHSS és a nemkívánatos terhességi kimenetelek közötti összefüggés várható alapjait.
A kedvezőtlen szülészeti eredménnyel járó asszociációs mechanizmusok Szuperfiziológiás petefészek-stimuláció
Számos tényező (a pár klinikai jellemzői, a nő életkora, a terhesség kimutatásának pontossága) nehezíti a különböző vizsgálatok során kapott adatok értelmezését a vetélés relatív kockázatáról a spontán és az asszisztált fogantatás között. Az asszisztált reprodukciós technológiák még nyilvánvaló OHSS hiányában is a petefészkek szuperfiziológiás stimulációjával járnak, ami magasabb ösztradiolszintet eredményez, mint a „természetes” ciklus. Az OHSS nagyobb valószínűséggel fordul elő, ha a petefészek stimulációra maximálisan reagál. Asch és mtsai. azt találták, hogy az ösztradiol csúcskoncentrációja és a tojásszám csekély hatást gyakorol a vetélések arányára. Ez arra utal, hogy a petefészek válaszának mértéke önmagában nem növeli a vetélés kockázatát OHSS-szövődmények esetén a szövődménymentes in vitro fertilis ciklusokhoz képest.
Kórélettan
A súlyos OHSS patofiziológiája magában foglalja a mélyreható szisztémás vaszkuláris diszfunkciót, megnövekedett vaszkuláris permeabilitással, folyadékszivárgással a harmadik térbe és intravaszkuláris dehidrációval. Kritikus esetekben thromboembolia, veseelégtelenség és felnőttkori légzési distressz szindróma lehetséges hipotenzióval, hipoxémiával és elektrolit-egyensúlyzavarral.
Ezek a jelenségek negatív hatással lehetnek a korai terhességre. A szisztémás koagulopátia, amelyet súlyos OHSS-es esetekben észleltek, befolyásolhatja a beültetési folyamatot.
A károsodott beültetés vetéléshez vezethet, vagy ezt követően preeclampsiában vagy placenta elégtelenségben nyilvánulhat meg. Egyre világosabbá válik az immunrendszer és az immunológiai mediátorok szerepe az OHSS-ben. A súlyos OHSS a proinflammatorikus citokinek és a vaszkuláris endothel növekedési faktor magas szintjével jár a szérumban és az asciticus folyadékban.
Feltételezték, hogy a beültetés során túlnyomórészt gyulladást elősegítő Th-1 válasz spontán vetélésekkel jár. A súlyos OHSS olyan állapotként írható le, amelynek legvalószínűbb eredménye a vetélés fokozott kockázata.
Tipikus interakciók. Az OHSS és a kedvezőtlen terhességi kimenetel közötti kapcsolatot közös kockázati tényezőik magyarázzák. A policisztás petefészek szindrómában szenvedő betegek nagyobb valószínűséggel reagálnak túl a gonadotrop stimulációra, ami fokozott kockázatot jelent az OHSS kialakulására. Szintén hatástalan lehet náluk az utólagos asszisztált reproduktív kezelés gonadotropin-releasing hormon agonisták (AGTRH) alkalmazása nélkül. A policisztás petefészek szindrómában szenvedő nőknél a vetélés fokozott kockázatát a luteinizáló hormon túlzott szekréciójával hozták összefüggésbe, amely az AGTRH-val korrigálható az agyalapi mirigy elnyomására, nem pedig az OHSS fokozott kockázatával.
Egy összehasonlító vizsgálatot végeztek 332 ciklusból normál petefészek-morfológiájú nőknél és 97 ciklusból nőknél. AGTRH-t kaptak a terápia részeként, és policisztás petefészkekkel rendelkeznek klinikai megnyilvánulások nélkül, de ultrahanggal megerősítették. A megváltozott petefészek morfológiájú csoportban az OHSS gyakrabban alakult ki (10,3 vs 0,3%), de nem volt különbség a vetélések kockázatában (6,9 vs 11,1%).
Lehetséges, hogy egyes nők genetikailag meghatározott hajlamot mutatnak az OHSS kialakulására és a rossz szülészeti eredményekre a citokinprofil eltérései miatt, ami a citokintermelésben, valamint a nem gyulladásos és gyulladásos citokinek egyensúlyának megváltozásához vezet. Génpolimorfizmust írtak le a TNF-a génre vonatkozóan, amelynek néhány allélja ennek a proinflammatorikus citokinnek a fokozott expressziójához kapcsolódik. A TNF 1 allél túlsúlya magyarázhatja a TNF-a mRNS fokozott expresszióját preeclampsiában. A TNF-a szintje a szérumban és az asciticus folyadékban nőtt az OHSS-ben szenvedő nőknél, de a TNF-a gén polimorfizmusának prevalenciáját az OHSS-ben szenvedő nők körében nem vizsgálták.
A luteális fázis második felében kezdődő OHSS-t („késői” OHSS) a humán koriongonadotropin felszabadulása jellemzi a beültetett embrióból, és a fogantatáshoz kapcsolódik. A humán chorion gonadotropin szintje többes terhességben magasabb, mint az egyszeri terhességben, ami megmagyarázza a késői OHSS előfordulási gyakoriságát, mint a korai OHSS-t vagy annak hiányát az ilyen nőkben. A többszörös terhesség gyakoribb előfordulása egy másik ok arra, hogy OHSS formájában jelentkező szövődmény esetén kedvezőtlen kimenetelre számítsunk, mint annak hiányában. A többes terhességnél a legnagyobb a koraszülés és az alacsony születési súly kockázata az egyedülállóknál.
Terhesség kimenetelének vizsgálata. Nyilvánvaló, hogy elméleti alapja van az OHSS és a kedvezőtlen terhességi kimenetel közötti összefüggésnek. A témával kapcsolatos szakirodalom azonban korlátozott, és nem lehet egyértelmű következtetést levonni. Abramov et al. , a másik kettő az OHSS által bonyolított in vitro fertilis ciklusok során előforduló vetélések gyakoriságának tanulmányozásával foglalkozik. És csak az egyikük hasonlítja össze a ciklusokat OHSS-sel és anélkül (kontrollcsoport). Chen et al. nem talált szignifikáns különbséget a vetélések arányában az OHSS-sel és anélkül végzett ciklusok között (4/15 (26,7%) vs. 19/110 (17,2%)). MacDougall et al. 14 (28,6%) OHSS által szövődött in vitro terhességből 4 vetélésről számolt be. Az OHSS nélküli egyidős terhességről csak Caspi és munkatársai szereztek adatokat. akik a vetélések magasabb arányát észlelték az OHSS-ben szenvedő HHT ciklusokban (10/29 (34,5%) vs. 20/114 (17,5%)). Két másik tanulmány a vetélés előfordulási gyakoriságát vizsgálta OHSS-ben szenvedő betegeknél gonadotropin-terápia után. Schenker és Weinstein 40%-os vetélési arányról számolt be (10-ből 4), Rabau et al. – körülbelül 25% (4-ből 1). Figyelemre méltó, hogy ezeknek a tanulmányoknak a többsége nem jelenti a vetélések arányát elsődleges eredménymérőként. Kettő kivételével ezek a vizsgálatok rosszul kontrolláltak, és Abramov et al. kis számú betegről szerzett adatokat. 1995. január 1. és 1998. szeptember 30. között 41, közepesen súlyos vagy súlyos OHSS-sel szövődött terhességet hajtott végre a Bristoli Egyetem In vitro megtermékenyítési szolgálata. A vetélések aránya nem különbözött szignifikánsan ebben a csoportban és egy 501 asszisztált terhességből álló kontrollcsoport között 40 év alatti nőknél, akiknél nem volt hidrosalping vagy OHSS. A spontán magzati halálozás aránya nem különbözött szignifikánsan a két csoport között (1. táblázat).
Abramov és munkatársai kivételével egyetlen tanulmány sem található az irodalomban, amely leírná az OHSS által komplikált terhességek in vitro perinatális kimenetelét. Saját központunkban 36 OHSS-sel szövődött terhesség és 546 szövődménymentes terhesség (40 év alatti nők) szülését vizsgáltuk egyszerre. Az OHSS-ben szenvedő csoportban gyakoribb volt a többes terhesség és a koraszülés, de a különbségek statisztikailag nem voltak szignifikánsak (2. táblázat).
Az OHSS-s anyák újszülöttjeinek medián súlya szignifikánsan alacsonyabb volt a kontrollokhoz képest, de az egyedülálló terhességek esetében a különbség nem volt szignifikáns.
Bár Abramov et al. összefüggést mutatnak az OHSS és a vetélés között, nem hasonlították össze az OHSS nélküli terhességek vetélési arányára vonatkozó izraeli adatokkal. Betegeiknél a vetélés kockázata magasabb, mint az elmúlt évtized különböző időszakaiban különböző országokból származó általános in vitro populációhoz képest. Azonban olyan tényezők, mint a meglévő elfogultság, a beteg életkora, a terhesség diagnosztizálásának kritériumai, a policisztás petefészek szindróma jelenléte és a többes terhesség esetei megnehezítik az adatok értékelését az egyenértékű kontrollcsoport hiánya miatt. Az egyetlen olyan vizsgálat, amely in vitro terhességeket vizsgált, és amelybe egy kontrollcsoport is beletartozott, nem talált szignifikáns különbséget a vetélések arányában az OHSS-es és az anélküli ciklusok között, ami összhangban van adatainkkal. Ellenőrzött vizsgálatunk és Abramov et al. tanulmánya közötti különbségek. összefüggésbe hozható a többes terhességek gyakoribb előfordulásával vagy esetleg az OHSS súlyosabb súlyosságával az Abramov-csoportban. Végül, az alacsony születési súly és a koraszülés gyakoribb előfordulása az OHSS-ben szenvedő nőknél a vizsgálatunkban annak tudható be, hogy ebben a csoportban magas a többes terhességek száma.
Következtetés
Megválaszolatlan marad a kérdés, hogy az OHSS-nek van-e káros hatása a fejlődő terhességre. Ha kimutatható, hogy az OHSS hátrányosan befolyásolja az asszisztált reprodukciós technológiás terhességek kimenetelét, annak nemcsak a szülészetre lesz kihatása, hanem jelentősen befolyásolja az asszisztált reprodukciós gyakorlatokban alkalmazott petefészek-hiperstimulációs sémákat is. A folyamat fiziológiásabbá tétele és a szuprafiziológiás petefészek-stimuláció azonnali és hosszú távú következményeinek kockázatának csökkentése érdekében „enyhébb” stimuláló kezelést végeztünk, amely nem eredményezett maximális petefészek választ. Ha a vizsgálatok azt mutatják, hogy az OHSS által szövődött terhességek szülészeti kimenetele rosszabb, mint az OHSS nélküli terhességeké, ez érvet jelentene a maximális petefészek-stimuláció elkerülése mellett. A mai napig az egyetlen ellenőrzött adat nem támaszt alá összefüggést az OHSS és a rossz szülészeti eredmény között. A probléma azonban továbbra is megoldatlan, és olyan vizsgálatokra van szükség, amelyek összehasonlítják az asszisztált reprodukciós technológiák alkalmazásával bekövetkezett és az OHSS által komplikált terhességeket egy egyenértékű kontrollcsoporttal.
Terhesség– új egyedek fogantatása által okozott biológiai állapot.
Meddőség– a fogamzóképes korú személyek nem képesek utódokat szaporítani. A házasság meddőnek minősül, ha egy nő a fogamzásgátló eszközök és módszerek alkalmazása nélkül történő rendszeres szexuális kapcsolatát követő egy éven belül nem esik teherbe.
A meddőség meglehetősen tág orvosi, pszichoszociális és etikai fogalom. Ha ez megtörténik, orvoshoz kell mennie, és meg kell határoznia a terhesség hiányának okát.
A női meddőség okai nagyon változatosak, három fő tényező van:
Méh;
Tubal-peritonealis (a petevezetékek elzáródása, összenövések);
Neuro-endokrin (policisztás petefészek szindrómával (PCOS) vagy hiperprolaktinémiával kapcsolatos ovulációs rendellenességek).
Immunológiai rendellenességek is megfigyelhetők, például antisperma antitestek jelenléte és ismeretlen eredetű meddőség, amelynek nincs látható oka.
A női meddőség ezen formáinak kezelésének első szakasza terápiás vagy műtéti korrekció. Ha ez nem hoz eredményt, az IVF és PE program megoldást jelenthet a problémára.
A bonyolultabb feltételek a következők:
Saját peték hiánya a petefészekben;
Az ivarmirigyek diszgenezise, például Shereshevsky-Turner szindrómában;
Kemoterápia rák kezelésére;
a petefészkek műtéti eltávolítása;
Genetikai rendellenességek.
A férfi meddőség okai között a következők szerepelnek:
A nemi szervek fejlődésének veleszületett rendellenességei (kriptorchidizmus stb.);
Káros környezeti tényezők hatása;
Allergia és az immunrendszer gyengülése;
gyógyszerek (beleértve az anabolikus szteroidokat és a kábítószereket) ellenőrizetlen használata;
Szexuális úton terjedő fertőzések;
Stressz tényezők;
Mozgásszegény életmód;
Alkoholizmus és dohányzás;
A nemi szervek sérülései;
Különféle hormonális rendellenességek, például alacsony FSH-szint, mellékvese hipo- és hiperplázia, cukorbetegség, pajzsmirigybetegségek stb.;
A spermatogenezis hiánya a magas FSH-szint hátterében;
Veleszületett genetikai rendellenességek, például Klinefelter-szindróma (XXY kariotípus);
Kemoterápia rák kezelésére.
VRT- asszisztált reprodukciós technológiák. Az asszisztált reprodukciós technológiák a következőket jelentik:
Méhen belüli megtermékenyítés a férj spermájával
In vitro megtermékenyítés
In vitro megtermékenyítés mikromanipulációval ICSI (ICSI)
A donor sperma alkalmazása az ART-ban.
Az ART főbb módszereinek és programjainak nevének rövidítéseinek listája:
ECO- in vitro megtermékenyítés
PE- embriók átvitele a méh üregébe
AJÁNDÉK- ivarsejtek átvitele a petevezetékbe
ZIFT- zigóták átvitele a petevezetékbe
AI- mesterséges megtermékenyítés
IISD- mesterséges megtermékenyítés donor spermával
IISM- mesterséges megtermékenyítés a férj spermájával
ICSI- spermium injekció a petesejtek citoplazmájába
ISO- szuperovuláció kiváltása
MESA- spermium leszívása a mellékhereből
PEZA- a spermiumok perkután aspirációja a mellékhereből
TÉZIS- spermium leszívása a hereszövetből
TESE- spermium kivonása a hereszövetből
EIFT- embriók átvitele a petevezetékbe.
Megtermékenyítés a férj (donor) spermájával - ISM (ISD)). A mesterséges megtermékenyítés a meddőség kezelésének legrégebbi módszere. Olyan freskók érkeztek hozzánk, amelyek egy mag behurcolásának folyamatát ábrázolják. A mesterséges megtermékenyítést endokrin, immunológiai és férfi meddőség egyes esetekben, nyitott petevezeték jelenlétében végezzük. A terhesség szempontjából kedvező napon a nő spermáját a férje vagy donora juttatja a méh üregébe.
A spermiumok közvetlenül a méh üregébe történő bejuttatása magában foglalja a méhnyak mesterséges átjutását olyan spermiumokkal, amelyek a méhnyak meddősége miatt elpusztulhatnak a természetes teherbe esés során. Az eljárás végrehajtásának előfeltétele legalább egy nyitott petevezeték megléte.
Megtermékenyítés (in vitro latinul) in vitro - Az eljárás lényege, hogy egy nő petefészkéből érett petesejtet nyerünk, férje spermájával (vagy mindkét házastárs kérésére donor spermával) megtermékenyítjük, a keletkező embriókat 48-72 órán át inkubátorban növesztjük, ill. az embriókat a beteg méhébe átültetni (újraültetni).
Az IVF eljárás a következő szakaszokból áll:
A betegek kiválasztása és vizsgálata;
Szuperovuláció indukálása, beleértve a follikulogenezis és az endometrium fejlődésének nyomon követését (a tüszők érésének és az endometrium növekedésének nyomon követése ultrahanggal). A stimuláció célja, hogy mindkét petefészekben nagyszámú érett petesejtet nyerjünk a terhesség esélyének növelése érdekében. Az SSO-t különféle modern hormonális gyógyszerekkel végzik, amelyeket minden házaspár számára egyedileg választanak ki, előzetes vizsgálat eredményei alapján;
A petefészek tüszőinek punkciója (a tüszők szúrását intravénás érzéstelenítésben és ultrahangos kontroll alatt végezzük a hüvely oldalsó fornixén keresztül). Ezen a napon a páciens férje spermát adományoz, amely speciális kezelésen esik át;
Petesejtek megtermékenyítése és embriók in vitro tenyésztése;
Az embriók átvitele a méh üregébe. Az embriótranszfer speciális katéterrel történik a méhnyakon keresztül a follikuláris punkciót követő 2., 3. vagy 5. napon. Általános szabály, hogy ehhez nincs szükség különleges felkészülésre. Általában 2 embriót helyeznek át. Ha a betegnek sok próbálkozása volt, vagy az embriók minősége rossz, 2-nél több embrió áthelyezése lehetséges. A fennmaradó jó minőségű embriókat kriofagyasztják. Ha a kísérlet sikertelen, ezeket az embriókat a következő átvitelhez használják fel;
Támogatja a stimulált menstruációs ciklus luteális fázisát. Az embriótranszfer után 2 hétig a terhességet támogató gyógyszereket írnak fel;
A korai terhesség diagnózisa. 2 hét elteltével a nő vért ad βhCG-hez, hogy megállapítsa, terhes-e. A vizsgálat eredményeitől függően meghatározzák a beteg kezelésének további taktikáját.
Az IVF a természetes menstruációs ciklusban is lehetséges, szuperovuláció kiváltása nélkül.
Az IVF indikációi:
Meddőség, amely nem kezelhető vagy nagyobb valószínűséggel legyőzhető IVF-el, mint más módszerekkel. Ellenjavallat hiányában IVF végezhető házaspár (hajadon nő) kérésére a meddőség bármely formája miatt.
Az IVF ellenjavallatai:
Szomatikus és mentális betegségek, amelyek ellenjavallatok a terhesség és a szülés során;
a méh üregének veleszületett rendellenességei vagy szerzett deformációi, amelyekben az embriók beültetése vagy terhesség lehetetlen;
petefészek daganatok;
a méh jóindulatú daganatai, amelyek műtéti kezelést igényelnek;
Bármilyen lokalizációjú akut gyulladásos betegségek;
Bármilyen helyről származó rosszindulatú daganatok, beleértve az anamnézist is.
A meddő házasság kompetens és hatékony kezelése csak az urológusok, a nőgyógyászok és az IVF-specialisták egyértelmű interakciójával lehetséges. Kötelező teljes körűen tájékoztatni a pácienst a termékenység helyreállításának minden lehetséges módszeréről, feltüntetve a sikeres intézkedések százalékos arányát és a szövődmények kockázatát saját maga és felesége számára.
A spermiumok befecskendezése a tojás citoplazmájába (ICSI). Az ICSI programot a férfi meddőség súlyos formáira, valamint bizonyos esetekben a házaspárok reproduktív egészségének egyéni jellemzőire vonatkozóan hajtják végre. A feleségtől kapott petesejtek megtermékenyítését úgy érik el, hogy spermát juttatnak be a tojás citoplazmájába.
Ha nem lehet megtermékenyíteni a petesejtet IVF-el, akkor az ICSI mikromanipulációs módszert alkalmazzák.
Az Intracytoplasmic Sperm Injection (ICSI) technika lényege, hogy mikroszkóp alatt, finom mikrosebészeti eljárással egyetlen spermiumot injektálnak az érett tojás citoplazmájába. Ezzel áthidaljuk a természetes megtermékenyítés ellehetetlenülésének akadályát, amely általában a gyermektelenség oka a férfi meddőség súlyos formáiban szenvedő pároknál. Az ICSI használatára vonatkozó javallatok a közelmúltban bővültek. Ezt a módszert az előző IVF-programban megtermékenyítés hiányában is alkalmazzák, kis számú petesejtekkel, vastag petehéjjal stb.
Az ICSI-t a következő férfi patológiák kezelésére használják:
nehéz oligozoospermia(a spermium koncentrációja az ejakulátumban kevesebb, mint 10 millió/ml, azaz olyan alacsony, hogy gyakorlatilag kizárja a tojás természetes megtermékenyülését);
asthenozoospermia minden formában oligozoospermia(az aktívan mozgó spermiumok kevesebb mint 30%-a, ha az ejakulátum teljes spermiumkoncentrációja kevesebb, mint 20 millió/ml);
azoospermia(érett spermium hiánya az ejakulátumban) különböző eredetű, ha a here vagy mellékhere szúrása során mozgékony spermiumokat észlelnek.
Az ICSI technika asszisztált reprodukciós technológiai programokban való alkalmazásában szerzett világtapasztalat azt mutatja, hogy ez az eljárás nem befolyásolja a született gyermekek egészségét. Azonban szem előtt kell tartania, hogy ha a férfi meddőség okai genetikai rendellenességekhez kapcsolódnak, akkor ezeket a rendellenességeket, ha ICSI-t alkalmaznak, fiai öröklik a spermium kromoszómáival együtt. A spermatogenezis súlyos formáiban szenvedő férfiak előzetes vizsgálata segít elkerülni a veleszületett patológiás utódok születését ICIS - intracitoplazmatikus spermium injekció.
Tojás adományozás. A petesejt-adományozási program lehetővé teszi azoknak a nőknek, akiknek nincs petesejt a petefészkükben, valamint akiknél magas a magzati örökletes betegségek kockázata, hogy egészséges gyermeket hordozzanak és szüljenek. Ilyen esetekben a petéket egészséges női donortól nyerik.
Béranyaság. A „béranyaság” program azoknak a nőknek ad lehetőséget a gyermekvállalásra, akiknek különböző okok miatt eltávolították a méhüket, vagy akiknek súlyos betegségek miatt nem szabad terhességet vállalniuk. Ezekben az esetekben egy terméketlen pár petesejtjeit és spermáját használják fel. Az így kapott embriókat egy egészséges nő – egy „helyettes anya” – méhüregébe helyezik át.
A várandósság kezdete és a magzat terhessége időnként háttérbe szorul a béranya anyától született gyermek anyakönyvezésével kapcsolatos jogi problémák tömkelege miatt.
Nem minden országban a biológiai szülőknek van joga a gyermekhez. A „béremanyák” pedig, ha a családot nem védik a törvények, folyamodhatnak az úgynevezett „helyettesítő” ütőhöz. A gyermek születése után nem hajlandók átadni a szüleinek, kényszerítve őt, hogy fizessen minden költséget a saját és a tartásáért stb.
Követelmények béranyákkal szemben:
Életkor 20-35 év;
saját egészséges gyermeke;
Mentális és szomatikus egészség.
Az embriók fagyasztása. Ez a program jól fejlődő embriók tárolására és későbbi felhasználására készült az IVF (in vitro fertilization) programban. Ha szükséges, ezeket az embriókat felolvasztják és a teljes IVF ciklus megismétlése nélkül a méh üregébe helyezik.
Donor spermabank. A donor spermát abszolút férfi meddőség vagy szexuális partner hiánya esetén használják.
A kemoterápiás kúra előtt a rákos betegek spermiummintákat fagyaszthatnak le, amelyeket később az ICIS módszerrel teherbe ejthetnek.