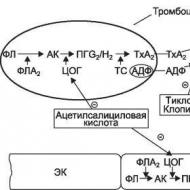
Gátolja a vérlemezke-aggregációt, ami azt jelenti. Thrombocyta aggregáció gátlók. Thrombocytaaggregáció ADP-vel
27.1. A vérlemezke-aggregációt csökkentő gyógyszerek (thrombocyta-aggregációt gátló szerek)
A trombociták kis korong alakú vérsejtek, amelyek csontvelői megakariociták töredékeiként képződnek. A vérlemezkék 6-12 napig keringenek a vérben, majd a szöveti makrofágok felfogják őket.
A vaszkuláris endotélium befolyásolja a vérlemezkék funkcionális aktivitását. Az endothelsejtek a véráramba szekretálják a prosztaciklint (prosztaglandin I 2) és az endoteliális relaxációs faktort, amelyet a nitrogén-monoxiddal azonosítanak. Ezek az anyagok megakadályozzák a vérlemezke-aggregációt. Ezenkívül az endothel sejtek olyan anyagokat választanak ki, amelyek csökkentik a véralvadást és elősegítik a thrombus lízisét. Mindez az intakt vaszkuláris endotélium antitrombogén tulajdonságait biztosítja.
A vaszkuláris endotélium károsodása esetén, amelyet különböző tényezők okozhatnak (mechanikai trauma, fertőzések, érfali atherosclerotikus elváltozások, megnövekedett vérnyomás stb.), az endotélium antitrombogén tulajdonságai csökkennek, ami megteremti a feltételeket a trombus kialakulása. A prosztaciklin és az endothel relaxáló faktor szintézise károsodik, ami megkönnyíti a kontaktust
sérült endothel felületű vérlemezkék. A vérlemezkék a sérülés helyén felhalmozódnak, és kölcsönhatásba lépnek a vaszkuláris szubendotheliummal: közvetlenül vagy a von Willebrand faktoron keresztül (az aktivált vérlemezkék és endothelsejtek választják ki) kollagénhez és más szubendoteliális fehérjékhez kötődnek, specifikus glikoproteinek részvételével, amelyek lokalizálódnak a vérben. vérlemezke membrán. A von Willebrand faktor az Ib glikoproteinhez, a kollagén pedig a vérlemezkemembrán Ia glikoproteinjéhez kötődik (lásd 27-1. ábra). A kollagén (valamint a trombin, amely kis mennyiségben lokálisan már a trombusképződés kezdeti szakaszában képződik) vérlemezkékre gyakorolt hatása állapotváltozást - aktivációt okoz. A vérlemezkék megváltoztatják alakjukat (a korongostól sok folyamattal laposodnak - pszeudopodiák) és lefedik az ér sérült felületét.
A vérlemezkék aktiválásakor különféle biológiailag aktív anyagokat bocsátanak ki, amelyek granulátumban vannak a nem aktivált vérlemezkékben (α-granulátumok, sűrű granulátumok). A sűrű granulátumok olyan anyagok tárháza, amelyek serkentik a vérlemezke-aggregációt: ADP és szerotonin. Ezeknek az anyagoknak a felszabadulása a thrombocyta granulátumokból a Ca 2+ intracelluláris koncentrációjának növekedése következtében következik be, a kollagén, a trombin és más aggregációt indukáló szerek hatására, beleértve magát az ADP-t is, a vérlemezkéken. A véráramba kerülő ADP stimulálja a vérlemezke membránjában lokalizált specifikus (purinerg) receptorokat. A G-fehérjékhez kapcsolódó receptorokon (P2Y 12 -purinerg receptorok) keresztül az ADP az adenilát-cikláz gátlását és a cAMP-szint csökkenését okozza, ami a thrombocyta citoplazmában a Ca 2 -szint növekedéséhez vezet (27-2. ábra).
Ezen túlmenően, amikor a vérlemezkék aktiválódnak, megnő a vérlemezke-membránok foszfolipáz A 2 aktivitása, egy enzim, amely részt vesz az arachidonsav képződésében a membrán foszfolipideiből. Az arachidonsavból származó vérlemezkékben a ciklooxigenáz hatására először ciklikus endoperoxidok (prosztaglandinok G 2 / H 2) szintetizálódnak, és ezekből a tromboxanzin közreműködésével.
tetáz, tromboxán A 2 képződik - a vérlemezke-aggregáció aktív stimulátora és érösszehúzó. A véráramba való felszabadulás után a tromboxán A 2 stimulálja a trombocita membránokon lévő tromboxán receptorokat. Ennek eredményeként a foszfolipáz C aktiválódik az ezekhez a receptorokhoz kapcsolódó Cq-fehérjéken keresztül, és képződik.
Rizs. 27-1. Thrombocyta adhézió és aggregáció az érfal károsodásakor: EC - endothel sejt; PV - von Willebrand faktor; TxA2 - tromboxán A2; PGI 2 - prosztaciklin; NO - endoteliális relaxációs faktor; GP - glikoproteinek; GP llb/llla – llb/llla glikoproteinek (Feladó: Katzung B.G. Bazic and Clinical Pharmacology – NY, 2001, a módosításokkal)
inozitol-1,4,5-trifoszfát, amely elősegíti a Ca 2+ felszabadulását a vérlemezkék intracelluláris depójából (a kalcium depó szerepét a vérlemezkékben sűrű tubulusok rendszere látja el). Ez a Ca 2+ citoplazmatikus koncentrációjának növekedéséhez vezet (27-2. ábra). A tromboxán A 2 a Ca 2+ koncentrációjának növekedését okozza a vaszkuláris simaizomsejtekben, ami érszűkülethez vezet.

Rizs. 27-2. Thrombocyta-aggregációt gátló szerek (acetilszalicilsav, tiklopidin és epoprosztenol) hatásmechanizmusai: EC - endothel sejt; PL - sejtmembránok foszfolipidei; AA - archidonsav; PLA 2 - foszfolipáz A2; COX - ciklooxigenáz; TS - tromboxán-szintetáz; PS - prosztaciklin szintetáz; PGG 2 /H 2 - ciklikus endoperoxidok; TxA2 - tromboxán A2; PGI 2 - prosztaciklin; AC - adenilát-cikláz; FLS - foszfolipáz C; IP 3 - inozitol-1, 4, 5-trifoszfát
Így az ADP és a tromboxán A 2 növeli a Ca 2+ szintet a thrombocyta citoplazmában. A citoplazmatikus Ca 2+ megváltoztatja a IIb / IIIa glikoproteinek konformációját a vérlemezke membránjában, aminek következtében képesek lesznek fibrinogén megkötődni. Egy fibrinogén molekulának két kötőhelye van a IIb / IIIa glikoproteinekhez, és így képes egyesíteni két vérlemezkét (27-3. ábra). A fibrinogén hidak által sok vérlemezke társulása vérlemezke-aggregátumok kialakulásához vezet.
Ezzel szemben a thrombocyta-aggregációt a prosztaciklin (prosztaglandin I 2) befolyásolja. Mint a tromboxán, a prosztaciklin
ciklikus endoperoxidokból képződik, de egy másik enzim - a prosztaciklin szintetáz - hatására. A prosztaciklint az endothel sejtek szintetizálják és a véráramba juttatják, ahol stimulálja a vérlemezke membránjában lévő prosztaciklin receptorokat, és a Gs protein adenilát ciklázon keresztül kapcsolódik hozzájuk. Ennek eredményeként a cAMP szintje a vérlemezkékben növekszik és a citoplazmatikus Ca 2+ koncentrációja csökken (lásd 27-2. ábra). Ez megakadályozza a IIb/IIIa glikoproteinek konformációs változását, és elveszítik fibrinogénkötő képességüket. Így a prosztaciklin megakadályozza a vérlemezke-aggregációt. A prosztaciklin hatására csökken a Ca 2+ koncentrációja a vaszkuláris simaizomsejtekben, ami értágulathoz vezet.

A thrombocyta-aggregációhoz vezető fő események alábbi sorozatát különböztethetjük meg (lásd a 27-1. sémát).
A klinikai gyakorlatban jelenleg használt thrombocyta-gátló szerek fő hatásiránya a tromboxán A 2 és az ADP hatásának megszüntetéséhez, valamint a vérlemezke membránok IIb / IIIa glikoproteinek blokkolásához kapcsolódik. Más hatásmechanizmusú anyagokat is alkalmaznak, amelyek növelik a cAMP koncentrációját a vérlemezkékben, és ennek következtében csökkentik bennük a Ca 2+ koncentrációját.
A következő szerek csoportjai vannak, amelyek csökkentik a vérlemezke-aggregációt.
2 . - Ciklooxigenáz inhibitorok:
acetilszalicilsav.

27.1. A vérlemezke-aggregáció mechanizmusa
Ciklooxigenáz és tromboxán szintetáz inhibitorok: indobufen.
A prosztaciklin receptorokat stimuláló gyógyszerek:
epoprosztenol**.
Eszközök, amelyek megakadályozzák az ADP hatását a vérlemezkékre:
tiklopidin; klopidogrél.
A vérlemezke-foszfodiészterázt gátló eszközök:
dipiridamol
Olyan szerek, amelyek blokkolják a vérlemezke membránok IIb/IIIa glikoproteinekjét.
Monoklonális antitestek: abciximab.
Szintetikus glikoprotein IIb/IIIa blokkolók: eptifibatid; tirofiban.
A tromboxán A szintézisét gátló szerek 2
Az acetilszalicilsav (aszpirin*) jól ismert gyulladáscsökkentő, fájdalomcsillapító és lázcsillapító szer. Jelenleg széles körben használják vérlemezke-gátló szerként. Az acetilszalicilsav thrombocyta-aggregáció-gátló hatása a trombocitákban a tromboxán A2 szintézisére kifejtett gátló hatásával függ össze.
Az acetilszalicilsav irreverzibilisen gátolja a ciklooxigenázt (az enzim irreverzibilis acetilezését okozza), és így megzavarja a ciklikus endoperoxidok, a tromboxán A 2 prekurzorai és az arachidonsavból származó prosztaglandinok képződését. Ezért az acetilszalicilsav hatására nem csak a trombociták tromboxán A 2 szintézise csökken, hanem a prosztaciklin szintézise is a vaszkuláris endothel sejtekben (lásd 27-2. ábra). A megfelelő dózisok és kezelési rend megválasztásával azonban elérhető az acetilszalicilsavnak a tromboxán A 2 szintézisére gyakorolt előnyös hatása. Ennek oka a vérlemezkék és az endothelsejtek közötti jelentős különbségek.
A vérlemezkék - nem nukleáris sejtek - nem rendelkeznek fehérje-újraszintézis rendszerrel, ezért nem képesek ciklooxigenázt szintetizálni. Ezért ezen enzim irreverzibilis gátlása esetén a tromboxán A 2 szintézise a vérlemezkék teljes élettartama alatt károsodik; 7-10 napon belül. Az új vérlemezkék képződése miatt az acetilszalicilsav thrombocyta-aggregáció gátló hatása rövidebb ideig tart, ezért a gyógyszer stabil hatásának (vagyis a tromboxánszint stabil csökkenésének) elérése érdekében javasolt a gyógyszer felírása. naponta 1 alkalommal.
A vaszkuláris endothel sejtekben a ciklooxigenáz újraszintézise megtörténik, és ennek az enzimnek az aktivitása az acetilszalicilsav bevétele után néhány órán belül helyreáll. Ezért a gyógyszer napi egyszeri felírásakor a prosztaciklin szintézisének jelentős csökkenése nem következik be.

Ezenkívül az acetilszalicilsav körülbelül 30%-a a májban megy keresztül first pass metabolizmuson, így koncentrációja a szisztémás keringésben alacsonyabb, mint a portális vérben. Ennek eredményeként az acetilszalicilsav nagyobb koncentrációban fejti ki hatását a portális keringésben keringő vérlemezkékre, mint a szisztémás erek endotélsejtjeire. Ezért a tromboxán A 2 szintézisének elnyomásához a vérlemezkékben kisebb dózisú acetilszalicilsavra van szükség, mint a prosztaciklin szintézisének elnyomására az endotélsejtekben.
Ezen okok miatt az acetilszalicilsav dózisának és beadási gyakoriságának növelésével a prosztaciklin szintézisére gyakorolt gátló hatása kifejezettebbé válik, ami a thrombocyta-aggregáció gátló hatásának csökkenéséhez vezethet. Ezekkel a tulajdonságokkal összefüggésben az acetilszalicilsavat, mint thrombocyta-aggregációt gátló szert, kis adagokban (átlagosan 100 mg) ajánlott naponta egyszer felírni.
Az acetilszalicilsavat thrombocyta-aggregáció gátló szerként használják instabil angina pectorisban, szívinfarktus, ischaemiás stroke és perifériás vaszkuláris trombózis megelőzésére, vérrögképződés megelőzésére koszorúér bypass graft és coronaria angioplasztika során. Az acetilszalicilsavat szájon át 75-160 mg-os adagokban (egyes indikációk szerint - 50-325 mg dózistartományban) naponta egyszer, hosszú ideig írják fel. Jelenleg az orvosok rendelkezésére állnak a trombózis megelőzésére szolgáló acetilszalicilsav készítmények, amelyek 50-325 mg hatóanyagot tartalmaznak, beleértve a bélben oldódó tablettákat - Acecardol *, Aspicor *, Cardiopyrin *, Aspirin cardio *, Novandol *, Thrombo ACC * és mások.Az acetilszalicilsav thrombocyta-aggregáció gátló hatása gyorsan (20-30 percen belül) jelentkezik. A bélben oldódó bevonatú gyógyszerformák lassabban kezdenek hatni, de hosszan tartó használat esetén hatékonyságuk gyakorlatilag megegyezik a hagyományos tablettákéval. A gyorsabb hatás elérése érdekében az acetilszalicilsav tablettákat meg kell rágni.
Az acetilszalicilsav fő mellékhatásai a ciklooxigenáz gátlásával kapcsolatosak. Ez megzavarja az E 2 és I 2 prosztaglandinok képződését, amelyek antiszekréciós és gyomorvédő hatásúak (csökkentik a gyomor parietális sejtjeinek sósav szekrécióját, növelik a nyálka és a bikarbonát szekrécióját). Ennek eredményeként az acetilszalicilsav már rövid használat mellett is károsíthatja a gyomor és a nyombél hámszövetét (ulcerogén hatás). A gyomor nyálkahártyájára gyakorolt hatás kevésbé kifejezett, ha bélben oldódó bevonattal ellátott adagolási formákat használnak. Az acetilszalicilsav alkalmazásakor gyomor-bélrendszeri vérzés és egyéb vérzéses szövődmények lehetségesek. Az ilyen szövődmények kockázata alacsonyabb, ha az acetilszalicilsavat 100 mg / nap vagy annál kisebb dózisban írják elő. A COX szelektív gátlása az arachidonsav átalakulásához és a hörgőösszehúzó tulajdonságokkal rendelkező leukotriének kialakulásához vezet a lipoxigenáz útvonal aktiválásához. A bronchiális asztmában szenvedő betegeknél az acetilszalicilsav rohamot válthat ki ("aszpirin asztma"). Allergiás reakciók lehetségesek.
Az acetilszalicilsav fekélyes hatásának csökkentése érdekében javasolt a Cardiomagnyl * kombinált készítmény, amely magnézium-hidroxidot tartalmaz. A magnézium-hidroxid semlegesíti a sósavat a gyomorban (antacid hatás), csökkentve a nyálkahártya károsító hatását. A gyógyszert ugyanazokra az indikációkra használják, mint az acetilszalicilsav, beleértve az ischaemiás stroke másodlagos megelőzését.
Az indobufen (ibusztrin *) csökkenti a tromboxán A 2 szintézisét, miközben gátolja a ciklooxigenázt és a tromboxán szintetázt. Az acetilszalicilsavval ellentétben az indobufen a ciklooxigenáz reverzibilis gátlását okozza. A gyógyszer szedése során a prosztaciklin mennyisége relatíve megnő (a prosztaciklin / tromboxán A 2 aránya nő). Az indobufen gátolja a vérlemezkék adhézióját és aggregációját. A használati javallatok és a mellékhatások megegyeznek az acetilszalicilsavéval.
A prosztaciklin receptorokat stimuláló gyógyszerek
A vérlemezke-aggregáció csökkentésének másik módja a prosztaciklin receptorok stimulálása. Erre a célra használja
prosztaciklin epoprosztenol készítése * . A prosztaciklin hatása ellentétes a tromboxán A 2 hatásával, nemcsak a vérlemezkékre, hanem az erek tónusára is. Vasodilatációt és vérnyomáscsökkenést okoz. A prosztaciklinnek ezt a hatását pulmonális hipertóniában alkalmazzák. Mivel a prosztaciklin gyorsan elpusztul a vérben (t 1/2 körülbelül 2 perc), és ezért nem tart sokáig, a gyógyszert infúzióban adják be. Rövid hatástartamának köszönhetően az epoprostenol* nem talált széles körben elterjedt thrombocyta-aggregációt gátló szerként. Az epoprosztenol thrombocyta-aggregációjának egyik lehetséges felhasználási területe a vérlemezke-aggregáció megelőzése az extracorporalis keringésben.
Olyan szerek, amelyek megzavarják az ADP vérlemezkékre gyakorolt hatását
A tiklopidin (ticlid*) egy tienopiridin-származék, amely gátolja az ADP által okozott vérlemezke-aggregációt. A tiklopidin egy prodrug, vérlemezke-gátló hatása a mikroszomális májenzimek részvételével aktív metabolit kialakulásához kapcsolódik. A tiklopidin metabolitja tiolcsoportokat tartalmaz, amelyeken keresztül irreverzibilisen kötődik a vérlemezke membránjában található P2Y 12 purinerg receptorokhoz. Ez az ADP vérlemezkékre gyakorolt stimuláló hatásának megszűnéséhez és a citoplazmatikus Ca 2+ koncentrációjának csökkenéséhez vezet bennük. Ennek eredményeként csökken a IIb / IIIa glikoproteinek expressziója a vérlemezke membránjában és a fibrinogénhez való kötődésük (lásd 27-2. ábra). A hatás visszafordíthatatlan jellege miatt a tiklopidin hosszan tartó thrombocyta-aggregáció gátló hatással rendelkezik.
A maximális hatás a tiklopidin folyamatos alkalmazásával 7-11 nap után érhető el (az aktív metabolit kialakulásához és kifejlődéséhez szükséges idő), és a gyógyszer abbahagyása után a vérlemezkék teljes élettartama alatt (7-10 nap) fennáll. .
A tiklopidint az ischaemiás stroke másodlagos megelőzésére, a trombózis megelőzésére az alsó végtagok obliteráló betegségeinél, a koszorúér bypass graftnál és a koszorúerek stentelésében írják fel. A gyógyszer hatásos szájon át szedve, naponta kétszer, étkezés közben felírva.
A tiklopidin alkalmazása mellékhatásai miatt korlátozott. Előfordulhat étvágycsökkenés, hányinger, hányás, hasmenés (20%), hasi fájdalom, bőrkiütések (11-14%). Neves
az aterogén lipoproteinek szintjének növekedése a vérplazmában. A vérzés gyakori szövődmény a vérlemezke-gátló szerek alkalmazásakor. Veszélyes szövődmény a neutropenia, amely a kezelés első három hónapjában a betegek 1-2,4%-ánál jelentkezik. Lehetséges thrombocytopenia, agranulocytosis, nagyon ritkán - aplasztikus anémia. Ebben a tekintetben a kezelés első hónapjaiban a vérkép szisztematikus monitorozása szükséges.
A klopidogrél (Plavix*, Zylt*) kémiai szerkezetében, főbb hatásaiban és hatásmechanizmusában hasonló a tiklopidinhez. A tiklopidinhez hasonlóan ez is egy prodrug, és a májban metabolizálódik, és aktív metabolitot képez. A thrombocyta-aggregáció jelentős gátlását a kezelés második napjától észlelték, a maximális hatást 4-7 nap után érik el. A gyógyszer abbahagyása után hatása 7-10 napig fennáll. A klopidogrél aktivitása jobb, mint a tiklopidin - napi 75 mg-os adagban ugyanolyan csökkenést okoz a vérlemezke-aggregációban és meghosszabbítja a vérzési időt, mint a tiklopidin napi 500 mg-os adagban.

A klopidogrél az acetilszalicilsavhoz hasonló indikációkra alkalmazható, annak intoleranciájával. Szájon át naponta 1 alkalommal, étkezéstől függetlenül. A klopidogrél kombinálható acetilszalicilsavval, mivel a gyógyszerek gátolják a vérlemezke-aggregáció különböző mechanizmusait, és ezáltal fokozzák egymás hatását (azonban ezzel a kombinációval nagyobb a vérzéses szövődmények kockázata).
A tiklopidinnel összehasonlítva a klopidogrél mellékhatásai kevésbé kifejezettek (hasmenés - 4,5%, kiütés - 6%). A klopidogrél alkalmazása csökkenti az olyan súlyos szövődmények kockázatát, mint a neutropenia (0,1%), a thrombocytopenia ritkábban fordul elő. Ritka szövődményként, csakúgy, mint a tiklopidin esetében, trombotikus thrombocytopeniás purpura alakulhat ki.
A vérlemezke-foszfodiészterázt gátló szerek
A dipiridamolt (Curantyl*, Persanthin*) először koszorúér-tágítóként javasolták. Később kiderült, hogy képes gátolni a vérlemezke-aggregációt. Jelenleg a dipiridamolt főként trombocita-gátló szerként használják trombózis megelőzésére. A dipiridamol vérlemezke-ellenes hatása a cAMP szintjének emelkedésével jár a vérlemezkékben, ami a citoplazmatikus Ca 2+ koncentrációjának csökkenését eredményezi bennük. Ez több okból is előfordul. Először is, a dipiridamol gátolja a foszfodiészterázt, amely inaktiválja a cAMP-t. Ezenkívül a dipiridamol gátolja az endothel sejtek és eritrociták adenozin felvételét és metabolizmusát (gátolja az adenozin-deaminázt), ezáltal növeli az adenozin szintjét a vérben (27-4. ábra). Az adenozin stimulálja a thrombocyta A 2 receptorokat, és növeli az ezekhez a receptorokhoz kapcsolódó adenilát-cikláz aktivitását, ennek eredményeként nő a cAMP képződése a vérlemezkékben, és csökken a citoplazmatikus Ca 2+ szintje. A dipiridamol növeli a cAMP szintjét a vaszkuláris simaizomsejtekben is, ami érrelaxációt okoz.

A dipiridamolt ischaemiás stroke megelőzésére, valamint perifériás artériás betegségekre használják (főleg acetilszalicilsavval kombinálva, mivel maga a dipiridamol gyenge vérlemezke-gátló hatással rendelkezik). Hozzárendelni belül 3-4 alkalommal naponta 1 órával étkezés előtt. Orális antikoagulánsokkal kombinálva dipiridamolt írnak fel a vérrögképződés megelőzésére mitrális szívbetegségben.
Dipiridamol alkalmazásakor fejfájás, szédülés, artériás hipotenzió, dyspepsia,
bőrkiütések. A vérzés kockázata kisebb, mint acetilszalicilsav esetén. A dipiridamol ellenjavallt angina pectoris (esetleges "lopás szindróma") esetén.

Rizs. 27-4. A dipiridamol vérlemezke-ellenes hatásának mechanizmusa: EC - endothel sejt; A2-P-adenozin A2 receptor; PDE-foszfodiészteráz cAMP; AC - adenilát-cikláz; GP IIb/IIIa - glikoproteinek IIb/IIIa
A pentoxifillin (agapurin*, trental*), a dipiridamolhoz hasonlóan gátolja a foszfodiészterázt és növeli a cAMP szintjét. Ennek eredményeként a citoplazmatikus Ca 2 + szintje a vérlemezkékben csökken, ami aggregációjuk csökkenéséhez vezet. A pentoxifillin egyéb tulajdonságokkal is rendelkezik: növeli a vörösvértestek deformálhatóságát, csökkenti a vér viszkozitását, értágító hatású, javítja a mikrokeringést.
A pentoxifillint agyi keringési zavarok, különböző eredetű perifériás keringési zavarok, a szem vaszkuláris patológiája esetén alkalmazzák (lásd "Az agyi keringés megsértésére használt eszközök" című fejezetet). Lehetséges mellékhatások: dyspepsia, szédülés, arcvörösség, valamint vérnyomáscsökkenés, tachycardia, allergiás reakciók, vérzés. A dipiridamolhoz hasonlóan angina pectoris rohamokat válthat ki.
Olyan szerek, amelyek blokkolják a vérlemezke membránok IIb/IIIa glikoproteinekjét
Az antiaggregánsok ezen csoportja, amely közvetlenül kölcsönhatásba lép a vérlemezke membránjainak IIb/IIIa glikoproteinjeivel, és megzavarja azok fibrinogénhez való kötődését, viszonylag nemrég jelent meg.
Abciximab (reopro *) - az első gyógyszer ebből a csoportból egy "kiméra" egér/humán monoklonális antitestek (a IIb / IIIa glikoproteinek elleni egér antitestek Fab-fragmentuma, amely a humán Ig Fc-fragmenséhez kapcsolódik). Az abciximab nem kompetitív módon gátolja a fibrinogén kötődését a IIb/IIIa glikoproteinekhez a vérlemezke membránján, megzavarva azok aggregációját (lásd 27-3. ábra). A vérlemezke-aggregáció egyetlen injekció beadása után 48 órával normalizálódik. A gyógyszert intravénásan (infúzió formájában) adják be a trombózis megelőzésére a koszorúér angioplasztikája során. Az abciximab alkalmazásakor vérzés lehetséges, beleértve a belső (gasztrointesztinális, intrakraniális, húgyúti vérzést), émelygést, hányást, hipotenziót, bradycardiát, allergiás reakciókat az anafilaxiás sokkig, thrombocytopeniát.
Az azonos hatásmechanizmusú, kevésbé allergén gyógyszerek keresése a IIb/IIIa glikoproteinek szintetikus blokkolóinak létrehozásához vezetett. A barborin (egy törpe csörgőkígyó mérgéből izolált peptid) alapján az ept és f és b a t és d (integrilin *) gyógyszert kapták - egy ciklikus hektapeptidet, amely utánozza a fibrinogén lánc aminosavszekvenciáját, amely közvetlenül kötődik a IIb / IIIa glikoproteinekhez. Az eptifibatid kompetitív módon kiszorítja a fibrinogént a receptorokhoz való kapcsolódásából, ami a vérlemezke-aggregáció reverzibilis károsodását okozza. A gyógyszert intravénásan adják be infúzió formájában; a thrombocyta-aggregáció gátló hatás 5 percen belül jelentkezik, és az alkalmazás abbahagyása után 6-12 órával megszűnik. A gyógyszer javasolt trombózis megelőzésére percutan coronaria angioplasztikában, instabil angina pectorisban, szívinfarktus megelőzésére. Az eptifibatid alkalmazása során veszélyes szövődmény a vérzés; lehetséges thrombocytopenia.
A tirofibán (agrastat*) egy nem peptid glikoprotein IIb/IIIa blokkoló, a tirozin analógja. Az eptifibatidhoz hasonlóan a tirofiban is kompetitív módon blokkolja a glikoprotein IIb/IIIa receptorokat. A gyógyszert intravénásan adják be (infúzió). A hatás kezdetének sebessége, a hatás időtartama és a használati javallatok megegyeznek az eptifibatiddal. Mellékhatások - vérzés, thrombocytopenia.
Ennek a gyógyszercsoportnak a felhasználási lehetőségeinek bővítése érdekében létrehozták a IIb/IIIa glikoproteinek blokkolóit, amelyek szájon át adva hatékonyak - xemilofiban *, sibrafiban * stb. Ezeknek a gyógyszereknek a tesztjei azonban nem kielégítő hatékonyságot és mellékhatást mutattak ki. súlyos thrombocytopenia formájában.
A vérlemezke-aggregáció az a folyamat, amikor egy sebet elzárnak nagyon kis vérsejtek, amelyek az erek falának közelében helyezkednek el, és részt vesznek azok fenntartásában.
Ha a kapilláris épsége megsérül, a sérüléshez mennek, lezárják, megakadályozva ezzel a vérzést. Hogyan csökkenthető a szedendő gyógyszerek száma?
Leírás
Amikor a plakkok a sérülés helyére rohannak, egymásra rétegezve trombust képeznek - ezt a jelenséget adhéziónak és aggregációnak nevezik, az egy rendszerbe olvadó folyamat (aggregatio joining) a seb bezáródásáig tart. Ennek köszönhetően az ember nem veszít sok vért.
A vérlemezke-aggregáció vizsgálata a plazma elemzésével történik. Egészséges emberben ezek a sejtek megvédik a szervezetet a vérzéstől, olyan eltérések léphetnek fel, amelyek különböző betegségeket provokálnak. Fel/le megy.
Életkori mutatók
Elemzés
Vénából vérlemezke-aggregációs tesztet vesznek. A szív, az erek, a vér egyes betegségei esetén szükséges.
Szállítás előtt bizonyos feltételeknek teljesülniük kell az elemzés pontosságához:
- 3 napig tartsa be az orvos által előírt étrendet.
- Napközben ne szedjen gyógyszert.
- 24 órán keresztül ne igyon alkoholt, koffeint, ne dohányozzon.
Ha az összes ajánlást betartják, az elemzés igaz lesz, nincsenek olyan anyagok, amelyek befolyásolják a vérrögképződés folyamatát. A laboratóriumban az eredmény elérése érdekében emberi sejteket utánzó induktorokat (stimulátorokat) adnak a plazmához.
Az elemzés végrehajtása folyamatban van:
- adenozin-difoszfát (ADP).
- Risztomicin (ristomycinum; syn. ristocein) antibiotikummal.
- Az adrenalin (epinefrin) (L-1 (3,4-Dioxiphenyl)-2-methylaminoethanol) a mellékvesevelő fő hormonja.
- Arachidonsav (többszörösen telítetlen omega-6 zsírsav).
- A kollagén egy fibrilláris fehérje.
- Szerotonin – 5-hidroxi-triptamin, neurotranszmitter, a boldogság hormonja.
Indukált aggregációt végeznek bizonyos betegségek diagnosztizálására. Ehhez lézerelemzőt használnak. Plazmát és induktort engednek bele, ami után a készülék kiszámolja a plakkok koagulálhatóságát.
Leggyakrabban a következőket veszik:
- ADP-vel.
- Arachidonsavval.
- Adrenalinnal (epinefrin).
- És risztocetinnel is.
Az első három stimulátor lehetővé teszi a sejt minden oldalról történő értékelését, a negyedik - patológia (vérzés).
Aggregációs mutatók - az elemzés dekódolása az induktortól függően
Fajták
- Spontán aggregáció, amikor plazmát veszünk, egy speciális eszközbe helyezzük, és egy bizonyos hőmérsékletre melegítjük, hogy feltárja a vérsejt működését.
- Indukált, amelyet egy thrombocyta-aggregációs analizátor végez induktorok segítségével bizonyos betegségek megállapítására.
- Mérsékelt - a méhlepény vérkeringése okozza a terhesség alatt.
- Fokozott - vérrögképződéshez, ödémához vezet.
Elemzés
Felírva:
- Túl gyors trombózis.
- Thrombophlebitis, thrombocytopenia.
- Vérzésre való hajlam (méh, orr).
- Gyenge sebgyógyulás.
- Ínyvérzés.
- Vérhígító gyógyszerek (szalicilsav) hosszú távú alkalmazása.
- Flebeurizma.
- Szív, érrendszeri betegségek.
- Komplikációk a terhesség alatt.
- Műtét előtt.
hanyatlás
Az aggregáció bizonyos betegségekben alacsony, esetleg örökletes. Rossz tapadás esetén a sejt gátolja (elnyomja) a vérleállítás folyamatát, súlyos vérzés léphet fel. Ez történik:
- Hiány, pajzsmirigyhormon-többlet.
- Súlyos májkárosodás (cirrhosis, hepatitis).
- Fertőző, vírusos (kanyaró, rubeola).
- Toxin mérgezés.
A plakk gyors csökkenése súlyos betegség, kémiai kezelés vagy gátlószerek hosszú távú alkalmazása során fordulhat elő.
- A csontvelő rákos elváltozásai, leukémia.
- A daganatos betegek besugárzása nagymértékben megváltoztatja a vér összetételét.
- Mellékhatásokkal járó gyógyszerek (acetil-szalicilsav, reopirin, antibiotikumok).
Súlyos betegségek esetén, amelyek a sejtek számának csökkenéséhez vezetnek, a koagulogram (véralvadás) további elemzését végzik el. Javasoljuk, hogy tegye:
- Műtét előtt.
- Terhesség tervezése.
- A szív patológiáival, szívrohamokkal.
- Magas vérnyomás.
- A kezelés során régóta használt inhibitorok.
Koagulogramra van szükség annak érdekében, hogy elkerüljük a súlyos vérzést a műtét idején, a betegségek súlyos következményeit és a veleszületett patológiákat. A rossz véralvadás ritka.
Növekedés
A hiperaggregáció hozzájárul a vér viszkozitásához, a vérrögök gyors képződéséhez. Ez a jelenség akkor fordul elő, ha:
- Magas cukortartalom (cukorbetegség).
- Magas vérnyomás.
- Onkológia a vesékben, gyomorban, leukémiában.
- Hemorrhagiás szindróma, amely csökkent vérzéscsillapításhoz vezet.
- A szív, az agy ereinek ateroszklerózisa.
A kapillárisokon belüli vérrögök (thrombusok) kialakulása súlyos következményekkel jár. A plakkok tapadása az artériák falához a lumen csökkenéséhez vezet, ami hátrányosan befolyásolja a vérkeringést.
A vérrögök megnövekedett tartalma olyan betegségeknek felelhet meg, amelyek rokkantsághoz vezetnek:
- A keringési zavarok miatt a szívizom szenved, szívroham lép fel.
- A fejben lévő vérrögök stroke-hoz vezetnek.
- A vérrögök a lábak vénáin telepednek meg, és thrombophlebitist képeznek.
Amikor az edények lumenje bezárul - súlyos patológia, amely halálhoz vezet, orvosi kezelést igényel. Ezekre a célokra van egy gátló (gátló - gátolja, késlelteti) a vérlemezke-aggregációt.
Ebben az esetben nyomasztóan hat a sejtek ragasztásának folyamatára, a patológia kialakulására. Az alábbiakban felsoroljuk azokat a gyógyszereket, amelyeket szív- és érrendszeri betegségek, veseelégtelenség kezelésére használnak.
Az Enazil, Lisinopril, Hartil, Diroton gyógyszerek - az alkalmazott inhibitorok nem csökkentik a nyomást. Bármilyen elemzés elvégezhető a laboratóriumban, ahol garantált a sürgősség és a gyorsaság.
Végezzen megelőző vizsgálatokat, vigyázzon egészségére. Szinte minden betegség korai szakaszában gyógyítható. Új információkért látogassa meg weboldalunkat.
A vérlemezkék, a legkisebb vérsejtek (a leukocitákhoz és eritrocitákhoz képest) a legfontosabb funkciót látják el - megvédik a szervezetet a vérveszteségtől. A thrombocytaaggregáció a sejtek összeragasztásának folyamata, a trombusképződés kezdeti szakasza.
A második szakasz a vérlemezkék rögzítése a sérült ér falán. Fibrinszálak, egyéb elemek, új tapadó sejtek rakódnak a vérlemezke tömegére. Így a trombus olyan méretűre nő, amely elzárhatja az ér átmérőjét és megállíthatja a vérzést. Az ember élete néha a folyamat sebességétől függ.
A vérlemezke-aggregáció szerepe a véralvadás folyamatában
A véralvadás sok tényezőtől függ. Ezek egyike, a vérlemezke-aggregáció egy egészséges szervezetben védekező adaptív jellegű. A sejtek csak a vérző edényben tapadnak össze. Ebben az esetben a folyamat pozitív szerepet játszik.
De ismertek olyan kóros állapotok, amelyekben a vérrögképződés nem kívánatos, mivel ez a létfontosságú szervek alultápláltságához vezet. Például szívinfarktus, stroke, vezető artériák trombózisa esetén. A vérlemezkék aggregációs aktivitása a kóros elváltozások oldalát veszi át. Különféle gyógyszerek segítségével kell ellene küzdeni.
Gyakorlatilag szükség van a jó és a rossz vérlemezke-aggregáció számszerűsítésére. Ehhez a normát kell használni, és különbséget kell tenni az eltérések között.
Hogyan lehet meghatározni a normát és a patológiát?
Egy vérvizsgálat kimutathatja egy adott személy vérlemezkéinek aggregációs képességét? Valójában a vizsgálathoz vért vesznek egy vénából, és ettől a pillanattól kezdve a test „parancsai” nem hatnak a vérsejtekre. Az ilyen típusú elemzést "in vitro"-nak nevezik, szó szerinti fordítása latinból "üvegen, kémcsőben". A tudósok mindig az emberi testhez közeli körülmények között próbálják tanulmányozni a reakciót. Csak az így nyert adatok tekinthetők megbízhatónak és használhatók fel a diagnosztikában.
A vérlemezkék képességét az indukált aggregáció határozza meg. Ez azt jelenti, hogy induktorként olyan szereket használnak, amelyek kémiai összetételét tekintve nem idegenek a szervezettől, és trombózist okozhatnak. Induktorként az érfal összetevőit használják: adenozin-difoszfát (ADP), risztocetin (ristomicin), kollagén, szerotonin, arachidonsav, adrenalin.
A spontán aggregációt induktorok nélkül határozzuk meg.
A kvantitatív meghatározás technikái a fényhullámok vérlemezkékben gazdag plazmán keresztül történő átvitelén alapulnak. Az aggregációs aktivitás mértékét a plazma fénysűrűségének különbsége vizsgálja a véralvadás megkezdése előtt és a maximális eredmény elérése után. Határozza meg az aggregáció sebességét is az első percben, a hullámok jellegét és alakját.
A norma az anyag-induktortól, annak koncentrációjától függ.
Az ADP-vel végzett vérlemezke-aggregációt általában kollagénnel, risztomicinnel és adrenalinnal együtt adják és értékelik.
Az ADP-vel végzett analízis normája 30,7-77,7%. A vérlemezke-aggregáció értéke adrenalinnal 35 és 92,5% között változik. A kollagénnel végzett vizsgálat során a normál értékek 46,4 és 93,1% között vannak.
Az elemzésre való felkészülés szabályai
Az aggregációs képesség vérvizsgálatához meg kell értenie, hogy a vizsgálat pontatlan lesz, ha megsértik az előkészítési szabályokat. A vérben olyan anyagok lesznek, amelyek befolyásolják az eredményt.
- Egy héttel a véradás előtt az összes aszpirin gyógyszert, a dipiridamolt, az indometacint, a szulfapiridazint és az antidepresszánsokat törölni kell. Ezen gyógyszerek alkalmazása gátolja (elnyomja) a trombózist. Ha nem lehet abbahagyni a szedést, értesíteni kell a laboránst.
- Legalább 12 órán keresztül nem lehet enni, az elfogyasztott zsíros ételek különösen befolyásolják az eredményeket.
- A betegnek a lehető legnyugodtabbnak kell lennie, ne végezzen fizikai munkát.
- Egy napig zárja ki az ételből a kávét, alkoholt, fokhagymát, ne dohányozzon.
- Az elemzést nem végzik el, ha aktív gyulladásos folyamat van.
A mikroszkóp alatt összetapadt vérlemezkék láthatók
A vérlemezke-aggregáció vérvizsgálatát az orvos írja elő, ha antikoaguláns kezelés szükséges, hatékonyságuk ellenőrzése, az optimális dózis kiválasztása, fokozott vérzés diagnosztizálása.
Az eredmények megfejtése
Az egyidejűleg három standard induktorral végzett vizsgálatok és szükség esetén újak hozzáadásának okai az egyik koagulációs faktor aktiválásának domináns mechanizmusában rejlenek. A feltárt megváltozott normának, például az ADP-vel, ha nincs dinamika más induktorokkal, diagnosztikai értéke van. Az eredmények értékelését orvos végzi.
A csökkent vérlemezke-aggregációt a következők okozhatják:
- a trombocita-ellenes terápia sikeres alkalmazása;
- a thrombocytopathiának nevezett betegségek csoportja.

Összesítési elemző készülék
A thrombocytopathia szerepe
A thrombocytopathiák lehetnek örökletesek vagy más betegségek eredményeként szerzettek. A statisztikák azt mondják, hogy a világ lakosságának akár 10% -a szenved ebben a patológiában. Mindegyikük a vérlemezkék funkcióinak megsértésével jár bizonyos anyagok felhalmozódása érdekében.
Ennek eredményeként nem alakul ki alvadás és a vérrögök képződése, ami fokozott vérzést okoz kis sebekkel, zúzódásokkal (belső vérzés).
A betegségek már gyermekkorban megnyilvánulnak fogínyvérzéssel, gyakori orrvérzéssel, sok zúzódással a gyermek testén, ízületi duzzanattal zúzódásokkal. A pubertás alatti lányoknál hosszú és erős menstruáció kezdődik. A vérzés vérszegénység (vérszegénység) kialakulásához vezet.
Az alacsony aggregációs képességet thrombocytopathiában vírusos és bakteriális fertőzés, gyógyszerek, fizioterápia aktiválhatja.

Az orrvérzést az esetek 80%-ában thrombocytopathia okozza, és csak 20%-ban a fül-orr-gégészeti szervek betegségei.
Másodlagos thrombocytopathiák
Tüneti (szekunder) thrombocytopathiák alakulnak ki krónikus leukémiában, myeloma multiplexben,. Ez az állapot a veseelégtelenség (urémia) végső szakaszára, a pajzsmirigy működésének csökkenésére jellemző.
A thrombocytopathiával a sebészek fokozott vérzéssel találkoznak a sebészeti beavatkozások során.
A vérlemezke-aggregáció növekedése figyelhető meg:
- az erek széles körben elterjedt ateroszklerózisa;
- magas vérnyomás;
- belső szervek infarktusa;
- a hasüreg artériáinak trombózisa;
- stroke
- cukorbetegség.
Az aggregáció változása a terhesség alatt
A terhesség alatti vérlemezke-aggregáció eltérhet a normál értékektől.
Az aggregáció csökken a vérlemezkék elégtelen termelése vagy minőségi összetételük megsértése miatt. Ez vérzésben, véraláfutásban nyilvánul meg. Szülésnél számolni kell a tömeges vérzés lehetőségével.
Az aggregáció leggyakrabban toxikózis során fokozódik a hányás és hasmenés következtében fellépő folyadékvesztés miatt. A vérkoncentráció növekedése fokozott trombózishoz vezet. Ez korai vetéléshez vezethet. A mérsékelt hiperaggregáció normálisnak tekinthető a terhesség alatt, a placenta keringésének kialakulásához kapcsolódik.
- vetélés esetén;
- meddőségi kezelés;
- fogamzásgátlók alkalmazása előtt és alatt;
- tervezett terhesség előtt.
A vérlemezkék aggregációs tulajdonságainak elemzése lehetővé teszi a kockázat azonosítását, a betegségek során fellépő veszélyes szövődmények előrejelzését és a megelőző terápia időben történő elvégzését.
A vérlemezkék olyan vérsejtek, amelyeknek nincs színük. Fontos funkciót töltenek be a szervezetben, megvédik a vérveszteségtől. Ez a folyamat a vérlemezkék aggregációja a vérben, saját normatív mutatói vannak.
Ahhoz, hogy megértsük, mi ez, meg kell értenie a vérrög képződését, a meglévő szabványokat, a normál értékektől való eltérések veszélyét.
Leírás és szerepe az emberi szervezetben
A szövetek sérülése után a vérlemezkék rögzítve vannak a sérült ér falán. Ennek eredményeként a sejtek egymáshoz tapadnak. A kapott masszához idővel fibrinszálak, új ragasztott sejtek és egyéb elemek csatlakoznak.
Ennek hátterében egy trombus nő, amely eléri a nagy méretet, ami az ér elzáródásához és a vérzés leállításához vezethet. Egy ilyen folyamat gyorsasága nagyon fontos, mivel néha az emberi élet megőrzése függ tőle.

A véralvadást számos tényező befolyásolja. Az egyik az aggregáció. Kóros állapotok hiányában védő adaptív funkciót lát el.
Az aggregációs jellemzők abból állnak, hogy a sejteket csak a sérült edényben ragasztják. Ebben az esetben a folyamat pozitívnak tekinthető.
.jpg)
Vannak azonban olyan helyzetek, amikor a trombózis nem kívánatos. Például, ha stroke-ot, szívinfarktust diagnosztizálnak.
Ez annak a ténynek köszönhető, hogy a vérrögképződés megakadályozza a szükséges anyagok normális áramlását a létfontosságú szervekbe.
Ebben az esetben a vérlemezkék a kóros folyamatok oldalára állnak.. A normától való eltérések kezelése csak gyógyszerek segítségével szükséges.
Az eltérések normál mutatóinak azonosítása érdekében kvantitatív elemzést kell végezni a pozitív és negatív aggregációról.
Fajták
Az orvosi gyakorlatban az aggregáció típus szerinti besorolása létezik. Ezek tartalmazzák:

- mérsékelt aggregáció. Főleg gyermekvállalás során diagnosztizálják. A placenta keringése provokálhatja az állapotot.
- spontán aggregáció. A definíció nem igényel induktort. Az aggregációs aktivitás kimutatására a vért egy kémcsőbe öntik, amelyet egy speciális eszközbe helyeznek, ahol 37 fokra melegítik.
- indukált aggregáció. A kutatáshoz induktorokat adnak a plazmához. Ebben az esetben aggregáció történik ADP-vel, kollagénnel, ristomicinnel és adrenalinnal. Ezt a módszert olyan esetekben alkalmazzák, amikor szükség van a vérfolyadék egyes patológiáinak diagnosztizálására.
- A fokozott aggregáció hozzájárul a vérrögök kialakulásához. Az ilyen kóros állapot jellegzetes tünete a zsibbadás és a duzzanat.
- A csökkent aggregációt leggyakrabban a keringési rendszer megsértése esetén észlelik. A vérlemezkeszám csökkenése különféle vérzéseket vált ki. A tisztességes nemnél a menstruációs ciklus alatt fordul elő.
Az aggregáció növekedése és csökkenése egyaránt veszélyes az emberi egészségre. Ezért rendszeresen ellenőrizni kell a vérlemezkék szintjét a vérben.
A mutatóktól való eltérés tünetei
A hiperaggregációt megnövekedett vér viszkozitása és áramlási sebességének csökkenése kíséri, ami hátrányosan érinti az összes emberi rendszert és szervet.
Vannak azonban kóros állapotok, amikor a kifejezett aggregáció normális, ami viszont nem tekinthető oknak a véralvadási paraméterek állandó tanulmányozásának megtagadására.
Ezek a betegségek a következők:
- megnövekedett vérnyomás;
- cukorbetegség;
- onkológiai betegségek;
- érrendszeri patológiák.
A hiperaggregáció idő előtti észlelése és a segítő intézkedések hiánya szívroham, stroke és vénás trombózis kialakulásához vezethet.
Az aggregációs paraméterek csökkenését elhúzódó vérzés kíséri, beleértve a belső vérzést is, amely hematómák képződésében nyilvánul meg.
Mi a norma
A vérlemezkeszint normái felnőtteknél és gyermekeknél kissé eltérnek. A mutatók optimális értékeit az alábbi táblázat mutatja be.
Ha normál aggregációs értékekről beszélünk, akkor ez 25-75 százalék lesz. Ebben az esetben a vérlemezkék eltérések nélkül összetapadnak, és nem jelentenek veszélyt az emberi szervezetre.
Milyen kutatás folyik
A thrombocyta-aggregációs analizátor teljes vérkép. Vannak azonban más tanulmányok is, amelyek pontosabb eredményeket adnak. A fő módszerek a következő teszteket tartalmazzák:
.jpg)
- Lee White szerint;
- koagulogram.
Lényegük abban rejlik, hogy speciális anyagok zavarják a vért, amelyek gátolják az aggregációt.
Ezek az összetevők hasonlóak az emberi szervezetben lévő anyagokhoz, amelyek trombózist váltanak ki. Az ilyen alkatrészeket induktoroknak nevezzük.
Felkészülés az elemzésre
Az elemzés elvégzése előtt bizonyos előkészületeken kell átesni. Annak érdekében, hogy az eredmények minél pontosabbak legyenek, a vérfolyadékban ne legyen olyan anyag, amely negatívan hathat rá.
Előkészítő tevékenységek:
- Egy héttel az elemzés előtt az aszpirin gyógyszereket kizárják, mivel beadásuk eredményeként a trombusképződés elnyomódik. Ha nem lehetséges ezeket az alapokat törölni, értesíteni kell a vizsgálatot végző laboratóriumi asszisztenst.
- 12 órán keresztül meg kell tagadnia az ételt. A termékek, különösen a magas zsírtartalmú termékek szintén negatívan befolyásolják az eredményeket.
- Kerülje a fizikai és érzelmi stresszt.
- Napközben ne igyon alkoholt, kávét, fokhagymát, ne dohányozzon.
Az elemzést elhalasztják, ha aktív gyulladásos folyamat van.
Holding
A vérvétel reggel, 7-10 óra között történik. A vizsgálatot csak éhgyomorra lehet elvégezni. Nem szénsavas vizet szabad inni.
A hemoteszt elvégzéséhez vegyen vért a vénából. Erre a célra eldobható fecskendőt használnak. Ezután az anyagot egy aggregométerbe helyezzük, amely 4% -os nátrium-citrát oldatot tartalmaz. Ezután a tartályt többször meg kell fordítani. Ezután a vérmintát a laboratóriumba küldik további elemzésre.
Az eredmények megfejtése
A vizsgálat során használt anyag figyelembevételével az elemzés dekódolásra kerül. Ehhez a kapott mutatókat összehasonlítják a normál értékekkel, amelyeket az alábbiakban mutatunk be.
Ha a normához képest növekedés tapasztalható, hiperaggregációt diagnosztizálnak. Olyan kóros állapotokban fordulhat elő, mint:
.jpg)
- leukémia;
- a gyomor-bél traktus vagy a vesék patológiája;
- érelmeszesedés;
- cukorbetegség;
- magas vérnyomás;
- vérmérgezés;
- lymphogranulomatosis.
A kisebb oldalra való eltérésekkel hipoaggregációt diagnosztizálnak. Vérpatológiák, vérlemezke-ellenes szerekkel végzett kezelés okozhatja.
A százalékos érték a plazma fényáteresztési szintjét mutatja, miután induktor anyagot adtunk hozzá. Alacsony vérlemezke-tartalom esetén ez a mutató 100 százalék, megnövekedett tartalom esetén nulla.
Az aggregáció jellemzői terhes nőknél
Terhesség alatt megengedettek a normától való eltérések, amelyek ebben az időszakban 30-60 százalék.
A szétesés megfigyelhető a vérlemezkék hiánya esetén, valamint ha minőségi összetételük megváltozik, ami vérzéssel és zúzódásokkal nyilvánul meg.
Az aggregáció növekedése toxikózis esetén fordul elő, amikor a beteg hányás vagy hasmenés következtében nagy mennyiségű folyadékot veszít. A vérkoncentráció növekedése fokozott vérrögképződést vált ki. Ez korai vetélést fenyeget.
Hogyan lehet az értékeket normalizálni?
Ha a vérfolyadék alvadásának megsértését diagnosztizálják, azonnali intézkedéseket kell tenni a kóros állapot megszüntetésére. Az aggregáció növekedése trombózishoz, az aggregáció csökkenése pedig erős és veszélyes vérzéshez vezethet.
A hiperaggregáció kialakulásának kezdeti szakaszában a szakemberek olyan gyógyszereket írnak fel, amelyek hígíthatják a vért. A közönséges aszpirin képes megbirkózni a feladattal.
A kiegészítő vizsgálat eredményei alapján gyakran előírják:
.jpg)
- fájdalomcsillapítók;
- novokain blokád;
- vazodilatációt elősegítő gyógyszerek;
- antikoagulánsok, amelyek megakadályozzák a gyors véralvadást.
Néha a népi módszerek nem kevésbé hatékonyak. Emlékeztetni kell arra, hogy az ilyen kezelést a kezelőorvossal feltétlenül egyeztetni kell.
A bevált receptek közé tartoznak a következők:
- Egy evőkanál édes lóherét öntsön 200 ml forralt vizet, és hagyja 30 percig főzni. Használja az elkészített készítményt a napra több adagban. A terápia időtartama egy hónap.
- Egyenlő mennyiségben (egy teáskanál) gyömbért és zöld teát forraljunk fel másfél liter forrásban lévő vizet. Adjunk hozzá egy csipet fahéjat. Ragaszkodjon negyed óráig, és vegye be a nap folyamán.
- Igyál minden nap frissen facsart narancslevet. Egyenlő arányban keverhető sütőtökkel.
Fontos a megfelelő étrend betartása is.. Az étrendnek tartalmaznia kell:
- citrusfélék;
- gyömbér;
- fokhagyma;
- piros és zöld zöldségek;
- tenger gyümölcsei.
Rossz véralvadás esetén tilos kábítószert szedni. amelyek hígítják a vért. Ha a folyamat lefolyása elhanyagolt formát kapott, akkor a terápiás intézkedéseket csak álló körülmények között hajtják végre.
A gyógyszerek közül kijelölik:

- Emosint;
- aminokapronsav és tranexámsav;
- Az ATP bevezetése;
A hajdina zabkása, tojás, répa és sárgarépa, gránátalma, marhamáj, vörös hús jelenléte kötelező az étrendben.
A vér normál állapotának fenntartása érdekében szigorúan be kell tartani az ivási rendet. Naponta legalább másfél liter tiszta víz számít normának. Az élelmiszernek frissnek és kiegyensúlyozottnak kell lennie.
A táplálkozási szabályok betartása az emberi test számos betegségének megelőzése. A fizikai aktivitás is fontos szerepet játszik. Nemcsak a test erősítéséhez, hanem az összes belső folyamat normalizálásához is hozzájárulnak.
Az aggregációs mutatók eltéréseinek időben történő diagnosztizálásával számos betegség és szövődmény megelőzhető. Rendszeresen ellenőrizni kell a vérlemezke-aggregáció szintjét.
A vérlemezkék részt vesznek az elsődleges hemosztázis folyamatában. Aktiválásuk három szakaszból áll: 1) adhézió az érintett területhez, 2) felszabadulási reakció (a vérlemezke-termékek szekréciója és a kulcsreceptorok aktiválása) és 3) aggregáció. Például, ha egy véredény megsérül, a vérlemezkék a membrán glikoprotein receptorai segítségével gyorsan megtapadnak a szubendoteliális tér (kollagén) hozzáférhetővé vált összetevőihez; ezt a folyamatot a von Willebrand faktor szabályozza. A vérlemezkék érfalhoz tapadását követően a citoplazmatikus granulátum tartalma (beleértve a kalciumot, ADP-t, szerotonint és trombint) felszabadul. A thrombocyta-aktiválást és a granulátum tartalmának szekrécióját az agonistákhoz (különösen a kollagénhez és a trombinhoz) való kötődésük serkenti. E folyamat során a thrombocyta aktiváció indukálja a tromboxán A2 (TXA2) de novo szintézisét és szekrécióját, amely egy erős érösszehúzó és aggregációt indukáló (17.17. ábra). Az ADP, a trombin és a TXA2 elősegítik a vérlemezke-aggregációt, és így hozzájárulnak az elsődleges vérrög kialakulásához. A vérlemezke aktiváció során fontos konformációs változások mennek végbe az Ilb/IIIa glikoprotein membrán receptorokban. Ezek a változások oda vezetnek, hogy a korábban inaktív Hb/IIIa receptorok megkötik a fibrinogén molekulákat, aminek következtében a vérlemezkék szorosan kapcsolódnak egymáshoz, aggregátumokat képezve.
A thrombocyta aktiváció szabályozása nagyrészt a thrombocyta raktárból történő Ca ++ felszabadulásának köszönhető. Ennek eredményeként megnő a kalcium koncentrációja a sejt citoszoljában, aktiválódnak a protein-kinázok, és végül a szabályozó fehérjék foszforilálódnak a vérlemezkékben. A [Ca++] növekedése a sejt citoszoljában emellett stimulálja a foszfolipáz A2-t, ami a TXA2 prekurzora, arachidonsav felszabadulását okozza (17.17. ábra). A kalcium felszabadulását számos tényező szabályozza. Amikor a trombin és más agonisták a vérlemezkemembrán megfelelő receptoraihoz kötődnek, közbenső vegyületek képződnek, amelyek serkentik a kalcium felszabadulását a depóból. A TXA2 növeli az intracelluláris [Ca++] szintjét a vérlemezkék felszínén lévő receptorához kötődve, ami gátolja az adenilát-cikláz aktivitását, ezáltal csökkenti a cAMP termelődését és fokozza a [Ca++] felszabadulását a depóból (17.17. ábra). . Ezzel szemben az endothelsejtek által termelt prosztaciklin (PGI2) serkenti az adenilát-cikláz aktivitását, növeli a cAMP koncentrációját a vérlemezkékben, és gátolja a [Ca++] szekréciót a depóból.
Rizs. 17.17. A vérlemezke-aktivációt az intracelluláris [Ca++] közvetíti. A kalcium felszabadulását a vérlemezkékben lévő raktárából gyorsító és gátló tényezőket mutatjuk be. A trombin és a szerotonin specifikus receptorokhoz kötődik, és a foszfolipáz C (PLS) hatására serkentik az inozit-trifoszfát (IFz) termelődését foszfatidil-inozitol-difoszfátból (FIFg). Az IGF fokozza a kalcium felszabadulását a sejt citoplazmájába. A tromboxán Ag (TXA2) a kalcium felszabadulását is elősegíti: gátolja az adenilát-cikláz (AC) aktivitását, ami a ciklikus AMP (cAMP) termelésének csökkenésével jár együtt. Normál körülmények között a cAMP megakadályozza a [Ca++] felszabadulását az ER-ből, ezért ennek a hatásnak a TXAg hatására bekövetkező csökkenése fokozza a kalcium felszabadulását a citoplazmába. Az endothel sejtekben képződő prosztaciklin ellenkező hatást fejt ki: az AC aktivitásának és a cAMP képződésének serkentésével csökkenti a kalcium felszabadulását a vérlemezkékben. A kalcium fokozza a foszfolipáz Kj (PLA2) aktivitását, melynek hatására a sejtmembrán foszfolipidjeiből TXAg prekurzorok képződnek. A vérlemezkék aktiválásakor a [Ca++] megváltozik, aminek következtében felszabadul a kalcium depó tartalma, megtörténik a citoszkeleton átrendeződése, és jelentősen megváltozik a glikoprotein IIb/IIIa receptorok konformációja, azaz a vérlemezke aggregációhoz szükséges folyamatok mennek végbe. Az ADP bizonyos mértékben hozzájárul a thrombocyta-aggregációhoz is, de ennek a folyamatnak a közvetítőit még nem sikerült megállapítani.
A modern thrombocyta-aggregációt gátló szerek aktiválási és aggregációs folyamataik különböző szakaszaiban befolyásolják a vérlemezkék működését. A leggyakoribb vérlemezke-ellenes gyógyszer az aszpirin. A klinikán alkalmazott egyéb gyógyszerek közé tartozik a dipiridamol és a tiklopidin. Aktívan vizsgálják a thrombocyta IIb/IIIa receptorokat blokkoló potenciális új gyógyszereket, és tisztázzák jelentőségüket a szív- és érrendszeri betegségek kezelésében.